| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
БИОФЛАВОНОИДЫ (ВЕЩЕСТВА Р-ВИТАМИННОГО ДЕЙСТВИЯ)
Общие сведения.
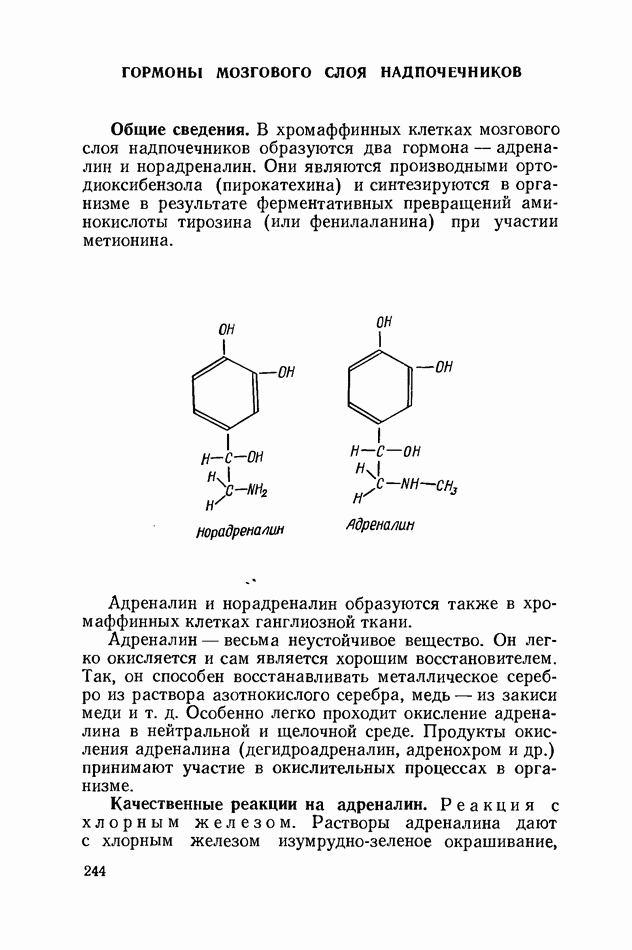
К веществам Р-витаминного действия относится ряд соединений фенольной природы, основное физиологическое действие которых заключается в уменьшении проницаемости и повышении прочности стенок кровеносных капилляров. Они способствуют усвояемости аскорбиновой кислоты в организме человека и животных. Биофлавоноиды принимают активное участие в окислительно-восстановительных процессах, обладают антиокислительными свойствами, задерживая, в частности, окисление гормона мозгового слоя надпочечников адреналина. Вещества Р-витаминного действия инактивируют фермент гиалуронидазу, которая катализирует процесс распада гетерополисахарида — гиалуроновой кислоты. Гиалуроновая кислота входит в состав основного вещества соединительной ткани.
Биофлавоноиды угнетают также активность холинэстеразы, сукциноксидазы и некоторых других ферментов. Считают, что в основе тормозящего действия флавоноидов на ферментативную активность лежат реакции их с белковыми компонентами биологических катализаторов.
В основе строения веществ Р-витаминного действия лежит ядро 2-фенилхромана — флавана

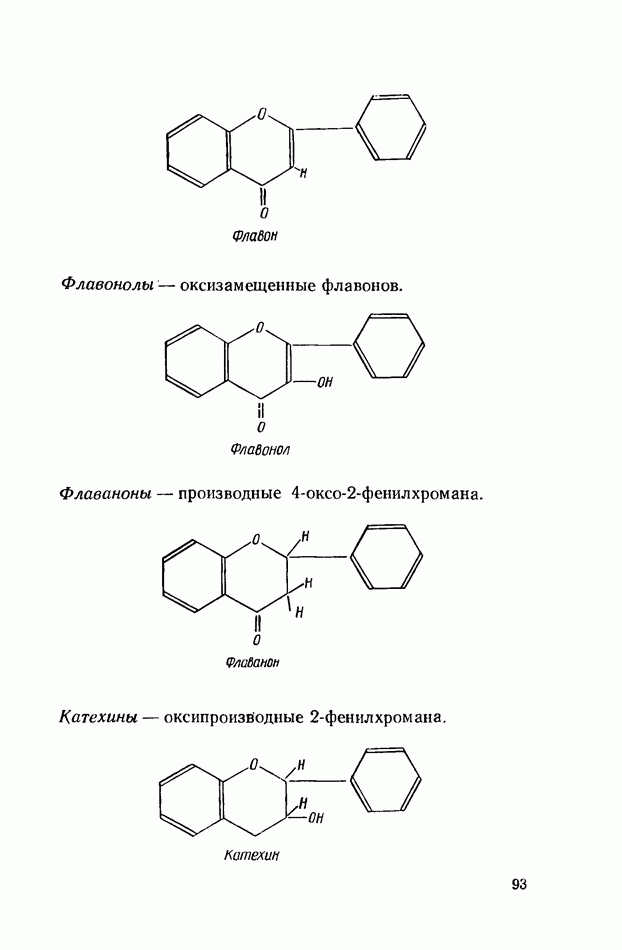
В растениях встречаются многочисленные производные 2-фенилхромана, например флавоны—производные 2,3-дегидрофлавана.

Флавон
Флавонолы — оксизамещенные флавонов.

Флашоп
Флаваноны — производные 4-оксо-2-фенилхромана.

Катехины — оксипроизйодные 2-фенилхромана.

Установлено, что витаминными свойствами обладает ряд флавонолов (рутин, кверцетин), флаванонов (эриодиктин и его метиловый эфир гесперидин), катехинов ( -эпикатехин, эпикатехингаллат и др.), кумаринов (эскулин и др.), галловая кислота и ее производные, антоцианы (красящие вещества плодов, ягод и цветов).
-эпикатехин, эпикатехингаллат и др.), кумаринов (эскулин и др.), галловая кислота и ее производные, антоцианы (красящие вещества плодов, ягод и цветов).
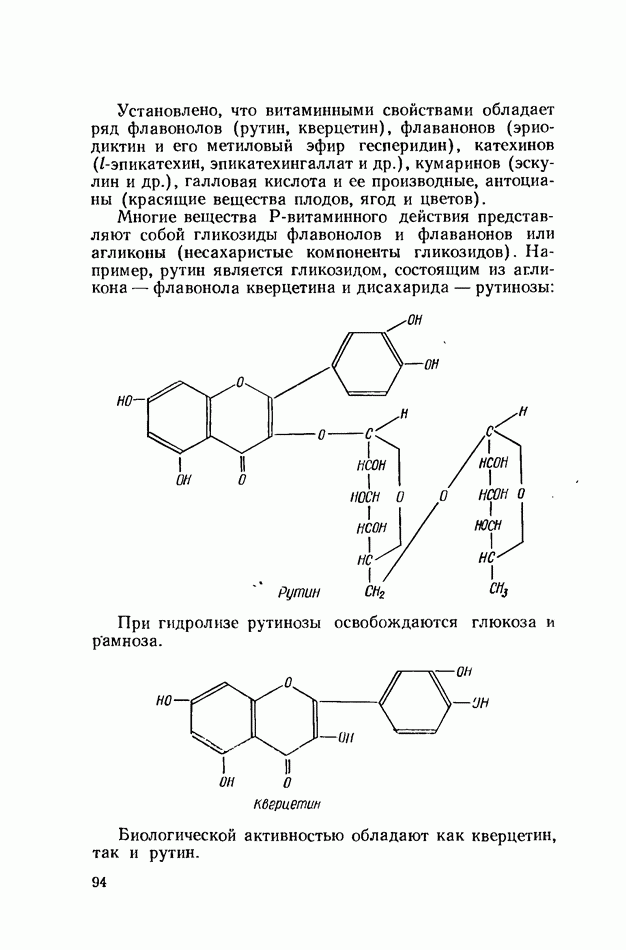
Многие вещества Р-витаминного действия представляют собой гликозиды флавонолов и флаванонов или агликоны (несахаристые компоненты гликозидов). Например, рутин является гликозидом, состоящим из агликона — флавонола кверцетина и дисахарида — рутинозы:

При гидролизе рутинозы освобождаются глюкоза и рамноза.

Биологической активностью обладают как кверцетин, так и рутин.
К группе веществ Р-витаминного действия следует также отнести агликоны ряда растительных пигментов — антоцианидины (например, цианидин — агликон цианина, пигмента, весьма распространенного в цветках и плодах ряда высших растений) и лейкоантоцианы.
Биофлавоноиды широко распространены в растительном мире. Ими богаты многие плоды и ягоды (цитрусовые, черная смородина, шиповник, голубика, черника, брусника, рябина, клюква и др.), листья чайного растения, гречиха (особенно в период цветения), рута и др.
Качественные реакции на рутин и кверцетин.
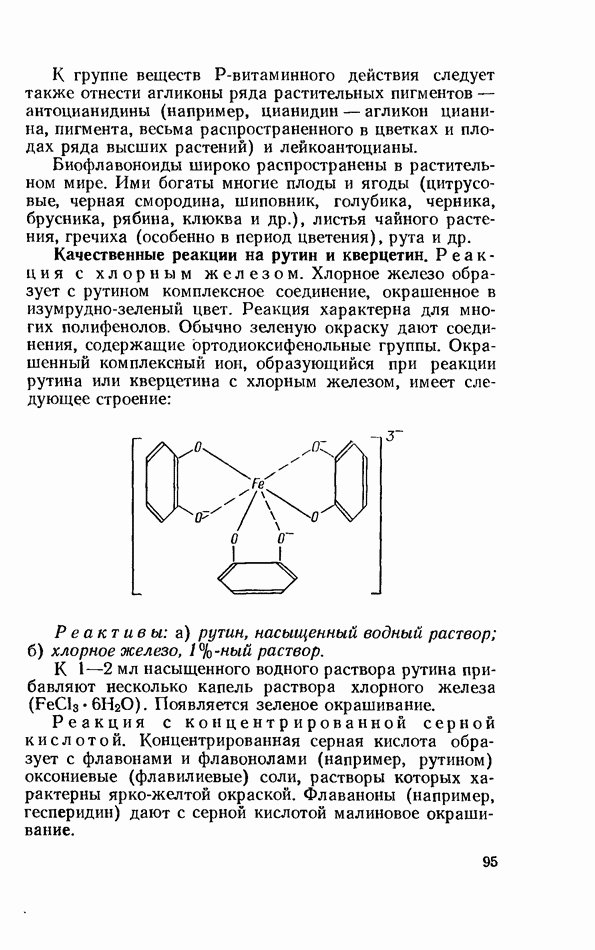
Реакция с хлорным железом. Хлорное железо образует с рутином комплексное соединение, окрашенное в изумрудно-зеленый цвет. Реакция характерна для многих полифенолов. Обычно зеленую окраску дают соединения, содержащие ортодиоксифенольные группы. Окрашенный комплексный ион, образующийся при реакции рутина или кверцетина с хлорным железом, имеет следующее строение:

Реактивы: а) рутин, насыщенный водный раствор; б) хлорное железо, 1%-ный раствор.
К 1-2 мл насыщенного водного раствора рутина прибавляют несколько капель раствора хлорного железа  Появляется зеленое окрашивание.
Появляется зеленое окрашивание.
Реакция с концентрированной серной кислотой. Концентрированная серная кислота образует с флавонами и флавонолами (например, рутином) оксониевые (флавилиевые) соли, растворы которых характерны ярко-желтой окраской. Флаваноны (например, гесперидин) дают с серной кислотой малиновое окрашивание.
Реактивы: а) рутин, насыщенный водный раствор; б) серная кислота, концентрированная ( ).
).
К 1-2 мл насыщенного водного раствора рутина осторожно, по стенке пробирки, добавляют  концентрированной серной кислоты. Содержимое пробирки окрашивается в желтый цвет.
концентрированной серной кислоты. Содержимое пробирки окрашивается в желтый цвет.
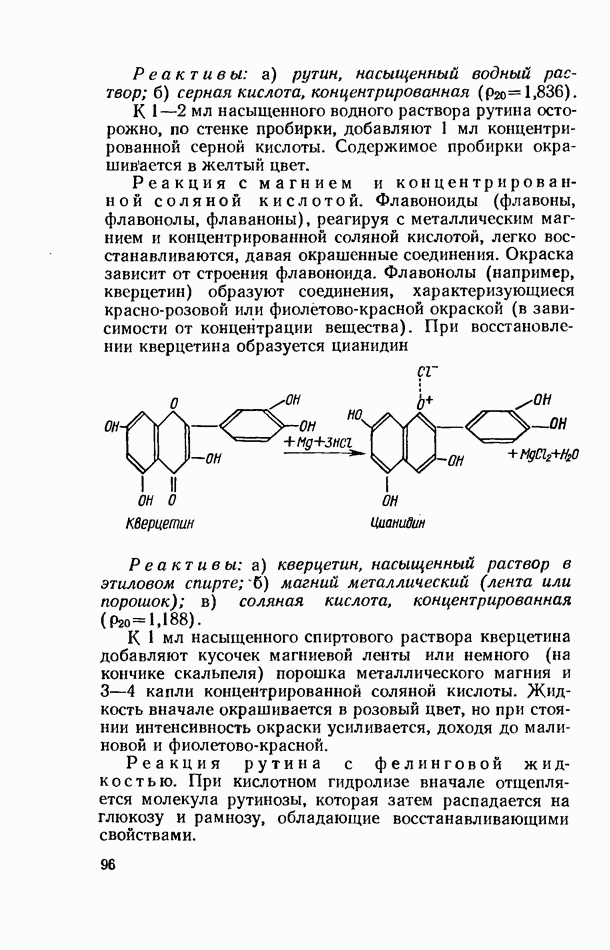
Реакция с магнием и концентрированной соляной кислотой. Флавоноиды (флавоны, флавонолы, флаваноны), реагируя с металлическим магнием и концентрированной соляной кислотой, легко восстанавливаются, давая окрашенные соединения. Окраска зависит от строения флавоноида. Флавонолы (например, кверцетин) образуют соединения, характеризующиеся красно-розовой или фиолетово-красной окраской (в зависимости от концентрации вещества). При восстановлении кверцетин а образуется цианидин

Реактивы: а) кверцетин, насыщенный раствор в этиловом спирте; б) магний металлический (лента или порошок); в) соляная кислота, концентрированная 
К 1 мл насыщенного спиртового раствора кверцетина добавляют кусочек магниевой ленты или немного (на кончике скальпеля) порошка металлического магния и 3—4 капли концентрированной соляной кислоты. Жидкость вначале окрашивается в розовый цвет, но при стоянии интенсивность окраски усиливается, доходя до малиновой и фиолетово-красной.
Реакция рутина с фелинговой жидкостью. При кислотном гидролизе вначале отщепляется молекула рутинозы, которая затем распадается на глюкозу и рамнозу, обладающие восстанавливающими свойствами.
Реактивы: а) рутин, в порошке; б) растворы Фелинга  (приготовление — см. с. 202); в) соляная кислота, 0,5%-ный раствор; г) едкий натр, 10%-ный раствор.
(приготовление — см. с. 202); в) соляная кислота, 0,5%-ный раствор; г) едкий натр, 10%-ный раствор.
К 0,5 г рутина добавляют 50 мл 0,5%-ного раствора соляной кислоты, нагревают до кипения, кипятят 1 мин., затем фильтруют. К 5 мл фильтрата приливают 3 мл 10%-ного раствора едкого натра и 3 мл фелинговой жидкости (которую готовят непосредственно перед употреблением, смешивая равные объемы I и II растворов Фе-линга) и снова нагревают до кипения. Выпадает красный осадок закиси меди.
Капельный метод определения катехинов в яблоках и грушах (по Л. И. Вигорову).
Катехины, реагируя с солянокислым раствором ванилина, образуют соединения, окрашенные в розовый или красный цвет. Используя указанную реакцию, можно очень быстро определить приблизительное содержание катехинов в яблоках или грушах.
Реактивы: а) солянокислый раствор ванилина: 10 мг ванилина растворяют в 10 мл концентрированной соляной кислоты. Раствор должен быть бесцветным. Хранят в склянке из оранжевого стекла. Реактив, который приобрел розовую окраску, непригоден к употреблению; б) сернистокислый натрий (сульфит натрия,  -ный водный раствор.
-ный водный раствор.
Куски хроматографической бумаги (10x10 см) пропитывают 1%-ным раствором сернистокислого натрия и высушивают. Через всю толщу мякоти плодов вырезают полулунные ломтики, доходящие до семенных камер. Из ломтиков отжимают сок (между двумя алюминиевыми пластинками или же на прессе от полевого рефрактометра). Каплю сока наносят на хроматографическую бумагу и место нанесения нумеруют графитовым карандашом (на один кусок бумаги наносят 8—10 образцов сока). Бумагу высушивают на воздухе (высушивание можно ускорить комнатным вентилятором или феном). Высушенную бумагу опрыскивают солянокислым раствором ванилина В зависимости от содержания катехинов в плодах места нанесения капель на бумагу принимают розовое, светло-красное или красное окрашивание.
Определение суммарного количества Р-витаминных веществ в чае.
В листьях растения витамин Р в основном
представлен катехинами и их производными (чайным танином). В числе суммы катехинов чайного листа почти  составляют L-эпикатехин, эпикатехингаллат, эпигаллокатехин и эпигаллокатехингаллат.
составляют L-эпикатехин, эпикатехингаллат, эпигаллокатехин и эпигаллокатехингаллат.
В основу метода количественного определения витамина Р в чае положена способность бесцветных катехинов окисляться марганцовокислым калием с образованием окрашенных соединений.
Реактивы и материалы: а) чай, черный или зеленый; б) марганцовокислый калий (перманганат калия), 0,1 н раствор: 3,16 г (навеска на аналитических весах) растворяют в прокипяченной и остуженной дистиллированной воде в мерной колбе емкостью 1 л, раствор доводят до метки той же водой. Поправку на титр раствора  устанавливают по химически чистому щавелевокислому натрию или аммонию; в) раствор индигокармина: 1 г индигокармина растирают в фарфоровой ступке и растворяют в 50 мл концентрированной серной кислоты. Раствор переносят в мерную колбу емкостью 1 л и доводят водой до метки, затем фильтруют через бумажный складчатый фильтр. Хранят в холодном месте в склянке из темного стекла; срок годности раствора — не более 10 дней.
устанавливают по химически чистому щавелевокислому натрию или аммонию; в) раствор индигокармина: 1 г индигокармина растирают в фарфоровой ступке и растворяют в 50 мл концентрированной серной кислоты. Раствор переносят в мерную колбу емкостью 1 л и доводят водой до метки, затем фильтруют через бумажный складчатый фильтр. Хранят в холодном месте в склянке из темного стекла; срок годности раствора — не более 10 дней.
Навеску чая (0,5-0,6 г) переносят в коническую колбу, заливают 200 мл кипящей воды, колбу закрывают пробкой с воздушным холодильником и продолжают кипячение в течение 5 мин., после чего охлаждают. Измеряют общий объем-водного экстракта.
В большую фарфоровую чашку наливают 500 мл дистиллированной воды, 25 мл раствора индигокармина и 10 мл водного экстракта из листьев чая (пипеткой). Раствор в чашке, окрашенный в синий цвет, титруют 0,1 н раствором марганцовокислого калия до появления желтого окрашивания. Раствор марганцовокислого калия прибавляют небольшими порциями, все время перемешивая жидкость в чашке стеклянной палочкой.
Одновременно проводят контрольный опыт: в чашку наливают 500 мл дистиллированной воды, 25 мл раствора индигокармина и титруют 0,1 н раствором перманганата. Опытное и контрольное титрования повторяют 3—4 раза.
Суммарное содержание веществ Р-витаминного действия в чае (в процентах)  вычисляют по формуле:
вычисляют по формуле:

где a — количество 0,1 н раствора  израсходованное на титрование опытного раствора,
израсходованное на титрование опытного раствора,  — то же для контрольного опыта; К — поправка на титр 0,1 и раствора марганцовокислого калия; 0,0064 — количество чайного танина, окисляемое
— то же для контрольного опыта; К — поправка на титр 0,1 и раствора марганцовокислого калия; 0,0064 — количество чайного танина, окисляемое  н раствора
н раствора  — объем водного экстракта из листьев чая,
— объем водного экстракта из листьев чая,  — количество водного экстракта, взятое для титрования,
— количество водного экстракта, взятое для титрования,  — навеска чая, г.
— навеска чая, г.
| << Предыдущий параграф | Следующий параграф >> |
- Раздел I. ХИМИЯ АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- Приготовление растворов белка
- Цветные реакции
- Исследование физико-химических свойств белковых веществ
- Распределительная хроматография аминокислот на бумаге
- Разделение белка и низкомолекулярных примесей методом гельфильтрации на сефадексе G 25 (по Р. Мардашеву, А. А. Покровскому, Н. А. Павловой, с дополнениями)
- Электрофорез белков и аминокислот на бумаге
- Электрофорез белков в полиакриламидном геле (по В. Бжескому и 3. Канюга, с дополнениями)
- СЛОЖНЫЕ БЕЛКИ (ПРОТЕИДЫ)
- Гликопротеиды
- Фосфопротеиды
- Раздел II. НУКЛЕОПРОТЕИДЫ. НУКЛЕИНОВЫЕ КИСЛОТЫ
- ВЫДЕЛЕНИЕ ДЕЗОКСИРИБОНУКЛЕОПРОТЕИДОВ ИЗ ПЕЧЕНИ ИЛИ СЕЛЕЗЕНКИ
- КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ДНК
- ВЫДЕЛЕНИЕ НУКЛЕОПРОТЕИДОВ ИЗ ДРОЖЖЕЙ
- ГИДРОЛИЗ НУКЛЕОПРОТЕИДОВ
- ИССЛЕДОВАНИЕ ПРОДУКТОВ ГИДРОЛИЗА НУКЛЕОПРОТЕИДОВ
- ОЧИСТКА И РАЗДЕЛЕНИЕ НУКЛЕИНОВЫХ КИСЛОТ (по Шмидту и Таннгаузеру, в прописи Г. П. Георгиева)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ДНК (по Дише)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ РНК (по Мейбаум)
- ХРОМАТОГРАФИЯ НА БУМАГЕ ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ, НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ
- Раздел III. ВИТАМИНЫ
- ВИТАМИНЫ ГРУППЫ А
- ВИТАМИНЫ ГРУППЫ D (КАЛЬЦИФЕРОЛЫ)
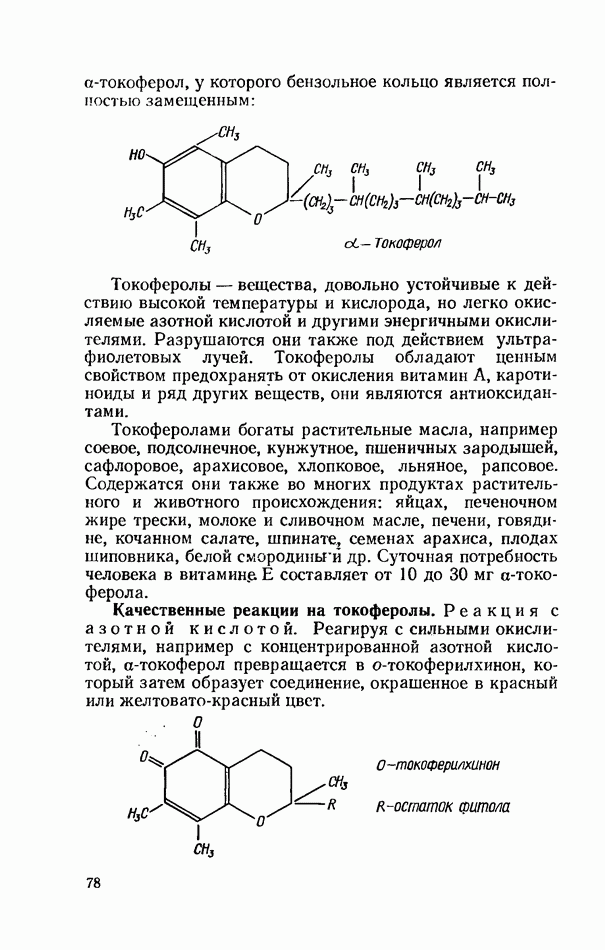
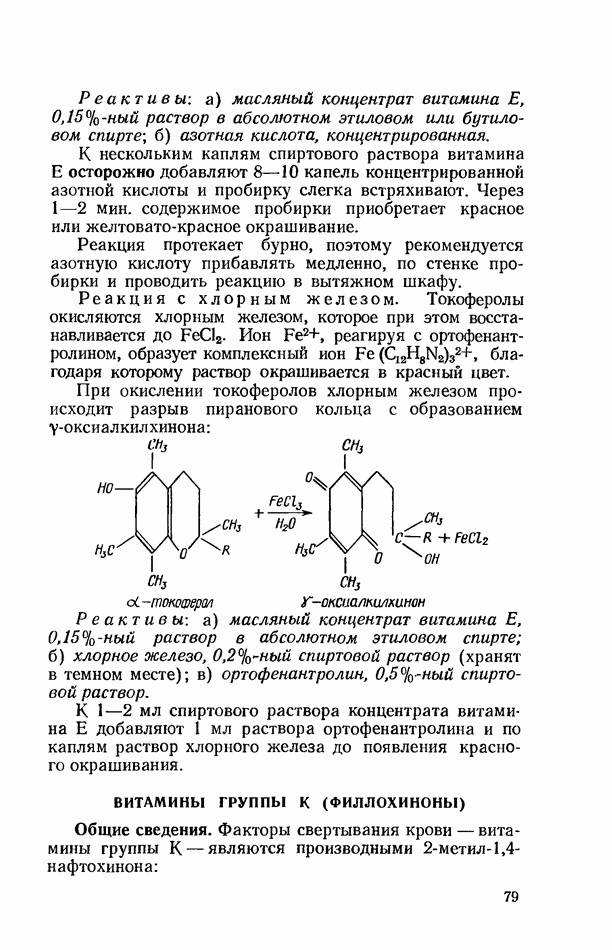
- ВИТАМИНЫ ГРУППЫ Е (ТОКОФЕРОЛЫ)
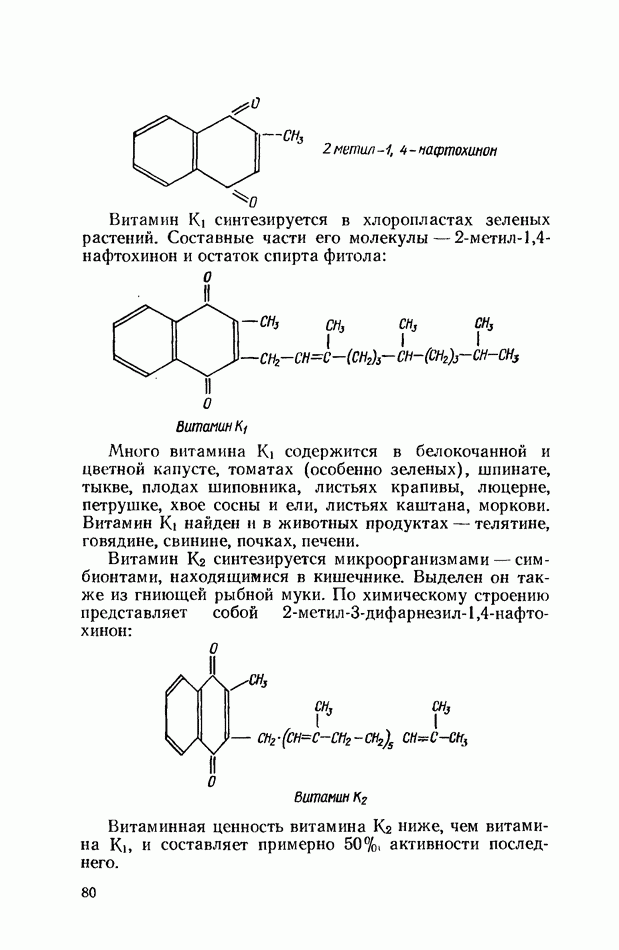
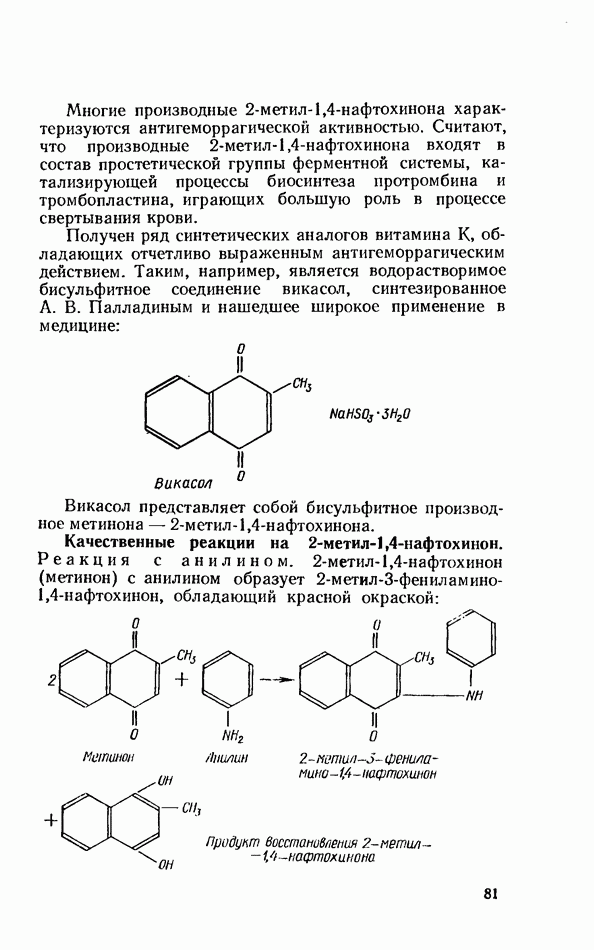
- ВИТАМИНЫ ГРУППЫ К (ФИЛЛОХИНОНЫ)
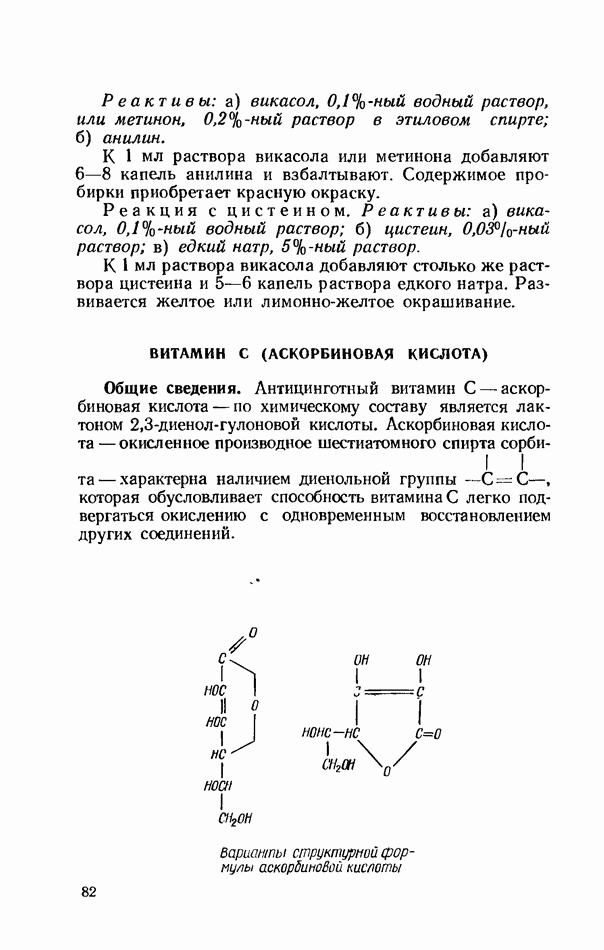
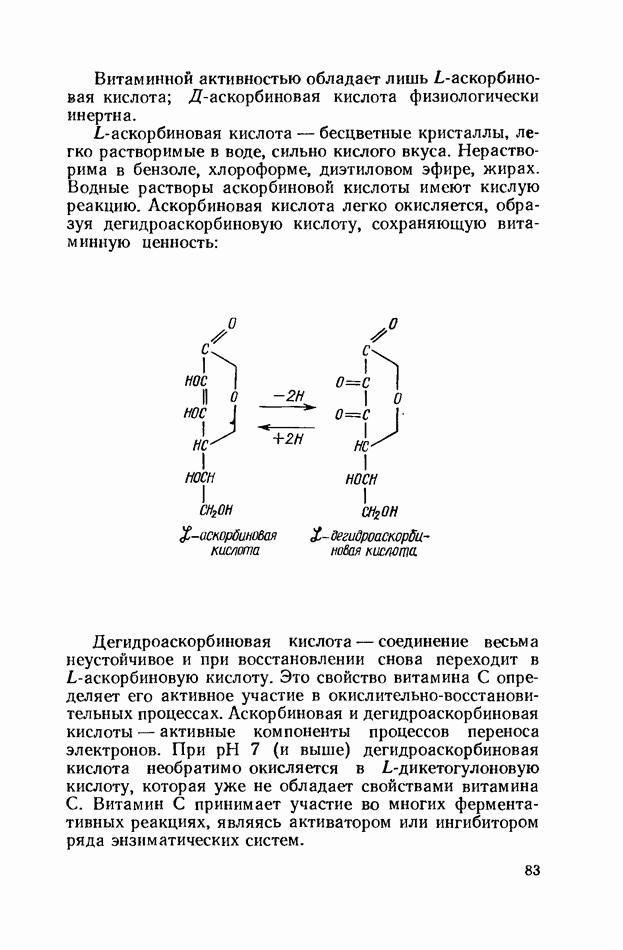
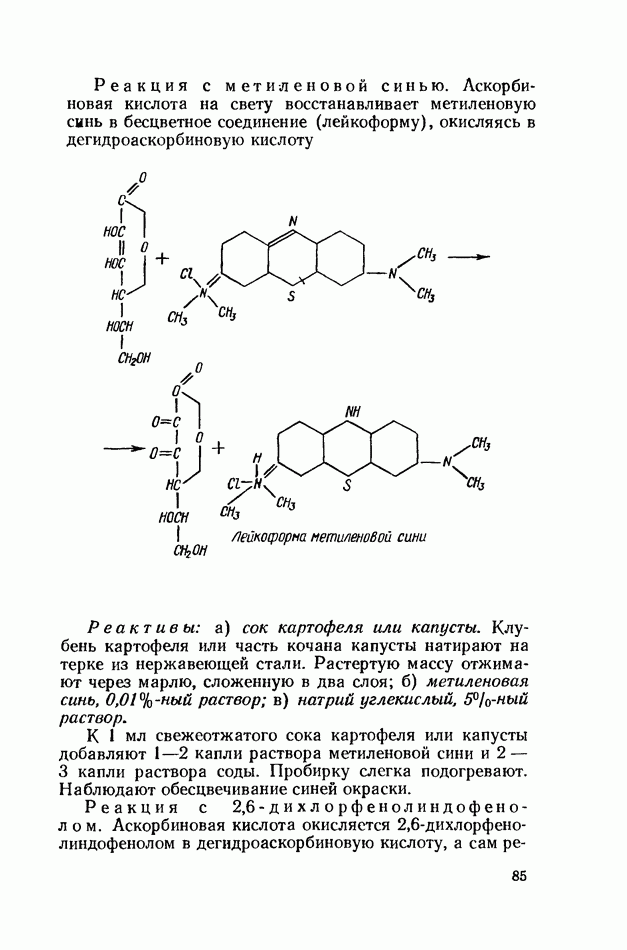
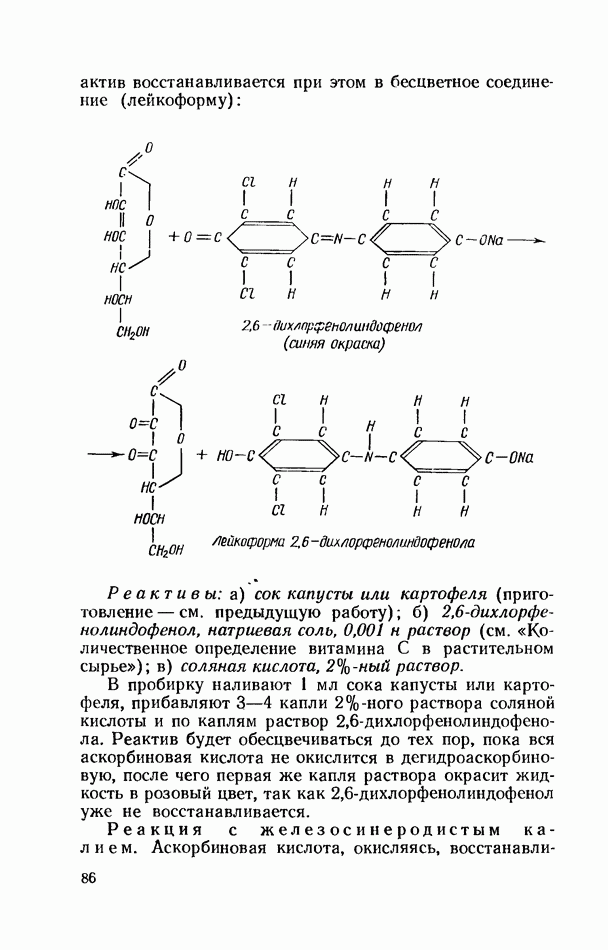
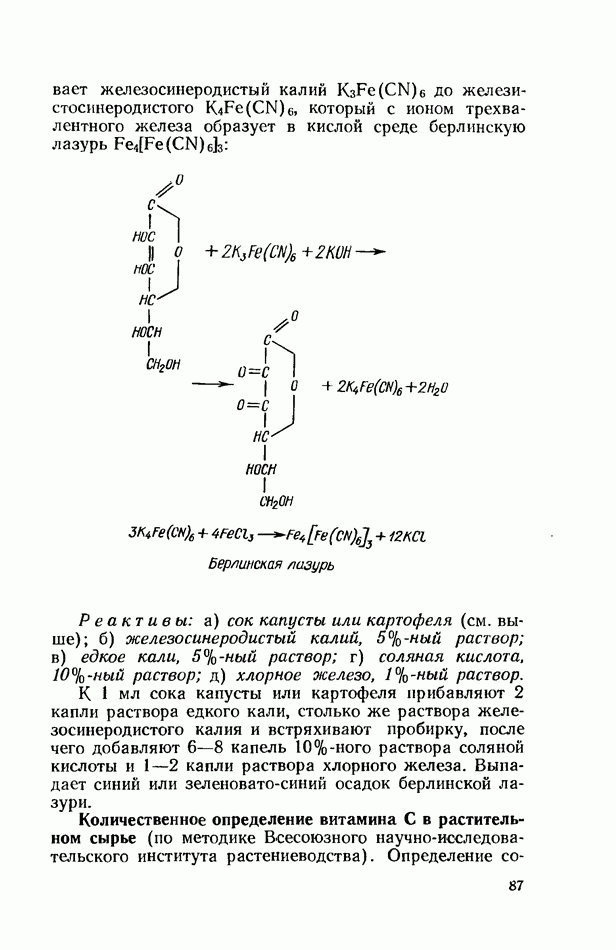
- ВИТАМИН С (АСКОРБИНОВАЯ КИСЛОТА)
- БИОФЛАВОНОИДЫ (ВЕЩЕСТВА Р-ВИТАМИННОГО ДЕЙСТВИЯ)
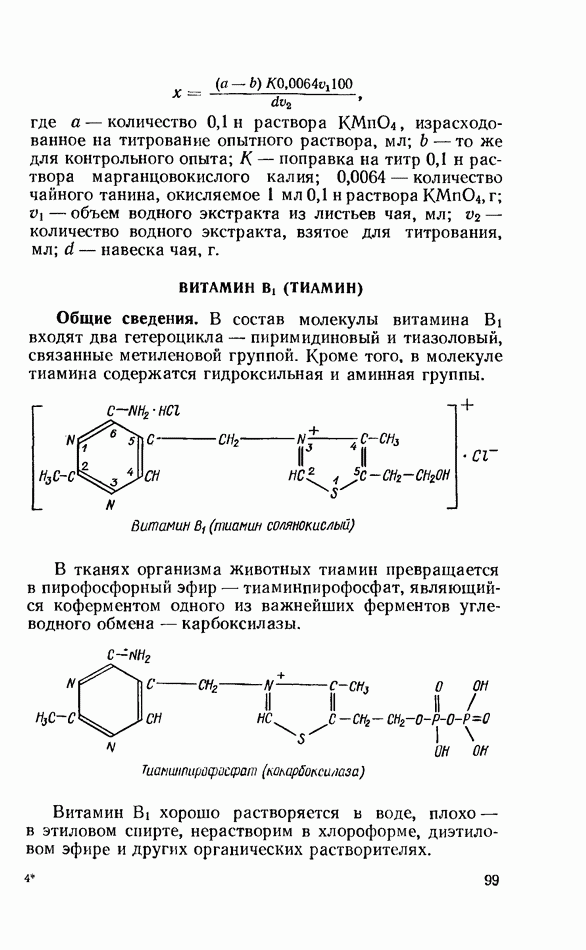
- ВИТАМИН В: (ТИАМИН)
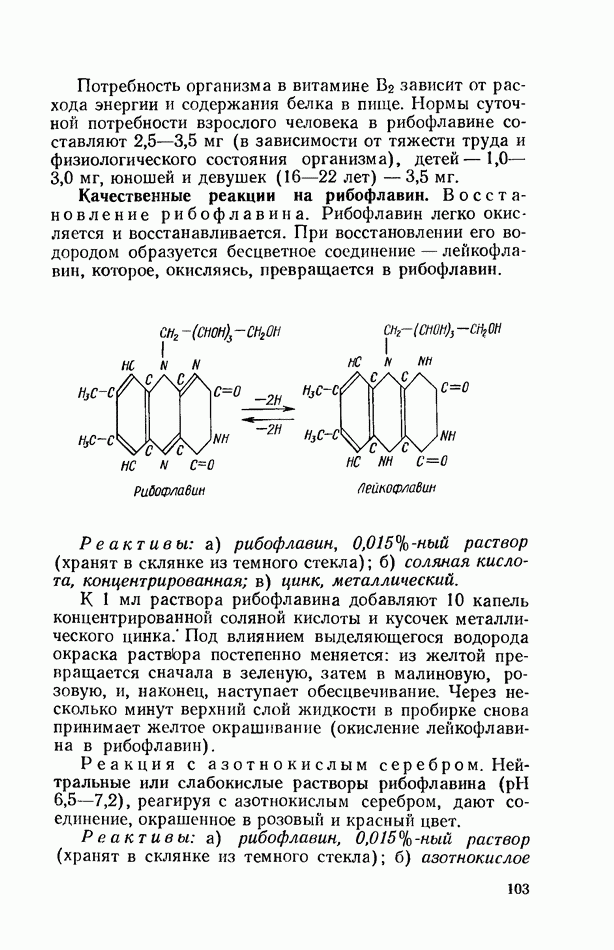
- ВИТАМИН В2 (РИБОФЛАВИН)
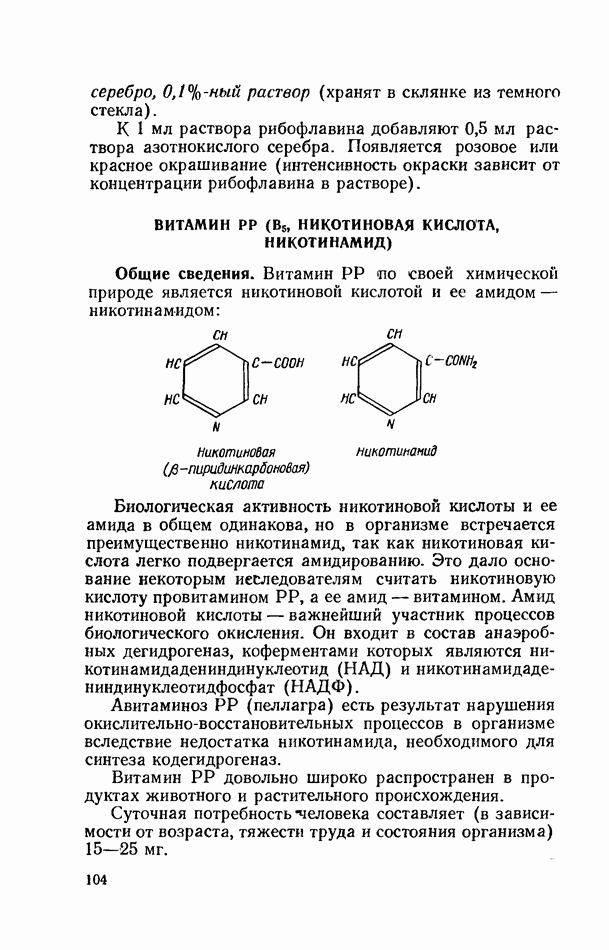
- ВИТАМИН РР (В5, НИКОТИНОВАЯ КИСЛОТА, НИКОТИНАМИД)
- ВИТАМИН В6 (ПИРИДОКСИН)
- Раздел IV. ФЕРМЕНТЫ (ЭНЗИМЫ)
- ИССЛЕДОВАНИЕ ОБЩИХ СВОЙСТВ ФЕРМЕНТОВ
- ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ГИДРОЛИТИЧЕСКИХ ФЕРМЕНТОВ (ГИДРОЛАЗ)
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ФЕРМЕНТЫ (ОКСИДОРЕДУКТАЗЫ)
- Раздел V. ОБМЕН АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО АЗОТА ПО КЪЕЛЬДАЛЮ (МИКРОМЕТОД)
- ОПРЕДЕЛЕНИЕ БЕЛКОВОГО И НЕБЕЛКОВОГО АЗОТА
- БЫСТРЫЙ МЕТОД КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕЛКОВ
- ОПРЕДЕЛЕНИЕ АЗОТА АМИНОКИСЛОТ
- ОПРЕДЕЛЕНИЕ СВОБОДНЫХ АМИНОКИСЛОТ В МЫШЕЧНОЙ ТКАНИ МЕТОДОМ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ (по Г. В. Колоболотскому)
- ГИДРОЛИТИЧЕСКОЕ РАСЩЕПЛЕНИЕ БЕЛКА ФЕРМЕНТАМИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
- ПЕРЕАМИНИРОВАНИЕ (ТРАНСАМИНИРОВАНИЕ) АМИНОКИСЛОТ
- Раздел VI. ХИМИЯ И ОБМЕН ЛИПИДОВ
- ЖИРЫ (НЕЙТРАЛЬНЫЕ ЖИРЫ)
- ФОСФАТИДЫ, ИЛИ ФОСФОЛИПИДЫ
- СТЕРИНЫ
- ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ ЛИПИДОВ
- КЕТОНОВЫЕ ТЕЛА
- Раздел VII. ХИМИЯ И ОБМЕН УГЛЕВОДОВ
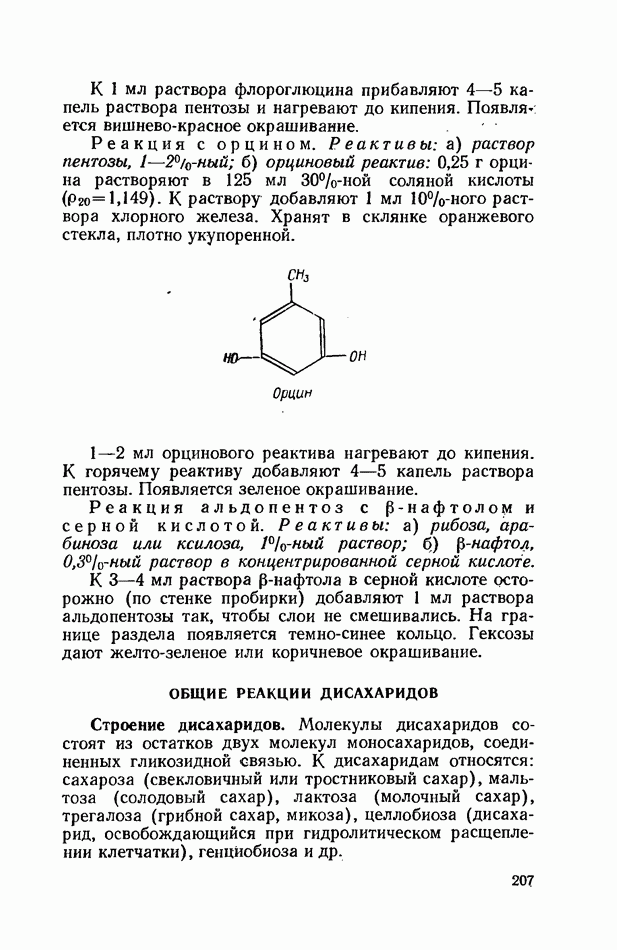
- КАЧЕСТВЕННЫЕ РЕАКЦИИ НА МОНОСАХАРИДЫ
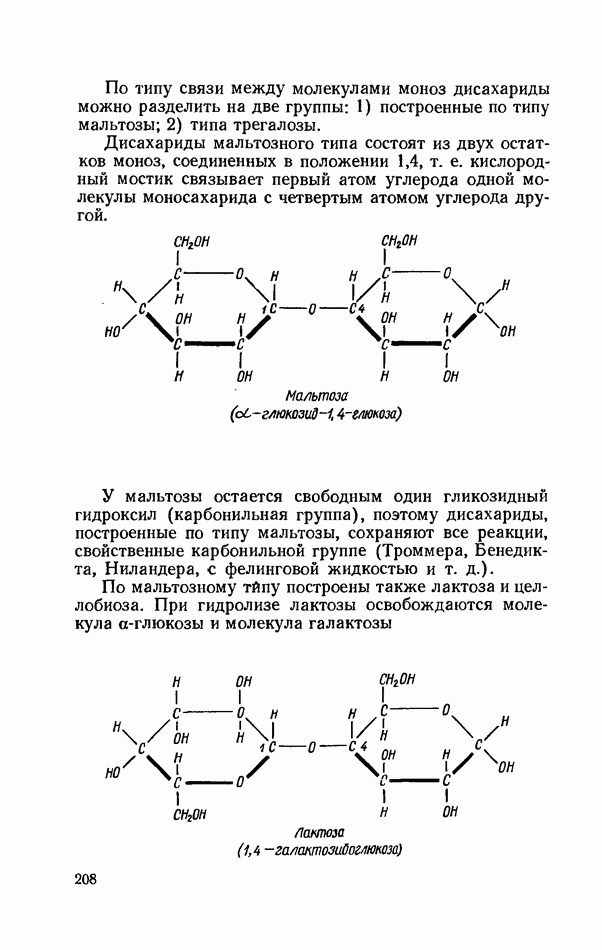
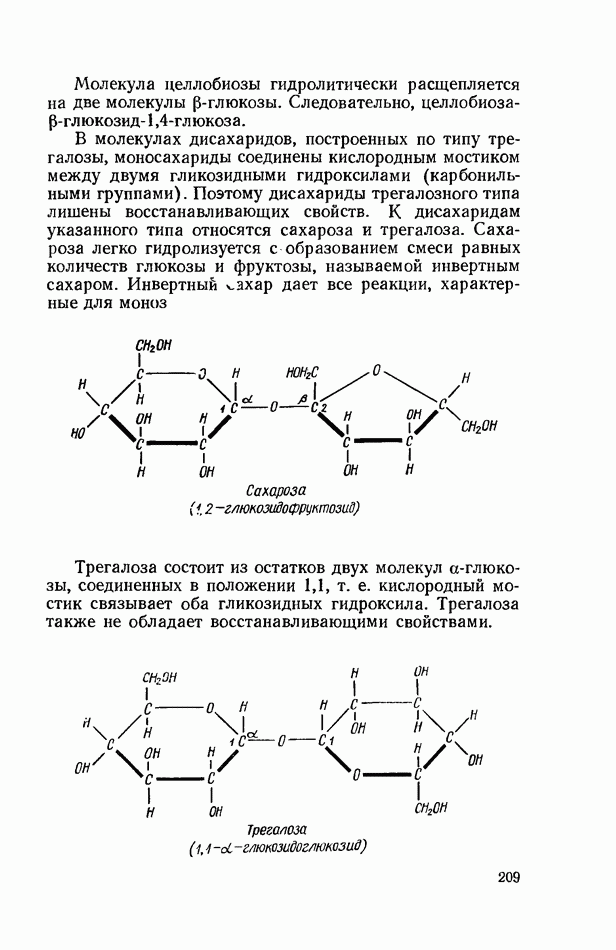
- ОБЩИЕ РЕАКЦИИ ДИСАХАРИДОВ
- ВЫСШИЕ ПОЛИСАХАРИДЫ
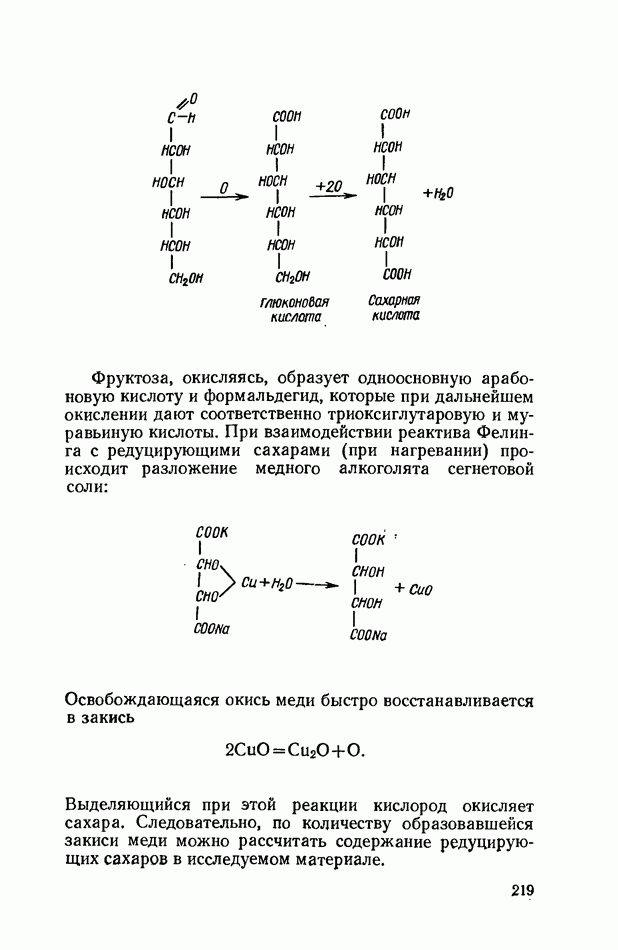
- ОПРЕДЕЛЕНИЕ РЕДУЦИРУЮЩИХ (ВОССТАНАВЛИВАЮЩИХ) САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ
- ФОТОМЕТРИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РЕДУЦИРУЮЩИХ САХАРОВ
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ С ПОМОЩЬЮ ХРОМАТОГРАФИИ НА БУМАГЕ (по О. А. Павлиновой)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ В КРОВИ (по Хагедорну — Иеисену)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КРАХМАЛА
- ИССЛЕДОВАНИЕ АНАЭРОБНОГО РАСПАДА ГЛИКОГЕНА ИЛИ КРАХМАЛА
- ОПРЕДЕЛЕНИЕ ПИРОВИНОГРАДНОЙ КИСЛОТЫ В МОЧЕ
- Раздел VIII. ГОРМОНЫ
- ОТКРЫТИЕ ИОДА В ЩИТОВИДНОЙ ЖЕЛЕЗЕ
- ГОРМОНЫ МОЗГОВОГО СЛОЯ НАДПОЧЕЧНИКОВ
- ГОРМОНЫ КОРКОВОГО СЛОЯ НАДПОЧЕЧНИКОВ (КОРТИКОСТЕРОИДЫ)
- ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- Раздел IX. ОБМЕН МИНЕРАЛЬНЫХ ВЕЩЕСТВ
- ОПРЕДЕЛЕНИЕ КАЛЬЦИЯ В СЫВОРОТКЕ КРОВИ
- ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО СОДЕРЖАНИЯ ФОСФОРА В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА В ПЛАЗМЕ ИЛИ СЫВОРОТКЕ КРОВИ (по прописи П. А. Розенберг и Н. К. Бялко)
- ОПРЕДЕЛЕНИЕ ХЛОРИДОВ В ПИЩЕВЫХ ПРОДУКТАХ (по А. С. Вечеру и В. В. Малоян)
- ЛИТЕРАТУРА
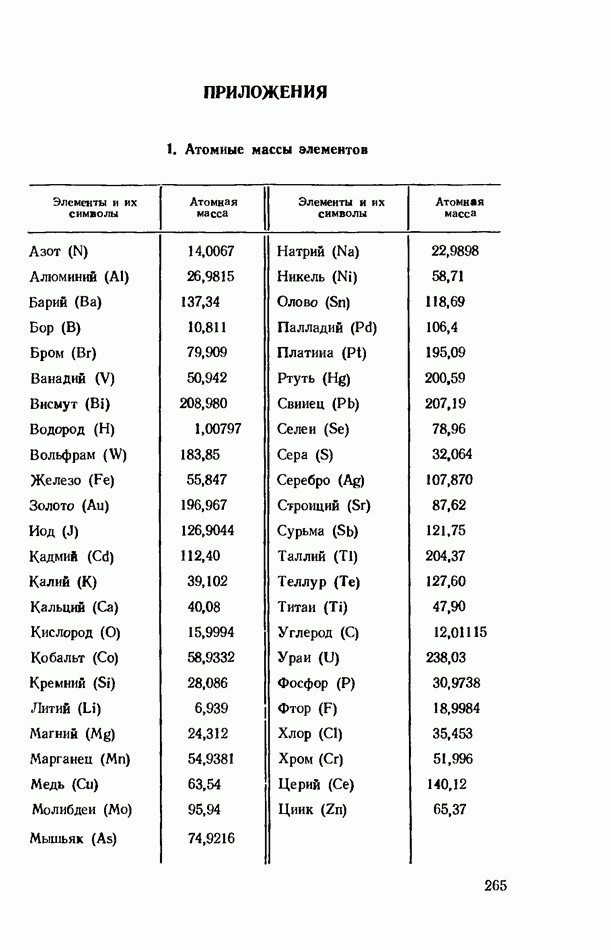
- ПРИЛОЖЕНИЯ