| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Раздел IV. ФЕРМЕНТЫ (ЭНЗИМЫ)
Ферменты (энзимы) — биологические катализаторы процессов обмена веществ. Они представляют собой высокомолекулярные соединения и относятся к простым или сложным белкам. По характеру своего действия ферментативный катализ чаще всего является гетерогенным (микрогетерогенным).
Обладая многими свойствами, сходными со свойствами неорганических катализаторов, ферменты характеризуются рядом особенностей, к которым следует отнести термолабильность, большую зависимость их активности от pH среды, высокую специфичность (как групповую, так и индивидуальную, включая стереохимическую), огромную эффективность каталитического действия и др. Протекает ферментативный катализ с большой скоростью и в мягких условиях.
Активность ферментов в значительной мере зависит от состава среды. Многие химические вещества способны усиливать (активаторы) или затормаживать (ингибиторы) каталитическую активность ферментов.
Ферменты можно разделить на две большие группы: ферменты-протеины (простые белки) и ферменты-протеиды (сложные белки). К протеинам относятся многочисленные ферменты, катализирующие процессы гидролитического расщепления сложных соединений на более простые (например, пепсин, амилазы, уреаза и др.).
Ферменты-протеиды состоят из белковой части — апофермента и термостабильной небелковой — кофермента, или простетической группы. В большинстве своем коферменты — это сопряженные (резонансные) органические молекулы.
Многие простетические группы представляют собой производные витаминов (главным образом группы В). Часто роль кофермента играют металлы (железо, магний, медь, кобальт, цинк, марганец, молибден). Существуют, наконец, ферменты, у которых имеются две или несколько простетическнх групп. Например, у карбо-ксилазы, фермента, катализирующего реакцию декар-боксилирования пировиноградной кислоты, простетическими трупами являются производное витамина  (тиаминпирофосфат) и металл магний, который служит связующим звеном между белковой частью фермента и тиаминпирофосфатом (кокарбоксилазой). Схему строения фермента можно представить следующим образом:
(тиаминпирофосфат) и металл магний, который служит связующим звеном между белковой частью фермента и тиаминпирофосфатом (кокарбоксилазой). Схему строения фермента можно представить следующим образом:

В названиях ферментов отражается не только характеристика катализируемой реакции, но и наименование субстрата, который подвергается превращению. Как правило, они составляются из двух частей. Первая указывает название субстрата или (при бимолекулярных реакциях) двух субстратов. Вторая часть названия с окончанием «аза» характеризует природу реакции. Например, ферменты, катализирующие реакцию отщепления атомов водорода в молекулах органических соединений и их перенос на молекулы других веществ, называются дегидрогеназами (дегидрогенизация — отщепление водорода). Фермент, катализирующий указанный процесс у первичных и вторичных спиртов, носит название алко-гольдегидрогеназы.
Наряду с рациональными названиями для ряда ферментов сохранились старые исторически сложившиеся названия, например пепсин, трипсин, папаин и др.
В соответствии с рекомендациями Международного биологического союза (1961 г.) все ферменты разделены на 6 классов.
1. Оксидоредуктазы. Катализируют окислительновосстановительные реакции. Оксидоредуктазы подразделяются на две большие группы: а) дегидрогеназы, катализирующие процесс окисления органических веществ путем отнятия водорода и переноса его на другой субстрат; б) оксидазы, катализирующие перенос водорода с субстрата, подвергающегося окислению, на кислород.
2. Трансферазы. Эти ферменты катализируют реакции переноса атомных групп (аминогрупп, остатков фосфорной кислоты, метальных групп и т. д.).
3. Гидролазы. Катализируют реакции гидролитического распада сложных соединений на более простые. К этому классу относятся многочисленные ферменты, действующие на сложно-эфирные связи (эстеразы, например, липазы, катализирующие процесс гидролитического расщепления липидов), гликозильные соединения (например, гликозидазы, катализирующие гидролитический распад поли- и олигосахаридов), пептидные связи (пептидазы или пептидгидролазы), кислотноангидридные (полифосфатазы) и др.
4. Лиазы. Катализируют негидролитическое отщепление от субстратов определенных групп с образованием двойной связи.
5. Изомеразы. Ферменты, отнесенные к этому классу, катализируют разнообразные реакции изомеризации, например превращение цисформы в трансформу, взаимопревращение альдоз и кетоз, внутримолекулярный перенос групп (в последнем случае ферменты называют мутазами) и т. д.
6. Лигазы (синтетазы). Катализируют присоединение друг к другу двух молекул, сопряженное с разрывом пирофосфорной связи в молекуле АТФ (или аналогичных трифосфатов). Сюда относятся ферменты, образующие связи между молекулами углерода и кислорода, серы, азота или между двумя молекулами углерода.
| << Предыдущий параграф | Следующий параграф >> |
- Раздел I. ХИМИЯ АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- Приготовление растворов белка
- Цветные реакции
- Исследование физико-химических свойств белковых веществ
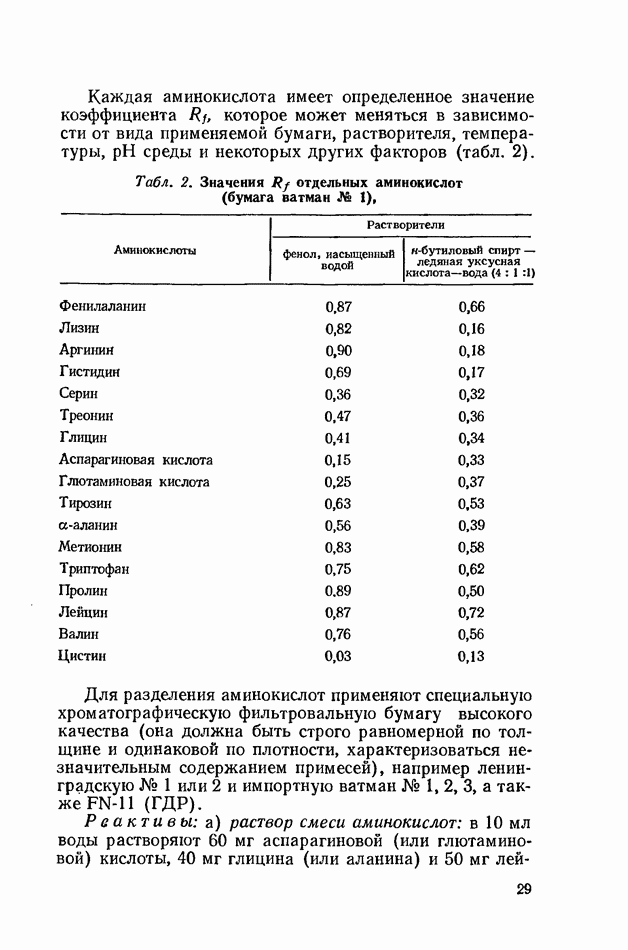
- Распределительная хроматография аминокислот на бумаге
- Разделение белка и низкомолекулярных примесей методом гельфильтрации на сефадексе G 25 (по Р. Мардашеву, А. А. Покровскому, Н. А. Павловой, с дополнениями)
- Электрофорез белков и аминокислот на бумаге
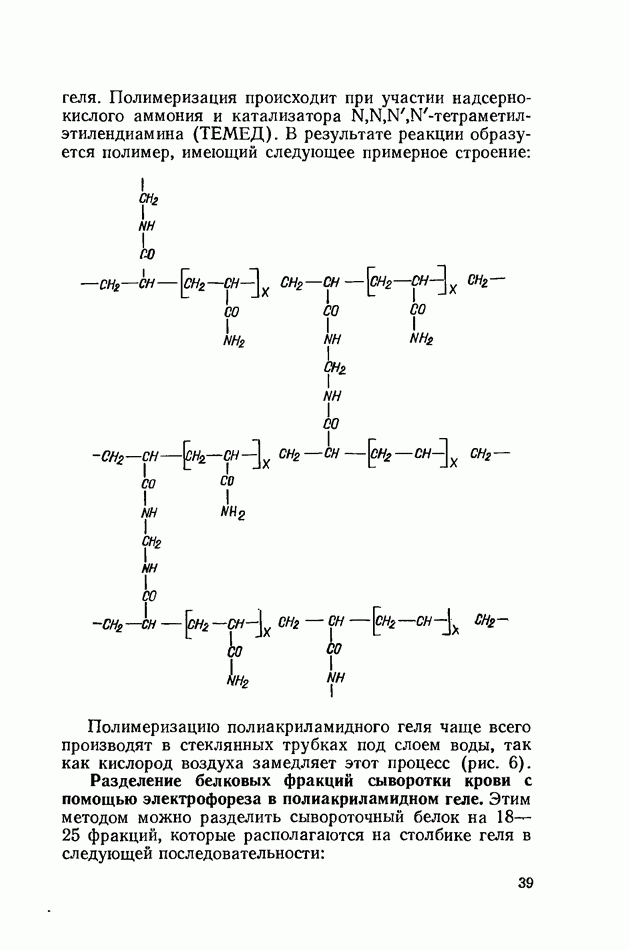
- Электрофорез белков в полиакриламидном геле (по В. Бжескому и 3. Канюга, с дополнениями)
- СЛОЖНЫЕ БЕЛКИ (ПРОТЕИДЫ)
- Гликопротеиды
- Фосфопротеиды
- Раздел II. НУКЛЕОПРОТЕИДЫ. НУКЛЕИНОВЫЕ КИСЛОТЫ
- ВЫДЕЛЕНИЕ ДЕЗОКСИРИБОНУКЛЕОПРОТЕИДОВ ИЗ ПЕЧЕНИ ИЛИ СЕЛЕЗЕНКИ
- КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ДНК
- ВЫДЕЛЕНИЕ НУКЛЕОПРОТЕИДОВ ИЗ ДРОЖЖЕЙ
- ГИДРОЛИЗ НУКЛЕОПРОТЕИДОВ
- ИССЛЕДОВАНИЕ ПРОДУКТОВ ГИДРОЛИЗА НУКЛЕОПРОТЕИДОВ
- ОЧИСТКА И РАЗДЕЛЕНИЕ НУКЛЕИНОВЫХ КИСЛОТ (по Шмидту и Таннгаузеру, в прописи Г. П. Георгиева)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ДНК (по Дише)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ РНК (по Мейбаум)
- ХРОМАТОГРАФИЯ НА БУМАГЕ ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ, НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ
- Раздел III. ВИТАМИНЫ
- ВИТАМИНЫ ГРУППЫ А
- ВИТАМИНЫ ГРУППЫ D (КАЛЬЦИФЕРОЛЫ)
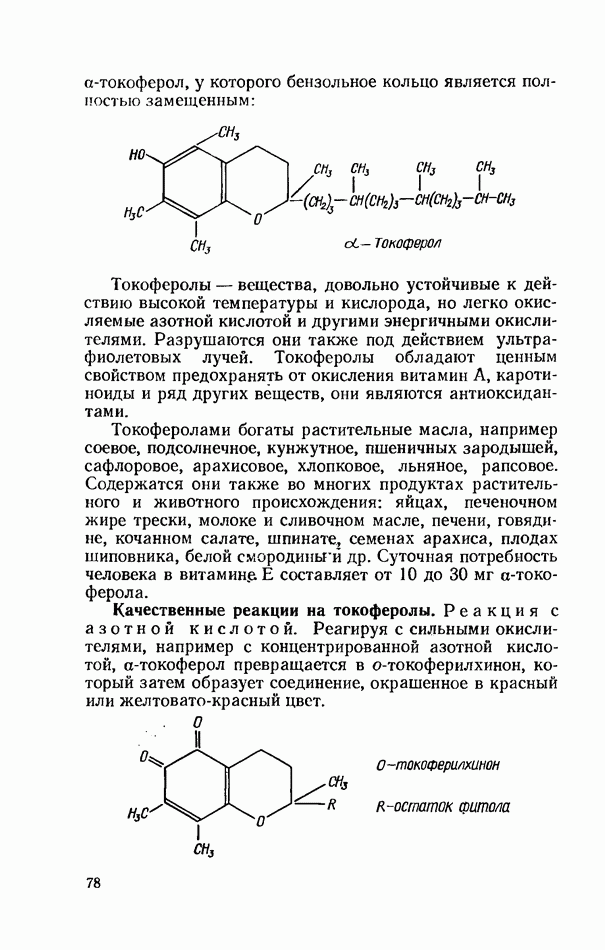
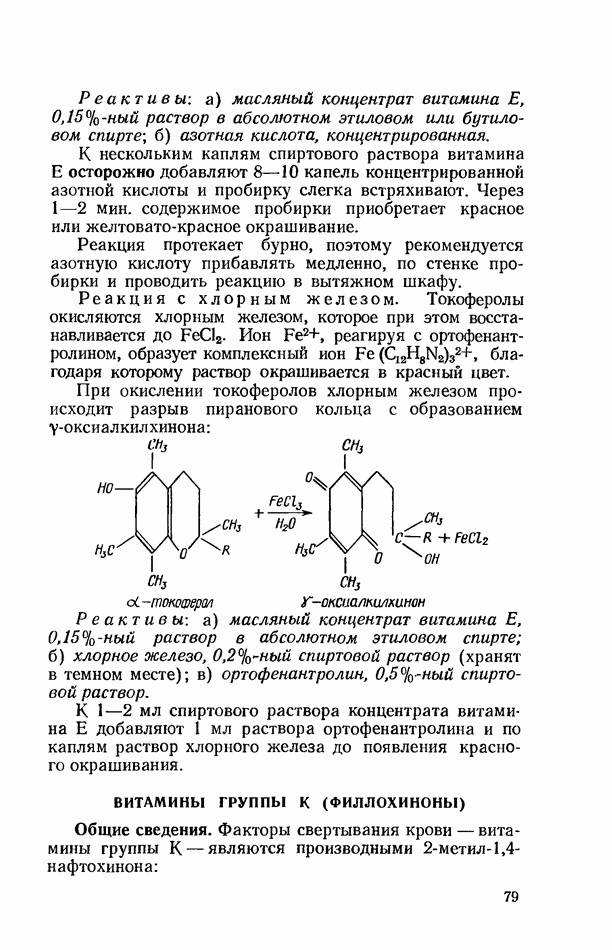
- ВИТАМИНЫ ГРУППЫ Е (ТОКОФЕРОЛЫ)
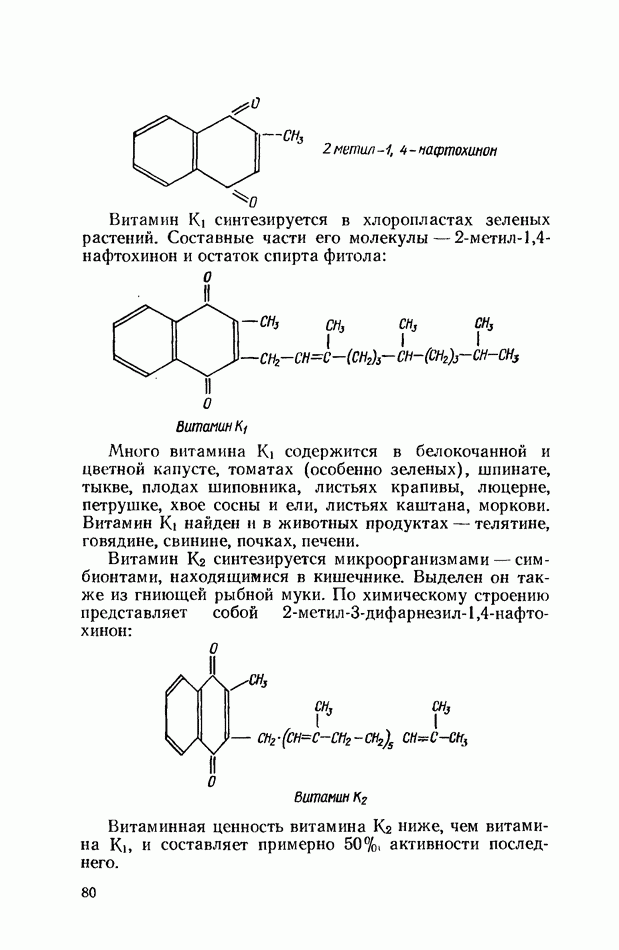
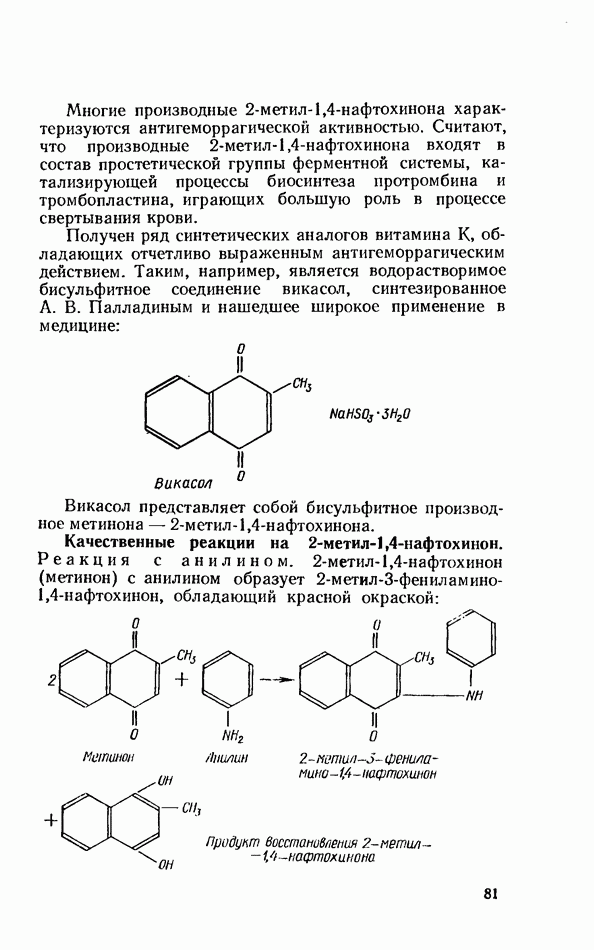
- ВИТАМИНЫ ГРУППЫ К (ФИЛЛОХИНОНЫ)
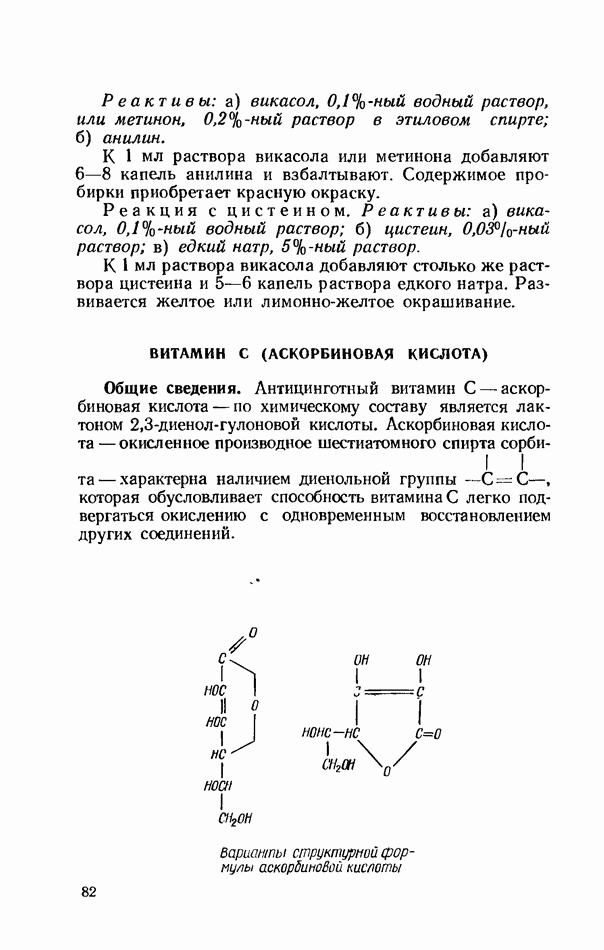
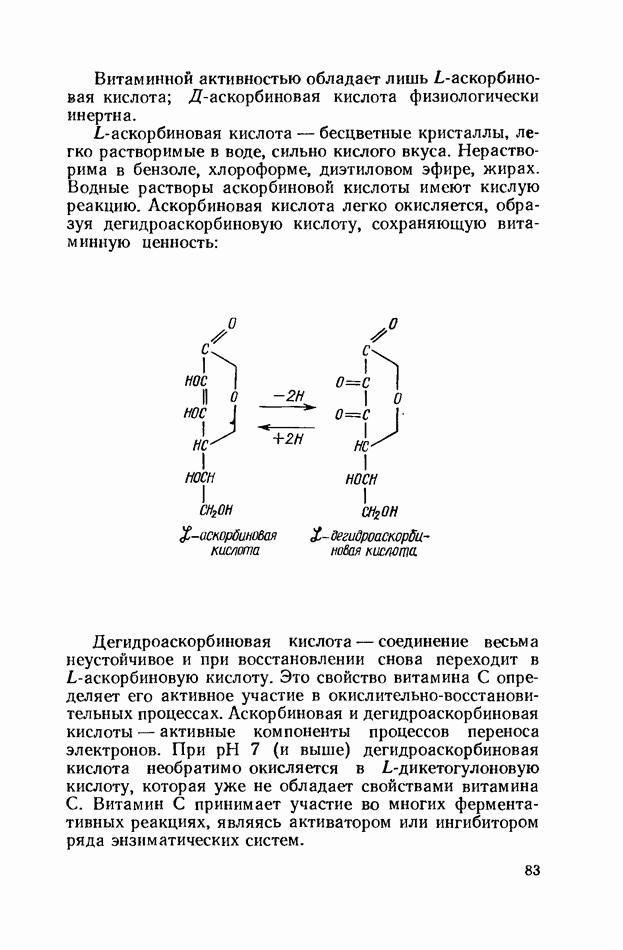
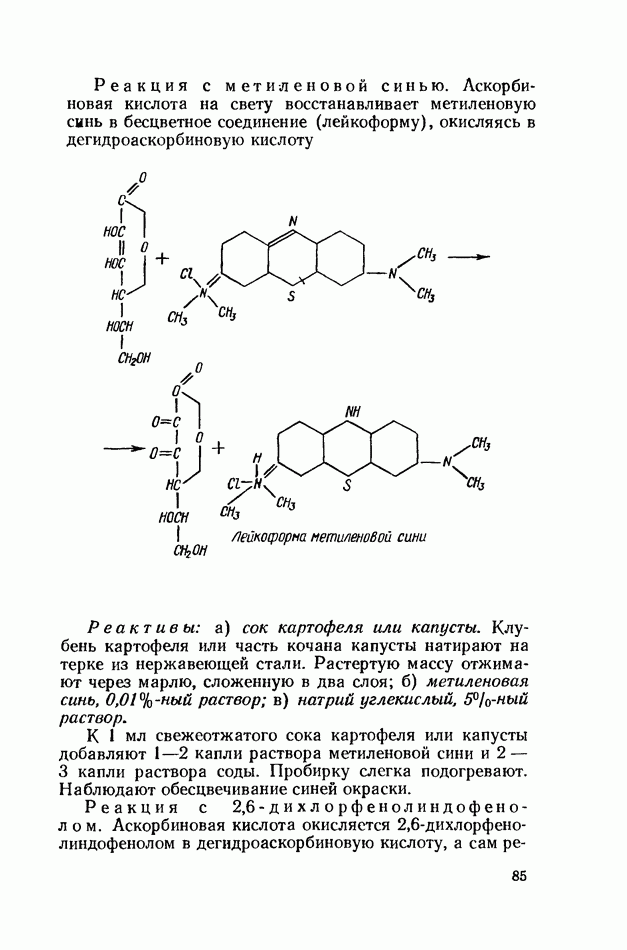
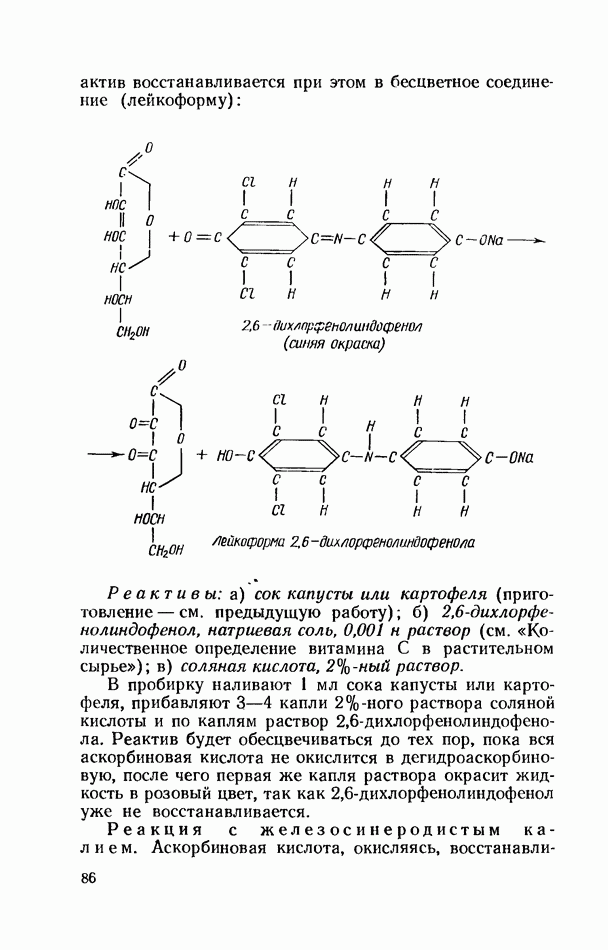
- ВИТАМИН С (АСКОРБИНОВАЯ КИСЛОТА)
- БИОФЛАВОНОИДЫ (ВЕЩЕСТВА Р-ВИТАМИННОГО ДЕЙСТВИЯ)
- ВИТАМИН В: (ТИАМИН)
- ВИТАМИН В2 (РИБОФЛАВИН)
- ВИТАМИН РР (В5, НИКОТИНОВАЯ КИСЛОТА, НИКОТИНАМИД)
- ВИТАМИН В6 (ПИРИДОКСИН)
- Раздел IV. ФЕРМЕНТЫ (ЭНЗИМЫ)
- ИССЛЕДОВАНИЕ ОБЩИХ СВОЙСТВ ФЕРМЕНТОВ
- ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ГИДРОЛИТИЧЕСКИХ ФЕРМЕНТОВ (ГИДРОЛАЗ)
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ФЕРМЕНТЫ (ОКСИДОРЕДУКТАЗЫ)
- Раздел V. ОБМЕН АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО АЗОТА ПО КЪЕЛЬДАЛЮ (МИКРОМЕТОД)
- ОПРЕДЕЛЕНИЕ БЕЛКОВОГО И НЕБЕЛКОВОГО АЗОТА
- БЫСТРЫЙ МЕТОД КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕЛКОВ
- ОПРЕДЕЛЕНИЕ АЗОТА АМИНОКИСЛОТ
- ОПРЕДЕЛЕНИЕ СВОБОДНЫХ АМИНОКИСЛОТ В МЫШЕЧНОЙ ТКАНИ МЕТОДОМ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ (по Г. В. Колоболотскому)
- ГИДРОЛИТИЧЕСКОЕ РАСЩЕПЛЕНИЕ БЕЛКА ФЕРМЕНТАМИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
- ПЕРЕАМИНИРОВАНИЕ (ТРАНСАМИНИРОВАНИЕ) АМИНОКИСЛОТ
- Раздел VI. ХИМИЯ И ОБМЕН ЛИПИДОВ
- ЖИРЫ (НЕЙТРАЛЬНЫЕ ЖИРЫ)
- ФОСФАТИДЫ, ИЛИ ФОСФОЛИПИДЫ
- СТЕРИНЫ
- ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ ЛИПИДОВ
- КЕТОНОВЫЕ ТЕЛА
- Раздел VII. ХИМИЯ И ОБМЕН УГЛЕВОДОВ
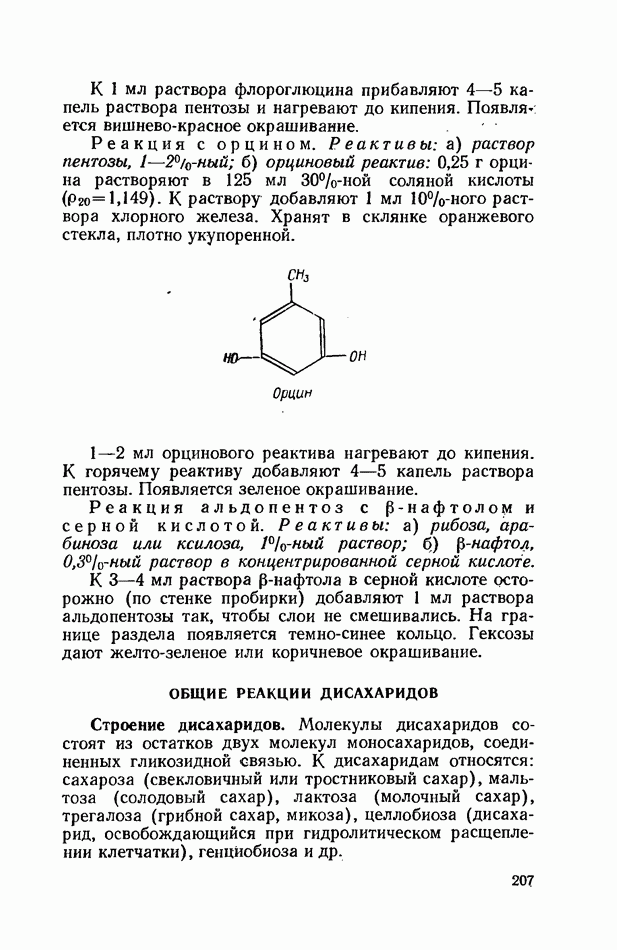
- КАЧЕСТВЕННЫЕ РЕАКЦИИ НА МОНОСАХАРИДЫ
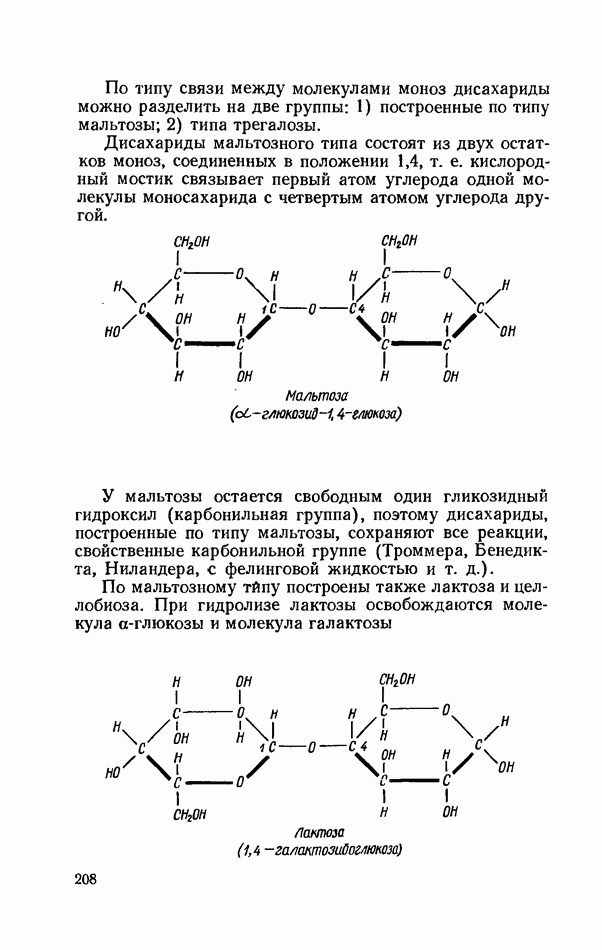
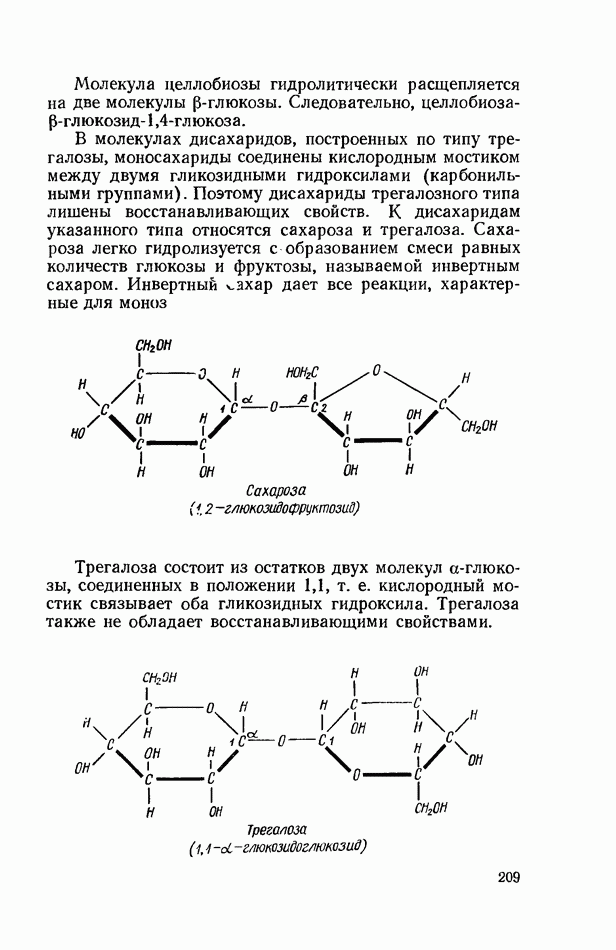
- ОБЩИЕ РЕАКЦИИ ДИСАХАРИДОВ
- ВЫСШИЕ ПОЛИСАХАРИДЫ
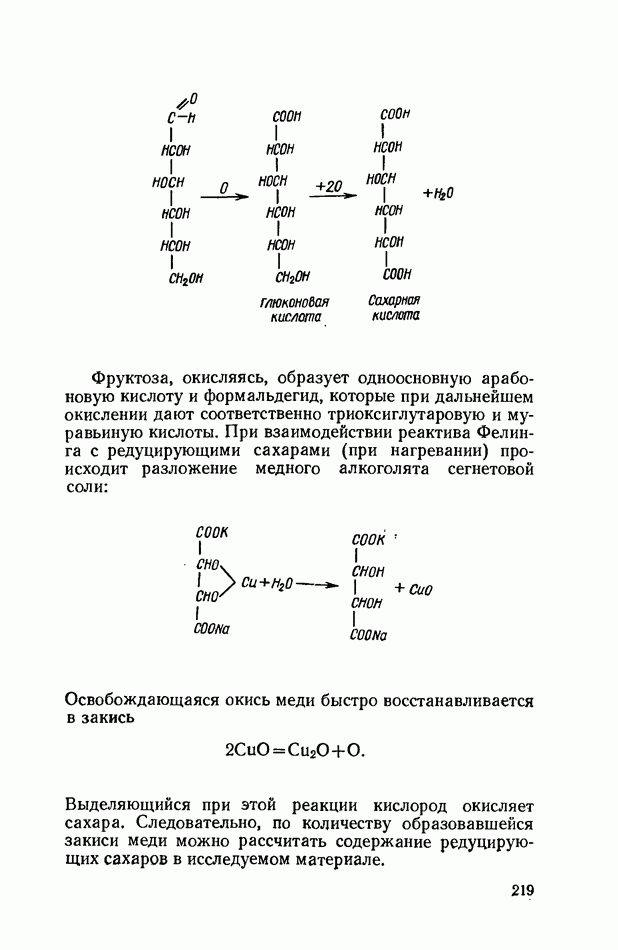
- ОПРЕДЕЛЕНИЕ РЕДУЦИРУЮЩИХ (ВОССТАНАВЛИВАЮЩИХ) САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ
- ФОТОМЕТРИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РЕДУЦИРУЮЩИХ САХАРОВ
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ С ПОМОЩЬЮ ХРОМАТОГРАФИИ НА БУМАГЕ (по О. А. Павлиновой)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ В КРОВИ (по Хагедорну — Иеисену)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КРАХМАЛА
- ИССЛЕДОВАНИЕ АНАЭРОБНОГО РАСПАДА ГЛИКОГЕНА ИЛИ КРАХМАЛА
- ОПРЕДЕЛЕНИЕ ПИРОВИНОГРАДНОЙ КИСЛОТЫ В МОЧЕ
- Раздел VIII. ГОРМОНЫ
- ОТКРЫТИЕ ИОДА В ЩИТОВИДНОЙ ЖЕЛЕЗЕ
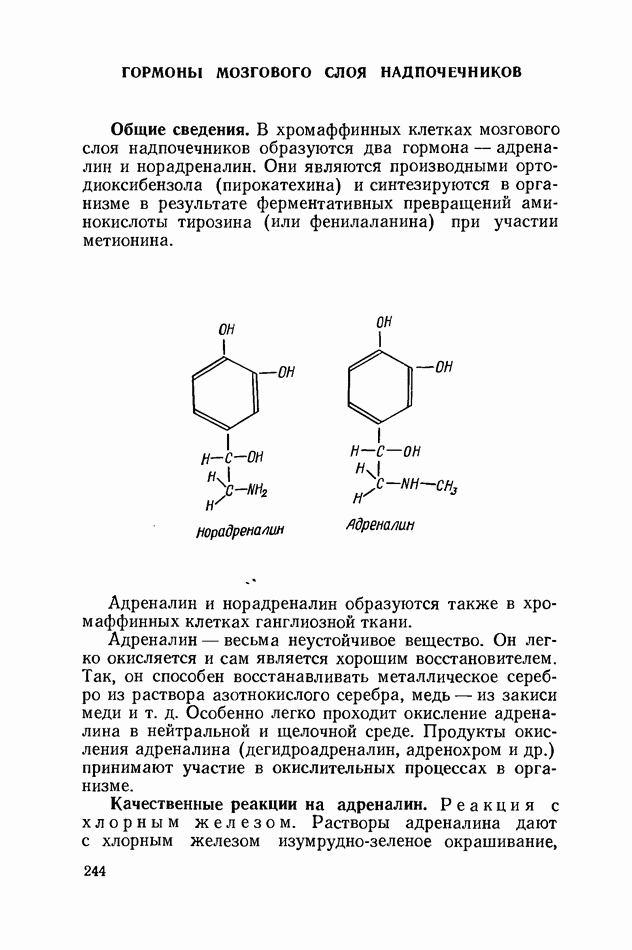
- ГОРМОНЫ МОЗГОВОГО СЛОЯ НАДПОЧЕЧНИКОВ
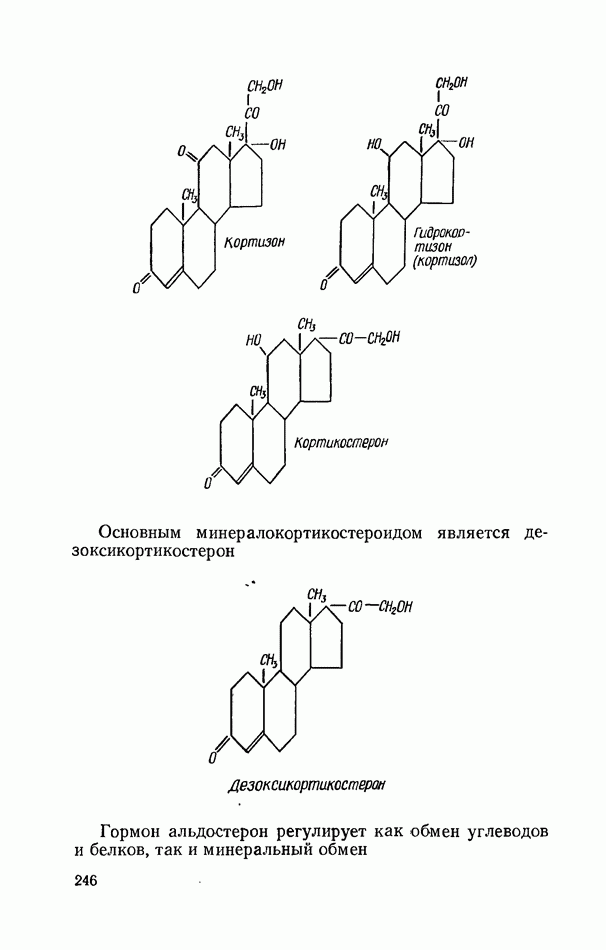
- ГОРМОНЫ КОРКОВОГО СЛОЯ НАДПОЧЕЧНИКОВ (КОРТИКОСТЕРОИДЫ)
- ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- Раздел IX. ОБМЕН МИНЕРАЛЬНЫХ ВЕЩЕСТВ
- ОПРЕДЕЛЕНИЕ КАЛЬЦИЯ В СЫВОРОТКЕ КРОВИ
- ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО СОДЕРЖАНИЯ ФОСФОРА В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА В ПЛАЗМЕ ИЛИ СЫВОРОТКЕ КРОВИ (по прописи П. А. Розенберг и Н. К. Бялко)
- ОПРЕДЕЛЕНИЕ ХЛОРИДОВ В ПИЩЕВЫХ ПРОДУКТАХ (по А. С. Вечеру и В. В. Малоян)
- ЛИТЕРАТУРА
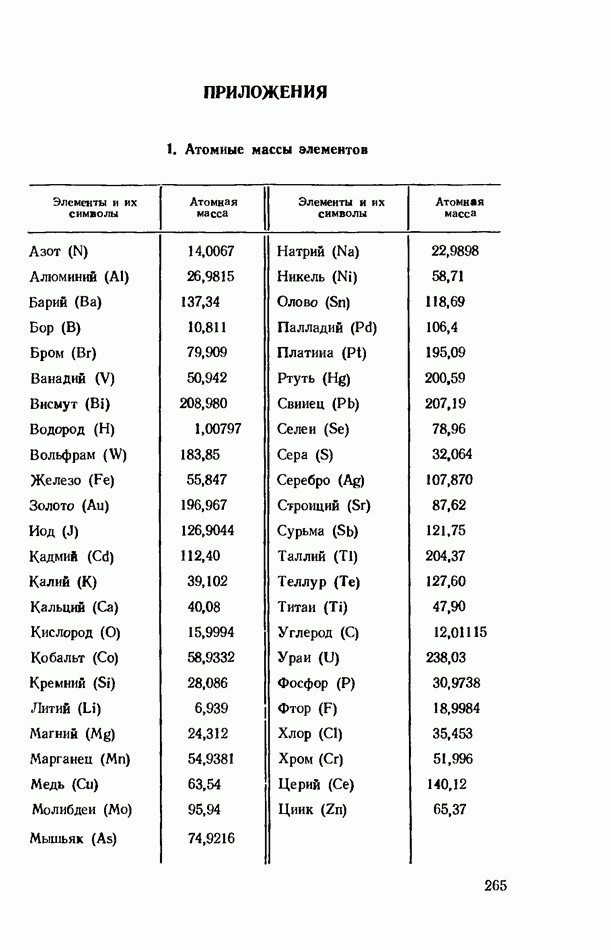
- ПРИЛОЖЕНИЯ