| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ФОТОМЕТРИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РЕДУЦИРУЮЩИХ САХАРОВ
Количественное определение сахаров по антроновому методу.
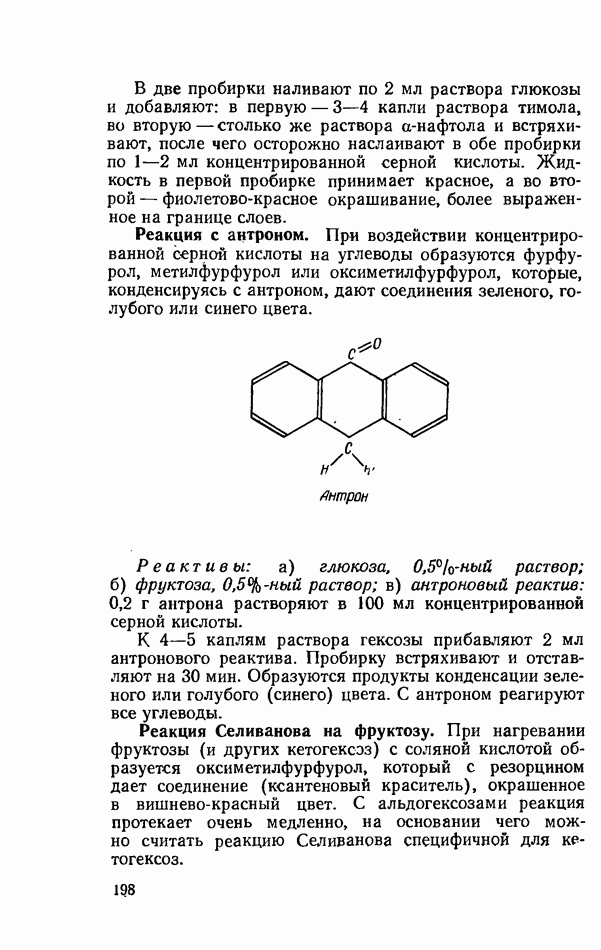
Химизм реакции — см. с. 198.
Реактивы и приборы: а) антроновый реактив: 0,2 г перекристаллизованного антрона растворяют в 100 мл 96%-ной серной кислоты  Употребляют только свежеприготовленный реактив. Продажный препарат антрона надо дважды перекристаллизовать из бензола или ледяной уксусной кислоты; б) стандартный раствор глюкозы: в 1 л кипящей воды растворяют 2,5 г бензойной кислоты. На аналитических весах отвешивают 1 г глюкозы. Навеску переносят в мерную колбу на 100 мл с помощью раствора бензойной кислоты, охлажденного до 20° С. Этим же раствором и доводят до метки. Стандартный раствор глюкозы хранят в склянке из темного стекла с притертой пробкой. Для приготовления калибровочной кривой стандартный раствор разбавляют, получая рабочие растворы с содержанием 20, 40, 60, 80 и 100 мкг глюкозы в 2 мл; в) фотоэлектроколориметр ФЭК-60, ФЭК-Н-57 или ФЭК-56, либо спектроколориметр «Спекол» (ГДР).
Употребляют только свежеприготовленный реактив. Продажный препарат антрона надо дважды перекристаллизовать из бензола или ледяной уксусной кислоты; б) стандартный раствор глюкозы: в 1 л кипящей воды растворяют 2,5 г бензойной кислоты. На аналитических весах отвешивают 1 г глюкозы. Навеску переносят в мерную колбу на 100 мл с помощью раствора бензойной кислоты, охлажденного до 20° С. Этим же раствором и доводят до метки. Стандартный раствор глюкозы хранят в склянке из темного стекла с притертой пробкой. Для приготовления калибровочной кривой стандартный раствор разбавляют, получая рабочие растворы с содержанием 20, 40, 60, 80 и 100 мкг глюкозы в 2 мл; в) фотоэлектроколориметр ФЭК-60, ФЭК-Н-57 или ФЭК-56, либо спектроколориметр «Спекол» (ГДР).
Экстракцию сахаров из материала и осаждение белков, пигментов, дубильных веществ производят, как описано в работе «Определение редуцирующих (восстанавливающих) сахаров в растительном материале».
В две пробирки вносят по 4 мл антронового реактива. Пробирки ставят в сосуд с проточной холодной водой и затем в одну из них, помешивая стеклянной палочкой, осторожно наливают 2 мл испытуемого раствора (в которых должно содержаться не более 100 мкг сахара). В другую пробирку добавляют 2 мл воды (контроль). Обе пробирки ставят на 14 мин. в баню с горячей водой (90°С), после чего охлаждают под краном и колориметрируют в фотоэлектроколориметре с красным светофильтром ( нм) против контрольного раствора, установленного на нуль. Толщина слоя жидкости в кюветах 0,5 см.
нм) против контрольного раствора, установленного на нуль. Толщина слоя жидкости в кюветах 0,5 см.
Содержание сахара в испытуемом растворе рассчитывают по калибровочной кривой, составленной по стандартным (рабочим) растворам глюкозы. На оси абсцисс откладывают величины, характеризующие содержание
держание сахара  а на оси ординат — оптическую плотность. Калибровочную кривую для каждого прибора проверяют
а на оси ординат — оптическую плотность. Калибровочную кривую для каждого прибора проверяют  раза в год.
раза в год.
Количественное определение сахаров по реакции с пикриновой кислотой.
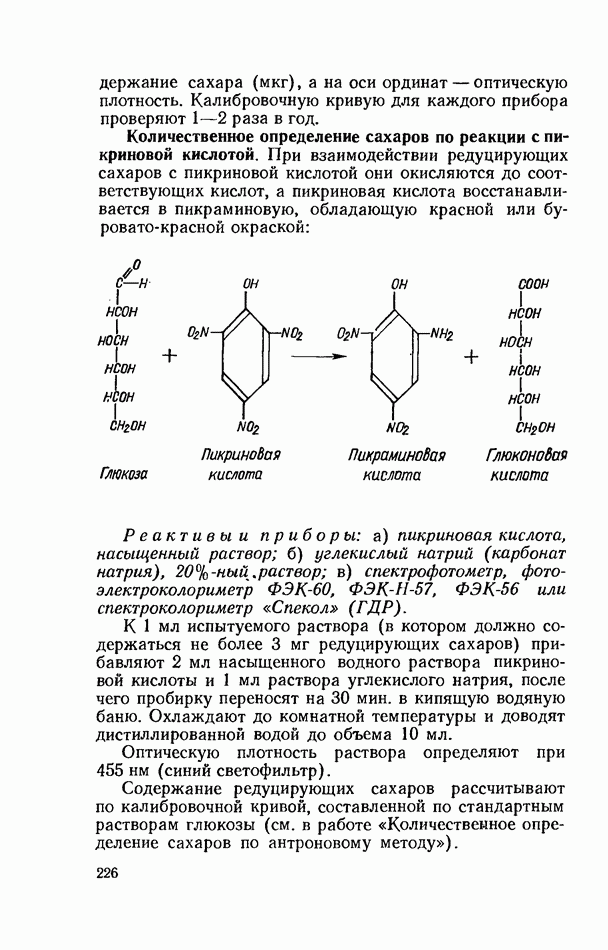
При взаимодействии редуцирующих сахаров с пикриновой кислотой они окисляются до соответствующих кислот, а пикриновая кислота восстанавливается в пикраминовую, обладающую красной или буровато-красной окраской:

Реактивы и приборы: а) пикриновая кислота, насыщенный раствор; б) углекислый натрий (карбонат натрия), 20%-ный раствор; в) спектрофотометр, фотоэлектроколориметр  ФЭК-Н-57,
ФЭК-Н-57,  или спектроколориметр «Спекол» (ГДР).
или спектроколориметр «Спекол» (ГДР).
К 1 мл испытуемого раствора (в котором должно содержаться не более 3 мг редуцирующих сахаров) прибавляют 2 мл насыщенного водного раствора пикриновой кислоты и 1 мл раствора углекислого натрия, после чего пробирку переносят на 30 мин. в кипящую водяную баню. Охлаждают до комнатной температуры и доводят дистиллированной водой до объема 10 мл.
Оптическую плотность раствора определяют при 455 нм (синий светофильтр).
Содержание редуцирующих сахаров рассчитывают по калибровочной кривой, составленной по стандартным растворам глюкозы (см. в работе «Количественное определение сахаров по антроновому методу»).
Метод пригоден для количественного определения глюкозы, галактозы, арабинозы, фруктозы, рамнозы, ксилозы, мальтозы, лактозы и крахмала.
Определение редуцирующих сахаров по реакции с 3,5-динитросалициловой кислотой. При взаимодействии сахаров с 3,5-динитросалициловой кислотой последняя восстанавливается в 3-амино-5-нитросалициловую. В остальном реакция протекает так же, как и с пикриновой кислотой.
Реактивы и приборы: а) динитросалициловый реактив: в мерной колбе на 1 л растворяют в дистиллированной воде 10 г 3,5-динитросалициловой кислоты, 300 г сегнетовой соли, 16 г едкого натра и доводят водой до метки. Раствор выдерживают два дня в темном месте, затем фильтруют в склянку оранжевого стекла и хранят в темноте; б) спектрофотометр, фотоэлектроколориметр ФЭК-60, ФЭК-Н-57, ФЭК-56 или спектроколориметр «Спекол» (ГДР).
К 1 мл испытуемого раствора (с содержанием не более 2 мг редуцирующих сахаров) прибавляют 2 мл динитросалицилового реактива, нагревают 5 мин. в кипящей водяной бане, охлаждают до комнатной температуры, после чего доводят до объема 25 мл.
Оптическую плотность раствора определяют при 530 нм (зеленый светофильтр).
| << Предыдущий параграф | Следующий параграф >> |
- Раздел I. ХИМИЯ АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- Приготовление растворов белка
- Цветные реакции
- Исследование физико-химических свойств белковых веществ
- Распределительная хроматография аминокислот на бумаге
- Разделение белка и низкомолекулярных примесей методом гельфильтрации на сефадексе G 25 (по Р. Мардашеву, А. А. Покровскому, Н. А. Павловой, с дополнениями)
- Электрофорез белков и аминокислот на бумаге
- Электрофорез белков в полиакриламидном геле (по В. Бжескому и 3. Канюга, с дополнениями)
- СЛОЖНЫЕ БЕЛКИ (ПРОТЕИДЫ)
- Гликопротеиды
- Фосфопротеиды
- Раздел II. НУКЛЕОПРОТЕИДЫ. НУКЛЕИНОВЫЕ КИСЛОТЫ
- ВЫДЕЛЕНИЕ ДЕЗОКСИРИБОНУКЛЕОПРОТЕИДОВ ИЗ ПЕЧЕНИ ИЛИ СЕЛЕЗЕНКИ
- КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ДНК
- ВЫДЕЛЕНИЕ НУКЛЕОПРОТЕИДОВ ИЗ ДРОЖЖЕЙ
- ГИДРОЛИЗ НУКЛЕОПРОТЕИДОВ
- ИССЛЕДОВАНИЕ ПРОДУКТОВ ГИДРОЛИЗА НУКЛЕОПРОТЕИДОВ
- ОЧИСТКА И РАЗДЕЛЕНИЕ НУКЛЕИНОВЫХ КИСЛОТ (по Шмидту и Таннгаузеру, в прописи Г. П. Георгиева)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ДНК (по Дише)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ РНК (по Мейбаум)
- ХРОМАТОГРАФИЯ НА БУМАГЕ ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ, НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ
- Раздел III. ВИТАМИНЫ
- ВИТАМИНЫ ГРУППЫ А
- ВИТАМИНЫ ГРУППЫ D (КАЛЬЦИФЕРОЛЫ)
- ВИТАМИНЫ ГРУППЫ Е (ТОКОФЕРОЛЫ)
- ВИТАМИНЫ ГРУППЫ К (ФИЛЛОХИНОНЫ)
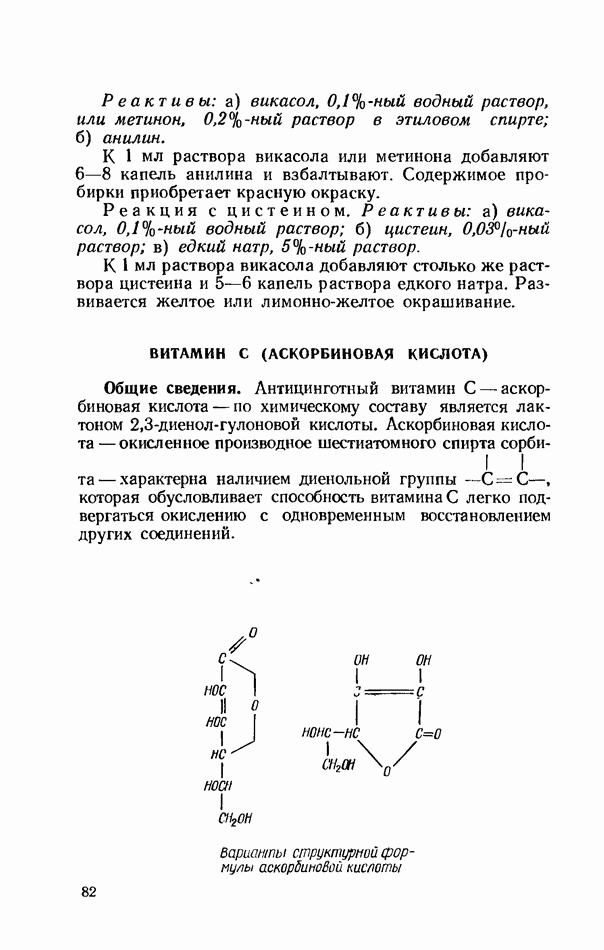
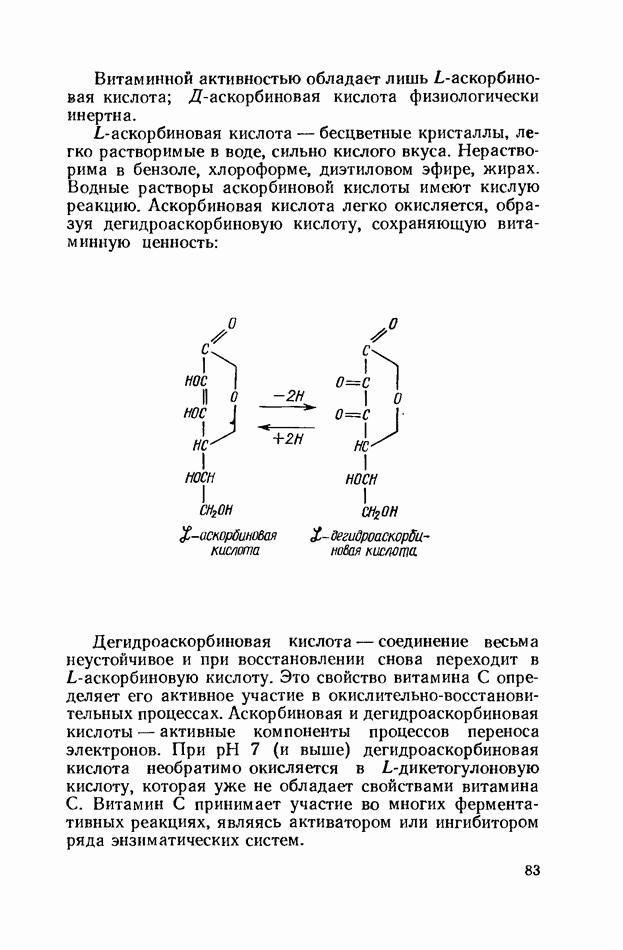
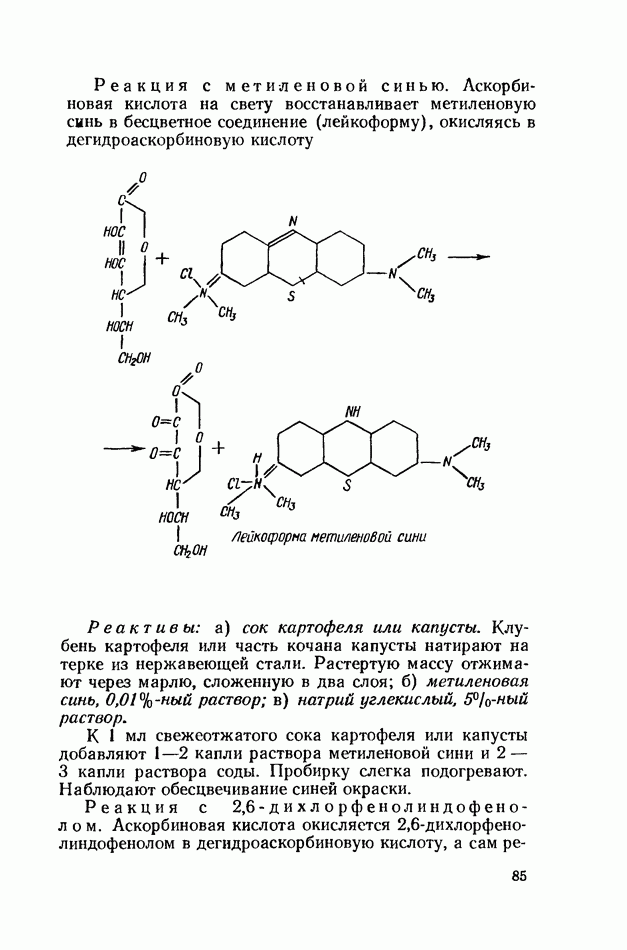
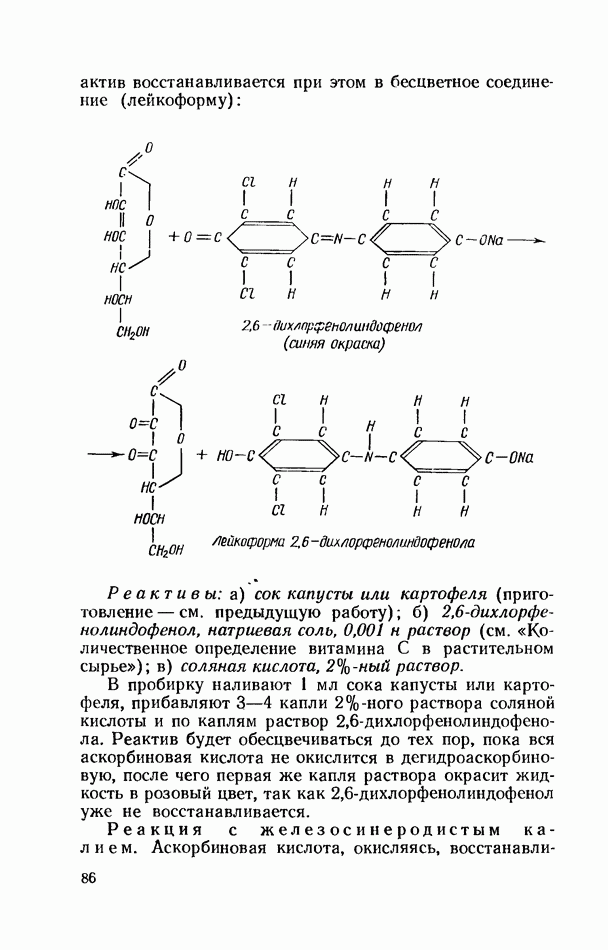
- ВИТАМИН С (АСКОРБИНОВАЯ КИСЛОТА)
- БИОФЛАВОНОИДЫ (ВЕЩЕСТВА Р-ВИТАМИННОГО ДЕЙСТВИЯ)
- ВИТАМИН В: (ТИАМИН)
- ВИТАМИН В2 (РИБОФЛАВИН)
- ВИТАМИН РР (В5, НИКОТИНОВАЯ КИСЛОТА, НИКОТИНАМИД)
- ВИТАМИН В6 (ПИРИДОКСИН)
- Раздел IV. ФЕРМЕНТЫ (ЭНЗИМЫ)
- ИССЛЕДОВАНИЕ ОБЩИХ СВОЙСТВ ФЕРМЕНТОВ
- ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ГИДРОЛИТИЧЕСКИХ ФЕРМЕНТОВ (ГИДРОЛАЗ)
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ФЕРМЕНТЫ (ОКСИДОРЕДУКТАЗЫ)
- Раздел V. ОБМЕН АМИНОКИСЛОТ, ПЕПТИДОВ И БЕЛКОВ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО АЗОТА ПО КЪЕЛЬДАЛЮ (МИКРОМЕТОД)
- ОПРЕДЕЛЕНИЕ БЕЛКОВОГО И НЕБЕЛКОВОГО АЗОТА
- БЫСТРЫЙ МЕТОД КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕЛКОВ
- ОПРЕДЕЛЕНИЕ АЗОТА АМИНОКИСЛОТ
- ОПРЕДЕЛЕНИЕ СВОБОДНЫХ АМИНОКИСЛОТ В МЫШЕЧНОЙ ТКАНИ МЕТОДОМ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ (по Г. В. Колоболотскому)
- ГИДРОЛИТИЧЕСКОЕ РАСЩЕПЛЕНИЕ БЕЛКА ФЕРМЕНТАМИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
- ПЕРЕАМИНИРОВАНИЕ (ТРАНСАМИНИРОВАНИЕ) АМИНОКИСЛОТ
- Раздел VI. ХИМИЯ И ОБМЕН ЛИПИДОВ
- ЖИРЫ (НЕЙТРАЛЬНЫЕ ЖИРЫ)
- ФОСФАТИДЫ, ИЛИ ФОСФОЛИПИДЫ
- СТЕРИНЫ
- ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ ЛИПИДОВ
- КЕТОНОВЫЕ ТЕЛА
- Раздел VII. ХИМИЯ И ОБМЕН УГЛЕВОДОВ
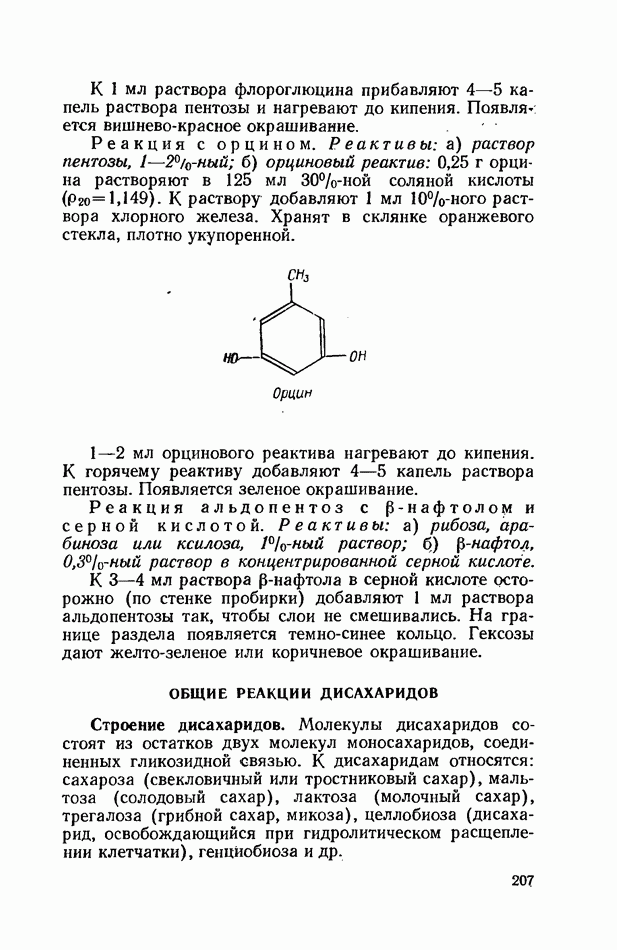
- КАЧЕСТВЕННЫЕ РЕАКЦИИ НА МОНОСАХАРИДЫ
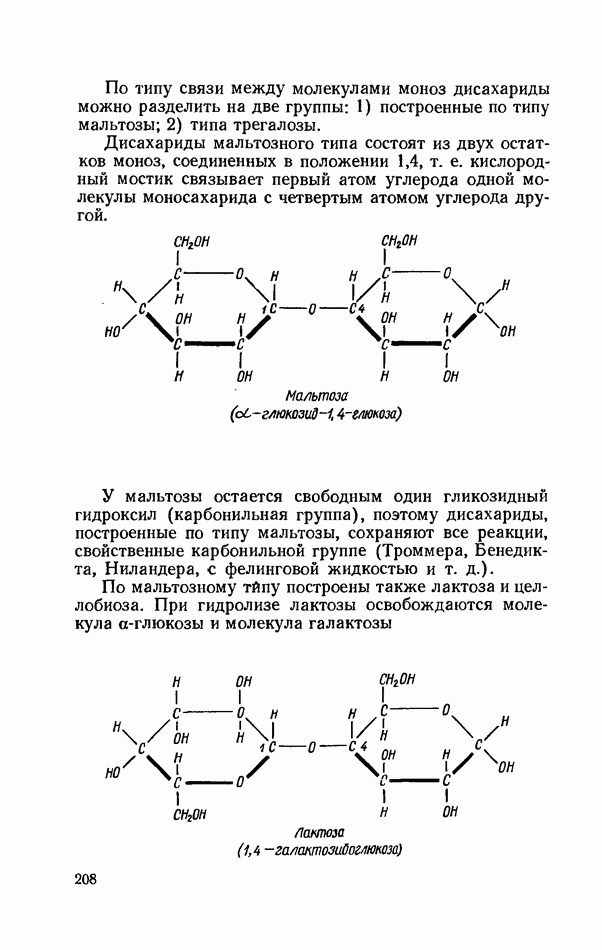
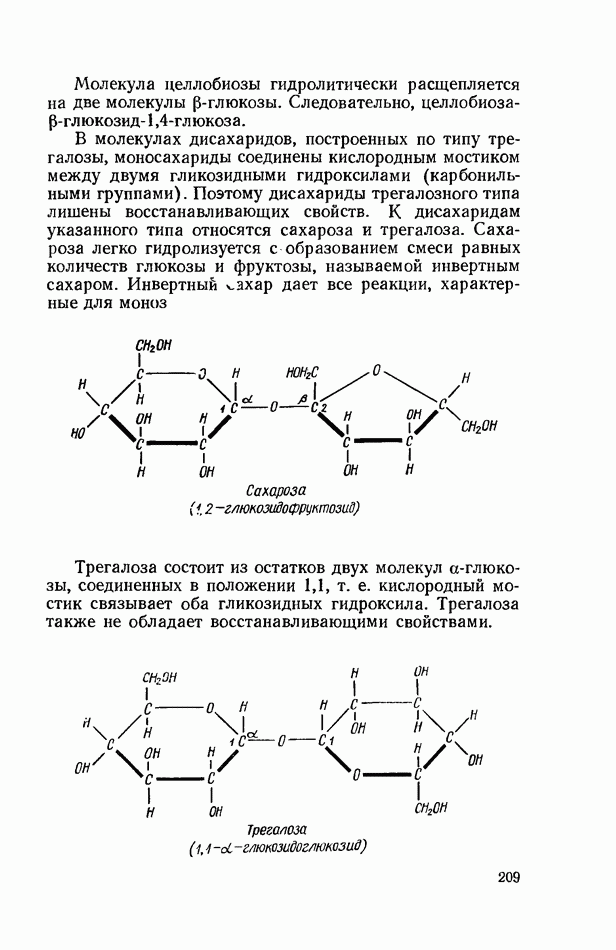
- ОБЩИЕ РЕАКЦИИ ДИСАХАРИДОВ
- ВЫСШИЕ ПОЛИСАХАРИДЫ
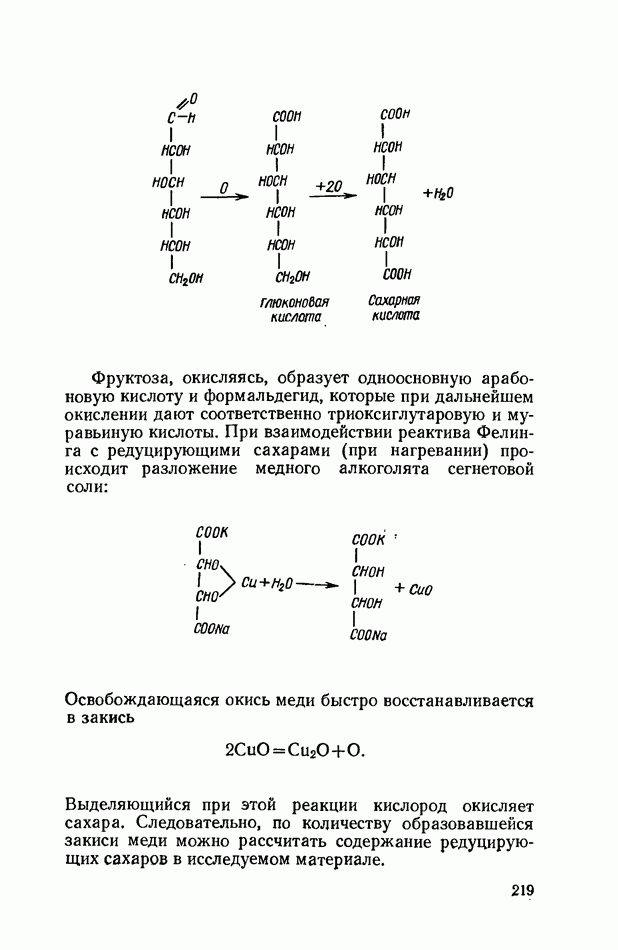
- ОПРЕДЕЛЕНИЕ РЕДУЦИРУЮЩИХ (ВОССТАНАВЛИВАЮЩИХ) САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ
- ФОТОМЕТРИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РЕДУЦИРУЮЩИХ САХАРОВ
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ САХАРОВ В РАСТИТЕЛЬНОМ МАТЕРИАЛЕ С ПОМОЩЬЮ ХРОМАТОГРАФИИ НА БУМАГЕ (по О. А. Павлиновой)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ В КРОВИ (по Хагедорну — Иеисену)
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КРАХМАЛА
- ИССЛЕДОВАНИЕ АНАЭРОБНОГО РАСПАДА ГЛИКОГЕНА ИЛИ КРАХМАЛА
- ОПРЕДЕЛЕНИЕ ПИРОВИНОГРАДНОЙ КИСЛОТЫ В МОЧЕ
- Раздел VIII. ГОРМОНЫ
- ОТКРЫТИЕ ИОДА В ЩИТОВИДНОЙ ЖЕЛЕЗЕ
- ГОРМОНЫ МОЗГОВОГО СЛОЯ НАДПОЧЕЧНИКОВ
- ГОРМОНЫ КОРКОВОГО СЛОЯ НАДПОЧЕЧНИКОВ (КОРТИКОСТЕРОИДЫ)
- ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
- Раздел IX. ОБМЕН МИНЕРАЛЬНЫХ ВЕЩЕСТВ
- ОПРЕДЕЛЕНИЕ КАЛЬЦИЯ В СЫВОРОТКЕ КРОВИ
- ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ОБЩЕГО СОДЕРЖАНИЯ ФОСФОРА В МОЛОКЕ
- ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА В ПЛАЗМЕ ИЛИ СЫВОРОТКЕ КРОВИ (по прописи П. А. Розенберг и Н. К. Бялко)
- ОПРЕДЕЛЕНИЕ ХЛОРИДОВ В ПИЩЕВЫХ ПРОДУКТАХ (по А. С. Вечеру и В. В. Малоян)
- ЛИТЕРАТУРА
- ПРИЛОЖЕНИЯ