| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
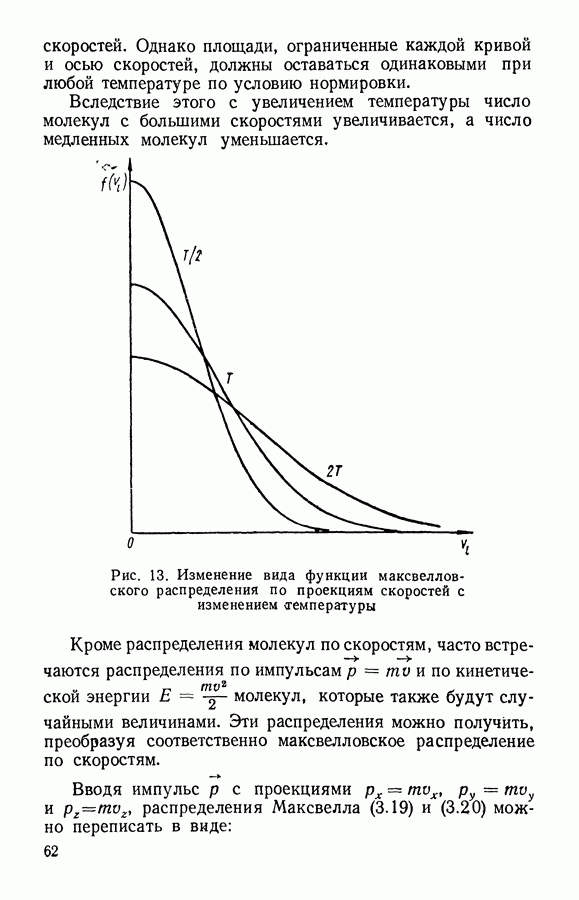
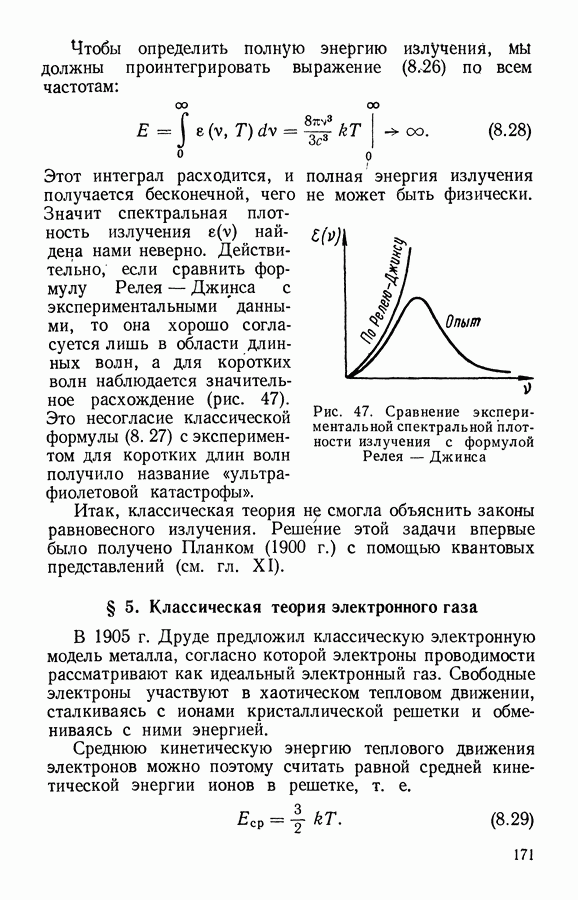
§ 2. Распределение молекул газа по скоростям
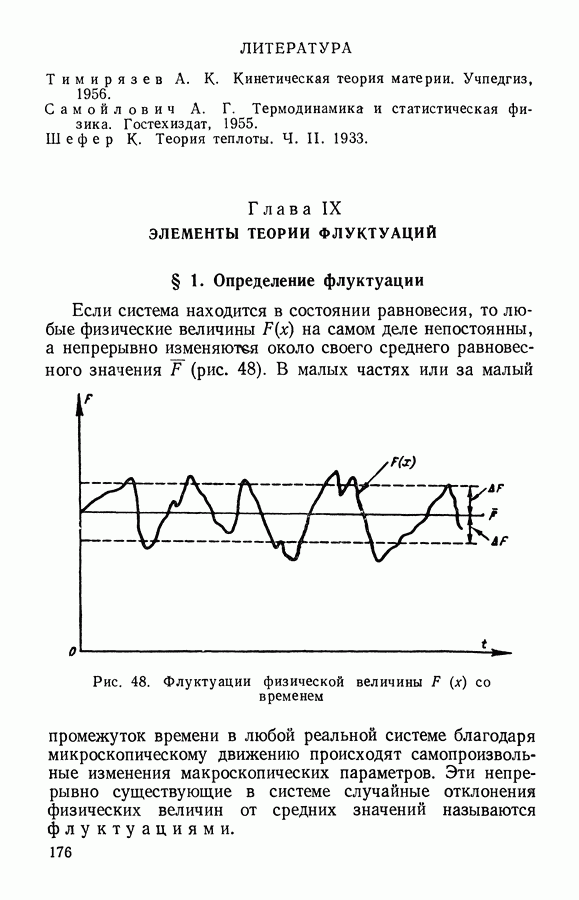
В предыдущем параграфе показано, что молекулы Газа участвуют в непрерывном хаотическом движении. В разные моменты времени молекулы имеют разные скорости, которым соответствует разное число молекул, но газ в целом не изменяет своих термодинамических параметров, находится в равновесии. Найдем соответствующее равновесному состоянию распределение молекул газа по скоростям, т. е. такое распределение, которое устанавливается в газе произвольно и которое в дальнейшем не изменяется вследствие молекулярного движения и столкновений.
Понятно, что в газе скорость одной молекулы при столкновениях будет меняться довольно разнообразно, так как молекула газа будет сталкиваться с другими молекулами газа, движущимися с разными скоростями. Такие столкновения будут случайными и скорость молекулы газа можно рассматривать как случайную величину.
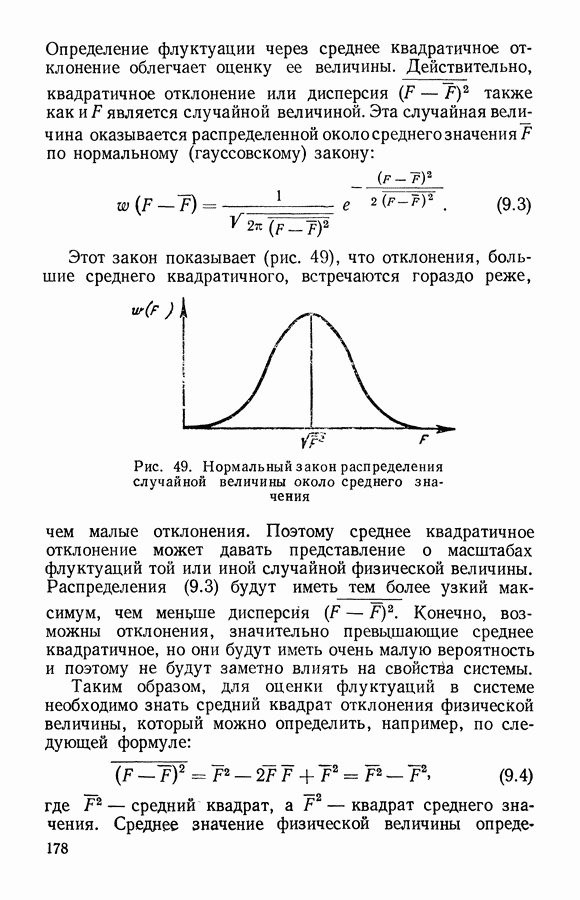
Будем искать распределение этой случайной величины исходя из картины движения молекул идеального газа. Во-первых, воспользуемся тем, что направления движения отдельных молекул газа во все стороны распределены равномерно. Другими словами, для молекул не существует какого-то избранного направления движения, и любое направление движения равновероятно.
Вследствие изотропности движения можно искать либо распределение скоростей молекул вдоль некоторого направления, либо распределение молекул по абсолютной величине скорости. Оказывается, что эти распределения связаны друг с другом. Абсолютная величина скорости молекулы, а также проекция скорости на любую ось могут принимать
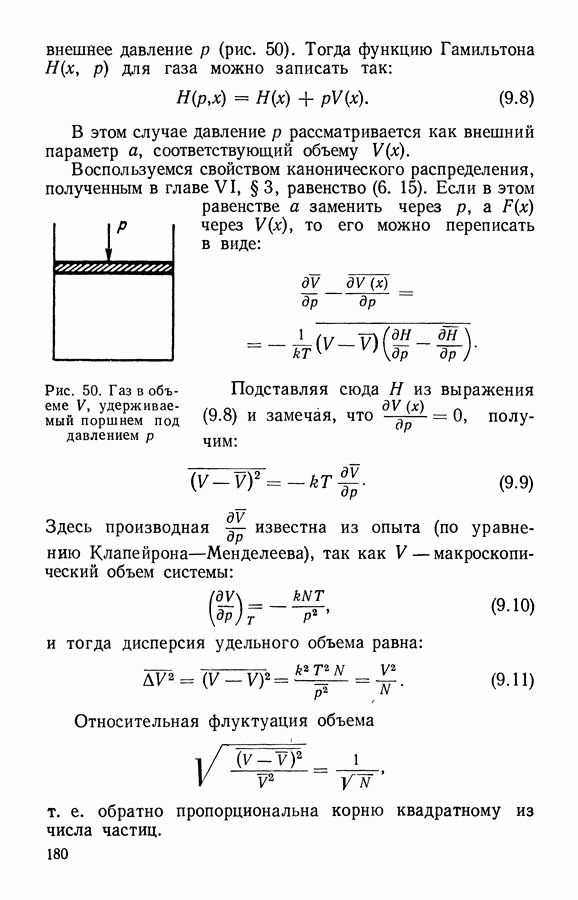
непрерывные значения от нуля и практически до бесконечности Значит должна существовать непрерывная функция распределения скоростей  Поскольку рассматривается состояние равновесия газа, то функция распределения не будет зависеть от времени.
Поскольку рассматривается состояние равновесия газа, то функция распределения не будет зависеть от времени.

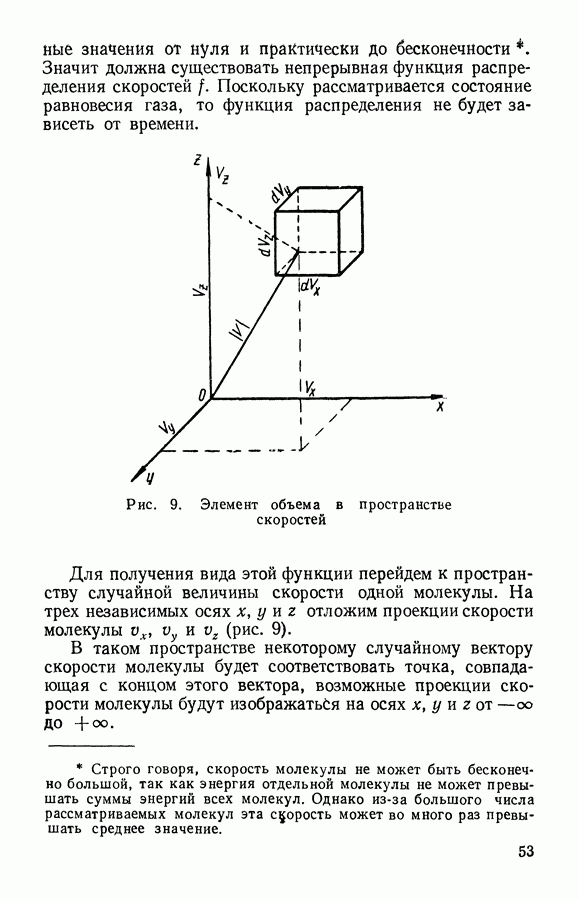
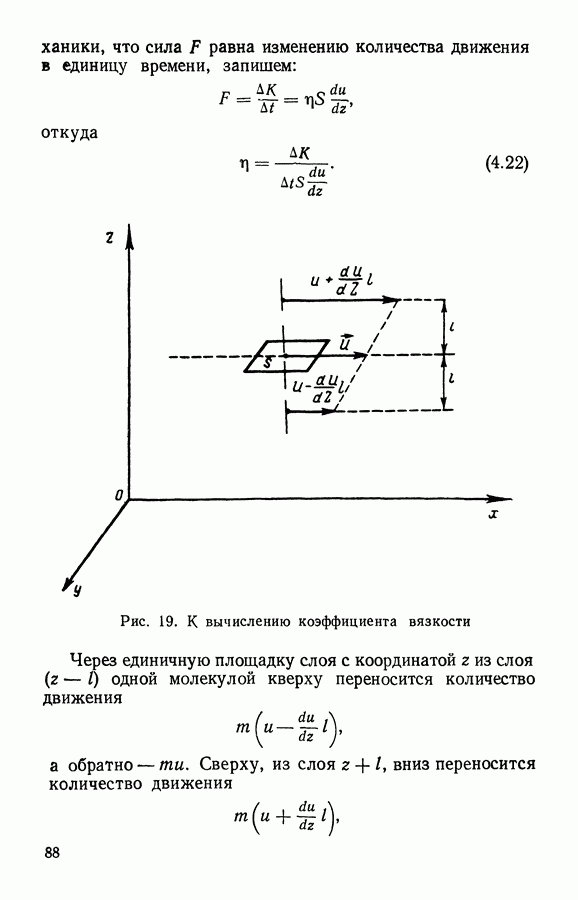
Рис. 9. Элемент объема в пространстве скоростей
Для получения вида этой функции перейдем к пространству случайной величины скорости одной молекулы. На трех независимых осях  отложим проекции скорости молекулы
отложим проекции скорости молекулы  (рис. 9).
(рис. 9).
В таком пространстве некоторому случайному вектору скорости молекулы будет соответствовать точка, совпадающая с концом этого вектора, возможные проекции скорости молекулы будут изображаться на осях  от
от 
Вероятность  что молекулы имеют проекцию скорости на ось
что молекулы имеют проекцию скорости на ось  в интервале от
в интервале от  до
до  будет определяться соотношением:
будет определяться соотношением:

где функция распределения  зависит только от величины проекции скорости. Но так как от изменения направления оси
зависит только от величины проекции скорости. Но так как от изменения направления оси  на обратное вероятность определенной проекции скорости не изменится, то функция распределения должна зависеть от
на обратное вероятность определенной проекции скорости не изменится, то функция распределения должна зависеть от 
Совершенно аналогично можно записать вероятности того, что молекула имеет проекции скорости на ось  от
от  до
до  и на ось
и на ось  от
от  до
до 

Здесь функции  из-за равноправности всех направлений имеют одинаковый вид и одинаковый постоянный множитель, определяемый условиями нормировки.
из-за равноправности всех направлений имеют одинаковый вид и одинаковый постоянный множитель, определяемый условиями нормировки.
Вероятность того, что у молекулы будет одновременно три проекции скорости  в интервалах
в интервалах  определится произведением трех вероятностей, если проекции скоростей молекулы рассматривать как независимые случайные величины:
определится произведением трех вероятностей, если проекции скоростей молекулы рассматривать как независимые случайные величины:

Равенство (3.2) определяет вероятность того, что скорость молекулы находится в элементарном объеме пространства скоростей  (см. рис. 9).
(см. рис. 9).
С другой стороны, наличие у молекулы трех проекций скорости  определяет направление движения и модуль скорости
определяет направление движения и модуль скорости

которые тоже будут случайными величинами.
Это направление движения является произвольным и распределение скоростей вдоль этого направления  должно иметь такой же вид, как и вдоль любой из осей.
должно иметь такой же вид, как и вдоль любой из осей.
Теперь вероятность нахождений молекулы в злементё пространства скоростей  с помощью функции
с помощью функции  имеющей другую нормировочную постоянную, можно записать так:
имеющей другую нормировочную постоянную, можно записать так:

Сравнивая вероятности (3.2) и (3.3), получим следующее уравнение:

из которого можно найти вид функции распределения скоростей 
Этому уравнению удовлетворяет функция  в виде
в виде

и

при любых значениях параметра а.
Предполагая, что проекция скорости, например  может принимать значения от
может принимать значения от  до
до  запишем условие нормировки:
запишем условие нормировки:

Этот интеграл сходится только при отрицательном показателе. Поэтому в дальнейшем, считая неопределенный параметр а положительным  функции распределения будем записывать в виде:
функции распределения будем записывать в виде:

Постоянную величину  определим из условия нормировки:
определим из условия нормировки:

Следовательно,

Вместо проекции на ось  можно взять проекции скорости молекулы на любое направление
можно взять проекции скорости молекулы на любое направление  Тогда распределение для проекций скорости
Тогда распределение для проекций скорости  на произвольное направление I запишется в виде:
на произвольное направление I запишется в виде:


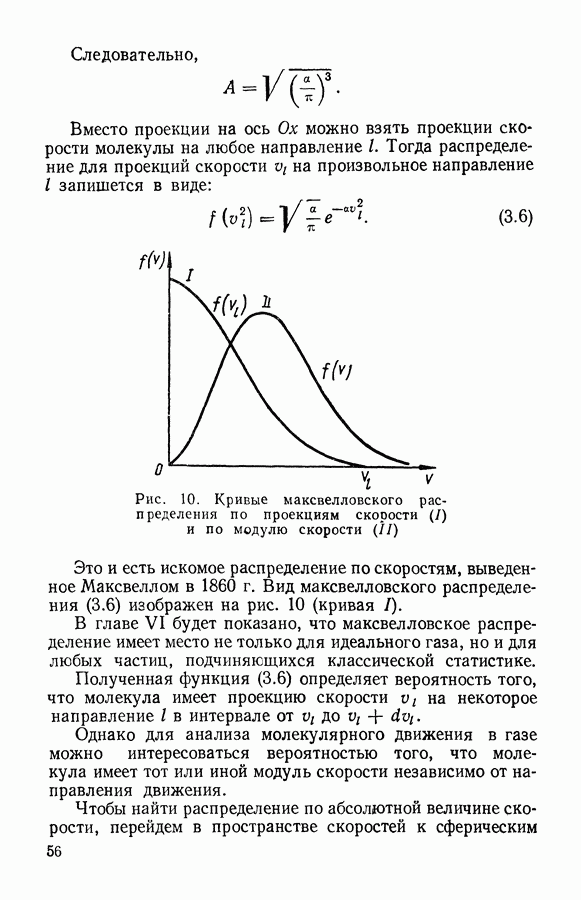
Рис. 10. Кривые максвелловского распределения по проекциям скорости  и по модулю скорости
и по модулю скорости 
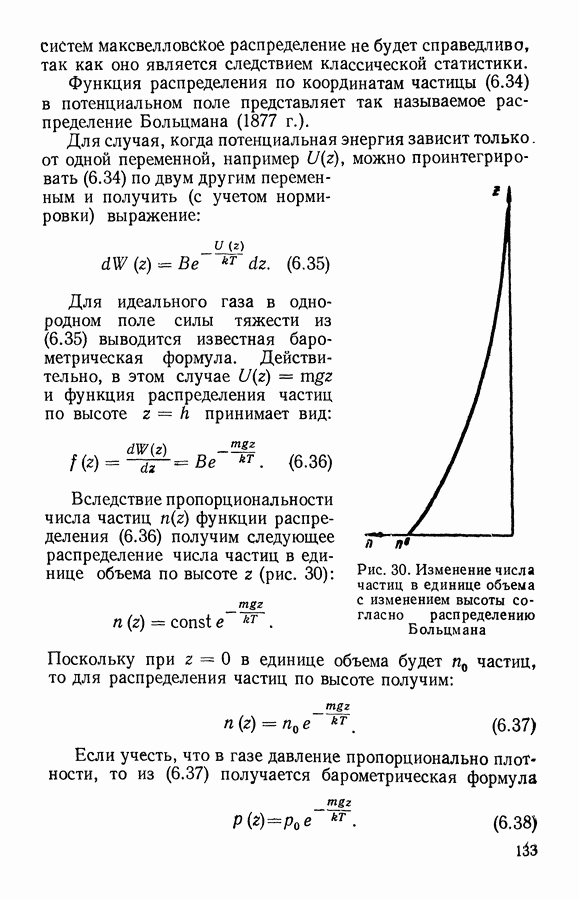
Это и есть искомое распределение по скоростям, выведенное Максвеллом в 1860 г. Вид максвелловского распределения (3.6) изображен на рис. 10 (кривая 
В главе VI будет показано, что максвелловское распределение имеет место не только для идеального газа, но и для любых частиц, подчиняющихся классической статистике.
Полученная функция (3.6) определяет вероятность того, что молекула имеет проекцию скорости  на некоторое направление I в интервале от
на некоторое направление I в интервале от  до
до 
Однако для анализа молекулярного движения в газе можно интересоваться вероятностью того, что молекула имеет тот или иной модуль скорости независимо от направления движения.
Чтобы найти распределение по абсолютной величине скорости, перейдем в пространстве скоростей к сферическим
координатам (см. §6, гл. II) и перепишем для этого случая равенство (3.3):

Так как движение молекул изотропно, то можно, интегрируя по углам, перейти к функции распределения только по модулю скорости 

Это и есть вероятность того, что молекула имеет модуль скорости  в интервале от
в интервале от  до
до  независимо от направления движения.
независимо от направления движения.
Функция распределения скоростей молекулы по модулю  будет иметь вид:
будет иметь вид:

Заменяя постоянную  можем переписать эту функцию в другом виде:
можем переписать эту функцию в другом виде:

Это распределение также называют максвелловским и его вид изображен на том же рис. 10 (кривая II).
Оба распределения (3.6) и (3.9) дают полное представление о движении молекул в газе.
Часто, особенно в практических приложениях, интересуются не распределением одной молекулы по скоростям, а числом молекул, имеющих данную скорость  или ее проекцию
или ее проекцию  в интервале
в интервале  или
или  соответственно. Если в системе имеется
соответственно. Если в системе имеется  частиц, то число частиц с проекцией скорости
частиц, то число частиц с проекцией скорости  в интервале от
в интервале от  до
до  или с модулем
или с модулем  от
от  до
до  определяется по формуле
определяется по формуле

где  соответствующая вероятность для одной молекулы. Заменяя
соответствующая вероятность для одной молекулы. Заменяя  с помощью (3.6) и по (3.9), получим:
с помощью (3.6) и по (3.9), получим:
для проекции скорости:

и для модуля скорости:

Соответственно функция распределения числа частиц будет нормирована не на единицу, а на полное число частиц  Между
Между  существует следующая связь:
существует следующая связь:

| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. Предмет и метод статистической физики
- § 2. К вопросу возникновения и развития молекулярно-кинетической теории материи
- § 3. Место статистической физики в раскрытии материалистической картины мира
- § 4. Феноменологические и молекулярно-кинетические теории
- § 5. Модельность в статистической физике. Классическая и квантовая модели вещества
- Глава II. НЕОБХОДИМЫЕ СВЕДЕНИЯ ИЗ ТЕОРИИ ВЕРОЯТНОСТЕЙ
- § 1. Случайные события и случайные величины
- § 2. Понятие вероятности
- § 3. Свойства вероятности. Формула сложения и умножения вероятностей
- § 4. Средние значения случайных величин
- § 5. Примеры законов распределения случайных величин
- § 6. Функция распределения для нескольких случайных величин
- ЧАСТЬ I. ЭЛЕМЕНТАРНАЯ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- § 1. Модель идеального газа
- § 2. Распределение молекул газа по скоростям
- § 3. Связь распределения Максвелла по скоростям с абсолютной температурой
- § 4. Характерные скорости максвелловского распределения
- § 5. Средние относительные скорости
- § 6. Соответствие модели идеального газа реальному газу
- Глава IV. ЭЛЕМЕНТЫ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ НЕРАВНОВЕСНЫХ ПРОЦЕССОВ
- § 1. Неравновесные состояния. Явления релаксации и переноса
- § 2. Поперечные сечения. Длина свободного пробега
- § 3. Распределение свободных пробегов частиц
- § 4. Вязкость газов
- § 5. Теплопроводность газов
- § 6. Диффузия газов
- ЧАСТЬ II. КЛАССИЧЕСКАЯ СТАТИСТИЧЕСКАЯ ФИЗИКА
- § 1. Невозможность последовательного механического описания физических систем многих частиц
- § 2. Макроскопическое и микроскопическое описание системы в термодинамическом равновесии
- § 3. Изображение системы в фазовом пространстве
- § 4. Элемент фазового объема. Вероятность нахождения системы в фазовом пространстве
- § 5. Теорема о сохранении фазового объема (Теорема Лиувилля)
- § 6. Макроскопические величины как фазовые средние
- Глава VI. СТАЦИОНАРНЫЕ ФУНКЦИИ РАСПРЕДЕЛЕНИЯ
- § 1. Микроканоническое распределение
- § 2. Каноническое распределение Гиббса
- § 3. Свойства канонического распределения
- § 4. Физический смысл параметров канонического распределения
- § 5. Энтропия и ее связь с вероятностью состояния
- § 6. Распределение Максвелла-Больцмана
- § 7. Большое каноническое распределение Гиббса
- Глава VII. ПРИМЕНЕНИЕ РАСПРЕДЕЛЕНИЯ ГИББСА К РЕАЛЬНЫМ СИСТЕМАМ
- § 1. Выражение термодинамических функций через интеграл состояний
- § 2. Интеграл состояний и термодинамические функции идеального газа
- § 3. Статистическое рассмотрение системы взаимодействующих частиц
- § 4. Вывод уравнения состояния реального газа
- § 5. Статистика диэлектриков
- Глава VIII. РАВНОМЕРНОЕ РАСПРЕДЕЛЕНИЕ КИНЕТИЧЕСКОЙ ЭНЕРГИИ ПО СТЕПЕНЯМ СВОБОДЫ
- § 1. Теорема о равномерном распределении энергии по степеням свободы
- § 2. Теплоемкость разреженных газов
- § 3. Теплоемкость твердых тел
- § 4. Применение методов статистической физики к равновесному излучению
- § 5. Классическая теория электронного газа
- Глава IX. ЭЛЕМЕНТЫ ТЕОРИИ ФЛУКТУАЦИЙ
- § 2. Связь флуктуаций со свободной энергией. Корреляция
- § 3. Чувствительность различных измерительных приборов
- § 4. Рассеяние света на флуктуациях плотности
- § 5. Броуновское движение
- § 6. Статистика полимеров
- ЧАСТЬ III. КВАНТОВАЯ СТАТИСТИЧЕСКАЯ ФИЗИКА
- § 1. Квантовые системы и их свойства
- § 2. Описание квантовых систем
- § 3. Применение статистического метода к квантовым системам
- § 4. Метод ячеек Больцмана
- § 5. Статистики квантовых систем
- § 6. Сопоставление статистик Максвелла-Больцмана, Бозе-Эйнштейна и Ферми-Дирака
- Глава XI. ЛОКАЛИЗОВАННЫЕ КВАНТОВЫЕ СИСТЕМЫ
- § 1. Квантовый осциллятор и квантовый ротатор
- § 2. Сумма по состояниям и внутренняя энергия систем осцилляторов и ротаторов
- § 3. Теплоемкость газов. Характеристические температуры
- § 4. Теплоемкость твердых тел. Закон Дебая
- § 5. Законы равновесного излучения
- § 6. Статистика парамагнетиков
- Глава XII. ПРИМЕНЕНИЕ СТАТИСТИК БОЗЕ — ЭЙНШТЕЙНА И ФЕРМИ — ДИРАКА
- § 1. Применение статистики Бозе — Эйнштейна к описанию системы частиц
- § 2. Равновесное излучение как фотонный газ
- § 3. Применение статистики Ферми — Дирака к описанию поведения системы частиц
- § 4. Электронный газ в металлах
- § 5. Магнитные свойства электронного газа
- § 6. Состояния систем с отрицательной абсолютной температурой
- ПРИЛОЖЕНИЯ.