| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
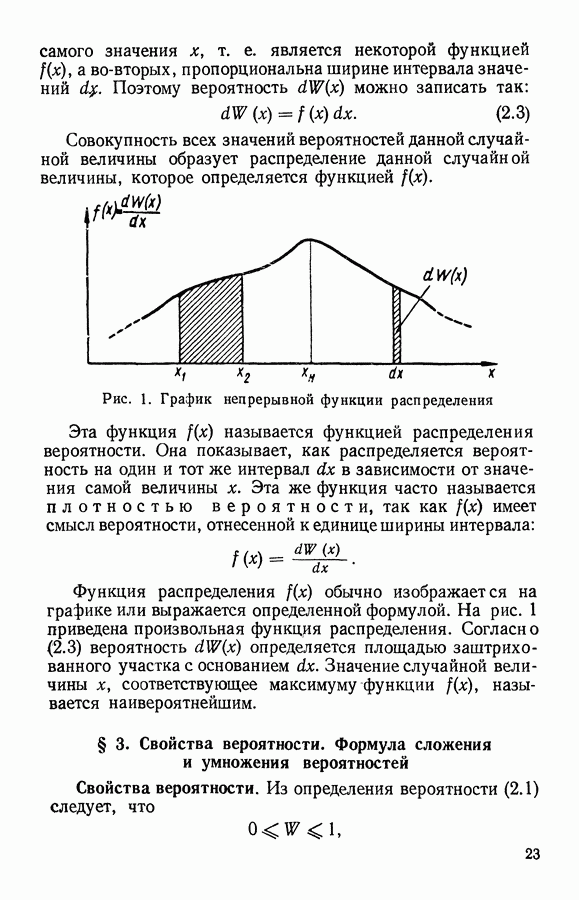
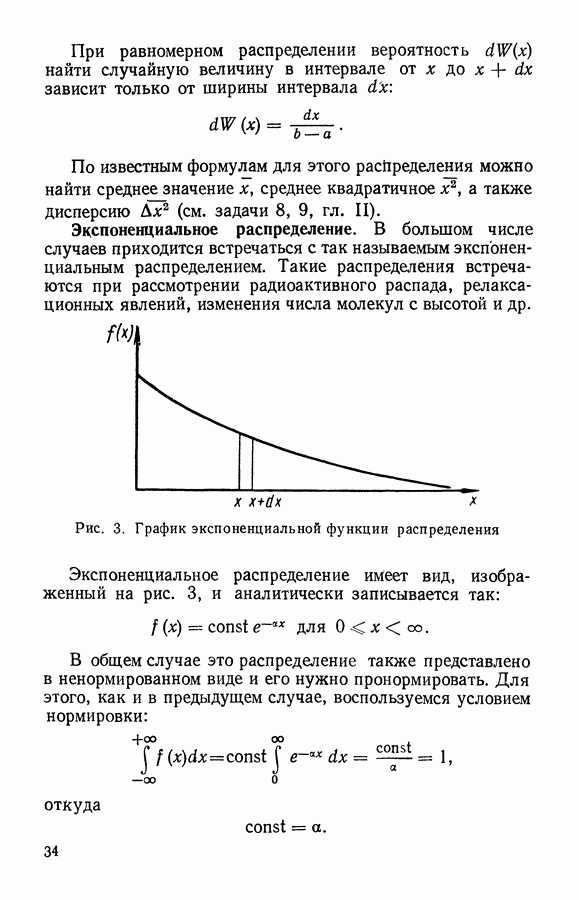
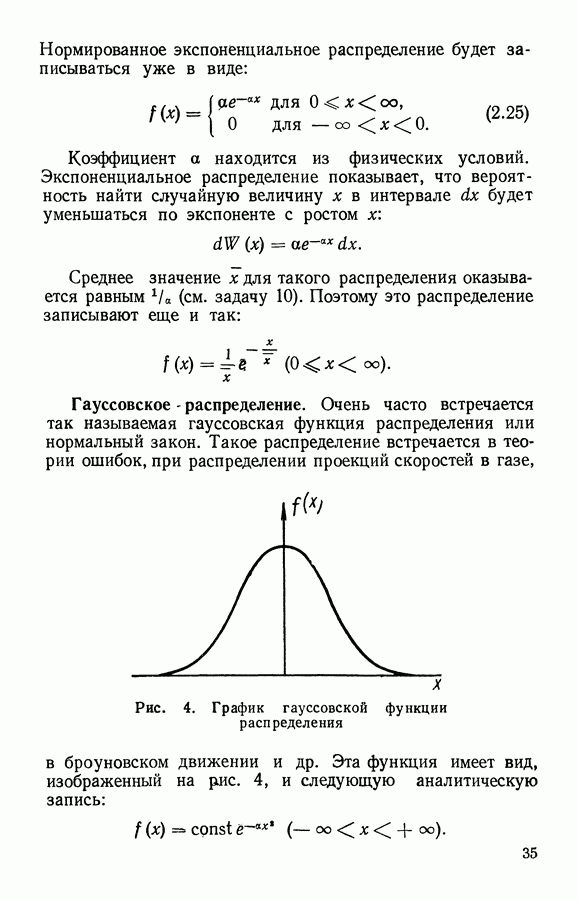
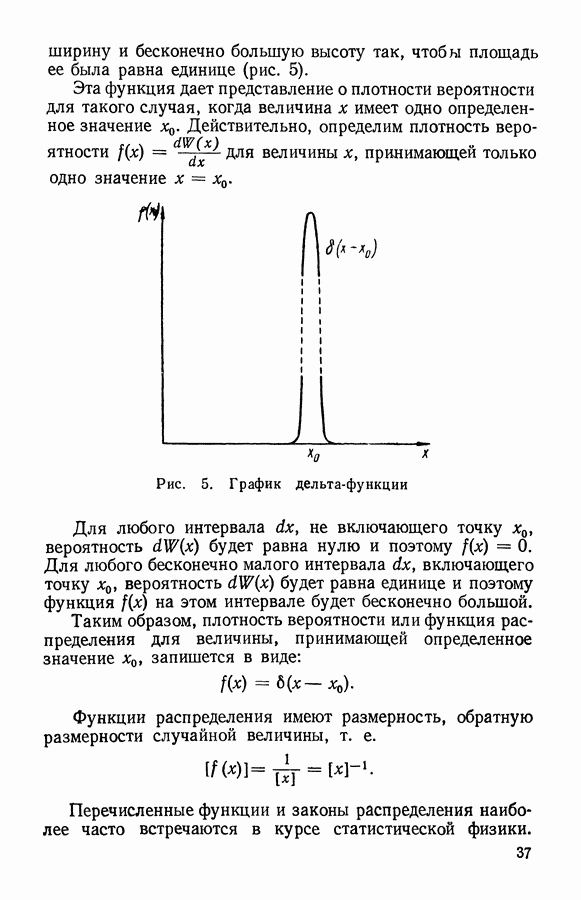
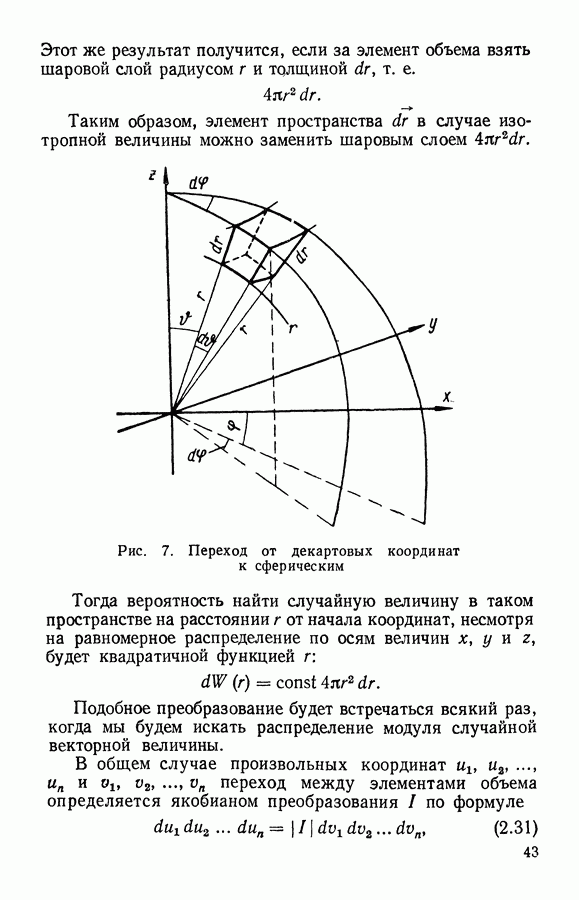
§ 3. Связь распределения Максвелла по скоростям с абсолютной температурой
В предыдущем параграфе мы получили распределение Максвелла с неопределенным параметром а, справедливое для разных газов при различных условиях. Однако при изменении температуры газа скорость хаотического движения молекул должна изменяться. С повышением температуры скорость молекул увеличивается, вследствие чего в распределении по скоростям должно увеличиваться число молекул с большими скоростями.
Такое изменение в распределении скоростей молекул с температурой может получаться лишь при наличии зависимости параметра а от температуры. Таким образом, самые общие соображения кинетической теории приводят к зависимости параметра а от температуры.
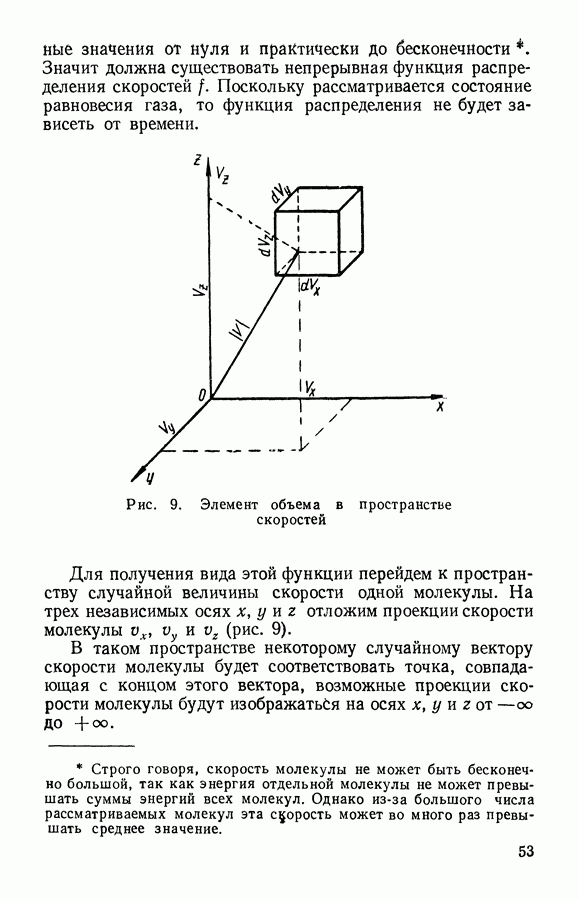
Но мы еще не ввели понятие температуры для механической модели идеального газа. Абсолютная температура — это термодинамический параметр. Чтобы придать ему статистический смысл, нужно приравнять статистические и термодинамические параметры системы. Выразим давление, оказываемое идеальным газом на неподвижную стенку, через параметр а максвелловского распределения и сравним с давлением газа по уравнению состояния.
Вспомним, что очень часто следующие друг за другом (см. задачу 2) упругие удары молекул о стенку будут создавать в среднем постоянную силу давления. Чтобы определить эту силу, нужно, во-первых, подсчитать силу, действующую на стенку со стороны одной йолекулы, и, во-вторых, усреднить эту силу по всем сталкивающимся со стенкой в единицу времени молекулам.
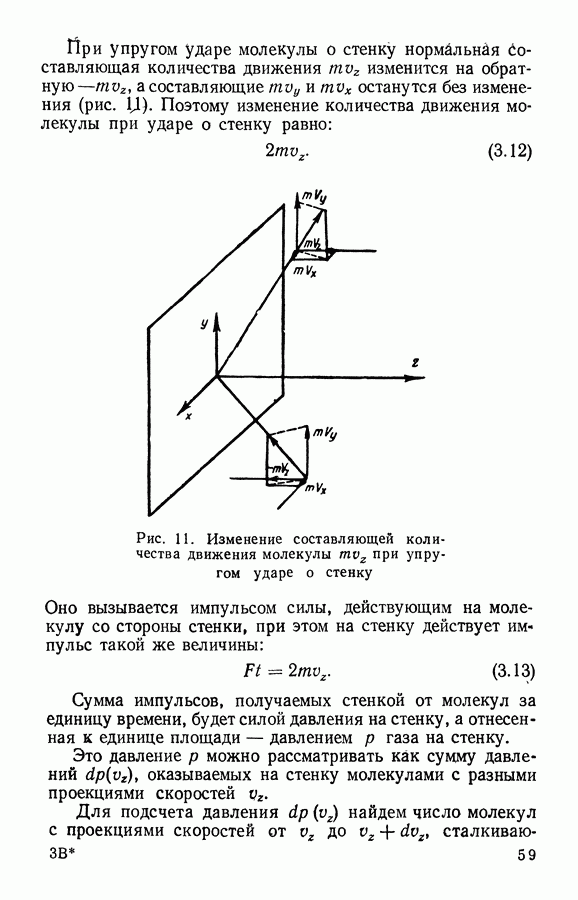
При упругом ударе молекулы о стенку нормальная Составляющая количества движения  изменится на обратную
изменится на обратную  , а составляющие
, а составляющие  останутся без изменения (рис. IX). Поэтому изменение количества движения молекулы при ударе о стенку равно:
останутся без изменения (рис. IX). Поэтому изменение количества движения молекулы при ударе о стенку равно:


Рис. 11. Изменение составляющей количества движения молекулы  при упругом ударе о стенку
при упругом ударе о стенку
Оно вызывается импульсом силы, действующим на молекулу со стороны стенки, при этом на стенку действует импульс такой же величины:

Сумма импульсов, получаемых стенкой от молекул за единицу времени, будет силой давления на стенку, а отнесенная к единице площади — давлением  газа на стенку.
газа на стенку.
Это давление  можно рассматривать как сумму давлений
можно рассматривать как сумму давлений  оказываемых на стенку молекулами с разными проекциями скоростей
оказываемых на стенку молекулами с разными проекциями скоростей 
Для подсчета давления  найдем число молекул с проекциями скоростей от
найдем число молекул с проекциями скоростей от  до
до 
сталкивающихся с единицеи поверхности стенкй в единицу времени 
Пусть в  газа содержится
газа содержится  молекул. Тогда число молекул в
молекул. Тогда число молекул в  имеющих проекцию скорости
имеющих проекцию скорости  в интервале от
в интервале от  до
до  мы определим по формуле
мы определим по формуле 


Рис. 12. К подсчету числа столкновений молекул со стенкой в единицу времени
В единицу времени с поверхностью стенки площадью в  столкнется столько молекул, имеющих скорость
столкнется столько молекул, имеющих скорость  сколько их находится в объеме цилиндра с основанием в
сколько их находится в объеме цилиндра с основанием в  и высотой, численно равной
и высотой, численно равной  (рис. 12), т. е.
(рис. 12), т. е.

Все эти молекулы будут оказывать на стенку давление

Для вычисления полного давления  необходимо взять интеграл:
необходимо взять интеграл:

Вычислим это выражение при условии, что нас интересуют только молекулы сталкивающиеся со стенкой, у которых  меняется от
меняется от  до
до 

Сравним полученное выражение с давлением идеального газа по закону Клапейрона — Менделеева, записанного для одного моля:

В этом случае и  где
где  число
число
Авогадро, V — объем системы,  постоянная Больцмана и
постоянная Больцмана и  универсальная газовая постоянная. Окончательно получим:
универсальная газовая постоянная. Окончательно получим:

Отсюда следует, что параметр максвелловског о распределения а связан с абсолютной температурой по формуле

Теперь максвелловское распределение можно будет записать, подставляя значение параметра а:

или

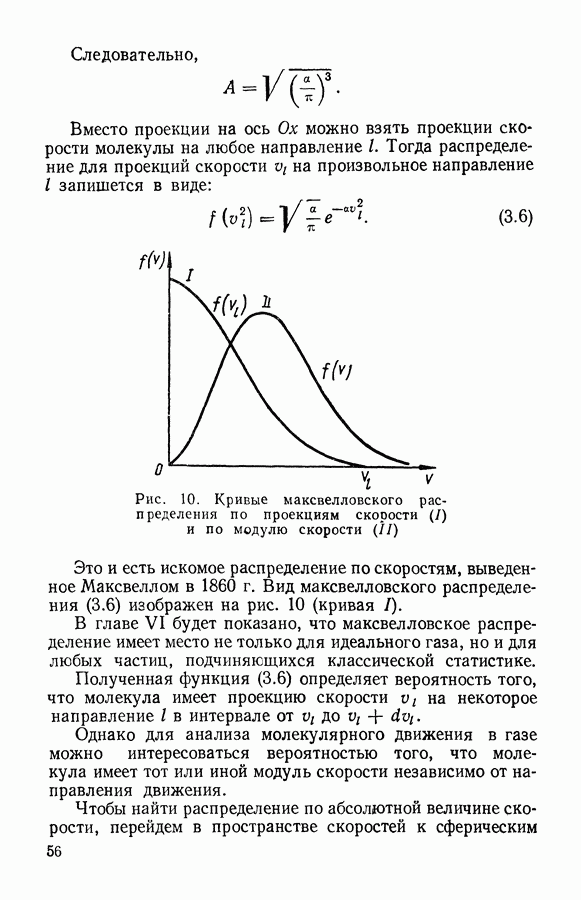
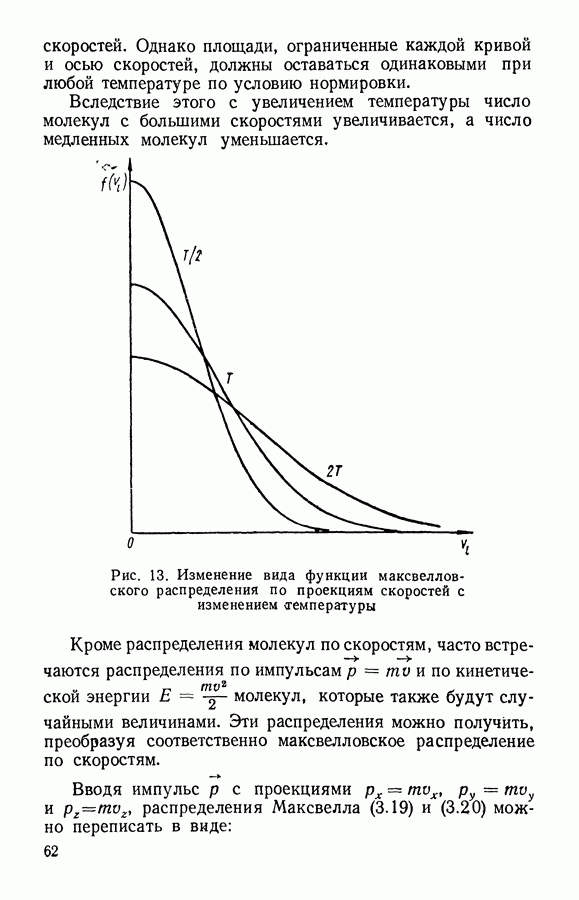
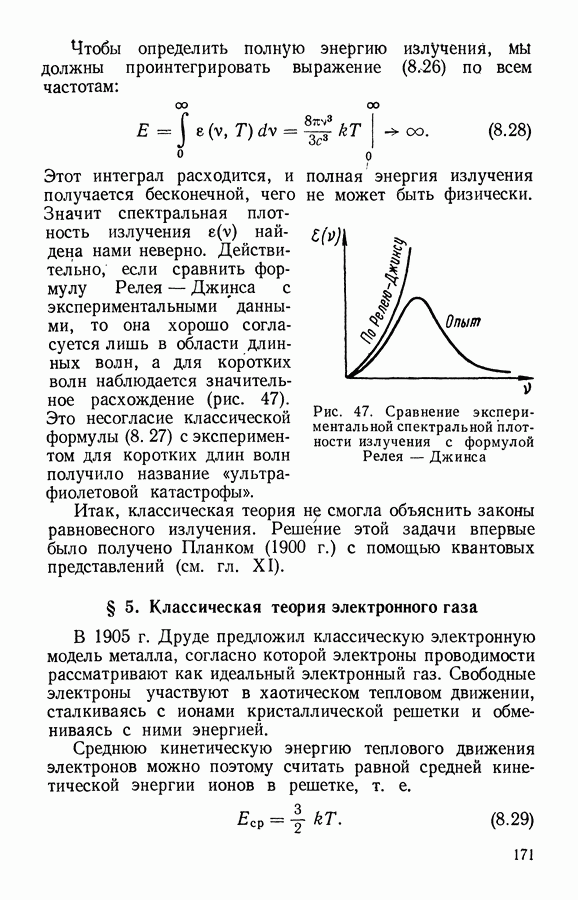
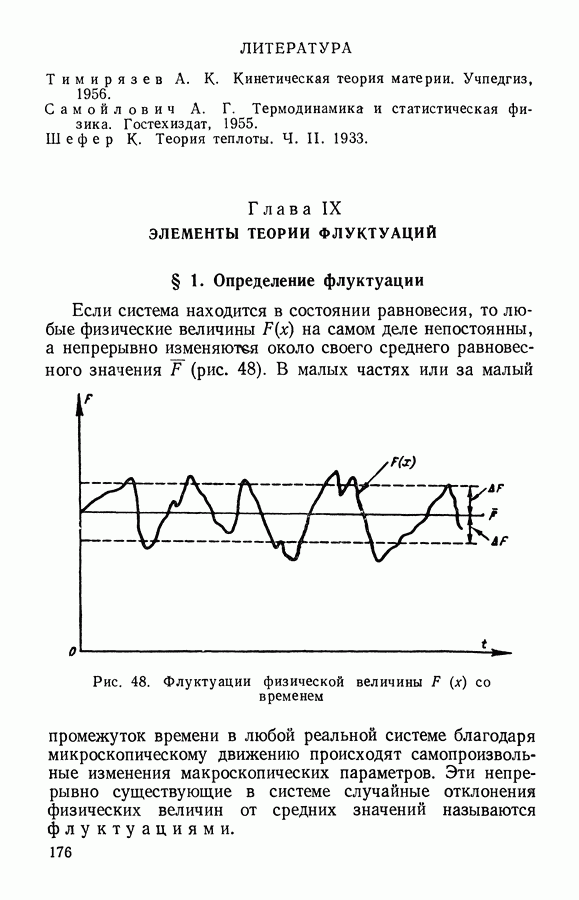
Кривые Максвелла при различных температурах представлены на рис. 13 и 14. Мы видим, что с увеличением температуры все кривые смещаются в сторону более высоких
скоростей. Однако площади, ограниченные каждой кривой и осью скоростей, должны оставаться одинаковыми при любой температуре по условию нормировки.
Вследствие этого с увеличением температуры число молекул с большими скоростями увеличивается, а число медленных молекул уменьшается.

Рис. 13. Изменение вида функции максвелловского распределения по проекциям скоростей с изменением <гемпературы
Кроме распределения молекул по скоростям, часто встречаются распределения по импульсам  и по кинетическои энергии
и по кинетическои энергии  молекул, которые также будут случайными величинами. Эти распределения можно получить, преобразуя соответственно максвелловское распределение по скоростям.
молекул, которые также будут случайными величинами. Эти распределения можно получить, преобразуя соответственно максвелловское распределение по скоростям.
Вводя импульс  с проекциями
с проекциями  распределения Максвелла (3.19) и (3.20) можно переписать в виде:
распределения Максвелла (3.19) и (3.20) можно переписать в виде:

и

откуда для функций распределения по проекциям и модулю импульса будем иметь соответственно:

и


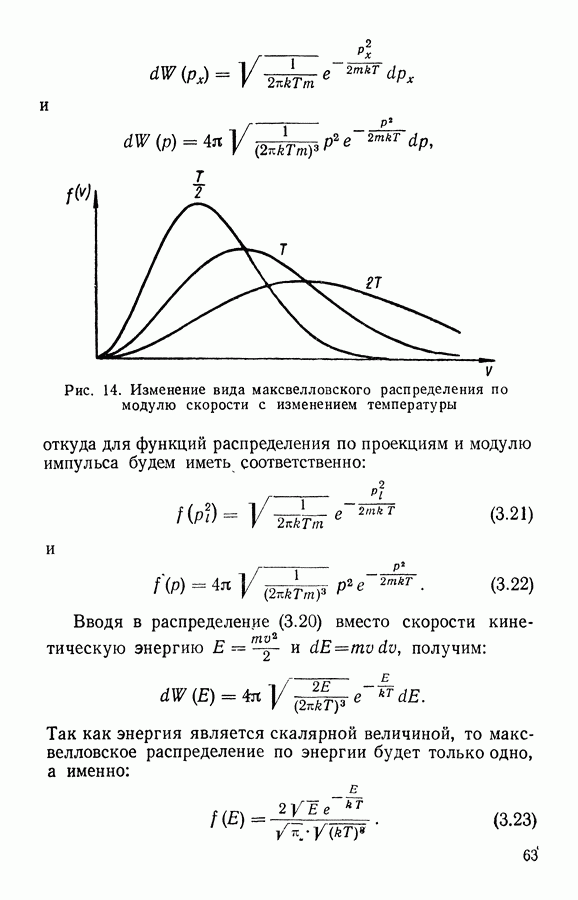
Рис. 14. Изменение вида максвелловского распределения по модулю скорости с изменением температуры
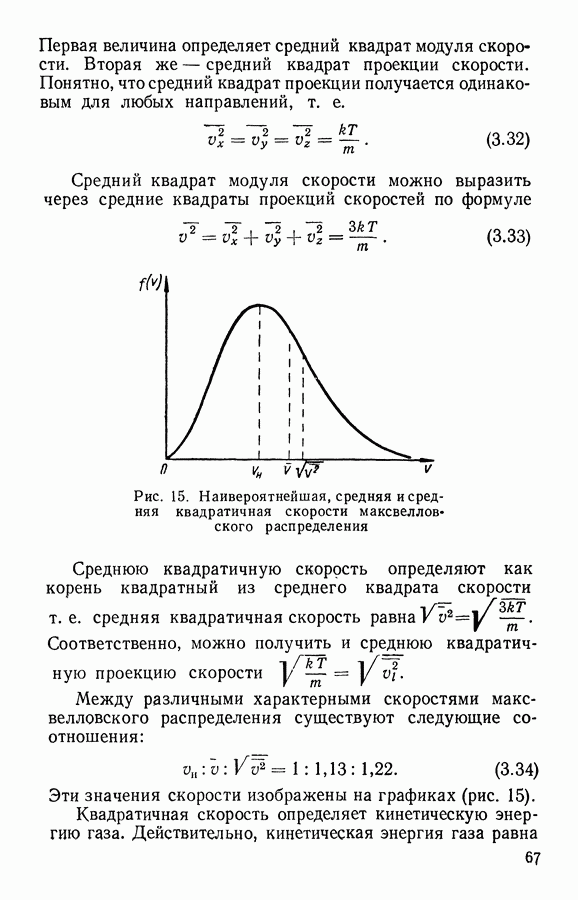
Вводя в распределение (3.20) вместо скорости кинетическую энергию  получим:
получим:

Так как энергия является скалярной величиной, то максвелловское распределение по энергии будет только одно, а именно:

| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. Предмет и метод статистической физики
- § 2. К вопросу возникновения и развития молекулярно-кинетической теории материи
- § 3. Место статистической физики в раскрытии материалистической картины мира
- § 4. Феноменологические и молекулярно-кинетические теории
- § 5. Модельность в статистической физике. Классическая и квантовая модели вещества
- Глава II. НЕОБХОДИМЫЕ СВЕДЕНИЯ ИЗ ТЕОРИИ ВЕРОЯТНОСТЕЙ
- § 1. Случайные события и случайные величины
- § 2. Понятие вероятности
- § 3. Свойства вероятности. Формула сложения и умножения вероятностей
- § 4. Средние значения случайных величин
- § 5. Примеры законов распределения случайных величин
- § 6. Функция распределения для нескольких случайных величин
- ЧАСТЬ I. ЭЛЕМЕНТАРНАЯ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- § 1. Модель идеального газа
- § 2. Распределение молекул газа по скоростям
- § 3. Связь распределения Максвелла по скоростям с абсолютной температурой
- § 4. Характерные скорости максвелловского распределения
- § 5. Средние относительные скорости
- § 6. Соответствие модели идеального газа реальному газу
- Глава IV. ЭЛЕМЕНТЫ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ НЕРАВНОВЕСНЫХ ПРОЦЕССОВ
- § 1. Неравновесные состояния. Явления релаксации и переноса
- § 2. Поперечные сечения. Длина свободного пробега
- § 3. Распределение свободных пробегов частиц
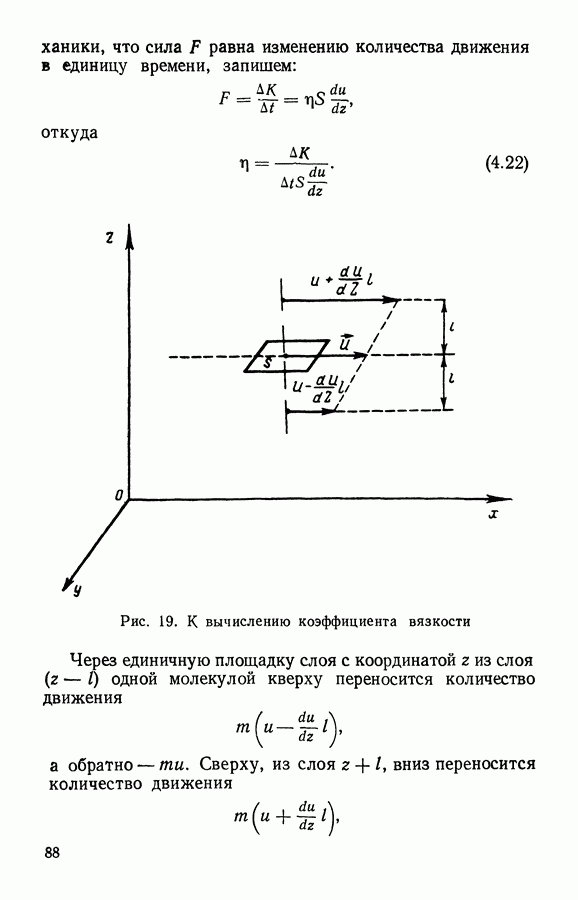
- § 4. Вязкость газов
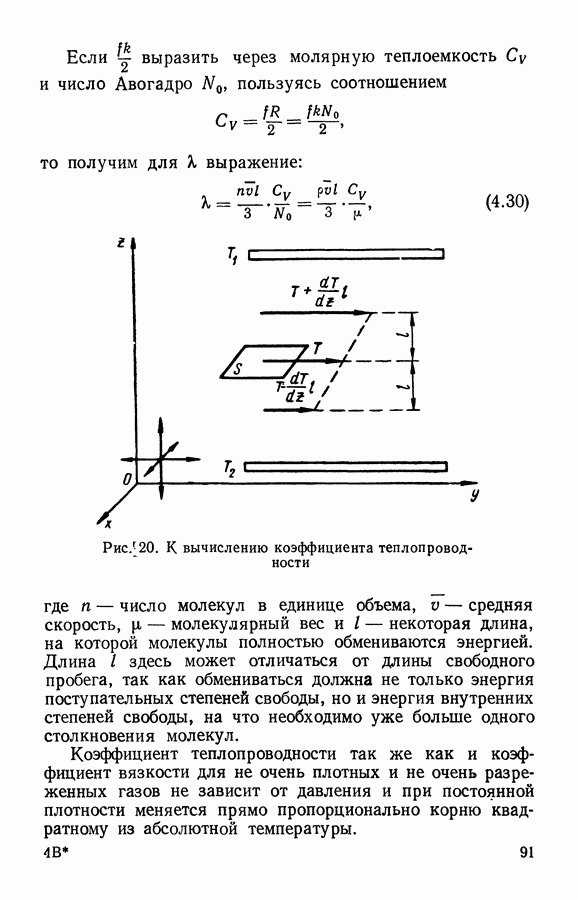
- § 5. Теплопроводность газов
- § 6. Диффузия газов
- ЧАСТЬ II. КЛАССИЧЕСКАЯ СТАТИСТИЧЕСКАЯ ФИЗИКА
- § 1. Невозможность последовательного механического описания физических систем многих частиц
- § 2. Макроскопическое и микроскопическое описание системы в термодинамическом равновесии
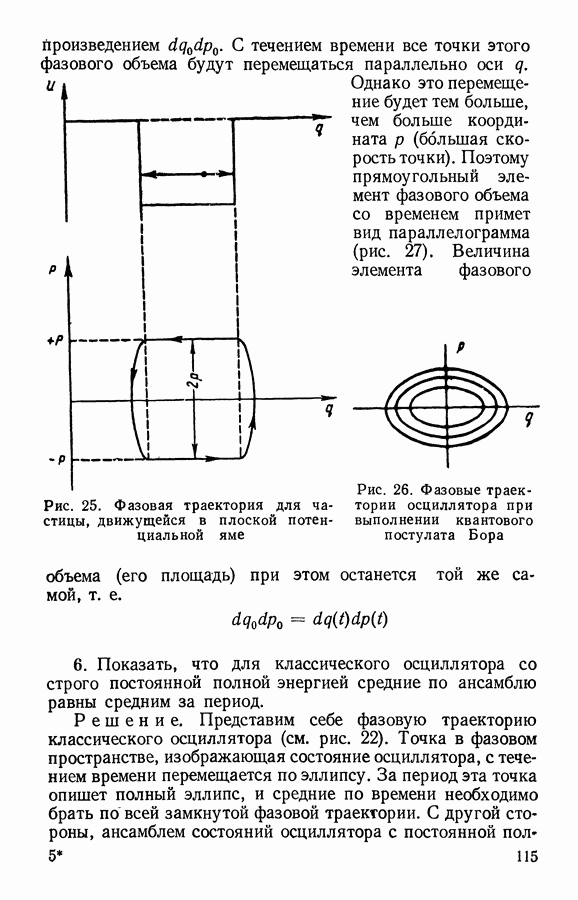
- § 3. Изображение системы в фазовом пространстве
- § 4. Элемент фазового объема. Вероятность нахождения системы в фазовом пространстве
- § 5. Теорема о сохранении фазового объема (Теорема Лиувилля)
- § 6. Макроскопические величины как фазовые средние
- Глава VI. СТАЦИОНАРНЫЕ ФУНКЦИИ РАСПРЕДЕЛЕНИЯ
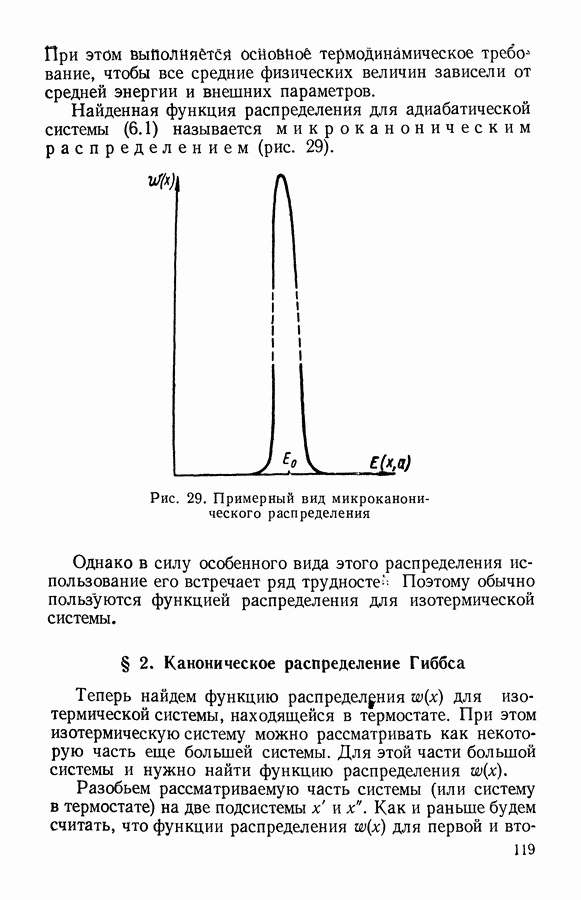
- § 1. Микроканоническое распределение
- § 2. Каноническое распределение Гиббса
- § 3. Свойства канонического распределения
- § 4. Физический смысл параметров канонического распределения
- § 5. Энтропия и ее связь с вероятностью состояния
- § 6. Распределение Максвелла-Больцмана
- § 7. Большое каноническое распределение Гиббса
- Глава VII. ПРИМЕНЕНИЕ РАСПРЕДЕЛЕНИЯ ГИББСА К РЕАЛЬНЫМ СИСТЕМАМ
- § 1. Выражение термодинамических функций через интеграл состояний
- § 2. Интеграл состояний и термодинамические функции идеального газа
- § 3. Статистическое рассмотрение системы взаимодействующих частиц
- § 4. Вывод уравнения состояния реального газа
- § 5. Статистика диэлектриков
- Глава VIII. РАВНОМЕРНОЕ РАСПРЕДЕЛЕНИЕ КИНЕТИЧЕСКОЙ ЭНЕРГИИ ПО СТЕПЕНЯМ СВОБОДЫ
- § 1. Теорема о равномерном распределении энергии по степеням свободы
- § 2. Теплоемкость разреженных газов
- § 3. Теплоемкость твердых тел
- § 4. Применение методов статистической физики к равновесному излучению
- § 5. Классическая теория электронного газа
- Глава IX. ЭЛЕМЕНТЫ ТЕОРИИ ФЛУКТУАЦИЙ
- § 2. Связь флуктуаций со свободной энергией. Корреляция
- § 3. Чувствительность различных измерительных приборов
- § 4. Рассеяние света на флуктуациях плотности
- § 5. Броуновское движение
- § 6. Статистика полимеров
- ЧАСТЬ III. КВАНТОВАЯ СТАТИСТИЧЕСКАЯ ФИЗИКА
- § 1. Квантовые системы и их свойства
- § 2. Описание квантовых систем
- § 3. Применение статистического метода к квантовым системам
- § 4. Метод ячеек Больцмана
- § 5. Статистики квантовых систем
- § 6. Сопоставление статистик Максвелла-Больцмана, Бозе-Эйнштейна и Ферми-Дирака
- Глава XI. ЛОКАЛИЗОВАННЫЕ КВАНТОВЫЕ СИСТЕМЫ
- § 1. Квантовый осциллятор и квантовый ротатор
- § 2. Сумма по состояниям и внутренняя энергия систем осцилляторов и ротаторов
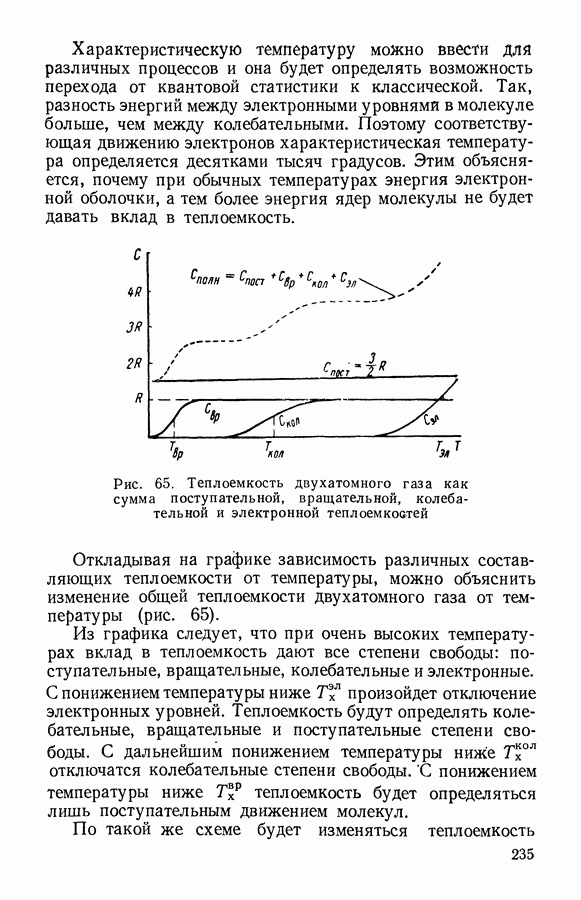
- § 3. Теплоемкость газов. Характеристические температуры
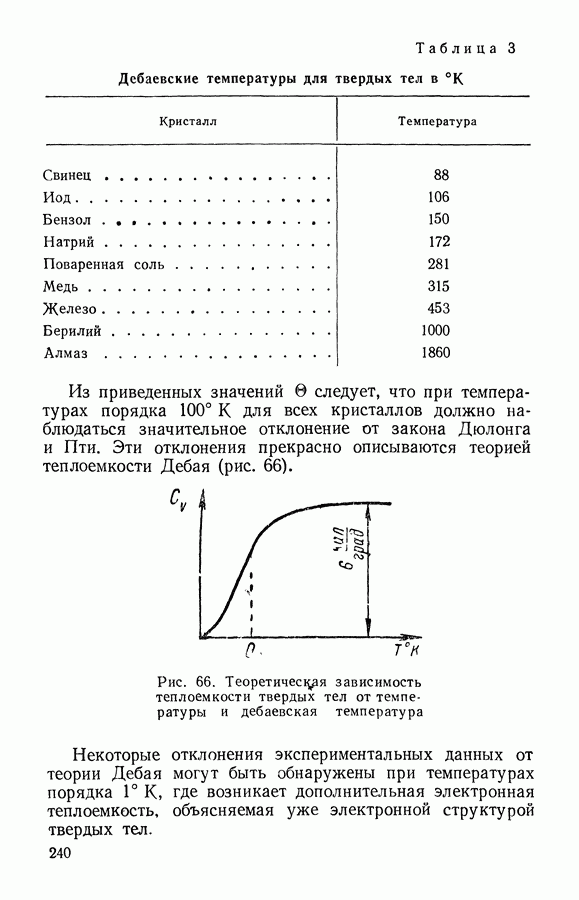
- § 4. Теплоемкость твердых тел. Закон Дебая
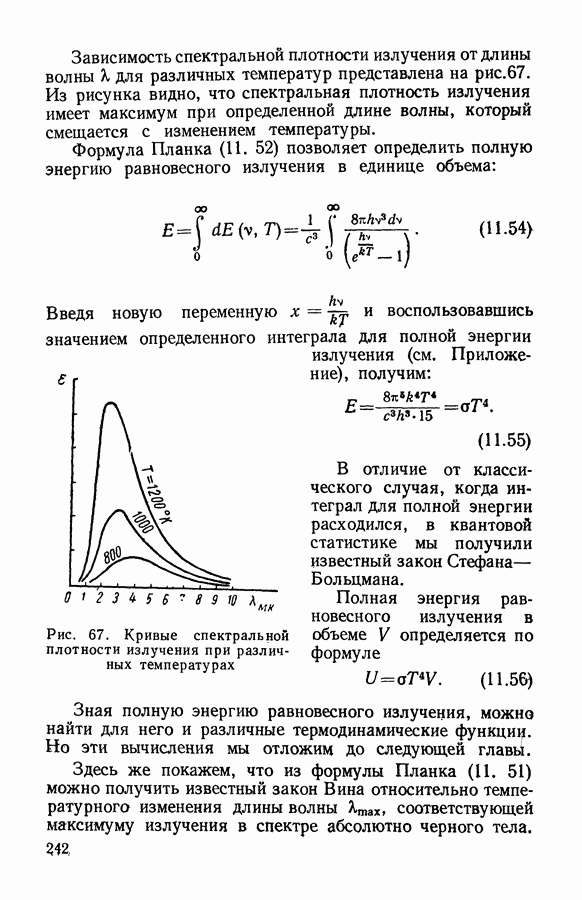
- § 5. Законы равновесного излучения
- § 6. Статистика парамагнетиков
- Глава XII. ПРИМЕНЕНИЕ СТАТИСТИК БОЗЕ — ЭЙНШТЕЙНА И ФЕРМИ — ДИРАКА
- § 1. Применение статистики Бозе — Эйнштейна к описанию системы частиц
- § 2. Равновесное излучение как фотонный газ
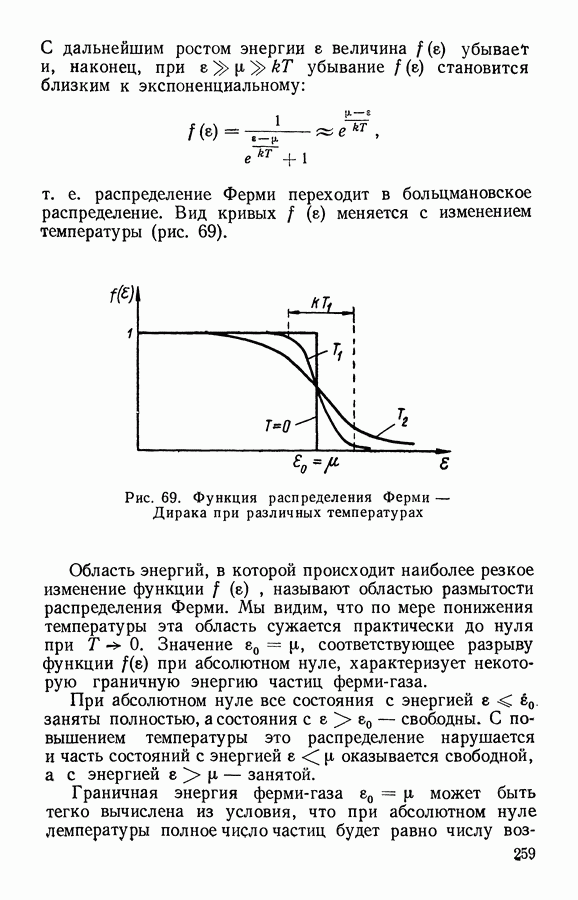
- § 3. Применение статистики Ферми — Дирака к описанию поведения системы частиц
- § 4. Электронный газ в металлах
- § 5. Магнитные свойства электронного газа
- § 6. Состояния систем с отрицательной абсолютной температурой
- ПРИЛОЖЕНИЯ.