| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
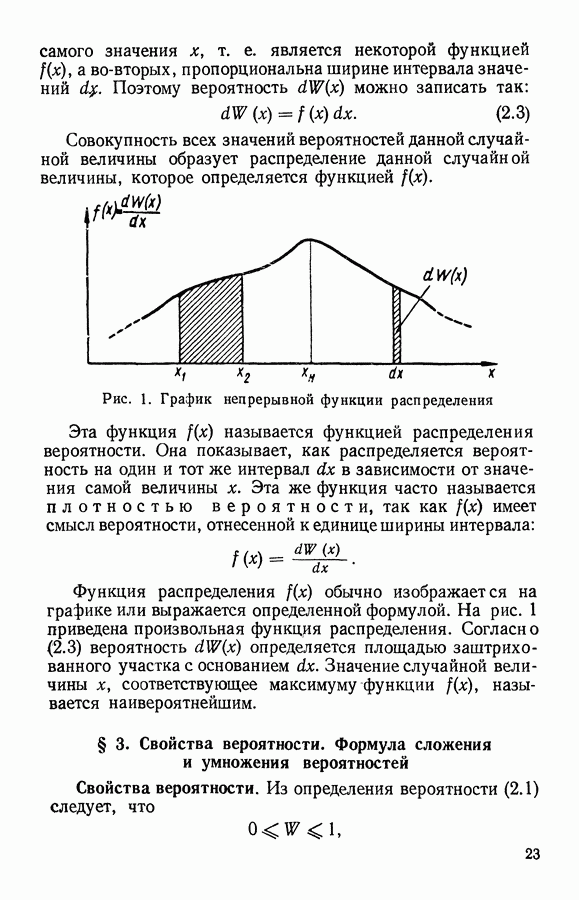
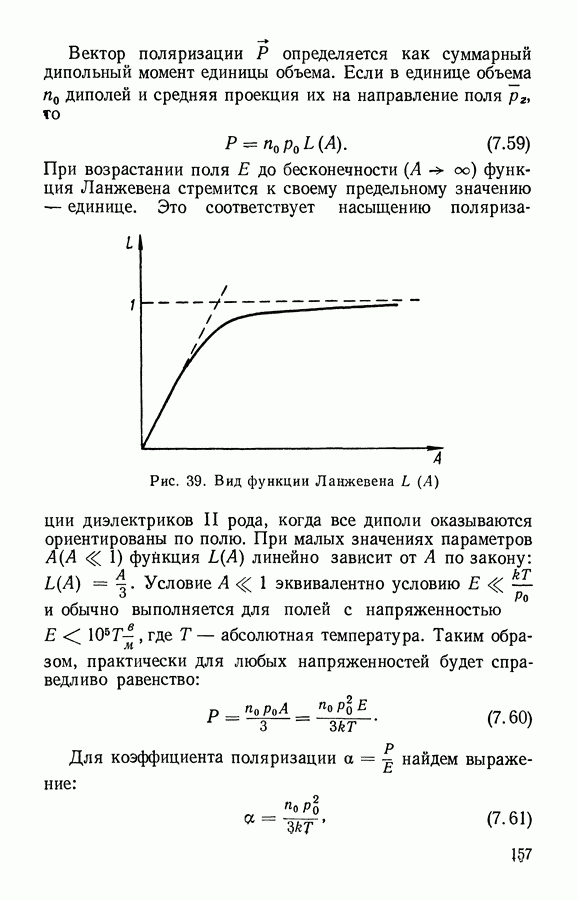
§ 2. Интеграл состояний и термодинамические функции идеального газа
Вычислим некоторые термодинамические функции идеального газа, пользуясь каноническим распределением (6.3).
Для вычисления интеграла состояний  нужно знать функцию Гамильтона
нужно знать функцию Гамильтона  которая для идеального газа определяется суммой энергий отдельных частиц, т. е.
которая для идеального газа определяется суммой энергий отдельных частиц, т. е.

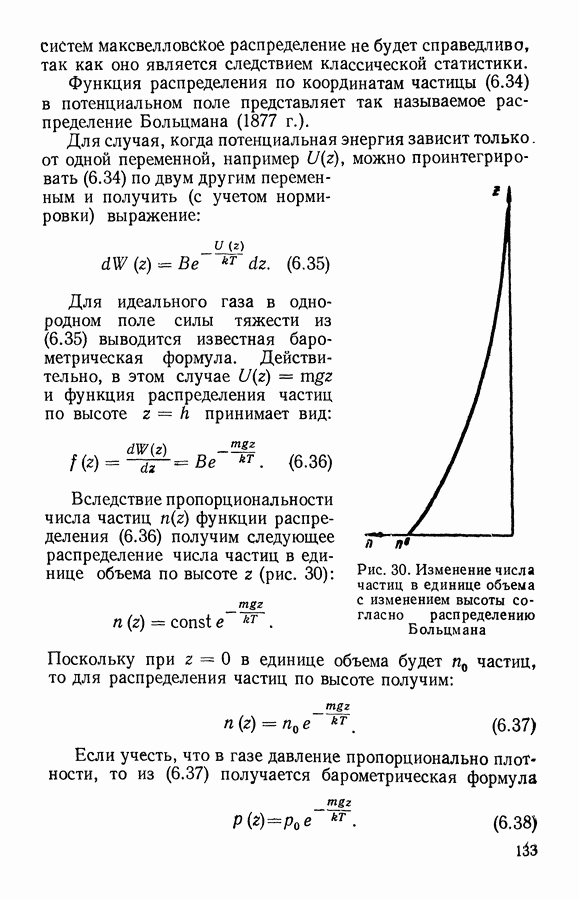
Здесь  представляет потенциальную энергию
представляет потенциальную энергию  частицы, которую мы введем из следующих соображений. Частицы идеального газа могут совершенно произвольно двигаться внутри сосуда объемом V, но не могут выйти за его пределы. Это эквивалентно тому, что частицы внутри сосуда имеют потенциальную энергию, равную нулю, а вне сосуда — бесконечно большую потенциальную энергию (рис. 32). (Внешние силовые поля на частицы идеального газа не действуют.)
частицы, которую мы введем из следующих соображений. Частицы идеального газа могут совершенно произвольно двигаться внутри сосуда объемом V, но не могут выйти за его пределы. Это эквивалентно тому, что частицы внутри сосуда имеют потенциальную энергию, равную нулю, а вне сосуда — бесконечно большую потенциальную энергию (рис. 32). (Внешние силовые поля на частицы идеального газа не действуют.)
Таким образом, внешний параметр V мы можем ввести в функцию Гамильтона  через потенциальную энергию
через потенциальную энергию  выраженную в виде:
выраженную в виде:

Поскольку все частицы независимы, выражение для интеграла состояний представим в виде:

Здесь  интеграл состояний для одной частицы.
интеграл состояний для одной частицы.
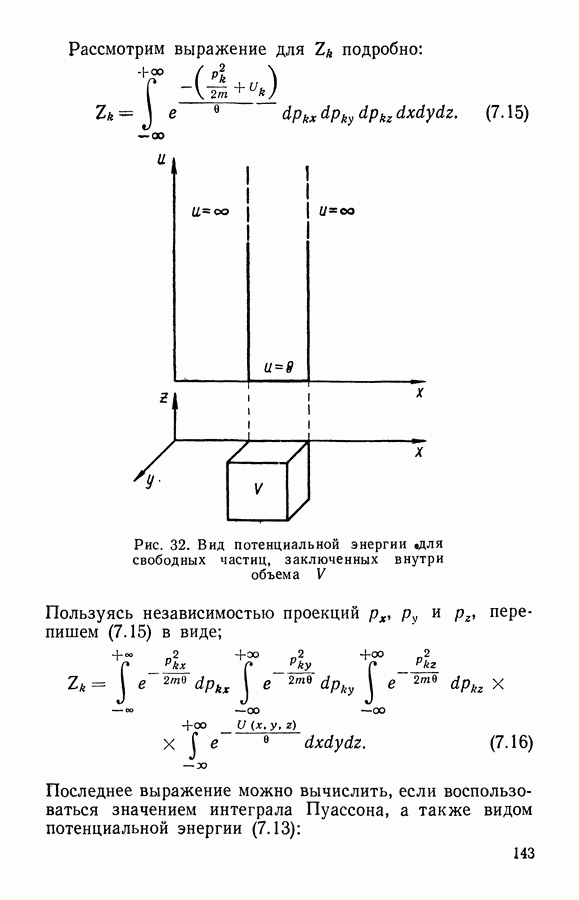
Рассмотрим выражение для  подробно:
подробно:


Рис. 32. Вид потенциальной энергии «для свободных частиц, заключенных внутри объема V
Пользуясь независимостью проекций  перепишем (7.15) в виде;
перепишем (7.15) в виде;

Последнее выражение можно вычислить, если воспользоваться значением интеграла Пуассона, а также видом потенциальной энергии (7.13)

и

Тогда

Следовательно, интеграл состояний всей системы

Свободная энергия  может быть выражена через интеграл состояний
может быть выражена через интеграл состояний  по следующей формуле:
по следующей формуле:

В нашем случае

Умножив последнее равенство на —0 и воспользовавшись формулой Стирлинга для больших  получим выражение для свободной энергии идеального газа:
получим выражение для свободной энергии идеального газа:

Уравнение состояния получим по формуле (7.2), вычисляя производную от свободной энергии по объему:

Для одного моля идеального газа оно должно совпадать с уравнением Клапейрона — Менделеева:  . Отсюда следует, что модуль канонического распределения связан с абсолютной температурой соотношением:
. Отсюда следует, что модуль канонического распределения связан с абсолютной температурой соотношением:

где  -постоянная Больцмана. На это соотношение мы уже ссылались в гл. V и использовали его в § 1, гл. VI.
-постоянная Больцмана. На это соотношение мы уже ссылались в гл. V и использовали его в § 1, гл. VI.
Таким образом, мы получаем определение статистической температуры как модуля канонического распределения.
Пользуясь выражением свободной энергии (6.23), можно вычислить энтропию идеального газа по формуле (7.5)

где в произвольную постоянную  входят члены
входят члены

Теперь можно вычислить внутреннюю энергию и теплоемкость  идеального одноатомного газа:
идеального одноатомного газа:

Таким образом, исходя из канонического распределения в случае идеального газа, мы получили основные термодинамические функции и уравнение состояния.
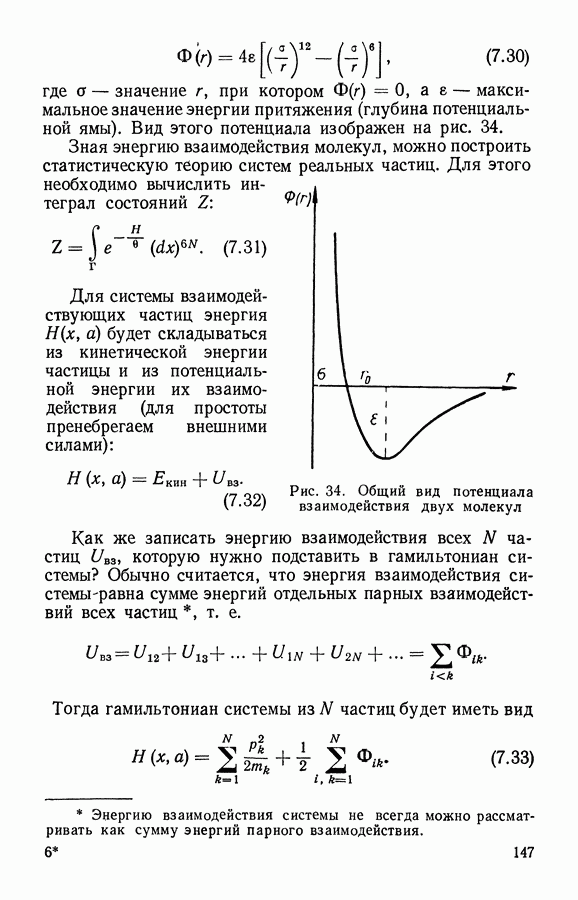
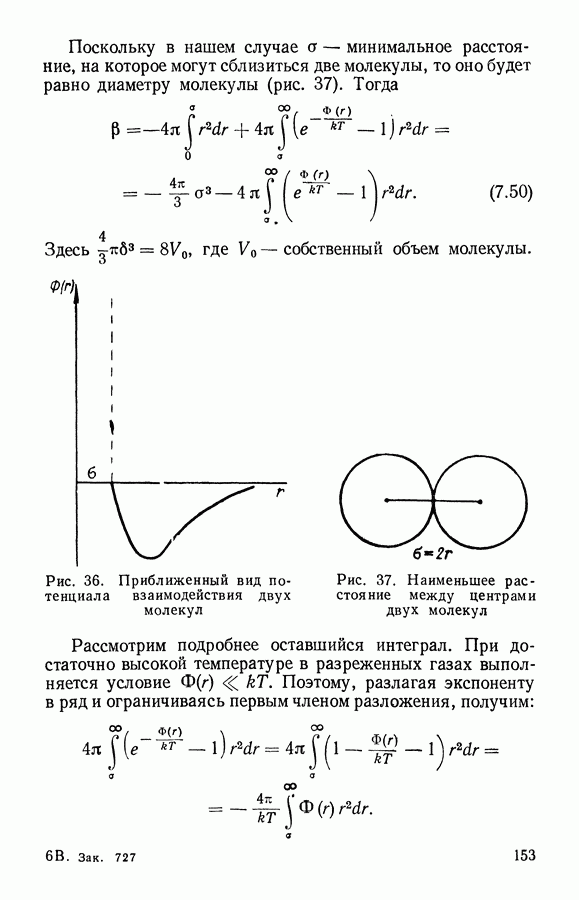
Применим теперь статистический метод к реальному газу. Как известно, реальный газ отличается от идеального характером взаимодействия молекул. Поэтому сначала рассмотрим вид потенциала взаимодействия реальных молекул.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. Предмет и метод статистической физики
- § 2. К вопросу возникновения и развития молекулярно-кинетической теории материи
- § 3. Место статистической физики в раскрытии материалистической картины мира
- § 4. Феноменологические и молекулярно-кинетические теории
- § 5. Модельность в статистической физике. Классическая и квантовая модели вещества
- Глава II. НЕОБХОДИМЫЕ СВЕДЕНИЯ ИЗ ТЕОРИИ ВЕРОЯТНОСТЕЙ
- § 1. Случайные события и случайные величины
- § 2. Понятие вероятности
- § 3. Свойства вероятности. Формула сложения и умножения вероятностей
- § 4. Средние значения случайных величин
- § 5. Примеры законов распределения случайных величин
- § 6. Функция распределения для нескольких случайных величин
- ЧАСТЬ I. ЭЛЕМЕНТАРНАЯ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- § 1. Модель идеального газа
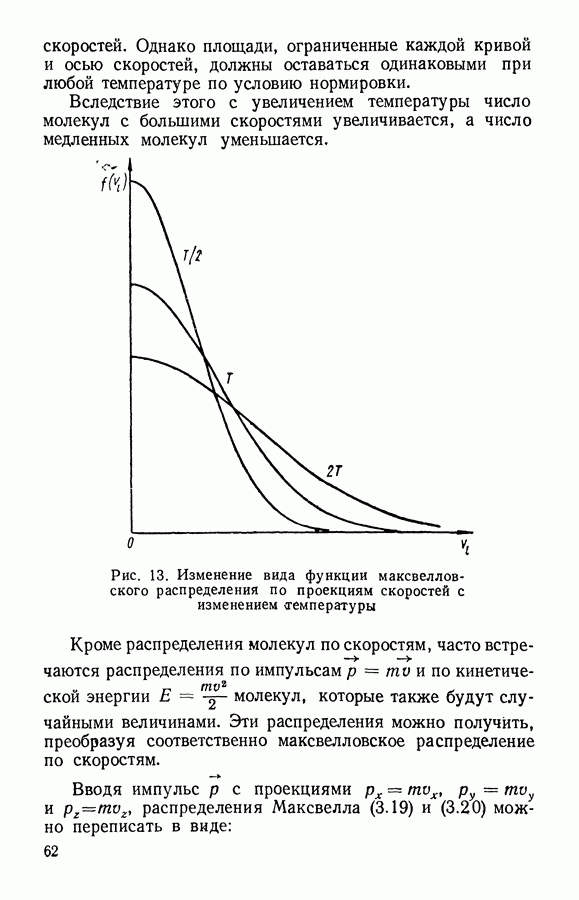
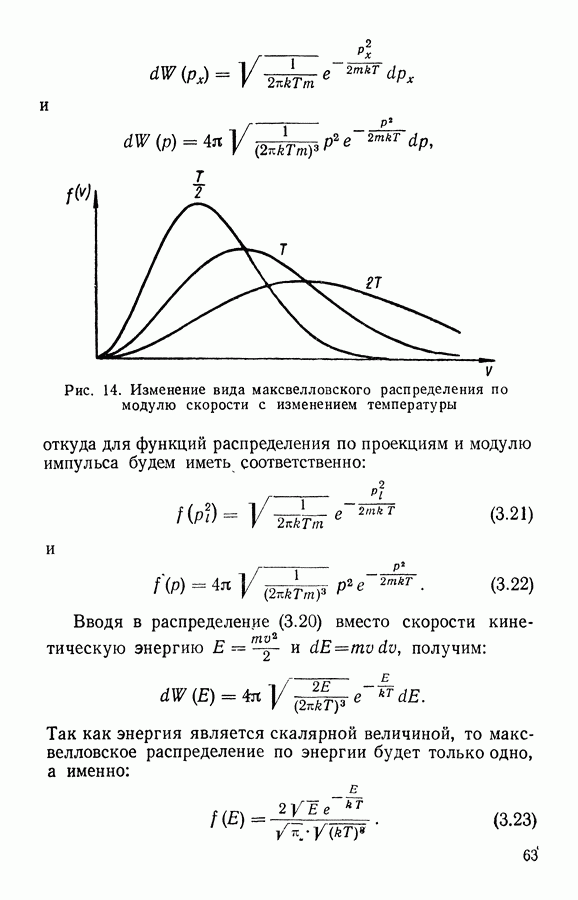
- § 2. Распределение молекул газа по скоростям
- § 3. Связь распределения Максвелла по скоростям с абсолютной температурой
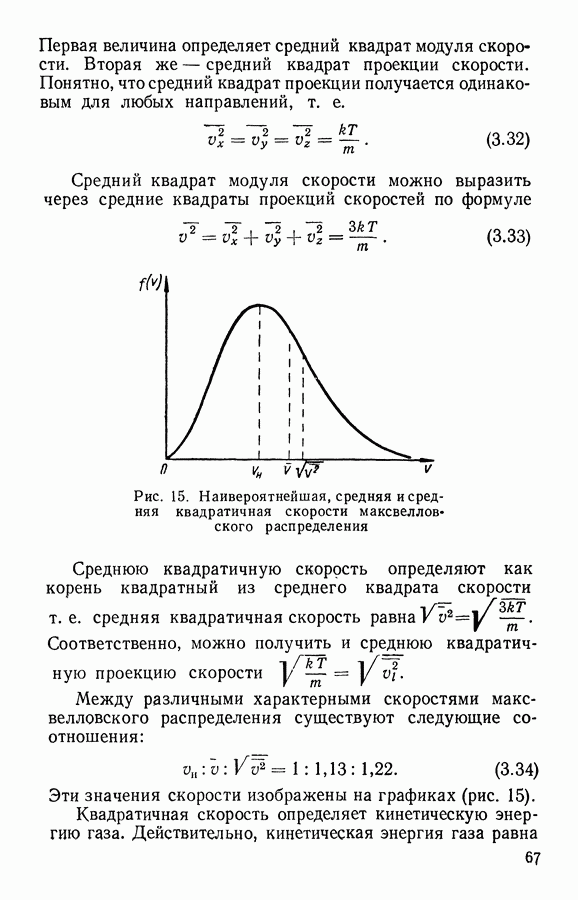
- § 4. Характерные скорости максвелловского распределения
- § 5. Средние относительные скорости
- § 6. Соответствие модели идеального газа реальному газу
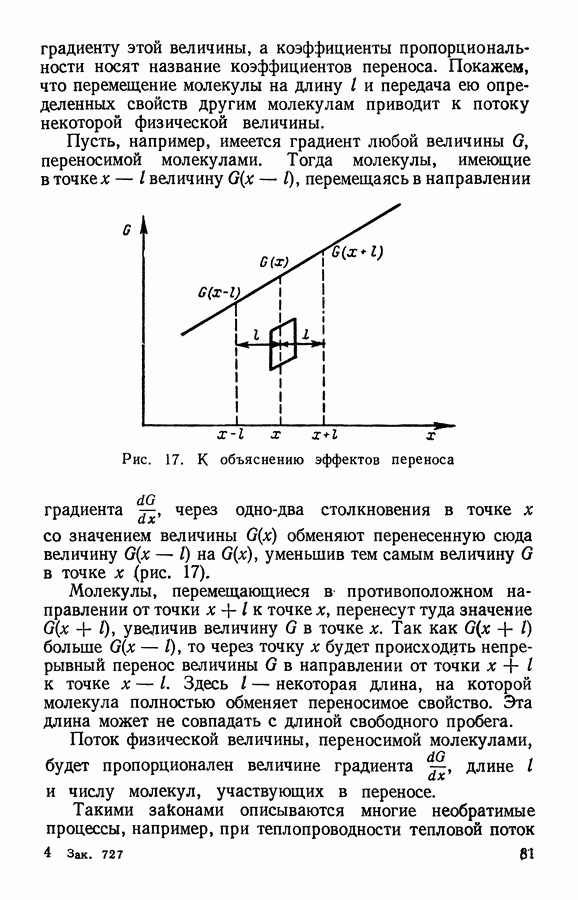
- Глава IV. ЭЛЕМЕНТЫ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ НЕРАВНОВЕСНЫХ ПРОЦЕССОВ
- § 1. Неравновесные состояния. Явления релаксации и переноса
- § 2. Поперечные сечения. Длина свободного пробега
- § 3. Распределение свободных пробегов частиц
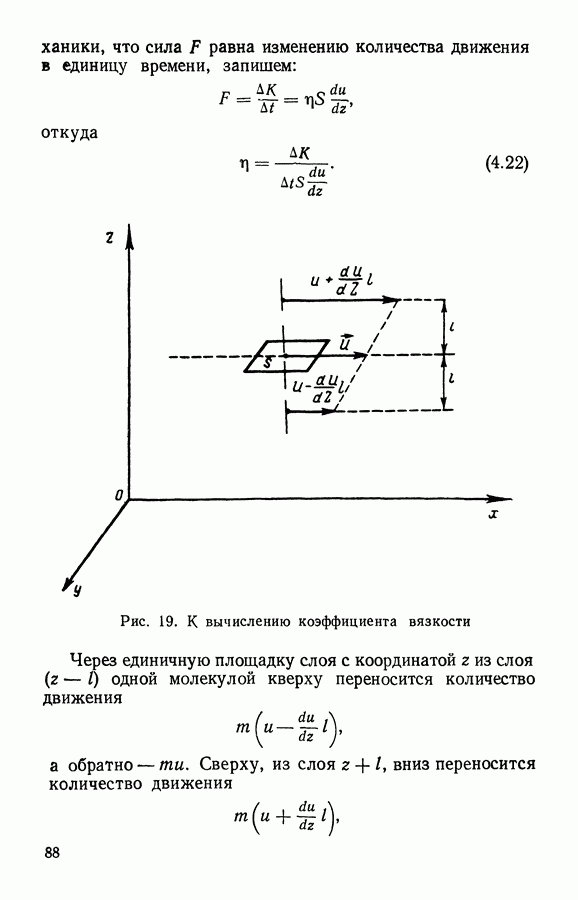
- § 4. Вязкость газов
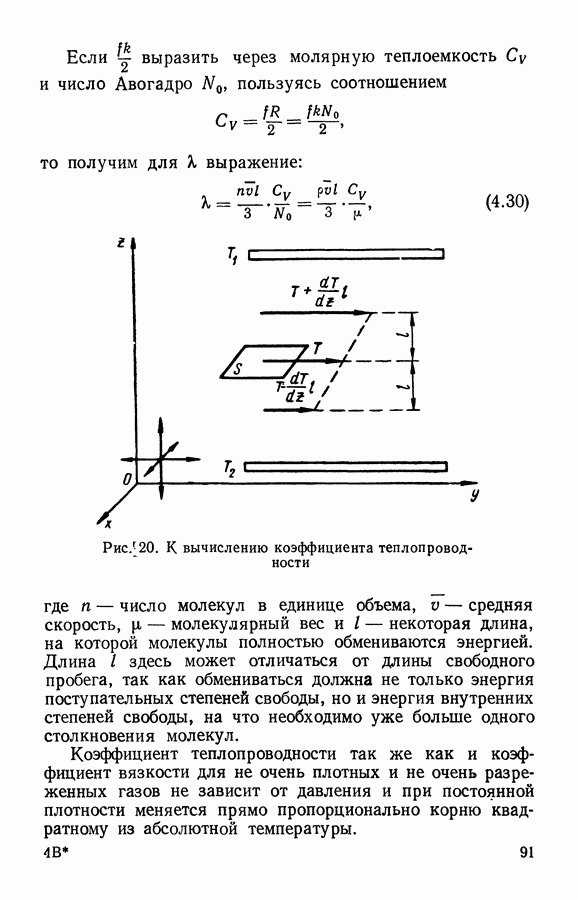
- § 5. Теплопроводность газов
- § 6. Диффузия газов
- ЧАСТЬ II. КЛАССИЧЕСКАЯ СТАТИСТИЧЕСКАЯ ФИЗИКА
- § 1. Невозможность последовательного механического описания физических систем многих частиц
- § 2. Макроскопическое и микроскопическое описание системы в термодинамическом равновесии
- § 3. Изображение системы в фазовом пространстве
- § 4. Элемент фазового объема. Вероятность нахождения системы в фазовом пространстве
- § 5. Теорема о сохранении фазового объема (Теорема Лиувилля)
- § 6. Макроскопические величины как фазовые средние
- Глава VI. СТАЦИОНАРНЫЕ ФУНКЦИИ РАСПРЕДЕЛЕНИЯ
- § 1. Микроканоническое распределение
- § 2. Каноническое распределение Гиббса
- § 3. Свойства канонического распределения
- § 4. Физический смысл параметров канонического распределения
- § 5. Энтропия и ее связь с вероятностью состояния
- § 6. Распределение Максвелла-Больцмана
- § 7. Большое каноническое распределение Гиббса
- Глава VII. ПРИМЕНЕНИЕ РАСПРЕДЕЛЕНИЯ ГИББСА К РЕАЛЬНЫМ СИСТЕМАМ
- § 1. Выражение термодинамических функций через интеграл состояний
- § 2. Интеграл состояний и термодинамические функции идеального газа
- § 3. Статистическое рассмотрение системы взаимодействующих частиц
- § 4. Вывод уравнения состояния реального газа
- § 5. Статистика диэлектриков
- Глава VIII. РАВНОМЕРНОЕ РАСПРЕДЕЛЕНИЕ КИНЕТИЧЕСКОЙ ЭНЕРГИИ ПО СТЕПЕНЯМ СВОБОДЫ
- § 1. Теорема о равномерном распределении энергии по степеням свободы
- § 2. Теплоемкость разреженных газов
- § 3. Теплоемкость твердых тел
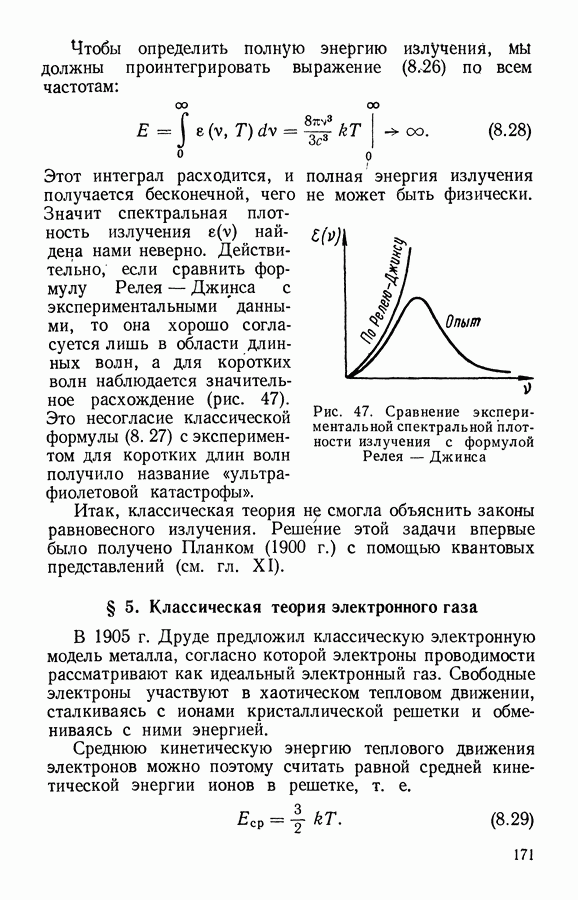
- § 4. Применение методов статистической физики к равновесному излучению
- § 5. Классическая теория электронного газа
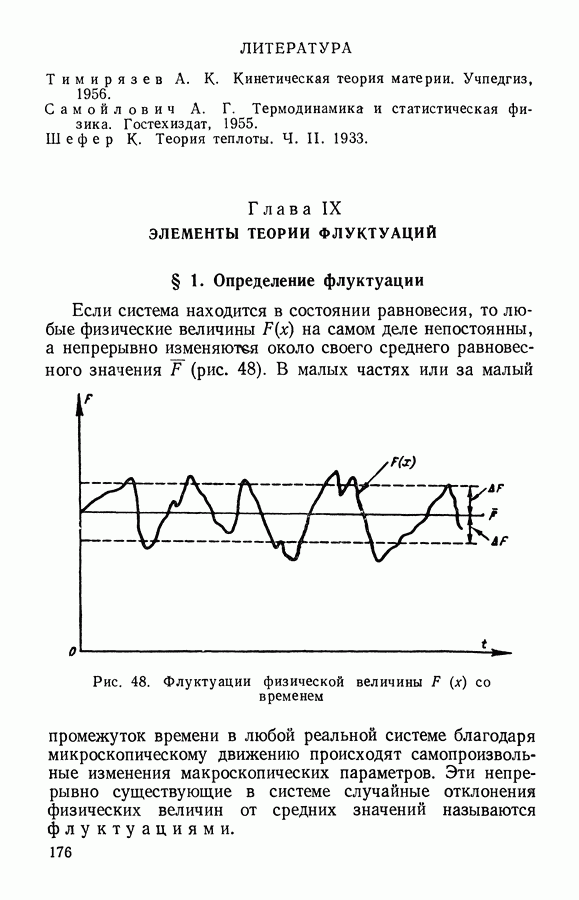
- Глава IX. ЭЛЕМЕНТЫ ТЕОРИИ ФЛУКТУАЦИЙ
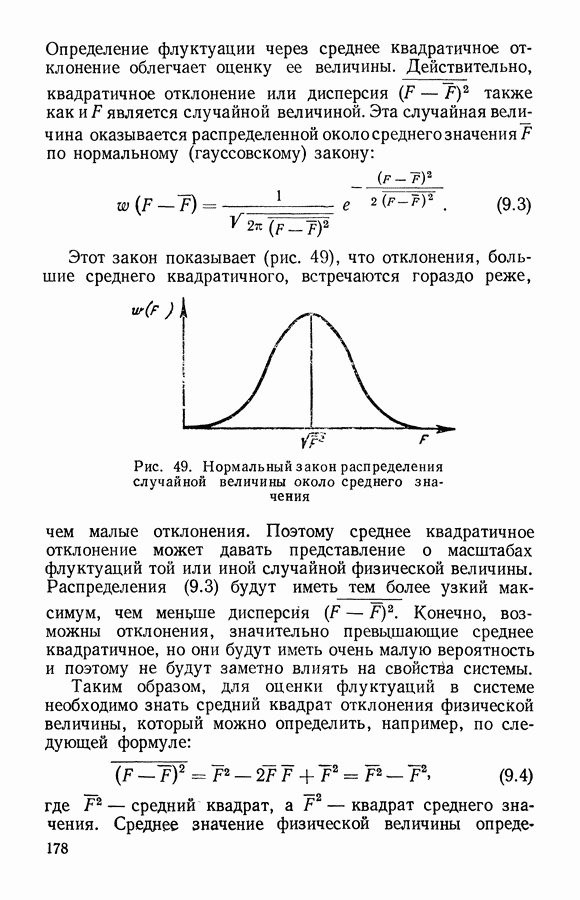
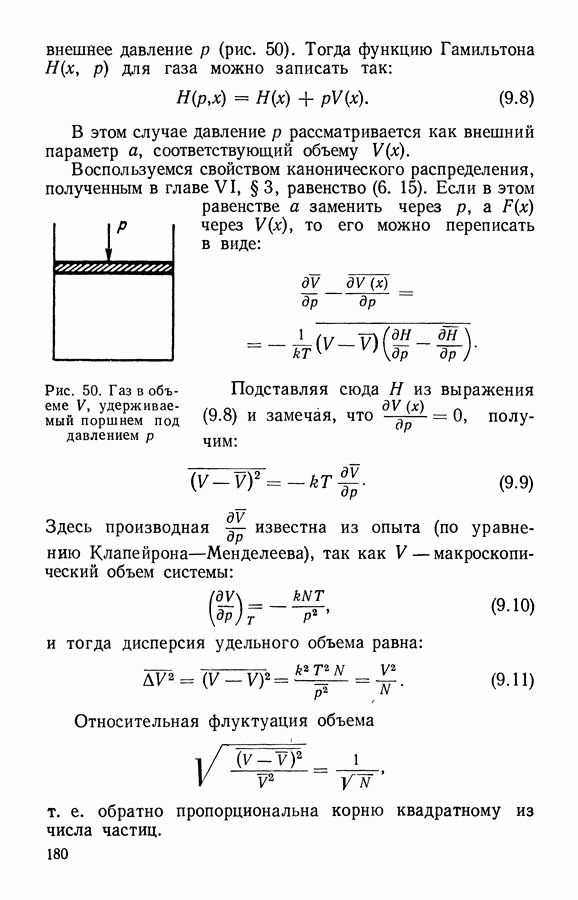
- § 2. Связь флуктуаций со свободной энергией. Корреляция
- § 3. Чувствительность различных измерительных приборов
- § 4. Рассеяние света на флуктуациях плотности
- § 5. Броуновское движение
- § 6. Статистика полимеров
- ЧАСТЬ III. КВАНТОВАЯ СТАТИСТИЧЕСКАЯ ФИЗИКА
- § 1. Квантовые системы и их свойства
- § 2. Описание квантовых систем
- § 3. Применение статистического метода к квантовым системам
- § 4. Метод ячеек Больцмана
- § 5. Статистики квантовых систем
- § 6. Сопоставление статистик Максвелла-Больцмана, Бозе-Эйнштейна и Ферми-Дирака
- Глава XI. ЛОКАЛИЗОВАННЫЕ КВАНТОВЫЕ СИСТЕМЫ
- § 1. Квантовый осциллятор и квантовый ротатор
- § 2. Сумма по состояниям и внутренняя энергия систем осцилляторов и ротаторов
- § 3. Теплоемкость газов. Характеристические температуры
- § 4. Теплоемкость твердых тел. Закон Дебая
- § 5. Законы равновесного излучения
- § 6. Статистика парамагнетиков
- Глава XII. ПРИМЕНЕНИЕ СТАТИСТИК БОЗЕ — ЭЙНШТЕЙНА И ФЕРМИ — ДИРАКА
- § 1. Применение статистики Бозе — Эйнштейна к описанию системы частиц
- § 2. Равновесное излучение как фотонный газ
- § 3. Применение статистики Ферми — Дирака к описанию поведения системы частиц
- § 4. Электронный газ в металлах
- § 5. Магнитные свойства электронного газа
- § 6. Состояния систем с отрицательной абсолютной температурой
- ПРИЛОЖЕНИЯ.