| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 76. ОСНОВНЫЕ СВОЙСТВА ЖИДКОСТЕЙ
Из существования непрерывных переходов от разреженных состояний вещества к плотным следует, что жидкость и ее пар должны описываться единым уравнением состояния:

Изучим, как изменяются свойства жидкости, находящейся в цилиндре под поршнем, с увеличением давления. Если мы попытаемся давлением уменьшить объем жидкости, то обнаружим, что при увеличении давления до нескольких тысяч атмосфер жидкость окажется мало сжимаемой. Более того, если уменьшить давление поршня до нуля, то жидкость сохранит определенный объем, мало отличающийся от объема при больших внешних давлениях. Из этого следует, что жидкости способны сохранять свой объем при нулевом значении внешнего давления. Таким образом, хотя уравнение состояния (76.1) для текучих сред (газов и жидкостей) едино, свойства газов в отношении зависимости объемов от давлений отличны от свойств жидкостей (при уменьшении давления газов до нуля их объем стремится к бесконечности).
Если в приведенном выше примере поршень отодвинуть от жидкости, то над жидкостью образуется ее насыщенный пар. Поэтому
когда говорят об объеме жидкости, то имеют в виду объем под давлением ее насыщенных паров.
Молекулы жидкости своим притяжением препятствуют выходу молекул за пределы ее объема. При переходе частицы из жидкости в объем, занятый паром, должна затрачиваться работа выхода  Средняя энергая поступательного движения молекул определяется известным соотношением:
Средняя энергая поступательного движения молекул определяется известным соотношением:  Можно предположить, что молекулы жидкости не разлетаются потому, что их средняя кинетическая энергия меньше работы выхода:
Можно предположить, что молекулы жидкости не разлетаются потому, что их средняя кинетическая энергия меньше работы выхода:

Перепишем это в несколько ином виде:

где  число Авогадро. Величина
число Авогадро. Величина  есть работа по преодолению взаимного притяжения молекул системы, масса которой равна массе моля вещества. Иными словами, величина
есть работа по преодолению взаимного притяжения молекул системы, масса которой равна массе моля вещества. Иными словами, величина  есть потенциальная энергия взаимодействия молекул системы
есть потенциальная энергия взаимодействия молекул системы  Таким образом,
Таким образом,  Учтя последнее, перепишем (76.3):
Учтя последнее, перепишем (76.3):

Следовательно, в жидкости потенциальная энергия взаимодействия частиц по абсолютной величине больше энергии их поступательного движения.
Газы отличаются от жидкостей тем, что в них энергия поступательного движения молекул больше абсолютного значения энергии их взаимодействия:

Именно поэтому газы не имеют какого-либо определенного объема (их молекулы не могут удержать друг друга в конечном объеме).
Согласно изложенному в критической точке (точке, в которой исчезает различие между газом и жидкостью) должно выполняться равенство

Для газов и жидкостей вблизи критического состояния  (а — силовая постоянная Ван-дер-Ваальса), поэтому критическую точку можно охарактеризовать отношением
(а — силовая постоянная Ван-дер-Ваальса), поэтому критическую точку можно охарактеризовать отношением

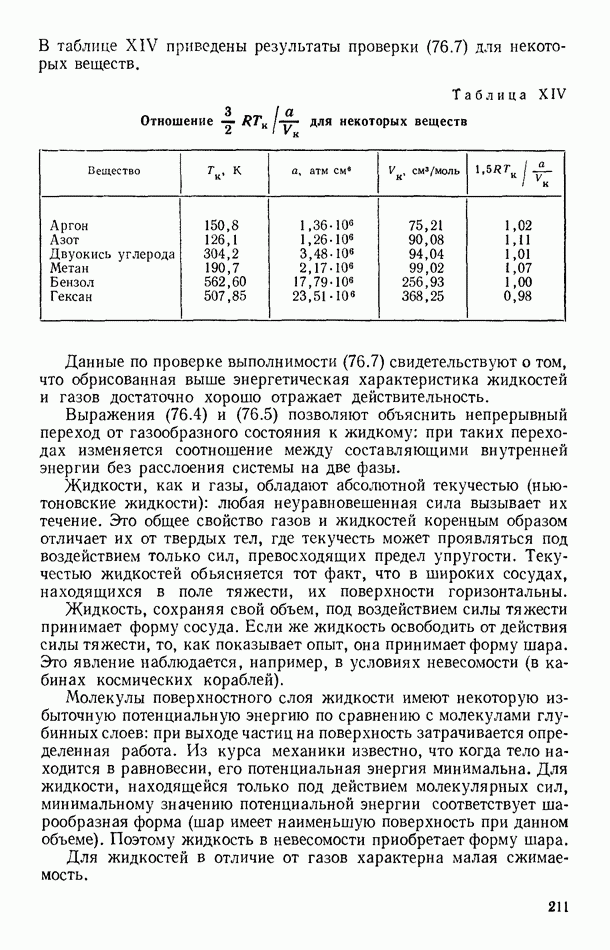
В таблице XIV приведены результаты проверки (76.7) для некоторых веществ.
Таблица XIV (см. скан) Отношение  для некоторых веществ
для некоторых веществ
Данные по проверке выполнимости (76.7) свидетельствуют о том, что обрисованная выше энергетическая характеристика жидкостей и газов достаточно хорошо отражает действительность.
Выражения (76.4) и (76.5) позволяют объяснить непрерывный переход от газообразного состояния к жидкому: при таких переходах изменяется соотношение между составляющими внутренней энергии без расслоения системы на две фазы.
Жидкости, как и газы, обладают абсолютной текучестью (ньютоновские жидкости): любая неуравновешенная сила вызывает их течение. Это общее свойство газов и жидкостей коренным образом отличает их от твердых тел, где текучесть может проявляться под воздействием только сил, превосходящих предел упругости. Текучестью жидкостей обьясняется тот факт, что в широких сосудах, находящихся в поле тяжести, их поверхности горизонтальны.
Жидкость, сохраняя свой объем, под воздействием силы тяжести принимает форму сосуда. Если же жидкость освободить от действия силы тяжести, то, как показывает опыт, она принимает форму шара. Это явление наблюдается, например, в условиях невесомости (в кабинах космических кораблей).
Молекулы поверхностного слоя жидкости имеют некоторую избыточную потенциальную энергию по сравнению с молекулами глубинных слоев: при выходе частиц на поверхность затрачивается определенная работа. Из курса механики известно, что когда тело находится в равновесии, его потенциальная энергия минимальна. Для жидкости, находящейся только под действием молекулярных сил, минимальному значению потенциальной энергии соответствует шарообразная форма (шар имеет наименьшую поверхность при данном объеме). Поэтому жидкость в невесомости приобретает форму шара.
Для жидкостей в отличие от газов характерна малая сжимаемость.
Сжимаемость жидкостей исследуется в приборах, которые называются пьезометрами. Схема простейшего пьезометра приведена на рисунке 8 2. Исследуемая жидкость помещается в сосуд А с капилляром а. Сосуд с жидкостью находится в камере В, в которой компрессором создается повышенное давление. Давление измеряется манометром  При увеличении давления уровень жидкости в капилляре понижается при неизменном объеме сосуда (давление внутри и снаружи сосуда изменяется одинаково). Если площадь сечения капилляра
При увеличении давления уровень жидкости в капилляре понижается при неизменном объеме сосуда (давление внутри и снаружи сосуда изменяется одинаково). Если площадь сечения капилляра  а уровень жидкости понизится в нем на
а уровень жидкости понизится в нем на  то изменение объема жидкости окажется равным
то изменение объема жидкости окажется равным  Зная начальный объем жидкости и определив по манометру изменение давления
Зная начальный объем жидкости и определив по манометру изменение давления  легко найти изотермический коэффициент сжатия:
легко найти изотермический коэффициент сжатия:

В таблице XV приведены данные о сжимаемости некоторых жидкостей.
Таблица XV (см. скан) Сжимаемость жидкостей (в единицах 

Рис. 8.2.
Изотермический коэффициент сжатия идеальных газов находится в обратной зависимости от давления:

Сжимаемость жидкостей намного меньше сжимаемости газов. Это объясняется тем, что межмолекулярные силы отталкивания столь велики, что даже внешнее давление в миллионы Па изменяет объем жидкостей на доли процента.
Жидкости обладают значительным коэффициентом теплового расширения (хотя и существенно меньшим, чем газы). Приборы для
измерения коэффициента теплового расширения тел называются дилатометрами. Дилатометр для жидкостей состоит из резервуара, изготовленного из плавленого кварца или стекла, снабженного калиброванным капилляром. Такой дилатометр имеет вид сосуда А с капилляром а, изображенного на рисунке 8.2. Расширение жидкости в дилатометре при изменении температуры определяется по перемещению ее уровня в капилляре. (Собственное расширение дилатометра может быть учтено введением поправок или его градуировкой по жидкости с известным коэффициентом расширения.) Измерив изменение объема жидкости  в дилатометре при изменении температуры
в дилатометре при изменении температуры  и зная начальный объем жидкости V, можно вычислить коэффициент объемного расширения (при постоянном давлении) по формуле
и зная начальный объем жидкости V, можно вычислить коэффициент объемного расширения (при постоянном давлении) по формуле

В таблице XVI приведены значения  для некоторых жидкостей при комнатной температуре.
для некоторых жидкостей при комнатной температуре.
Таблица XVI (см. скан) Коэффициенты объемного расширения некоторых жидкостей при 
Для идеальных газов

и при  следовательно,
следовательно, 
Из всех жидкостей, приведенных в таблице XVI, наибольшим коэффициентом объемного расширения обладает эфир, наименьшим — ртуть.
В заключение остановимся на теплоемкости жидкостей. Первое начало термодинамики в дифференциальной форме

при  можно представить в виде
можно представить в виде

Эта формула позволяет записать выражение для теплоемкости при постоянном давлении 

так как

Величина  характеризует изменение потенциальной энергии системы в зависимости от изменения объема; именно эта зависимость приводит к тому, что для жидкостей разность мольных величин
характеризует изменение потенциальной энергии системы в зависимости от изменения объема; именно эта зависимость приводит к тому, что для жидкостей разность мольных величин  отлична от
отлична от  Существует общее термодинамическое соотношение, связывающее для любого тела мольные теплоемкости:
Существует общее термодинамическое соотношение, связывающее для любого тела мольные теплоемкости:

где V — мольный объем вещества  коэффициент теплового расширения,
коэффициент теплового расширения,  изотермический коэффициент сжатия). Таким образом, зная
изотермический коэффициент сжатия). Таким образом, зная  из (76.14) можно определить
из (76.14) можно определить  Известен и другой способ определения теплоемкости
Известен и другой способ определения теплоемкости  основанный на измерениях скорости звука. Так, согласно (23.7)
основанный на измерениях скорости звука. Так, согласно (23.7)

где  плотность,
плотность,  скорость распространения механических возмущений (звука),
скорость распространения механических возмущений (звука),  Таким образом, зная
Таким образом, зная  можно найти
можно найти 
В таблице XVII приведены значения  для некоторых жидкостей.
для некоторых жидкостей.
Таблица XVII (см. скан) Значения  и
и  для некоторых жидкостей при
для некоторых жидкостей при 
Интересно отметить, что для многоатомных веществ при температурах, лежащих ниже точек кипения, молярные теплоемкости жидкостей и соответствующие теплоемкости паров отличаются друг от друга, как показывает опыт, примерно на 

Таким образом, теплоемкости жидкостей значительно превышают теплоемкости их паров; но, как это видно из последней таблицы, значения у у жидкостей примерно такие же, как и у газов.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Глава I. ОСНОВНЫЕ ТЕРМОДИНАМИЧЕСКИЕ ПОНЯТИЯ И СВОЙСТВА ИДЕАЛЬНЫХ ГАЗОВ
- § 1 О ДВУХ МЕТОДАХ ИССЛЕДОВАНИЯ ФИЗИЧЕСКИХ ЯВЛЕНИЙ
- § 2. ОСНОВНЫЕ ПОНЯТИЯ И ПРЕДСТАВЛЕНИЯ ТЕРМОДИНАМИЧЕСКОГО ОПИСАНИЯ СИСТЕМ
- § 3 ТЕРМИЧЕСКОЕ УРАВНЕНИЕ СОСТОЯНИЯ. РАВНОВЕСНЫЕ ПРОЦЕССЫ
- § 4. ИЗОПРОЦЕССЫ
- § 5. МЕЖДУНАРОДНАЯ ПРАКТИЧЕСКАЯ ТЕМПЕРАТУРНАЯ ШКАЛА
- § 6. МЕТОДЫ ИЗМЕРЕНИЯ ТЕМПЕРАТУРЫ
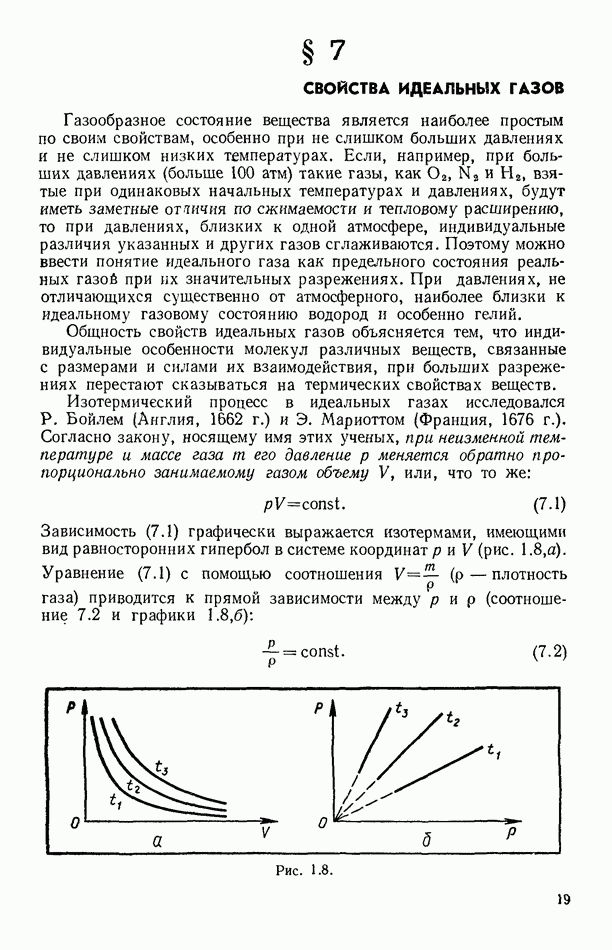
- § 7. СВОЙСТВА ИДЕАЛЬНЫХ ГАЗОВ
- § 8. РАБОТА РАСШИРЕНИЯ СИСТЕМЫ И ФИЗИЧЕСКИЙ СМЫСЛ УНИВЕРСАЛЬНОЙ ГАЗОВОЙ ПОСТОЯННОЙ
- § 9. УРАВНЕНИЕ СОСТОЯНИЯ СМЕСИ ИДЕАЛЬНЫХ ГАЗОВ
- § 10. ИЗМЕРЕНИЕ ДАВЛЕНИЙ
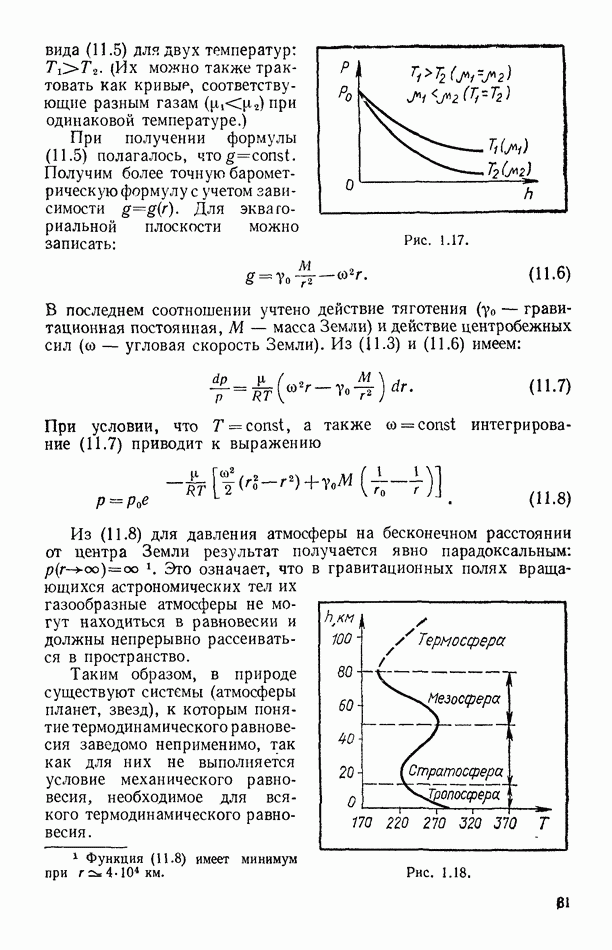
- § 11. БАРОМЕТРИЧЕСКАЯ ФОРМУЛА
- Глава II. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- § 12. О ЗАКОНЕ СОХРАНЕНИЯ И ПРЕВРАЩЕНИЯ ЭНЕРГИИ
- § 13. РАБОТА КАК МАКРОСКОПИЧЕСКИЙ СПОСОБ ПЕРЕДАЧИ ЭНЕРГИИ
- § 14. ТЕПЛОТА КАК МИКРОФИЗИЧЕСКИЙ СПОСОБ ПЕРЕДАЧИ ЭНЕРГИИ. ТЕПЛОЕМКОСТЬ
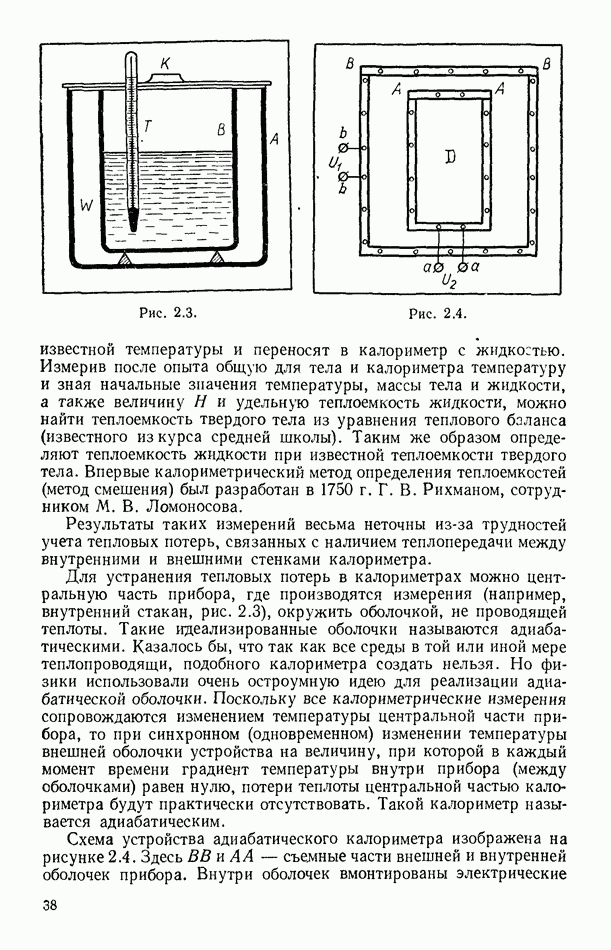
- § 15. ИЗМЕРЕНИЕ ТЕПЛОЕМКОСТИ
- § 16. ВНУТРЕННЯЯ ЭНЕРГИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ СИСТЕМЫ
- § 17. ФОРМУЛИРОВКА ПЕРВОГО НАЧАЛА ТЕРМОДИНАМИКИ
- § 18. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ ДЛЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 19. ИЗОБАРИЧЕСКИЙ ПРОЦЕСС В ИДЕАЛЬНОМ ГАЗЕ
- § 20. ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС В ИДЕАЛЬНОМ ГАЗЕ
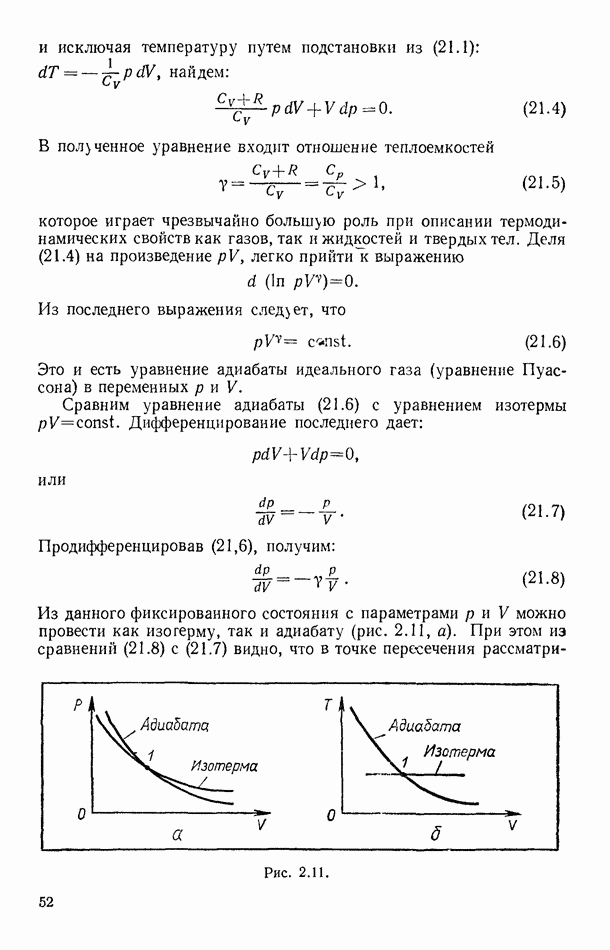
- § 21. АДИАБАТИЧЕСКИЙ ПРОЦЕСС В ИДЕАЛЬНОМ ГАЗЕ
- § 22. ПОЛИТРОПИЧЕСКИЕ ПРОЦЕССЫ В ИДЕАЛЬНОМ ГАЗЕ
- § 23. ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ ТЕПЛОЕМКОСТЕЙ Cp/Cv
- § 24. ТЕПЛОЕМКОСТЬ СМЕСИ ГАЗОВ
- § 18. ЭНТАЛЬПИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ СИСТЕМЫ
- Глава III. МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ И ЕЕ ПРИМЕНЕНИЕ К ИДЕАЛЬНЫМ ГАЗАМ
- § 26. ИСХОДНЫЕ ПОЛОЖЕНИЯ МОЛЕКУЛЯРНОЙ ТЕОРИИ
- § 27. СРЕДНИЕ ВЕЛИЧИНЫ В ОПИСАНИИ МОЛЕКУЛЯРНЫХ СИСТЕМ
- § 28. ОСНОВНЫЕ ПОНЯТИЯ ТЕОРИИ ВЕРОЯТНОСТЕЙ
- § 29. РАСПРЕДЕЛЕНИЕ ЧАСТИЦ ПО ЭНЕРГИЯМ (РАСПРЕДЕЛЕНИЕ БОЛЬЦМАНА)
- § 30. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ПО КОМПОНЕНТАМ СКОРОСТЕЙ ИХ ТЕПЛОВОГО ДВИЖЕНИЯ (РАСПРЕДЕЛЕНИЕ МАКСВЕЛЛА)
- § 31. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ПО СКОРОСТЯМ ИХ ТЕПЛОВОГО ДВИЖЕНИЯ (РАСПРЕДЕЛЕНИЕ МАКСВЕЛЛА)
- § 32. ОПЫТНАЯ ПРОВЕРКА РАСПРЕДЕЛЕНИЯ МАКСВЕЛЛА
- § 33. УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА ПО КИНЕТИЧЕСКОЙ ТЕОРИИ
- § 34. ПЛОТНОСТЬ ПОТОКА МОЛЕКУЛ В ИДЕАЛЬНОМ ГАЗЕ
- § 35. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ИДЕАЛЬНОГО ГАЗА В ПОЛВ СИЛЫ ТЯЖЕСТИ
- § 36. БРОУНОВСКОЕ ДВИЖЕНИЕ. ОПРЕДЕЛЕНИЕ ПЕРРЕНОМ ЧИСЛА АВОГАДРО
- § 37. ТЕОРЕМА О РАВНОРАСПРЕДЕЛЕНИИ И ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 38. КВАНТОВАЯ ТЕОРИЯ ТЕПЛОЕМКОСТИ ГАЗОВ
- § 39. ТЕРМОДИНАМИЧЕСКАЯ ВЕРОЯТНОСТЬ И РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ИДЕАЛЬНОГО ГАЗА В ПРОСТРАНСТВЕ
- Глава IV. ЯВЛЕНИЯ ПЕРЕНОСА И ИХ ТЕОРИЯ ДЛЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 40. ТЕПЛОПРОВОДНОСТЬ
- § 41. ВНУТРЕННЕЕ ТРЕНИЕ (ВЯЗКОСТЬ)
- § 42. ДИФФУЗИЯ
- § 43. СРЕДНЯЯ ДЛИНА СВОБОДНОГО ПРОБЕГА МОЛЕКУЛ
- § 44. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ПО ДЛИНАМ ИХ СВОБОДНЫХ ПРОБЕГОВ
- § 45. ОБЩЕЕ УРАВНЕНИЕ ДЛЯ ЯВЛЕНИИ ПЕРЕНОСА В ИДЕАЛЬНЫХ ГАЗАХ
- § 46. ДИФФУЗИЯ В ИДЕАЛЬНЫХ ГАЗАХ
- § 47. ВНУТРЕННЕЕ ТРЕНИЕ В ИДЕАЛЬНЫХ ГАЗАХ
- § 48. ТЕПЛОПРОВОДНОСТЬ ИДЕАЛЬНЫХ ГАЗОВ
- § 49. СВЯЗЬ МЕЖДУ КОЭФФИЦИЕНТАМИ ПЕРЕНОСА
- Глава V. СИЛЬНО РАЗРЕЖЕННЫЕ ГАЗЫ
- § 50. ПОЛУЧЕНИЕ И ИЗМЕРЕНИЕ ВАКУУМА
- § 51. СИЛЫ ТРЕНИЯ в ВАКУУМЕ
- § 52. ТЕПЛОПЕРЕДАЧА В ВАКУУМЕ
- § 53. ДИФФУЗИЯ В ВАКУУМЕ
- Глава VI. РЕАЛЬНЫЕ ГАЗЫ
- § 54. ОТКЛОНЕНИЕ ОТ ЗАКОНА БОЙЛЯ—МАРИОТТА
- § 55. РАВНОВЕСИЕ СИСТЕМЫ ЖИДКОСТЬ — ПАР
- § 56. ЭКСПЕРИМЕНТАЛЬНЫЕ ИЗОТЕРМЫ. КРИТИЧЕСКОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- § 57. ПОТЕНЦИАЛ ПАРНОГО ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ
- § 58. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- § 59. ИЗОТЕРМЫ ВАН-ДЕР-ВААЛЬСА. КРИТИЧЕСКИЕ ПАРАМЕТРЫ И ПОСТОЯННЫЕ ВАН-ДЕР-ВААЛЬСА
- § 60. ВНУТРЕННЯЯ ЭНЕРГИЯ РЕАЛЬНОГО ГАЗА. ЭФФЕКТ ДЖОУЛЯ — ТОМСОНА
- § 61. СЖИЖЕНИЕ ГАЗОВ
- § 62. УРАВНЕНИЕ СОСТОЯНИЯ РЕАЛЬНЫХ ГАЗОВ В ВИРИАЛЬНОЙ ФОРМЕ
- Глава VII. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- § 63. РАВНОВЕСНЫЕ И НЕРАВНОВЕСНЫЕ ПРОЦЕССЫ
- § 64. ОБРАТИМЫЕ И НЕОБРАТИМЫЕ ПРОЦЕССЫ
- § 65. ЦИКЛИЧЕСКИЕ (КРУГОВЫЕ) ПРОЦЕССЫ
- § 66. ЦИКЛ КАРНО
- § 67. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ ДЛЯ ОБРАТИМЫХ ПРОЦЕССОВ
- § 68. ЭНТРОПИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ СИСТЕМЫ
- § 69. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ ДЛЯ НЕОБРАТИМЫХ ПРОЦЕССОВ
- § 70. НЕРАВЕНСТВО КЛАУЗИУСА. ПРИНЦИП ВОЗРАСТАНИЯ ЭНТРОПИИ
- § 71. ЭНТРОПИЯ И ВЕРОЯТНОСТЬ СОСТОЯНИЯ СИСТЕМЫ
- § 72. О ТАК НАЗЫВАЕМОЙ «ТЕПЛОВОЙ СМЕРТИ ВСЕЛЕННОЙ»
- § 73. ИЗОЭНТРОПИЧЕСКОЕ СОСТОЯНИЕ ТРОПОСФЕРЫ ЗЕМЛИ
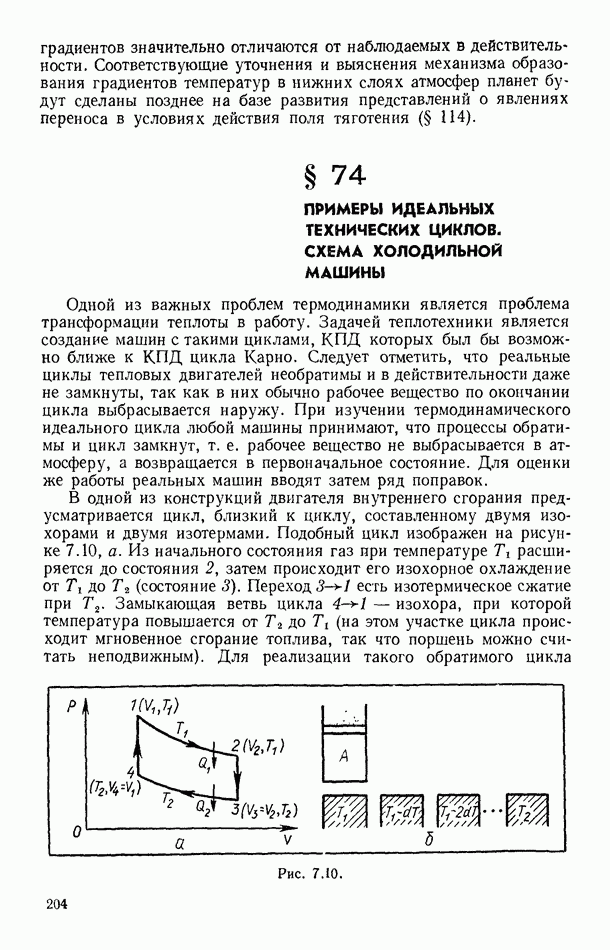
- § 74. ПРИМЕРЫ ИДЕАЛЬНЫХ ТЕХНИЧЕСКИХ ЦИКЛОВ. СХЕМА ХОЛОДИЛЬНОЙ МАШИНЫ
- Глава VIII. ЖИДКОСТИ
- § 75. ТЕПЛОВОЕ ДВИЖЕНИЕ И СТРУКТУРА ЖИДКОСТЕЙ
- § 76. ОСНОВНЫЕ СВОЙСТВА ЖИДКОСТЕЙ
- § 77. ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ ЖИДКОСТЕЙ
- § 78. МОЛЕКУЛЯРНОЕ ДАВЛЕНИЕ ПОВЕРХНОСТНОГО СЛОЯ ЖИДКОСТИ
- § 79. СИЛЫ, ВОЗНИКАЮЩИЕ НА КРИВОЙ ПОВЕРХНОСТИ ЖИДКОСТЕЙ
- § 80. КРАЕВОЙ УГОЛ. КАПИЛЛЯРНЫЕ ЯВЛЕНИЯ
- § 81. КИПЕНИЕ ЖИДКОСТЕЙ
- § 82. ТЕПЛОТА ПАРООБРАЗОВАНИЯ ЖИДКОСТЕЙ
- § 83. УРАВНЕНИЕ КЛАПЕЙРОНА — КЛАУЗИУСА
- § 84. ВЯЗКОСТЬ ЖИДКОСТЕЙ
- § 85. ЖИДКИЕ РАСТВОРЫ. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ. ЗАКОН РАУЛЯ
- § 86. ЖИДКИЙ ГЕЛИЙ. СВЕРХТЕКУЧЕСТЬ
- Глава IX. ТВЕРДЫЕ ТЕЛА
- § 87. ОСНОВНЫЕ ОСОБЕННОСТИ ТВЕРДЫХ ТЕЛ
- § 88. СТРУКТУРА КРИСТАЛЛОВ
- § 89. ФИЗИЧЕСКИЕ ТИПЫ КРИСТАЛЛИЧЕСКИХ РЕШЕТОК
- § 90. ТЕПЛОВОЕ ДВИЖЕНИЕ В КРИСТАЛЛАХ
- § 91. МЕХАНИЧЕСКИЕ СВОЙСТВА КРИСТАЛЛОВ
- § 92. ДЕФЕКТЫ В ТВЕРДЫХ ТЕЛАХ
- § 93. ТЕПЛОВОЕ РАСШИРЕНИЕ ТВЕРДЫХ ТЕЛ
- § 94. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ
- § 95. ПЛАВЛЕНИЕ И КРИСТАЛЛИЗАЦИЯ
- § 96. ДИАГРАММЫ СОСТОЯНИЙ. ТРОЙНАЯ ТОЧКА
- § 97. ТЕПЛОТА ПЛАВЛЕНИЯ ПРОСТЫХ КРИСТАЛЛИЧЕСКИХ СТРУКТУР
- Глава X. ПОЛИМЕРЫ
- § 98. ОБЩИЕ ПРЕДСТАВЛЕНИЯ
- § 99. ПОЛУЧЕНИЕ ПОЛИМЕРОВ
- § 100. НЕКОТОРЫЕ ТИПЫ ПОЛИМЕРОВ. РОЛЬ МЕЖМОЛЕКУЛЯРНЫХ ВЗАИМОДЕЙСТВИЙ
- § 101. ТРИ СОСТОЯНИЯ АМОРФНЫХ ПОЛИМЕРОВ И ТЕПЛОВОЕ ДВИЖЕНИЕ В НИХ
- § 102. ЭЛАСТИЧНОСТЬ ПОЛИМЕРОВ
- § 103. КРИСТАЛЛИЧЕСКИЕ ПОЛИМЕРЫ
- § 104. ПРИМЕНЕНИЕ ПОЛИМЕРНЫХ МАТЕРИАЛОВ
- Глава XI. ЭЛЕМЕНТЫ ТЕРМОДИНАМИКИ ТЕКУЧИХ СРЕД И РАКЕТНОЙ ТЕХНИКИ
- § 105. РАБОТА ПЕРЕМЕЩЕНИЯ В ТЕКУЧИХ СРЕДАХ
- § 106. ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИ ДЛЯ ПОТОКОВ ГАЗОВ И ЖИДКОСТЕЙ
- § 107. ЧАСТНЫЕ СЛУЧАИ ТЕЧЕНИЯ СРЕД
- § 108. ИСТЕЧЕНИЕ ГАЗОВ ИЗ СОПЕЛ. КРИТИЧЕСКАЯ СКОРОСТЬ
- § 109. ПРИНЦИП ДВИЖЕНИЯ РАКЕТ
- § 110. ЭЛЕМЕНТАРНАЯ ТЕРМОДИНАМИКА РАКЕТНОГО ДВИГАТЕЛЯ
- § 111. СХЕМЫ РАКЕТНЫХ ДВИГАТЕЛЕЙ
- § 112. МНОГОСТУПЕНЧАТЫЕ РАКЕТЫ
- § 113. ДВИЖЕНИЕ СО СВЕРХЗВУКОВОЙ СКОРОСТЬЮ. УДАРНЫЕ ВОЛНЫ
- § 114. О ГРАДИЕНТЕ ТЕМПЕРАТУРЫ В ТРОПОСФЕРЕ ЗЕМЛИ