| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
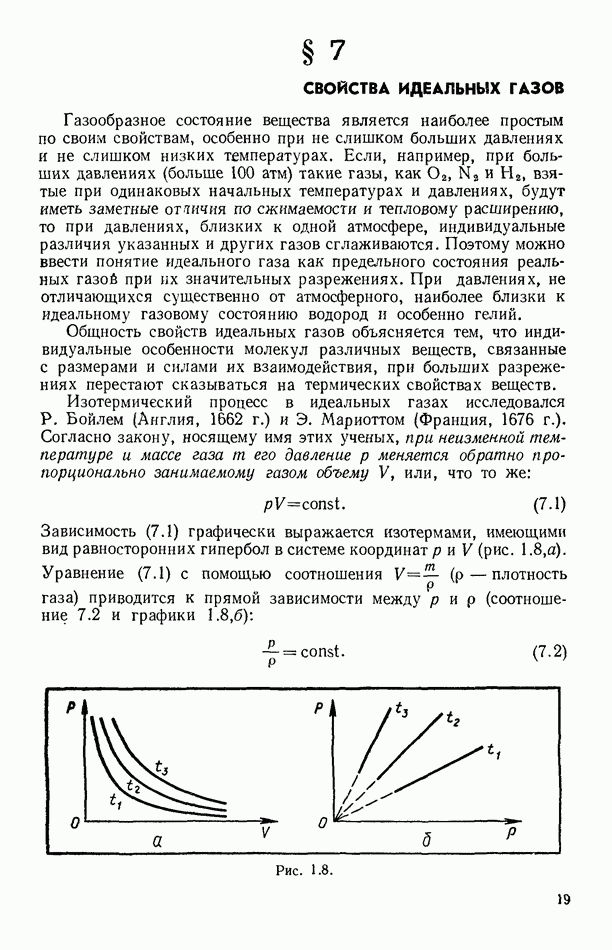
§ 85. ЖИДКИЕ РАСТВОРЫ. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ. ЗАКОН РАУЛЯ
Многие жидкости являются хорошими растворителями (вода, бензин, ацетон, изопентан, скипидар и др.). В жидкостях могут растворяться твердые вещества, жидкости, газы. При образовании раствора молекулы растворенного вещества равномерно распределяются между молекулами растворителя, в результате образуется однородная по физическим свойствам система.
Количественно растворы характеризуются концентрацией, определяющей содержание растворенного вещества в растворе. Существует несколько способов определения концентраций, при этом чаще используются весовая и мольная концентрации. Весовая концентрация — отношение массы растворенного вещества к массе всего растворителя. Мольная концентрация — отношение числа молей растворенного вещества к общему числу молей в растворе.
Растворение является следствием взаимодействия молекул растворенного вещества с молекулами растворителя, при этом в случае растворения твердого тела или жидкости происходит разделение частиц растворяемого вещества и их сближение с частицами растворителя. Разделение частиц требует затраты энергии, а сближение сопровождается ее выделением. Поэтому растворение, как правило, сопровождается тепловым эффектом — поглощением или выделением теплоты. И только в тех случаях, когда работа разделения частиц компенсируется энергией, выделяющейся при сближении разнородных молекул, тепловой эффект растворения равен нулю.
Растворение спирта в воде сопровождается выделением теплоты и нагревом раствора. Растворение же сахара в воде вызывает охлаждение раствора: при растворении поглощается теплота. Легко понять, что в первом случае энергия взаимодействия однородных молекул меньше, чем разнородных (во втором случае соотношение обратное).
При растворении твердого вещества (а в некоторых случаях и жидкости) можно получить насыщенный раствор (раствор, в котором вещество перестает растворяться). Очевидно, насыщенный раствор находится в динамическом равновесии с твердым телом. Если при растворении происходит охлаждение, то с повышением температуры растворение увеличивается. Охлаждение подобных насыщенных растворов ведет к пересыщению — неустойчивому (метастабиль-ному) состоянию. При внесении в такой раствор зародыша твердой фазы — частицы вещества — он будет служить центром кристаллизации, начнется рост кристалла растворенного вещества.
Если при растворении наблюдается нагревание, то с повышением температуры растворимость уменьшается, и получить пересыщенный раствор в этом случае можно повышением температуры.
Растворение газа в жидкости очень сильно зависит от природы газа. Например, углекислый газ очень хорошо поглощается водой: один литр воды при атмосферном давлении поглощает примерно один литр углекислого газа. Другие газы поглощаются водой меньше. Азота при атмосферном давлении поглощается  на литр воды, кислорода —
на литр воды, кислорода —  Растворимость кислорода в воде примерно вдвое больше, чем растворимость азота, и, следовательно, растворенный в воде воздух значительно богаче кислородом, чем воздух над поверхностью воды.
Растворимость кислорода в воде примерно вдвое больше, чем растворимость азота, и, следовательно, растворенный в воде воздух значительно богаче кислородом, чем воздух над поверхностью воды.
Растворение газов подчиняется закону Генри: при не очень больших давлениях масса растворенного газа пропорциональна его давлению над растворителем.
Поглощение газов жидкостями зависит также и от температуры: как правило, с повышением температуры оно уменьшается.
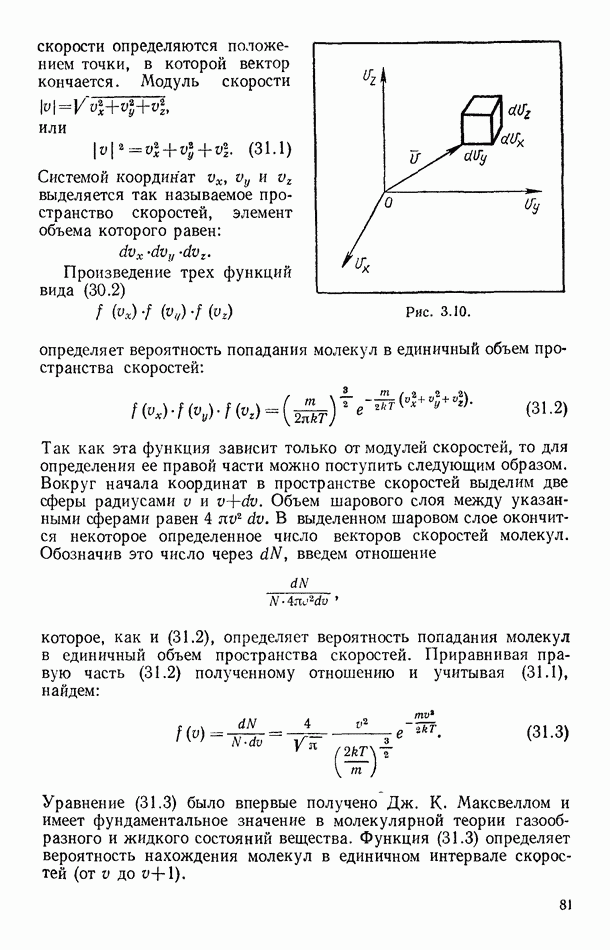
Если раствор разбавленный (концентрация мала), то расстояния между молекулами растворенного вещества будут намного больше их размеров, вследствие чего поведение растворенного вещества в слабом растворе подобно поведению идеального газа. Подобно тому как газ оказывает давление на стенки сосуда, растворенное вещество тоже должно оказывать давление в растворе. Парциальное термическое давление растворенного вещества называется осмотическим давлением и обозначается роси. Осмотическое давление вещества в растворе, содержащем массу  растворенного вещества, можно подсчитать, пользуясь уравнением Клапейрона — Менделеева:
растворенного вещества, можно подсчитать, пользуясь уравнением Клапейрона — Менделеева:


Рис. 8.19.
где  молекулярная масса вещества, V — объем раствора. Величина
молекулярная масса вещества, V — объем раствора. Величина  определяет массу растворенного вещества в единице объема раствора (одна из характеристик концентрации). С использованием этого обозначения уравнение (85.1) можно записать в следующем виде:
определяет массу растворенного вещества в единице объема раствора (одна из характеристик концентрации). С использованием этого обозначения уравнение (85.1) можно записать в следующем виде:

Выражение (85.2) называется законом Вант-Гоффа
Осмотическое давление может достигать значительных величин. Так, растворение одного куска сахара в стакане воды создает осмотическое давление, превышающее 2 атм.
Для обнаружения осмотического давления прибегают к использованию полупроницаемых перегородок, способных свободно пропускать растворитель, но задерживающих молекулы растворенного вещества.
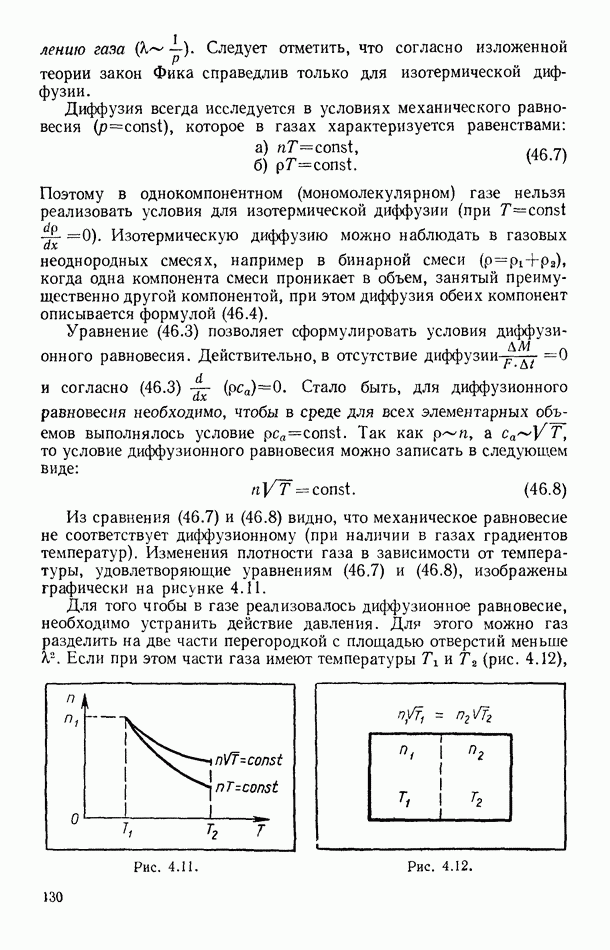
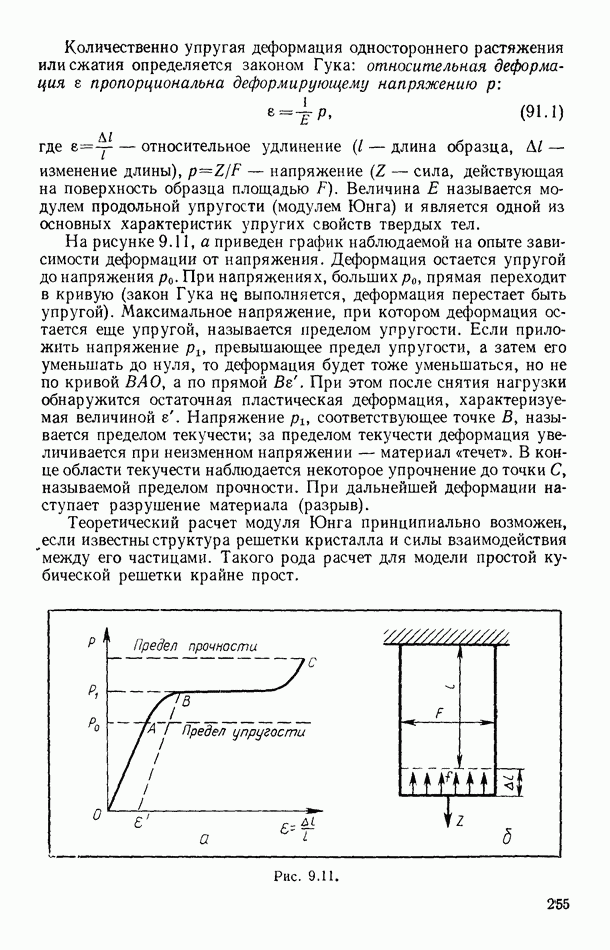
Схема опыта по демонстрации осмотического давления представлена на рисунке 8.19. В сосуде а, опущенном в воду, находится раствор сахара. Дном этого сосуда служит полупроницаемая перегородка  Верхняя часть сосуда оканчивается длинной трубкой
Верхняя часть сосуда оканчивается длинной трубкой  В начале опыта сосуд а располагают так, чтобы верхний уровень раствора в нем совпадал бы с уровнем воды
В начале опыта сосуд а располагают так, чтобы верхний уровень раствора в нем совпадал бы с уровнем воды  в которую опущен прибор. Через достаточно большое время, которое длится часами, можно наблюдать поднятие уровня жидкости в измерительной трубке
в которую опущен прибор. Через достаточно большое время, которое длится часами, можно наблюдать поднятие уровня жидкости в измерительной трубке  Под воздействием осмотического давления уровень раствора поднимается до тех пор, пока гидростатическое давление поднявшегося столба жидкости не окажется равным осмотическому (парциальному) давлению растворенного сахара:
Под воздействием осмотического давления уровень раствора поднимается до тех пор, пока гидростатическое давление поднявшегося столба жидкости не окажется равным осмотическому (парциальному) давлению растворенного сахара:

где  плотность раствора. При этом, очевидно, поднятие раствора в трубке связано с засасыванием воды в сосуд через полупроницаемую перегородку.
плотность раствора. При этом, очевидно, поднятие раствора в трубке связано с засасыванием воды в сосуд через полупроницаемую перегородку.
Измеряя таким способом осмотическое давление, Вант-Гофф установил, что оно в соответствии с уравнением (85.2) пропорционально концентрации растворенного вещества и температуре.
Для слабых растворов многих веществ закон Вант-Гоффа оправдывается хорошо. Однако в ряде случаев, например для растворов неорганических солей, осмотическое давление оказывается значительно больше вычисленного по (85.2). Это объясняется электролитической диссоциацией — распадом молекул некоторых веществ
на ионы (электрически заряженные атомы и группы атомов), в результате чего возрастает число частиц, создающих осмотическое давление, соответственно возрастает и само осмотическое давление.
Осмотическое давление играет большую роль в процессах, происходящих в живых организмах. Это объясняется тем, что оболочки клеток животных и растений представляют собой полупроницаемые перегородки.
В конце прошлого века французским химиком Ф. Раулем (1884 г.) на основании многочисленных измерений было показано, что давление насыщенных паров  растворителя над раствором нелетучего вещества меньше, чем давление насыщенных паров
растворителя над раствором нелетучего вещества меньше, чем давление насыщенных паров  над чистым растворителем при той же температуре. Например, давление паров воды над водным раствором сахара ниже, чем давление паров чистой воды. Опытным путем Рауль нашел, что для разбавленных растворов относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества:
над чистым растворителем при той же температуре. Например, давление паров воды над водным раствором сахара ниже, чем давление паров чистой воды. Опытным путем Рауль нашел, что для разбавленных растворов относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества:

где  число молей растворенного вещества,
число молей растворенного вещества,  число молей растворителя. Соотношение (85.4) носит название закона Рауля.
число молей растворителя. Соотношение (85.4) носит название закона Рауля.
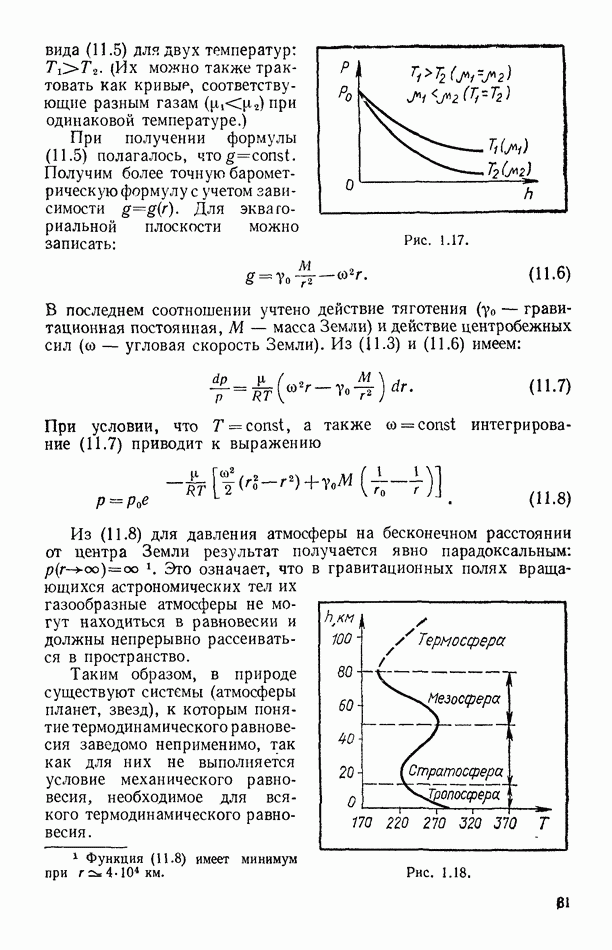
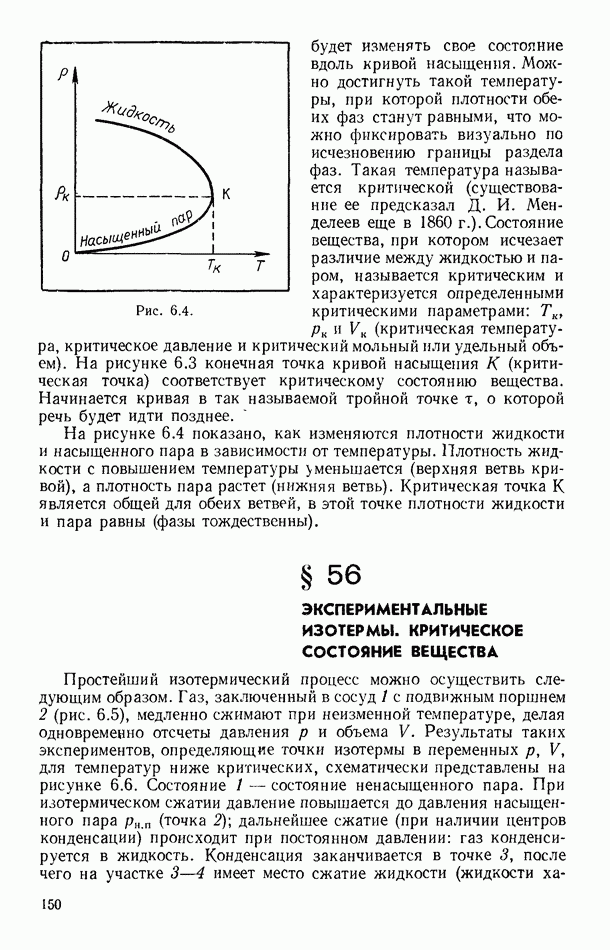
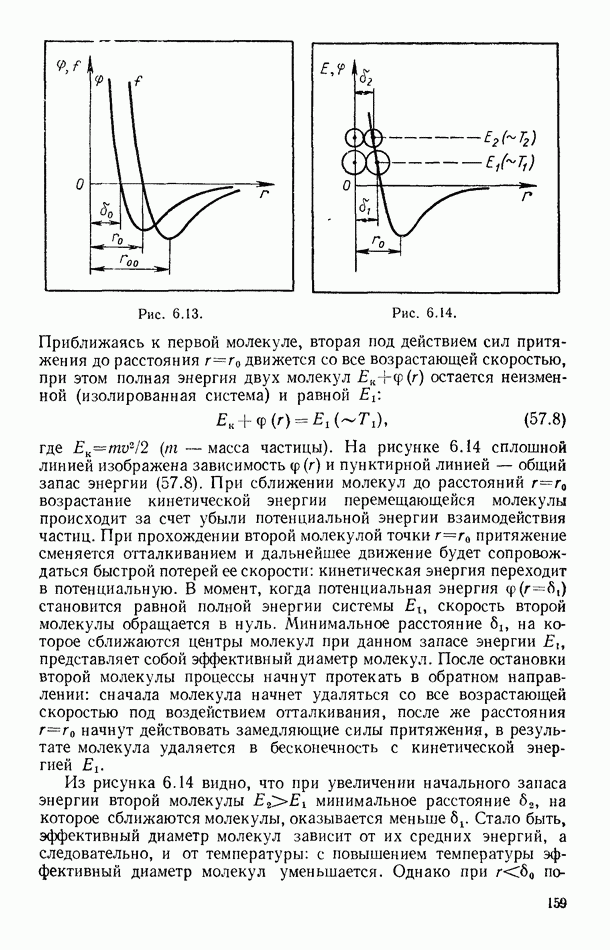
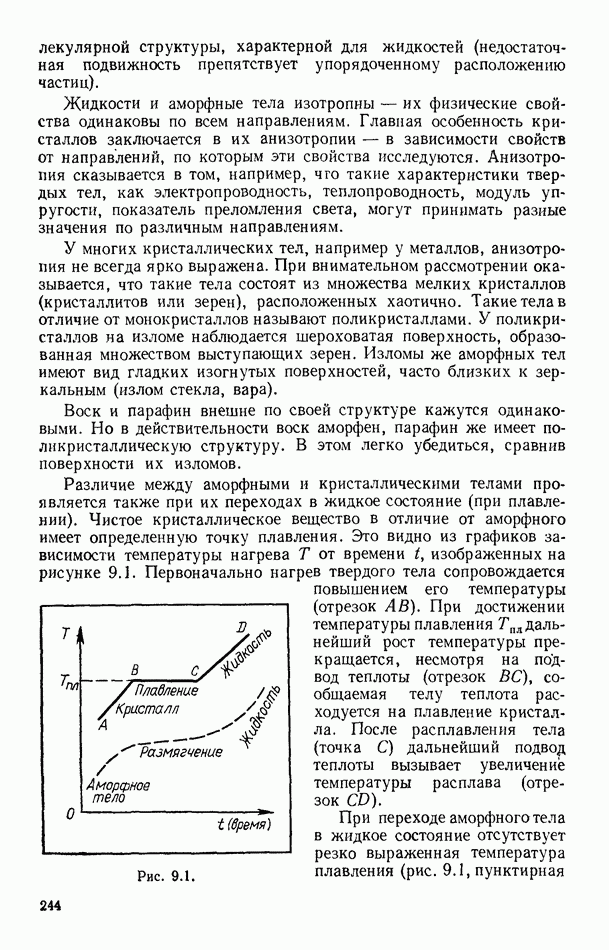
Понижение давления пара растворителя над раствором является причиной повышения температуры кипения раствора по сравнению с температурой кипения чистого растворителя. Действительно, при кипении жидкостей давление их насыщенных паров должно быть равным внешнему давлению (например, атмосферному). Если же давление насыщенного пара над раствором меньше, чем над чистым растворителем, то раствор следует нагреть до более высокой температуры, чтобы возросшее давление стало бы равным внешнему давлению. Рассматриваемое явление поясняет рисунок 8.20, на котором сплошной линией изображена зависимость давления насыщенного пара чистого растворителя от температуры, пунктирной линией — давление паров растворителя над раствором. Температура кипения чистого растворителя  и раствора
и раствора  определяются пересечением изображенных кривых с прямой, параллельной оси абсцисс (температур) и соответствующей внешнему давлению
определяются пересечением изображенных кривых с прямой, параллельной оси абсцисс (температур) и соответствующей внешнему давлению 
Для разбавленных растворов повышение температуры кипения

Рис. 7.20.
раствора  пропорционально мольной доле растворенного вещества:
пропорционально мольной доле растворенного вещества:

где X — мольная теплота испарения растворителя. Соотношение (85.5) легко получить из уравнения Клапейрона — Клаузиуса (83.6) и закона Рауля (85.4).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Глава I. ОСНОВНЫЕ ТЕРМОДИНАМИЧЕСКИЕ ПОНЯТИЯ И СВОЙСТВА ИДЕАЛЬНЫХ ГАЗОВ
- § 1 О ДВУХ МЕТОДАХ ИССЛЕДОВАНИЯ ФИЗИЧЕСКИХ ЯВЛЕНИЙ
- § 2. ОСНОВНЫЕ ПОНЯТИЯ И ПРЕДСТАВЛЕНИЯ ТЕРМОДИНАМИЧЕСКОГО ОПИСАНИЯ СИСТЕМ
- § 3 ТЕРМИЧЕСКОЕ УРАВНЕНИЕ СОСТОЯНИЯ. РАВНОВЕСНЫЕ ПРОЦЕССЫ
- § 4. ИЗОПРОЦЕССЫ
- § 5. МЕЖДУНАРОДНАЯ ПРАКТИЧЕСКАЯ ТЕМПЕРАТУРНАЯ ШКАЛА
- § 6. МЕТОДЫ ИЗМЕРЕНИЯ ТЕМПЕРАТУРЫ
- § 7. СВОЙСТВА ИДЕАЛЬНЫХ ГАЗОВ
- § 8. РАБОТА РАСШИРЕНИЯ СИСТЕМЫ И ФИЗИЧЕСКИЙ СМЫСЛ УНИВЕРСАЛЬНОЙ ГАЗОВОЙ ПОСТОЯННОЙ
- § 9. УРАВНЕНИЕ СОСТОЯНИЯ СМЕСИ ИДЕАЛЬНЫХ ГАЗОВ
- § 10. ИЗМЕРЕНИЕ ДАВЛЕНИЙ
- § 11. БАРОМЕТРИЧЕСКАЯ ФОРМУЛА
- Глава II. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- § 12. О ЗАКОНЕ СОХРАНЕНИЯ И ПРЕВРАЩЕНИЯ ЭНЕРГИИ
- § 13. РАБОТА КАК МАКРОСКОПИЧЕСКИЙ СПОСОБ ПЕРЕДАЧИ ЭНЕРГИИ
- § 14. ТЕПЛОТА КАК МИКРОФИЗИЧЕСКИЙ СПОСОБ ПЕРЕДАЧИ ЭНЕРГИИ. ТЕПЛОЕМКОСТЬ
- § 15. ИЗМЕРЕНИЕ ТЕПЛОЕМКОСТИ
- § 16. ВНУТРЕННЯЯ ЭНЕРГИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ СИСТЕМЫ
- § 17. ФОРМУЛИРОВКА ПЕРВОГО НАЧАЛА ТЕРМОДИНАМИКИ
- § 18. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ ДЛЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 19. ИЗОБАРИЧЕСКИЙ ПРОЦЕСС В ИДЕАЛЬНОМ ГАЗЕ
- § 20. ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС В ИДЕАЛЬНОМ ГАЗЕ
- § 21. АДИАБАТИЧЕСКИЙ ПРОЦЕСС В ИДЕАЛЬНОМ ГАЗЕ
- § 22. ПОЛИТРОПИЧЕСКИЕ ПРОЦЕССЫ В ИДЕАЛЬНОМ ГАЗЕ
- § 23. ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ ТЕПЛОЕМКОСТЕЙ Cp/Cv
- § 24. ТЕПЛОЕМКОСТЬ СМЕСИ ГАЗОВ
- § 18. ЭНТАЛЬПИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ СИСТЕМЫ
- Глава III. МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ И ЕЕ ПРИМЕНЕНИЕ К ИДЕАЛЬНЫМ ГАЗАМ
- § 26. ИСХОДНЫЕ ПОЛОЖЕНИЯ МОЛЕКУЛЯРНОЙ ТЕОРИИ
- § 27. СРЕДНИЕ ВЕЛИЧИНЫ В ОПИСАНИИ МОЛЕКУЛЯРНЫХ СИСТЕМ
- § 28. ОСНОВНЫЕ ПОНЯТИЯ ТЕОРИИ ВЕРОЯТНОСТЕЙ
- § 29. РАСПРЕДЕЛЕНИЕ ЧАСТИЦ ПО ЭНЕРГИЯМ (РАСПРЕДЕЛЕНИЕ БОЛЬЦМАНА)
- § 30. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ПО КОМПОНЕНТАМ СКОРОСТЕЙ ИХ ТЕПЛОВОГО ДВИЖЕНИЯ (РАСПРЕДЕЛЕНИЕ МАКСВЕЛЛА)
- § 31. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ПО СКОРОСТЯМ ИХ ТЕПЛОВОГО ДВИЖЕНИЯ (РАСПРЕДЕЛЕНИЕ МАКСВЕЛЛА)
- § 32. ОПЫТНАЯ ПРОВЕРКА РАСПРЕДЕЛЕНИЯ МАКСВЕЛЛА
- § 33. УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА ПО КИНЕТИЧЕСКОЙ ТЕОРИИ
- § 34. ПЛОТНОСТЬ ПОТОКА МОЛЕКУЛ В ИДЕАЛЬНОМ ГАЗЕ
- § 35. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ИДЕАЛЬНОГО ГАЗА В ПОЛВ СИЛЫ ТЯЖЕСТИ
- § 36. БРОУНОВСКОЕ ДВИЖЕНИЕ. ОПРЕДЕЛЕНИЕ ПЕРРЕНОМ ЧИСЛА АВОГАДРО
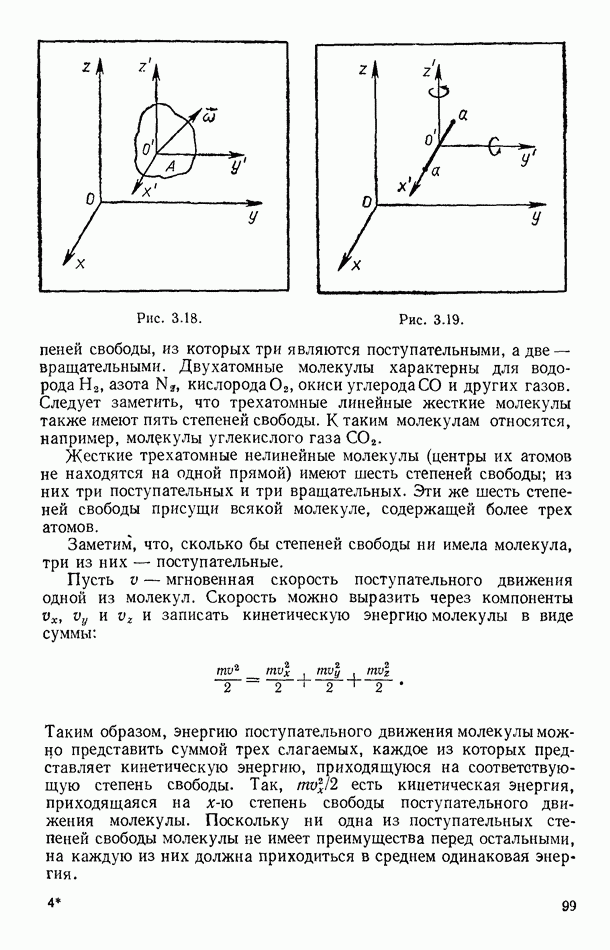
- § 37. ТЕОРЕМА О РАВНОРАСПРЕДЕЛЕНИИ И ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 38. КВАНТОВАЯ ТЕОРИЯ ТЕПЛОЕМКОСТИ ГАЗОВ
- § 39. ТЕРМОДИНАМИЧЕСКАЯ ВЕРОЯТНОСТЬ И РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ИДЕАЛЬНОГО ГАЗА В ПРОСТРАНСТВЕ
- Глава IV. ЯВЛЕНИЯ ПЕРЕНОСА И ИХ ТЕОРИЯ ДЛЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 40. ТЕПЛОПРОВОДНОСТЬ
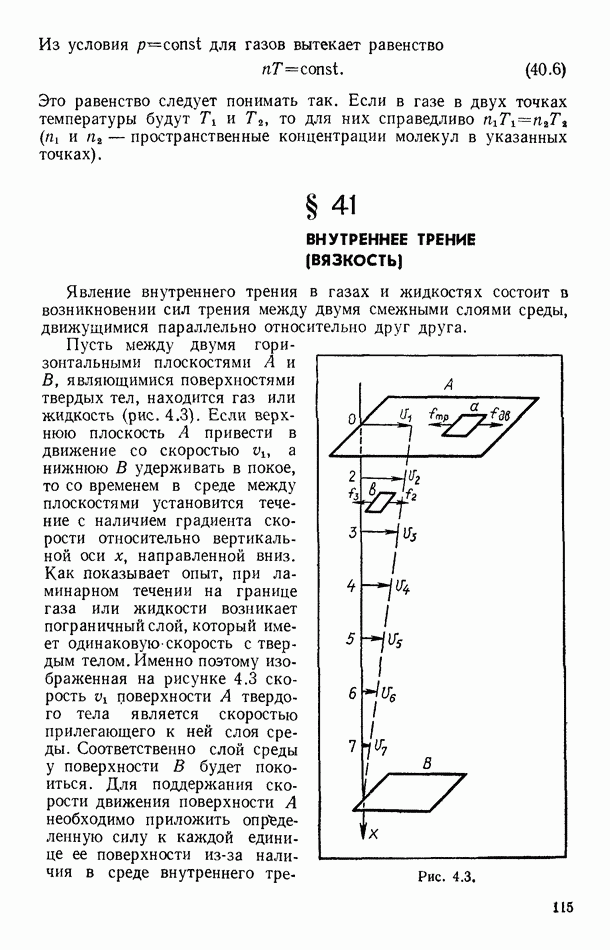
- § 41. ВНУТРЕННЕЕ ТРЕНИЕ (ВЯЗКОСТЬ)
- § 42. ДИФФУЗИЯ
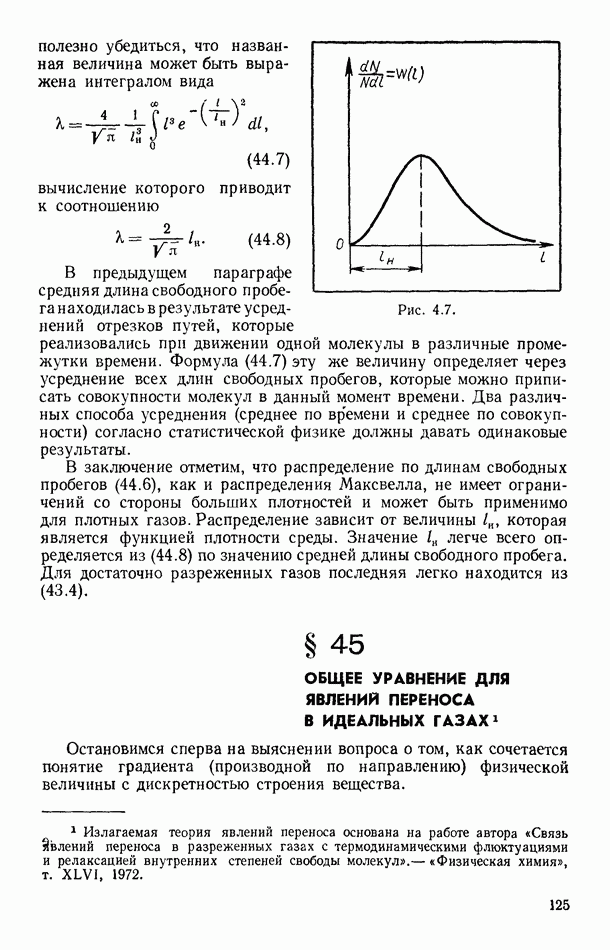
- § 43. СРЕДНЯЯ ДЛИНА СВОБОДНОГО ПРОБЕГА МОЛЕКУЛ
- § 44. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ПО ДЛИНАМ ИХ СВОБОДНЫХ ПРОБЕГОВ
- § 45. ОБЩЕЕ УРАВНЕНИЕ ДЛЯ ЯВЛЕНИИ ПЕРЕНОСА В ИДЕАЛЬНЫХ ГАЗАХ
- § 46. ДИФФУЗИЯ В ИДЕАЛЬНЫХ ГАЗАХ
- § 47. ВНУТРЕННЕЕ ТРЕНИЕ В ИДЕАЛЬНЫХ ГАЗАХ
- § 48. ТЕПЛОПРОВОДНОСТЬ ИДЕАЛЬНЫХ ГАЗОВ
- § 49. СВЯЗЬ МЕЖДУ КОЭФФИЦИЕНТАМИ ПЕРЕНОСА
- Глава V. СИЛЬНО РАЗРЕЖЕННЫЕ ГАЗЫ
- § 50. ПОЛУЧЕНИЕ И ИЗМЕРЕНИЕ ВАКУУМА
- § 51. СИЛЫ ТРЕНИЯ в ВАКУУМЕ
- § 52. ТЕПЛОПЕРЕДАЧА В ВАКУУМЕ
- § 53. ДИФФУЗИЯ В ВАКУУМЕ
- Глава VI. РЕАЛЬНЫЕ ГАЗЫ
- § 54. ОТКЛОНЕНИЕ ОТ ЗАКОНА БОЙЛЯ—МАРИОТТА
- § 55. РАВНОВЕСИЕ СИСТЕМЫ ЖИДКОСТЬ — ПАР
- § 56. ЭКСПЕРИМЕНТАЛЬНЫЕ ИЗОТЕРМЫ. КРИТИЧЕСКОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- § 57. ПОТЕНЦИАЛ ПАРНОГО ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ
- § 58. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- § 59. ИЗОТЕРМЫ ВАН-ДЕР-ВААЛЬСА. КРИТИЧЕСКИЕ ПАРАМЕТРЫ И ПОСТОЯННЫЕ ВАН-ДЕР-ВААЛЬСА
- § 60. ВНУТРЕННЯЯ ЭНЕРГИЯ РЕАЛЬНОГО ГАЗА. ЭФФЕКТ ДЖОУЛЯ — ТОМСОНА
- § 61. СЖИЖЕНИЕ ГАЗОВ
- § 62. УРАВНЕНИЕ СОСТОЯНИЯ РЕАЛЬНЫХ ГАЗОВ В ВИРИАЛЬНОЙ ФОРМЕ
- Глава VII. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- § 63. РАВНОВЕСНЫЕ И НЕРАВНОВЕСНЫЕ ПРОЦЕССЫ
- § 64. ОБРАТИМЫЕ И НЕОБРАТИМЫЕ ПРОЦЕССЫ
- § 65. ЦИКЛИЧЕСКИЕ (КРУГОВЫЕ) ПРОЦЕССЫ
- § 66. ЦИКЛ КАРНО
- § 67. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ ДЛЯ ОБРАТИМЫХ ПРОЦЕССОВ
- § 68. ЭНТРОПИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ СИСТЕМЫ
- § 69. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ ДЛЯ НЕОБРАТИМЫХ ПРОЦЕССОВ
- § 70. НЕРАВЕНСТВО КЛАУЗИУСА. ПРИНЦИП ВОЗРАСТАНИЯ ЭНТРОПИИ
- § 71. ЭНТРОПИЯ И ВЕРОЯТНОСТЬ СОСТОЯНИЯ СИСТЕМЫ
- § 72. О ТАК НАЗЫВАЕМОЙ «ТЕПЛОВОЙ СМЕРТИ ВСЕЛЕННОЙ»
- § 73. ИЗОЭНТРОПИЧЕСКОЕ СОСТОЯНИЕ ТРОПОСФЕРЫ ЗЕМЛИ
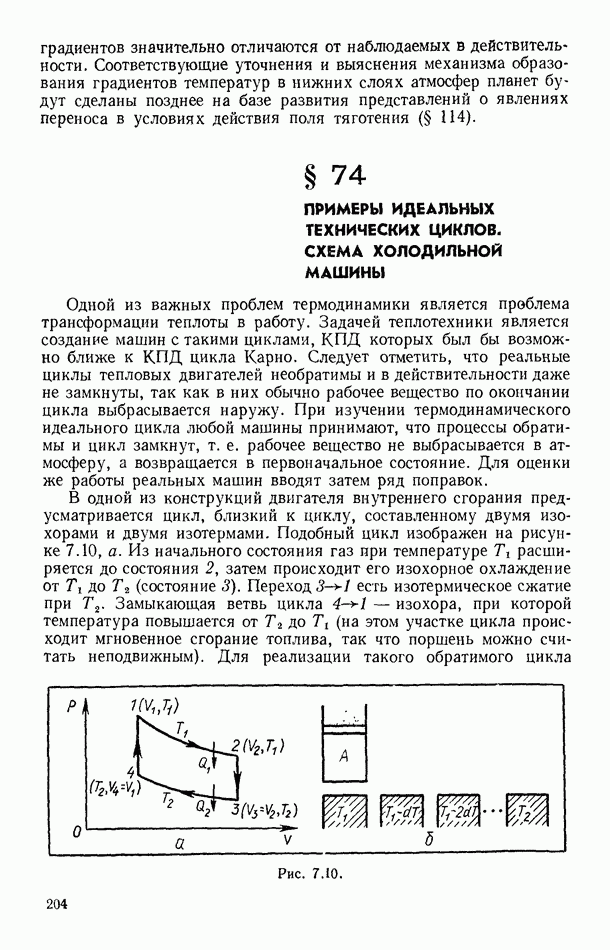
- § 74. ПРИМЕРЫ ИДЕАЛЬНЫХ ТЕХНИЧЕСКИХ ЦИКЛОВ. СХЕМА ХОЛОДИЛЬНОЙ МАШИНЫ
- Глава VIII. ЖИДКОСТИ
- § 75. ТЕПЛОВОЕ ДВИЖЕНИЕ И СТРУКТУРА ЖИДКОСТЕЙ
- § 76. ОСНОВНЫЕ СВОЙСТВА ЖИДКОСТЕЙ
- § 77. ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ ЖИДКОСТЕЙ
- § 78. МОЛЕКУЛЯРНОЕ ДАВЛЕНИЕ ПОВЕРХНОСТНОГО СЛОЯ ЖИДКОСТИ
- § 79. СИЛЫ, ВОЗНИКАЮЩИЕ НА КРИВОЙ ПОВЕРХНОСТИ ЖИДКОСТЕЙ
- § 80. КРАЕВОЙ УГОЛ. КАПИЛЛЯРНЫЕ ЯВЛЕНИЯ
- § 81. КИПЕНИЕ ЖИДКОСТЕЙ
- § 82. ТЕПЛОТА ПАРООБРАЗОВАНИЯ ЖИДКОСТЕЙ
- § 83. УРАВНЕНИЕ КЛАПЕЙРОНА — КЛАУЗИУСА
- § 84. ВЯЗКОСТЬ ЖИДКОСТЕЙ
- § 85. ЖИДКИЕ РАСТВОРЫ. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ. ЗАКОН РАУЛЯ
- § 86. ЖИДКИЙ ГЕЛИЙ. СВЕРХТЕКУЧЕСТЬ
- Глава IX. ТВЕРДЫЕ ТЕЛА
- § 87. ОСНОВНЫЕ ОСОБЕННОСТИ ТВЕРДЫХ ТЕЛ
- § 88. СТРУКТУРА КРИСТАЛЛОВ
- § 89. ФИЗИЧЕСКИЕ ТИПЫ КРИСТАЛЛИЧЕСКИХ РЕШЕТОК
- § 90. ТЕПЛОВОЕ ДВИЖЕНИЕ В КРИСТАЛЛАХ
- § 91. МЕХАНИЧЕСКИЕ СВОЙСТВА КРИСТАЛЛОВ
- § 92. ДЕФЕКТЫ В ТВЕРДЫХ ТЕЛАХ
- § 93. ТЕПЛОВОЕ РАСШИРЕНИЕ ТВЕРДЫХ ТЕЛ
- § 94. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ
- § 95. ПЛАВЛЕНИЕ И КРИСТАЛЛИЗАЦИЯ
- § 96. ДИАГРАММЫ СОСТОЯНИЙ. ТРОЙНАЯ ТОЧКА
- § 97. ТЕПЛОТА ПЛАВЛЕНИЯ ПРОСТЫХ КРИСТАЛЛИЧЕСКИХ СТРУКТУР
- Глава X. ПОЛИМЕРЫ
- § 98. ОБЩИЕ ПРЕДСТАВЛЕНИЯ
- § 99. ПОЛУЧЕНИЕ ПОЛИМЕРОВ
- § 100. НЕКОТОРЫЕ ТИПЫ ПОЛИМЕРОВ. РОЛЬ МЕЖМОЛЕКУЛЯРНЫХ ВЗАИМОДЕЙСТВИЙ
- § 101. ТРИ СОСТОЯНИЯ АМОРФНЫХ ПОЛИМЕРОВ И ТЕПЛОВОЕ ДВИЖЕНИЕ В НИХ
- § 102. ЭЛАСТИЧНОСТЬ ПОЛИМЕРОВ
- § 103. КРИСТАЛЛИЧЕСКИЕ ПОЛИМЕРЫ
- § 104. ПРИМЕНЕНИЕ ПОЛИМЕРНЫХ МАТЕРИАЛОВ
- Глава XI. ЭЛЕМЕНТЫ ТЕРМОДИНАМИКИ ТЕКУЧИХ СРЕД И РАКЕТНОЙ ТЕХНИКИ
- § 105. РАБОТА ПЕРЕМЕЩЕНИЯ В ТЕКУЧИХ СРЕДАХ
- § 106. ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИ ДЛЯ ПОТОКОВ ГАЗОВ И ЖИДКОСТЕЙ
- § 107. ЧАСТНЫЕ СЛУЧАИ ТЕЧЕНИЯ СРЕД
- § 108. ИСТЕЧЕНИЕ ГАЗОВ ИЗ СОПЕЛ. КРИТИЧЕСКАЯ СКОРОСТЬ
- § 109. ПРИНЦИП ДВИЖЕНИЯ РАКЕТ
- § 110. ЭЛЕМЕНТАРНАЯ ТЕРМОДИНАМИКА РАКЕТНОГО ДВИГАТЕЛЯ
- § 111. СХЕМЫ РАКЕТНЫХ ДВИГАТЕЛЕЙ
- § 112. МНОГОСТУПЕНЧАТЫЕ РАКЕТЫ
- § 113. ДВИЖЕНИЕ СО СВЕРХЗВУКОВОЙ СКОРОСТЬЮ. УДАРНЫЕ ВОЛНЫ
- § 114. О ГРАДИЕНТЕ ТЕМПЕРАТУРЫ В ТРОПОСФЕРЕ ЗЕМЛИ