| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 27. СРЕДНИЕ ВЕЛИЧИНЫ В ОПИСАНИИ МОЛЕКУЛЯРНЫХ СИСТЕМ
Основная задача молекулярно-кинетической теории состоит в установлении количественных связей между макроскопическими свойствами физических систем (сжимаемостью, давлением, температурой и др.) и особенностями теплового движения образующих, систему молекул.
Механическое описание отдельно взятого тела как целого сводится к установлению зависимости его движения от действия внешних сил. В молекулярной же физике рассматривают явления, связанные с движением и взаимодействием колоссального числа частиц. Так, при нормальных условиях в  газа содержится приблизительно
газа содержится приблизительно  молекул. Каждая из них испытывает около миллиарда столкновений в секунду с другими молекулами. При столкновениях меняются скорости молекул (по величине и направлению), траектории молекул представляют собой сложные ломаные линии. Предугадать траектории и скорости всех отдельно взятых молекул практически невозможно, да в этом и нет необходимости. Дело в том, что свойства систем, обусловленные взаимодействием и движением огромного числа частиц, нельзя описать механически: в системах с большим числом частиц возникают новые качества и новые свойства, которые чужды механике. Так, например, движения одной молекулы в пространстве описываются полностью в терминах и понятиях механики. Но если взять систему из множества частиц, то она уже требует для своего описания таких понятий и представлений, как температура и уравнение состояния, которые бессмысленно относить к отдельно взятым молекулам.
молекул. Каждая из них испытывает около миллиарда столкновений в секунду с другими молекулами. При столкновениях меняются скорости молекул (по величине и направлению), траектории молекул представляют собой сложные ломаные линии. Предугадать траектории и скорости всех отдельно взятых молекул практически невозможно, да в этом и нет необходимости. Дело в том, что свойства систем, обусловленные взаимодействием и движением огромного числа частиц, нельзя описать механически: в системах с большим числом частиц возникают новые качества и новые свойства, которые чужды механике. Так, например, движения одной молекулы в пространстве описываются полностью в терминах и понятиях механики. Но если взять систему из множества частиц, то она уже требует для своего описания таких понятий и представлений, как температура и уравнение состояния, которые бессмысленно относить к отдельно взятым молекулам.
Для решения задач молекулярной физики пользуются методами статистической физики. Статистическая физика оперирует средними значениями величин, характеризующих свойства отдельных молекул: средним размером молекул, средним расстоянием между ними и средней скоростью молекул.
В предыдущем параграфе отмечалось, что сложные молекулы имеют определенную структуру, форма многих молекул заведомо отличается от сферической. Для описания же усредненной картины столкновения частиц довольно сложные молекулы (такие, как молекулы бензола, гексана и др.) можно считать сферическими с диаметром  Дело в том, что молекулы, начиная с двухатомных, имеют, кроме поступательного движения, еще и вращательное движение
Дело в том, что молекулы, начиная с двухатомных, имеют, кроме поступательного движения, еще и вращательное движение  вращение молекул вокруг осей, проходящих через центр их масс. Наличие вращений не позволяет молекулам определенным образом ориентироваться при соударениях: при соударениях реализуются самые различные ориентации одной молекулы по отношению к другой. Диаметры молекул — это средние расстояния, на которые они сближаются при соударениях.
вращение молекул вокруг осей, проходящих через центр их масс. Наличие вращений не позволяет молекулам определенным образом ориентироваться при соударениях: при соударениях реализуются самые различные ориентации одной молекулы по отношению к другой. Диаметры молекул — это средние расстояния, на которые они сближаются при соударениях.
Если известен объем системы V и число частиц в ней  то легко найти среднее расстояние между ними. Отношение
то легко найти среднее расстояние между ними. Отношение  определяет объем, приходящийся на одну частицу. Полагая, что элементарные объемы
определяет объем, приходящийся на одну частицу. Полагая, что элементарные объемы  являются кубиками, содержащими внутри по одной молекуле, найдем среднее расстояние между частицами:
являются кубиками, содержащими внутри по одной молекуле, найдем среднее расстояние между частицами:

Плоская модель, иллюстрирующая нахождение межмолекулярных расстояний по (27.1), изображена на рисунке 3.3. На этом рисунке большой квадрат символизирует объем V, маленькие квадратики — элементарные объемы  Легко видеть, что ребра элементарных кубиков (27.1) будут определять расстояния между молекулами, если последние располагаются в центрах кубиков.
Легко видеть, что ребра элементарных кубиков (27.1) будут определять расстояния между молекулами, если последние располагаются в центрах кубиков.
Следует отметить, что величина (27.1) не определяет каких-либо действительных расстояний между любыми двумя фиксированными частицами. Так, если взять газ и разбить его объем на  элементарных объемов
элементарных объемов  то многие элементарные объемы окажутся пустыми (в данный момент), в других объемах будет по две, три и более молекул. При этом картина заполнения элементарных
то многие элементарные объемы окажутся пустыми (в данный момент), в других объемах будет по две, три и более молекул. При этом картина заполнения элементарных

Рис. 1.20.

Рис. 3.4.
объемов с течением времени будет меняться. Тем не менее величина (27.1) будет являться некоторой усредненной характеристикой распределения молекул в пространстве. Можно ставить более сложную задачу — отыскание возможного числа пустых элементарных объемов или заселенных по две или три молекулы. Такая задача позднее будет также рассмотрена (§ 39).
Из сопоставления свойств газов и жидкостей легко сделать заключение, что средние межмолекулярные расстояния в газах намного больше таких же расстояний в жидкостях, именно поэтому газы намного легче сжать, чем жидкости. В первом приближении будем полагать (а это в действительности так и есть), что молекулы жидкостей столь тесно примыкают друг к другу, что свободные промежутки между ними пренебрежительно малы. Тогда при разбиении жидкости на  элементарных кубиков величиной
элементарных кубиков величиной  в каждом кубике будет находиться только одна молекула, и при этом ее диаметр будет примерно равен ребру кубика (27.1). Таким образом, по объему жидкостей можно судить о размерах молекул:
в каждом кубике будет находиться только одна молекула, и при этом ее диаметр будет примерно равен ребру кубика (27.1). Таким образом, по объему жидкостей можно судить о размерах молекул:

Рисунок 3.4 раскрывает содержание соотношения (27.2). Следует отметить, что, несмотря на грубое усреднение, картина, соответствующая рисунку 3.4, позволяет правильно оценить размеры молекул.
Плотность воды  при комнатной температуре близка к
при комнатной температуре близка к  соответственно при мольной массе воды
соответственно при мольной массе воды  ее мольный объем равен:
ее мольный объем равен:  Так как моль вещества содержит
Так как моль вещества содержит  молекул, то согласно (27.2) диаметр молекул воды примерно равен:
молекул, то согласно (27.2) диаметр молекул воды примерно равен:

что близко к результатам других способов определения этой величины. Заметим, что молекулы обычных веществ (исключая полимеры) имеют размеры порядка  см и что при переходе вещества из газообразного состояния в жидкое размеры молекул практически сохраняются.
см и что при переходе вещества из газообразного состояния в жидкое размеры молекул практически сохраняются.
Моль любого газа при нормальных условиях  ,
,
 занимает объем
занимает объем  При таких условиях среднее расстояние между молекулами согласно
При таких условиях среднее расстояние между молекулами согласно  Полученные результаты позволяют заключить, что средние расстояния между молекулами в газах значительно превышают размеры молекул.
Полученные результаты позволяют заключить, что средние расстояния между молекулами в газах значительно превышают размеры молекул.
Выше отмечалась сложность детальной картины теплового движения. Скорости молекул могут резко различаться как по величине, так и по направлению, при этом распределение фиксированных молекул по скоростям с течением времени из-за столкновений меняется. Можно ввести среднюю скорость теплового движения молекул, которая в равновесных  условиях остается неизменной.
условиях остается неизменной.
Если известны скорости всех молекул в данный момент времени, то среднее арифметическое значение скорости или просто средняя скорость  или
или

где  скорость молекулы с порядковым номером
скорость молекулы с порядковым номером 
Кроме средней скорости, для характеристики теплового движения вводят еще среднюю квадратичную скорость молекул, квадрат которой согласно определению равен:

или

Для выяснения смысла соотношения (27.4) найдем энергию поступательного движения всех молекул. Искомая величина определяется как сумма кинетических энергий отдельных молекул системы:

где  -масса одной молекулы, или
-масса одной молекулы, или

Используя (27.4), перепишем (27.5) в виде

Таким образом, суммарная энергия поступательного движения всех молекул выражается через среднюю квадратичную скорость их теплового движения. Из (27.6) следует также, что

т. е. средняя кинетическая энергия поступательного движения молекулы  определяется через среднюю квадратичную скорость молекул.
определяется через среднюю квадратичную скорость молекул.
Для более детального усредненного описания теплового движения ансамбля частиц рассматривают три составляющие скорости каждой молекулы по трем взаимно перпендикулярным осям  Тогда для молекулы с порядковым номером
Тогда для молекулы с порядковым номером  можно записать:
можно записать:

где  составляющие скорости выбранной молекулы. Используя (27.8), перепишем (27.4):
составляющие скорости выбранной молекулы. Используя (27.8), перепишем (27.4):

Это выражение представляет собой сумму вида:

Введем обозначения

Величины  являются средними квадратичными скоростями движения молекул по осям
являются средними квадратичными скоростями движения молекул по осям  Таким образом,
Таким образом,

Отметим, что в правой части (27.11) стоят величины, которые не являются компонентами каких-либо скоростей, они характеризуют усредненное движение молекул по осям  Для теплового движения нет преимущественных направлений, поэтому средние квадратичные скорости движения молекул по любой из осей будут одинаковыми. Соответственно (27.11) можно представить в форме
Для теплового движения нет преимущественных направлений, поэтому средние квадратичные скорости движения молекул по любой из осей будут одинаковыми. Соответственно (27.11) можно представить в форме

Полученные результаты позволяют доказать возможность представления сложного теплового движения упорядоченным, что упрощает рассмотрение многих конкретных задач молекулярной физики. Из (27.12) и (27.6) легко получить:

Левая часть (27.13) характеризует тепловое движение относительно одной из осей прямоугольной системы координат. Согласно последнему выражению сложное тепловое движение молекул в условиях равновесия можно рассматривать как упорядоченное, при этом молекулам приписывается одна и та же скорость, равная средней квадратичной скорости, и все они движутся по трем взаимно перпендикулярным осям так, что по одной из осей (в обоих направлениях) движется третья часть всех частиц.
Как показывает исследование диффузии и броуновского движения, средние скорости движения молекул зависят от температуры. Раскрытие этой зависимости возможно только с использованием более сложных методов статистической физики.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Глава I. ОСНОВНЫЕ ТЕРМОДИНАМИЧЕСКИЕ ПОНЯТИЯ И СВОЙСТВА ИДЕАЛЬНЫХ ГАЗОВ
- § 1 О ДВУХ МЕТОДАХ ИССЛЕДОВАНИЯ ФИЗИЧЕСКИХ ЯВЛЕНИЙ
- § 2. ОСНОВНЫЕ ПОНЯТИЯ И ПРЕДСТАВЛЕНИЯ ТЕРМОДИНАМИЧЕСКОГО ОПИСАНИЯ СИСТЕМ
- § 3 ТЕРМИЧЕСКОЕ УРАВНЕНИЕ СОСТОЯНИЯ. РАВНОВЕСНЫЕ ПРОЦЕССЫ
- § 4. ИЗОПРОЦЕССЫ
- § 5. МЕЖДУНАРОДНАЯ ПРАКТИЧЕСКАЯ ТЕМПЕРАТУРНАЯ ШКАЛА
- § 6. МЕТОДЫ ИЗМЕРЕНИЯ ТЕМПЕРАТУРЫ
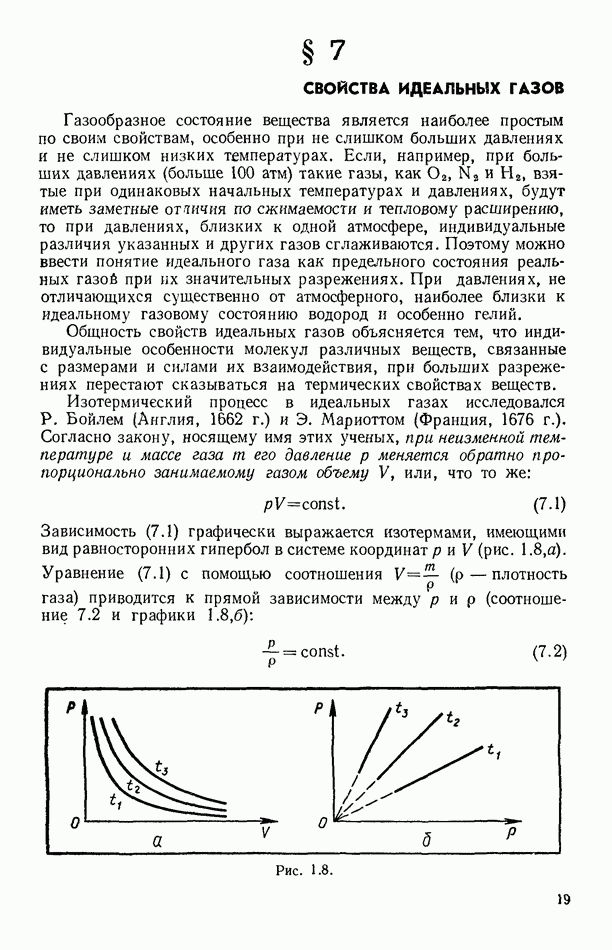
- § 7. СВОЙСТВА ИДЕАЛЬНЫХ ГАЗОВ
- § 8. РАБОТА РАСШИРЕНИЯ СИСТЕМЫ И ФИЗИЧЕСКИЙ СМЫСЛ УНИВЕРСАЛЬНОЙ ГАЗОВОЙ ПОСТОЯННОЙ
- § 9. УРАВНЕНИЕ СОСТОЯНИЯ СМЕСИ ИДЕАЛЬНЫХ ГАЗОВ
- § 10. ИЗМЕРЕНИЕ ДАВЛЕНИЙ
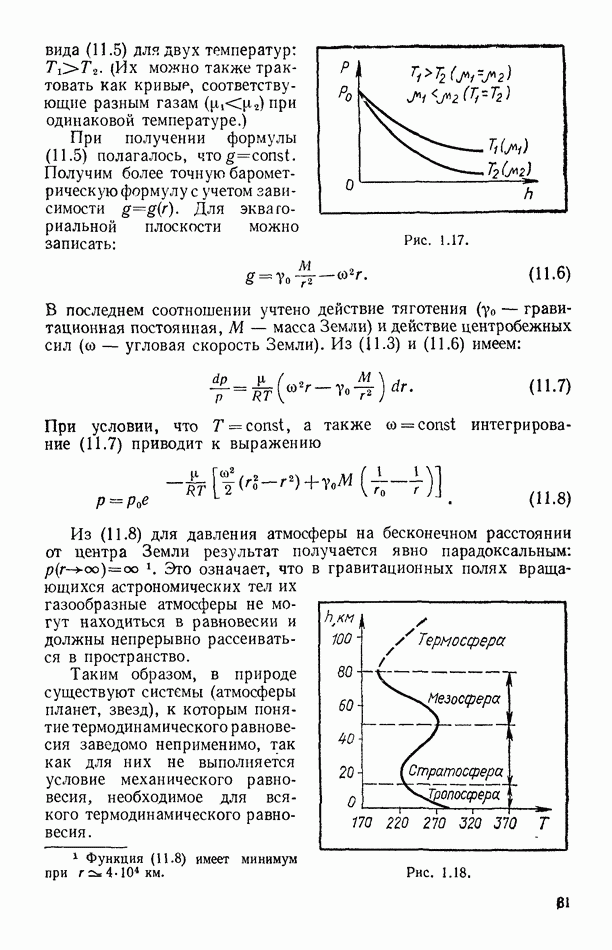
- § 11. БАРОМЕТРИЧЕСКАЯ ФОРМУЛА
- Глава II. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- § 12. О ЗАКОНЕ СОХРАНЕНИЯ И ПРЕВРАЩЕНИЯ ЭНЕРГИИ
- § 13. РАБОТА КАК МАКРОСКОПИЧЕСКИЙ СПОСОБ ПЕРЕДАЧИ ЭНЕРГИИ
- § 14. ТЕПЛОТА КАК МИКРОФИЗИЧЕСКИЙ СПОСОБ ПЕРЕДАЧИ ЭНЕРГИИ. ТЕПЛОЕМКОСТЬ
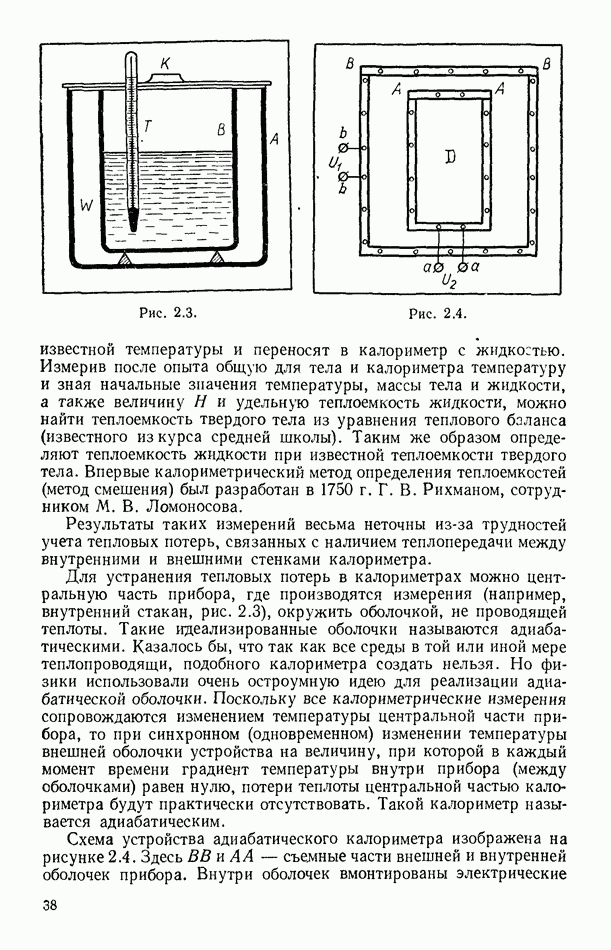
- § 15. ИЗМЕРЕНИЕ ТЕПЛОЕМКОСТИ
- § 16. ВНУТРЕННЯЯ ЭНЕРГИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ СИСТЕМЫ
- § 17. ФОРМУЛИРОВКА ПЕРВОГО НАЧАЛА ТЕРМОДИНАМИКИ
- § 18. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ ДЛЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 19. ИЗОБАРИЧЕСКИЙ ПРОЦЕСС В ИДЕАЛЬНОМ ГАЗЕ
- § 20. ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС В ИДЕАЛЬНОМ ГАЗЕ
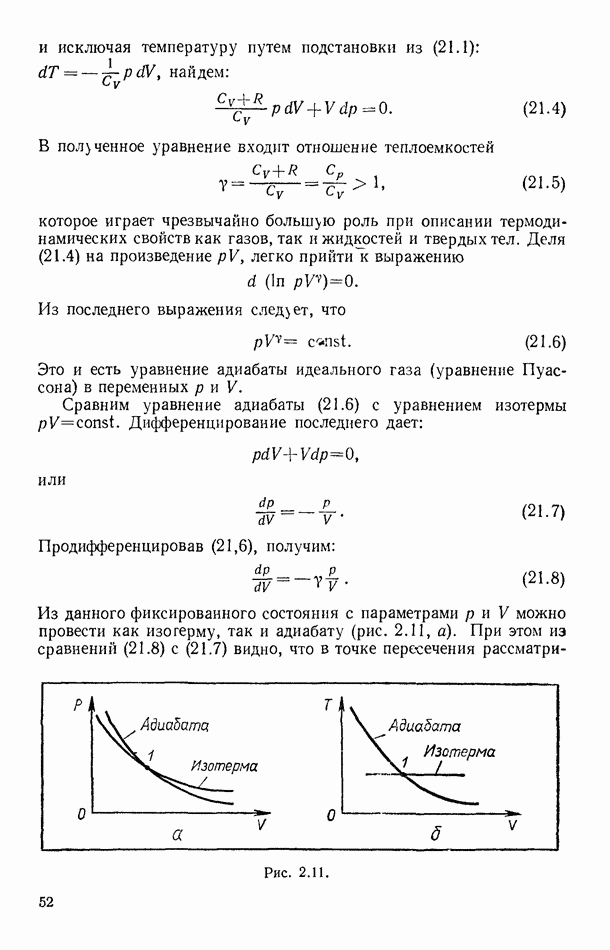
- § 21. АДИАБАТИЧЕСКИЙ ПРОЦЕСС В ИДЕАЛЬНОМ ГАЗЕ
- § 22. ПОЛИТРОПИЧЕСКИЕ ПРОЦЕССЫ В ИДЕАЛЬНОМ ГАЗЕ
- § 23. ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ ТЕПЛОЕМКОСТЕЙ Cp/Cv
- § 24. ТЕПЛОЕМКОСТЬ СМЕСИ ГАЗОВ
- § 18. ЭНТАЛЬПИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ СИСТЕМЫ
- Глава III. МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ И ЕЕ ПРИМЕНЕНИЕ К ИДЕАЛЬНЫМ ГАЗАМ
- § 26. ИСХОДНЫЕ ПОЛОЖЕНИЯ МОЛЕКУЛЯРНОЙ ТЕОРИИ
- § 27. СРЕДНИЕ ВЕЛИЧИНЫ В ОПИСАНИИ МОЛЕКУЛЯРНЫХ СИСТЕМ
- § 28. ОСНОВНЫЕ ПОНЯТИЯ ТЕОРИИ ВЕРОЯТНОСТЕЙ
- § 29. РАСПРЕДЕЛЕНИЕ ЧАСТИЦ ПО ЭНЕРГИЯМ (РАСПРЕДЕЛЕНИЕ БОЛЬЦМАНА)
- § 30. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ПО КОМПОНЕНТАМ СКОРОСТЕЙ ИХ ТЕПЛОВОГО ДВИЖЕНИЯ (РАСПРЕДЕЛЕНИЕ МАКСВЕЛЛА)
- § 31. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ПО СКОРОСТЯМ ИХ ТЕПЛОВОГО ДВИЖЕНИЯ (РАСПРЕДЕЛЕНИЕ МАКСВЕЛЛА)
- § 32. ОПЫТНАЯ ПРОВЕРКА РАСПРЕДЕЛЕНИЯ МАКСВЕЛЛА
- § 33. УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА ПО КИНЕТИЧЕСКОЙ ТЕОРИИ
- § 34. ПЛОТНОСТЬ ПОТОКА МОЛЕКУЛ В ИДЕАЛЬНОМ ГАЗЕ
- § 35. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ИДЕАЛЬНОГО ГАЗА В ПОЛВ СИЛЫ ТЯЖЕСТИ
- § 36. БРОУНОВСКОЕ ДВИЖЕНИЕ. ОПРЕДЕЛЕНИЕ ПЕРРЕНОМ ЧИСЛА АВОГАДРО
- § 37. ТЕОРЕМА О РАВНОРАСПРЕДЕЛЕНИИ И ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 38. КВАНТОВАЯ ТЕОРИЯ ТЕПЛОЕМКОСТИ ГАЗОВ
- § 39. ТЕРМОДИНАМИЧЕСКАЯ ВЕРОЯТНОСТЬ И РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ИДЕАЛЬНОГО ГАЗА В ПРОСТРАНСТВЕ
- Глава IV. ЯВЛЕНИЯ ПЕРЕНОСА И ИХ ТЕОРИЯ ДЛЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 40. ТЕПЛОПРОВОДНОСТЬ
- § 41. ВНУТРЕННЕЕ ТРЕНИЕ (ВЯЗКОСТЬ)
- § 42. ДИФФУЗИЯ
- § 43. СРЕДНЯЯ ДЛИНА СВОБОДНОГО ПРОБЕГА МОЛЕКУЛ
- § 44. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ПО ДЛИНАМ ИХ СВОБОДНЫХ ПРОБЕГОВ
- § 45. ОБЩЕЕ УРАВНЕНИЕ ДЛЯ ЯВЛЕНИИ ПЕРЕНОСА В ИДЕАЛЬНЫХ ГАЗАХ
- § 46. ДИФФУЗИЯ В ИДЕАЛЬНЫХ ГАЗАХ
- § 47. ВНУТРЕННЕЕ ТРЕНИЕ В ИДЕАЛЬНЫХ ГАЗАХ
- § 48. ТЕПЛОПРОВОДНОСТЬ ИДЕАЛЬНЫХ ГАЗОВ
- § 49. СВЯЗЬ МЕЖДУ КОЭФФИЦИЕНТАМИ ПЕРЕНОСА
- Глава V. СИЛЬНО РАЗРЕЖЕННЫЕ ГАЗЫ
- § 50. ПОЛУЧЕНИЕ И ИЗМЕРЕНИЕ ВАКУУМА
- § 51. СИЛЫ ТРЕНИЯ в ВАКУУМЕ
- § 52. ТЕПЛОПЕРЕДАЧА В ВАКУУМЕ
- § 53. ДИФФУЗИЯ В ВАКУУМЕ
- Глава VI. РЕАЛЬНЫЕ ГАЗЫ
- § 54. ОТКЛОНЕНИЕ ОТ ЗАКОНА БОЙЛЯ—МАРИОТТА
- § 55. РАВНОВЕСИЕ СИСТЕМЫ ЖИДКОСТЬ — ПАР
- § 56. ЭКСПЕРИМЕНТАЛЬНЫЕ ИЗОТЕРМЫ. КРИТИЧЕСКОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- § 57. ПОТЕНЦИАЛ ПАРНОГО ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ
- § 58. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- § 59. ИЗОТЕРМЫ ВАН-ДЕР-ВААЛЬСА. КРИТИЧЕСКИЕ ПАРАМЕТРЫ И ПОСТОЯННЫЕ ВАН-ДЕР-ВААЛЬСА
- § 60. ВНУТРЕННЯЯ ЭНЕРГИЯ РЕАЛЬНОГО ГАЗА. ЭФФЕКТ ДЖОУЛЯ — ТОМСОНА
- § 61. СЖИЖЕНИЕ ГАЗОВ
- § 62. УРАВНЕНИЕ СОСТОЯНИЯ РЕАЛЬНЫХ ГАЗОВ В ВИРИАЛЬНОЙ ФОРМЕ
- Глава VII. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- § 63. РАВНОВЕСНЫЕ И НЕРАВНОВЕСНЫЕ ПРОЦЕССЫ
- § 64. ОБРАТИМЫЕ И НЕОБРАТИМЫЕ ПРОЦЕССЫ
- § 65. ЦИКЛИЧЕСКИЕ (КРУГОВЫЕ) ПРОЦЕССЫ
- § 66. ЦИКЛ КАРНО
- § 67. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ ДЛЯ ОБРАТИМЫХ ПРОЦЕССОВ
- § 68. ЭНТРОПИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ СИСТЕМЫ
- § 69. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ ДЛЯ НЕОБРАТИМЫХ ПРОЦЕССОВ
- § 70. НЕРАВЕНСТВО КЛАУЗИУСА. ПРИНЦИП ВОЗРАСТАНИЯ ЭНТРОПИИ
- § 71. ЭНТРОПИЯ И ВЕРОЯТНОСТЬ СОСТОЯНИЯ СИСТЕМЫ
- § 72. О ТАК НАЗЫВАЕМОЙ «ТЕПЛОВОЙ СМЕРТИ ВСЕЛЕННОЙ»
- § 73. ИЗОЭНТРОПИЧЕСКОЕ СОСТОЯНИЕ ТРОПОСФЕРЫ ЗЕМЛИ
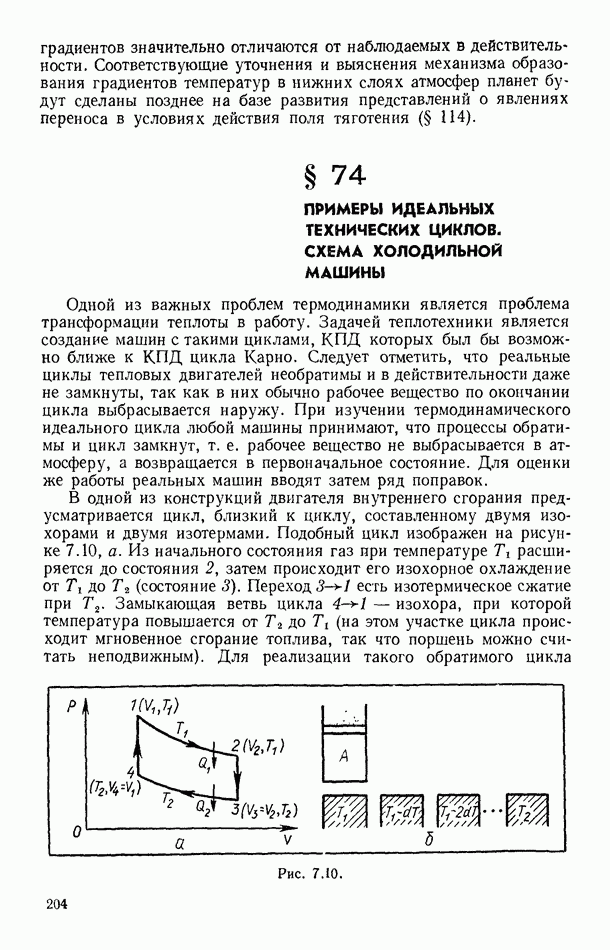
- § 74. ПРИМЕРЫ ИДЕАЛЬНЫХ ТЕХНИЧЕСКИХ ЦИКЛОВ. СХЕМА ХОЛОДИЛЬНОЙ МАШИНЫ
- Глава VIII. ЖИДКОСТИ
- § 75. ТЕПЛОВОЕ ДВИЖЕНИЕ И СТРУКТУРА ЖИДКОСТЕЙ
- § 76. ОСНОВНЫЕ СВОЙСТВА ЖИДКОСТЕЙ
- § 77. ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ ЖИДКОСТЕЙ
- § 78. МОЛЕКУЛЯРНОЕ ДАВЛЕНИЕ ПОВЕРХНОСТНОГО СЛОЯ ЖИДКОСТИ
- § 79. СИЛЫ, ВОЗНИКАЮЩИЕ НА КРИВОЙ ПОВЕРХНОСТИ ЖИДКОСТЕЙ
- § 80. КРАЕВОЙ УГОЛ. КАПИЛЛЯРНЫЕ ЯВЛЕНИЯ
- § 81. КИПЕНИЕ ЖИДКОСТЕЙ
- § 82. ТЕПЛОТА ПАРООБРАЗОВАНИЯ ЖИДКОСТЕЙ
- § 83. УРАВНЕНИЕ КЛАПЕЙРОНА — КЛАУЗИУСА
- § 84. ВЯЗКОСТЬ ЖИДКОСТЕЙ
- § 85. ЖИДКИЕ РАСТВОРЫ. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ. ЗАКОН РАУЛЯ
- § 86. ЖИДКИЙ ГЕЛИЙ. СВЕРХТЕКУЧЕСТЬ
- Глава IX. ТВЕРДЫЕ ТЕЛА
- § 87. ОСНОВНЫЕ ОСОБЕННОСТИ ТВЕРДЫХ ТЕЛ
- § 88. СТРУКТУРА КРИСТАЛЛОВ
- § 89. ФИЗИЧЕСКИЕ ТИПЫ КРИСТАЛЛИЧЕСКИХ РЕШЕТОК
- § 90. ТЕПЛОВОЕ ДВИЖЕНИЕ В КРИСТАЛЛАХ
- § 91. МЕХАНИЧЕСКИЕ СВОЙСТВА КРИСТАЛЛОВ
- § 92. ДЕФЕКТЫ В ТВЕРДЫХ ТЕЛАХ
- § 93. ТЕПЛОВОЕ РАСШИРЕНИЕ ТВЕРДЫХ ТЕЛ
- § 94. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ
- § 95. ПЛАВЛЕНИЕ И КРИСТАЛЛИЗАЦИЯ
- § 96. ДИАГРАММЫ СОСТОЯНИЙ. ТРОЙНАЯ ТОЧКА
- § 97. ТЕПЛОТА ПЛАВЛЕНИЯ ПРОСТЫХ КРИСТАЛЛИЧЕСКИХ СТРУКТУР
- Глава X. ПОЛИМЕРЫ
- § 98. ОБЩИЕ ПРЕДСТАВЛЕНИЯ
- § 99. ПОЛУЧЕНИЕ ПОЛИМЕРОВ
- § 100. НЕКОТОРЫЕ ТИПЫ ПОЛИМЕРОВ. РОЛЬ МЕЖМОЛЕКУЛЯРНЫХ ВЗАИМОДЕЙСТВИЙ
- § 101. ТРИ СОСТОЯНИЯ АМОРФНЫХ ПОЛИМЕРОВ И ТЕПЛОВОЕ ДВИЖЕНИЕ В НИХ
- § 102. ЭЛАСТИЧНОСТЬ ПОЛИМЕРОВ
- § 103. КРИСТАЛЛИЧЕСКИЕ ПОЛИМЕРЫ
- § 104. ПРИМЕНЕНИЕ ПОЛИМЕРНЫХ МАТЕРИАЛОВ
- Глава XI. ЭЛЕМЕНТЫ ТЕРМОДИНАМИКИ ТЕКУЧИХ СРЕД И РАКЕТНОЙ ТЕХНИКИ
- § 105. РАБОТА ПЕРЕМЕЩЕНИЯ В ТЕКУЧИХ СРЕДАХ
- § 106. ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИ ДЛЯ ПОТОКОВ ГАЗОВ И ЖИДКОСТЕЙ
- § 107. ЧАСТНЫЕ СЛУЧАИ ТЕЧЕНИЯ СРЕД
- § 108. ИСТЕЧЕНИЕ ГАЗОВ ИЗ СОПЕЛ. КРИТИЧЕСКАЯ СКОРОСТЬ
- § 109. ПРИНЦИП ДВИЖЕНИЯ РАКЕТ
- § 110. ЭЛЕМЕНТАРНАЯ ТЕРМОДИНАМИКА РАКЕТНОГО ДВИГАТЕЛЯ
- § 111. СХЕМЫ РАКЕТНЫХ ДВИГАТЕЛЕЙ
- § 112. МНОГОСТУПЕНЧАТЫЕ РАКЕТЫ
- § 113. ДВИЖЕНИЕ СО СВЕРХЗВУКОВОЙ СКОРОСТЬЮ. УДАРНЫЕ ВОЛНЫ
- § 114. О ГРАДИЕНТЕ ТЕМПЕРАТУРЫ В ТРОПОСФЕРЕ ЗЕМЛИ