| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
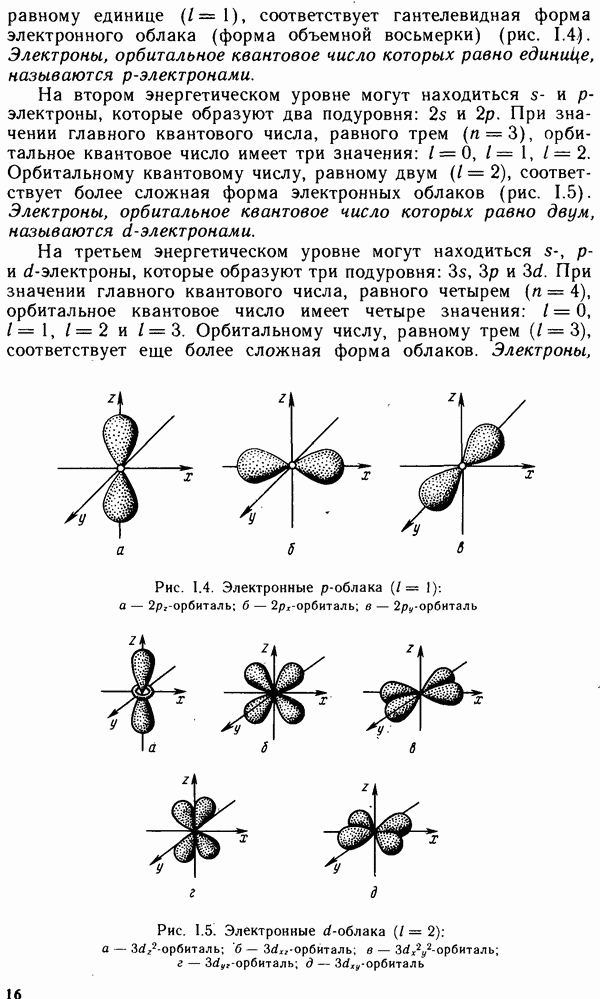
§ II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
Метод валентных связей.
В методе  предполагается, что химическая связь образуется двумя неспаренными электронами с антипараллельными спинами. При этом происходит обобществление электронов т. е. образуется электронная пара, принадлежащая двум атомам.
предполагается, что химическая связь образуется двумя неспаренными электронами с антипараллельными спинами. При этом происходит обобществление электронов т. е. образуется электронная пара, принадлежащая двум атомам.
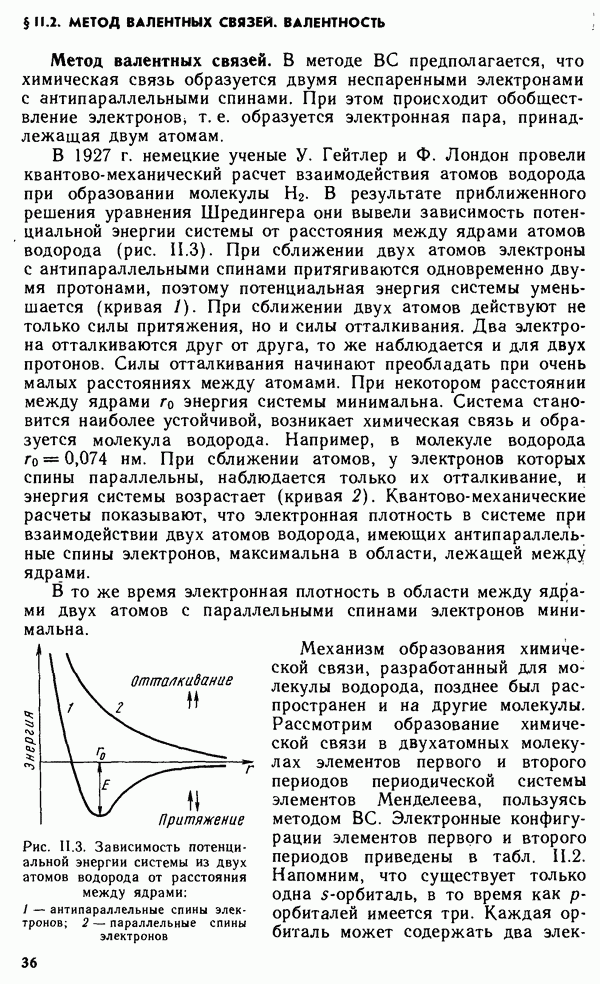
В 1927 г. немецкие ученые У. Гейтлер и Ф. Лондон провели квантово-механический расчет взаимодействия атомов водорода при образовании молекулы  . В результате приближенного решения уравнения Шредингера они вывели зависимость потенциальной энергии системы от расстояния между ядрами атомов водорода (рис. II. 3). При сближении двух атомов электроны с антипараллельными спинами притягиваются одновременно двумя протонами, поэтому потенциальная энергия системы уменьшается (кривая
. В результате приближенного решения уравнения Шредингера они вывели зависимость потенциальной энергии системы от расстояния между ядрами атомов водорода (рис. II. 3). При сближении двух атомов электроны с антипараллельными спинами притягиваются одновременно двумя протонами, поэтому потенциальная энергия системы уменьшается (кривая  При сближении двух атомов действуют не только силы притяжения, но и силы отталкивания. Два электрона отталкиваются друг от друга, то же наблюдается и для двух протонов. Силы отталкивания начинают преобладать при очень малых расстояниях между атомами. При некотором расстоянии между ядрами
При сближении двух атомов действуют не только силы притяжения, но и силы отталкивания. Два электрона отталкиваются друг от друга, то же наблюдается и для двух протонов. Силы отталкивания начинают преобладать при очень малых расстояниях между атомами. При некотором расстоянии между ядрами  энергия системы минимальна. Система становится наиболее устойчивой, возникает химическая связь и образуется молекула водорода. Например, в молекуле водорода
энергия системы минимальна. Система становится наиболее устойчивой, возникает химическая связь и образуется молекула водорода. Например, в молекуле водорода  нм. При сближении атомов, у электронов которых спины параллельны, наблюдается только их отталкивание, и энергия системы возрастает (кривая 2). Квантово-механические расчеты показывают, что электронная плотность в системе при взаимодействии двух атомов водорода, имеющих антипараллельные спины электронов, максимальна в области, лежащей между ядрами.
нм. При сближении атомов, у электронов которых спины параллельны, наблюдается только их отталкивание, и энергия системы возрастает (кривая 2). Квантово-механические расчеты показывают, что электронная плотность в системе при взаимодействии двух атомов водорода, имеющих антипараллельные спины электронов, максимальна в области, лежащей между ядрами.
В то же время электронная плотность в области между ядрами двух атомов с параллельными спинами электронов минимальна.
Механизм образования химической связи, разработанный для молекулы водорода, позднее был распространен и на другие молекулы. Рассмотрим образование химической связи в двухатомных молекулах элементов первого и второго периодов периодической системы элементов Менделеева, пользуясь методом  Электронные конфигурации элементов первого и второго периодов приведены в табл. II.2. Напомним, что существует только одна
Электронные конфигурации элементов первого и второго периодов приведены в табл. II.2. Напомним, что существует только одна  -орбиталь, в то время как
-орбиталь, в то время как  -орбиталей имеется три. Каждая орбиталь может содержать два электрона
-орбиталей имеется три. Каждая орбиталь может содержать два электрона

Рис. II.3. Зависимость потенциальной энергии системы из двух атомов водорода от расстояния между ядрами: 1 — антипараллельные спины электронов; 2 — параллельные спины электронов
Та6лица II.2. Электронные конфигурации элементов первого и второго периодов и строение двухатомных молекул согласно методу ВС (см. скан)
с антипараллельными спинами. Значит, наибольшее число неспаренных электронов в  -подуровне равно трем, как, например, у атома азота, электронная конфигурация которого
-подуровне равно трем, как, например, у атома азота, электронная конфигурация которого 
Поэтому при образовании молекулы азота обобществляются три пары электронов (тройная связь  Атом кислорода, электронная конфигурация которого
Атом кислорода, электронная конфигурация которого  должен иметь два спаренных электрона на одной из трех
должен иметь два спаренных электрона на одной из трех  -орбиталей. Таким образом, он обладает лишь двумя неспаренными электронами, которые участвуют в образовании химической связи. Вследствие этого в молекуле кислорода общими являются две пары электронов (двойная связь
-орбиталей. Таким образом, он обладает лишь двумя неспаренными электронами, которые участвуют в образовании химической связи. Вследствие этого в молекуле кислорода общими являются две пары электронов (двойная связь  ).
).
Валентность.
В учении о химической связи широко используют очень важное понятие о валентности элементов. Способность атома к образованию химических связей называют в а-лентностью элемента. Количественной мерой валентности принято считать число разных атомов в молекуле, с которыми данный атом образует связи. Согласно обменному механизму метода  валентность элементов определяется числом содержащихся в атоме неспаренных электронов. Для s- и
валентность элементов определяется числом содержащихся в атоме неспаренных электронов. Для s- и  -электронов — это электроны внешнего уровня, для d-элементов — внешнего и предвнешнего уровней.
-электронов — это электроны внешнего уровня, для d-элементов — внешнего и предвнешнего уровней.
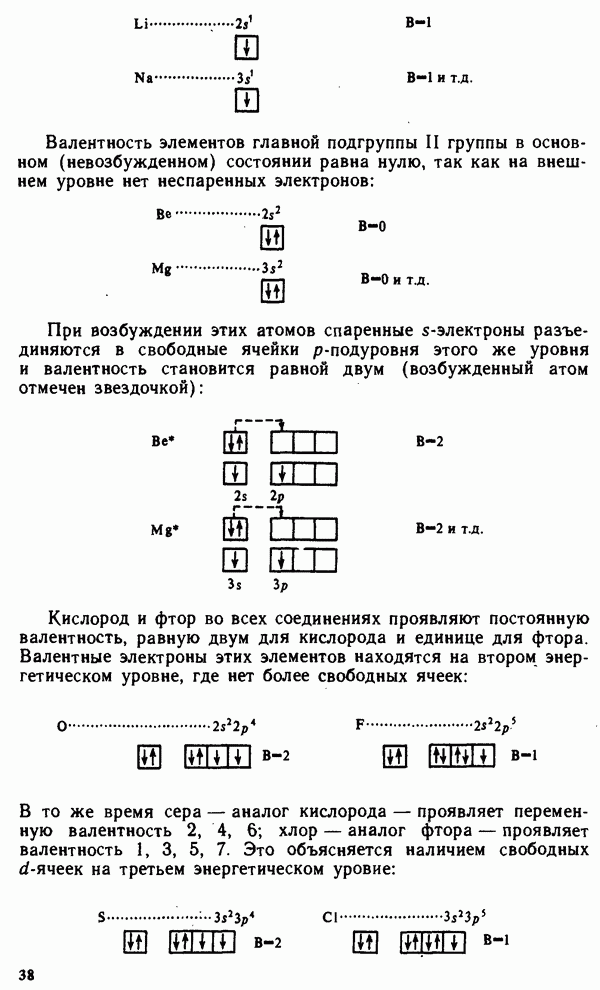
Спаренные (расположенные по два на атомных орбиталях) электроны при возбуждении могут разъединяться при наличии свободных ячеек того же уровня (разъединение электронов в какой-либо иной уровень невозможно). Например, валентность (В) элементов главной подгруппы I группы равна единице, так как на внешнем уровне атомы этих элементов имеют один электрон:

Валентность элементов главной подгруппы II группы в основном (невозбужденном) состоянии равна нулю, так как на внешнем уровне нет неспаренных электронов:

При возбуждении этих атомов спаренные  -электроны разъединяются в свободные ячейки
-электроны разъединяются в свободные ячейки  -подуровня этого же уровня и валентность становится равной двум (возбужденный атом отмечен звездочкой):
-подуровня этого же уровня и валентность становится равной двум (возбужденный атом отмечен звездочкой):

Кислород и фтор во всех соединениях проявляют постоянную валентность, равную двум для кислорода и единице для фтора. Валентные электроны этих элементов находятся на втором энергетическом уровне, где нет более свободных ячеек:

В то же время сера — аналог кислорода — проявляет переменную валентность 2, 4, 6; хлор — аналог фтора — проявляет валентность 1, 3, 5, 7. Это объясняется наличием свободных d-ячеек на третьем энергетическом уровне:

При возбуждении

Для большинства d-элементов валентность в невозбужденном состоянии равна нулю, так как на внешнем уровне нет неспаренных электронов. Например, для железа

При возбуждении атома железа  -электроны разъединяются и переходят на свободный
-электроны разъединяются и переходят на свободный  -подуровень четвертого уровня, валентность становится равной двум:
-подуровень четвертого уровня, валентность становится равной двум:

Кроме электронов внешнего уровня валентными могут быть неспаренные d-электроны предвнешнего уровня, и валентность атома железа с учетом d-электронов может быть равна 3, 4, 5 и максимально 6.
Осмий — аналог железа — может проявлять максимальную валентность, равную восьми:

При возбуждении атома осмия  -электроны разъединяются и переходят на свободный
-электроны разъединяются и переходят на свободный  -подуровень шестого уровня, валентность становится равной двум. Неспаренные d-электроны увеличивают ее до шести. Кроме того, спаренные d-электроны имеют возможность разъединяться и переходить на свободный
-подуровень шестого уровня, валентность становится равной двум. Неспаренные d-электроны увеличивают ее до шести. Кроме того, спаренные d-электроны имеют возможность разъединяться и переходить на свободный  -подуровень пятого уровня, тогда максимальная валентность атома осмия становится равной восьми:
-подуровень пятого уровня, тогда максимальная валентность атома осмия становится равной восьми:

Донорно-акцепторный механизм образования ковалентной связи.
Рассмотренный механизм возникновения ковалентных связей путем обобществления неспаренных электронов двух атомов получил название обменного механизма. Образование ковалентной связи может происходить также при взаимодействии одного атома или иона с заполненной атомной орбиталью с другим атомом или ионом, имеющим вакантную (свободную) атомную орбиталь. Такой механизм образования
ковалентной связи называется донорно-акцепторным. Атом или ион, поставляющий пару электронов, называют донором, а атом или ион, к которому эта пара электронов перемещается, — акцептором. Согласно методу  ковалентная связь по донорно-акцепторному механизму возникает при перекрывании вакантной орбитали акцептора с заполненными орбиталями донора или донорной группы. Поэтому донорная группа должна содержать по меньшей мере одну неподеленную пару электронов.
ковалентная связь по донорно-акцепторному механизму возникает при перекрывании вакантной орбитали акцептора с заполненными орбиталями донора или донорной группы. Поэтому донорная группа должна содержать по меньшей мере одну неподеленную пару электронов.
Рассмотрим образование химической связи по донорно-акцепторному механизму при взаимодействии молекулы аммиака с ионом водорода. Атом азота имеет на внешнем энергетическом уровне два спаренных b три неспаренных электрона:
[Ытттгп

В молекуле аммиака неспаренные  -электроны атома азота образуют три электронные пары с электронами атомов водорода. У атома азота остается неподеленная пара электронов
-электроны атома азота образуют три электронные пары с электронами атомов водорода. У атома азота остается неподеленная пара электронов  , т. е. два электрона с антипаралелльными спинами на одной атомной орбитали. Атомная орбиталь иона водорода не содержит электронов (вакантная орбиталь). При сближении молекулы аммиака и иона водорода происходит взаимодействие неподеленной пары электронов атома азота и вакантной орбитали иона водорода. Неподеленная пара электронов становится общей для атомов азота и водорода, возникает химическая связь по донорно-акцепторному механизму. Атом азота молекулы аммиака является донором, а ион водорода — акцептором. Обозначив неподеленную пару электронов двумя точками, вакантную орбиталь квадратом, а связи черточками, можно представить образование иона аммония следующей схемой;
, т. е. два электрона с антипаралелльными спинами на одной атомной орбитали. Атомная орбиталь иона водорода не содержит электронов (вакантная орбиталь). При сближении молекулы аммиака и иона водорода происходит взаимодействие неподеленной пары электронов атома азота и вакантной орбитали иона водорода. Неподеленная пара электронов становится общей для атомов азота и водорода, возникает химическая связь по донорно-акцепторному механизму. Атом азота молекулы аммиака является донором, а ион водорода — акцептором. Обозначив неподеленную пару электронов двумя точками, вакантную орбиталь квадратом, а связи черточками, можно представить образование иона аммония следующей схемой;

Образование химических связей по донорно-акцепторному механизму — весьма распространенное явление при химических реакциях. Рассмотрим еще пример образования такой связи при взаимодействии молекулы  с гидрид-ионом
с гидрид-ионом  В молекуле
В молекуле  имеется вакантная р-орбиталь, а у гидрид-иона — неподеленная пара электронов, поэтому молекула
имеется вакантная р-орбиталь, а у гидрид-иона — неподеленная пара электронов, поэтому молекула  служит акцептором, а ион
служит акцептором, а ион  — донором. Схему образования химической связи по донорно-акцепторному механизму при взаимодействии молекулы
— донором. Схему образования химической связи по донорно-акцепторному механизму при взаимодействии молекулы  с ионом
с ионом  можно записать в виде
можно записать в виде

Соответственно валентность элементов согласно методу  определяется как числом неспаренных электронов у атома (обменный механизм), так и числом связей, которые атом образует по донорно-акцепторному механизму. В рассмотренных выше примерах атомы азота и бора в ионах
определяется как числом неспаренных электронов у атома (обменный механизм), так и числом связей, которые атом образует по донорно-акцепторному механизму. В рассмотренных выше примерах атомы азота и бора в ионах  и
и  имеют валентность, равную четырем.
имеют валентность, равную четырем.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
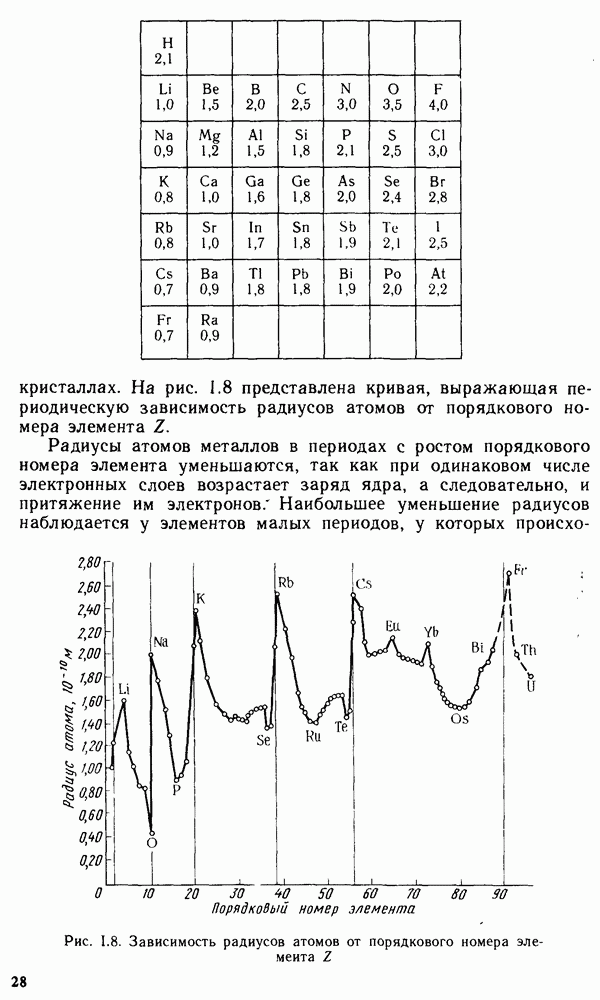
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
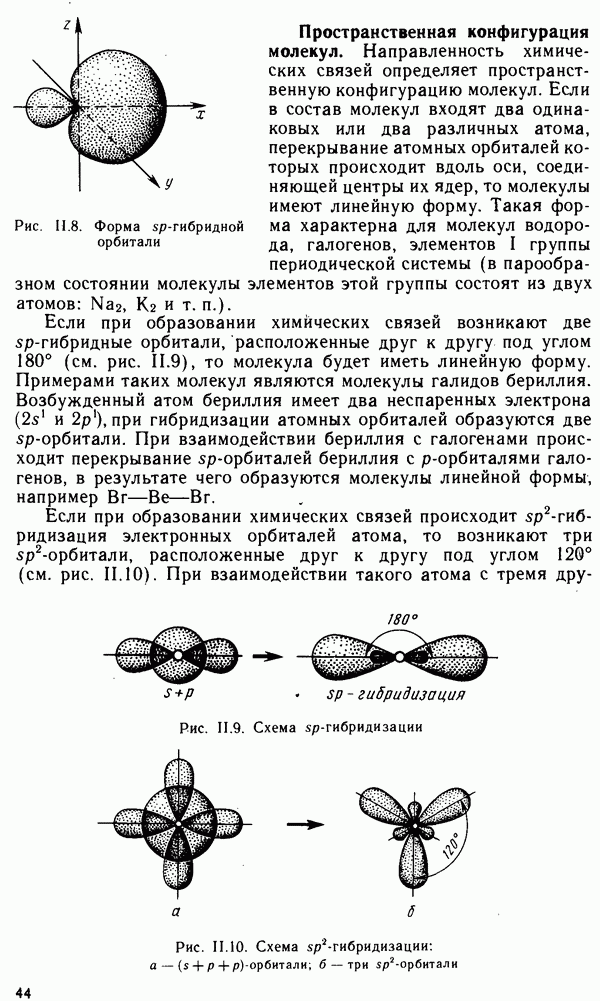
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
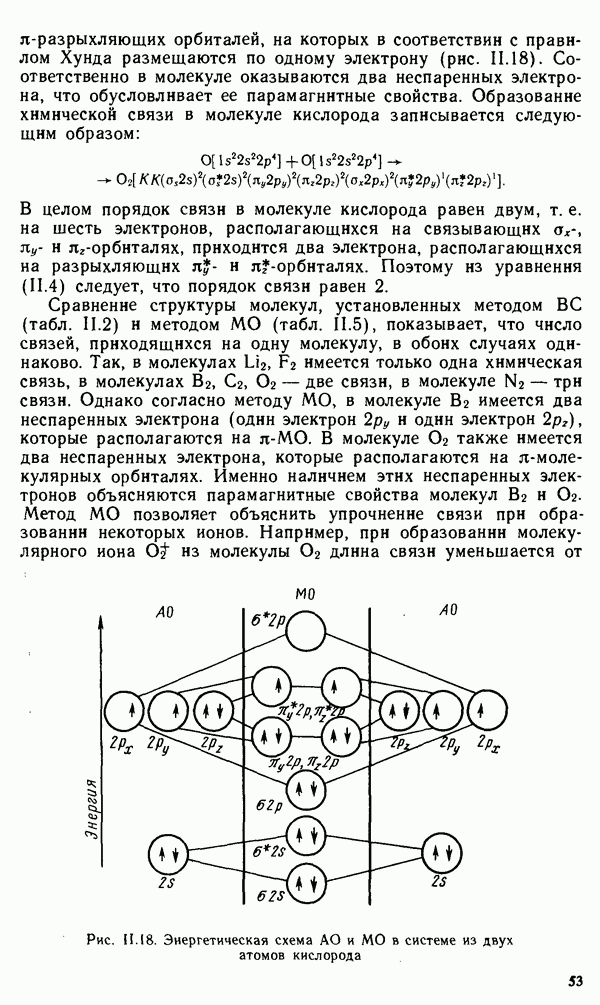
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
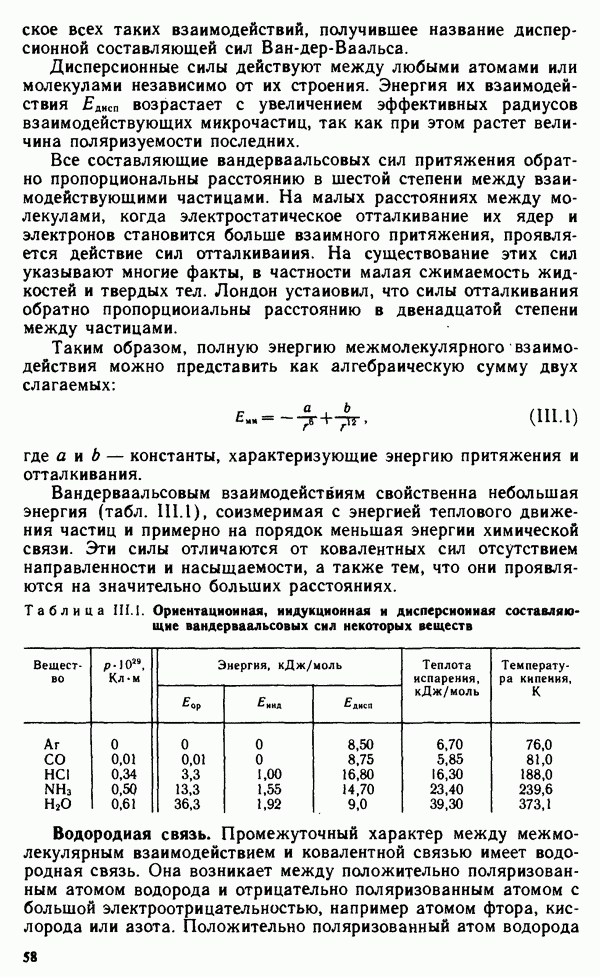
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
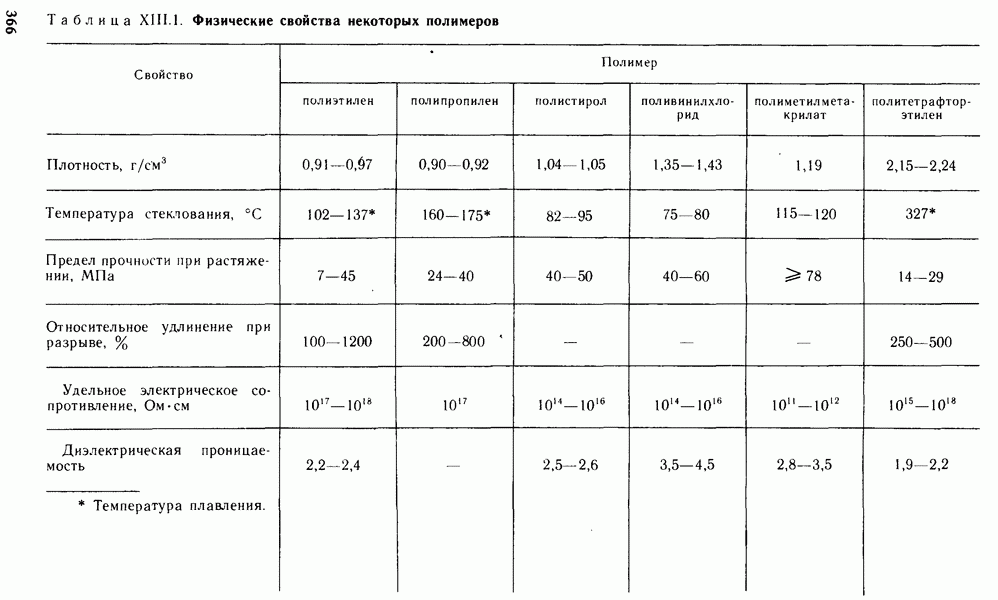
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ