| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
Гальваническими называются металлические покрытия, наносимые на поверхность какого-либо изделия методом электролиза. Гальваническим способом можно получить покрытия всеми металлами и сплавами, которые могут выделяться на катоде. Толщина покрытий в зависимости от их назначения составляет 1 —100 мкм.
Гальванические покрытия широко применяются во многих областях техники и имеют различные назначения: а) защита от коррозии: цинкование, кадмирование, лужение и др.; б) защита от коррозии и придание красивого внешнего вида (защитнодекоративные): никелирование, хромирование, серебрение и золочение; в) повышение электрической проводимости: меднение, серебрение, золочение; г) повышение твердости и износостойкости: хромирование, родирование, палладирование; д) получение магнитных пленок: осаждение сплавов никель — кобальт и железо — никель; е) улучшение отражательной способности поверхности: серебрение, родирование, палладирование, хромирование; ж) улучшение способности к пайке: лужение, осаждение сплава олово — свинец; з) уменьшение коэффициента трения: свинцевание, хромирование, осаждение сплавов олово — свинец, индий — свинец и др.
Нанесение гальванических покрытий проводится в электролизере, называемом гальванической ванной. Электролизер имеет два электрода и раствор электролита. Катодом служит изделие, на которое наносится покрытие. На катоде идет процесс восстановления находящихся в растворе электролита ионов металла (электроосаждение металла):  . Анодом обычно служит такой же металл, что и металл покрытия. Процесс на аноде противоположен процессу на катоде:
. Анодом обычно служит такой же металл, что и металл покрытия. Процесс на аноде противоположен процессу на катоде: 
Электролиз с растворимым анодом имеет большие достоинства, так как равновесные потенциалы анода и катода одинаковы и напряжение электролизера является лишь суммой поляризации и омических потерь. Кроме того, содержание ионов металла в растворе остается постоянным, так как расход ионов на катоде компенсируется поступлением их с анода.
Однако иногда применение растворимых анодов невозможно, например при хромировании, так как металлический хром очень быстро растворяется химически и раствор пересыщается солями хрома (VI). Поэтому ведут электролиз с нерастворимыми анодами, и на аноде выделяется кислород.
В состав растворов для получения гальванических покрытий кроме соли металла, осаждаемого на катоде, вводятся добавки, увеличивающие электрическую проводимость раствора, например серная кислота, сульфат натрия; активирующие анодный процесс, например хлорид натрия, а также обеспечивающие постоянное значение pH раствора (буферные добавки). Кроме того, введение некоторых добавок, называемых блескообразователями, позволяет получить на катоде металлические покрытия, не требующие механической или электрохимической полировки.
Если обрабатываемое изделие имеет сложную форму, то возникает сложная задача обеспечения равномерного осаждения металла по всей поверхности изделия, так как плотность тока на выступах, расположенных ближе к аноду, соответственно и толщина осадка металла на выступах будут больше, чем в углублениях. Для более равномерного осаждения металла используют несколько способов, в том числе повышение катодной поляризации. Так как поляризация возрастает с увеличением плотности тока, то ее величина на выступающих участках будет выше, чем в углублениях. Это вызывает перераспределение тока и соответственно толщины осадка в сторону большей равномерности. Катодную поляризацию повышают, добавляя в раствор комплексные соединения, поверхностно-активные вещества.
Для обеспечения прочного сцепления металла-покрытия с основным металлом необходимо перед нанесением покрытия удалить с поверхности основного металла загрязнения и оксиды. Это достигается обезжириванием поверхностей в органических растворителях или щелочах, травлением их в растворах кислот и тщательной промывкой в воде.
Никелирование проводят в растворах, содержащих сульфат никеля, борную кислоту и хлорид натрия. Борная кислота обеспечивает сохранение pH раствора в пределах  . В растворах с более высоким значением pH выпадает гидроксид никеля и ухудшается качество покрытия. В более кислых растворах
. В растворах с более высоким значением pH выпадает гидроксид никеля и ухудшается качество покрытия. В более кислых растворах  растет доля тока, идущая на выделение водорода на катоде, и соответственно снижается выход никеля по току. Хлорид натрия необходим для предотвращения пассивации никелевых анодов. Ионы
растет доля тока, идущая на выделение водорода на катоде, и соответственно снижается выход никеля по току. Хлорид натрия необходим для предотвращения пассивации никелевых анодов. Ионы  адсорбируются на поверхности никеля и предупреждают образование оксидных слоев. Кроме того,
адсорбируются на поверхности никеля и предупреждают образование оксидных слоев. Кроме того,
в растворы никелирования нередко вводят блескообразователь, например кумарин и  -толуолсульфамид.
-толуолсульфамид.
Меднение изделий осуществляется в сернокислотных или цианистых растворах. Первые кроме сульфата меди содержат серную кислоту, необходимую для повышения электрической проводимости раствора и предотвращения гидролиза соли меди. Достоинством меднения в сернокислотном растворе является высокая скорость процесса, поэтому такие растворы применяются в случае необходимости получения толстых покрытий. Однако потенциал меди в этих растворах положительнее потенциала железа  поэтому при погружении стальных изделий в раствор происходит контактное вытеснение меди с образованием рыхлого осадка металла:
поэтому при погружении стальных изделий в раствор происходит контактное вытеснение меди с образованием рыхлого осадка металла:

Для меднения стальных изделий необходим подслой меди, осажденный из цианистых растворов, в которых медь находится в основном в виде комплексных ионов 
Константа нестойкости комплексного иона меди очень мала  , соответственно очень мала и концентрация «свободных» ионов меди
, соответственно очень мала и концентрация «свободных» ионов меди  Электродный потенциал меди в цианистом растворе становится отрицательнее потенциала железа
Электродный потенциал меди в цианистом растворе становится отрицательнее потенциала железа  и контактное вытеснение меди из раствора не происходит, поэтому в таком растворе можно проводить меднение стальных изделий
и контактное вытеснение меди из раствора не происходит, поэтому в таком растворе можно проводить меднение стальных изделий  Кроме того, электроосаждение меди из комплексных ионов протекает с высокой поляризацией, что обеспечивает равномерное распределение металла по поверхности изделия сложной формы. В первом приближении процесс у катода можно представить уравнениями:
Кроме того, электроосаждение меди из комплексных ионов протекает с высокой поляризацией, что обеспечивает равномерное распределение металла по поверхности изделия сложной формы. В первом приближении процесс у катода можно представить уравнениями:

Цианистые растворы очень токсичны.
Цинкование проводят в основном в сульфатном или цианистом растворах. Сульфатный электролит содержит кроме сульфата цинка сульфат натрия, сульфат алюминия (буферная добавка), блескообразователь (декстрин и др.). В цианистом растворе цинк находится в виде комплексного иона  Из такого раствора удается осадить на катоде гладкие мелкокристаллические покрытия, равномерно распределенные по поверхности изделия.
Из такого раствора удается осадить на катоде гладкие мелкокристаллические покрытия, равномерно распределенные по поверхности изделия.
Хромирование проводят из раствора, содержащего оксид хрома  и серную кислоту (соотношение по массе примерно
и серную кислоту (соотношение по массе примерно  Выход по току хрома на катоде составляет
Выход по току хрома на катоде составляет  остальная доля электричества расходуется на выделение водорода.
остальная доля электричества расходуется на выделение водорода.
Анодом служит листовой свинец, устойчивый в растворе хромирования. Хромовые покрытия отличаются высокой твердостью,
износостойкостью и красивым внешним видом, поэтому, несмотря на сложность процесса хромирования, он широко применяется в различных областях техники.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
Пример 1. Рассчитайте ЭДС элемента

при 298 К и активностях ионов  равных соответственно 0,1 и
равных соответственно 0,1 и  Определите теоретически возможное количество электричества и энергии, которые можно получить в элементе, если масса кадмия
Определите теоретически возможное количество электричества и энергии, которые можно получить в элементе, если масса кадмия  а ионов меди
а ионов меди  Определите удельную энергию на единицу массы окислителя и восстановителя.
Определите удельную энергию на единицу массы окислителя и восстановителя.
Решение. В элементе протекает токообразующая реакция

ЭДС этого элемента при 298 К определяется по уравнению

Стандартна ЭДС элемента равна разности стандартных потенциалов электродов

Соответственно ЭДС элемента равна

Теоретически возможное количество электричества  которое можно получить в элементе, определяется законом Фарадея:
которое можно получить в элементе, определяется законом Фарадея:

где  — масса вещества, испытавшая превращение на электроде;
— масса вещества, испытавшая превращение на электроде;  — масса 1 моль эквивалентов этого вещества. Масса 1 моль эквивалентов кадмия равна
— масса 1 моль эквивалентов этого вещества. Масса 1 моль эквивалентов кадмия равна  меди —
меди —  Отношения массы кадмия и меди к массе эквивалентов в данном случае равны
Отношения массы кадмия и меди к массе эквивалентов в данном случае равны

тогда  .
.
Теоретическое количество энергии  которое можно получить в элементе, равно произведению количества электричества на
которое можно получить в элементе, равно произведению количества электричества на 

Удельная энергия  на единицу массы окислителя и восстановителя равна
на единицу массы окислителя и восстановителя равна

В данном случае 
Ответ: 
Пример 2. Рассчитайте толщину никелевого покрытия на изделии и изменение толщины никелевого анода при электрохимическом никелировании в течение  если плотность тока составляет на катоде
если плотность тока составляет на катоде  и на аноде
и на аноде  а выход по току на катоде равен 0,8, на аноде — 0,9. Плотность никеля
а выход по току на катоде равен 0,8, на аноде — 0,9. Плотность никеля 
Решение. Количество электричества, прошедшее через единицу поверхности электродов  равно: на катоде
равно: на катоде  на аноде —
на аноде —  По закону Фарадея на единицу поверхности катода выделилось никеля
По закону Фарадея на единицу поверхности катода выделилось никеля

где  масса 1 моль эквивалентов никеля
масса 1 моль эквивалентов никеля  выход по току никеля;
выход по току никеля;  число Фарадея,
число Фарадея, 

С единицы поверхности анода растворилось никеля

Толщина покрытия на катоде равна

Изменение толщины никелевого анода равно

Ответ: 10,7 и 5,6 мкм.
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ
(см. скан)
(см. скан)
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
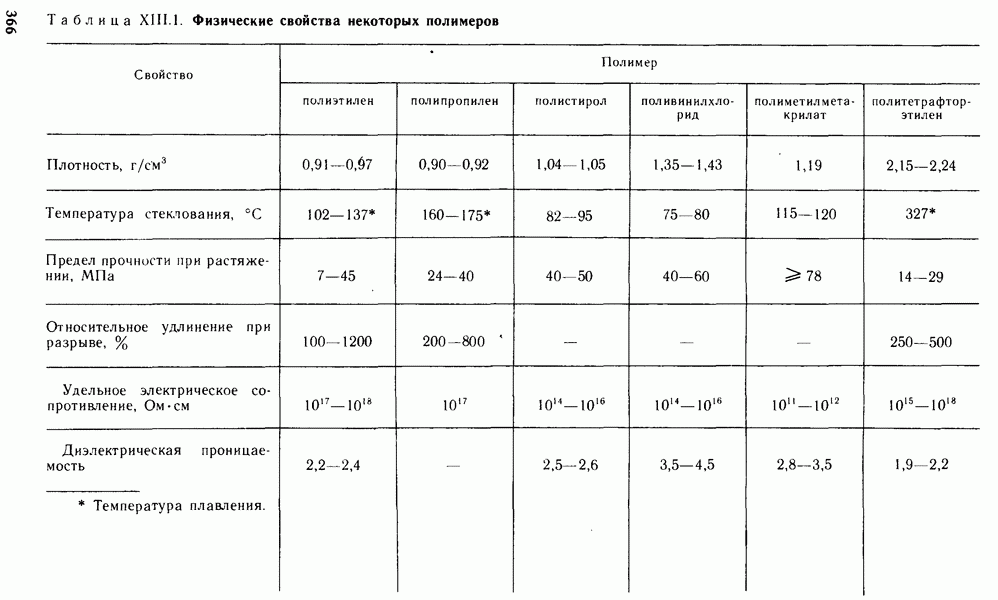
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ