| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
Номенклатура комплексных соединений.
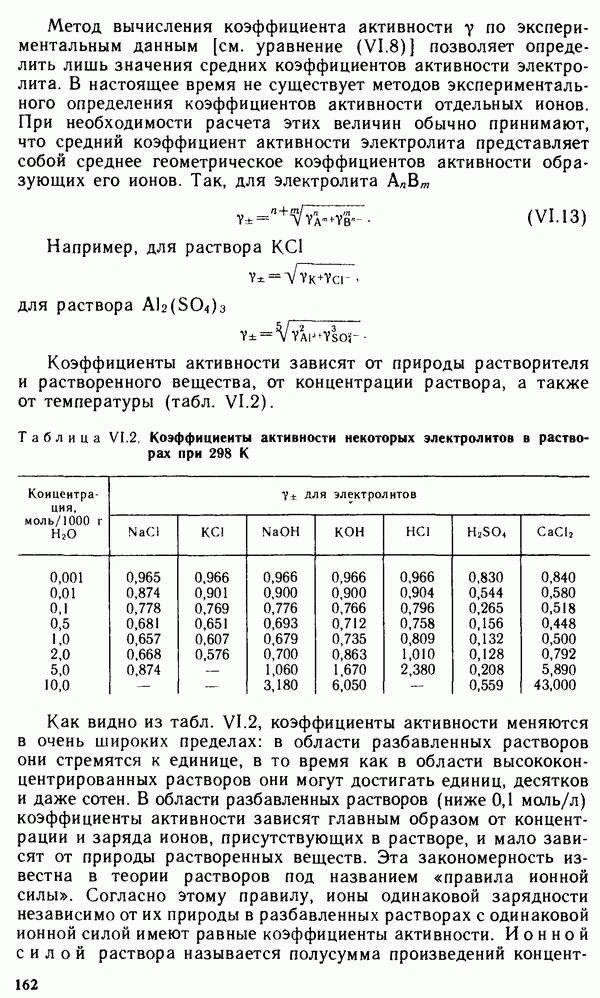
В соответствии с правилами  в названия комплексов входят названия как лигандов, так и комплексообразователей, причем вначале указываются лиганды (в алфавитном порядке), а затем комплексообразователи. К анионным лигандам добавляют окончание -о (например,
в названия комплексов входят названия как лигандов, так и комплексообразователей, причем вначале указываются лиганды (в алфавитном порядке), а затем комплексообразователи. К анионным лигандам добавляют окончание -о (например,  — карбонато;
— карбонато;  — циано;
— циано;  — азидо;
— азидо;  — гидроксо), нейтральные лиганды имеют те же названия, что и молекулы, за исключением
— гидроксо), нейтральные лиганды имеют те же названия, что и молекулы, за исключением  (акво),
(акво),  (аммин),
(аммин),  (карбонил). Названия комплексных анионов содержат суффикс -ат (например, феррат, никелат, хромат). Число лигандов в комплексе обозначают граческими приставками (ди, три, тетра, пента, гекса и т.д.). Степень окисления металла в комплексе указывается в скобках после названия комплекса. Если металл образует ион с одной степенью окисления, то она в название комплекса может не входить. Приведем некоторые примеры названий комплексных соединений:
(карбонил). Названия комплексных анионов содержат суффикс -ат (например, феррат, никелат, хромат). Число лигандов в комплексе обозначают граческими приставками (ди, три, тетра, пента, гекса и т.д.). Степень окисления металла в комплексе указывается в скобках после названия комплекса. Если металл образует ион с одной степенью окисления, то она в название комплекса может не входить. Приведем некоторые примеры названий комплексных соединений:  — дихлорид
— дихлорид

(кликните для просмотра скана)
тетрааммин цинка;  калия;
калия;  натрия;
натрия;  калия;
калия;  дихлорид пентаамминохлороко-бальта (III).
дихлорид пентаамминохлороко-бальта (III).
Комплексные соединения очень разнообразны по строению и свойствам. Системы их классификации основываются на различных принципах. Одна из соовременных систем классификации делит их на четыре класса: 1 — комплексные соединения, содержащие молекулярные монодентатные лиганды; 2 — комплексные соединения, содержащие ионные лиганды; 3 — циклические комплексные соединения; 4 — многоядерные комплексные соединения.
1. Комплексные соединения, содержащие молекулярные монодентатные лиганды.
К ним отосятся такие широко распространенные комплексные соединения, как аммиакаты, аквокомплексы, карбонилы металлов.
Аквокомплексами, или гидратами, называют комплексные соединения, в которых лигандами являются молекулы воды, например  . В водных растворах каждый ион гидратирован и представляет собой аквокомплекс преимущественно переменного состава. При кристаллизации некоторые из этих комплексов удерживают определенное число молекул воды, образуя кристаллогидраты, например
. В водных растворах каждый ион гидратирован и представляет собой аквокомплекс преимущественно переменного состава. При кристаллизации некоторые из этих комплексов удерживают определенное число молекул воды, образуя кристаллогидраты, например 
Аммиакатами называют комплексные соединения, в которых лигандами являются молекулы аммиака, например 
Карбонилами металлов называют комплексные соединения, в которых лигандами служат молекулы оксида углерода, например 
2. Комплексные соединения, содержащие ионные лиганды.
Такие комплексные соединения могут содержать в качестве лигандов анионы каких-либо кислот. Их называют ацидокомплексами. В качестве лигандов в ацидокомплексах могут быть следующие анионы:  и др. К ацидокомплексам относятся также соединения, называемые двойными солями, например
и др. К ацидокомплексам относятся также соединения, называемые двойными солями, например  Двойные соли можно рассматривать как соединения, в узлах кристаллических решеток которых находятся одинаковые анионы, но разные катионы. Химические связи в этих соединениях носят преимущественно ионный характер и поэтому в водных растворах они распадаются на отдельные ионы.
Двойные соли можно рассматривать как соединения, в узлах кристаллических решеток которых находятся одинаковые анионы, но разные катионы. Химические связи в этих соединениях носят преимущественно ионный характер и поэтому в водных растворах они распадаются на отдельные ионы.
К числу ионных лигандов относится также и гидроксид-ион  (гидроксокомплексы).
(гидроксокомплексы).
3. Циклические комплексные соединения.
К наиболее важным циклическим комплексным соединениям относятся хелаты или клешнеобразные соединения, в которых центральный атом и полидентатный лиганд образуют цикл. Например, в реакции
гидроксида меди (II) с аминоуксусной кислотой образуется нейтральный комплекс — глицинат меди:

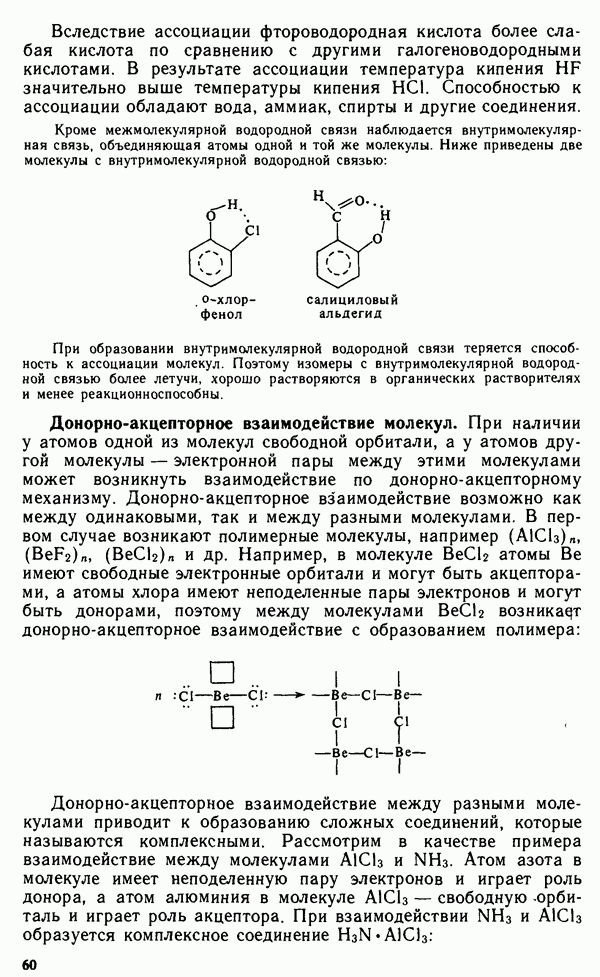
Каждая молекула глицина использует обе функциональные группы. Одна группа может связываться с центральным атомом через азот аминогруппы по донорно-акцепторному механизму, вторая — через кислород карбоксильной группы обычной ковалентной связью. Комплексообразователь при этом оказывается как бы втянутым внутрь лиганда, охвачен связями наподобие клешней рака. Отсюда и происходит название хелат (клешни рака).
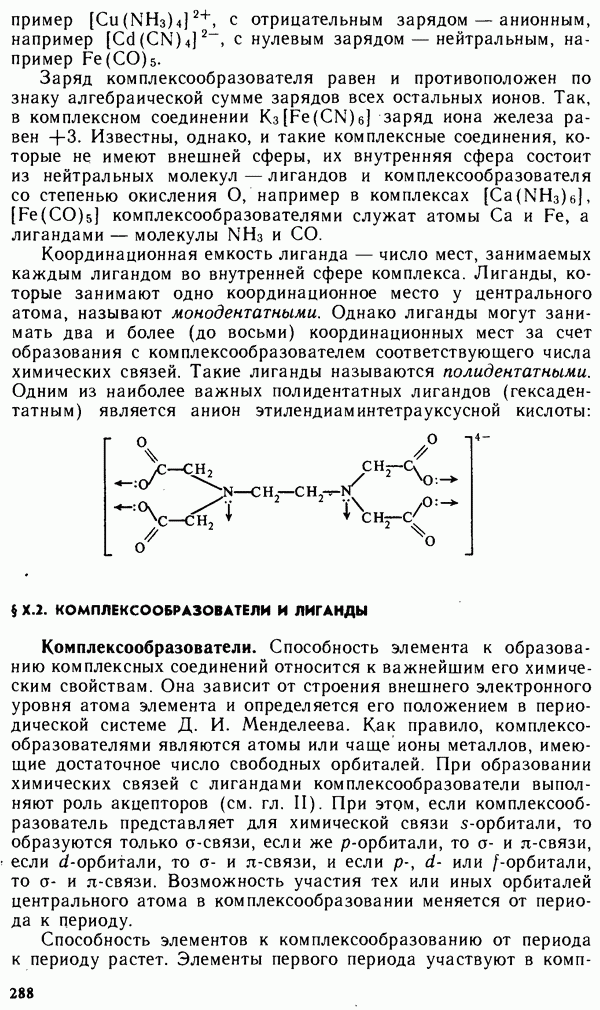
Широко применяются циклические комплексные соединения на основе этилендиаминтетрауксусной кислоты  и других аминополикарбоновых кислот, называемых комплексонами. Они образуют прочные соединения с большинством катионов. Поэтому комплексоны используют в аналитической химии для определения содержания металлов в различных материалах (метод анализа называется комплексонометрией), а также для определения жесткости воды. Применение комплексонов для очистки воды и растворения накипи в парогенераторах, а также для удаления продуктов коррозии позволило почти полностью заменить малоэффективные, трудоемкие механические методы высокопроизводительными и надежными химическими методами.
и других аминополикарбоновых кислот, называемых комплексонами. Они образуют прочные соединения с большинством катионов. Поэтому комплексоны используют в аналитической химии для определения содержания металлов в различных материалах (метод анализа называется комплексонометрией), а также для определения жесткости воды. Применение комплексонов для очистки воды и растворения накипи в парогенераторах, а также для удаления продуктов коррозии позволило почти полностью заменить малоэффективные, трудоемкие механические методы высокопроизводительными и надежными химическими методами.
4. Многоядерные комплексные соединения.
Распространены комплексные соединения, в которых два или несколько комплексообразователей соединены посредством лигандов. Например, в двухъядерном комплексном соединении  два иона
два иона  (комплексообразователь) связаны посредством группы
(комплексообразователь) связаны посредством группы  Такая связующая группа называется мостиковой. В качестве мостиковых групп могут выступать все полидентатные лиганды (за исключением лигандов, образующих комплексоны), а также монодентатные лиганды, обладающие неподеленными электронными парами: ионы
Такая связующая группа называется мостиковой. В качестве мостиковых групп могут выступать все полидентатные лиганды (за исключением лигандов, образующих комплексоны), а также монодентатные лиганды, обладающие неподеленными электронными парами: ионы  и др. К многоядерным комплексным соединениям относятся изополикислоты, гетерополикислоты и их соли. Кислоты, в состав которых входят ядра одного и того же элемента, называются изополикислотами, например
и др. К многоядерным комплексным соединениям относятся изополикислоты, гетерополикислоты и их соли. Кислоты, в состав которых входят ядра одного и того же элемента, называются изополикислотами, например 
—двухромовая кислота,  — полиметакремниевая кислота. Кислоты, в состав которых входят ядра различных элементов, называют гетерополикислотами, например
— полиметакремниевая кислота. Кислоты, в состав которых входят ядра различных элементов, называют гетерополикислотами, например  — фосфорномолибденовая кислота. Молекулы гетерополикислот удерживают до 30 молекул связанной воды, например
— фосфорномолибденовая кислота. Молекулы гетерополикислот удерживают до 30 молекул связанной воды, например 
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
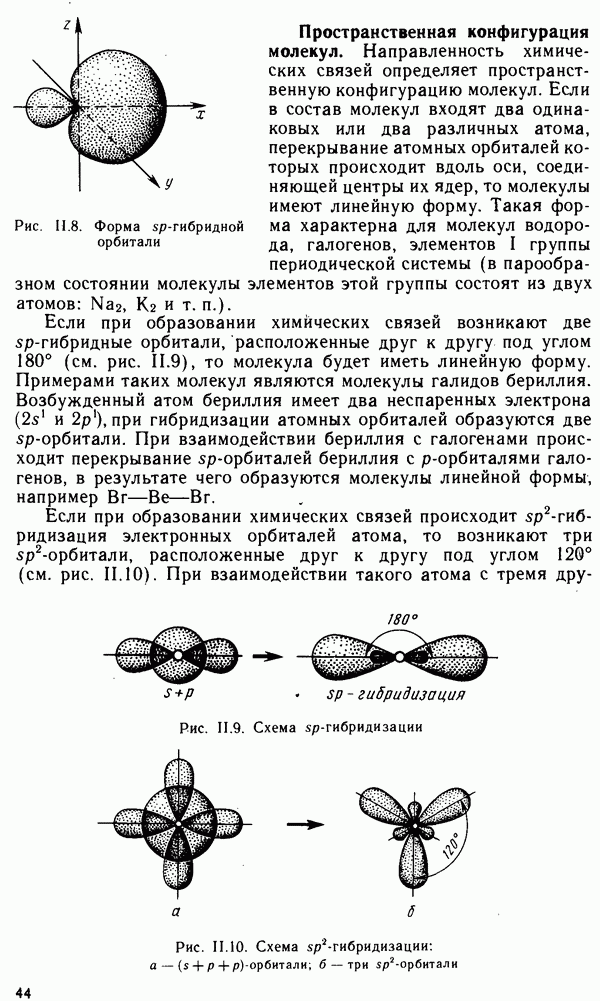
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
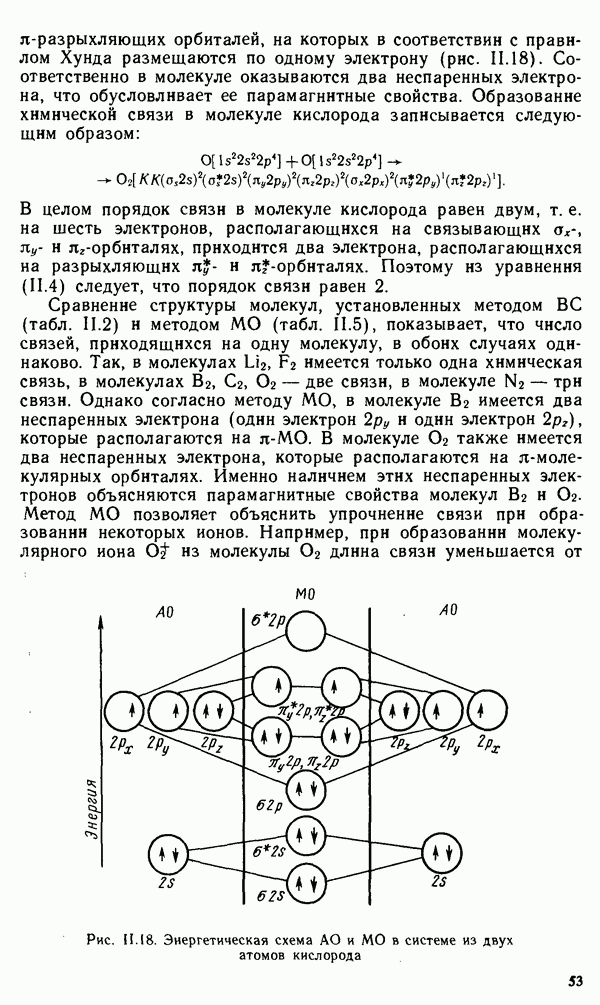
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
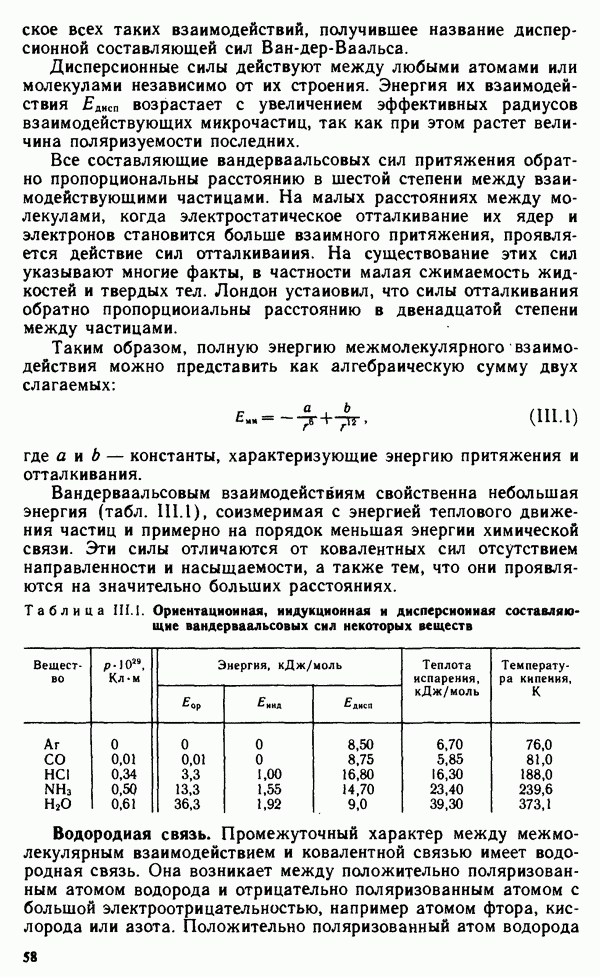
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
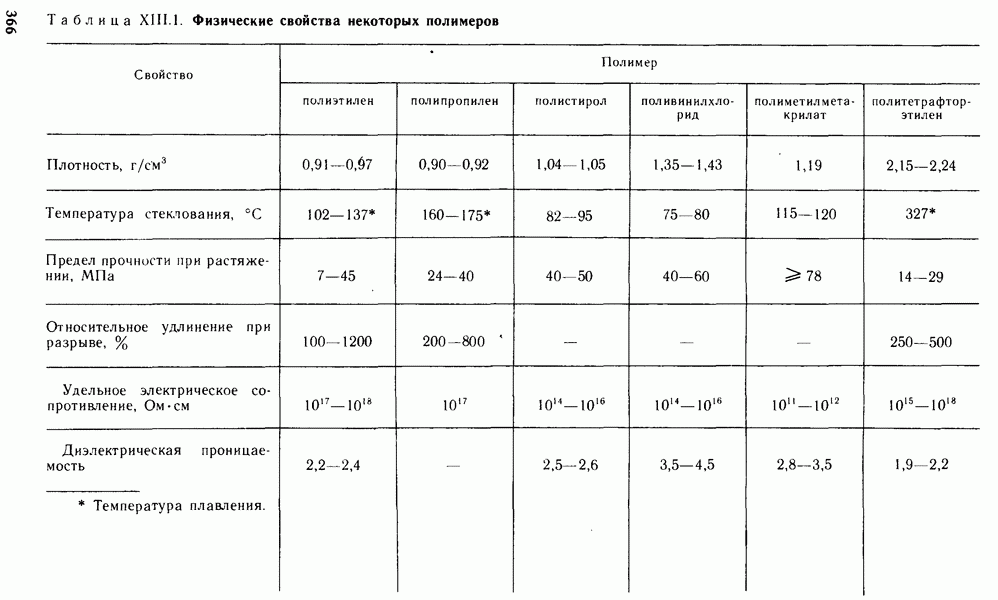
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ