| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
Металлы VIII группы образуют три побочные подгруппы — железа, кобальта и никеля. Но по исторически сложившейся систематике и по сходству свойств принято объединять  и
и  в семейство железа, а остальные шесть элементов
в семейство железа, а остальные шесть элементов  называть платиновыми металлами.
называть платиновыми металлами.
Семейство железа.
Атомы элементов  и
и  имеют соответственно следующую электронную конфигурацию:
имеют соответственно следующую электронную конфигурацию:  Отвечающие максимальному числу неспаренных электронов валентные состояния для данных элементов
Отвечающие максимальному числу неспаренных электронов валентные состояния для данных элементов
нетипичны. Наиболее характерными для них являются степени окисления  Причем в ряду
Причем в ряду  устойчивость соединений с низшей степенью окисления элемента возрастает, а с высшей — падает.
устойчивость соединений с низшей степенью окисления элемента возрастает, а с высшей — падает.
Железо — самый распространенный после алюминия металл на земном шаре. Его масса составляет  всей массы земной коры. Наиболее распространены в природе алюмосиликаты железа. Массовые содержания кобальта и никеля в земной коре равны примерно
всей массы земной коры. Наиболее распространены в природе алюмосиликаты железа. Массовые содержания кобальта и никеля в земной коре равны примерно  соответственно.
соответственно.
Из всех металлов, используемых человечеством, железо имеет наибольшее значение. Вся современная техника связана с применением железа и его сплавов. Ежегодное мировое потребление железа превышает 500 млн. т. Потребление никеля меньше (около  ); еще меньше потребление кобальта (около
); еще меньше потребление кобальта (около 
Железо, кобальт и никель представляют собой блестящие белые металлы с сероватым  или серебристым
или серебристым  оттенком. Железо и никель легко куются и прокатываются. Кобальт более тверд и хрупок. В отличие от других металлов
оттенком. Железо и никель легко куются и прокатываются. Кобальт более тверд и хрупок. В отличие от других металлов  и
и  притягиваются магнитом. Ниже приведены некоторые константы, характеризующие физико-химические свойства элементов семейства железа:
притягиваются магнитом. Ниже приведены некоторые константы, характеризующие физико-химические свойства элементов семейства железа:

Значения стандартных электродных потенциалов железа, кобальта и никеля позволяют отнести их к числу металлов средней химической активности. При этом железо активнее, чем кобальт и никель.
Железо (компактное) устойчиво по отношению к сухому воздуху, но во влажном быстро корродирует и покрывается бурым гидроксидом  рыхлым и не предохраняющим металл от дальнейшего окисления. Реакция образования ржавчины многостадийна; суммарно ее можно выразить уравнением
рыхлым и не предохраняющим металл от дальнейшего окисления. Реакция образования ржавчины многостадийна; суммарно ее можно выразить уравнением

При температуре каления железо сгорает, превращаясь в «железную окалину»  При нагревании железо взаимодействуют
При нагревании железо взаимодействуют

Рис. XII.1. Зависимость скорости растворения железа в  от концентрации кислоты
от концентрации кислоты
со многими неметаллами; реакции протекают особенно энергично, если железо мелко раздроблено. В зависимости от активности неметалла и условий проведения процесса образуются твердые растворы  , металлоподобные соединения
, металлоподобные соединения  или соли
или соли  Железо легко растворяется в кислотах, вытесняя из них водород:
Железо легко растворяется в кислотах, вытесняя из них водород:

Концентрированная азотная кислота пассивирует железо. Отношение  к серной кислоте зависит от концентрации
к серной кислоте зависит от концентрации  (рис. XII.1). Железу соответствуют три устойчивых оксида:
(рис. XII.1). Железу соответствуют три устойчивых оксида:  Все они имеют преимущественно основный характер. Гидроксиды
Все они имеют преимущественно основный характер. Гидроксиды  — труднорастворимые соединения;
— труднорастворимые соединения;  — основание,
— основание,  проявляет слабо выраженные амфотерные свойства, что позволяет получить соль
проявляет слабо выраженные амфотерные свойства, что позволяет получить соль  Известны также соли железной кислоты
Известны также соли железной кислоты  в которых железо имеет степень окисления
в которых железо имеет степень окисления  Растворы солей железа (II) окрашены в бледно-зеленый цвет, а безводные соли (например,
Растворы солей железа (II) окрашены в бледно-зеленый цвет, а безводные соли (например,  бесцветны. Это объясняется образованием при растворении солей железа аквакомплексов состава
бесцветны. Это объясняется образованием при растворении солей железа аквакомплексов состава 
При действии цианида калия на растворы солей железа (И) получается белый осадок цианида железа:

В избытке цианида калия осадок растворяется вследствие образования комплексной соли  называемой гексацианоферратом (II) калия:
называемой гексацианоферратом (II) калия:

Гексацианоферрат(II) калия, кристаллизующийся с тремя молекулами воды  называется также желтой кровяной солью. При растворении в воде желтая кровяная соль диссоциирует на ионы:
называется также желтой кровяной солью. При растворении в воде желтая кровяная соль диссоциирует на ионы:

Анион  является чувствительным реактивом на ионы
является чувствительным реактивом на ионы 

Образующийся осадок имеет характерную синюю окраску (берлинская лазурь). Под действием окислителей гексациано-ферраты(II) переходят в гексацианоферраты(III):

 калия
калия  называется также красной кровяной солью. Ее анион
называется также красной кровяной солью. Ее анион  служит чувствительным реактивом на ионы
служит чувствительным реактивом на ионы 

Образующийся осадок имеет характерный интенсивный синий цвет (турибулева синь).
Способ получения железа из руд основан на восстановлении оксидов железа углем. Поскольку расплавленное железо обладает способностью растворять углерод, то при выплавке получается не чистое железо, а сплав его с углеродом (до 4%), называемый чугуном. Чугун перерабатывается в сталь (до  углерода) и в мягкое (ковкое) железо (менее 0,3% углерода). Последнее идет на изготовление кровельного железа, гвоздей, проволоки и т.
углерода) и в мягкое (ковкое) железо (менее 0,3% углерода). Последнее идет на изготовление кровельного железа, гвоздей, проволоки и т. 
В настоящее время нельзя назвать ни одной отрасли народного хозяйства, где бы ни применялось железо и его сплавы. Все сплавы железа делятся на чугуны и стали. Углерод в чугунах может находиться в различных формах: или в виде соединения  (цементит), или в виде графита (пластинчатого, хлопьевидного или сферического). От формы графита в значительной мере зависят свойства чугуна. Среди чугунов различают белый, серый, высокопрочный и ковкий.
(цементит), или в виде графита (пластинчатого, хлопьевидного или сферического). От формы графита в значительной мере зависят свойства чугуна. Среди чугунов различают белый, серый, высокопрочный и ковкий.
Белый чугун содержит весь углерод в виде цементита. Он хрупок и поэтому имеет ограниченное применение. В основном он идет на переработку в сталь. Серый чугун (содержит только пластинчатый графит) характеризуется высокими литейными свойствами и широко применяется в машиностроении для отливки, станков и механизмов. Многие марки серого чугуна содержат  углерода, 1—4% кремния и до 1,4% марганца. Высокопрочный чугун получают введение специальных добавок (например,
углерода, 1—4% кремния и до 1,4% марганца. Высокопрочный чугун получают введение специальных добавок (например,  в жидкий чугун. Под влиянием добавок графит кристаллизуется в сферической форме. Сферический графит улучшает механические свойства чугуна. Из высокопрочного чугуна изготовляют коленчатые валы, насосы, вентили и т.
в жидкий чугун. Под влиянием добавок графит кристаллизуется в сферической форме. Сферический графит улучшает механические свойства чугуна. Из высокопрочного чугуна изготовляют коленчатые валы, насосы, вентили и т.  При длительном нагревании отливок из белого чугуна графит принимает хлопьевидную форму; чугун становится ковким. Ковкий чугун характеризуется высокими механическими свойствами. Из него делают детали, материал которых должен быть пластичным и прочным (например, задние мосты автомобилей).
При длительном нагревании отливок из белого чугуна графит принимает хлопьевидную форму; чугун становится ковким. Ковкий чугун характеризуется высокими механическими свойствами. Из него делают детали, материал которых должен быть пластичным и прочным (например, задние мосты автомобилей).
Стали подразделяются на различные группы, во-первых, по химическому составу и, во-вторых, по назначению. По химическому составу они делятся на углеродистые и легированные.
В углеродистых кроме углерода (до 2 %) имеются небольшие количества марганца и кремния (вводятся при раскислении стали), а также фосфор и сера. Производство легированных сталей предусматривает введение легирующих элементов  и др.) для придания сплаву определенных свойств: высокой прочности, пластичности и т.
и др.) для придания сплаву определенных свойств: высокой прочности, пластичности и т.  По своему назначению стали делятся на конструкционные, инструментальные и стали с особыми свойствами.
По своему назначению стали делятся на конструкционные, инструментальные и стали с особыми свойствами.
Конструкционные стали могут быть и углеродистыми и легированными. Основные легирующие элементы конструкционных сталей  Они хорошо поддаются обработке давлением, резанием; хорошо свариваются. Конструкционные стали применяются для изготовления деталей машин, конструкций и сооружений. Инструментальные стали тоже могут быть и углеродистыми и легированными. Основной легирующий элемент — хром. Эти стали характеризуются высокой твердостью, прочностью, износостойкостью. Их применяют для изготовления режущих и измерительных инструментов, штампов и т. п. К сталям с особыми свойствами относятся нержавеющие, жаростойкие, жаропрочные, магнитные и некоторые другие. Нержавеющие стали устойчивы против коррозии в агрессивных средах, жаростойкие — против коррозии при высоких температурах. В энергетике важны жаропрочные стали, сохраняющие высокие механические свойства при нагревании до значительных температур, что важно при изготовлении лопаток газовых турбин. В электротехнике важны магнитные стали, которые используются для постоянных магнитов и сердечников магнитных устройств, работающих в переменных полях. Постоянные магниты делают из высокоуглеродистых сталей, легированных хромом и вольфрамом. Они хорошо намагничиваются и долго сохраняют остаточную индукцию. Сердечники, наоборот, делают из низкоуглеродистых сталей, легированных кремнием. Они легко перемагничиваются и характеризуются малыми электрическими потерями.
Они хорошо поддаются обработке давлением, резанием; хорошо свариваются. Конструкционные стали применяются для изготовления деталей машин, конструкций и сооружений. Инструментальные стали тоже могут быть и углеродистыми и легированными. Основной легирующий элемент — хром. Эти стали характеризуются высокой твердостью, прочностью, износостойкостью. Их применяют для изготовления режущих и измерительных инструментов, штампов и т. п. К сталям с особыми свойствами относятся нержавеющие, жаростойкие, жаропрочные, магнитные и некоторые другие. Нержавеющие стали устойчивы против коррозии в агрессивных средах, жаростойкие — против коррозии при высоких температурах. В энергетике важны жаропрочные стали, сохраняющие высокие механические свойства при нагревании до значительных температур, что важно при изготовлении лопаток газовых турбин. В электротехнике важны магнитные стали, которые используются для постоянных магнитов и сердечников магнитных устройств, работающих в переменных полях. Постоянные магниты делают из высокоуглеродистых сталей, легированных хромом и вольфрамом. Они хорошо намагничиваются и долго сохраняют остаточную индукцию. Сердечники, наоборот, делают из низкоуглеродистых сталей, легированных кремнием. Они легко перемагничиваются и характеризуются малыми электрическими потерями.
Чугун дешевле стали. Он почти не способен к пластической деформации: однако его хорошие литейные свойства делают его незаменимым материалом в некоторых областях техники.
Кобальт вполне устойчив по отношению к воде и воздуху. В разбавленных кислотах он растворяется труднее, чем железо. Кислород окисляет кобальт лишь при температурах выше  При нагревании кобальт (особенно в виде порошка) взаимодействует, как и железо, со многими неметаллами. Соединения его с галогенами (
При нагревании кобальт (особенно в виде порошка) взаимодействует, как и железо, со многими неметаллами. Соединения его с галогенами ( и др.) — соли, с водородом и бором твердые растворы. Кобальт образует и металлоподобные соединения типа
и др.) — соли, с водородом и бором твердые растворы. Кобальт образует и металлоподобные соединения типа  и др. Кобальту соответствуют два оксида
и др. Кобальту соответствуют два оксида  Оксиды и отвечающие им гидроксиды имеют преимущественно основный характер.
Оксиды и отвечающие им гидроксиды имеют преимущественно основный характер.  — сильнейший окислитель:
— сильнейший окислитель:  . Относительно более устойчив
. Относительно более устойчив
смешанный оксид  но и он является энергичным окислителем. У кобальта сильно выражена способность к комплексообразованию. Причем акцепторные свойства более характерны для
но и он является энергичным окислителем. У кобальта сильно выражена способность к комплексообразованию. Причем акцепторные свойства более характерны для  чем для
чем для  Ионы
Ионы  образуют и катионные, и анионные комплексы (координационное число
образуют и катионные, и анионные комплексы (координационное число  равно шести), например
равно шести), например  Применение кобальта связано, главным образом, с производством сплавов. Его вводят в некоторые сплавы, чтобы сообщить им твердость. Среди таких сплавов следует отметить стеллит (сплав кобальта с хромом и вольфрамом), используемый в качестве конструкционного материала в турбинах, и победит (сверхтвердый сплав), содержащий
Применение кобальта связано, главным образом, с производством сплавов. Его вводят в некоторые сплавы, чтобы сообщить им твердость. Среди таких сплавов следует отметить стеллит (сплав кобальта с хромом и вольфрамом), используемый в качестве конструкционного материала в турбинах, и победит (сверхтвердый сплав), содержащий  Со. Изотоп
Со. Изотоп  широко применяется в медицине в борьбе с раком («кобальтовая пушка»).
широко применяется в медицине в борьбе с раком («кобальтовая пушка»).
Никель не окисляется на воздухе и легко растворяется только в разбавленной азотной кислоте. Химическая стойкость никеля обусловлена его склонностью к пассивированию, связанному с образованием на поверхности металла защитной оксидной пленки. С кислородом он начинает взаимодействовать только при  . И лишь в измельченном состоянии при нагревании
. И лишь в измельченном состоянии при нагревании  реагирует с галогенами, серой и другими неметаллами. С большинством из них он, как и многие d-элементы, образует соединения переменного состава (в том числе и металлоподобные). Из соединений никеля практическое значение имеют главным образом те, в которых степень окисления никеля
реагирует с галогенами, серой и другими неметаллами. С большинством из них он, как и многие d-элементы, образует соединения переменного состава (в том числе и металлоподобные). Из соединений никеля практическое значение имеют главным образом те, в которых степень окисления никеля  Оксид
Оксид  и гидроксид
и гидроксид  в воде не растворяются, но легко растворяются в кислотах и растворе аммиака. Взаимодействия идут с образованием комплексных ионов:
в воде не растворяются, но легко растворяются в кислотах и растворе аммиака. Взаимодействия идут с образованием комплексных ионов:

Для ионов  характерны координационные числа 4 и 6. Из соединений никеля (III) важным для практики является оксид №20з, который применяется при изготовлении щелочных аккумуляторов.
характерны координационные числа 4 и 6. Из соединений никеля (III) важным для практики является оксид №20з, который применяется при изготовлении щелочных аккумуляторов.
Основная масса металлического никеля используется в производстве различных сплавов. Сплавы на основе никеля можно разделить на жаропрочные, магнитные и сплавы с особыми свойствами. К важнейшим жаропрочным сплавам никеля относятся нимоник  Со, остальное
Со, остальное  и инконель
и инконель  остальное
остальное  Эти сплавы используются в современных турбинах и реактивных двигателях, где температура достигает
Эти сплавы используются в современных турбинах и реактивных двигателях, где температура достигает  . В качестве связующего материала никель используется в металлокерамических жаропрочных сплавах, сохраняющих свои механические характеристики при
. В качестве связующего материала никель используется в металлокерамических жаропрочных сплавах, сохраняющих свои механические характеристики при  . К жаропрочным сплавам относится и нихром, который применяется для изготовления
. К жаропрочным сплавам относится и нихром, который применяется для изготовления
элементов электронагревательных приборов. Из магнитных сплавов никеля нужно отметить пермаллой  остальное
остальное  способный интенсивно намагничиваться даже в слабых полях вследствие очень высокой начальной магнитной проницаемости. К сплавам никеля с особыми свойствами принадлежат монельметалл (30% Cu, остальное Ni), инвар
способный интенсивно намагничиваться даже в слабых полях вследствие очень высокой начальной магнитной проницаемости. К сплавам никеля с особыми свойствами принадлежат монельметалл (30% Cu, остальное Ni), инвар  , остальное
, остальное  платинит
платинит  , остальное
, остальное  Все эти сплавы уникальны (каждый в своем роде). Так, например, инвар практически не расширяется при нагревании до
Все эти сплавы уникальны (каждый в своем роде). Так, например, инвар практически не расширяется при нагревании до  а платинит имеет коэффициент термического расширения такой же, как у стекла, и используется для впаивания вводов металлических контактов в стекло. Чистый никель используют для никелирования. Мелко раздробленный никель применяется в качестве катализатора.
а платинит имеет коэффициент термического расширения такой же, как у стекла, и используется для впаивания вводов металлических контактов в стекло. Чистый никель используют для никелирования. Мелко раздробленный никель применяется в качестве катализатора.
Платиновые металлы.
Все платиновые металлы относятся к числу малораспространенных элементов. В природе они встречаются только в самородном состоянии и почти всегда сопутствуют друг другу. Они не образуют сколько-нибудь значительных скоплений и обычно являются лишь незначительной примесью к продуктам выветривания горных пород. Разделение платиновых металлов представляет значительные трудности. Будучи сильно рассеяны, платиновые металлы стали известны сравнительно недавно. Первой была открыта платина (1750). И только в  русский исследователь К. К. Клаус открыл рутений; Клаус назвал элемент в честь России
русский исследователь К. К. Клаус открыл рутений; Клаус назвал элемент в честь России 
Элементы платиновой группы в свободном виде представляют собой серебристо-белые достаточно тугоплавкие металлы  имеет сероватый оттенок,
имеет сероватый оттенок,  имеет синеватый оттенок). Палладий, родий и платина хорошо поддаются механической обработке; рутений, иридий и осмий более тверды и хрупки. Ниже приведены некоторые сведения о платиновых металлах:
имеет синеватый оттенок). Палладий, родий и платина хорошо поддаются механической обработке; рутений, иридий и осмий более тверды и хрупки. Ниже приведены некоторые сведения о платиновых металлах:


Платиновые металлы чрезвычайно устойчивы по отношению к химическим реагентам. Рутений, родий и иридий (компактные) не растворяются даже в царской водке. Последняя растворяет платину и осмий, а палладий растворяется также в 
Несмотря на близость атомных радиусов и энергий ионизации (см. выше), химические свойства платиновых металлов во многом индивидуальны (даже когда речь идет об электронных аналогах). Рутений и осмий — элементы, способные проявлять степень окисления  известны их оксиды
известны их оксиды  Кроме этих оксидов они образуют диоксиды
Кроме этих оксидов они образуют диоксиды  Диоксиды образуют также иридий и платина;
Диоксиды образуют также иридий и платина;  Родий имеет только один устойчивый оксид
Родий имеет только один устойчивый оксид  . Моноксиды дают платина и палладий:
. Моноксиды дают платина и палладий:  и
и  . Также разнообразно отношение платиновых металлов (мелко раздробленных) к ряду неметаллов, проявляемое в реакциях, протекающих при нагревании: по отношению к кислороду устойчивее других
. Также разнообразно отношение платиновых металлов (мелко раздробленных) к ряду неметаллов, проявляемое в реакциях, протекающих при нагревании: по отношению к кислороду устойчивее других  по отношению к сере —
по отношению к сере —  по отношению к хлору — 1г. Наименее устойчивы по отношению к кислороду
по отношению к хлору — 1г. Наименее устойчивы по отношению к кислороду  (тонкий порошок металла медленно переходит в
(тонкий порошок металла медленно переходит в  на воздухе уже на холоду) и
на воздухе уже на холоду) и 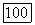 . В настоящее время более других платиновых металлов используются платина и палладий.
. В настоящее время более других платиновых металлов используются платина и палладий.
Платина устойчива на воздухе. Она растворяется только в царской водке, образуя гексахлороплатиновую кислоту 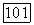 Из-за своей жаростойкости и химической инертности платина применяется в химической промышленности для изготовления коррозионно-стойких деталей аппаратуры, в электрохимических процессах — для изготовления платиновых электродов, а также для изготовления специальной лабораторной посуды — тиглей, чашек и т.
Из-за своей жаростойкости и химической инертности платина применяется в химической промышленности для изготовления коррозионно-стойких деталей аппаратуры, в электрохимических процессах — для изготовления платиновых электродов, а также для изготовления специальной лабораторной посуды — тиглей, чашек и т. 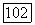 . В мелкораздробленном состоянии платина широко используется как катализатор. Благодаря стабильности электрических, механических и химических свойств платина применяется в электротехнике, автоматике и радиотехнике.
. В мелкораздробленном состоянии платина широко используется как катализатор. Благодаря стабильности электрических, механических и химических свойств платина применяется в электротехнике, автоматике и радиотехнике.
Палладий — самый легкий из платиновых металлов, наиболее мягкий и ковкий. В химическом отношении он менее инертен, чем платина и другие платиновые металлы. При нагревании палладий окисляется кислородом: 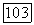 Он растворяется в азотной и горячей концентрированной серной кислотах. С царской водкой палладий реагирует более энергично, чем платина.
Он растворяется в азотной и горячей концентрированной серной кислотах. С царской водкой палладий реагирует более энергично, чем платина.
Характерные особенности палладия — устойчивость в степени окисления 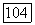 способность поглощать водород (до 800 объемов на 1 объем
способность поглощать водород (до 800 объемов на 1 объем 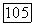 При поглощении водорода объем металла заметно увеличивается, он становится более хрупким и ломким. Палладий широко используется как катализатор многих химических реакций (его наносят на фарфор, асбест или другие носители). Сплавы палладия применяются в электротехнике, радиотехнике и автоматике как электроэмиссионные и другие материалы. Так, сплавы палладия с серебром идут для изготовления электрических контактов; сплавы палладия с золотом, платиной и родием используются в термопарах и терморегуляторах.
При поглощении водорода объем металла заметно увеличивается, он становится более хрупким и ломким. Палладий широко используется как катализатор многих химических реакций (его наносят на фарфор, асбест или другие носители). Сплавы палладия применяются в электротехнике, радиотехнике и автоматике как электроэмиссионные и другие материалы. Так, сплавы палладия с серебром идут для изготовления электрических контактов; сплавы палладия с золотом, платиной и родием используются в термопарах и терморегуляторах.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
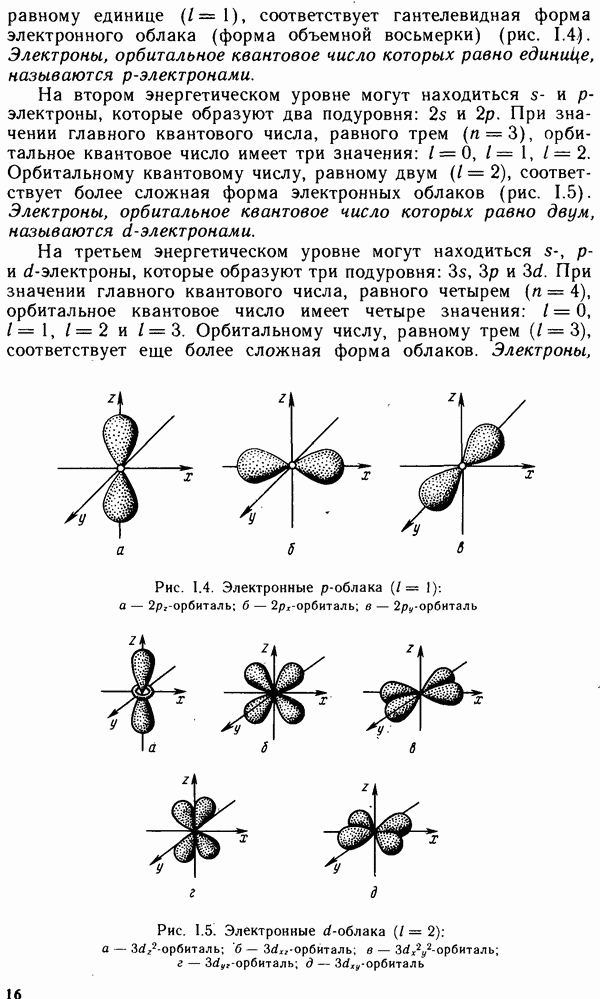
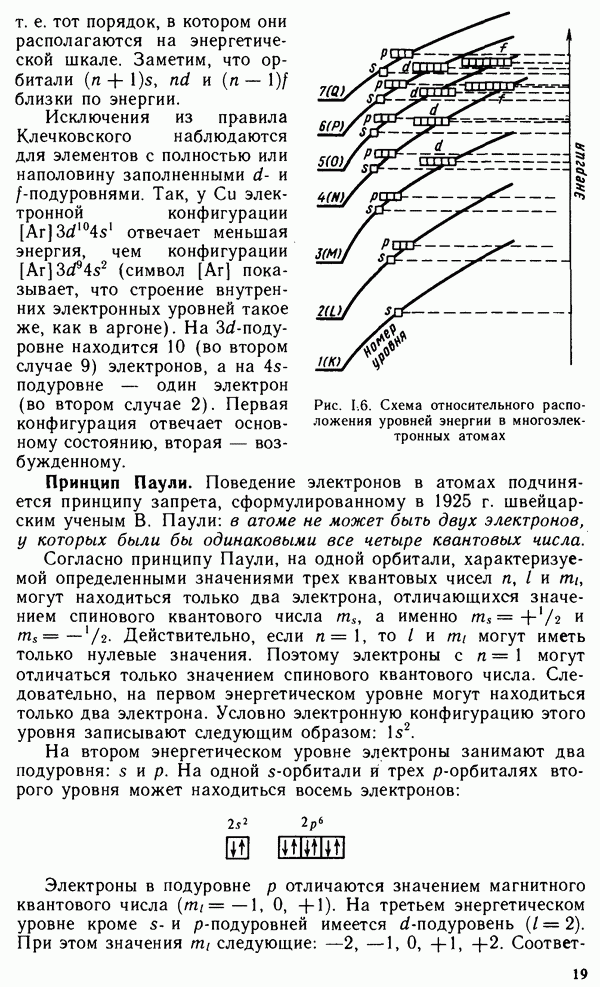
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
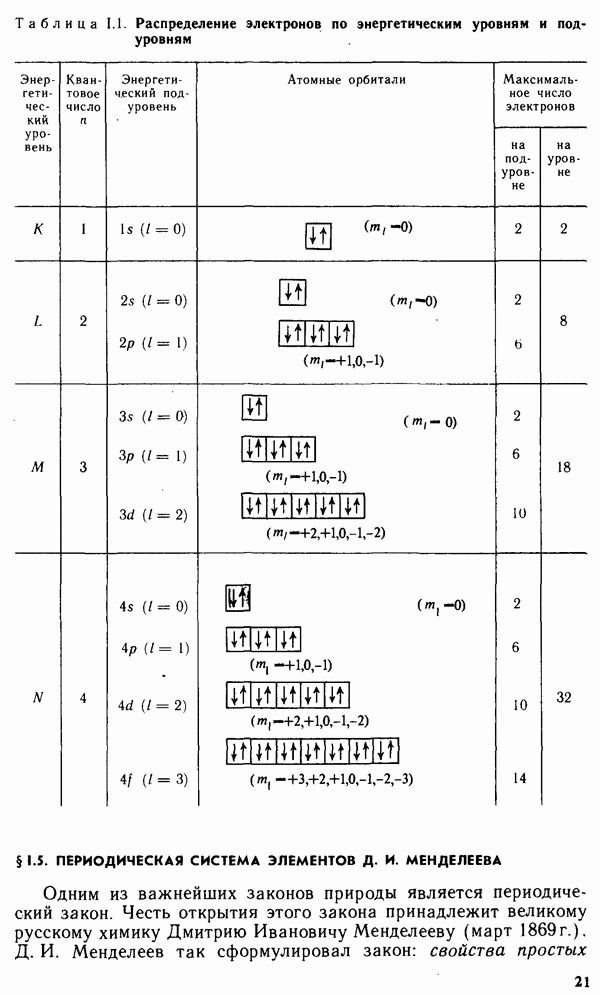
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
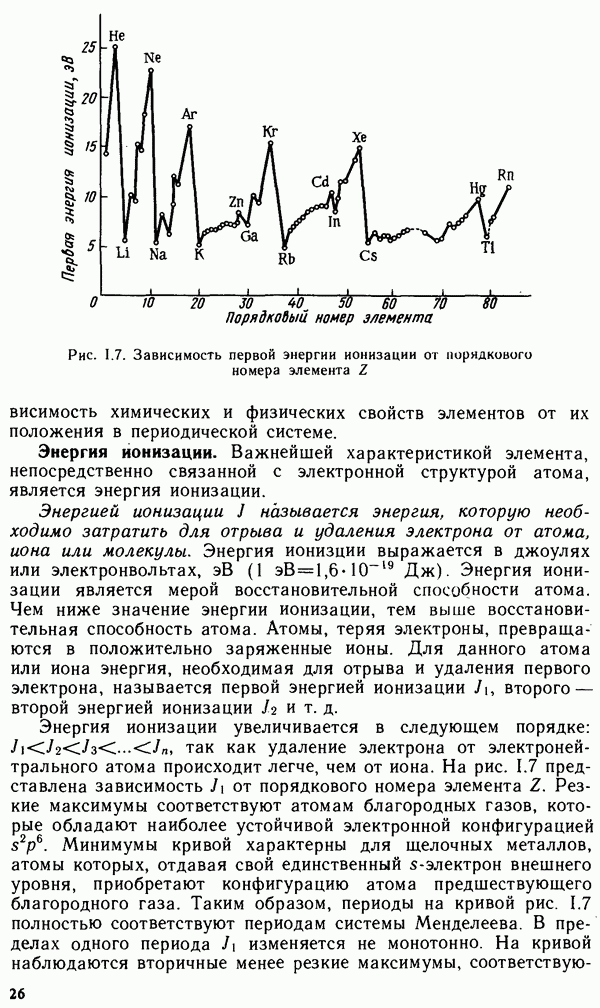
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
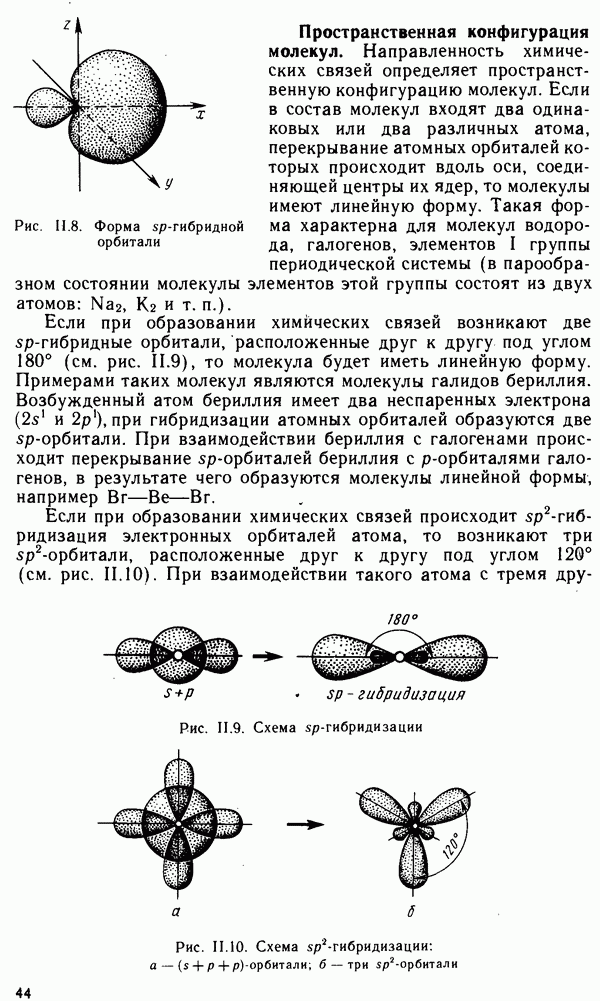
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
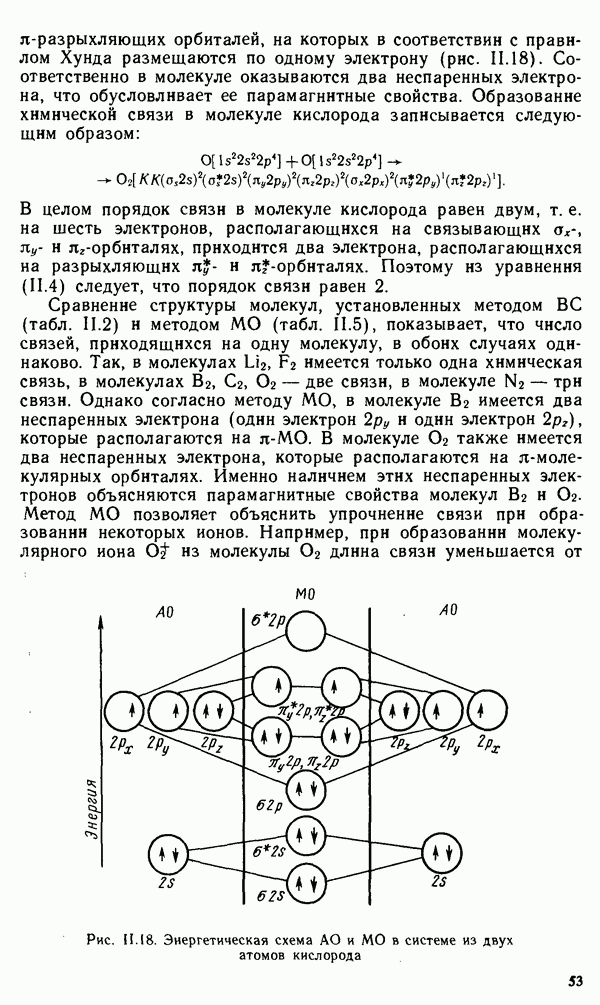
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
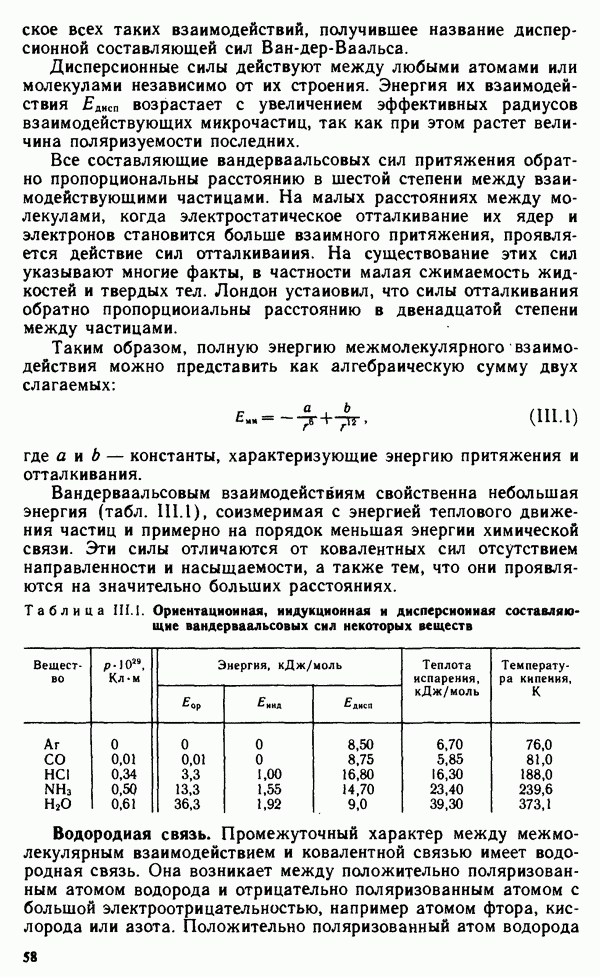
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
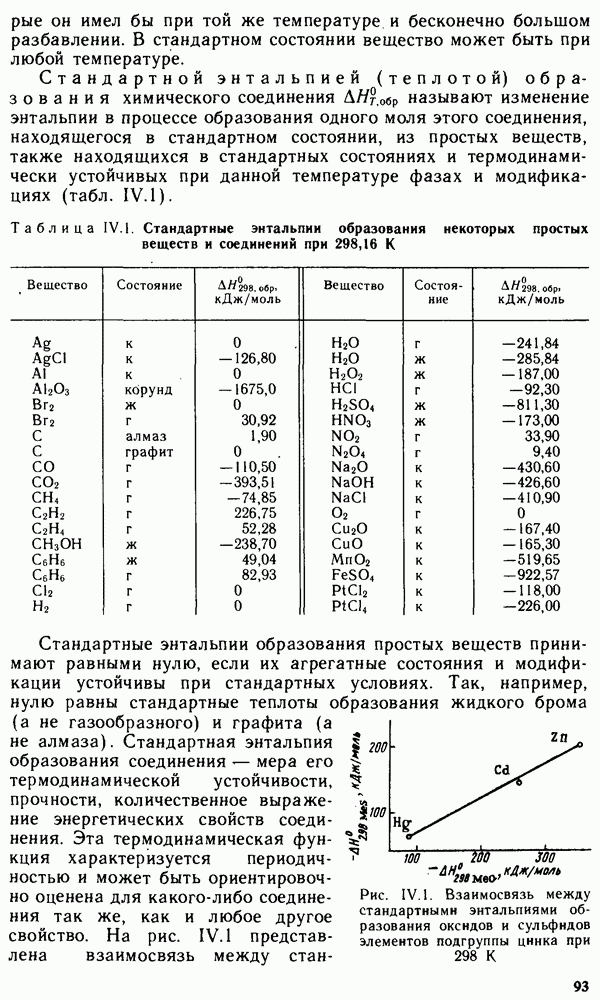
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
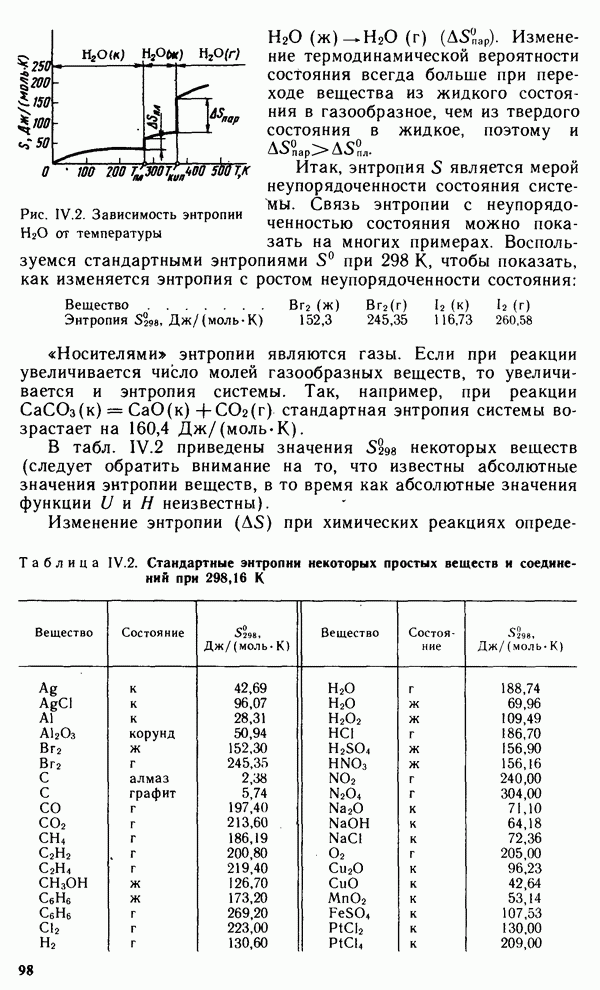
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
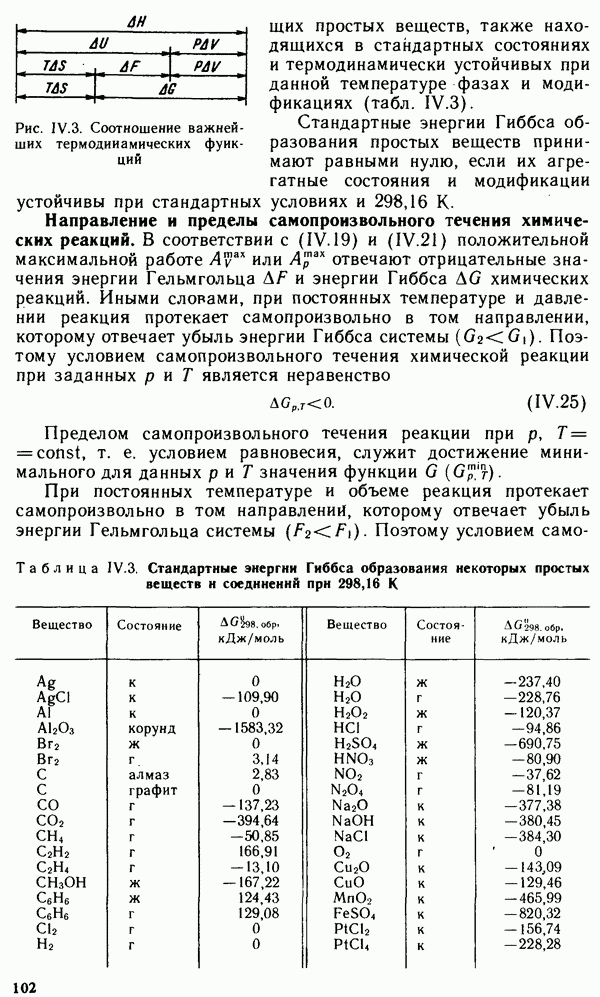
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
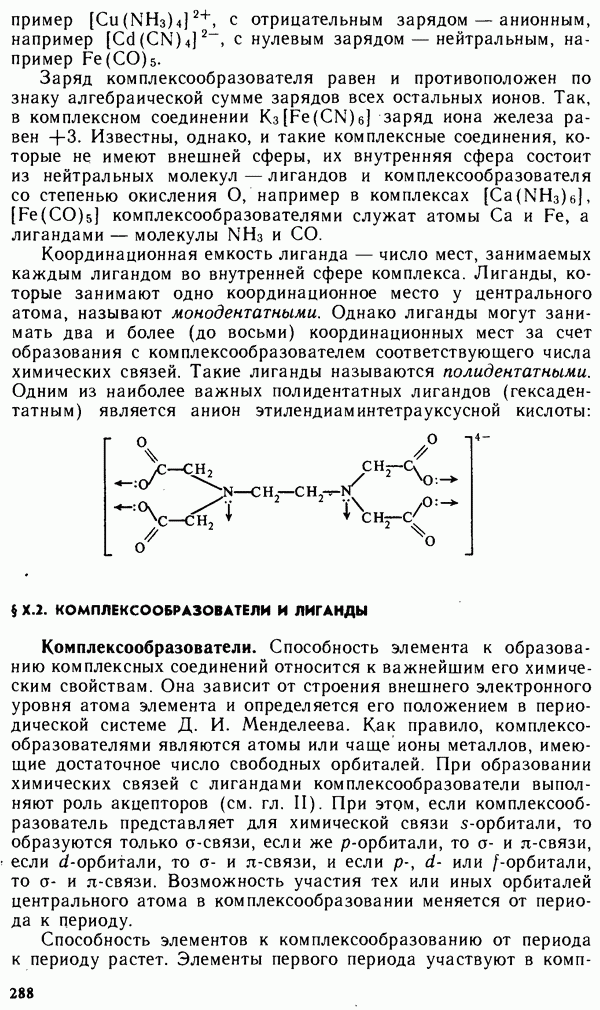
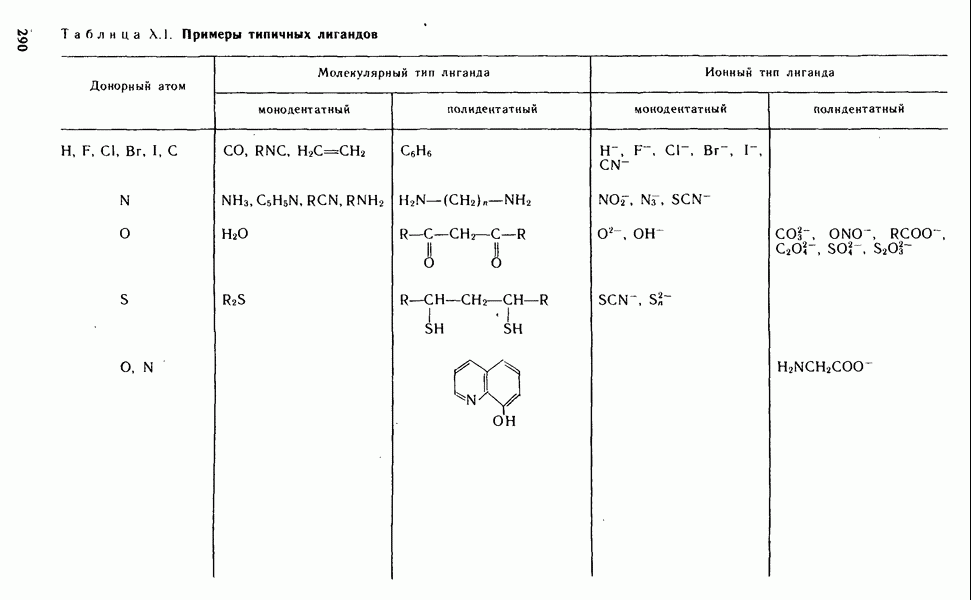
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
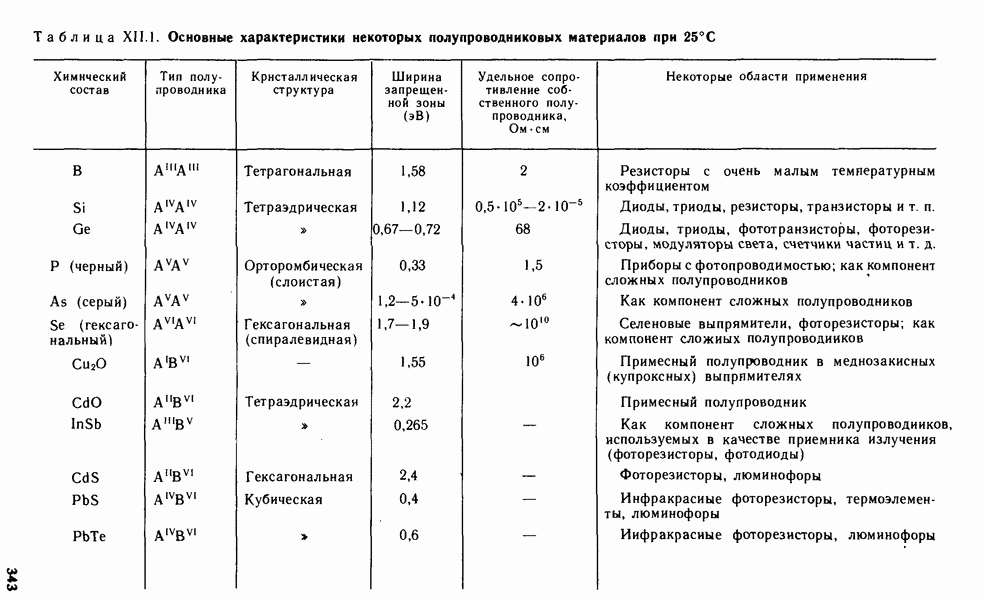
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ