| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ V.8. КАТАЛИЗ
Общие понятия.
Одним из наиболее распространенных методов ускорения химических реакций является катализ. Этот метод осуществляется с помощью катализаторов — веществ, резко увеличивающих скорость реакции, но не расходующихся в результате ее протекания. Катализаторы могут участвовать в образовании промежуточных продуктов реакции, но к концу взаимодействия они полностью регенерируются.
Если катализатор и взаимодействующие вещества образуют однофазную систему, катализ называют гомогенным. Если же катализатор находится в системе в виде самостоятельной фазы, катализ называют гетерогенным.
Современная техника очень широко использует катализаторы. В настоящее время химическая промышленность более чем на 90 % является каталитической. Велика роль катализа в осуществлении новых процессов органического синтеза. Крупнейшим успехом в этом направлении стало получение искусственного синтетического каучука из этанола, осуществленное впервые в СССР акад. С. В. Лебедевым; в 1930 г. был построен опытный завод, а в 1932 г. началось промышленное производство. Каталитические
методы используют и при переработке нефти. До 1940 г. переработка нефти осуществлялась преимущественно термическими способами. В настоящее время их заменили каталитические процессы.
Катализ — наиболее эффективный метод интенсификации промышленных химических процессов. От развития катализа в значительной мере зависит прогресс не только химической, но и других отраслей народного хозяйства. Осуществление многих термодинамически возможных и экономически выгодных процессов: получение новых материалов, реализация более совершенных технологических схем, использование более доступных сырьевых ресурсов, решение ряда проблем охраны окружающей среды (очистки сточных вод и газовых выбросов) — неразрывно связано с изысканием достаточно активных катализаторов.
Большинство химических реакций, протекающих в пищеварительном тракте, в крови, в клетках человека и животных, являются каталитическими реакциями; они ускоряются ферментами. Все ферменты — белковые вещества. Так, слюна содержит фермент птиалин, который катализирует превращение крахмала в сахар. Расщепление белков в желудке катализируется ферментом пепсином. Ферменты — исключительно активные катализаторы; их действие отличается высокой избирательностью.
Теория каталитических реакций исходит из некоторых общих положений: а) катализ как метод изменения скорости реакции применим только тогда, когда энергия Гиббса взаимодействия при данных условиях отрицательна  в присутствии катализатора изменяется механизм химической реакции, она протекает через новые стадии, каждая из которых характеризуется невысокой энергией активации. Таким образом действие катализатора сводится к тому, что он значительно снижает энергию активации катализируемой реакции; в) при катализе не изменяется тепловой эффект реакции; г) если катализируемая реакция обратима, катализатор не влияет на равновесие, не меняет константы равновесия и равновесных концентраций компонентов системы. Он в равной степени ускоряет и прямую, и обратную реакции, тем самым сокращая время достижения равновесия; д) катализаторы обычно действуют избирательно, селективно. Катализатор, активно ускоряющий одно взаимодействие, безразличен к другому. Избирательность действия зависит не только от природы катализатора, но и от условий его применения.
в присутствии катализатора изменяется механизм химической реакции, она протекает через новые стадии, каждая из которых характеризуется невысокой энергией активации. Таким образом действие катализатора сводится к тому, что он значительно снижает энергию активации катализируемой реакции; в) при катализе не изменяется тепловой эффект реакции; г) если катализируемая реакция обратима, катализатор не влияет на равновесие, не меняет константы равновесия и равновесных концентраций компонентов системы. Он в равной степени ускоряет и прямую, и обратную реакции, тем самым сокращая время достижения равновесия; д) катализаторы обычно действуют избирательно, селективно. Катализатор, активно ускоряющий одно взаимодействие, безразличен к другому. Избирательность действия зависит не только от природы катализатора, но и от условий его применения.
Активность того или иного катализатора зависит от многих факторов. Изменяя эти факторы, можно соответствующим образом изменять активность и избирательность действия катализатора. Прежде всего при неизменных условиях скорость каталитической реакции пропорциональна (в определенных пределах) количеству катализатора. Активность того или иного катализатора может быть резко повышена или понижена различными добавками. Добавки, увеличивающие активность катализатора, называются промоторами. Активность, селективность и срок службы катализатора во многом зависят от температуры
проведения каталитической реакции. Для каждой каталитической реакции максимальная активность катализатора отвечает строго определенному температурному режиму процесса.
До настоящего времени еще не создана общая теория катализа, которая позволяла бы предвидеть, какой катализатор для данной реакции является наилучшим. Часто это важнейшая проблема решается чисто эмпирическим путем, подбором катализатора для данной реакции.
Гомогенный катализ.
Для объяснения механизма гомогенного катализа наибольшее распространение получила теория промежуточных соединений, предложенная французским химиком Сабатье и развитая в работах Н. Д. Зелинского и его школы. Согласно этой теории катализатор реагирует с исходными веществами, образуя нестойкие промежуточные соединения, последующие превращения которых приводят к образованию нужных продуктов реакции и регенерации катализатора.
Химическое взаимодействие катализатора с исходными веществами направляет реакцию по пути, отличному от того, что осуществляется в отсутствие катализатора. В результате этого уменьшается энергия активации протекающего взаимодействия и увеличивается его скорость. В общем виде схему гомогенной каталитической реакции можно представить себе так:
в отсутствие катализатора

в присутствии катализатора К

Примером может служить реакция разложения пероксида водорода (жидкость) в присутствии растворенного иода: в отсутствие катализатора реакция протекает с невысокой скоростью и отвечает уравнению

В присутствии катализатора (12) реакция ускоряется и идет по стадиям:

Промежуточный продукт реакции HI образуется в первой стадии процесса и разлагается во второй. В образовании HI участвует катализатор, но к концу взаимодействия он полностью регенерируется. В качестве гомогенных катализаторов в последние годы все шире применяют комплексные соединения переходных металлов.
Гетерогенный катализ.
Гетерогенный катализ всегда начинается с адсорбции молекул исходных веществ на поверхности твердого катализатора. При этом только обратимая адсорбция Является началом каталитической реакции. Необратимая хемосорбция приводит к образованию на поверхности катализатора устойчивых соединений и тем самым к снижению активности катализатора.
При обратимой адсорбции молекул исходных веществ поверхностью твердого катализатора происходит ослабление связей между атомами в молекулах адсорбата. За этот счет снижается энергия активации катализируемой реакции, течение которой с высокой скоростью осуществляется на поверхности катализатора. Например, энергия активации реакции разложения аммиака  в присутствии платинового катализатора уменьшается с 330 до 160 кДж/моль.
в присутствии платинового катализатора уменьшается с 330 до 160 кДж/моль.
В 1929 г. А. А. Баландиным была создана мультиплетная теория гетерогенного катализа, в основу которой положен принцип структурного и энергетического соответствия между катализатором и реагирующими веществами. Согласно этой теории, каталитически активными центрами катализатора являются мультиплеты — совокупности поверхностных атомов, участвующих в акте химического превращения. Катализатор активен лишь в том случае, если соблюдается соответствие расположения атомов в мультиплете и в реагирующей молекуле. Структурное соответствие обеспечивает избирательность катализатора. Вторым условием активности катализатора является энергетическое соответствие связей между атомами в молекулах реагирующих веществ и связей, которые образуют эти атомы с атомами катализатора. Мультиплетная теория позволяет рассчитывать оптимальные значения энергий связей и межатомных расстояний у реагирующих веществ и катализаторов и осуществлять выбор наилучшего катализатора.
Учение о гетерогенном катализе получило дальнейшее развитие в исследованиях Н. И. Кобозева (теория активных ансамблей), Н. Н. Семенова и В. В. Воеводского (радикальная или цепная теория катализа), Ф. Ф. Волькенштейна и других ученых (электронная теория катализа).
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
Пример I. Во сколько раз изменится скорость прямой и обратной реакций в системе  если объем газовой смеси уменьшить в три раза? В какую сторону сместится равновесие системы?
если объем газовой смеси уменьшить в три раза? В какую сторону сместится равновесие системы?
Решение. Обозначим концентрации реагирующих веществ  . Согласно закоиу действующих масс, скорости прямой и обратной реакций до изменения объема равны
. Согласно закоиу действующих масс, скорости прямой и обратной реакций до изменения объема равны

После уменьшения объема гомогенной системы в три раза концентрация каждого из реагирующих веществ увеличится в три раза:  При новых концентрациях скорости
При новых концентрациях скорости  прямой и обратной реакций будут равны
прямой и обратной реакций будут равны

Из четырех указанных уравнений получим

Следовательно, скорость прямой реакции увеличилась в 27 раз, а обратной — в 9 раз. Равновесие системы сместилось в сторону образования 
Пример 2. Во сколько раз увеличится скорость реакции, протекающей в газовой фазе, при повышении температуры от 30 до  если температурный коэффициент реакции равен 2?
если температурный коэффициент реакции равен 2?
Решение. Зависимость скорости химической реакции от температуры определяется эмпирическим правилом Вант-Гоффа по формуле

Следовательно, скорость реакции протекающей при  увеличилась по сравнению со скоростью реакции
увеличилась по сравнению со скоростью реакции  протекающей при
протекающей при  в 16 раз.
в 16 раз.
Пример 3. Коистаита равновесия гомогенной системы

при  равна 1. Вычислите концентрации всех веществ при равновесии, если исходные концентрации
равна 1. Вычислите концентрации всех веществ при равновесии, если исходные концентрации 
Решение. При равновесии скорости прямой и обратной реакций равны, а отношение констант этих скоростей есть тоже величина постоянная и называется константой равновесия данной системы:

В условии задачи даны исходные концентрации, тогда как в выражение  входят только равновесные концентрации всех веществ системы. Предположим, что к моменту равновесия концентрация
входят только равновесные концентрации всех веществ системы. Предположим, что к моменту равновесия концентрация  Количество молей образовавшегося водорода при этом будет также
Количество молей образовавшегося водорода при этом будет также  Столько же молей
Столько же молей  расходуется для образования
расходуется для образования  молей
молей  Следовательно, равновесные концентрации всех веществ составляют:
Следовательно, равновесные концентрации всех веществ составляют:

Зная константу равновесия, рассчитаем х:

Таким образом, искомые равновесные концентрации:

Пример 4. Эндотермическая реакция разложения пентахлорида фосфора протекает по уравнению

Как надо изменить: а) температуру; б) давление; в) концентрацию, чтобы сместить равновесие в сторону реакции разложения 
Решение. Смещением, или сдвигом, химического равновесия называют изменение равновесных концентраций реагирующих веществ в результате изменения одного из условий реакции. Направление, в котором сместилось равновесие, определяется по принципу Ле Шателье: а) так как реакция разложения  эндотермическая
эндотермическая  то для смещения равновесия в сторону прямой реакции нужно повысить температуру; б) так как в данной системе разложение
то для смещения равновесия в сторону прямой реакции нужно повысить температуру; б) так как в данной системе разложение  ведет к увеличению объема (из одной молекулы газа образуются две газообразные молекулы), то для смещения равновесия в сторону прямой реакции надо уменьшить давление; в) смещения равновесия в указанном направлении можно достигнуть как увеличением концентрации
ведет к увеличению объема (из одной молекулы газа образуются две газообразные молекулы), то для смещения равновесия в сторону прямой реакции надо уменьшить давление; в) смещения равновесия в указанном направлении можно достигнуть как увеличением концентрации  так и уменьшением концентрации
так и уменьшением концентрации  или
или 
Пример 5. Рассчитайте изменение константы скорости реакции, имеющей энергию активации  при увеличении температуры от 330 до 400 К.
при увеличении температуры от 330 до 400 К.
Решение. Зависимость константы скорости реакции от температуры определяется уравнением Аррениуса

Логарифм отношения констант скоростей реакции при температурах и  соответственно равен
соответственно равен

где  — универсальная газовая постоянная, рабная
— универсальная газовая постоянная, рабная  Подставив в это уравнение данные задачи, получим
Подставив в это уравнение данные задачи, получим

откуда

Пример 6. Рассчитать константу равновесия химической реакции  при 1000 К, если стандартная энергия Гиббса при этой температуре равна
при 1000 К, если стандартная энергия Гиббса при этой температуре равна 
Решение. Константа равновесия химической реакции связана со стандартной энергией Гиббса уравнением

откуда

Подставляя в это уравнение числовые значения, получаем

откуда 
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ
(см. скан)
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
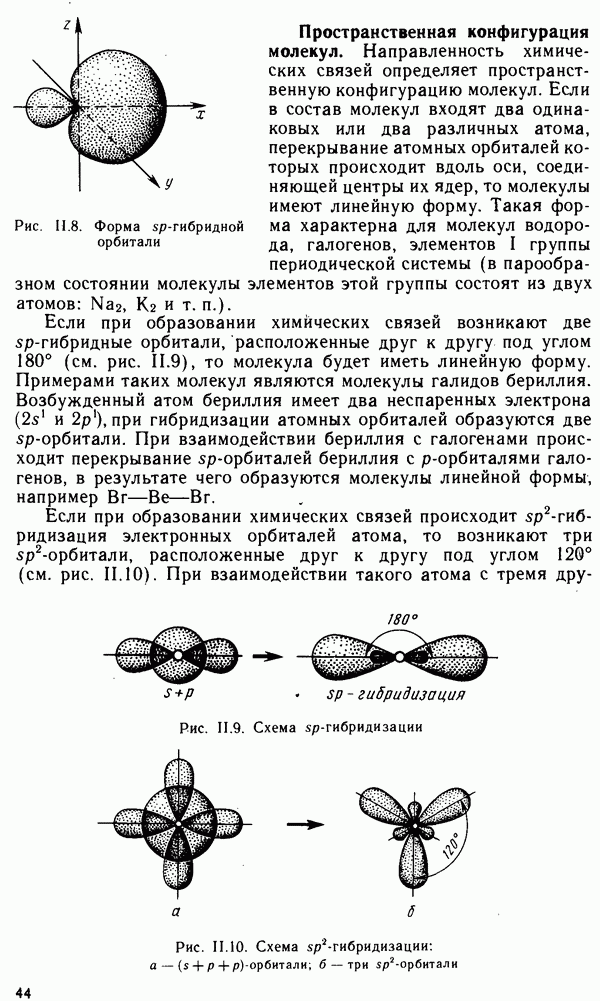
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
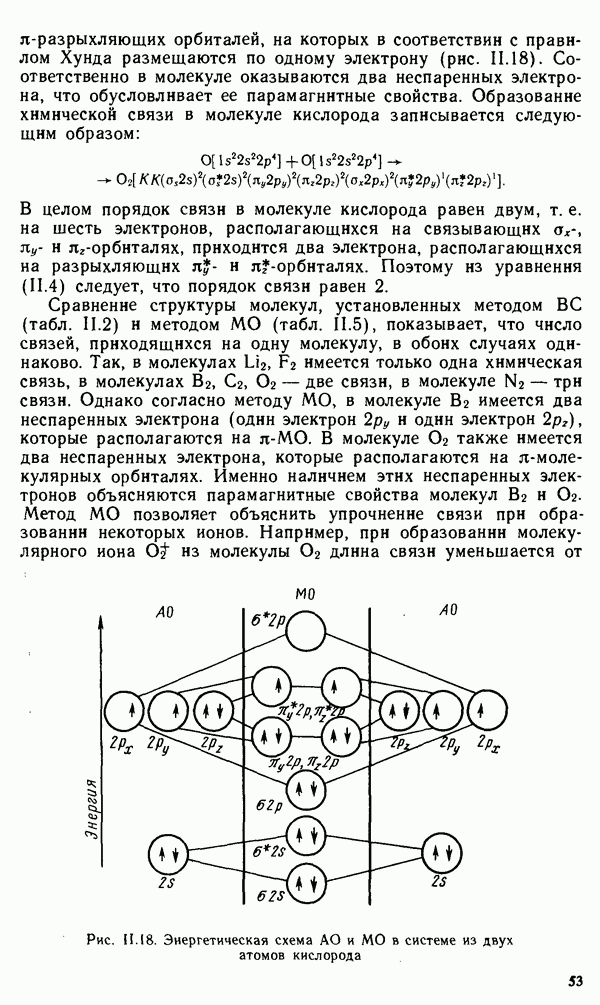
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
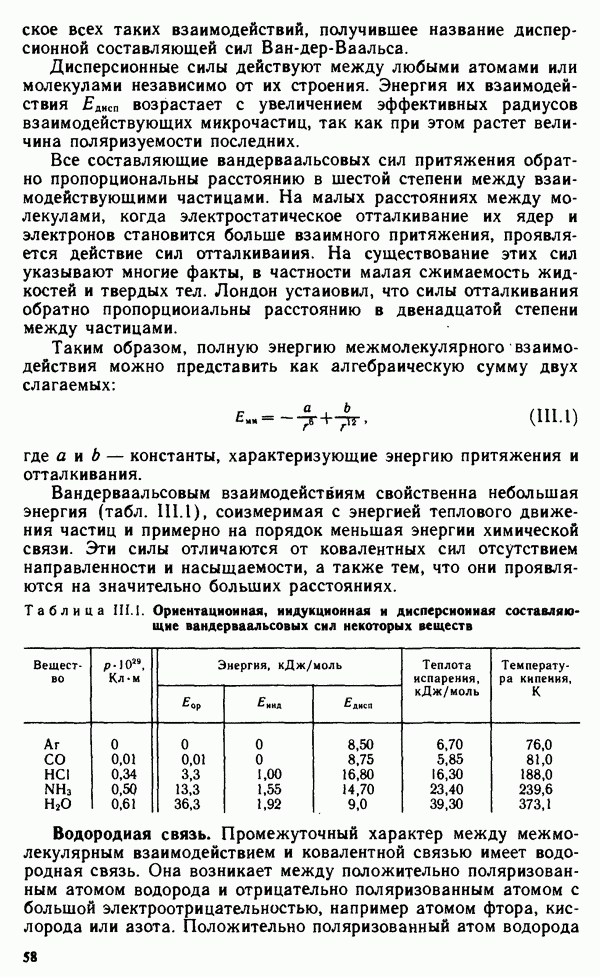
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ