| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
§ ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
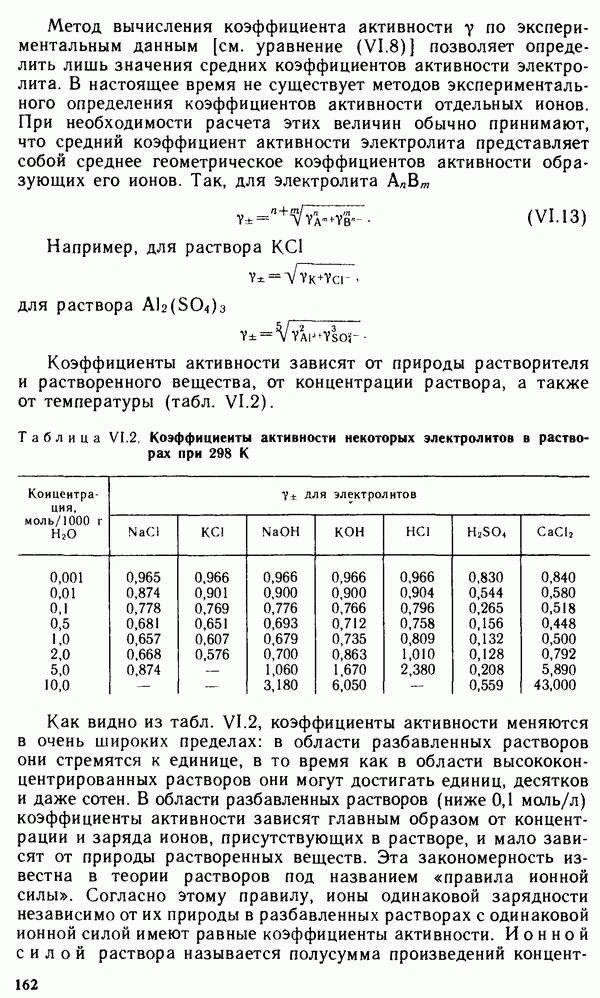
В настоящее время человечество использует для своих нужд в основном химическую энергию ископаемого топлива. Химическая энергия превращается в электрическую на паротурбинных тепловых электростанциях и в механическую энергию в двигателях внутреннего сгорания, применяемых на транспорте. Однако указанные способы преобразования химической энергии не удовлетворяют требованиям современной техники по ряду причин. Тепловые электростанции и двигатели внутреннего сгорания дают большое число вредных выбросов, они в значительной мере ответственны за загрязнение воздушного бассейна Земли. Хотя запасы ископаемого топлива ограничены, однако при современных способах преобразования химической энергии топливо используется не эффективно: КПД двигателей внутреннего сгорания
рания и электростанций составляет 15-40 %. Кроме того, паротурбинные установки и двигатели внутреннего сгорания не могут быть использованы во многих областях техники, например в системах, работающих в космосе и под водой, в портативных устройствах. Поэтому ведется разработка новых методов преобразования энергии.
Одним из наиболее перспективных является электрохимический способ преобразования химической энергии в электрическую, который осуществляется в химических источниках тока. К достоинствам последних относится высокий КПД, бесшумность, безвредность, возможность использования в космосе и под водой, в переносных устройствах, на транспорте и т. п. К химическим источникам тока относят гальванические элементы, аккумуляторы и топливные элементы.
Гальванические первичные элементы.
Гальваническими первичными элементами называют устройства для прямого преобразования химической энергии заключенных в них реагентов в электрическую. Реагенты (окислитель и восстановитель) входят непосредственно в состав гальванического элемента и расходуются в процессе его работы. После расхода реагентов элемент не может больше работать. Таким образом, это источник тока одноразового действия, поэтому его еще называют первичным химическим источником тока. Гальванический элемент характеризуется ЭДС, напряжением, емкостью и энергией, которую он может отдать во внешнюю цепь. ЭДС элемента определяется термодинамическими функциями протекающих в нем процессов (см. § VII.2). Напряжение элемента  меньше ЭДС из-за поляризации электродов и омических потерь:
меньше ЭДС из-за поляризации электродов и омических потерь:

где  — ЭДС элемента; I — ток;
— ЭДС элемента; I — ток;  — сопротивление проводников первого и второго рода внутри элемента;
— сопротивление проводников первого и второго рода внутри элемента;  — поляризация элемента, равная сумме катодной и анодной поляризаций
— поляризация элемента, равная сумме катодной и анодной поляризаций

В свою очередь катодная  и анодная
и анодная  поляризации являются суммой концентрационной и электрохимической поляризаций анода и катода:
поляризации являются суммой концентрационной и электрохимической поляризаций анода и катода:

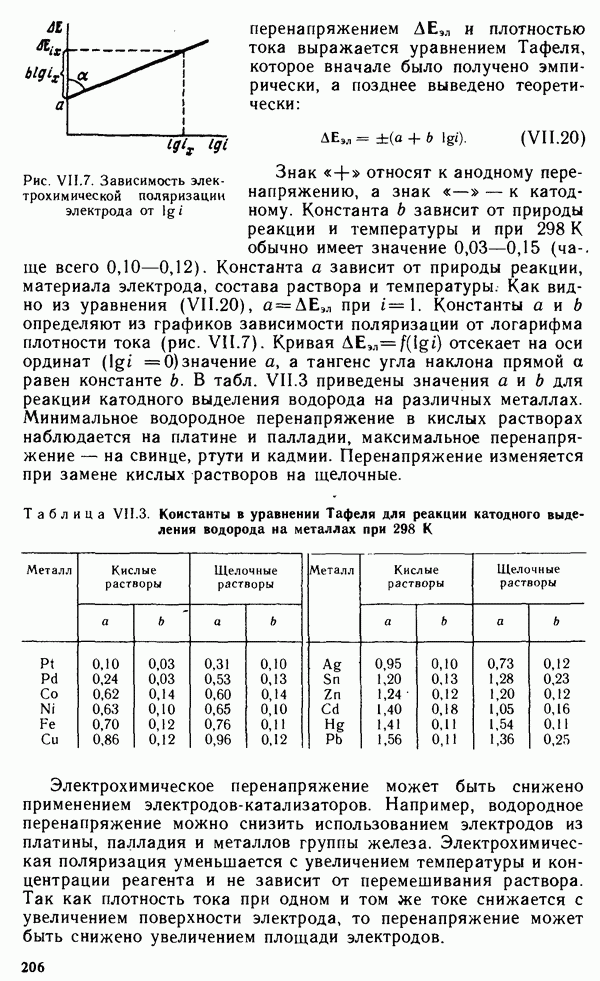
Поляризация возрастает с увеличением плотности тока (см. § VII.5). Кроме того, при увеличении плотности тока растет омическое падение напряжения. Таким образом, при увеличении плотности тока напряжение элемента падает. Кривая зависимости
напряжения элемента от силы или плотности тока получила название вольт-амперной кривой элемента. По мере работы элемента (разряда) уменьшается концентрация исходных реагентов и растет концентрация продуктов реакции, поэтому в соответствии с уравнением Нернста ЭДС элемента уменьшается. Кроме того, возрастает поляризация элемента. Поэтому при разряде элемента напряжение его постепенно падает. Кривая изменения напряжения во времени в процессе разряда называется разрядной кривой элемента. Чем меньше меняется напряжение при разряде элемента, тем больше возможностей его применения.
Емкость элемента — это количество электричества, которое источник тока отдает при разряде. Она определяется массой реагентов в элементе, их эквивалентом и степенью превращения. Если элемент разряжается при постоянном токе  , то емкость определяют по уравнению
, то емкость определяют по уравнению

а если элемент разряжается при постоянном внешнем сопротивлении  то по уравнению
то по уравнению

где  — емкость при постоянном токе или постоянном внешнем сопротивлении соответственно,
— емкость при постоянном токе или постоянном внешнем сопротивлении соответственно,  — время разряда элемента.
— время разряда элемента.
Если элемент разряжается при постоянном токе  то энергию элемента определяют по уравнению
то энергию элемента определяют по уравнению

и если элемент разряжается при постоянном внешнем сопротивлении  то по уравнению
то по уравнению

где  — энергия элемента, которую он отдает во внешнюю цепь, соответственно при постоянном токе I или постоянном внешнем сопротивлении
— энергия элемента, которую он отдает во внешнюю цепь, соответственно при постоянном токе I или постоянном внешнем сопротивлении  — среднее напряжение при разряде элемента.
— среднее напряжение при разряде элемента.
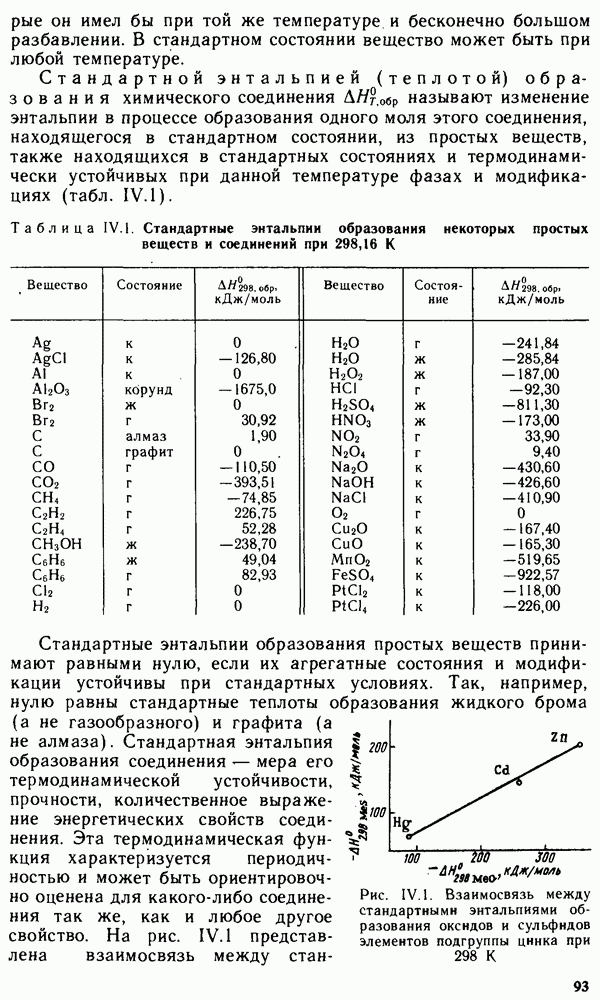
Важной характеристикой элемента служит удельная энергия, т. е. энергия, отнесенная к единице массы или объема элемента. Так как при увеличении тока напряжение элемента падает, то энергия и удельная энергия элемента также падают. Более высокую удельную энергию можно получить в элементах с большим значением  малой поляризацией, малыми значениями электрохимических эквивалентов и высокими степенями превращения реагентов. В качестве анодов обычно применяются электроды из цинка и магния, катодов — электроды из оксидов металлов
малой поляризацией, малыми значениями электрохимических эквивалентов и высокими степенями превращения реагентов. В качестве анодов обычно применяются электроды из цинка и магния, катодов — электроды из оксидов металлов
(марганца, меди, ртути, серебра) и хлоридов (меди и свинца) на графите, а также кислородный электрод.
Рассмотрим для примера работу сухого марганцово-цинкового элемента, широко применяемого для питания радиоаппаратуры, аппаратуры связи, магнитофонов, карманных фонарей и др. Анодом в элементе служит цинковый электрод, катодом — электрод из смеси диоксида марганца с графитом, токоотводом
служит графит. В качестве электролита используется паста, состоящая из раствора хлорида аммония с добавкой муки или крахмала (загустители). Схема элемента

На аноде происходит анодное окисление цинка, на катоде  восстанавливается до
восстанавливается до  Суммарное уравнение токообразующей реакции:
Суммарное уравнение токообразующей реакции:

Элемент имеет напряжение 1,2-1,6 В, удельную энергию  . В элементах с такими же реагентами, но с щелочным электролитом
. В элементах с такими же реагентами, но с щелочным электролитом  получают более высокую удельную энергию
получают более высокую удельную энергию  Если требуется высокая сохранность в рабочем состоянии, постоянное напряжение и высокая удельная энергия на единицу объема, используют ртутно-цинковые элементы:
Если требуется высокая сохранность в рабочем состоянии, постоянное напряжение и высокая удельная энергия на единицу объема, используют ртутно-цинковые элементы:

Напряжение элемента  , удельная энергия
, удельная энергия  Элементы применяются в портативных радиоприемниках и передатчиках, слуховых аппаратах, кардиостимуляторах.
Элементы применяются в портативных радиоприемниках и передатчиках, слуховых аппаратах, кардиостимуляторах.
Напряжение элементов можно увеличить при использовании анодов, имеющих электроотрицательный потенциал (см. табл. VII.1), например магния. Однако такие аноды в водных растворах подвергаются коррозии с выделением водорода, что приводит к потере емкости элемента при хранении (саморазряд). Поэтому разработаны резервные элементы, которые приводятся в рабочее состояние (активируются) непосредственно перед началом их использования. Примером может служить медно-хлористо-магниевый элемент, в котором анодом служит магний, а окислителем — хлорид меди (I). Элемент хранится в сухом состоянии и перед использованием заливается водой. Напряжение элемента  , удельная энергия
, удельная энергия 
Коррозию можно предотвратить применением неводных растворов электролитов, в которых устойчивы даже щелочные металлы. В последние годы разработаны элементы с литиевыми анодами, неводными растворами электролитов (в гетрагидрофуране, пропиленкарбонате и др.) и катодными материалами на основе оксида марганца, оксида или сульфида меди (II), фторуглерода  или диоксида серы. Такие элементы характеризуются
или диоксида серы. Такие элементы характеризуются

Рис. XVI. I. Схема кислородно-водородного топливного элемента
высокими разрядным напряжением (2,0-3,0 В) и удельной энергией (200-500 Втч/кг).
Топливные элементы и электрохимические энергоустановки.
Если окислитель и восстановитель хранятся вне элемента и в процессе работы подаются к электродам, которые не расходуются, то элемент может работать длительное время. Такие элементы называют топливными. В топливных элементах химическая энергия восстановителя (топлива) и окислителя, непрерывно и раздельно подаваемых к электродам, непосредственно превращается в электрическую энергию. Удельная энергия топливных элементов зачительно выше гальванических. В топливных элементах используют жидкие или газообразные восстановители (водород, гидразии, метанол, углеводороды) и окислители (кислород и пероксид водорода).
Рассмотрим работу топливного элемента (рис. XVI. 1) на примере кислородно-водородной системы с щелочным электролитом. В таком элементе происходит превращение химической энергии реакции окисления водорода  в электрическую энергию. Топливный элемент состоит из анода
в электрическую энергию. Топливный элемент состоит из анода  катода 3 и ионного проводника 2. К аноду подводится топливо (восстановитель), в данном примере водород, к катоду — окислитель, обычно чистый кислород или кислород воздуха. Схема кислородно-водородного топливного элемента может быть записана в виде
катода 3 и ионного проводника 2. К аноду подводится топливо (восстановитель), в данном примере водород, к катоду — окислитель, обычно чистый кислород или кислород воздуха. Схема кислородно-водородного топливного элемента может быть записана в виде

где М — проводник 1-го рода, играющий роль катализатора электродного процесса и токоотвода. На аноде элемента протекает реакция окисления водорода по уравнению

На катоде восстанавливается кислород

Во внешней цепи происходит движение электронов от аиода к катоду, а в растворе — движение ионов  от катода к аноду. Суммированием уравнений анодной и катодной реакций получаем уравнение токообразующей реакции:
от катода к аноду. Суммированием уравнений анодной и катодной реакций получаем уравнение токообразующей реакции:  . В результате протекания этой реакции в цепи генерируется постоянный ток и химическая энергия непосредственно превращается в электрическую.
. В результате протекания этой реакции в цепи генерируется постоянный ток и химическая энергия непосредственно превращается в электрическую.
Топливные элементы характеризуются  напряжением, мощностью и
напряжением, мощностью и  элемента можно рассчитать по уравнению (VII.3). Например, ЭДС кислородно-водородного топливного элемента при стандартных условиях равна
элемента можно рассчитать по уравнению (VII.3). Например, ЭДС кислородно-водородного топливного элемента при стандартных условиях равна

где  — стандартная энергия Гиббса образования воды при
— стандартная энергия Гиббса образования воды при 
Для большинства топливных элементов ЭДС составляет  Напряжение элементов можно рассчитать по уравнению (XVI.1). Оно возрастает при уменьшении поляризации электродов и омического сопротивления раствора электролита. Снижение поляризации топливного элемента достигается применением катализаторов, увеличением поверхности электродов, повышением температуры и концентрации (или давления) реагентов. Для уменьшения омического сопротивления элемента применяют электролиты с высокой электрической проводимостью.
Напряжение элементов можно рассчитать по уравнению (XVI.1). Оно возрастает при уменьшении поляризации электродов и омического сопротивления раствора электролита. Снижение поляризации топливного элемента достигается применением катализаторов, увеличением поверхности электродов, повышением температуры и концентрации (или давления) реагентов. Для уменьшения омического сопротивления элемента применяют электролиты с высокой электрической проводимостью.
Особую роль в топливных элементах играют электроды, поскольку они определяют электродную поляризацию и соответственно поляризацию элемента. Для увеличения поверхности обычно применяют пористые электроды, изготовленные из мелких порошков металла или угля.
В качестве катализаторов электродов топливных элементов используются металлы платиновой группы, серебро, специально обработанные никель и кобальт и активированный уголь. На этих электродах уже при  удается достичь высоких скоростей восстановления кислорода и окисления таких видов топлива, как водород и гидразин
удается достичь высоких скоростей восстановления кислорода и окисления таких видов топлива, как водород и гидразин  при относительно невысоких поляризациях. Топливные элементы, работающие при таких температурах, называют низкотемпературными. Ионными проводниками в них служат растворы
при относительно невысоких поляризациях. Топливные элементы, работающие при таких температурах, называют низкотемпературными. Ионными проводниками в них служат растворы  или
или  а также ионообменные мембраны.
а также ионообменные мембраны.
Однако природные виды топлива: нефть, природный газ и особенно уголь окисляются в низкотемпературных топливных элементах с очень малыми скоростями, т. е. практически не окисляются. Процесс электроокисления этих видов топлива значительно ускоряется в высокотемпературных топливных элементах, работающих при 500 °С и выше. В таких элементах, естественно, не могут применяться водные растворы электролитов, поэтому используются или расплавленные соли, или твердые ионные проводники — твердые электролиты, например смесь  Основная проблема в разработке высокотемпературных элементов — это повышение срока их службы.
Основная проблема в разработке высокотемпературных элементов — это повышение срока их службы.
Обычно природные виды топлива предварительно обрабатывают для получения электрохимически активных веществ. Например, природный газ обрабатывают водяным паром (паровая конверсия) в присутствии катализаторов. В результате конверсии метана получают газы, содержащие водород, который затем направляется в топливный элемент:

В отличие от гальванических топливные элементы не могут работать без вспомогательных устройств. Для увеличения напряжения и тока элементы соединяют в батареи. При обеспечении непрерывной работы батареи топливных элементов необходимы устройства для подвода реагентов, отвода продуктов реакции и теплоты и др. Установка, состоящая из батарей топливных элементов, систем хранения, обработки и подвода топлива и окислителя, отвода из элементов продуктов реакции, поддержания и регулирования температуры в элементах, а также преобразования тока и напряжения, получила название электрохимической энергоустановки. Уже созданы электрохимические энергоустановки мощностью от десятков ватт до тысяч киловатт. Электрохимические энергоустановки обеспечивают прямое преобразование химической энергии в электрическую и имеют более высокий КПД (примерно в 1,5-2,0 раза) по сравнению с тепловыми машинами. Кроме того, они меньше загрязняют окружающую среду. Наиболее разработаны кислородно-водородные энергоустановки, которые уже применяются на космических кораблях. Они обеспечивают космический корабль и космонавтов не только электроэнергией, но и водой, которая является продуктом реакции в топливном элементе. Удельная энергия этих установок составляет 400-800 Вт-ч/кг, а КПД - 60-70 %.
Построены первые электрохимические электростанции мощностью до 5 МВт, работающие на природном топливе и предназначенные для выравнивания графика нагрузок в энергосетях.
Для широкого применения электрохимических энергоустановок необходимо снизить их стоимость и увеличить срок службы.
Аккумуляторы.
Устройства, в которых электрическая энергия превращается в химическую, а химическая — снова в электрическую, называют аккумуляторами. В аккумуляторах под воздействием внешнего источника тока накапливается (аккумулируется) химическая энергия, которая затем переходит в электрическую энергию. Процессы накопления химической энергии получили название заряда аккумуляторов, процессы превращения химической энергии в электрическую — разряда аккумулятора. При заряде аккумулятор работает как электролизер, при разряде — как гальванический элемент. Процессы заряда аккумуляторов осуществляются многократно.
Аккумулятор в наиболее простом виде имеет два электрода (анод и катод) и ионный проводник между ними. На аноде как при разряде, так и при заряде протекают реакции окисления, на катоде — реакции восстановления. Так как при разряде аккумулятор работает как гальванический элемент, то разрядные характеристики его описываются уравнениями (XVI. 1) — (XVI.5). Напряжение аккумулятора при разряде меньше ЭДС из-за поляризации и омических потерь. Емкость аккумулятора зависит от природы и количества реагентов (активных масс) и уменьшается при увеличении плотности тока из-за снижения степени использования активных масс. Емкость также может
падать при хранении из-за побочных реакций (саморазряда). Поскольку при заряде аккумулятор работает как электролизер, то его напряжение описывается уравнением для электролизера [см. уравнение (VII.21)]. Напряжение аккумулятора при заряде выше ЭДС и возрастает с увеличением плотности тока.
В процессе разряда и заряда изменяется состав активных масс аккумулятора и соответственно ЭДС и напряжение. Разрядное напряжение уменьшается, а зарядное напряжение возрастает во времени. Кривые изменения напряжения аккумулятора во времени называют разрядными и зарядными кривыми.
В аккумуляторах могут применяться химические реакции, которые при заряде и разряде протекают обратимо с большими скоростями и малыми потерями на побочные процессы. Аккумулятор должен иметь высокую емкость, применяемые материалы должны быть доступными и недорогими.
В настоящее время наиболее распространенными являются свинцовые аккумуляторы, в которых в качестве электролита используется раствор  поэтому они называются еще кислотными. Электроды кислотного аккумулятора представляют собой свинцовые решетки, погруженные в электролит
поэтому они называются еще кислотными. Электроды кислотного аккумулятора представляют собой свинцовые решетки, погруженные в электролит  Решетки вначале заполняются оксидом свинца, который при взаимодействии с
Решетки вначале заполняются оксидом свинца, который при взаимодействии с  превращается в
превращается в  При работе аккумулятора из одном электроде (аноде) протекают реакции, при которых степень окисления свинца меняется от
При работе аккумулятора из одном электроде (аноде) протекают реакции, при которых степень окисления свинца меняется от  до 0 и обратно:
до 0 и обратно:

а на другом электроде (катоде) степень окисления свинца меняется от  до
до  и обратно:
и обратно:

Суммарная реакция в аккумуляторе

ЭДС аккумулятора, равная разности потенциалов электродов, может быть рассчитана по уравнению

где  В результате заряда активная масса одного электрода превращается из
В результате заряда активная масса одного электрода превращается из  в
в  а активная масса второго электрода из
а активная масса второго электрода из  превращается в
превращается в  Так как ЭДС аккумулятора зависит от концентрации серной кислоты, которая при заряде аккумулятора возрастает, то растет и ЭДС аккумулятора. Можно было бы увеличить ЭДС аккумулятора путем заливки его концентрированной серной кислотой, однако при повышении концентрации
Так как ЭДС аккумулятора зависит от концентрации серной кислоты, которая при заряде аккумулятора возрастает, то растет и ЭДС аккумулятора. Можно было бы увеличить ЭДС аккумулятора путем заливки его концентрированной серной кислотой, однако при повышении концентрации
 свыше
свыше  уменьшается ее электрическая проводимость и растет растворимость свинца, поэтому оптимальными являются
уменьшается ее электрическая проводимость и растет растворимость свинца, поэтому оптимальными являются  растворы
растворы  Напряжение при заряде выше ЭДС и растет в течение заряда. В конце заряда напряжение достигает значения, достаточного для электролиза воды, тогда начинается выделение водорода и кислорода:
Напряжение при заряде выше ЭДС и растет в течение заряда. В конце заряда напряжение достигает значения, достаточного для электролиза воды, тогда начинается выделение водорода и кислорода:

В конце заряда происходит только электролиз воды, поэтому выделение пузырьков газа («кипение») служит признаком окончания заряда свинцового аккумулятора.
При разряде аккумулятора падает его ЭДС и напряжение. Первоначально напряжение изменяется относительно мало. Однако при напряжении ниже 1,7 В  темп уменьшения напряжения возрастает. При этом на электродах образуется неактивная пленка
темп уменьшения напряжения возрастает. При этом на электродах образуется неактивная пленка  особой кристаллической структуры (происходит так называемое сульфатирование), которая изолирует активную массу электрода от электролита. Вследствие этого рекомендуется проводить разряд аккумулятора до напряжения не ниже 1,7 В.
особой кристаллической структуры (происходит так называемое сульфатирование), которая изолирует активную массу электрода от электролита. Вследствие этого рекомендуется проводить разряд аккумулятора до напряжения не ниже 1,7 В.
Свинцовый аккумулятор обладает существенными достоинствами: высоким КПД (около  высокой ЭДС и относительно малым ее изменением при разряде, простотой и невысокой ценой. Недостатки свинцовых аккумуляторов: небольшая удельная энергия
высокой ЭДС и относительно малым ее изменением при разряде, простотой и невысокой ценой. Недостатки свинцовых аккумуляторов: небольшая удельная энергия  саморазряд аккумулятора при хранении и малый срок службы (2—5 лет). Свинцовые аккумуляторы широко используют на электростанциях, телефонных узлах, на железных дорогах, подводных лодках, самолетах, автомобилях, электрокарах и других устройствах.
саморазряд аккумулятора при хранении и малый срок службы (2—5 лет). Свинцовые аккумуляторы широко используют на электростанциях, телефонных узлах, на железных дорогах, подводных лодках, самолетах, автомобилях, электрокарах и других устройствах.
Промышленность выпускает также щелочные аккумуляторы. Наиболее распространенные из них никель-кадмиевые и никель-железные аккумуляторы. Положительный электрод содержит гидроксид никеля, отрицательный электрод — соответственно кадмий или железо. Ионным проводником служит 20-23 %-ный раствор КОН. Суммарные реакции в наиболее простом виде можно записать уравнениями:

Все реагенты, кроме воды, находятся в твердом состоянии, поэтому ЭДС аккумуляторов мало изменяется при заряде и разряде. Однако из-за поляризации и омических потерь напряжение аккумуляторов при заряде растет, а при разряде уменьшается. Активные массы аккумуляторов или помещаются в перфорированные коробки-ламели (ламельные аккумуляторы), или готовятся методом прессования и спекания (безламельные аккумуляторы).
К достоинствам никель-кадмиевых и никель-железных аккумуляторов относятся большой срок службы (до 10 лет) и высокая механическая прочность, к недостаткам — невысокие  Никель-железные аккумуляторы дешевле никель-кадмиевых, но имеют несколько худшие показатели на единицу массы. Они применяются для питания электрокар, погрузчиков и рудничных электровозов. Никель-кадмиевые аккумуляторы используются для питания аппаратуры связи, радиоприемников, магнитофонов и различной электронной аппаратуры.
Никель-железные аккумуляторы дешевле никель-кадмиевых, но имеют несколько худшие показатели на единицу массы. Они применяются для питания электрокар, погрузчиков и рудничных электровозов. Никель-кадмиевые аккумуляторы используются для питания аппаратуры связи, радиоприемников, магнитофонов и различной электронной аппаратуры.
В последние годы разработаны никель-водородные аккумуляторы, в которых отрицательным электродом является водородный, аналогичный электроду топливного элемента. При заряде аккумулятора водород собирается в баллон, при разряде расходуется из этого баллона. Такие аккумуляторы имеют достаточно высокую удельную энергию 
Промышленность выпускает также щелочные серебряно-цинковые аккумуляторы, у которых окислителем служит оксид серебра, а восстановителем — цинк. Удельная энергия этого аккумулятора относительно велика  однако он дорог и имеет малый срок службы, поэтому применяется ограниченно.
однако он дорог и имеет малый срок службы, поэтому применяется ограниченно.
Проводятся исследования по совершенствованию существующих и созданию новых аккумуляторов. Это в значительной степени обусловлено необходимостью создания электромобилей, не дающих вредных выбросов в окружающую среду. В настоящее время в Советском Союзе и других странах уже создано несколько моделей электромобилей со свинцовыми аккумуляторами. Однако эти электромобили имеют малый пробег между зарядами аккумулятора (до 60 км) из-за невысокого значения его удельной энергии. Такие электромобили могут использоваться, если пробег за день невелик (грузовые фургоны, машины коммунального хозяйства). Необходимо создать недорогой аккумулятор, удельная энергия которого значительно превышала бы удельную энергию свинцового аккумулятора.
Разработаны никель-цинковые аккумуляторы, в которых отрицательным электродом служит цинк, а положительным электродом — гидроксид никеля. Удельная энергия около  что обеспечивает пробег электромобиля без заряда 100—150 км. Ведется разработка серно-натриевого аккумулятора с твердым электролитом. Отрицательным электродом служит натрий, положительным — сера в смеси с графитом, электролитом — соединение
что обеспечивает пробег электромобиля без заряда 100—150 км. Ведется разработка серно-натриевого аккумулятора с твердым электролитом. Отрицательным электродом служит натрий, положительным — сера в смеси с графитом, электролитом — соединение  , обладающее нонной (по Na) проводимостью. Удельная энергия аккумулятора достигает
, обладающее нонной (по Na) проводимостью. Удельная энергия аккумулятора достигает  .
.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
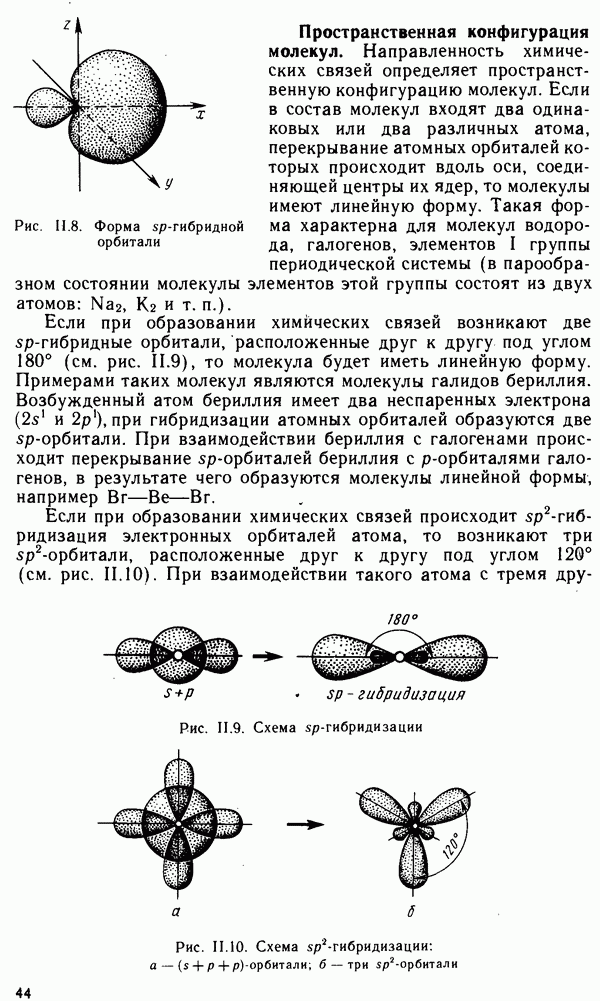
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
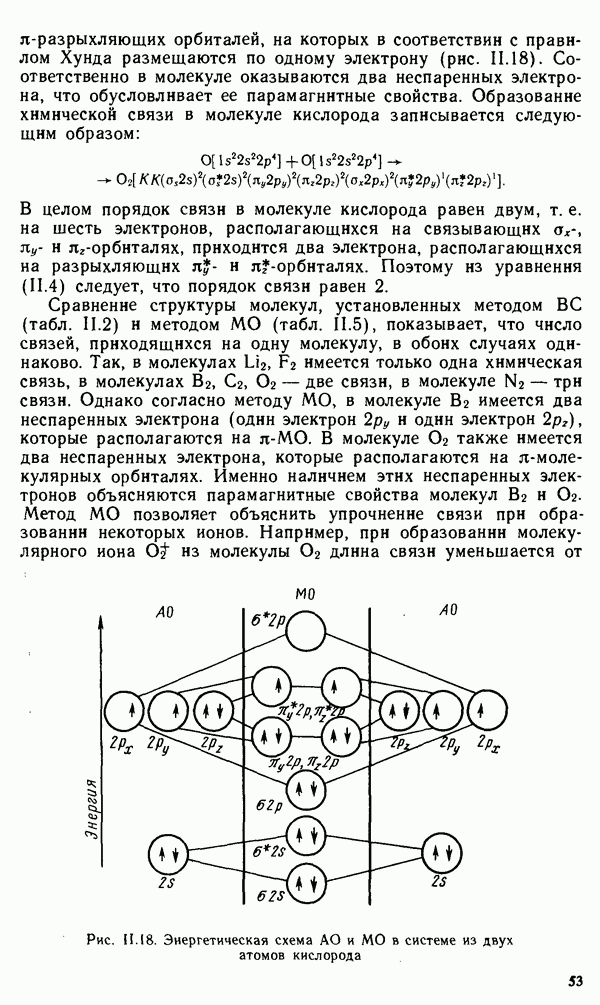
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
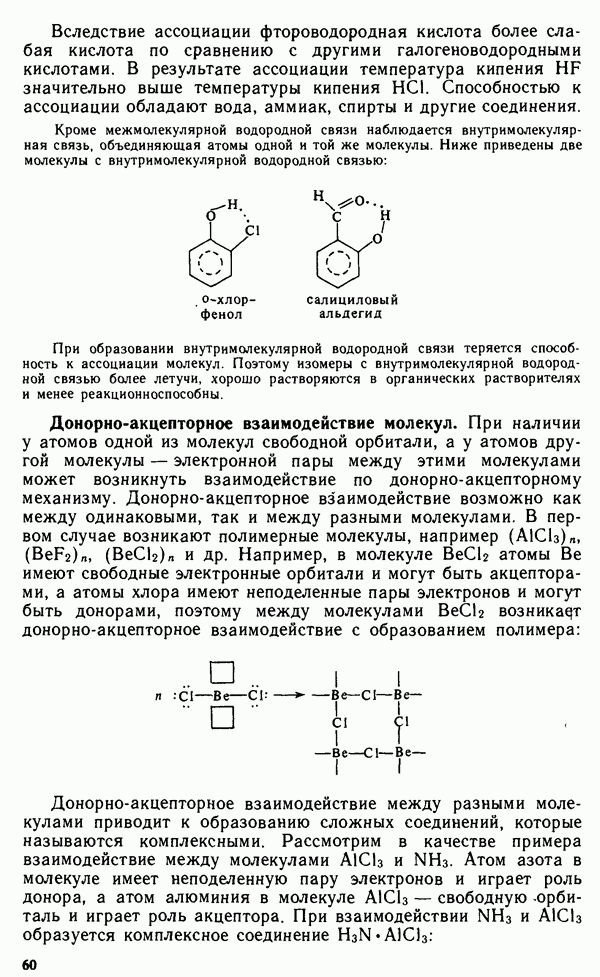
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
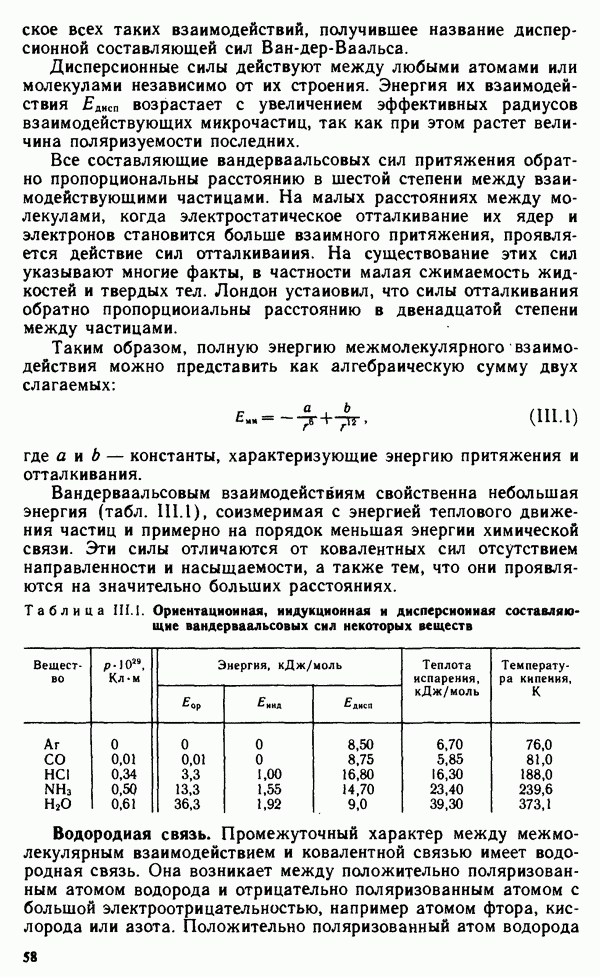
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
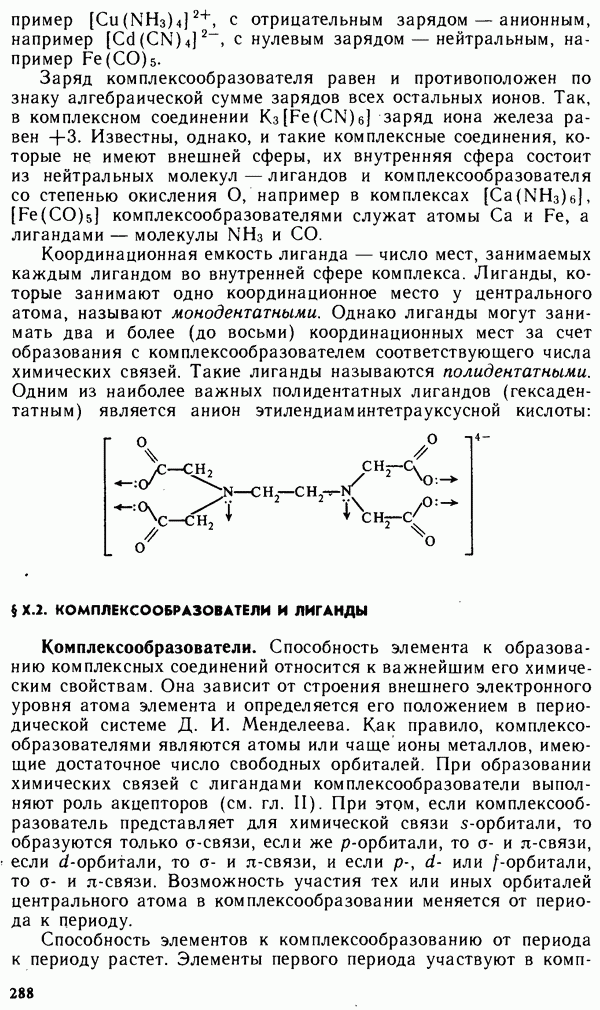
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
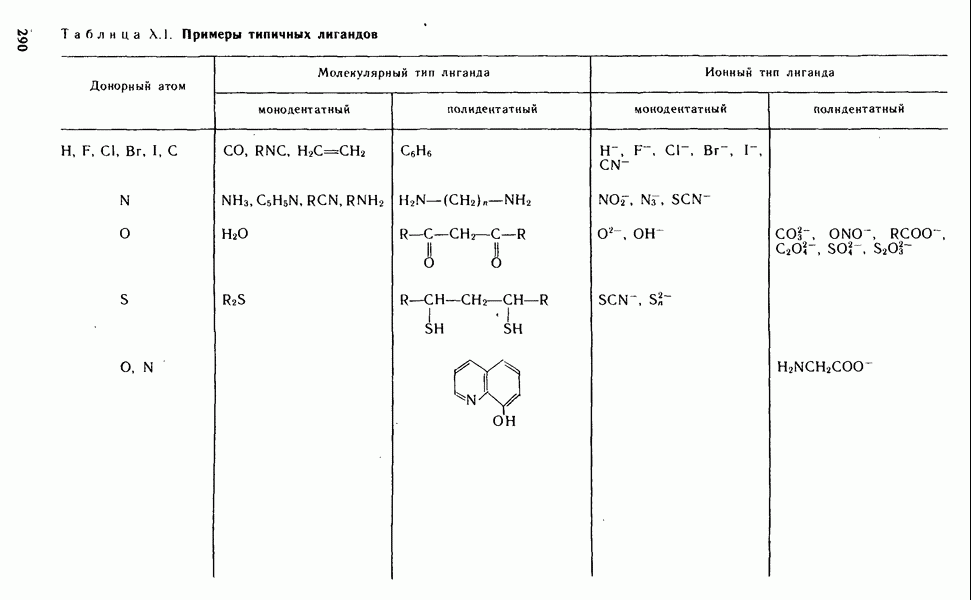
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
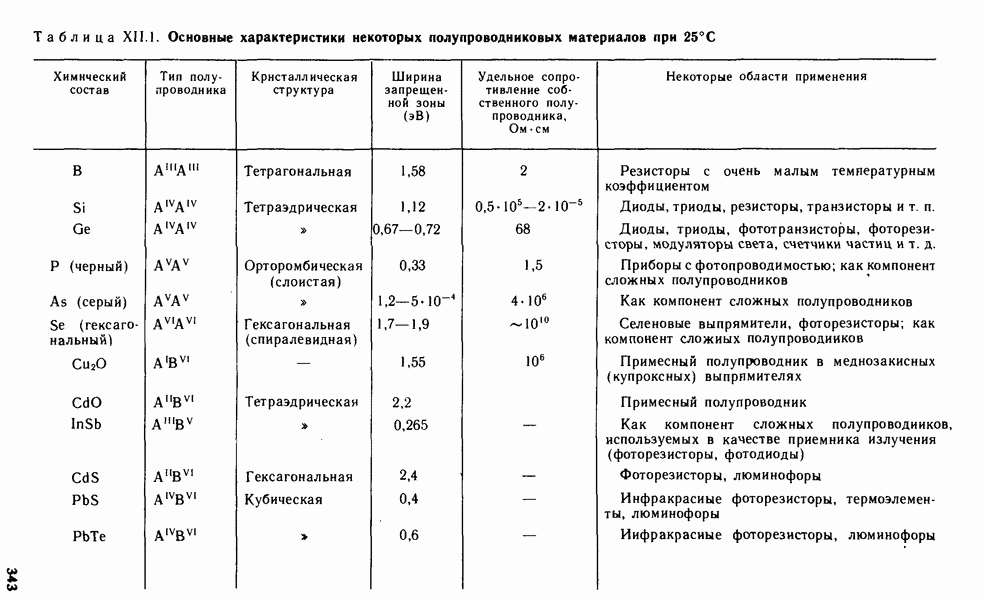
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
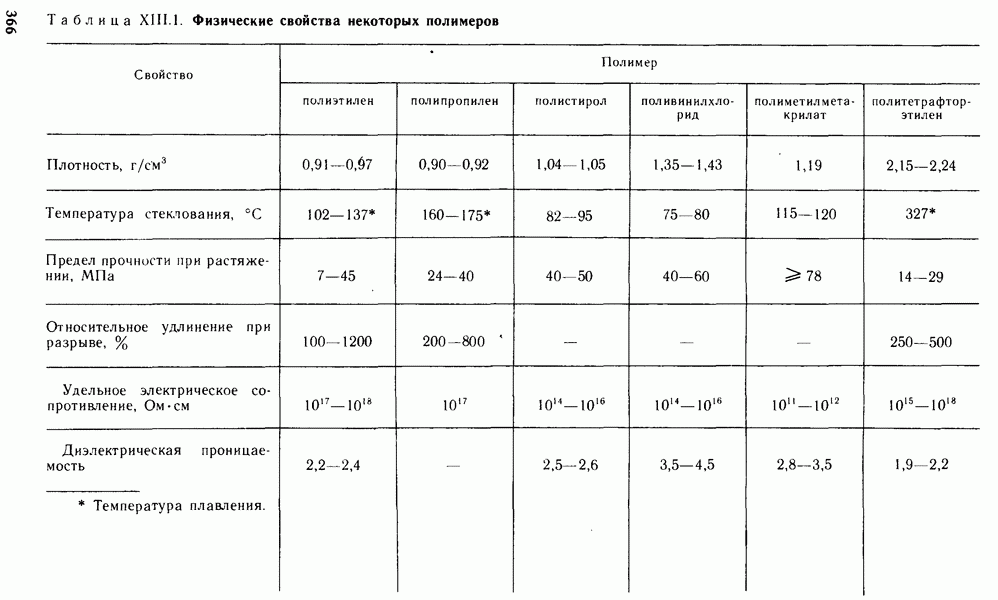
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
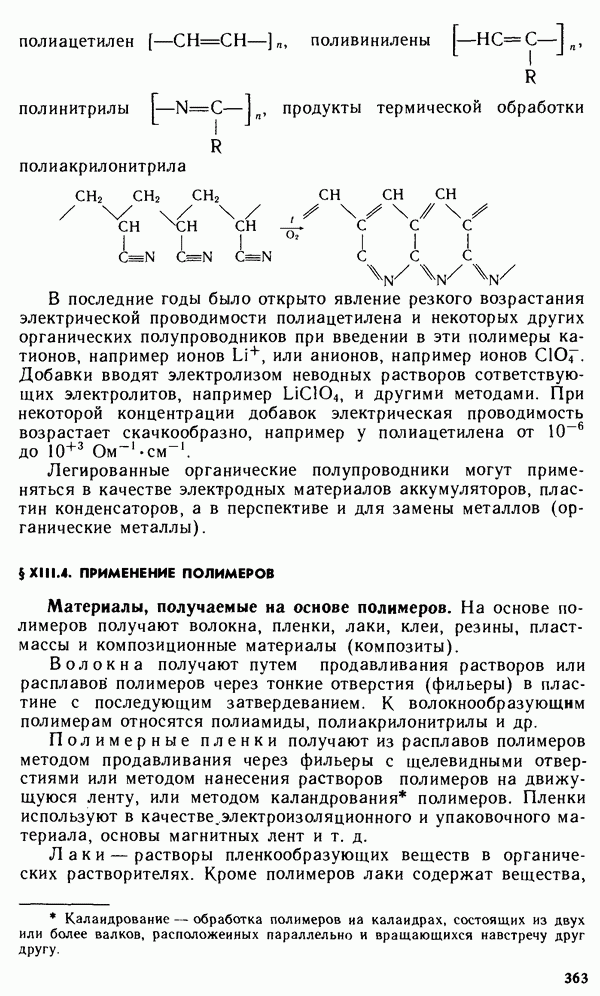
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ