| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
В первых трех главах было рассмотрено строение вещества, взаимодействие между ядром и электронами, между атомами, ионами и молекулами.
Важной задачей химии является изучение процессов превращения веществ — химических реакций. В данной главе будут рассмотрены энергетические эффекты и направление химических реакций, возможность или невозможность самопроизвольного протекания химических процессов. Так как эти вопросы входят в круг задач, изучаемых химической термодинамикой, то вначале рассмотрим некоторые общие понятия этой науки: внутренняя энергия и энтальпия системы: термохимические законы и расчеты; энтальпия образования химических соединений и т. п.
§ IV.1. ОСНОВНЫЕ ПОНЯТИЯ И ВЕЛИЧИНЫ В ХИМИЧЕСКОЙ ТЕРМОДИНАМИКЕ. ВНУТРЕННЯЯ ЭНЕРГИЯ И ЭНТАЛЬПИЯ СИСТЕМЫ
Химическая термодинамика
изучает переходы химической энергии в другие формы — тепловую, электрическую и т. п., устанавливает количественные законы этих переходов, а также направление и пределы самопроизвольного протекания химических реакций при заданных условиях.Объектом изучения в термодинамике является система. Системой называется совокупность находящихся во взаимодействии веществ, мысленно (или фактически) обособленная от окружающей среды. Различают гомогенные и гетерогенные системы. Гомогенные системы состоят из одной фазы, гетерогенные — из двух или нескольких фаз. Фаза — это часть системы, однородная во всех точках по составу и свойствам и отделенная от других частей системы поверхностью раздела. Примером гомогенной системы может служить водный раствор сульфата меди или нитрата калия. Но если раствор насыщен и на дне сосуда есть кристаллы солей, то рассматриваемая система гетерогенна. Другим примером гомогенной системы может служить вода, но вода с плавающим в ней льдом — система гетерогенная.
Одна и та же система может находиться в различных состояниях. Каждое состояние системы характеризуется определенным набором значений термодинамических параметров. К термодинамическим параметрам относятся температура, давление, плотность, концентрация и т. п. Изменение хотя бы только одного термодинамического параметра приводит к изменению состояния системы в целом. Термодинамическое состояние системы называют равновесным, если оно характеризуется постоянством термодинамических параметров во всех точках системы и не изменяется самопроизвольно (без затраты работы).
В химической термодинамике свойства системы рассматриваются в ее равновесных состояниях. Представим, что некоторая система Y переходит из равновесного состояния I, характеризующегося температурой  и давлением в равновесное состояние 2, характеризующееся температурой
и давлением в равновесное состояние 2, характеризующееся температурой  и давлением
и давлением  Изучение скорости процесса перехода системы Y из равновесного состояния 1 в равновесное состояние 2 и его молекулярного механизма — область химической кинетики. Химическая термодинамика изучает систему в двух равновесных состояниях (конечном и начальном) и на этом основании определяет возможность (или невозможность) самопроизвольного течения процесса при заданных условиях в указанном направлении, характеризует энергетические изменения, происходящие в результате перехода, устанавливает значения температуры, давления, концентраций веществ в системе, при которых достигается максимальный выход продуктов реакции, и решает еще целый ряд очень важных вопросов. В зависимости от условий перехода системы из одного
Изучение скорости процесса перехода системы Y из равновесного состояния 1 в равновесное состояние 2 и его молекулярного механизма — область химической кинетики. Химическая термодинамика изучает систему в двух равновесных состояниях (конечном и начальном) и на этом основании определяет возможность (или невозможность) самопроизвольного течения процесса при заданных условиях в указанном направлении, характеризует энергетические изменения, происходящие в результате перехода, устанавливает значения температуры, давления, концентраций веществ в системе, при которых достигается максимальный выход продуктов реакции, и решает еще целый ряд очень важных вопросов. В зависимости от условий перехода системы из одного
состояния в другое в термодинамике различают изотермические, изобарические, изохорические и адиабатические процессы. Первые — протекают при постоянной температуре  вторые — при постоянном давлении
вторые — при постоянном давлении  третьи — при постоянном объеме
третьи — при постоянном объеме  четвертые — в условиях отсутствия обмена теплотой между системой и окружающей средой
четвертые — в условиях отсутствия обмена теплотой между системой и окружающей средой 
Химические реакции часто протекают в изобарно-изотермических условиях  Такие условия соблюдаются, когда взаимодействия между веществами осуществляются в открытых сосудах без нагревания или при более высокой, но постоянной температуре. Иногда для химических реакций соблюдаются изохорно-изотермические условия
Такие условия соблюдаются, когда взаимодействия между веществами осуществляются в открытых сосудах без нагревания или при более высокой, но постоянной температуре. Иногда для химических реакций соблюдаются изохорно-изотермические условия 
Внутренняя энергия системы.
При переходе системы из одного состояния в другое изменяются некоторые ее свойства, в частности внутренняя энергия 
Внутренняя энергия системы представляет собой ее полную энергию, которая складывается из кинетической и потенциальной энергий молекул, атомов, атомных ядер и электронов. Внутренняя энергия включает в себя энергию поступательного, вращательного и колебательного движений, а также потенциальную энергию, обусловленную силами притяжения и отталкивания, действующими между молекулами, атомами и внутриатомными частицами. Она не включает потенциальную энергию положения системы в пространстве и кинетическую энергию движения системы как целого.
Абсолютная внутренняя энергия системы не может быть определена, однако можно измерить ее изменение  при переходе из одного состояния в другое. Величина
при переходе из одного состояния в другое. Величина  считается положительной
считается положительной  если в каком-либо процессе внутренняя энергия системы возрастает.
если в каком-либо процессе внутренняя энергия системы возрастает.
Внутренняя энергия является термодинамической функцией состояния системы. Это значит, что всякий раз, когда система оказывается в данном состоянии, ее внутренняя энергия принимает определенное присущее этому состоянию значение. Следовательно, изменение внутренней энергии не зависит от пути и способа перехода системы из одного состояния в другое и определяется разностью значений внутренней энергии системы в этих двух состояниях:

где  — внутренняя энергия системы в конечном и начальном состояниях соответственно.
— внутренняя энергия системы в конечном и начальном состояниях соответственно.
Теплота и работа.
Система может обмениваться с внешней средой веществом и энергией в форме теплоты  и работы А. Если этого обмена нет, то систему называют изолированной. Теплота и работа характеризуют качественно и количественно две различные формы передачи энергии от одного тела к другому.
и работы А. Если этого обмена нет, то систему называют изолированной. Теплота и работа характеризуют качественно и количественно две различные формы передачи энергии от одного тела к другому.
Теплота является мерой энергии, переданной от одного тела к другому, за счет разницы температур этих тел. Эта форма
передачи энергии связана с хаотическими столкновениями молекул соприкасающихся тел. При соударениях молекулы более нагретого тела передают энергию молекулам менее нагретого тела. Переноса вещества при этом не происходит.
Работа является мерой энергии, переданной от одного тела к другому за счет перемещения масс под действием каких-либо сил.
Теплоту и работу измеряют в джоулях или килоджоулях. В химической термодинамике считают положительными теплоту, подводимую к системе, и работу, которую система совершает против внешних сил. Теплота и работа не являются функциями состояния системы и имеют значение только в процессе перехода системы из одного состояния в другое. Количество поглощенной (или выделенной) в процессе теплоты и совершенной работы зависят от способа проведения процесса, т. е. теплота и работа — функции пути.
Первый закон термодинамики.
В любом процессе соблюдается закон сохранения энергии, выражаемый равенством

которое означает, что теплота  подведенная к системе, расходуется на увеличение ее внутренней энергии
подведенная к системе, расходуется на увеличение ее внутренней энергии  и на совершение системой работы А над внешней средой. Уравнение
и на совершение системой работы А над внешней средой. Уравнение  математическое выражение первого закона термодинамики.
математическое выражение первого закона термодинамики.
Из первого закона термодинамики следует, что приращение внутренней энергии системы  в любом процессе равно количеству сообщенной системе теплоты
в любом процессе равно количеству сообщенной системе теплоты  за вычетом количества совершенной системой работы
за вычетом количества совершенной системой работы  ; поскольку величины
; поскольку величины  и А поддаются непосредственному измерению, с помощью уравнения (IV.2) всегда можно рассчитать значение
и А поддаются непосредственному измерению, с помощью уравнения (IV.2) всегда можно рассчитать значение 
В первом законе термодинамики под работой А подразумевают сумму всех видов работы против сил, действующих на систему со стороны внешней среды. В эту сумму могут входить и работа против сил внешнего электрического поля, и работа против сил гравитационного поля, и работа расширения против сил внешнего давления, и другие виды работ.
Энтальпия системы.
В связи с тем что для химических взаимодействий наиболее характерна работа расширения, ее обычно выделяют из общей суммы:

где А — все виды работы, кроме работы расширения;  — внешнее давление;
— внешнее давление;  — изменение объема системы, равное разности
— изменение объема системы, равное разности  — объем продуктов реакции,
— объем продуктов реакции,  — объем исходных веществ).
— объем исходных веществ).
Еслн при протекании того или иного процесса работа расширения является единственным видом работы, уравнение (IV.3) принимает вид

Тогда математическое выражение первого закона термодинамики (IV.2) запишется так:

где  — теплота, подведенная к системе при постоянном давлении.
— теплота, подведенная к системе при постоянном давлении.
С учетом того, что  уравнение (IV.5) можно преобразовать, сгруппировав величины
уравнение (IV.5) можно преобразовать, сгруппировав величины  и V по индексам, относящимся к конечному и начальному состояниям системы:
и V по индексам, относящимся к конечному и начальному состояниям системы:

Сумму  называют энтальпией системы и обозначают буквой
называют энтальпией системы и обозначают буквой 

Подставив энтальпию Н в уравнение (IV.6), получим

т. е. теплота, подведенная к системе при постоянном давлении, расходуется на приращение энтальпии системы
Так же как и для внутренней энергии, абсолютное значение энтальпии системы определить экспериментально невозможно, но можно, измерив величину  найти изменение энтальпии
найти изменение энтальпии  при переходе системы из одного состояния в другое. Величину
при переходе системы из одного состояния в другое. Величину  считают положительной
считают положительной  еслиэнтальпия системы возрастает. Поскольку значение
еслиэнтальпия системы возрастает. Поскольку значение  определяется разностью
определяется разностью  и не зависит от пути и способа проведения процесса, энтальпию, как и внутреннюю энергию, относят к термодинамическим функциям состояния системы.
и не зависит от пути и способа проведения процесса, энтальпию, как и внутреннюю энергию, относят к термодинамическим функциям состояния системы.
Термодинамические функции состояния характеризуют термодинамические свойства вещества. К их числу наряду с внутренней энергией  и энтальпией Н относятся энтропия
и энтальпией Н относятся энтропия  энергия Гельмгольца
энергия Гельмгольца  и энергия Гиббса
и энергия Гиббса  Значения этих функций связаны с особенностями состава и внутреннего строения вещества, а также с внешними условиями: давлением, температурой, концентрацией растворенных веществ и т. п. Термодинамические функции состояния являются экстенсивными свойствами: их величины зависят от количества вещества. Именно поэтому
Значения этих функций связаны с особенностями состава и внутреннего строения вещества, а также с внешними условиями: давлением, температурой, концентрацией растворенных веществ и т. п. Термодинамические функции состояния являются экстенсивными свойствами: их величины зависят от количества вещества. Именно поэтому  и
и  принято относить к одному молю вещества и выражать в
принято относить к одному молю вещества и выражать в  имея в виду, что и объем V в произведении
имея в виду, что и объем V в произведении  [см. уравнение (IV.7)] — молярный объем газообразного вещества.
[см. уравнение (IV.7)] — молярный объем газообразного вещества.
Если химическая реакция идет в автоклаве (изохорический процесс;  и система не совершает работы, в том числе
и система не совершает работы, в том числе
и работы расширения, так как  то вся подведенная к системе теплота расходуется на приращение ее внутренней энергии:
то вся подведенная к системе теплота расходуется на приращение ее внутренней энергии:

| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
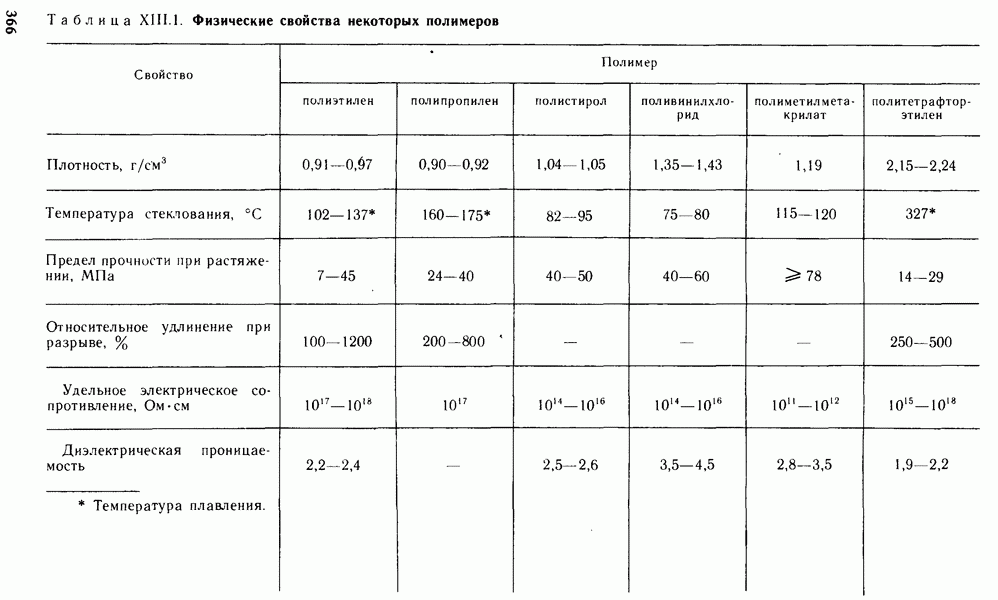
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
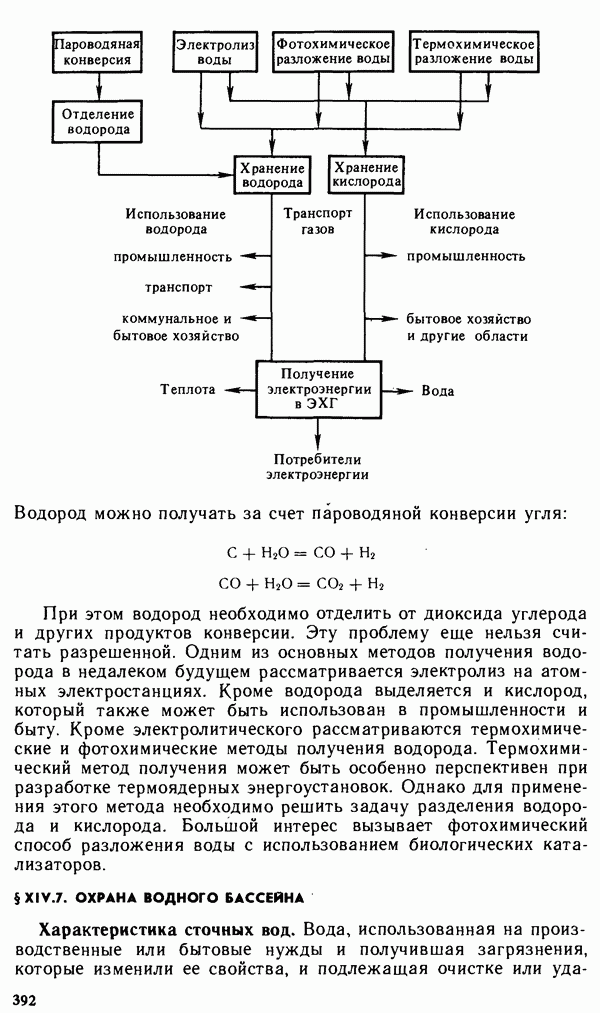
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ