| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
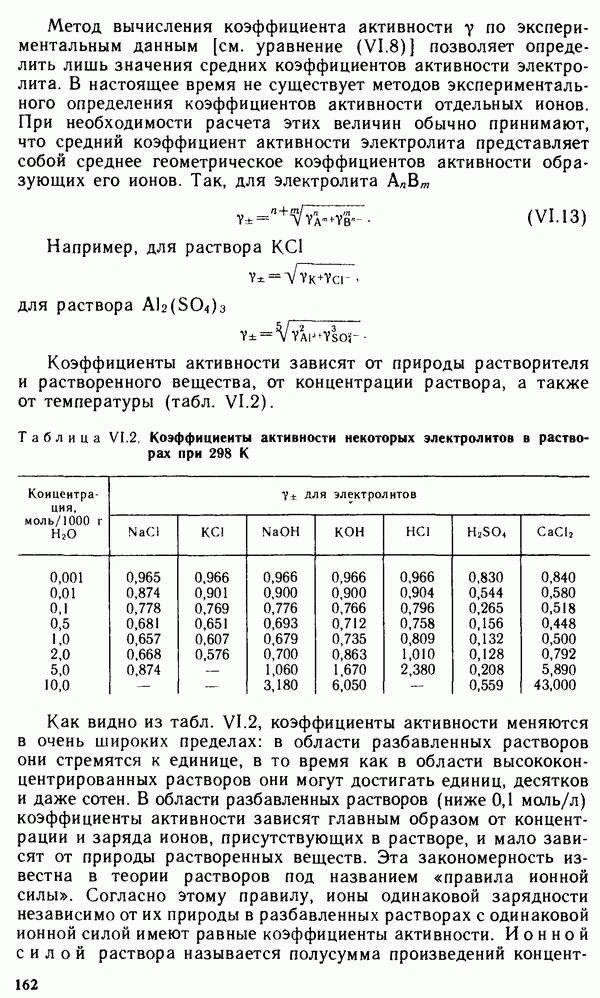
§ 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
Рассмотрим, используя метол  возникновение связей в некоторых гомоядерных молекулах, образуемых первыми 10 элементами периодической системы. Образование молекулы
возникновение связей в некоторых гомоядерных молекулах, образуемых первыми 10 элементами периодической системы. Образование молекулы  двух атомов водорода, каждый
двух атомов водорода, каждый  которых имеет по одному 1s-электрону, отражает следующая запись:
которых имеет по одному 1s-электрону, отражает следующая запись:

Два электрона в молекуле  занимают одну связывающую молекулярную орбиталь, образующуюся из 1s-атомных орбиталей. Наличие двух электронов на одной молекулярной орбитали отражено в записи
занимают одну связывающую молекулярную орбиталь, образующуюся из 1s-атомных орбиталей. Наличие двух электронов на одной молекулярной орбитали отражено в записи  верхним индексом. Молекула
верхним индексом. Молекула  стабильна, так как оба ее электрона занимают только связывающую
стабильна, так как оба ее электрона занимают только связывающую  -орбиталь, энергия которой меньше энергии орбиталей
-орбиталь, энергия которой меньше энергии орбиталей
отдельных атомов, порядок связи равен 1. При взаимодействии двух атомов гелия, каждый  которых содержит по два
которых содержит по два  -электрона, на
-электрона, на  должны разместиться четыре электрона. На основании принципа Паули на связывающей орбитали может разместиться только два электрона, поэтому два других электрона в молекуле
должны разместиться четыре электрона. На основании принципа Паули на связывающей орбитали может разместиться только два электрона, поэтому два других электрона в молекуле  должны разместиться на
должны разместиться на  энергия которой больше энергии
энергия которой больше энергии  По уравнению (11.4) можно легко подсчитать, что порядок связи равен нулю, т. е. химическая связь не возникает и молекула не может быть устойчивой. Согласно методу
По уравнению (11.4) можно легко подсчитать, что порядок связи равен нулю, т. е. химическая связь не возникает и молекула не может быть устойчивой. Согласно методу  достаточно устойчивыми являются молекулярные ноны и Не? Образование частицы из атома водорода Н, в котором имеется? один
достаточно устойчивыми являются молекулярные ноны и Не? Образование частицы из атома водорода Н, в котором имеется? один  -электрон, и иона водорода
-электрон, и иона водорода  не содержащего электронов, может быть представлено записью
не содержащего электронов, может быть представлено записью

Эта запись показывает, что из  образуется одна связывающая
образуется одна связывающая  порядок связи равен
порядок связи равен 
Молекулярный ион Н обнаружен экспериментально. Длина связи у этого нона 0,106 нм, а энергия связи  Увеличение длины связи и уменьшение энергии связи у частицы
Увеличение длины связи и уменьшение энергии связи у частицы  по сравнению с длиной (0,074 нм) и энергией связи
по сравнению с длиной (0,074 нм) и энергией связи  молекулы
молекулы  обусловлено уменьшением порядка связи с 1 до
обусловлено уменьшением порядка связи с 1 до  Рассмотрим образование частицы Не? из атома гелия, содержащего два
Рассмотрим образование частицы Не? из атома гелия, содержащего два  -электрона, и нона гелия, содержащего один
-электрона, и нона гелия, содержащего один  -электрон:
-электрон:

При этом на  надо разместить три электрона, два
надо разместить три электрона, два  которых заполняют связывающую
которых заполняют связывающую  а третий разместится на разрыхляющей
а третий разместится на разрыхляющей  (в соответствии с рядом уровней энергии
(в соответствии с рядом уровней энергии  Таким образом, частица
Таким образом, частица  будет иметь электронное строение:
будет иметь электронное строение: 
Порядок связи у молекулярного нона равен  и он может быть достаточно устойчив. Экспериментально доказано существование этого нона.
и он может быть достаточно устойчив. Экспериментально доказано существование этого нона.
Рассмотрим заполнение  на примере кислорода, молекула которого
на примере кислорода, молекула которого  образуется из атомов, содержащих по два
образуется из атомов, содержащих по два  -электрона, по два
-электрона, по два  -электрона и по четыре
-электрона и по четыре  -электрона. Электронная конфигурация
-электрона. Электронная конфигурация  Атомные орбитали первого энергетического уровня образуют
Атомные орбитали первого энергетического уровня образуют  создавая остов молекулы. Эти заполненные
создавая остов молекулы. Эти заполненные  обозначают буквой К.
обозначают буквой К.
 -Электроны второго энергетического уровня перейдут с
-Электроны второго энергетического уровня перейдут с  на
на  с образованием одной
с образованием одной  -связывающей и одной
-связывающей и одной  -разрыхляющей орбиталей, р-Электроны второго энергетического уровня (в соответствии с порядком возрастания энергии связи) перейдут с трех
-разрыхляющей орбиталей, р-Электроны второго энергетического уровня (в соответствии с порядком возрастания энергии связи) перейдут с трех  на
на  с образованием одной
с образованием одной  -связывающей
-связывающей  на которой размещаются два электрона с
на которой размещаются два электрона с  образованием двух
образованием двух  -связывающнх
-связывающнх  на которых размещаются четыре электрона с
на которых размещаются четыре электрона с  и образованием двух
и образованием двух
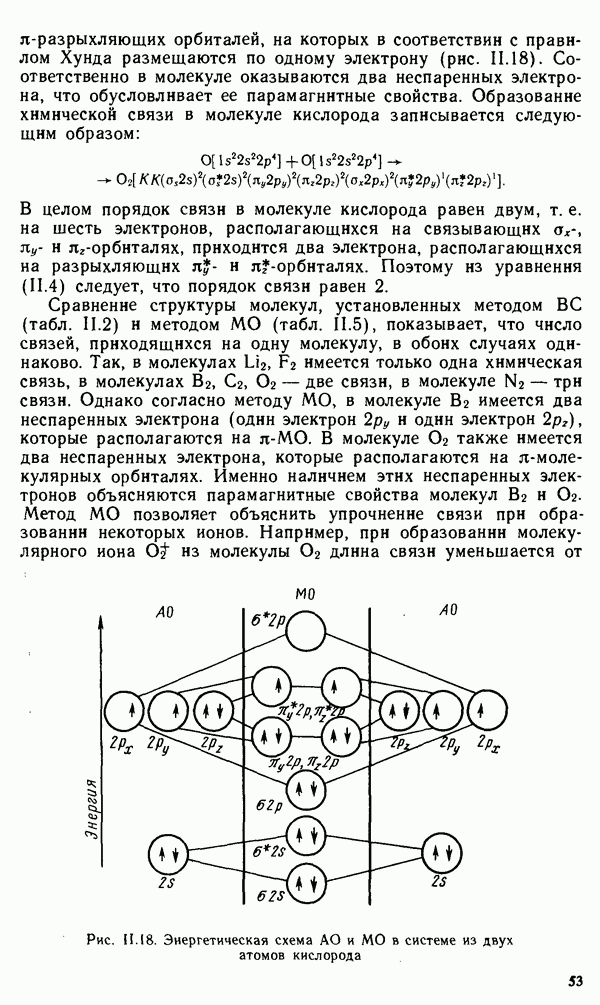
 -разрыхляющих орбиталей, на которых в соответствии с правилом Хунда размещаются по одному электрону (рис. 11.18). Соответственно в молекуле оказываются два неспаренных электрона, что обусловливает ее парамагнитные свойства. Образование химической связи в молекуле кислорода записывается следующим образом:
-разрыхляющих орбиталей, на которых в соответствии с правилом Хунда размещаются по одному электрону (рис. 11.18). Соответственно в молекуле оказываются два неспаренных электрона, что обусловливает ее парамагнитные свойства. Образование химической связи в молекуле кислорода записывается следующим образом:

В целом порядок связи в молекуле кислорода равен двум, т. е. на шесть электронов, располагающихся на связывающих  и
и  -орбиталях, приходится два электрона, располагающихся на разрыхляющих
-орбиталях, приходится два электрона, располагающихся на разрыхляющих  и
и  -орбнталях. Поэтому из уравнения (11.4) следует, что порядок связи равен 2.
-орбнталях. Поэтому из уравнения (11.4) следует, что порядок связи равен 2.
Сравнение структуры молекул, установленных методом  (табл. 11.2) и методом
(табл. 11.2) и методом  (табл. 11.5), показывает, что число связей, приходящихся на одну молекулу, в обоих случаях одинаково. Так, в молекулах
(табл. 11.5), показывает, что число связей, приходящихся на одну молекулу, в обоих случаях одинаково. Так, в молекулах  имеется только одна химическая связь, в молекулах
имеется только одна химическая связь, в молекулах  — две связи, в молекуле
— две связи, в молекуле  — три связи. Однако согласно методу
— три связи. Однако согласно методу  в молекуле
в молекуле  имеется два неспаренных электрона (один электрон
имеется два неспаренных электрона (один электрон  и один электрон
и один электрон  которые располагаются на
которые располагаются на  . В молекуле
. В молекуле  также имеется два неспаренных электрона, которые располагаются на
также имеется два неспаренных электрона, которые располагаются на  -молекулярных орбиталях. Именно наличием этих неспаренных электронов объясняются парамагнитные свойства молекул
-молекулярных орбиталях. Именно наличием этих неспаренных электронов объясняются парамагнитные свойства молекул  Метод
Метод  позволяет объяснить упрочнение связи при образовании некоторых ионов. Например, при образовании молекулярного иона О из молекулы
позволяет объяснить упрочнение связи при образовании некоторых ионов. Например, при образовании молекулярного иона О из молекулы  длина связи уменьшается от
длина связи уменьшается от

Рис. 11.18. Энергетическая схема  и
и  в системе из двух атомов кислорода
в системе из двух атомов кислорода
0,121 до 0,112 нм, а энергия связи увеличивается от 494 до  Упрочнение связи обусловлено удалением электрона с разрыхляющей
Упрочнение связи обусловлено удалением электрона с разрыхляющей  -орбитали и соответственно увеличением порядка связи с 2 до 2,5. Энергия связи в молекулярном ноне
-орбитали и соответственно увеличением порядка связи с 2 до 2,5. Энергия связи в молекулярном ноне  значительно больше энергии связи в молекуле
значительно больше энергии связи в молекуле  Возрастание энергии связи объясняется удалением электрона с разрыхляющей
Возрастание энергии связи объясняется удалением электрона с разрыхляющей  -орбитали, что увеличивает порядок связи с 1 до 1,5.
-орбитали, что увеличивает порядок связи с 1 до 1,5.
Данные об энергии связи в молекулярных нонах являются ярким подтверждением справедливости метода  . Метод
. Метод  позволяет рассмотреть и строение гетероядерных двух- и многоатомных молекул. Например, образование молекулы
позволяет рассмотреть и строение гетероядерных двух- и многоатомных молекул. Например, образование молекулы  можно представить схемой
можно представить схемой

Как и для молекулы азота, на  внешнего энергетического уровня молекулы
внешнего энергетического уровня молекулы  находятся 10 электронов, в том числе 8 электронов на связывающих
находятся 10 электронов, в том числе 8 электронов на связывающих  и 2 электрона на разрыхляющих
и 2 электрона на разрыхляющих  Порядок связи в молекуле
Порядок связи в молекуле  как и в молекуле
как и в молекуле  равен 3. Это обусловливает сходство в свойствах азота и оксида углерода: длина связи 0,110 и 0,113 нм, энергия связи 940 и
равен 3. Это обусловливает сходство в свойствах азота и оксида углерода: длина связи 0,110 и 0,113 нм, энергия связи 940 и  температура плавления 63 и 66 К соответственно.
температура плавления 63 и 66 К соответственно.
Таблица II.5. Электронные конфигурации и параметры связи гомоядерных двухатомных молекул и ионов согласно методу МО

Таким образом, с помощью метода молекулярных орбиталей успешно объясняют свойства различных молекул. Этот метод важен тем, что позволяет получить данные о свойствах молекул исходя из соответствующих характеристик атомов. Метод МО не исключает метода валентных связей, оба метода взаимно дополняют друг друга. В целом оба метода (и ВС, и МО) служат квантово-механическим обоснованием и дальнейшим развитием теории химического строения А. М. Бутлерова.
КОНТРОЛЬНЫЕ ВОПРОСЫ
(см. скан)
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
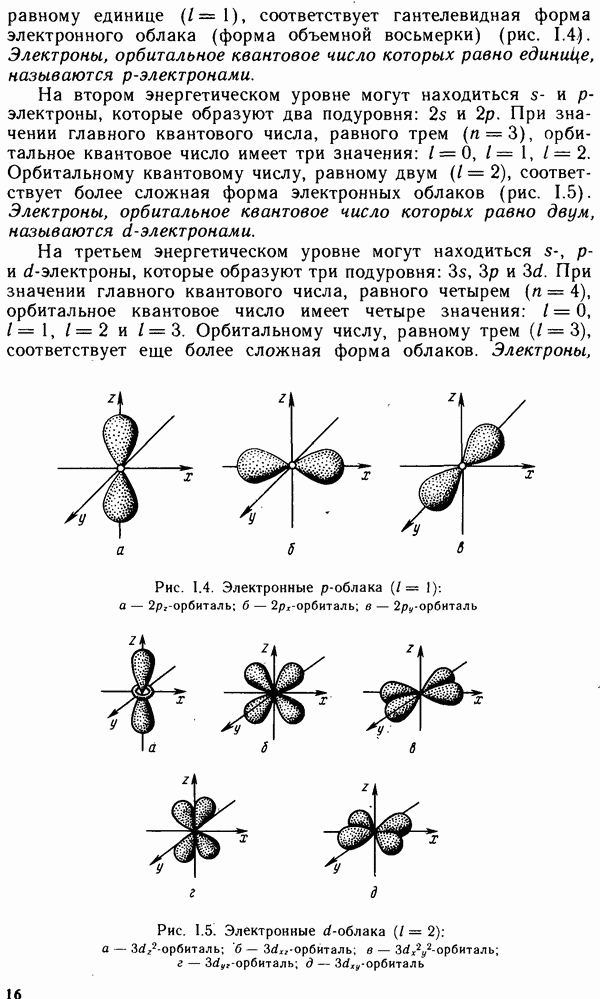
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
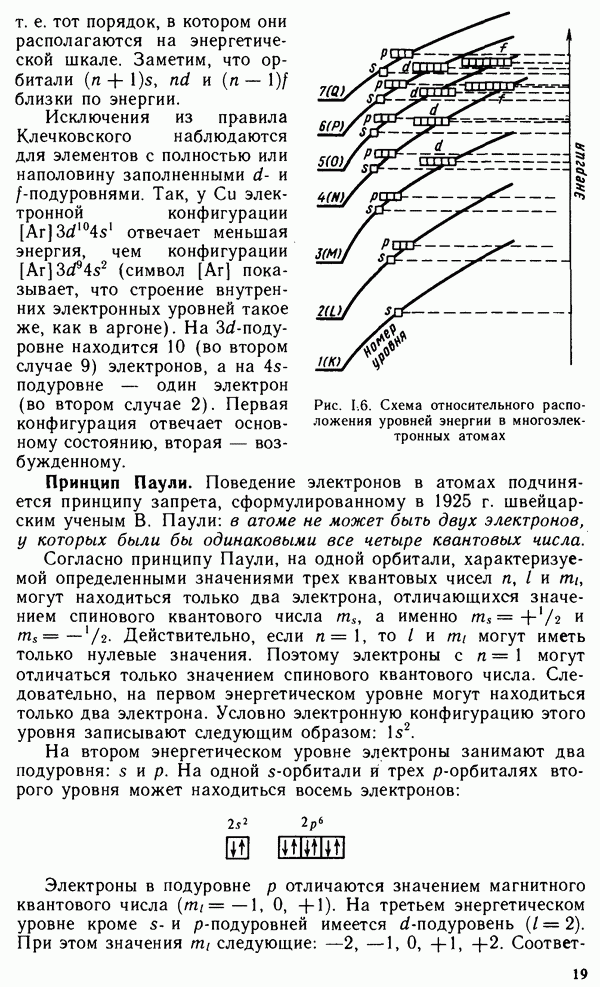
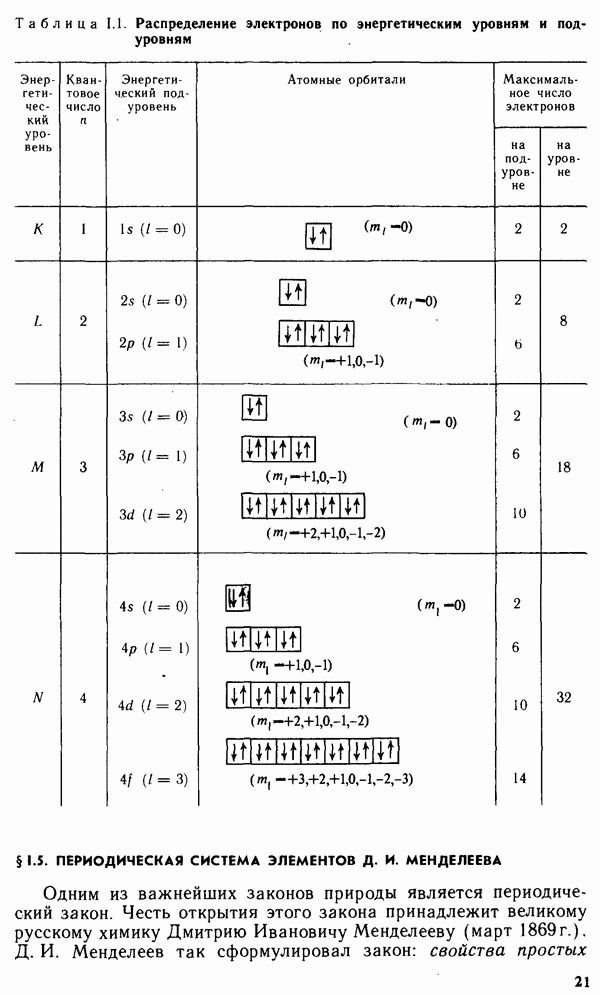
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
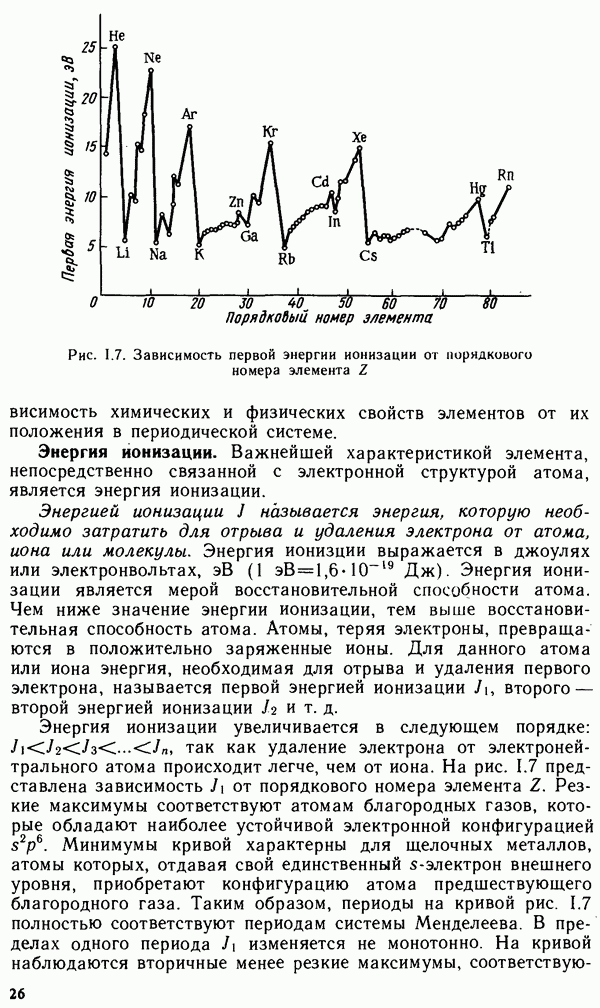
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
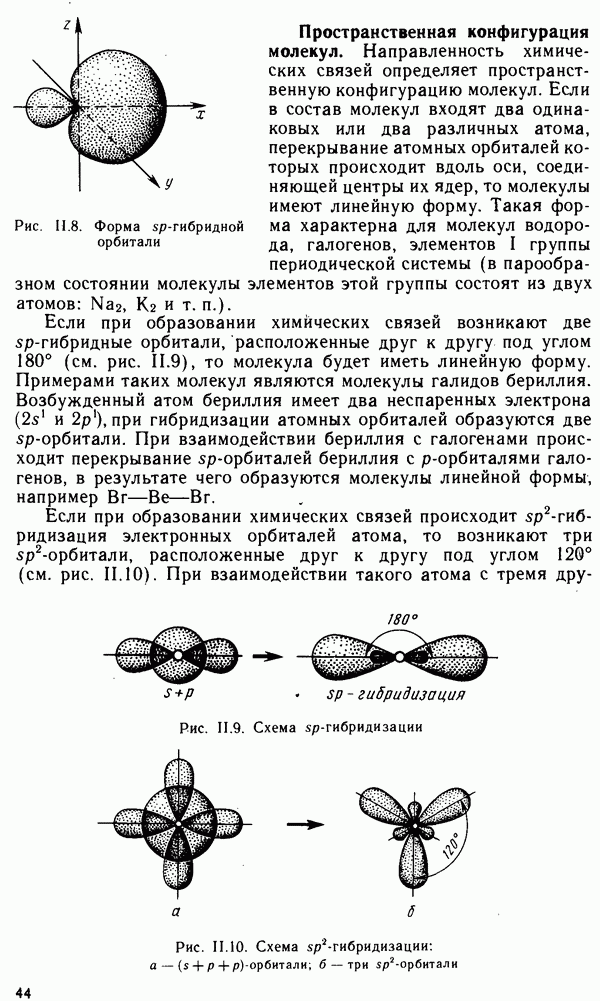
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
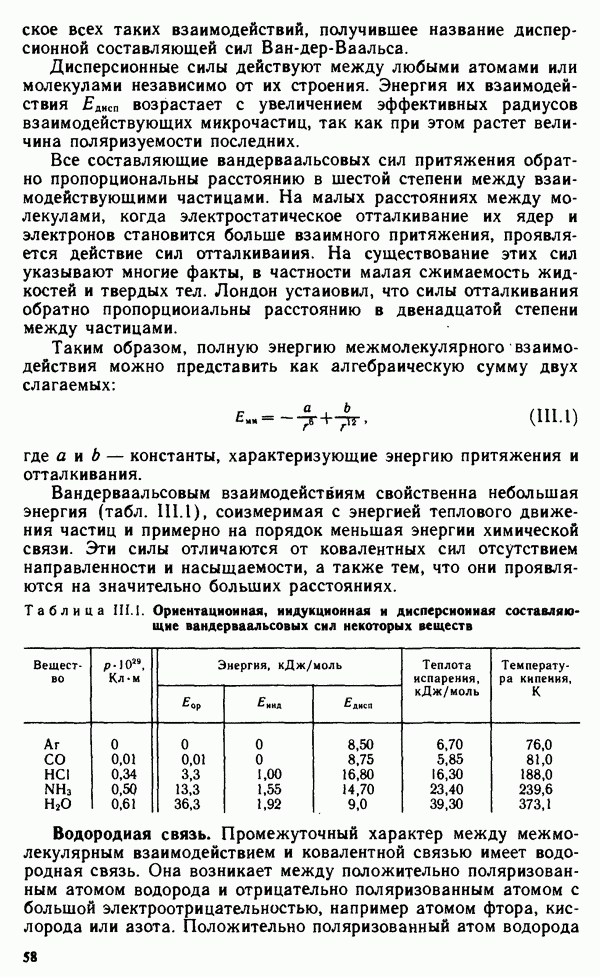
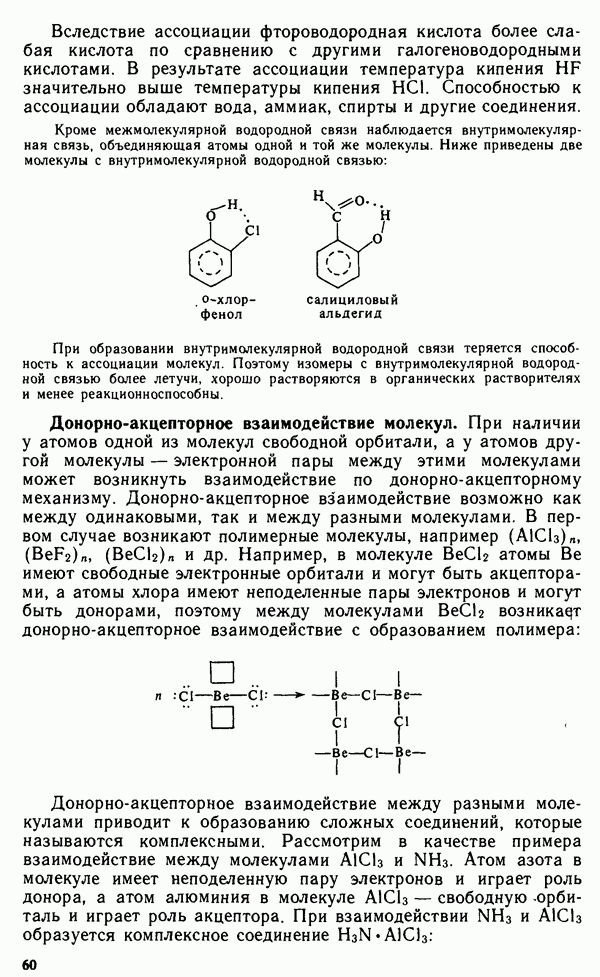
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
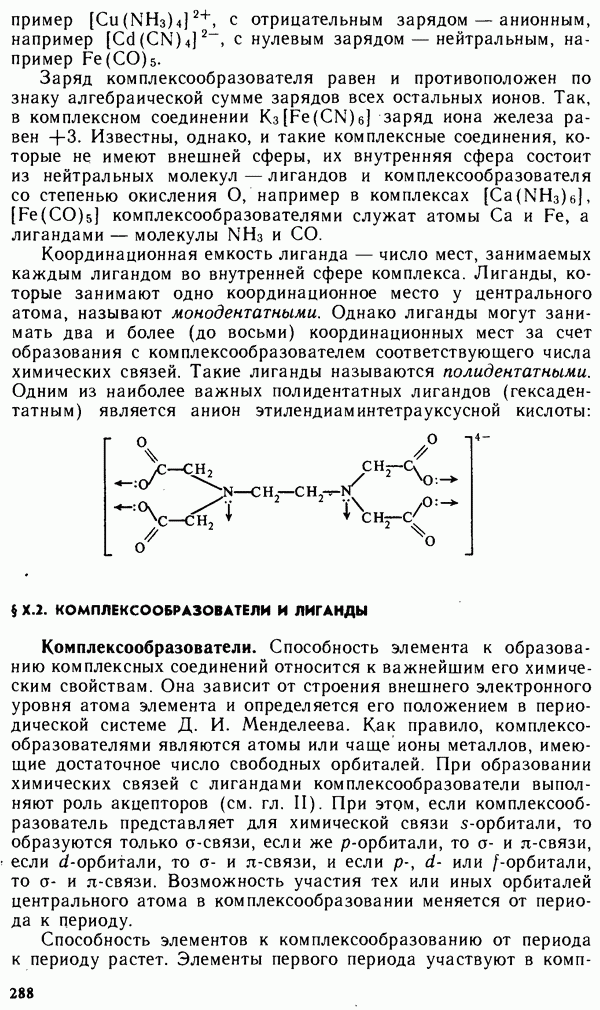
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
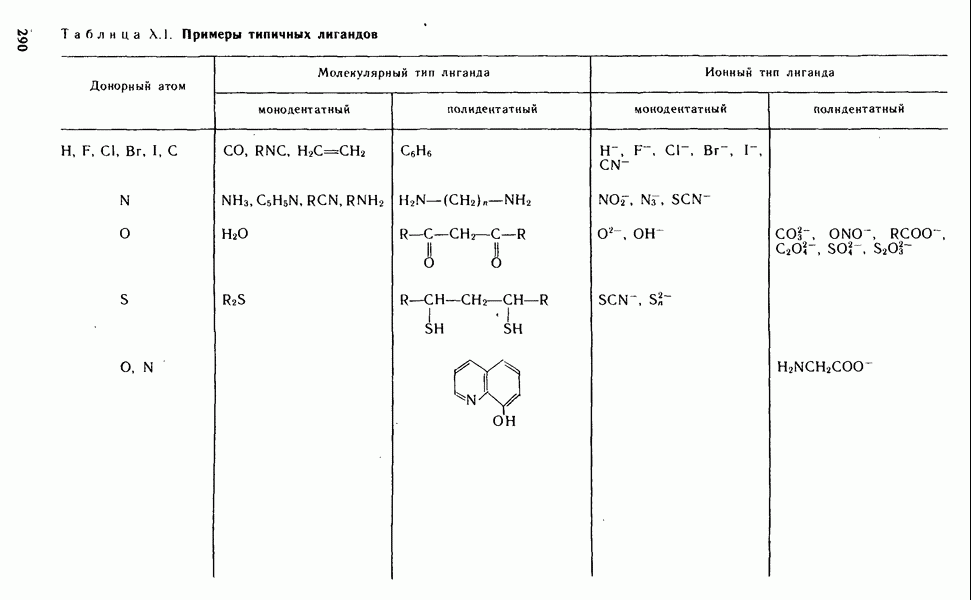
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
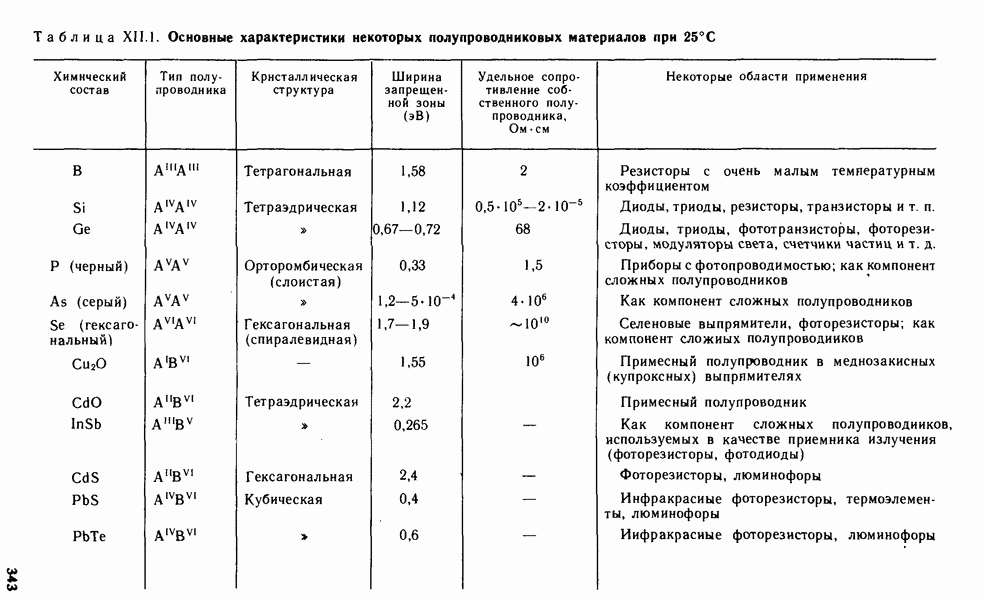
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
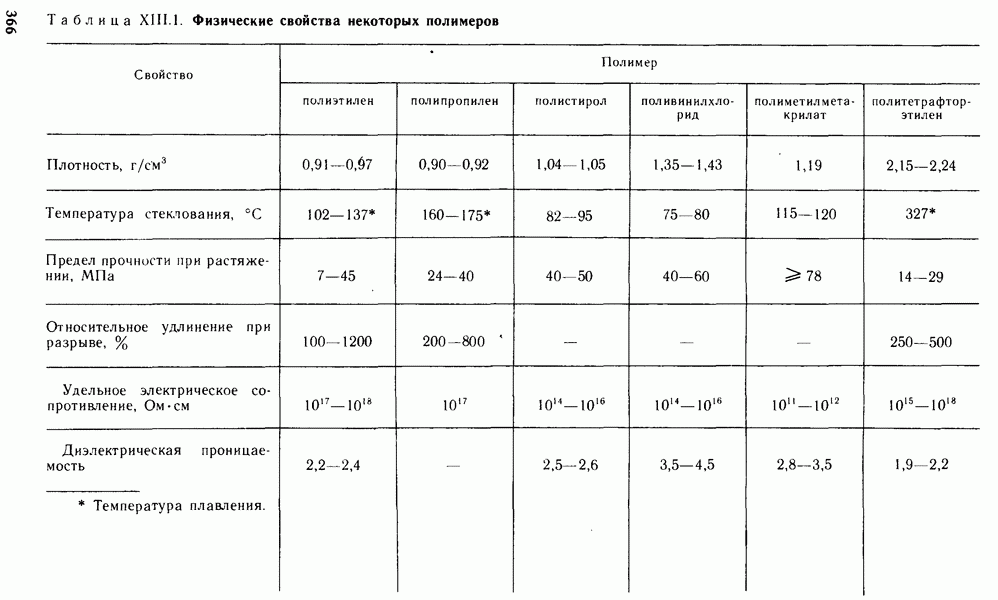
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
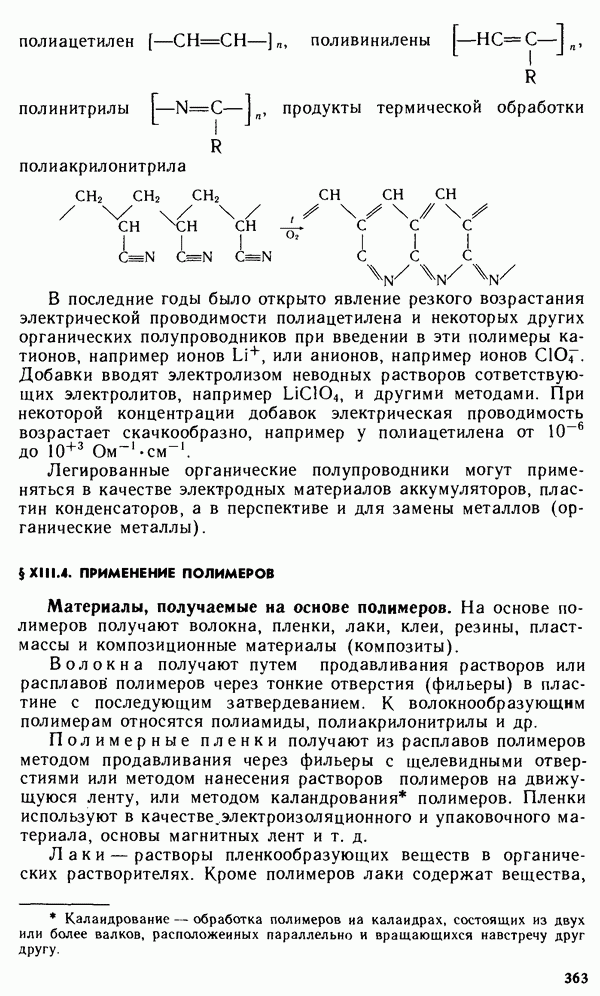
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ