| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
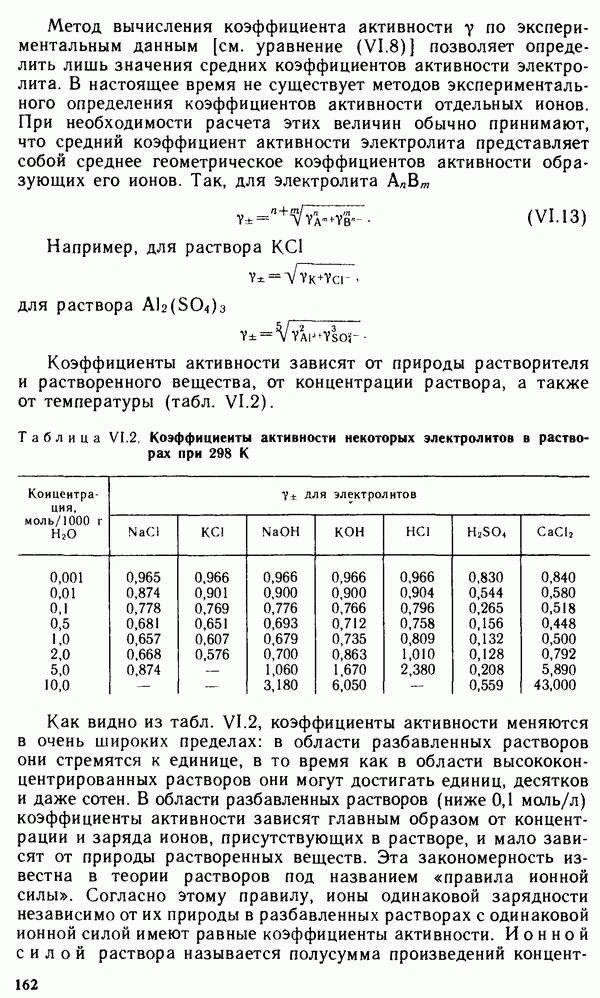
Для изменения размеров и формы, а также состояния поверхности металлических изделий используют электрохимические способы обработки, при которых производится электроокисление металлических изделий: электрохимическая размерная обработка, электрохимическое полирование и анодирование.
Электрохимическая размерная обработка металлов и сплавов.
Анодная обработка изделий для придания им требуемой формы получила название электрохимической обработки металлов (ЭХОМ). Этот способ обработки металлов во многих случаях имеет важные достоинства, так как позволяет обрабатывать детали сложной конфигурации и металлы, которые механически или вообще не могут быть обработаны, или обрабатываются с большим трудом (например, очень твердые металлы и сплавы). Кроме того, инструмент (катод) при этом не изнашивается, а обработка не влечет изменения структуры металла. К недостаткам ЭХОМ относится большой расход энергии, поэтому этот метод не применяется для обработки обычных металлов, сплавов и изделий простой конфигурации. Как и при обычном электролизе с растворимыми анодами, при ЭХОМ происходит анодное растворение металла:  На катоде, который при электрохимической обработке называют инструментом, обычно выделяется водород:
На катоде, который при электрохимической обработке называют инструментом, обычно выделяется водород: 
Особенностью ЭХОМ по сравнению с другими методами электролиза является высокая скорость растворения металлов. Плотность тока при электрохимической обработке металлов в сотни и тысячи раз выше плотности тока других электрохимических процессов. Для обеспечения высоких скоростей процесса (высоких плотностей тока) при относительно невысоких напряжениях необходимо снизить омическое падение напряжения и поляризацию электродов. Омическое падение напряжения уменьшается снижением зазора между электродами (до 0,1 мм) и использованием раствора электролита с высокой электрической проводимостью.
К особенности анодных процессов относится пассивность металлов, при которой резко падает скорость анодного растворения металла, несмотря на увеличение анодной поляризации. Как видно из рис. XVI.6, при увеличении анодной поляризации растет плотность анодного тока. При некоторой поляризации, равной  потенциал анода становится равным потенциалу
потенциал анода становится равным потенциалу

Рис. XVI.6. Поляризационная кривая металлического анода при пассивации металла
пассивации  после этого анодный ток начинает резко уменьшаться до минимального значения
после этого анодный ток начинает резко уменьшаться до минимального значения  . Скорость анодного процесса начинает снова возрастать лишь после достижения потенциала
. Скорость анодного процесса начинает снова возрастать лишь после достижения потенциала  при котором начинается новый процесс, например выделение кислорода. Всю анодную кривую можно разделить на несколько областей. В области
при котором начинается новый процесс, например выделение кислорода. Всю анодную кривую можно разделить на несколько областей. В области  происходит активное растворение металла, в области
происходит активное растворение металла, в области  — пассивация металла и падение скорости процесса, в области
— пассивация металла и падение скорости процесса, в области  — пассивное состояние металла, при котором скорость анодного растворения очень мала, и в области
— пассивное состояние металла, при котором скорость анодного растворения очень мала, и в области  протекает новый анодный процесс. Причиной пассивности металлов является адсорбция кислорода, образование оксидных пленок на поверхности металла или действие обоих факторов. Из-за наличия адсорбированного кислорода или оксидной пленки растворение металла тормозится.
протекает новый анодный процесс. Причиной пассивности металлов является адсорбция кислорода, образование оксидных пленок на поверхности металла или действие обоих факторов. Из-за наличия адсорбированного кислорода или оксидной пленки растворение металла тормозится.
Для предотвращения пассивации металла процесс необходимо вести в активной области, т. е. снижать анодную поляризацию. Существенную роль при электрохимической обработке металлов играет концентрационная поляризация, так как при высоких скоростях растворения металла и малом расстоянии между электродами может происходить быстрое изменение концентрации продуктов реакции в межэлектродном пространстве. Для снижения концентрационной поляризации и предотвращения пассивации анода необходимо принудительно с высокой скоростью выводить продукты анодного растворения металла из зазора между анодом и катодом.
Схема электрохимической обработки металла представлена на рис. XVI.7. Обрабатываемое изделие служит анодом и растворяется при прохождении тока. К отрицательному полюсу источника тока подключается катод (инструмент), обычно изготавливаемый из стали. На катоде выделяется водород. Между электродами сохраняется небольшой зазор, по мере растворения анода передвигают катод, чтобы сохранить малое расстояние между анодом и катодом. В зазор между электродами подается под давлением раствор электролита, в данной установке через полость в центре катода. Раствор электролита выносит из межэлектродного пространства продукты анодного растворения и газообразные продукты катодной реакции. Последние затем удаляются в атмосферу, а продукты растворения тем или иным способом выводятся из раствора электролита. В качестве растворов электролитов для обработки сталей и многих цветных металлов (никель, медь, кобальт, титан) и их сплавов применяется раствор  ; для обработки алюминия, цинка, олова и
; для обработки алюминия, цинка, олова и

Рис. XVI.7. Схема электрохимической обработки металла: 1 — раствор электролита; 2 — катод (инструмент); 3 — анод (изделие)
их сплавов — раствор  для обработки молибдена и вольфрама — раствор NaOH.
для обработки молибдена и вольфрама — раствор NaOH.
В настоящее время ЭХОМ используется для обработки лопаток турбин, штампов и пресс-форм, твердых и тугоплавких металлов и сплавов, получения и обработки отверстий и полостей, для фрезерования, точения и шлифования различных изделий, заточки инструмента.
Электрохимическое полирование
представляет собой анодную обработку металла для создания ровной и блестящей поверхности. Изделие, имеющее микро- и макронеровности, является анодом электролизера. Катодом служит металл, химически не растворимый в растворе электролита. В качестве растворов электролитов используют растворы фосфорной, хромовой, серной, уксусной, плавиковой кислот и др. В процессе электрополировки происходит анодное растворение металла на макро- и микровыступах, в результате чего поверхность становится гладкой и блестящей. На катоде выделяется водород. Механизм электрополировки окончательно не выяснен. Эффект электрополирования обычно связывается с действием вязкой пленки, образующейся в прианодном слое, затрудняющем растворение металла в углублениях по сравнению с растворением на выступах, а также поочередным пассивированием и активированием металла.
По сравнению с механической полировкой электрополировка менее трудоемка, лучше поддается автоматизации, позволяет обрабатывать металлы, которые трудно полировать механически. Кроме того, при электрополировке не происходит искажения структуры металла. Электрополировка широко используется для изучения структуры металлов и сплавов, а также в промышленности для обработки нержавеющей и углеродистой сталей, никеля, алюминия, меди и ее сплавов.
Анодное оксидирование (анодирование)
широко применяется для обработки алюминия. Алюминиевое изделие играет роль анода электролизера. Электролитом служит раствор серной, хромовой, борной или щавелевой кислот, катодом может быть металл, не взаимодействующий с раствором электролита, например свинец. На катоде выделяется водород, на аноде происходит образование оксида алюминия  . Суммарный процесс на аноде можно представить следующим уравнением:
. Суммарный процесс на аноде можно представить следующим уравнением:

Механизм реакции имеет сложный характер. Электродная реакция протекает в несколько стадий. Наряду с образованием оксида происходит его частичное растворение в кислоте:

В результате пленка становится пористой, через поры пленки проникают ионы и процесс роста пленки продолжается. Полученная пленка  имеет ценные свойства. Она весьма пориста, причем размеры пор очень малы. Вследствие этого пленка может быть пропитана различными составами, повышающими коррозионную стойкость поверхности. Красители также могут придать поверхности разнообразную окраску, что используется при декоративной обработке алюминия.
имеет ценные свойства. Она весьма пориста, причем размеры пор очень малы. Вследствие этого пленка может быть пропитана различными составами, повышающими коррозионную стойкость поверхности. Красители также могут придать поверхности разнообразную окраску, что используется при декоративной обработке алюминия.
Оксидная пленка весьма тверда, поэтому после анодирования повышается износостойкость металла. Пленка  имеет высокое электросопротивление. Так, на алюминии высокой чистоты удается получить пленки с удельным электросопротивлением 1014 Ом «см. Поэтому оксидирование используется для получения изолирующих слоев на алюминиевых лентах, применяемых в конденсаторах.
имеет высокое электросопротивление. Так, на алюминии высокой чистоты удается получить пленки с удельным электросопротивлением 1014 Ом «см. Поэтому оксидирование используется для получения изолирующих слоев на алюминиевых лентах, применяемых в конденсаторах.
Кроме алюминия производят также электрохимическое оксидирование магния и меди.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
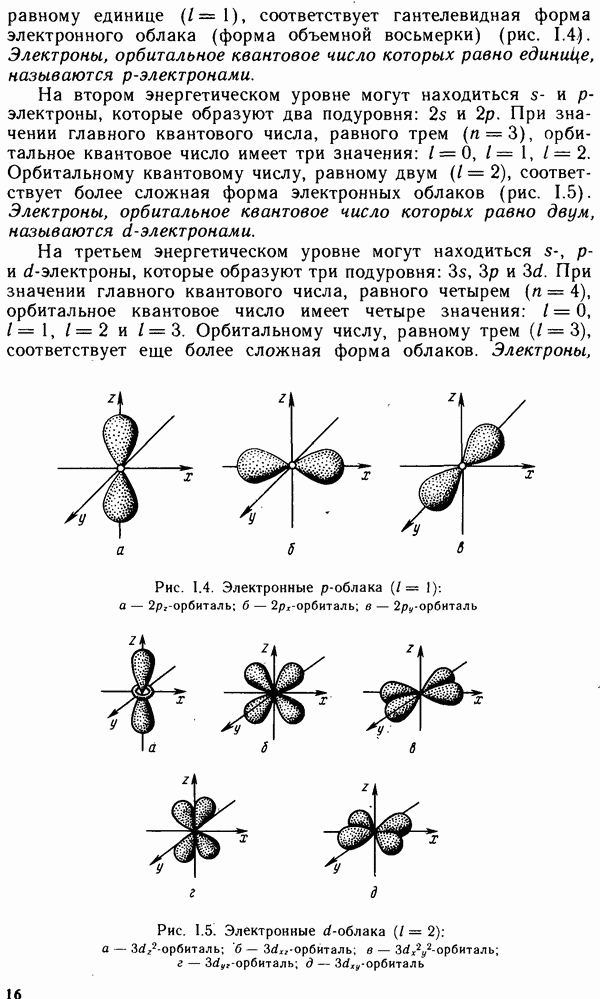
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
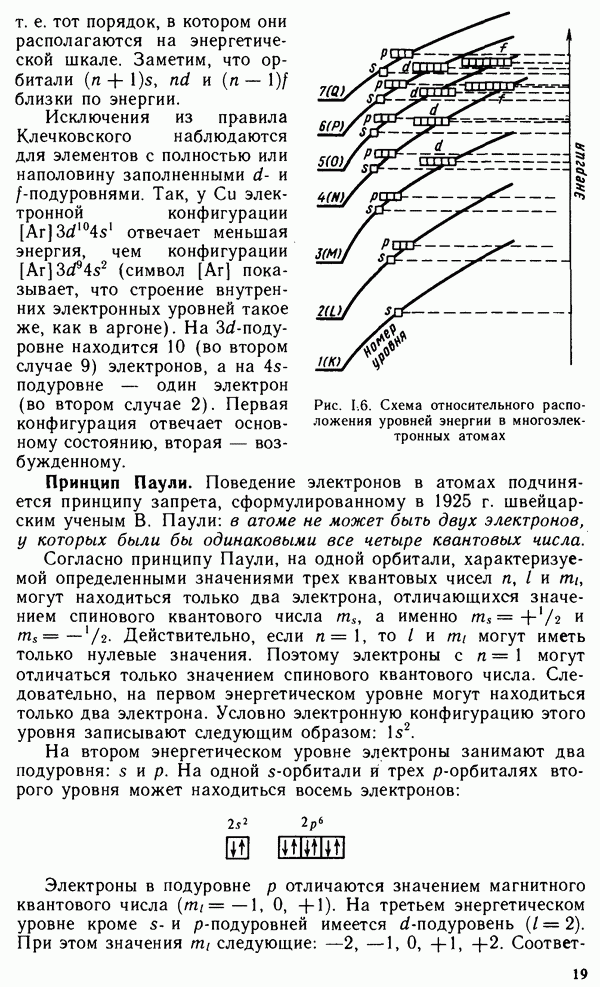
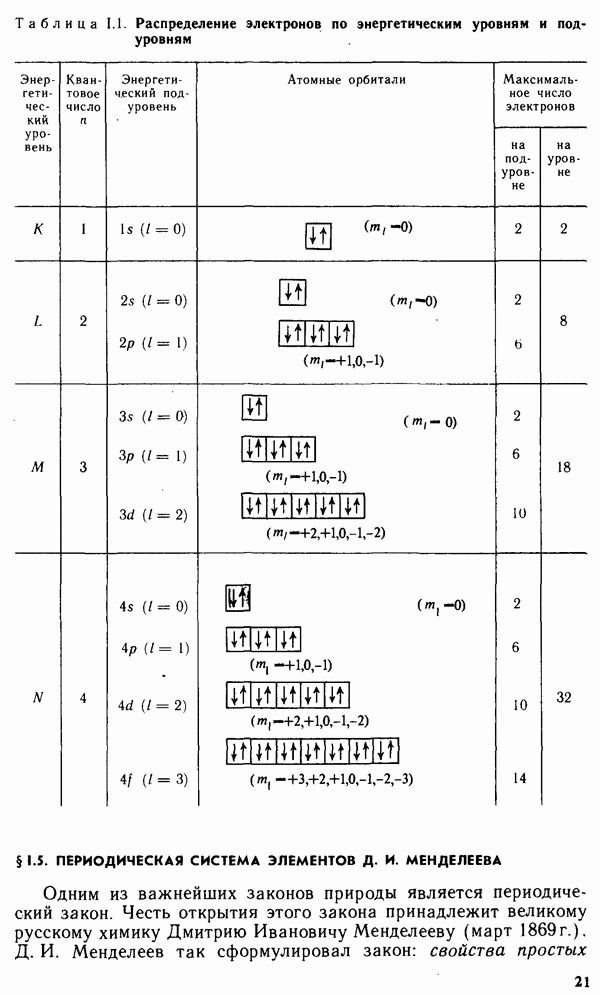
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
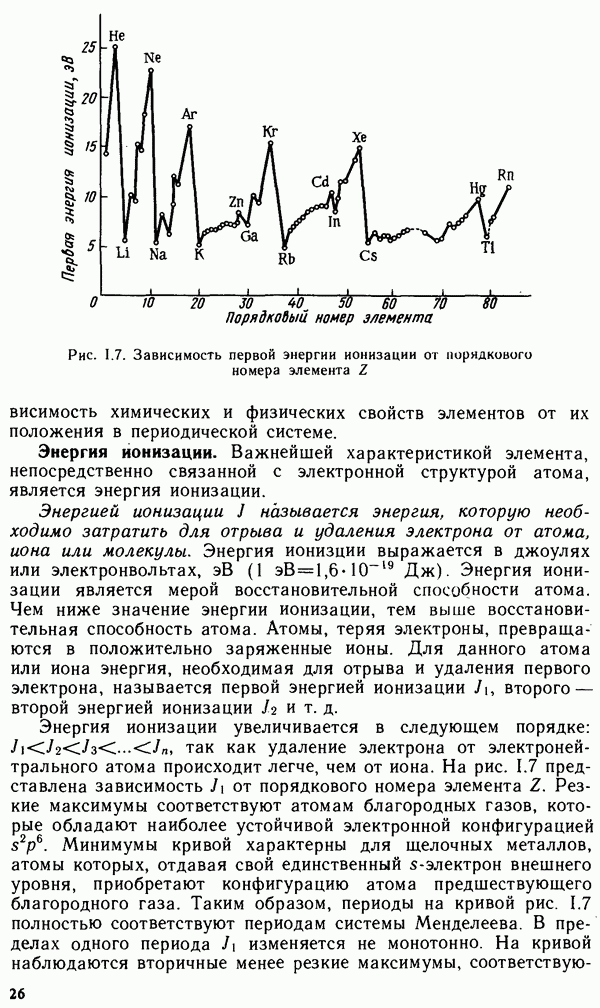
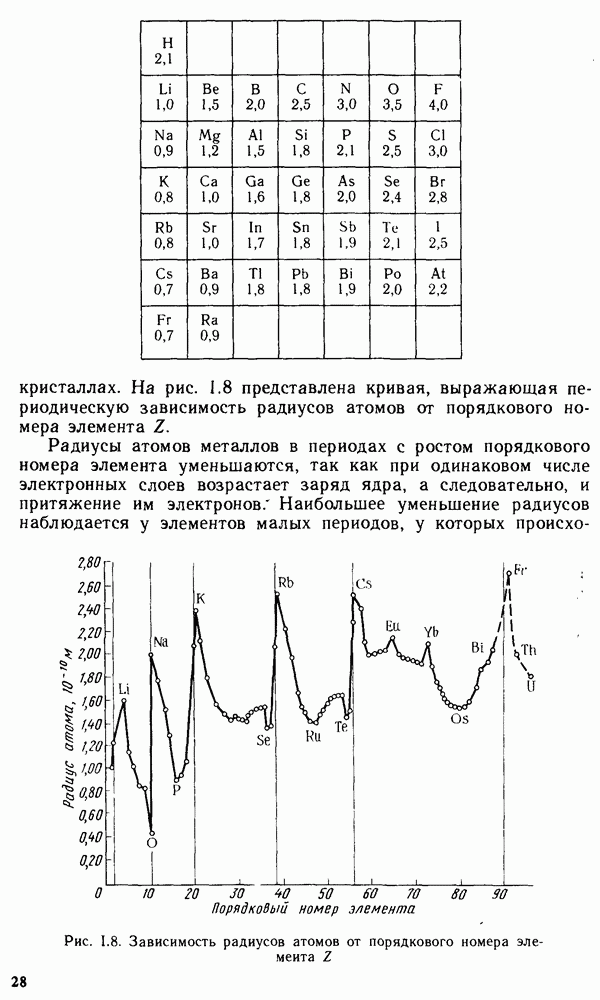
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
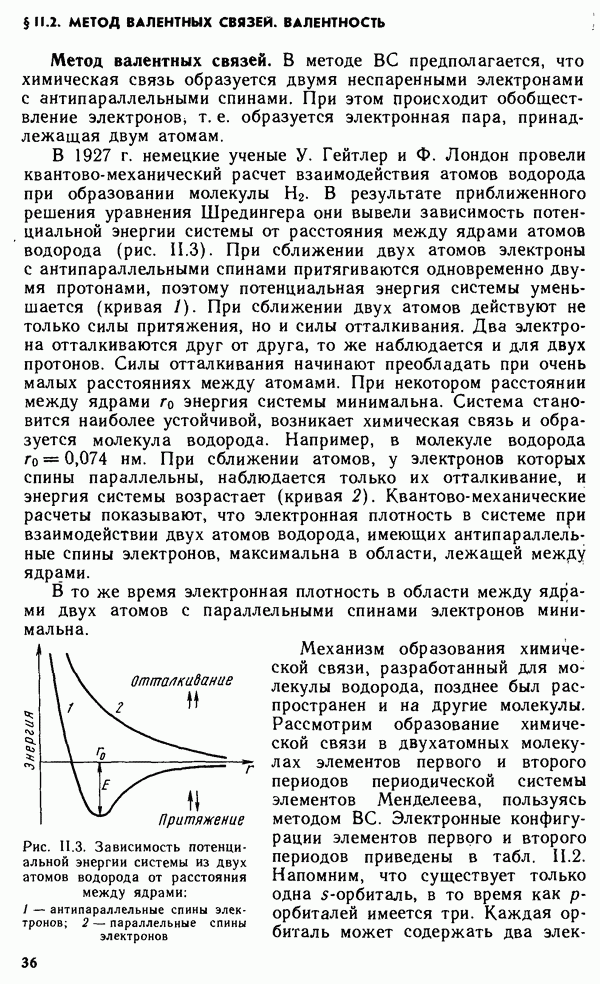
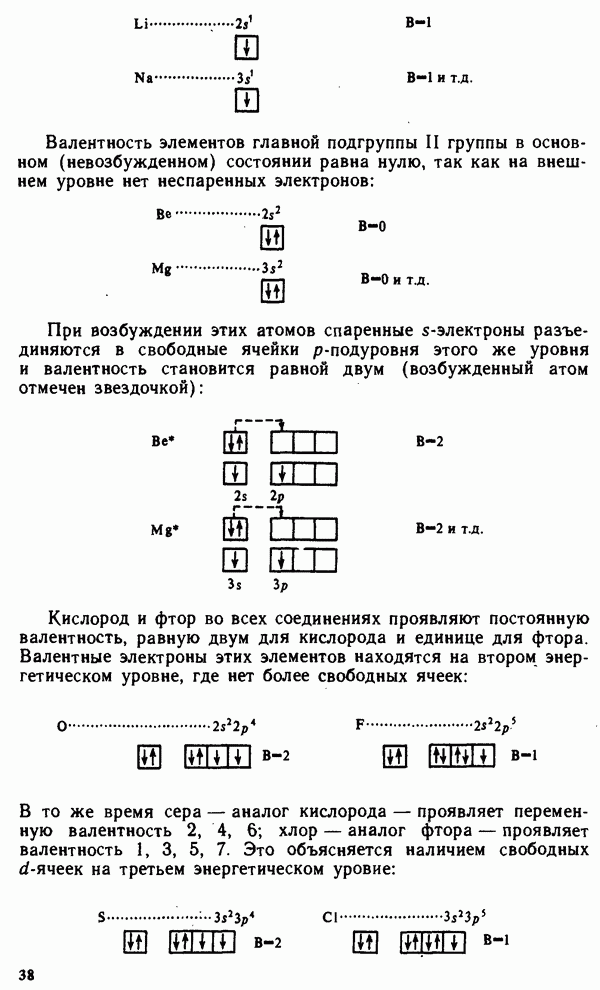
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
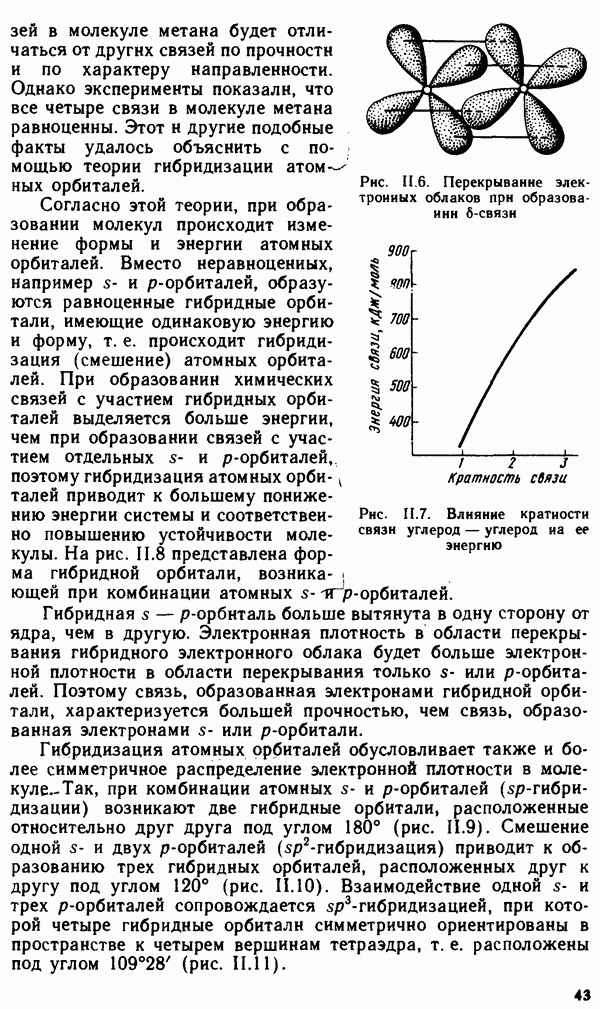
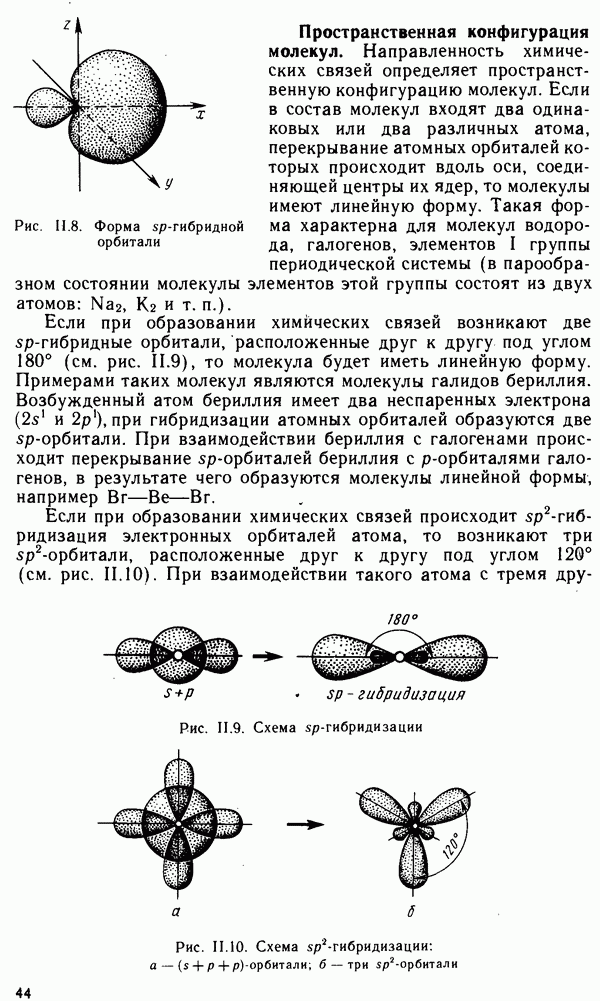
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
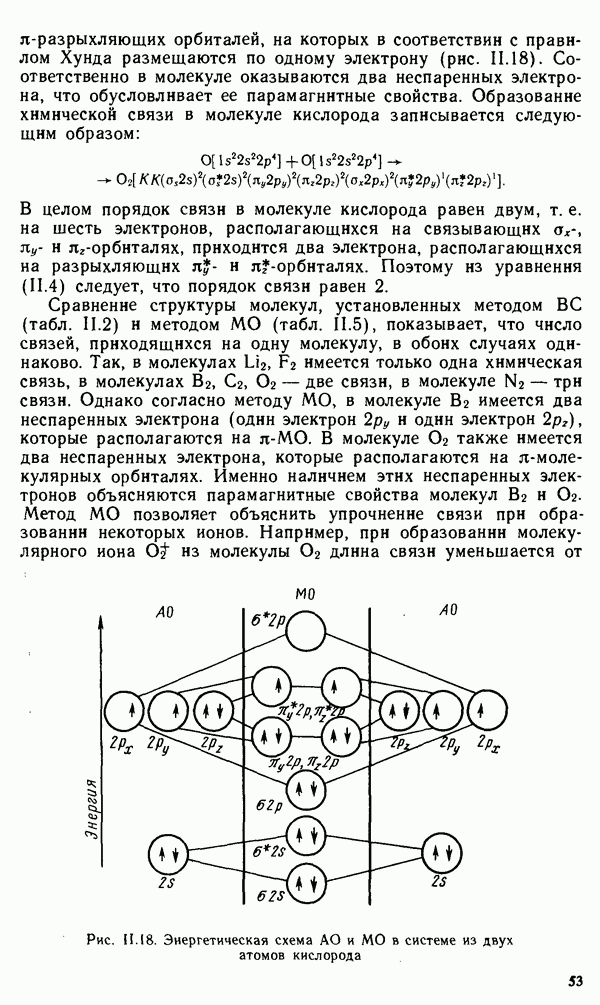
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
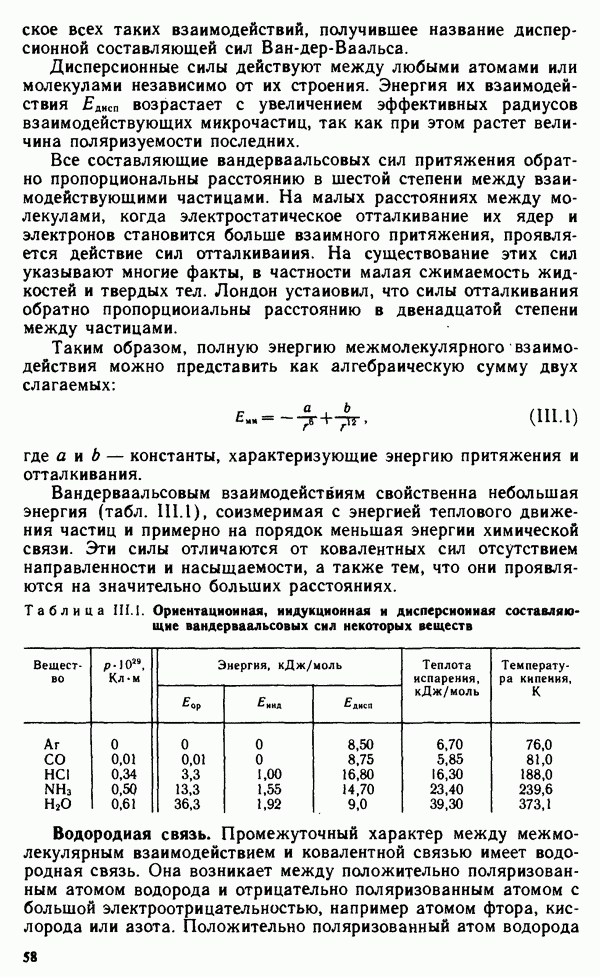
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
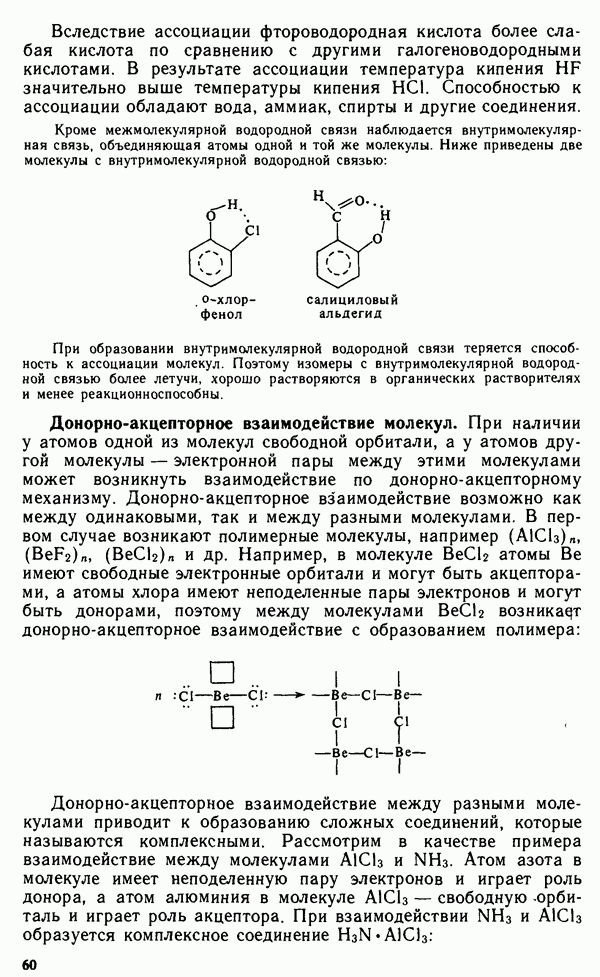
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
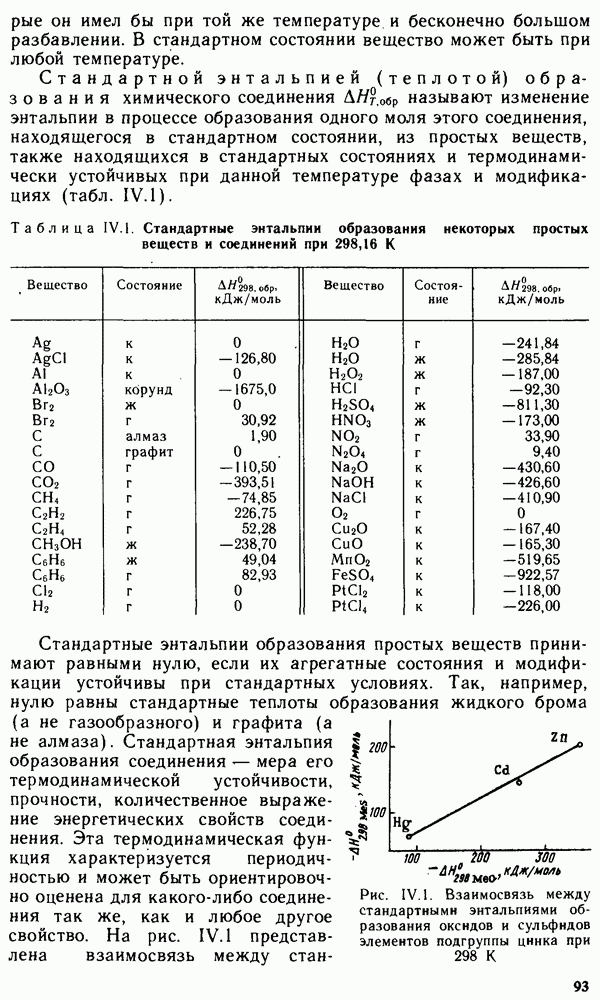
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
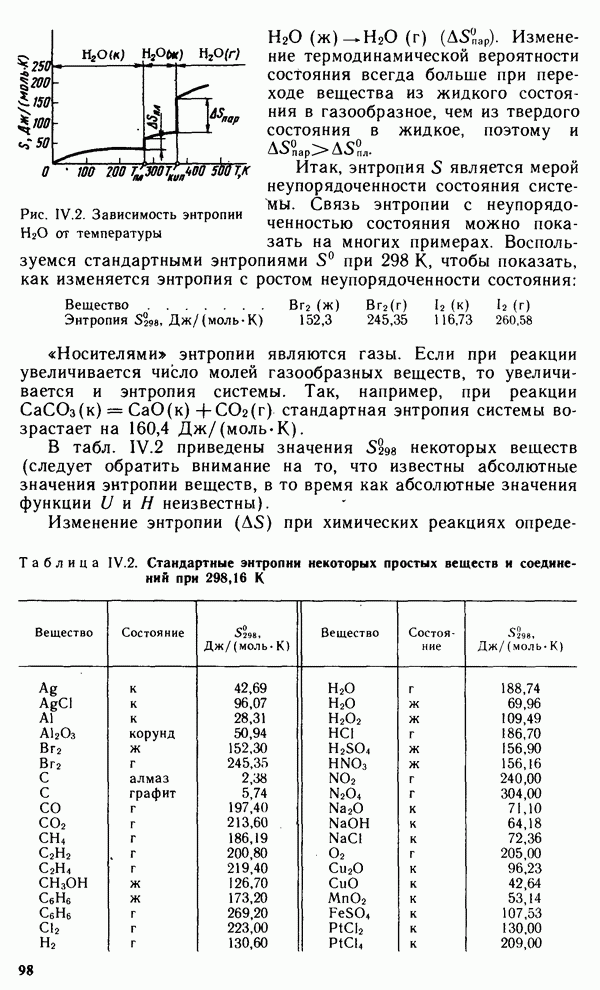
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
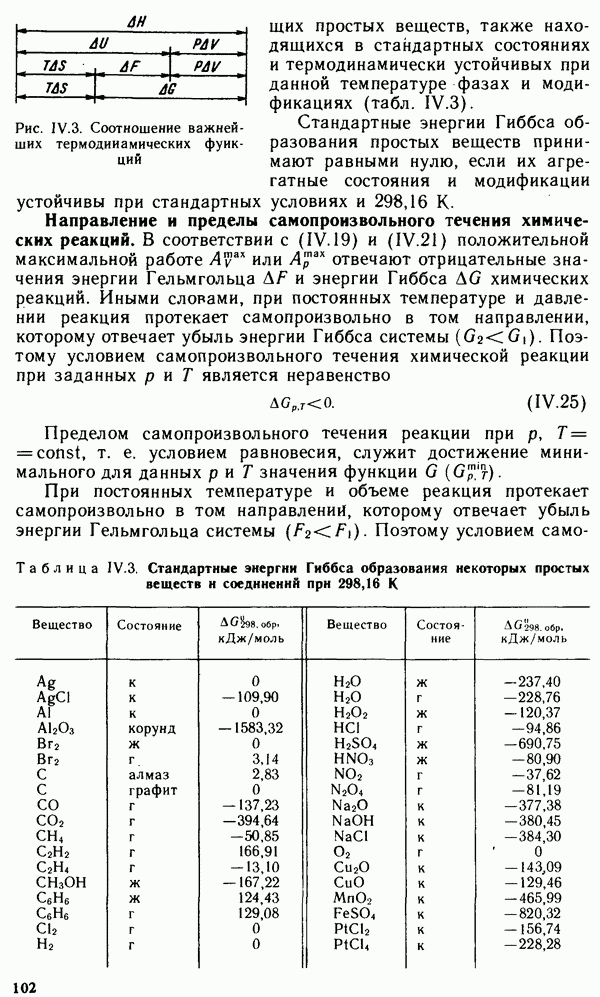
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
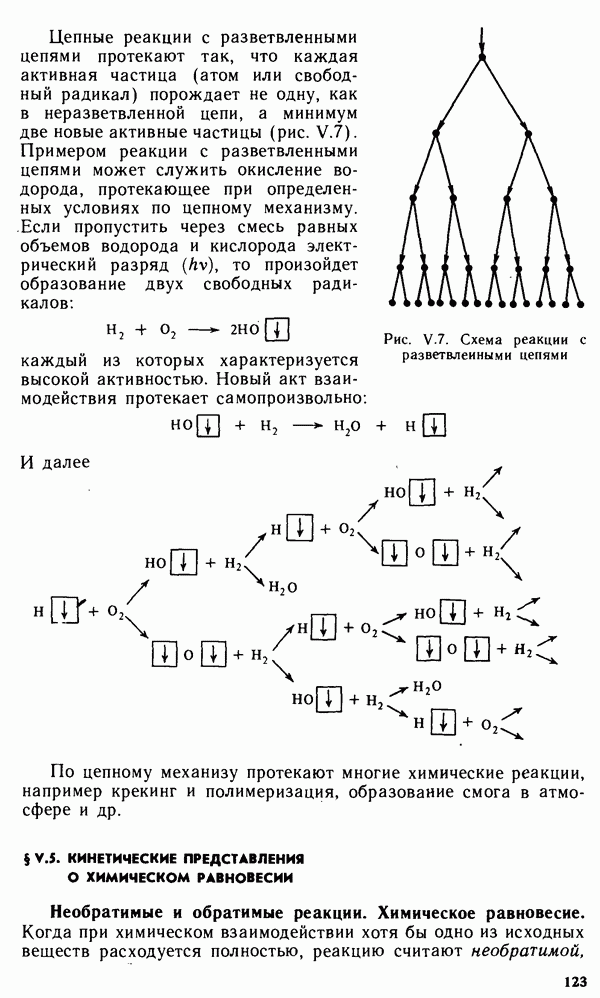
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
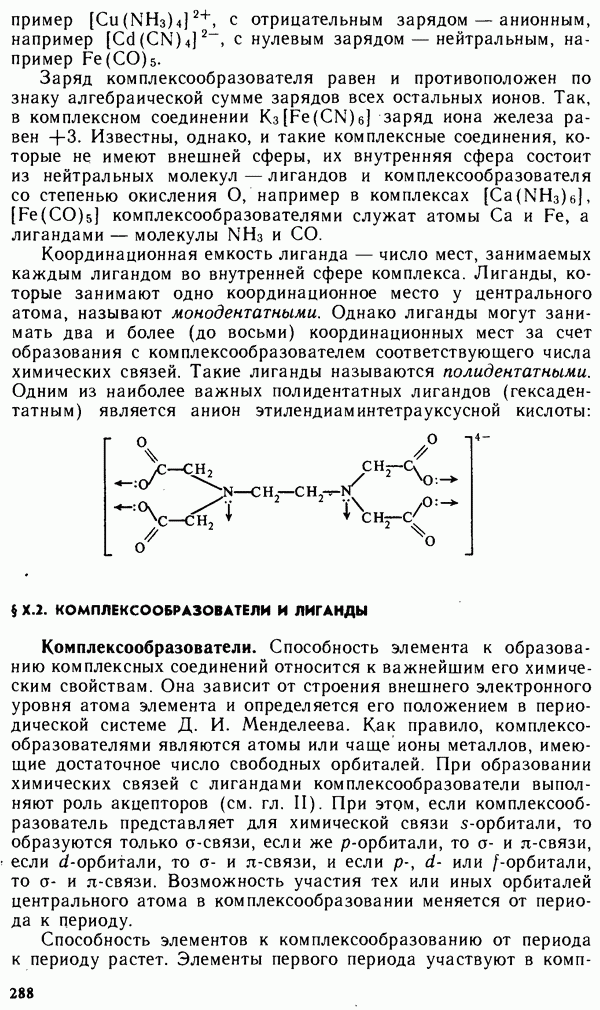
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
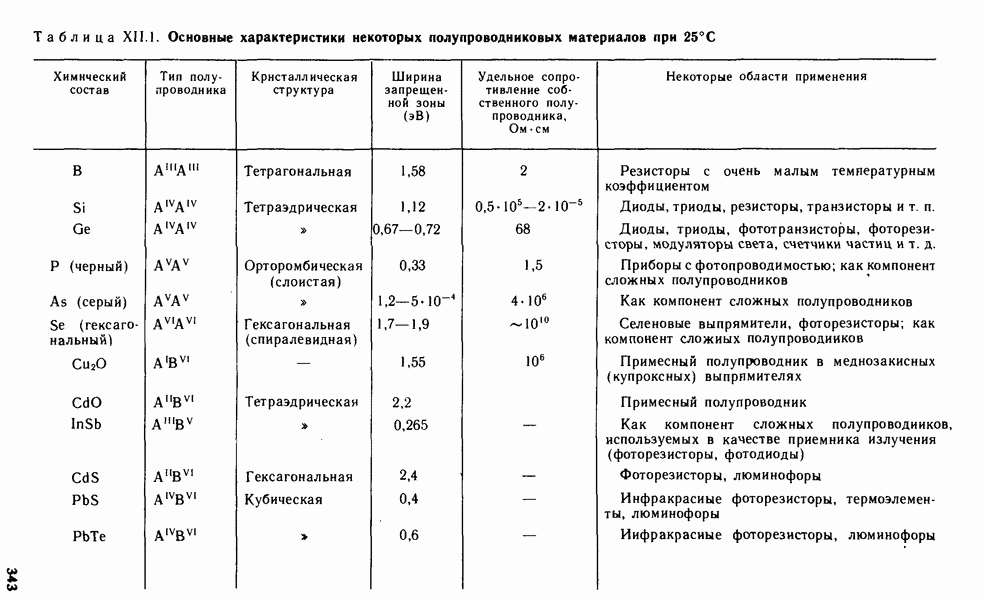
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
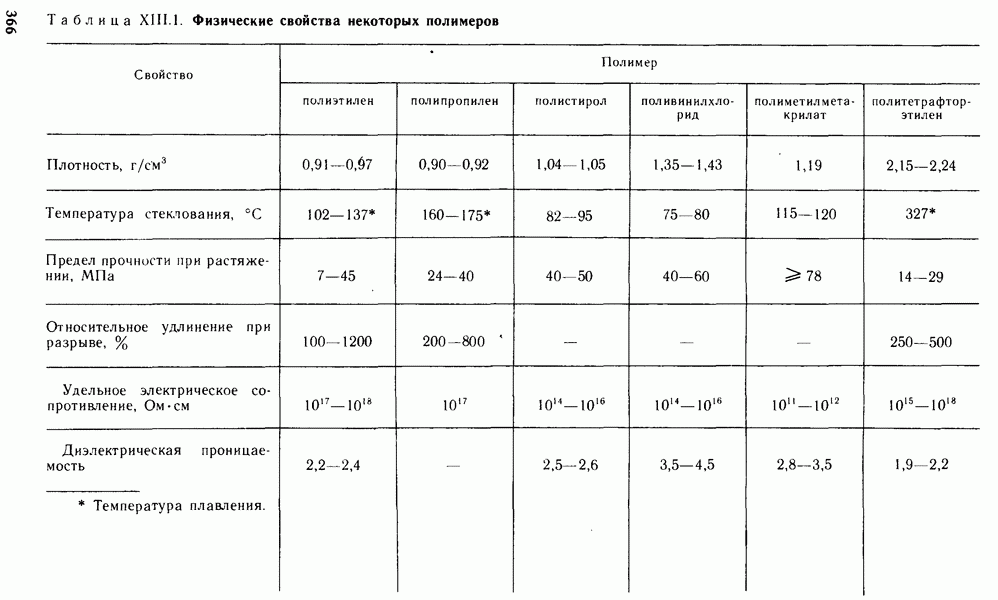
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
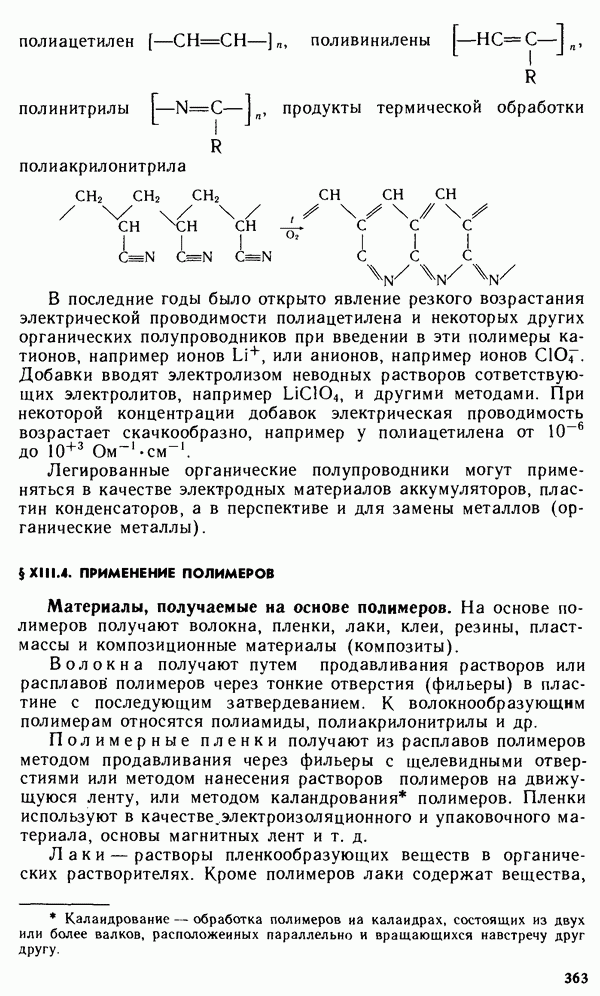
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ