| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
В зависимости от условий окружающей среды и в первую очередь от температуры и давления химические вещества могут находиться в различных агрегатных состояниях. Эти агрегатные состояния отличаются друг от друга величиной и природой сил, действующих между частицами, а также характером движения самих частиц. Различают твердое, жидкое, газообразное и плазменное состояния веществ.
Между четырьмя агрегатными состояниями нет резких границ. В зависимости от природы веществ, образующих систему, а также температуры и давления возможно существование промежуточных или переходных агрегатных состояний.
Газообразное состояние.
В газообразном состоянии вещество заполняет весь объем и принимает форму сосуда, обладает большой сжимаемостью и образует однородные смеси. Эти свойства газов обусловлены тем, что их отдельные молекулы находятся на сравнительно далеком расстоянии друг от друга, поэтому не оказывают значительного взаимного влияния.
Кинетическая энергия молекул в этом состоянии максимальна, а энергия их взаимодействия минимальна. Главным видом движения молекул в газах является поступательное движение. При этом они испытывают огромное число соударений: для одного моля газа более чем  соударений в секунду при комнатной температуре. Молекулы в газах движутся хаотически. Они сохраняют свою химическую индивидуальность, поэтому многие физико-химические свойства таких систем могут быть получены по правилу аддитивности: суммированием характеристик образующих их молекул. Так, давление р, объем V и число молей
соударений в секунду при комнатной температуре. Молекулы в газах движутся хаотически. Они сохраняют свою химическую индивидуальность, поэтому многие физико-химические свойства таких систем могут быть получены по правилу аддитивности: суммированием характеристик образующих их молекул. Так, давление р, объем V и число молей  идеального газа связаны между собой уравнением Менделеева — Клапейрона
идеального газа связаны между собой уравнением Менделеева — Клапейрона

где  — молярная газовая постоянная; Т — термодинамическая температура.
— молярная газовая постоянная; Т — термодинамическая температура.
При переходе к реальным газам в уравнение (III.2) необходимо
димо вводить поправки, учитывающие как силы взаимодействия между молекулами, так и собственный их объем:

где  — поправка на объем молекул; а — коэффициент пропорциональности, учитывающий энергию их взаимодействия. Формально уравнение
— поправка на объем молекул; а — коэффициент пропорциональности, учитывающий энергию их взаимодействия. Формально уравнение  может быть применено и к жидкостям. Однако поправочный член
может быть применено и к жидкостям. Однако поправочный член  будет значительно превышать давление
будет значительно превышать давление  . Уравнение
. Уравнение  впервые было предложено Ван-дер-Ваальсом и называется его именем. Точные количественные расчеты для газов требуют введения еще и других поправок. К настоящему времени предложено большое число различных уравнений состояния газов, дающих хорошие результаты в том или ином интервале изменения температуры и давления.
впервые было предложено Ван-дер-Ваальсом и называется его именем. Точные количественные расчеты для газов требуют введения еще и других поправок. К настоящему времени предложено большое число различных уравнений состояния газов, дающих хорошие результаты в том или ином интервале изменения температуры и давления.
Плазменное состояние.
При нагревании разреженных газообразных систем до высоких температур, как правило, превышающих десятки тысяч градусов, происходит ионизация молекул, и газ переходит в специфическое состояние с электронно-ионной проводимостью, называемое плазменным состоянием. Ионы, появившиеся в низкотемпературной плазме в результате отщепления электронов, способны к дальнейшим химическим реакциям, поэтому в плазмах можно обнаружить такие экзотические с точки зрения химии частицы, как иоиы  Кинетическая и потенциальная энергия частиц в плазменном состоянии превышает аналогичные параметры газообразных молекул, но наиболее существенные различия между плазмой и газами возникают при наложении электрического и магнитного полей большой напряженности. При этом движение частиц в плазме становится направленным, и придавая ему винтообразную форму, можно до известной степени управлять плазмой.
Кинетическая и потенциальная энергия частиц в плазменном состоянии превышает аналогичные параметры газообразных молекул, но наиболее существенные различия между плазмой и газами возникают при наложении электрического и магнитного полей большой напряженности. При этом движение частиц в плазме становится направленным, и придавая ему винтообразную форму, можно до известной степени управлять плазмой.
Конденсированное состояние.
При охлаждении газ конденсируется, превращаясь в жидкость, которая при дальнейшем охлаждении переходит в твердое состояние.
В поведении жидкостей и твердых тел есть много общего: незначительная сжимаемость, медленная диффузия частиц и другие, поэтому жидкое и твердое состояния часто объединяют общим термином «конденсированное состояние вещества».
Жидкое состояние.
Молекулы в жидкости находятся значительно ближе друг к другу, чем в газах, и удерживаются относительно друг друга силами межмолекулярного взаимодействия. Доля свободного объема в жидкости очень невелика, поэтому жидкости обладают незначительной сжимаемостью. Молекулы в жидкости свободно перемещаются относительно друг друга, поэтому жидкости обладают текучестью и способностью принимать форму той части сосуда, которую они занимают, либо форму шара в невесомости. Повышенное тепловое движение частиц в жидкостях и низкая вязкость их приводят, в среднем, к неупорядоченному
размещению частиц. В связи с этим жидкости обладают изотропностью, т. е. идентичностью свойств в любой ее точке, тождественностью свойств по любому из выбранных направлений. В то же время в среднем во времени ближайшие друг к другу частицы в жидкостях располагаются не хаотически, а более или менее упорядоченно, реализуя так называемый «ближний порядок». Согласно теории советского ученого Я. И. Френкеля, частицы, находясь в этом положении, совершают тепловое колебательное движение и лишь изредка осуществляют поступательный скачок за пределы своей группировки. Совершение частицей такого «активированного» скачка требует преодоления некоторого потенциального барьера.
Жидкие кристаллы.
Известно много веществ, которые в жидком состоянии обладают анизотропностью, т. е. зависимостью свойств от направления. Такие вещества называют жидкими кристаллами. Своеобразие структуры жидких кристаллов проявляется в том, что образующие их частицы могут свободно перемещаться друг относительно друга, при этом их ориентация сохраняется. Частицы или располагаются таким образом, что их оси ориентированы нитеобразно в одном направлении, или размещены в параллельных слоях, внутри которых движение частиц разупорядочено. Первый тип жидких кристаллов называют нематическим или нитеобразным, второй — смектическим (смегма — мыло). Жидкокристаллическое состояние реализуется, например, при растворении в воде ацетата холестерина, олеатов калия и аммония, различных липидов, а также других веществ, как правило, органической природы, молекулы которых имеют нитеобразную структуру.
Структура жидких кристаллов легко изменяется при нагревании, воздействии электрических и магнитных полей, механических напряжений и т. д., в результате чего изменяются их физические свойства. Таким образом можно управлять физическими свойствами жидких кристаллов с помощью слабых внешних воздействий. Жидкие кристаллы широко применяются в цветных дисплеях, термометрах, буквенно-цифровых индикаторах и других устройствах записи и хранения информации.
Твердое состояние.
В твердом агрегатном состоянии вещества средние расстояния между образующими его микрочастицами равны размеру частиц, а энергия взаимодействия значительно превышает их среднюю кинетическую энергию. Основным видом движения микрочастиц является их тепловое колебательное движение, поэтому вероятность пребывания частиц вблизи фиксированных равновесных положений максимальна. Это объясняет наличие у твердых тел собственной формы, отсутствие текучести, незначительную сжимаемость и механическую прочность. Твердые вещества могут быть в аморфном и кристаллическом состояниях.
Аморфное состояние. Методом изобарического охлаждения (при постоянном давлении), изотермического сжатия жидкостей
или переохлаждением расплавов можно получить некоторые вещества в аморфном состоянии. Вещество в таком состоянии не имеет дальнего порядка, оно изотропно (т. е. его свойства не зависят от направления), плавится не при определенной фиксированной температуре, а в некотором температурном интервале. Твердое аморфное состояние вещества может рассматриваться как переохлажденная жидкость. Типичными примерами аморфных тел могут служить стекла, поэтому аморфное состояние называют также стеклообразным. В стеклообразном состоянии могут находиться простые вещества (S, Se, As, С, Р), оксиды, некоторые многокомпонентные системы, большинство органических полимеров. В последние годы разработаны методы получения некоторых металлов в стеклообразном состоянии («металлических стекол»). Металлы в стеклообразном состоянии обладают некоторыми специфическими свойствами, например повышенной устойчивостью к химическому воздействию внешней среды.
Кристаллическое состояние.
Большинство твердых тел в окружающем нас мире являются кристаллическими, т. е. образующие их частицы расположены регулярно в трехмерном пространстве. В монокристаллах эта регулярность распространяется на весь объем твердого тела, в поликристаллических образцах имеются регулярные области — зерна, размеры которых значительно превышают расстояния между микрочастицами (на границах между этими областями ориентация регулярной структуры резко меняется). Таким образом, в кристаллических телах реализуется в отличие от жидкостей «дальний порядок».
Регулярное расположение образующих кристалл микрочастиц может быть изображено в виде так называемой кристаллической решетки, представляющей собой сетку из регулярно повторяющихся в пространстве и параллельно размещенных точек, называемых узлами решетки. В узлах располагаются центры частиц, формирующих данный кристалл.
В отличие от аморфных тел монокристаллы обладают анизотропными свойствами, т. е. величина того или иного параметра в кристалле будет различной в направлении разных его осей. Переход из кристаллического твердого в жидкое агрегатное состояние осуществляется скачкообразно при постоянной температуре, называемой температурой плавления.
Высокая степень упорядоченности частиц в кристалле сообщает последним высокую энергетическую устойчивость. С этой точки зрения аморфные тела, в которых частицы размещены менее упорядоченно, находятся и в менее устойчивом состоянии, и при переходе из аморфного состояния тела в кристаллическое должна выделяться энергия. Правда, скорость этого процесса незначительна из-за высокой вязкости системы.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
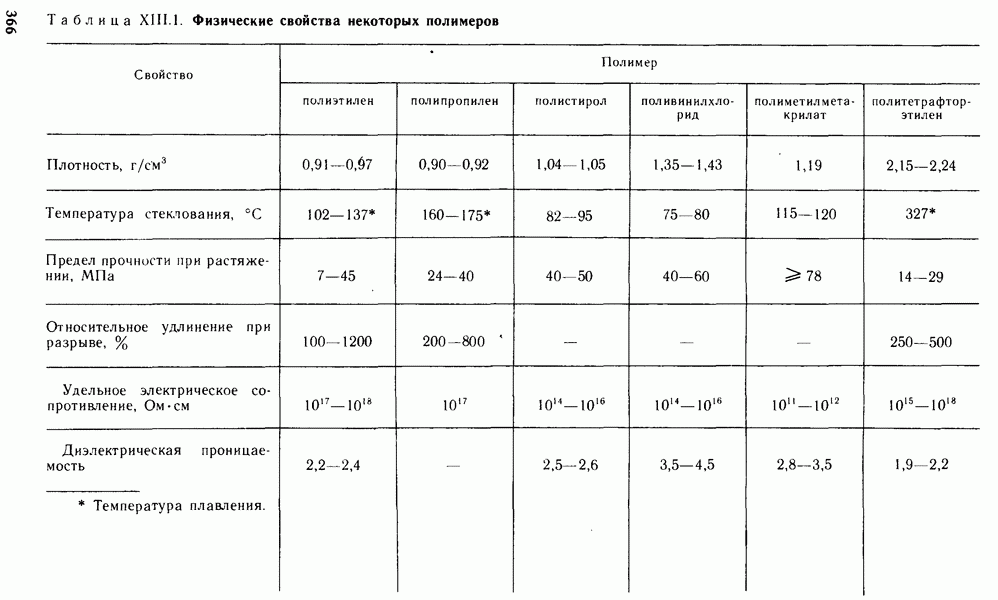
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ