| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
Одно из наиболее характерных свойств металлов — высокая электрическая проводимость, обусловленная направленным переносом их электронов в электрическом поле. С другом стороны, имеется большая группа твердых веществ с молекулярной, ионной или ковалентной решеткой, которые образуют класс диэлектриков. Их электрическая проводимость на 20—30 порядков ниже электрической проводимости металлов.
Известно большое число веществ, занимающих промежуточное положение между металлами и диэлектриками и относящихся к классу полупроводников. При очень низких температурах полупроводники не проводят электрический ток, т. е. являются типичными диэлектриками. Однако по мере роста температуры отмечается возрастание их электрической проводимости.
Любая теория твердого тела должна удовлетворительно объяснить наблюдающиеся огромные различия в электрической проводимости веществ, принадлежащих разным классам. К сожалению, ни теория ковалентной связи, рассматривающая электроны, принадлежащие лишь данной химической связи, как в ковалентных кристаллах, ни модель свободного электрона в металлах не в состоянии объяснить изменение электрической проводимости твердых тел больше чем на два порядка. С этой точки зрения применение в теории твердого тела квантово-механических представлений может быть весьма успешным.
Зонная теория кристаллов.
В модели свободного электрона волновое движение электрона может осуществляться по любому направлению и будет ограничиваться лишь размерами кристалла. Для простоты ограничимся одномерной задачей, рассматривая движение электрона лишь вдоль одной оси (одномерный
ящик). Решение уравнения Шредингера для такого свободного электрона дает следующее выражение для его энергии:

где  — целое число;
— целое число;  — постоянная Планка;
— постоянная Планка;  — масса электрона; а — размеры кристалла в направлении характеристической оси (постоянная решетки).
— масса электрона; а — размеры кристалла в направлении характеристической оси (постоянная решетки).
Из формулы (III.4) видно, что с увеличением размеров кристалла разность энергий соседних уровней электрона будет уменьшаться. При большом числе энергетических уровней разность между ними будет настолько мала, что они образуют почти непрерывную зону энергий.
В процессе образования кристалла происходит перекрывание внешних электронных орбиталей атомов по аналогии с образованием химической связи в молекулах. В соответствии с методом  при взаимодействии двух атомных орбиталей образуются две молекулярные орбитали: связывающая и разрыхляющая. При одновременном взаимодействии N микрочастиц образуется N молекулярных орбиталей. Величина N в кристаллах может достигать огромных значений (порядка 1023). Поэтому и число электронных орбиталей в твердом теле чрезвычайно велико. При этом разность между энергиями соседних орбиталей будет ничтожно мала. Так, в кристалле натрия разность энергетических уровней двух соседних орбиталей имеет порядок
при взаимодействии двух атомных орбиталей образуются две молекулярные орбитали: связывающая и разрыхляющая. При одновременном взаимодействии N микрочастиц образуется N молекулярных орбиталей. Величина N в кристаллах может достигать огромных значений (порядка 1023). Поэтому и число электронных орбиталей в твердом теле чрезвычайно велико. При этом разность между энергиями соседних орбиталей будет ничтожно мала. Так, в кристалле натрия разность энергетических уровней двух соседних орбиталей имеет порядок  Дж. Таким образом, в кристалле металла образуется энергетическая зона с почти непрерывным распределением энергии, называемая зоной проводимости. Каждая орбиталь в этой зоне охватывает кристалл по всем его трем измерениям. Заполнение орбиталей зоны проводимости электронами происходит в соответствии с положениями квантовой механики. Так, из условий минимума энергии электроны будут последовательно заполнять все орбитали, начиная с наинизшей, причем на каждой орбитали в соответствии с запретом Паули может располагаться лишь два электрона с антипараллельными спинами. С повышением температуры за счет теплового возбуждения электроны будут последовательно перемещаться на более высокие энергетические уровни, передавая тепловую энергию с одного конца кристалла на другой и обеспечивая таким образом его теплопроводность.
Дж. Таким образом, в кристалле металла образуется энергетическая зона с почти непрерывным распределением энергии, называемая зоной проводимости. Каждая орбиталь в этой зоне охватывает кристалл по всем его трем измерениям. Заполнение орбиталей зоны проводимости электронами происходит в соответствии с положениями квантовой механики. Так, из условий минимума энергии электроны будут последовательно заполнять все орбитали, начиная с наинизшей, причем на каждой орбитали в соответствии с запретом Паули может располагаться лишь два электрона с антипараллельными спинами. С повышением температуры за счет теплового возбуждения электроны будут последовательно перемещаться на более высокие энергетические уровни, передавая тепловую энергию с одного конца кристалла на другой и обеспечивая таким образом его теплопроводность.
Аналогично можно объяснить и действие приложенного к кристаллу электрического поля. Оно несколько изменяет относительные энергии орбиталей в зоне, понижая одни уровни и повышая другие (по отношению к силовым линиям поля). Это в свою очередь приводит к направленному переносу электронов на энергетически более выгодные орбитали, т. е. вызывает электронную проводимость кристалла.
С позиций квантовой механики орбиталь, занимаемая электроном, характеризует его полную энергию. Переходя с одного уровня на другой в зоне проводимости, электрон приобретает дополнительную энергию, за счет которой он ускоряется в силовом
поле. Какую же максимальную энергию способен приобрести электрон в твердом теле? Этот вопрос тесно связан с определением ширины энергетических зон в кристалле, т. е. разности энергий между самой высшей и самой низшей орбиталями в зоне.
Ширина энергетической зоны зависит от характера электронных орбиталей взаимодействующих атомов  и
и  -состояния), а также от глубины их перекрывания. Так, внутренние электронные орбитали атомов перекрываются довольно слабо. Поэтому образуемые ими зоны узки. Кроме того, такие зоны полностью или почти полностью заполнены электронами, так что их вклад в проводимость кристалла незначителен. Напротив, зоны, соответствующие валентным электронным состояниям, широки, хотя и в этом случае зоны, образованные d-орбнталямн, обычно значительно уже зон, сформированных р- и особенно
-состояния), а также от глубины их перекрывания. Так, внутренние электронные орбитали атомов перекрываются довольно слабо. Поэтому образуемые ими зоны узки. Кроме того, такие зоны полностью или почти полностью заполнены электронами, так что их вклад в проводимость кристалла незначителен. Напротив, зоны, соответствующие валентным электронным состояниям, широки, хотя и в этом случае зоны, образованные d-орбнталямн, обычно значительно уже зон, сформированных р- и особенно  -орбиталямн с тем же главным квантовым числом.
-орбиталямн с тем же главным квантовым числом.
Количество взаимодействующих атомных орбиталей не влияет на ширину зоны, а определяет лишь плотность ее заполнения электронами. Ширина энергетических зон в твердых телах существенно зависит от внутренней структуры их кристаллов. Эта зависимость тесно связана с волновой природой движения электронов. Перемещаться по кристаллу способны лишь те электроны, длины волн которых не укладываются целое число раз между узлами кристаллической решетки. Электроны с длиной волны, равной  где а — постоянная решетки, будут находиться в кристалле в условиях замкнутого отражения и не способны переносить энергию.
где а — постоянная решетки, будут находиться в кристалле в условиях замкнутого отражения и не способны переносить энергию.
Таким образом, в кристаллах между энергетическими зонами, образованными взаимодействиями атомных орбиталей разного характера, могут возникать области запрещенных энергий, называемые запрещенными зонами. Теория, объясняющая свойства твердых тел на основании анализа строения и плотности заполнения электронами энергетических зон в их кристаллах, называется зонной теорией.
Металлы.
Рассмотрим в соответствии с положениями зонной теории энергетическую структуру металлов. На рис. II 1.5, а показано образование зон в кристалле натрия. Внутренние электронные орбитали атомов, в частности  в кристалле натрия практически не перекрываются.
в кристалле натрия практически не перекрываются.
В зоне проводимости, образованной за счет взаимодействия З-орбиталей, N атомов натрия образуют такое же число энергетических уровней. Так как у каждого атома натрия имеется лишь по одному валентному электрону, при низких температурах в зоне проводимости будет заполнена только половина уровней. Большое число незанятых энергетических уровней в зоне приводит к высокой подвижности электронов и обеспечивает высокую электрическую проводимость металлического натрия. Аналогичное строение зоны проводимости имеют кристаллы и других элементов первой группы периодической системы элементов, причем ширина зоны проводимости максимальна у элементов побочной

Рис. III. 5. Возникновение энергетических зон кристалла из энергетических уровней атомов по мере их сближения: а натрий; б — алмаз
подгруппы: меди, серебра и золота, а у элементов главной подгруппы ширина зоны убывает с ростом их порядкового номера.
Итак, с точки зрения зонной теории металлические свойства проявляют те твердые тела, в кристаллах которых зона проводимости заполнена электронами лишь частично. При этом в переносе электричества будут участвовать не все электроны, находящиеся в зоне, а лишь те, для которых доступны незанятые орбитали с низкой энергией. Так, при нагревании металла тепловое возбуждение перемещает электроны с низкой энергией на более высокие энергетические уровни и тем самым ограничивает их возможность участвовать в переносе тока.
В кристаллическом натрии происходит перекрывание зон, образованных 3s- и 3р-орбиталями. Для металлов первой группы это перекрывание не играет существенной роли, так как число свободных орбиталей в  -зоне у них велико. Однако такое перекрывание s- и р-зон, наблюдаемое и для металлов второй группы периодической системы элементов, играет важную роль. Атомы этих элементов имеют по два валентных
-зоне у них велико. Однако такое перекрывание s- и р-зон, наблюдаемое и для металлов второй группы периодической системы элементов, играет важную роль. Атомы этих элементов имеют по два валентных  -электрона, следовательно, все орбитали в
-электрона, следовательно, все орбитали в  -зоне их кристаллов будут полностью заполнены. Лишь глубокое перекрывание зон, образованных
-зоне их кристаллов будут полностью заполнены. Лишь глубокое перекрывание зон, образованных  -орбиталями их атомов, сообщает металлические свойства кристаллам этих элементов. Образование зон проводимости в кристаллах d-элементов обычно сопровождается значительным перекрыванием
-орбиталями их атомов, сообщает металлические свойства кристаллам этих элементов. Образование зон проводимости в кристаллах d-элементов обычно сопровождается значительным перекрыванием  -зон, причем последние значительно уже зон, образованных
-зон, причем последние значительно уже зон, образованных  -орбиталями. Это значит, что перекрывание d-орбиталей в таких кристаллах невелико. Поэтому целый ряд свойств d-элементов можно трактовать на основании модели
-орбиталями. Это значит, что перекрывание d-орбиталей в таких кристаллах невелико. Поэтому целый ряд свойств d-элементов можно трактовать на основании модели
локализованных d-электронов. Последние придают металлической связи в кристаллах d-элементов частично ковалентный характер. Так, малую химическую активность металлов, расположенных близко к концам периодов, качественно можно объяснить значительной ролью, которую играют в их кристаллах направленные ковалентные связи. Поэтому d-элементы иногда называют переходными металлами в отличие от типичных металлов главных подгрупп.
Электрическая проводимость кристаллов d-элементов обеспечивается главным образом электронами внешних  -орбиталей. В связи с этим электрическая проводимость переходных металлов ниже, чем у типичных металлов. Исключением являются металлы подгрупп меди и цинка, у которых d-орбитали полностью заполнены электронами и не перекрываются с внешними
-орбиталей. В связи с этим электрическая проводимость переходных металлов ниже, чем у типичных металлов. Исключением являются металлы подгрупп меди и цинка, у которых d-орбитали полностью заполнены электронами и не перекрываются с внешними  -зонами.
-зонами.
Диэлектрики и полупроводники.
Рассмотрим применение зонной теории к кристаллам с ковалентными связями. При формировании подобных кристаллов наружные электронные орбитали их атомов, взаимодействуя, также образуют энергетические зоны. Однако направленный характер ковалентных связей приводит к тому, что симметрия кристалла полностью изменяет характер волновых функций электронов взаимодействующих атомов.
У атомов подавляющего большинства элементов, образующих ковалентные кристаллы (углерод, кремний, германий, серое олово), во внешнем квантовом слое имеются четыре орбитали: одна  и три
и три  При образовании кристалла из N атомов эти орбитали расщепляются, образуя две энергетические зоны по
При образовании кристалла из N атомов эти орбитали расщепляются, образуя две энергетические зоны по  орбиталей в каждой, как это показано на рис. III.5,б для кристалла алмаза.
орбиталей в каждой, как это показано на рис. III.5,б для кристалла алмаза.
Из условий минимума энергии все валентные электроны атомов углерода заполняют нижнюю зону, а так как их число составляет 4, то эта зона (ее называют валентной) оказывается заполненной полностью. Зона же проводимости кристалла пуста. Для перехода в эту зону электронам необходимо сообщить энергию порядка 7 эВ  Требуемая энергия превышает энергию связи в кристалле алмаза и не может быть реализована. Поэтому подобные вещества не проводят электрический ток и являются диэлектриками.
Требуемая энергия превышает энергию связи в кристалле алмаза и не может быть реализована. Поэтому подобные вещества не проводят электрический ток и являются диэлектриками.
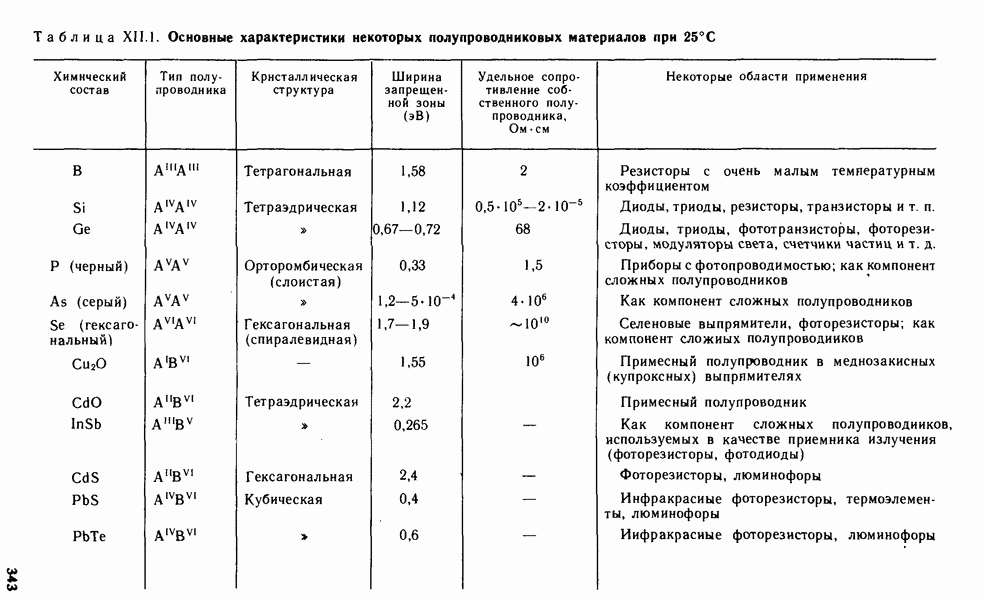
Если же ширина запрещенной зоны относительно невелика, то при сообщении твердому телу определенного количества энергии часть его электронов может переброситься из полностью заполненной валентной зоны в зону проводимости и принять участие в переносе тока. Подобные вещества называют собственными полупроводниками. Так, у типичных собственных полупроводников германия и кремния ширина запрещенной зоны при 0 К соответственно составляет 0,75 и 0,21 эВ (73 и 137 кДж/моль).
Особенность собственных полупроводников состоит в том, что при переходе части электронов в зону проводимости в валентной зоне появляется эквивалентное им число так называемых дырок,
имеющих положительный заряд, которые также могут участвовать в переносе тока. Собственные полупроводники имеют электронно-дырочную проводимость.
Наряду с собственными большое распространение получили также полупроводники примесного типа. В них основное число переносчиков тока — электронов или дырок — поставляют введенные в собственный полупроводник специальные примеси, энергетические уровни которых располагаются между валентными зонами и зонами проводимости полупроводника. Так, при введении в кристалл германия так называемых донорных примесей, как, например, фосфора, мышьяка, сурьмы, электроны последних переходят в зону проводимости полупроводника, резко увеличивая в ней число электронов — переносчиков тока (п-про-водимость). При добавлении к германию акцепторных примесей типа бора, алюминия, индия электроны валентной зоны полупроводника переходят на свободные уровни зоны примесей, что увеличивает число дырок (р-проводимость) в валентной зоне.
При 0 К полупроводники представляют собой типичные диэлектрики, так как их зона проводимости пуста. При нагревании их проводимость растет, так как все большее число электронов перебрасывается в зону проводимости. Температурная зависимость электрической проводимости полупроводников обратна аналогичной зависимости для металлов.
Большая часть ионных кристаллов относится к классу диэлектриков. Изучение проводимости этих кристаллов позволило установить основные черты их зонной структуры. Особенность ионных кристаллов состоит в том, что они образованы при взаимодействии атомов разных элементов, внешние электронные орбитали которых имеют неодинаковую энергию. Так как зона образуется взаимодействием близких по энергии орбиталей, в ионных кристаллах всегда имеется две раздельные внешние зоны с большей и меньшей средней энергией.
Как и в ковалентных кристаллах, валентные электроны взаимодействующих атомов полностью заполняют зону с более низкой энергией (валентная зона). Зона же проводимости, образованная внешними орбиталями второго атома, пуста, и переброс в нее электронов требует затраты энергии. В кристалле  например, все 3р-электроны атомов хлора и
например, все 3р-электроны атомов хлора и  -электроны атомов натрия заполняют зону с более низкой энергией, образованную взаимодействием 3р-орбиталей атомов хлора. Зона же, соответствующая
-электроны атомов натрия заполняют зону с более низкой энергией, образованную взаимодействием 3р-орбиталей атомов хлора. Зона же, соответствующая  -орбиталям атомов натрия (зона проводимости), оказывается незаполненной, причем ширина запрещенной зоны достигает 7 эВ. Электронная проводимость большинства ионных кристаллов примерно на двадцать порядков ниже, чем у металлов. Известен ряд ионных кристаллов, ширина запрещенной зоны у которых не так велика и составляет порядка 2—3 эВ, как, например, у кристаллов
-орбиталям атомов натрия (зона проводимости), оказывается незаполненной, причем ширина запрещенной зоны достигает 7 эВ. Электронная проводимость большинства ионных кристаллов примерно на двадцать порядков ниже, чем у металлов. Известен ряд ионных кристаллов, ширина запрещенной зоны у которых не так велика и составляет порядка 2—3 эВ, как, например, у кристаллов  Такие вещества при повышенных температурах проявляют полупроводниковые свойства.
Такие вещества при повышенных температурах проявляют полупроводниковые свойства.
Наконец, все твердые вещества типа молекулярных кристаллов
принадлежат к классу диэлектриков. Перекрывание электронных орбиталей взаимодействующих частиц в их кристаллах ничтожно мало. В связи с этим состояние электронов у частиц, занимающих узлы пространственных решеток в таких кристаллах, мало отличается от состояний в соответствующих свободных атомах и молекулах.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
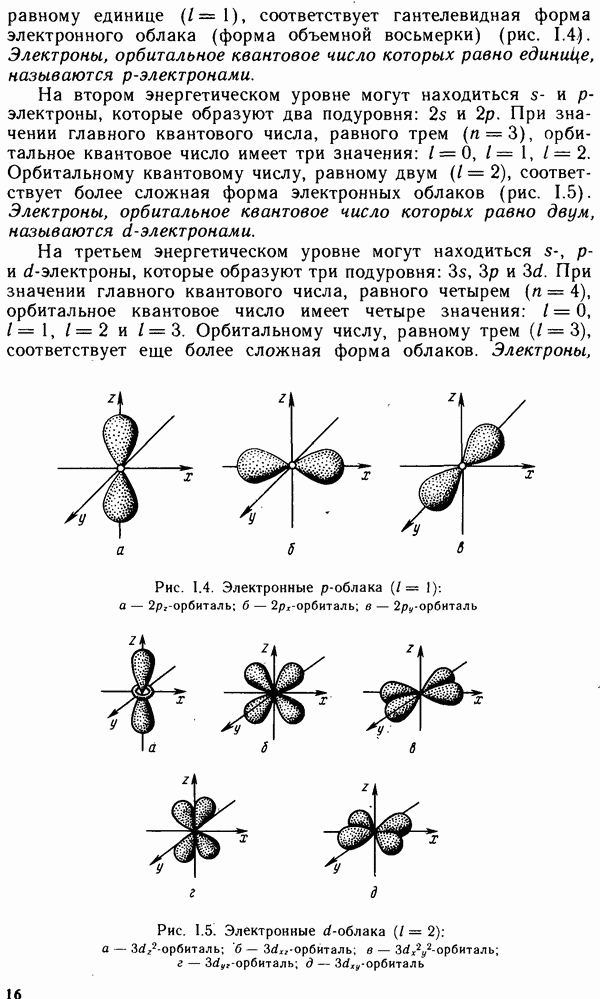
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
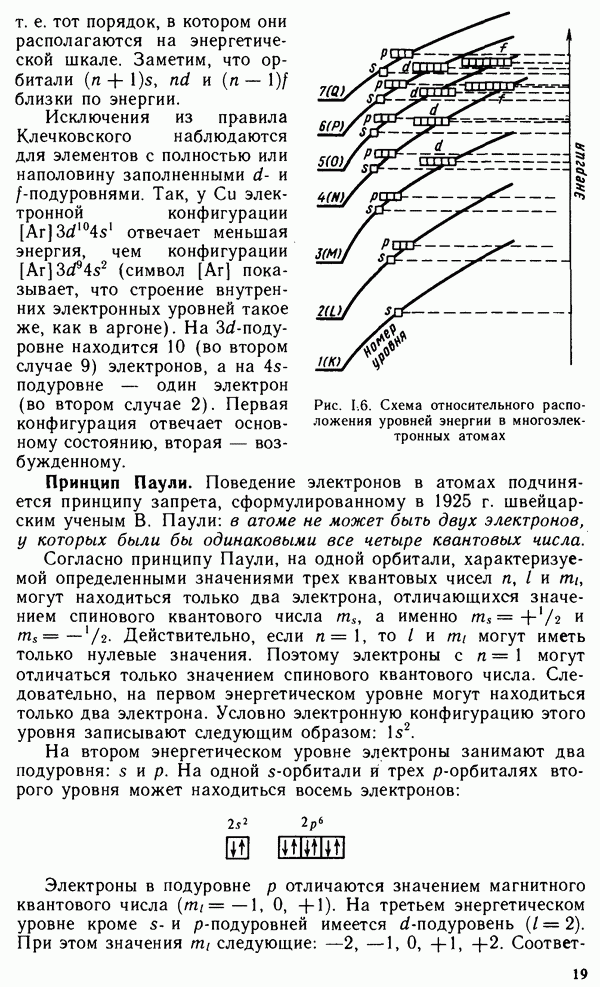
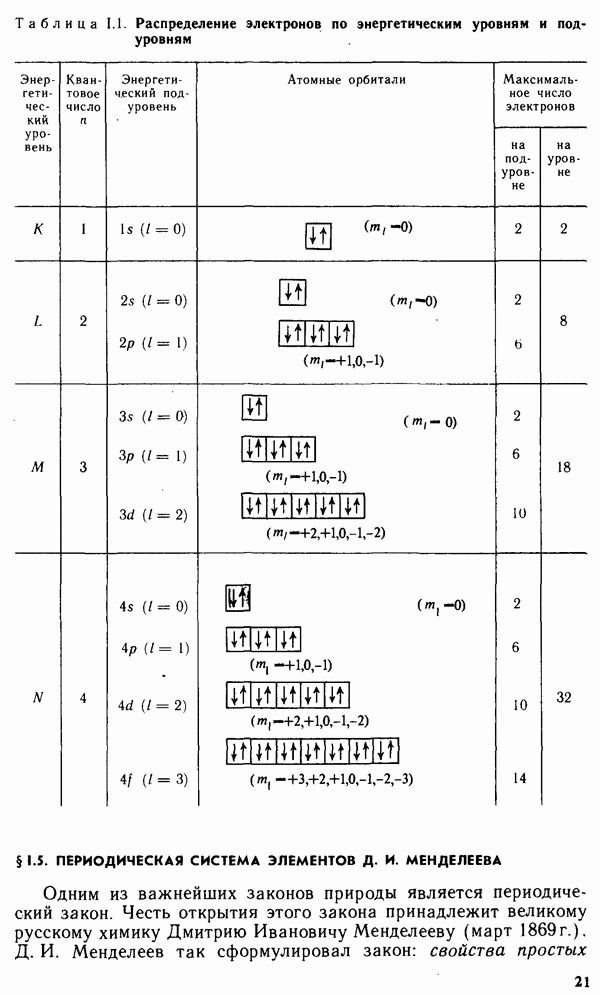
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
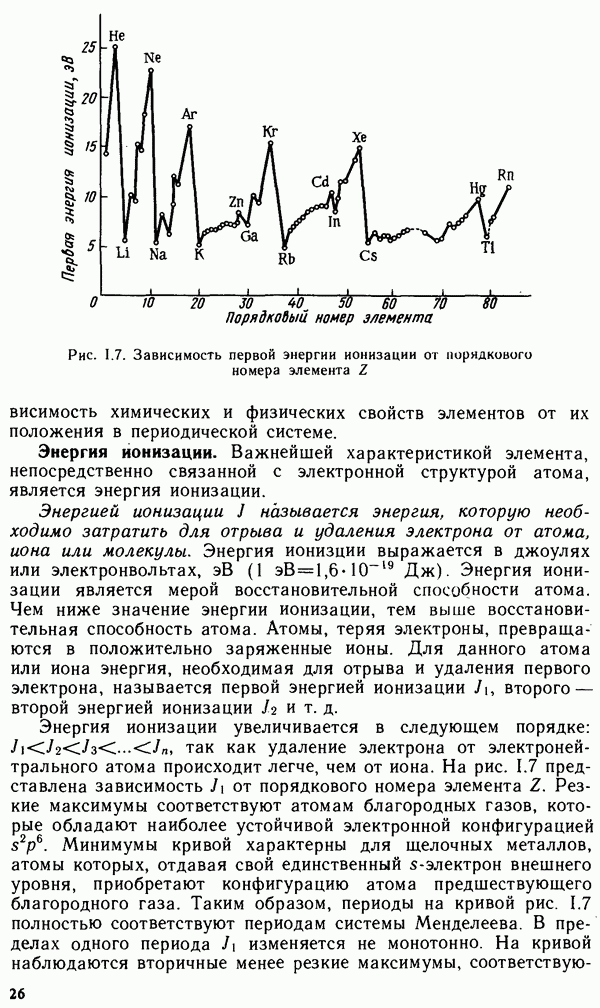
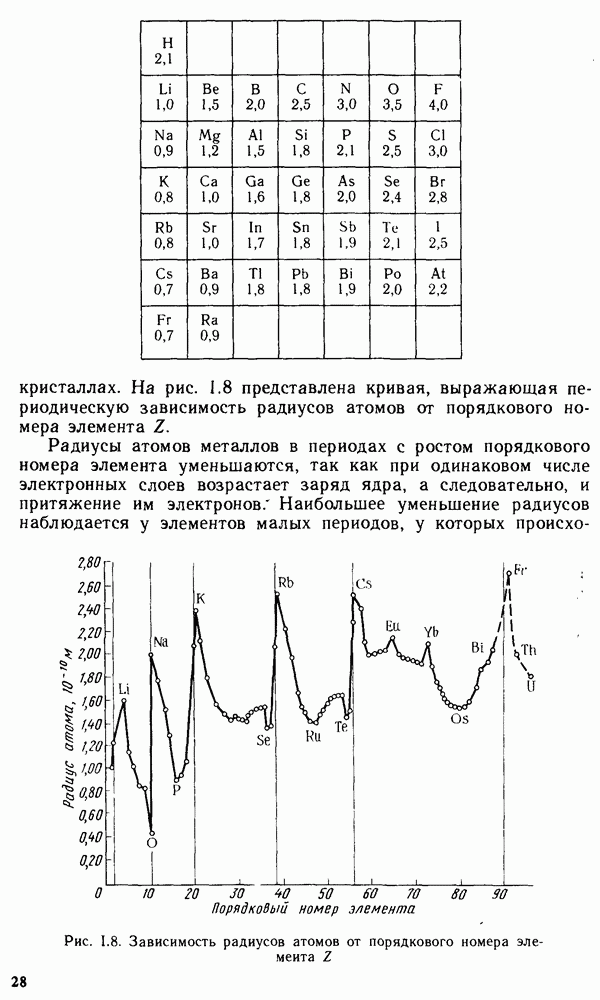
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
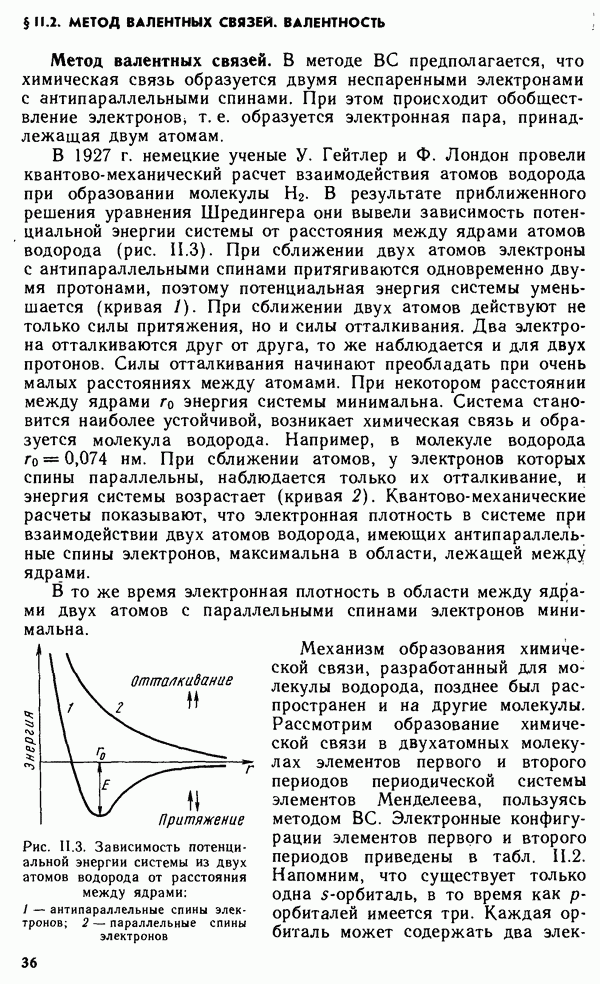
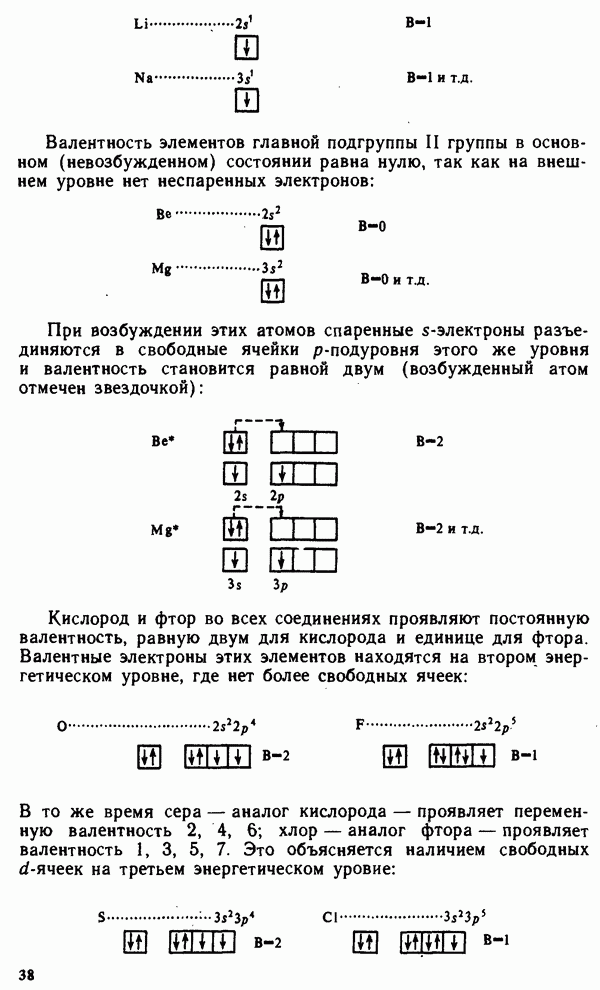
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
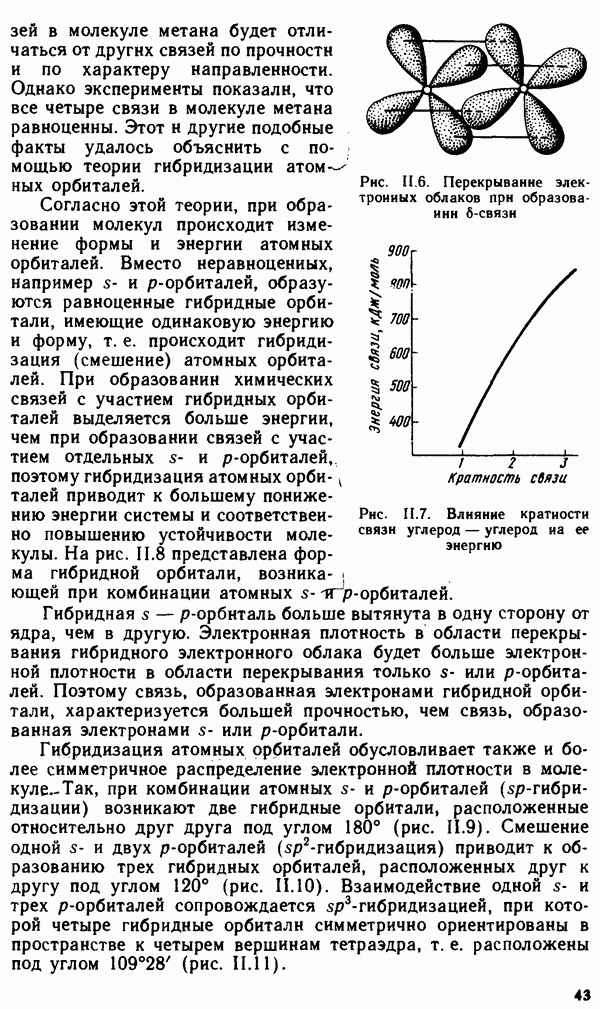
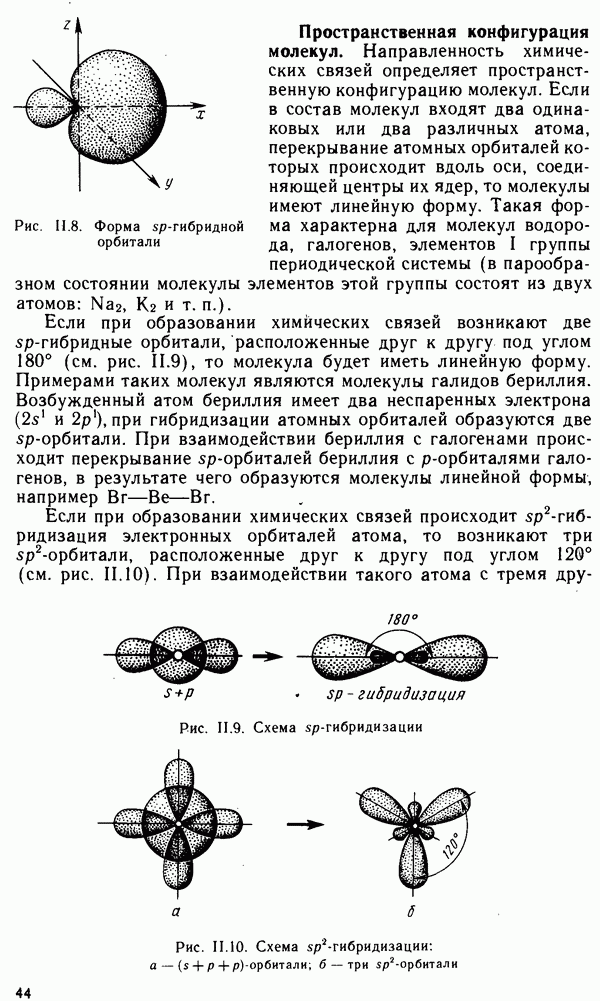
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
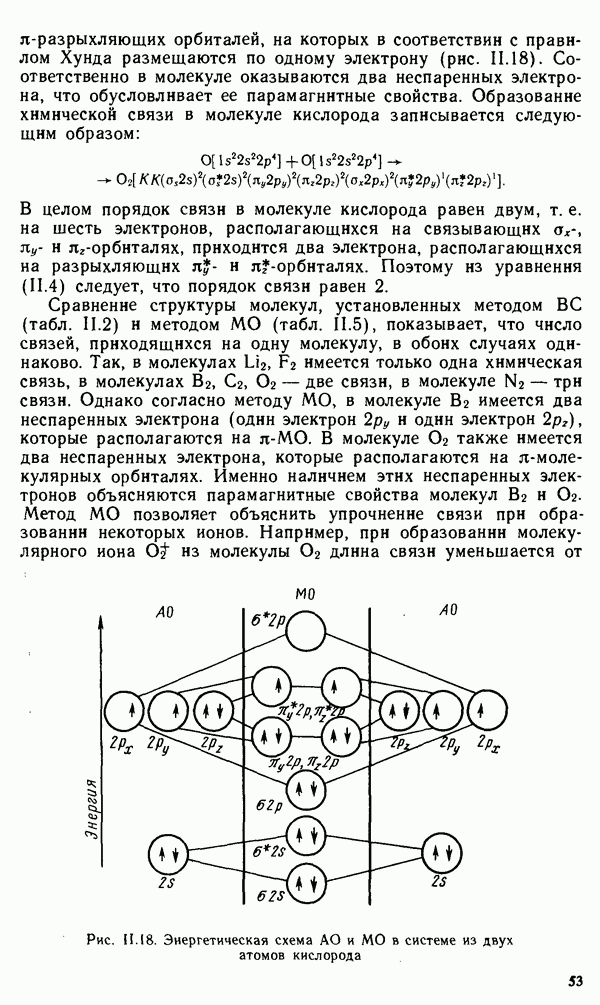
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
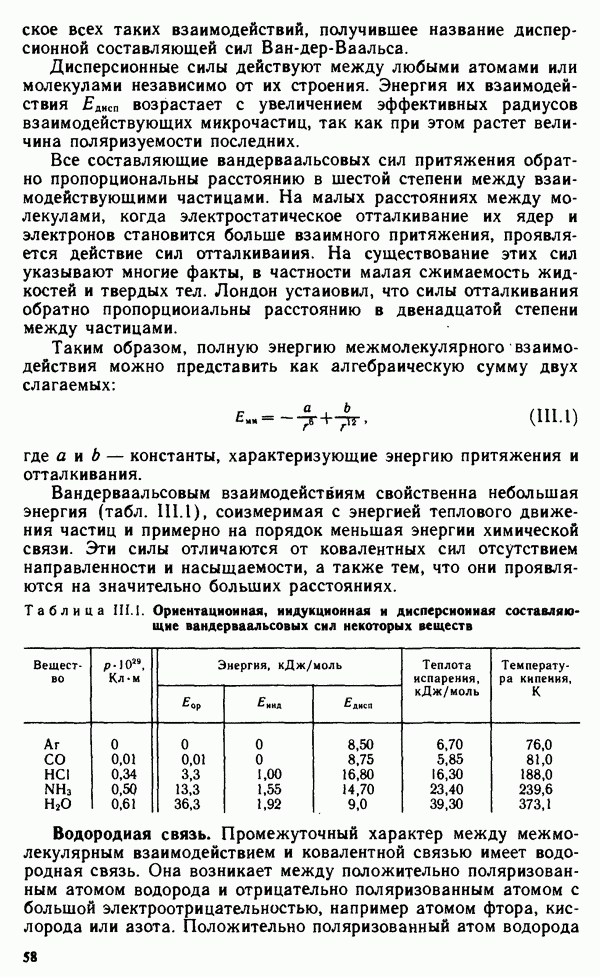
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
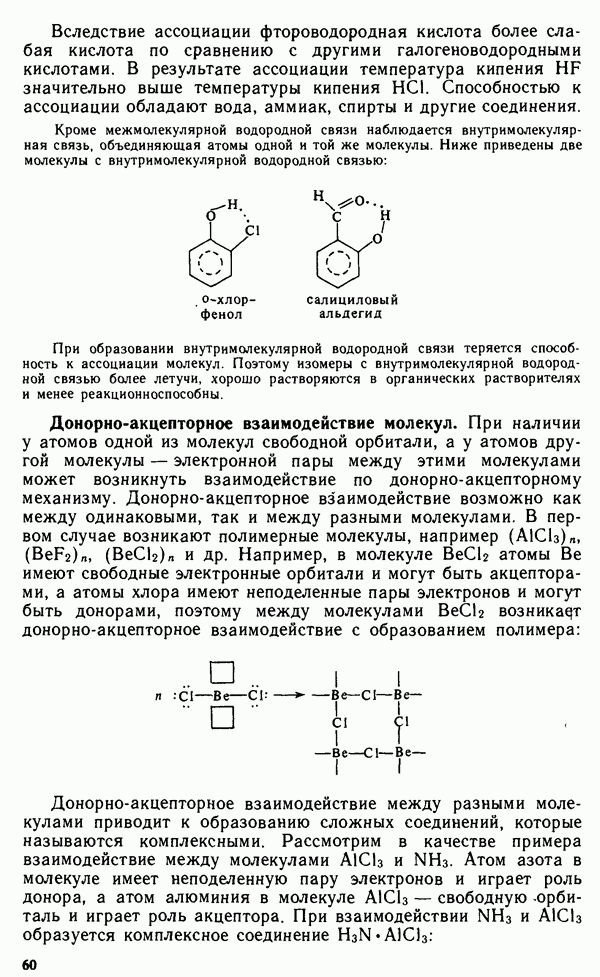
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
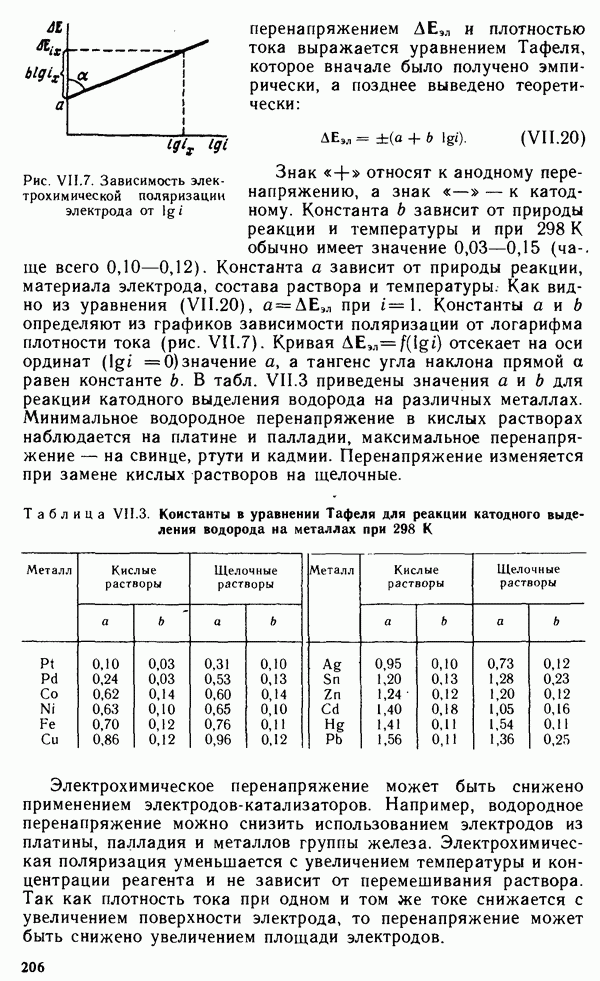
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
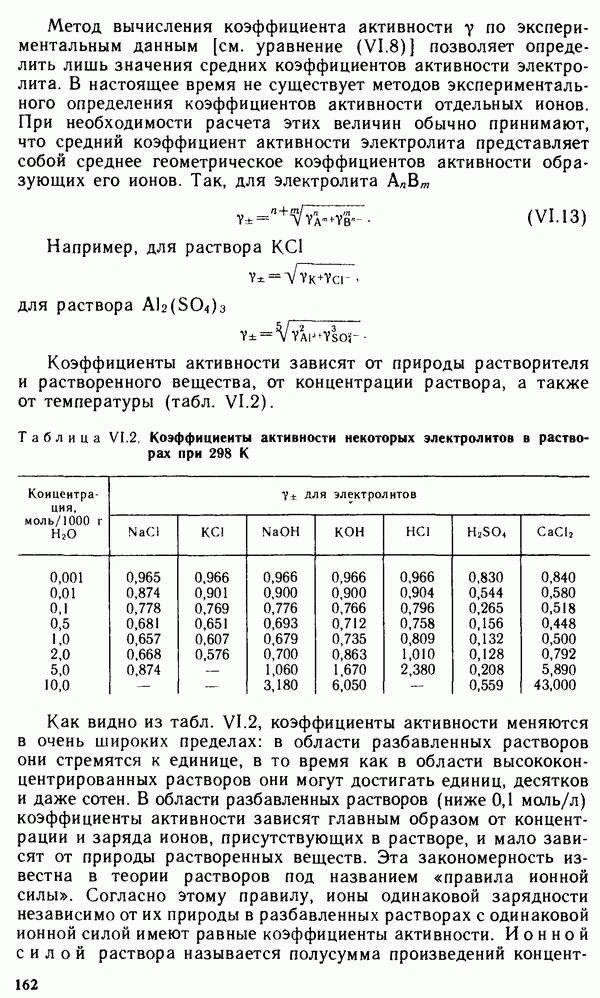
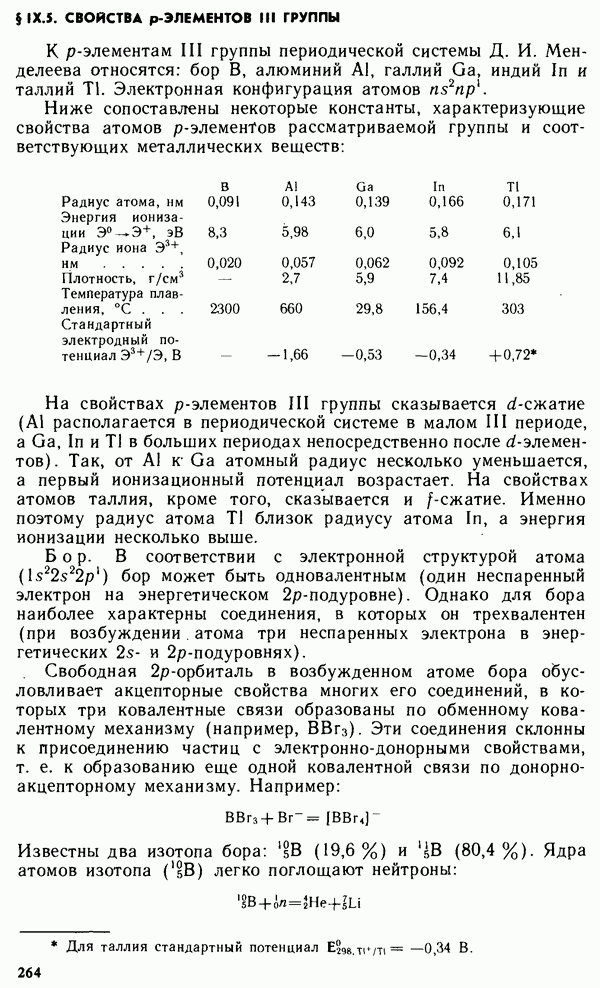
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
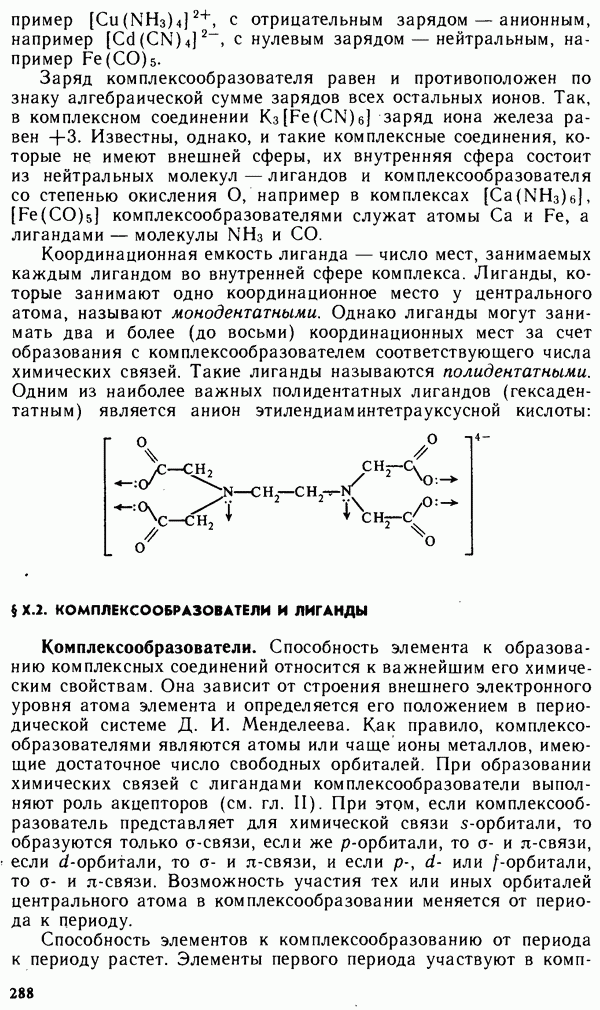
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
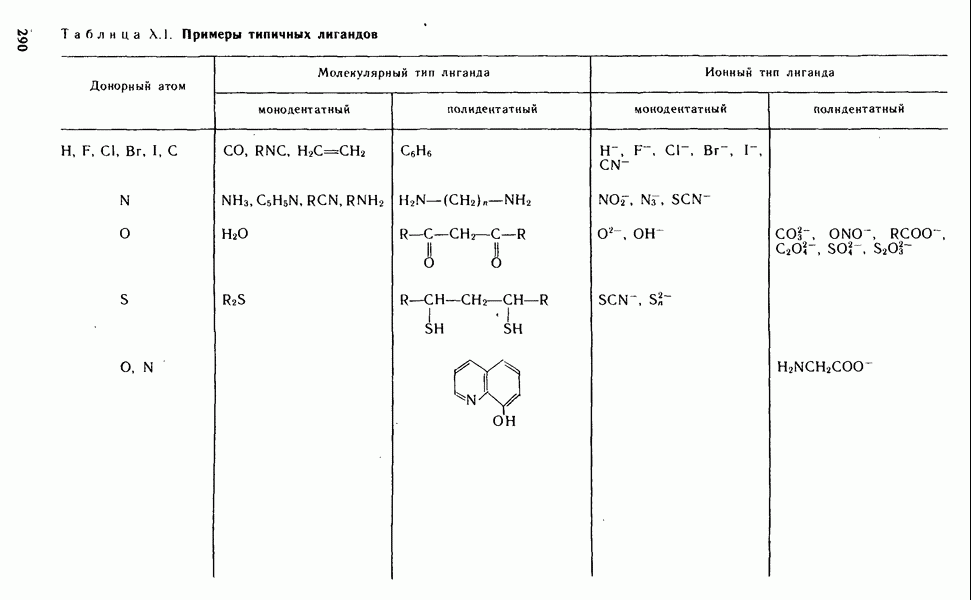
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
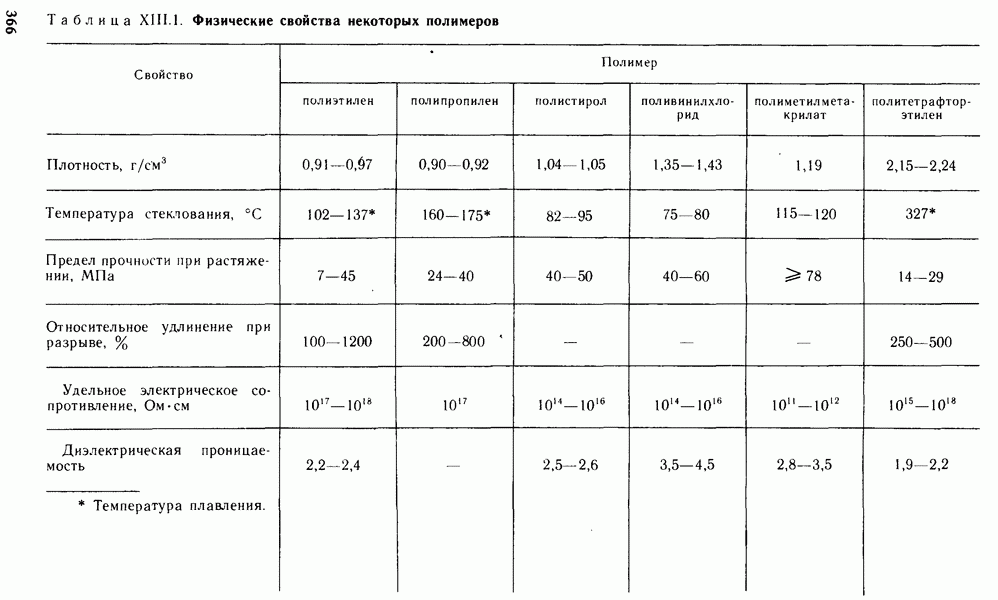
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
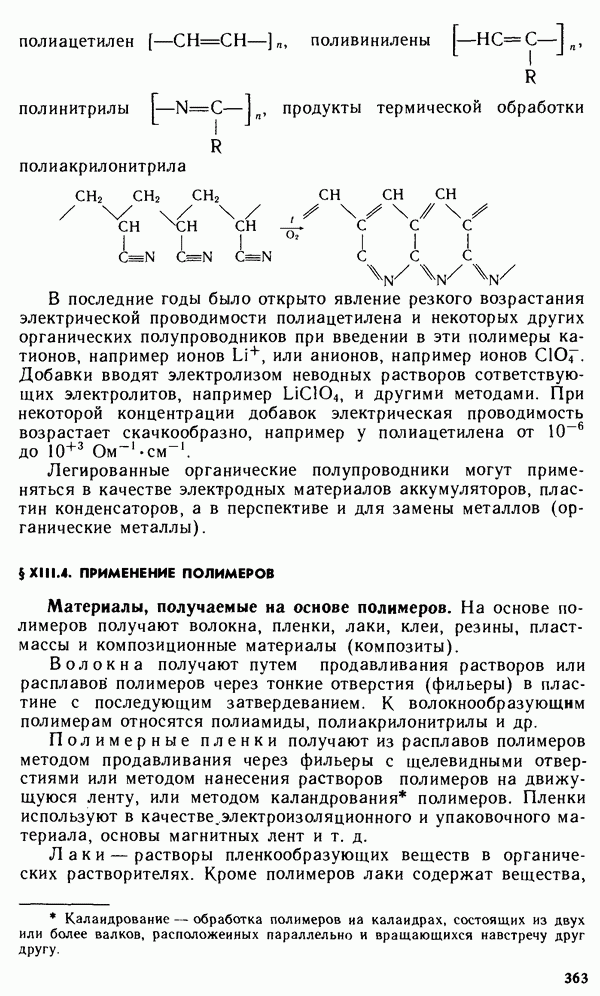
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ