| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
При замещении одного или нескольких атомов водорода в углеводородах на другие атомы или группы атомов, называемых функциональными группами, получают производные углеводородов: галогенопроизводные, спирты, альдегиды, кетоны, кислоты и т. д. Введение той или иной функциональной группы в состав соединения, как правило, коренным образом изменяет его свойства. Например, введение карбокси-группы —  приводит к появлению кислотных свойств у органических соединений. Сокращенную формулу производных углеводородов можно записать в виде
приводит к появлению кислотных свойств у органических соединений. Сокращенную формулу производных углеводородов можно записать в виде  где
где  — остаток углеводородов (радикал), Ф — функциональная
— остаток углеводородов (радикал), Ф — функциональная
группа. Например, карбоновую кислоту в общем виде можно представить формулой 
Галогенопроизводные углеводородов.
Формулу галогенопроизводного углеводорода можно представить в виде  где
где  — галоген;
— галоген;  — число атомов галогена. Вследствие полярности связи галоген — углерод галоген относительно легко замещается на другие атомы или функциональные группы, поэтому галогенопроизводные углеводородов широко используются в органическом синтезе. Прочность связи углерод — галоген растет от иода к фтору
— число атомов галогена. Вследствие полярности связи галоген — углерод галоген относительно легко замещается на другие атомы или функциональные группы, поэтому галогенопроизводные углеводородов широко используются в органическом синтезе. Прочность связи углерод — галоген растет от иода к фтору  поэтому фтороуглеводороды имеют высокую химическую устойчивость. Галогенопроизводные углеводородов широко применяются в технике. Так, многие из них (дихлорметан
поэтому фтороуглеводороды имеют высокую химическую устойчивость. Галогенопроизводные углеводородов широко применяются в технике. Так, многие из них (дихлорметан  тетрахлорметан
тетрахлорметан  дихлорэтан
дихлорэтан  и др.) используются как растворители.
и др.) используются как растворители.
Вследствие высокой теплоты испарения, негорючести, нетоксичности и химической инертности фтороуглероды и смешанные галогенопроизводные нашли применение в качестве рабочих тел в холодильных устройствах — хладонов (фреонов), например:  (хладон 12),
(хладон 12),  (хладон
(хладон  (хладон 22),
(хладон 22),  (хладон 114). Хладоны также используются при тушении пожаров. В связи с массовым применением хладонов (фреонов) возникла проблема предотвращения их вредного влияния на окружающую среду, поскольку при испарении хладонов происходит их разложение и взаимодействие галогенов, особенно фтора, с озонным слоем.
(хладон 114). Хладоны также используются при тушении пожаров. В связи с массовым применением хладонов (фреонов) возникла проблема предотвращения их вредного влияния на окружающую среду, поскольку при испарении хладонов происходит их разложение и взаимодействие галогенов, особенно фтора, с озонным слоем.
Галогенопроизводные предельных углеводородов, например  служат исходными мономерами для получения ценных полимеров (поливинилхлорида, фторопласта).
служат исходными мономерами для получения ценных полимеров (поливинилхлорида, фторопласта).
Спирты и фенолы.
Спирты — это производные углеводородов, у которых один или несколько атомов водорода замещены на гидроксидные группы. В зависимости от углеводородов, спирты подразделяются на предельные и непредельные, по числу гидроксидных групп в соединении различают одноатомные (например,  и многоатомные (например, глицерин
и многоатомные (например, глицерин  спирты. В зависимости от числа углеродных атомов, соединенных с атомом углерода, у которого расположена гидроксидная группа, различают первичные
спирты. В зависимости от числа углеродных атомов, соединенных с атомом углерода, у которого расположена гидроксидная группа, различают первичные 
вторичные  и третичные
и третичные  спирты.
спирты.
Название спиртов получают добавлением суффикса  к названию углеводорода (или -диол, триол и т. д. в случае многоатомных спиртов), а также указанием номера атома углерода, у которого расположена гидроксидная группа, например:
к названию углеводорода (или -диол, триол и т. д. в случае многоатомных спиртов), а также указанием номера атома углерода, у которого расположена гидроксидная группа, например:


Из-за полярности связи кислород — водород молекулы спиртов полярны. Низшие спирты хорошо растворимы в воде, однако по мере увеличения числа атомов углерода в углеводородном радикале влияние гидроксидной группы на свойства уменьшается и растворимость спиртов в воде понижается. Молекулы спиртов ассоциированы из-за образования водородных связей между ними, поэтому температуры их кипения выше температур кипения соответствующих углеводородов.
Спирты являются амфотериыми соединениями, при воздействии щелочных металлов образуются легко гидролизуемые алкоголяты:

При взаимодействии с галогеноводородными кислотами происходит образование галогенопроизводных углеводородов и воды:

Однако спирты — очень слабые электролиты.
Простейшим из предельных спиртов является метанол  который получают из оксида углерода и водорода под давлением, при повышенной температуре в присутствии катализатора:
который получают из оксида углерода и водорода под давлением, при повышенной температуре в присутствии катализатора:

Учитывая относительную простоту синтеза метанола, возможность получения исходных реагентов из угля, некоторые ученые предполагают, что метанол в будущем найдет более широкое применение в технику, в том числе в транспортной энергетике. Смесь метанола и бензина может быть эффективно использована в двигателях внутреннего сгорания. Недостатком метаиола является его высокая токсичность.
Этанол  получают брожением углеводов (сахара или крахмала):
получают брожением углеводов (сахара или крахмала):

Исходным сырьем в этом случае служат либо пищевые продукты, либо целлюлоза, которую гидролизом превращают в глюкозу. В последние годы все более широкое применение получает метод каталитической гидратации этилена:

Использование метода гидролиза целлюлозы и гидратации этилена позволяет экономить пищевое сырье. Хотя этанол один из наименее токсичных спиртов, однако из-за него гибнет значительно
больше людей, чем из-за любого другого химического вещества.
При замещении водорода ароматического кольца на гидроксидную группу образуется фенол. Под влиянием бензольного кольца полярность связи кислород — водород возрастает, поэтому фенолы диссоциируют в большей степени, чем спирты, проявляют кислотные свойства. Атом водорода в гидроксидной группе фенола может быть замещен на катион металла под воздействием основания:

Фенол широко используется в промышленности, в частности служит сырьем для получения фенолформальдегидных полимеров.
Альдегиды и кетоны.
При окислении и каталитическом дегидрировании спиртов можно получить альдегиды и кетоны — соединения, содержащие карбонильную группу 

Как видно, при окислении или дегидрировании первичного спирта получается альдегид, вторичного спирта — кетон. Атом углерода карбонильной группы альдегидов связан с одним атомом водорода и с одним атомом углерода (радикалом). Атом углерода карбонильной группы кетонов связан с двумя атомами углерода (с двумя радикалами).
Названия альдегидов и кетонов производят от названий углеводородов, прибавляя суффиксы -аль в случае альдегида и -он в случае кетона, например:

Связь кислород — углерод карбонильной группы альдегидов сильно поляризована, поэтому альдегиды характеризуются высокой реакционной способностью, они являются хорошими восстановителями, легко вступают в реакции замещения, присоединения, конденсации и полимеризации. Простейший альдегид — метаналь (формальдегид или муравьиный альдегид)  склонен к
склонен к
самопроизвольной полимеризации. Его применяют для получения фенолформальдегидных и мочевиноформальдегидных смол и полиформальдегида.
Кетоны обладают меньшей реакционной способностью, чем альдегиды, так как карбонильная группа менее полярна. Поэтому они труднее окисляются, восстанавливаются и полимеризуются. Многие кетоны, в частности ацетон, являются хорошими растворителями.
Карбоновые кислоты.
У карбоновых кислот функциональной является карбоксильная группа -СООН. В зависимости от числа карбоксильных групп в молекуле кислоты их подразделяют на одно-, двух- и многоосновные, а в зависимости от радикала, связанного с карбоксильной группой, — на алифатические (предельные и непредельные), ароматические, алициклические и гетероциклические. По систематической номенклатуре названия кислот производят от названия углеводорода, добавляя окончание -овая и слово кислота, например  — бутановая кислота.
— бутановая кислота.
Однако часто применяют тривиальные названия, сложившиеся исторически, например:

Кислоты обычно получают окислением альдегидов. Например, при гидратации ацетилена с последующим окислением образующегося ацетальдегида получают уксусную кислоту:

Недавно был предложен способ получения уксусной кислоты, основанный на реакции метанола с монооксидом углерода в присутствии родиевого катализатора

Кислотные свойства карбоксильной группы обусловлены отщеплением протона при электролитической диссоциации кислот. Отщепление протона связано со значительной поляризованностью связи О-Н, вызванной смещением электронной плотности от атома углерода к атому кислорода карбоксильной группы

Все карбоновые кислоты — слабые электролиты и в химическом отношении ведут себя подобно неорганическим слабым кислотам. Они взаимодействуют с оксидами и гидроксидами металлов, образуя соли.
К одной из особенностей карбоновых кислот можно отнести их взаимодействие с галогеном, приводящее к образованию галогенозамещенных карбоновых кислот. Из-за присутствия галогенов в молекуле кислоты происходит поляризация связи О-Н, поэтому галогенозамещенные кислоты являются более сильными, чем исходные карбоновые кислоты. Со спиртами кислоты образуют сложные эфиры

При замещении гидроксидной группы кислот на аминогруппу  образуются амиды кислот, например
образуются амиды кислот, например

Карбоновые кислоты широко применяются в технике. Некоторые из них являются исходными соединениями для получения волокон, пленок и лаков. Например, терефталевая кислота используется для получения лавсана и терилена, адипиновая кислота  — найлона, акриловая кислота — органического стекла.
— найлона, акриловая кислота — органического стекла.
Амины.
При замещении в аммиаке водорода на органические радикалы получают амины. По числу замещаемых радикалов различают первичные  вторичные
вторичные  и третичные
и третичные  амины. Амин также можно считать производными углеводородов, у которых водород замещен на аминогруппу
амины. Амин также можно считать производными углеводородов, у которых водород замещен на аминогруппу
 или
или  Амины, как и аммиак, проявляют основные свойства.
Амины, как и аммиак, проявляют основные свойства.

При взаимодействии с кислотами они образуют соли

Амины являются исходным сырьем для получения красителей, высокомолекулярных и других соединений.
КОНТРОЛЬНЫЕ ВОПРОСЫ
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
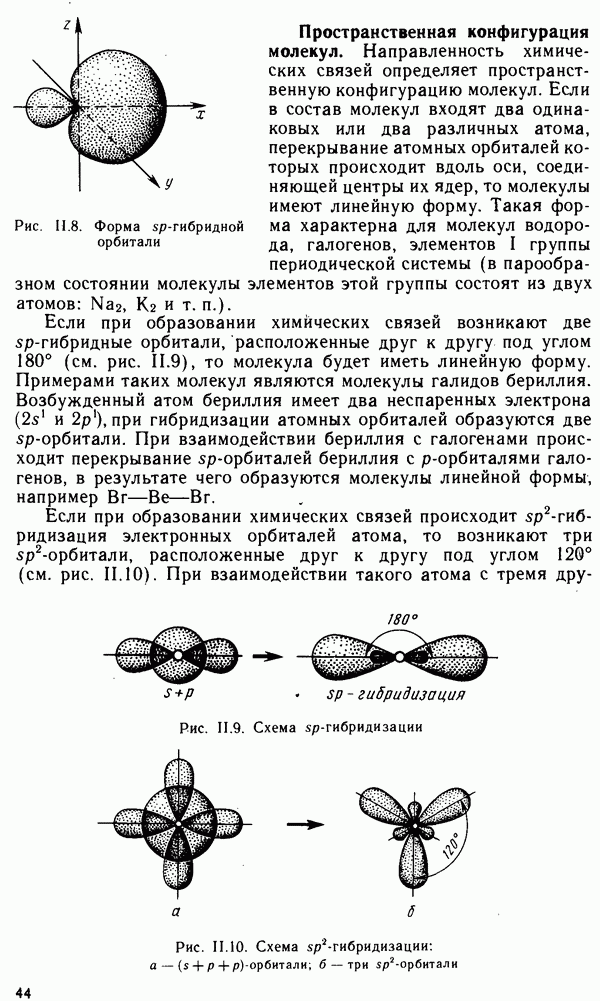
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
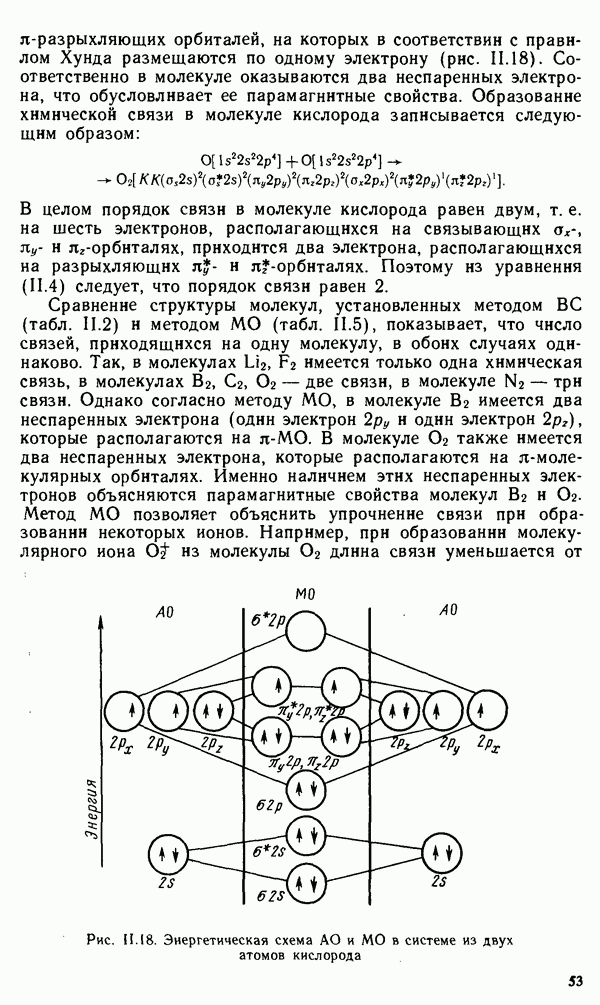
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
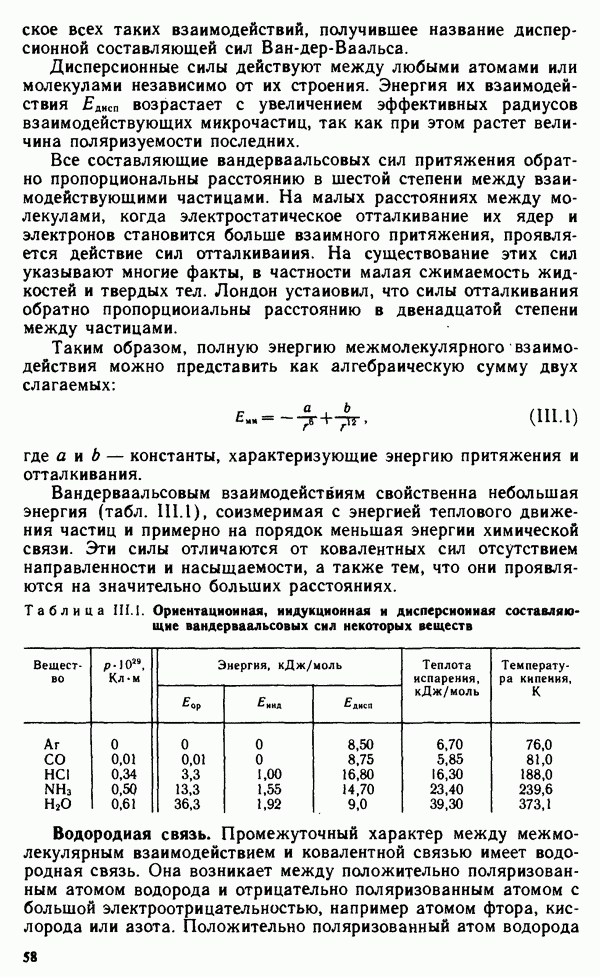
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
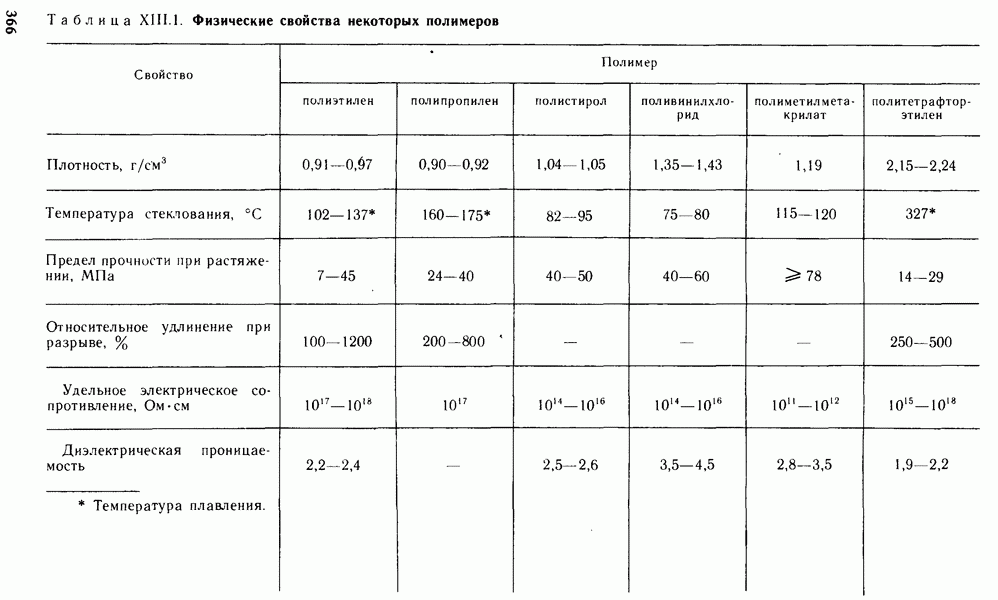
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ