| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
Успешное развитие техники привело к значительному расширению номенклатуры используемых химических веществ. При этом существенно возросли требования к чистоте применяемых материалов. Если раньше приемлемыми считались вещества с содержанием примесей порядка десятых долей процента, то в настоящее время для многих веществ предельно допустимая концентрация примесей не должна превышать  причем с каждым годом эти требования становятся все более жесткими.
причем с каждым годом эти требования становятся все более жесткими.
Материалы столь высокой чистоты можно получить или с помощью глубокой очистки соответствующих технических продуктов, или синтезом из других особо чистых веществ. Однако ни тот, ни другой методы не позволяют получить абсолютно химически чистое вещество. Скорость любого химического процесса, в том числе и процесса удаления примесей, падает с уменьшением концентрации реагентов. Поэтому удаление из вещества следов примесей потребовало бы бесконечно большого времени. На практике вещество считают чистым, если оно не содержит примесей такого рода и в таких количествах, которые затрудняют использование этого вещества для данной конкретной цели.
Количественным показателем степени чистоты вещества служит концентрация в нем примесей, выраженная в атомных либо молярных долях. В СССР принято несколько способов классификации чистоты химических веществ. Так, вещества подразделяют по допустимой области их применения, например вещества реакторной, полупроводниковой чистоты и т. п. Чистоту вещества можно оценить по так называемому «баллу чистоты», равному десятичному логарифму числа атомов основного вещества, приходящихся на один атом примеси. В производстве химических реактивов вещества по степени их чистоты подразделяют на три класса и десять подклассов: класс А с содержанием примесей от  (I) до
(I) до  класс В с содержанием примесей от
класс В с содержанием примесей от  (III) до
(III) до  и класс С с содержанием примесей от
и класс С с содержанием примесей от  (VII) до
(VII) до  Начиная с
Начиная с  примесные компоненты называют микропримесями. Те или иные примеси в веществе по-разному влияют на его свойства, поэтому их предельно допустимая концентрация может быть различной. Компоненты, влияние которых на рабочие характеристики материала наиболее значительно, получили название лимитирующих примесей. Примерами подобных примесей в материалах ядерной энергетики служат бор, гафний и кадмий, атомное содержание которых в основном материале не должно превышать
примесные компоненты называют микропримесями. Те или иные примеси в веществе по-разному влияют на его свойства, поэтому их предельно допустимая концентрация может быть различной. Компоненты, влияние которых на рабочие характеристики материала наиболее значительно, получили название лимитирующих примесей. Примерами подобных примесей в материалах ядерной энергетики служат бор, гафний и кадмий, атомное содержание которых в основном материале не должно превышать  в то
в то
время как допустимое содержание других примесей составляет 0,03-0,04 %,
В основе процессов глубокой очистки веществ лежат методы, использующие какой-либо разделительный эффект, обусловленный различием свойств основного компонента и примеси, например разными энергиями связи, летучестью, растворимостью и т. п. Для получения веществ высокой чистоты применяют химические, физико-химические, электрохимические, хроматографические, дистилляционные, кристаллизационные и другие методы. При этом, за редким исключением, перечисленные методы комбинируют в виде многоступенчатых процессов. Лишь такой подход позволяет получать вещества заданной степени чистоты.
Химические методы очистки материалов являются самыми универсальными. Многообразие химических веществ почти всегда позволяет подобрать реагент, по-разному взаимодействующий с основными и примесными компонентами, например переводящий один из них в осадок или в газообразное состояние. При этом появляется возможность разделить указанные компоненты фильтрацией, перегонкой, газоулавливанием или другими физико-химическими методами. Среди химических реагентов, применяемых в процессах очистки веществ, широко используются минеральные кислоты, щелочи, сильные окислители, а также различные комплексообразователи. Химическая обработка твердых веществ позволяет освободиться лишь от примесных включений, находящихся на их поверхности. Поэтому при очистке твердых веществ проводят их предварительное измельчение.
Не менее ответственной операцией после реагентной обработки является отделение примесей от основного материала. На этой стадии эффективность процесса очистки во многом будет зависеть как от полноты разделения компонентов, так и от степени их вторичного загрязнения материалом аппаратуры. Вторичное загрязнение заметно при больших поверхностях соприкосновения, например в процессах фильтрации или газоулавливания, а также при повышенных температурах процессов. Так, пропускание паров серы через кварцевый реактор, нагретый до 800 °С, приводит к повышению содержания кремния от 0,005 до  Вероятность вторичного загрязнения следует учитывать не только в процессе очистки, но и при выборе условий хранения и использования очищенного вещества. Вторичное загрязнение продукта можно снизить, используя для изготовления аппаратуры химически стойкие материалы, такие, как фторопласты, нитриды бора, кремния и др.
Вероятность вторичного загрязнения следует учитывать не только в процессе очистки, но и при выборе условий хранения и использования очищенного вещества. Вторичное загрязнение продукта можно снизить, используя для изготовления аппаратуры химически стойкие материалы, такие, как фторопласты, нитриды бора, кремния и др.
Понижение температуры процессов очистки возможно переводом очищаемого вещества в форму какого-либо летучего или легкоплавкого соединения. Так, т. пл. германия 959 °С, а его гидрида  и хлорида
и хлорида  соответственно 165 и 49,6 °С. Чаще всего в процессах химической очистки материалов практикуется их перевод в летучие гидриды, галиды, карбонилы или
соответственно 165 и 49,6 °С. Чаще всего в процессах химической очистки материалов практикуется их перевод в летучие гидриды, галиды, карбонилы или
элементоорганические соединения. После перевода очищаемого тугоплавкого вещества в одну из подобных форм проводится глубокая очистка полученного соединения, а затем его перевод в состояние исходного материала в очищенном виде. Последнюю операцию обычно проводят или термическим разложением летучего соединения, или его восстановлением водородом. Специфика химических методов очистки требует обязательного контакта очищаемого вещества как с вводимым реагентом, так и с материалом аппаратуры. Поэтому химические способы часто не позволяют достичь высоких степеней очистки и их обычно используют на начальных стадиях процесса или для удаления отдельных примесей, или для перевода в форму, легко отделимую последующими операциями.
Одним из способов очистки является метод транспортных реакций. Транспортными называют обратимые гетерогенные реакции, при протекании которых вещество в форме, как правило, газообразного соединения способно переноситься из одной зоны реактора в другую при наличии между этими зонами разности температур или давлений. Примером метода транспортных реакций является иодидный способ очистки циркония. Порошкообразный металл нагревают в вакуумированной ампуле до 300 °С вместе с кристаллами иода. При этом протекает обратимая реакция по уравнению

Образовавшийся газообразный  затем разлагается на циркониевой проволоке, нагретой до 300 °С, причем чистый цирконий оседает на ней в виде кристаллов, а выделившийся иод вновь реагирует с исходным металлом.
затем разлагается на циркониевой проволоке, нагретой до 300 °С, причем чистый цирконий оседает на ней в виде кристаллов, а выделившийся иод вновь реагирует с исходным металлом.
Преимущества метода транспортных реакций заключаются в стерильности всех операций, возможности очистки малых количеств материала, а также получении его в удобной для практических целей форме, например в виде пленок, пластинок или монокристаллов.
К недостаткам метода следует отнести малую скорость процесса, низкий выход продукта, а также невозможность глубокого разделения элементов-аналогов.
Широкое применение в производстве особо чистых веществ находят электрохимические методы. Они базируются на хорошо известном в прикладной электрохимии правиле, согласно которому на аноде из нескольких возможных процессов окисления прежде всего протекает тот, потенциал которого в данных условиях наиболее отрицателен. На катоде в первую очередь будут восстанавливаться те частицы, потенциал которых наиболее положителен. Таким образом, в процессе электролиза появляется возможность отделения основного компонента от примеси с более положительными потенциалами за счет анодных процессов, а также от примесей с более отрицательными потенциалами
за счет протекания катодных реакций. Для глубокой электрохимической очистки материалов обычно используют многоступенчатый электролиз. Наибольшее распространение электрохимические методы получили в процессах очистки (рафинирования) металлов.
Электрохимические методы широко используются и в процессах очистки растворов. Скорость движения ионов в растворе пропорциональна напряженности приложенного электрического поля, в то время как скорость движения молекул от него не зависит. Эта закономерность позволяет проводить эффективное отделение электролитов от неэлектролитов.
Для разделения смесей электролитов на пути движения ионов в электролизере ставят различные диафрагмы или камеры с гранулированным, как правило, ионообменным материалом. За счет различного взаимодействия ионов с материалом гранул, или диафрагм, скорость их движения в электрическом поле изменяется и появляется возможность пространственного разделения
ионных потоков. Подобные процессы получили название электродиализа.
К электродиализным методам очистки близки по закономерностям процессы ультрафнльтрации, в которых растворы продавливаются через диафрагмы или колонки с разделительным материалом за счет градиента давления.
Однако перечисленные методы не могут обеспечить высокой степени очистки из-за обратимости ионного взаимодействия, а также больших площадей контакта с разделяющим материалом.
Более глубокой степени очистки растворов позволяют достичь хроматографические методы, основанные на пропускании порций раствора через колонки, заполненные материалом, специфически взаимодействующим с растворенными компонентами. Хроматографические методы наиболее эффективны при удалении следов примесей. Так, 35-38-кратное пропускание дистиллированной воды через колонки, заполненные катионо- и анионообменными смолами, позволило получить воду с электрической проводимостью, близкой к теоретически рассчитанной величине 
Недостатком рассматриваемого метода очистки служит малая скорость процесса. Для ее повышения используют реакторы с «кипящим» слоем ионообменного материала; однако при этом заметно снижается эффективность разделения.
В последнее время широкое распространение получили экстракционные методы очистки веществ, при которых очищаемый водный раствор контактирует с соответствующим растворителем, не смешивающимся с водой. Скорость разделения веществ в экстракционных процессах весьма высока, да и возможности метода значительно шире из-за наличия большого числа известных растворителей, специфически растворяющих то или иное из разделяемых веществ.
Дистилляционные методы глубокой очистки основаны
на известном законе Коновалова, согласно которому насыщенный пар по сравнению с раствором относительно богаче тем компонентом, добавление которого к системе повышает общее давление пара. Содержание устраняемой примеси в паровой фазе почти всегда иное, чем в жидкости.
Если коэффициент разделения значителен, то очистку раствора можно провести простой перегонкой, испаряя очищаемую жидкость с последующей конденсацией образовавшегося пара. Однако значительно более эффективными являются процессы ректификации. Они осуществляются в аппаратах колонного типа, заполненных насадкой или имеющих многочисленные поперечные перегородки — тарелки с отверстиями. В процессе ректификации происходит испарение жидкости, и сконденсировавшийся в верхней части колонны пар стекает вниз по тарелкам или насадке. За счет встречного движения пара и жидкости достигается многократный массо- и теплообмен, в результате которого более летучий компонент накапливается преимущественно в верхней, а менее летучий — в нижней части колонны.
В настоящее время дистилляционные методы являются самыми распространенными в процессах очистки веществ. Суммарное атомное содержание примесей в очищенных веществах при этом снижается до  а лимитирующих — до
а лимитирующих — до 
Наиболее эффективными для глубокой очистки веществ являются методы, основанные на процессах кристаллизации и на том, что содержание примесей в твердой фазе иное, чем в равновесной с ней жидкости. Для оценки этого различия используют коэффициент распределения, представляющий собой отношение молярных долей примесей в твердой и жидкой фазах.
Кристаллизацию веществ в процессе их очистки проводят или из раствора, или из расплава. Первый способ широко используется как одна из начальных стадий очистки солей и щелочей и относительно малоэффективен. Способы второго типа включают в себя направленную и противоточную кристаллизацию, зонную плавку, а также вытягивание из расплава. Все они базируются на постепенной кристаллизации очищаемого вещества за счет перемещения нагревательных элементов вдоль его объема. При этом примеси, для которых коэффициент распределения меньше единицы, будут обогащать жидкую часть слитка, а примеси, для которых он больше единицы, концентрируются в его кристаллической части. Многократное повторение процессов плавления и кристаллизации (от 10 до нескольких сотен) приводит к накоплению примесей в головной и концевой частях слитка, составляющих около 30 % его объема.
Преимущество методов кристаллизации из расплавов заключается в возможности исключения прямого контакта очищаемого образца со вспомогательной аппаратурой. Поэтому эти методы применяют для глубокой очистки тугоплавких материалов, оксидов и солей. В методе вытягивания из расплава проводят выращивание
монокристалла вещества на вращающейся затравочной пластинке с параллельной его очисткой от примесей с коэффициентом распределения меньшим единицы. Рассматриваемые методы кристаллизации из расплава позволяют не только очищать вещества, но и вводить в них заданные количества тех или иных микропримесей. В настоящее время кристаллизационные методы очистки считаются самыми тонкими и их обычно применяют на заключительных стадиях получения особо чистых веществ, в том числе полупроводниковых материалов.
КОНТРОЛЬНЫЕ ВОПРОСЫ
(см. скан)
(см. скан)
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
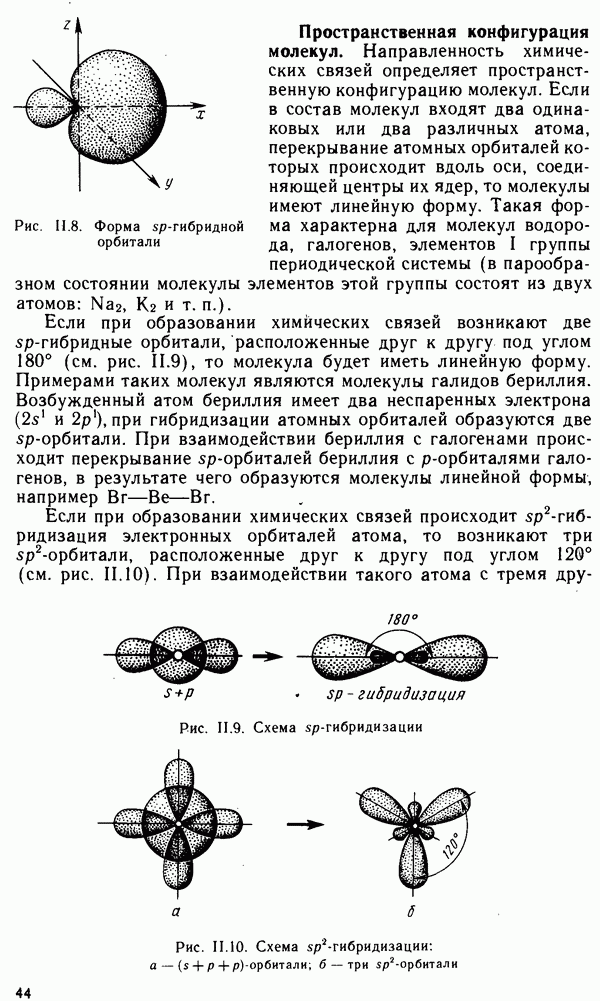
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
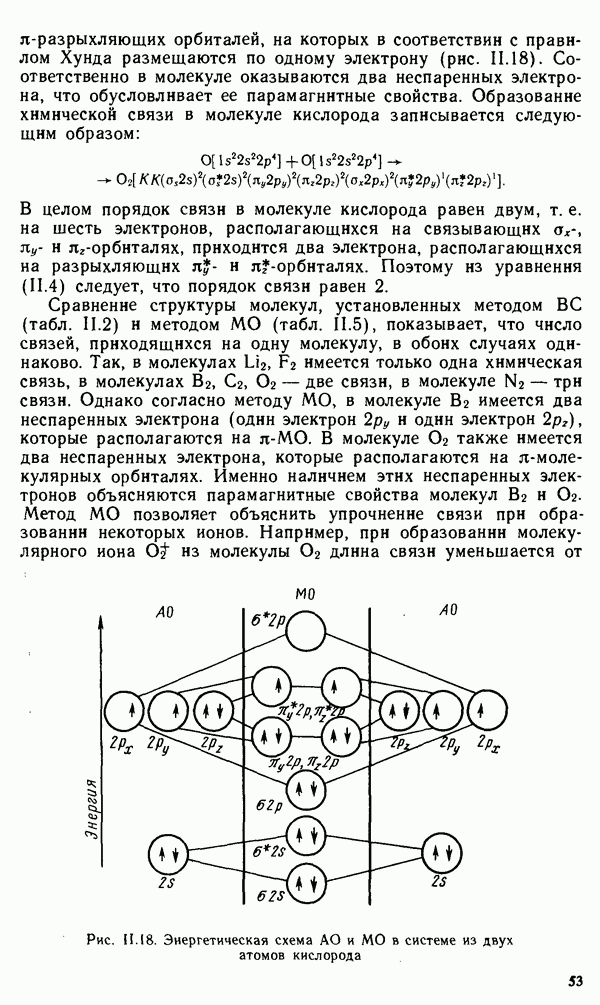
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
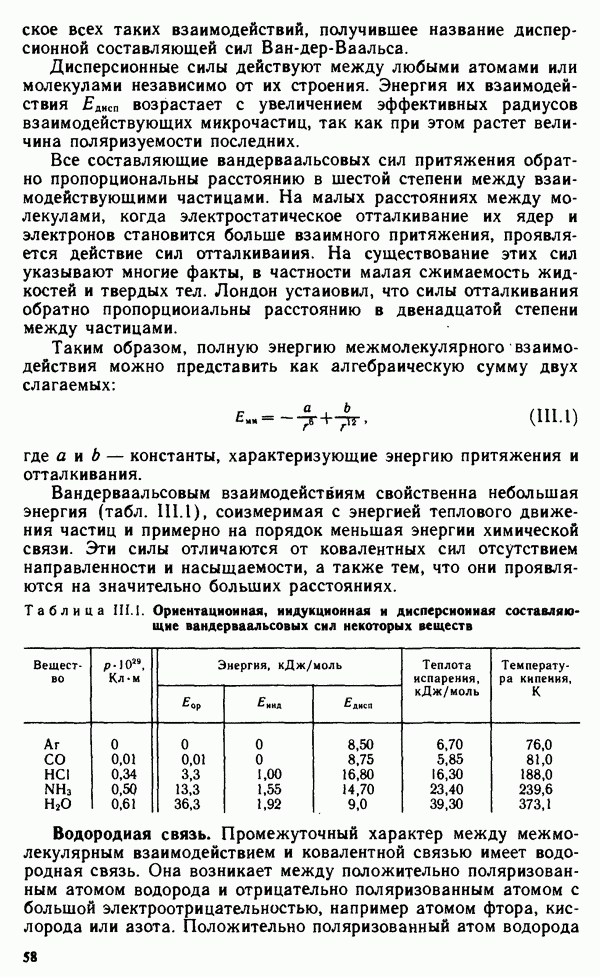
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
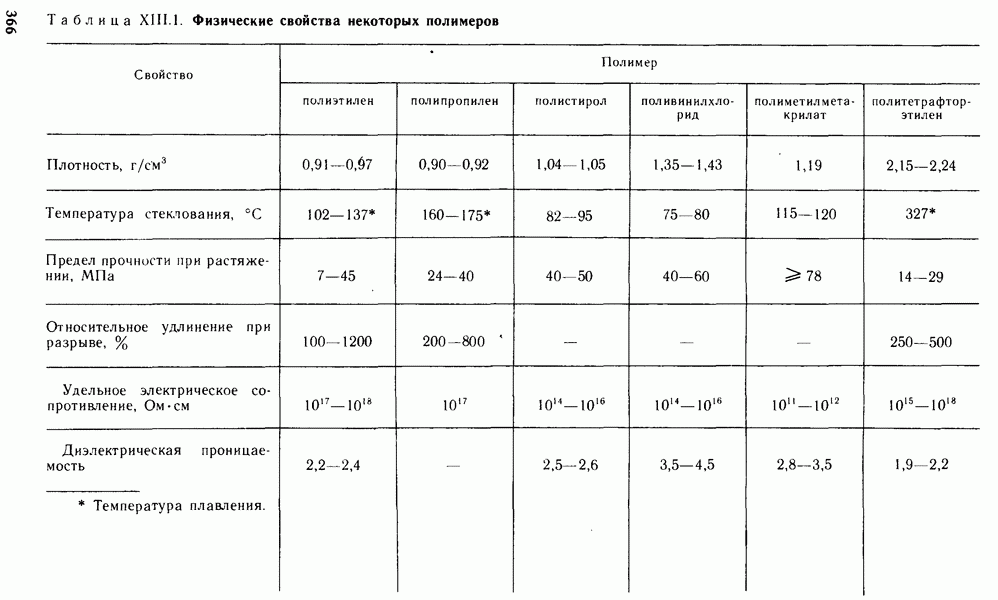
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ