| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ XI.2. УГЛЕВОДОРОДЫ
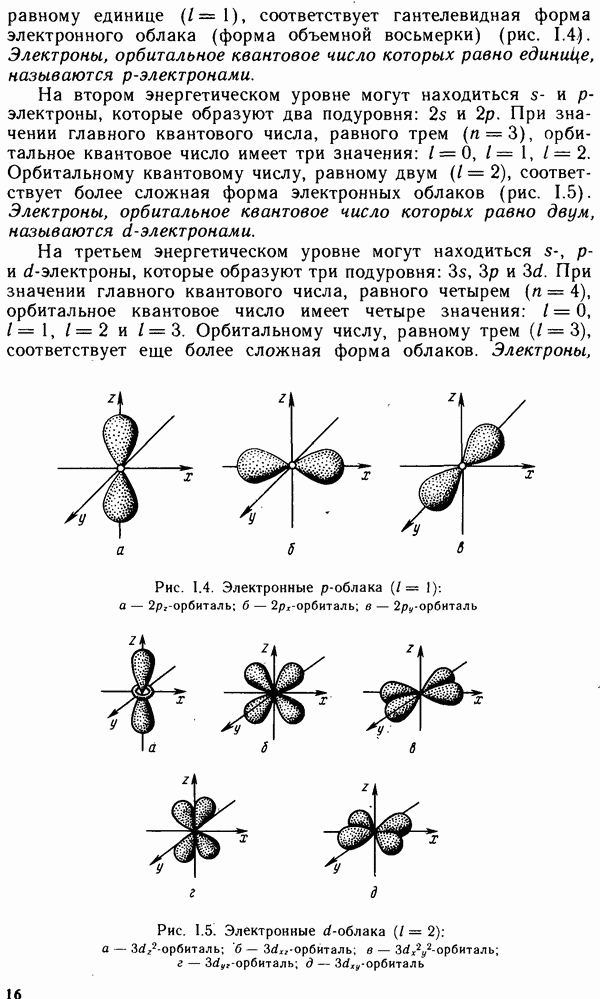
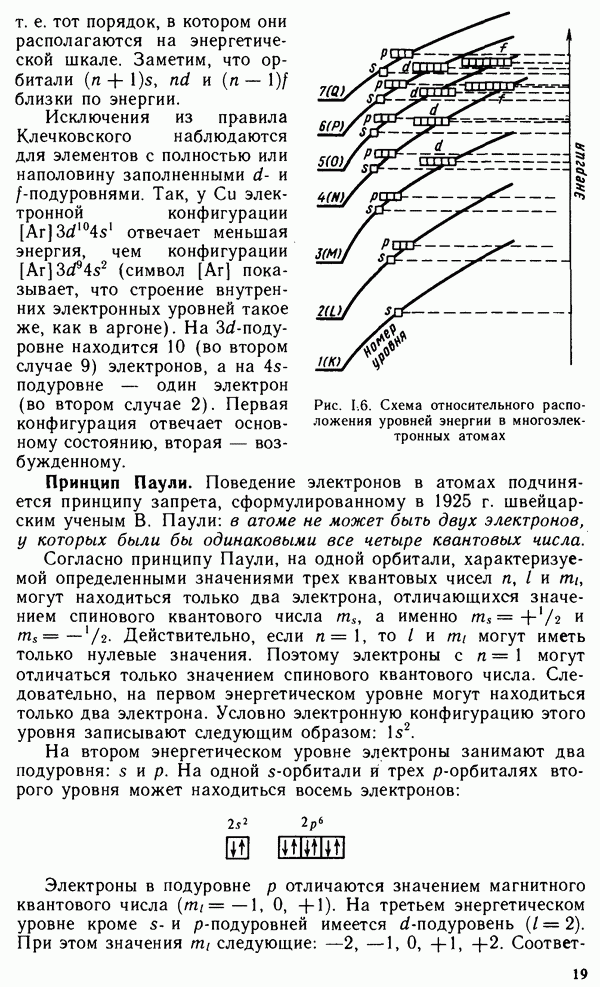
Природа химических связей в углеводородах.
Атом углерода в возбужденном состоянии имеет четыре неспаренных электрона.

При образовании химических связей может происходить  или
или  -гибридизация атомных орбиталей углерода.
-гибридизация атомных орбиталей углерода.
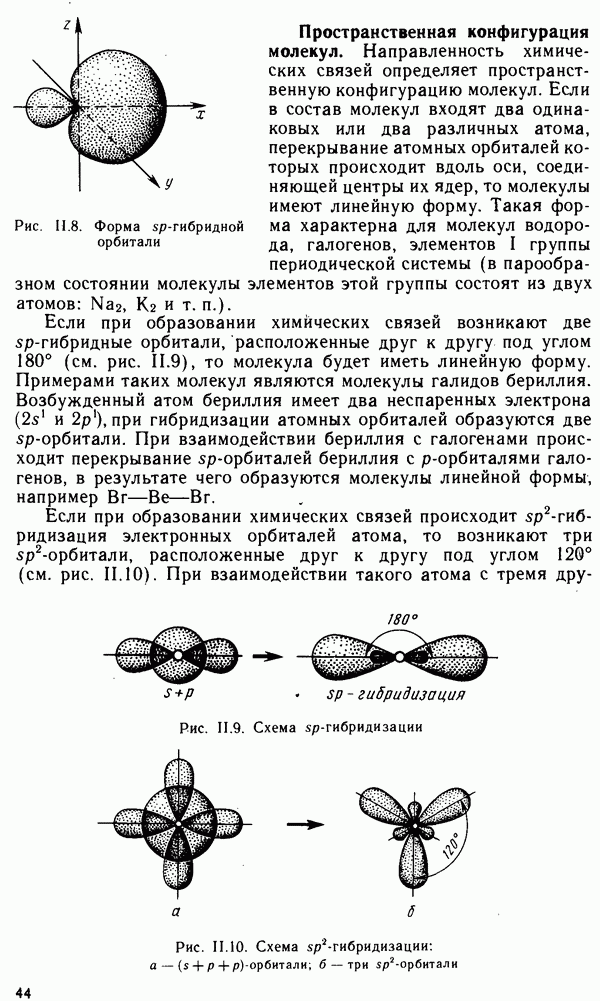
При  -гибридизации возникают четыре равноценные орбитали, расположенные в пространстве относительно друг друга под углом 109,5°. Каждый атом углерода образует четыре ковалентные связи с другими атомами углерода и с атомами водорода. В результате образуются предельные углеводороды или алканы, у которых все валентности углеродных атомов насыщены
-гибридизации возникают четыре равноценные орбитали, расположенные в пространстве относительно друг друга под углом 109,5°. Каждый атом углерода образует четыре ковалентные связи с другими атомами углерода и с атомами водорода. В результате образуются предельные углеводороды или алканы, у которых все валентности углеродных атомов насыщены

Простая углерод-углеродная связь способна вращаться вокруг своей оси, поэтому происходит постоянное изменение (конформация) формы молекул. Вследствие внутреннего движения в молекулах углеродные цепи могут образовать кольца (циклы), в результате возникают алициклические соединения или циклоалканы.
В случае  -гибридизации у атома углерода появляются три гибридные орбитали и сохраняется одна негибридная р-орбиталь. Гибридные орбитали находятся в одной плоскости под углом 120° относительно друг друга, а р-орбиталь расположена перпендикулярно этой плоскости. Соответственно атом углерода образует три
-гибридизации у атома углерода появляются три гибридные орбитали и сохраняется одна негибридная р-орбиталь. Гибридные орбитали находятся в одной плоскости под углом 120° относительно друг друга, а р-орбиталь расположена перпендикулярно этой плоскости. Соответственно атом углерода образует три  -связи с атомом углерода и атомом водорода и одну
-связи с атомом углерода и атомом водорода и одну  -связь с атомом углерода. При
-связь с атомом углерода. При  -гибридизации атомных орбиталей у двух атомов углерода образуются алкены — непредельные углеводороды с одной двойной связью
-гибридизации атомных орбиталей у двух атомов углерода образуются алкены — непредельные углеводороды с одной двойной связью

При  -гибридизации атомных орбиталей у четырех атомов углерода образуются диены (алкадиены) — непредельные углеводороды с двумя двойными связями.
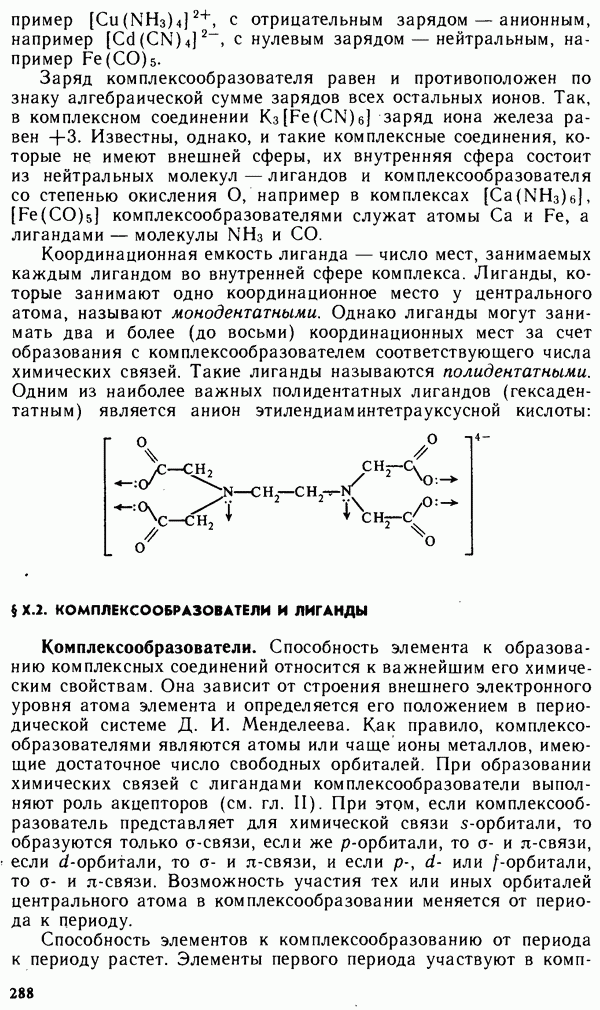
-гибридизации атомных орбиталей у четырех атомов углерода образуются диены (алкадиены) — непредельные углеводороды с двумя двойными связями.  -Гибридизация шести атомов углерода приводит к замыканию шестичленного кольца и возникновению плоской молекулы бензола. У каждого атома углерода имеется также по одному негибридизованному р-электрону, который в случае бензола является нелокализованным. Эти шесть р-электронов образуют сопряженные
-Гибридизация шести атомов углерода приводит к замыканию шестичленного кольца и возникновению плоской молекулы бензола. У каждого атома углерода имеется также по одному негибридизованному р-электрону, который в случае бензола является нелокализованным. Эти шесть р-электронов образуют сопряженные  -связи и принадлежат всем атомам углерода в молекуле. Поэтому молекула
-связи и принадлежат всем атомам углерода в молекуле. Поэтому молекула
бензола изображается следующей схемой: 
При  -гибридизации у атома углерода возникают две гибридные орбитали под углом 180° относительно друг друга и сохраняются две негибридные р-орбитали, расположенные под углом 90° друг к другу. Атом углерода образует две
-гибридизации у атома углерода возникают две гибридные орбитали под углом 180° относительно друг друга и сохраняются две негибридные р-орбитали, расположенные под углом 90° друг к другу. Атом углерода образует две  -связи с атомом углерода и (или) с атомом водорода и две
-связи с атомом углерода и (или) с атомом водорода и две  -связи с атомом углерода. В результате образуется алкин — непредельный углеводород с тройной связью.
-связи с атомом углерода. В результате образуется алкин — непредельный углеводород с тройной связью.
Алканы.
Гомологический ряд алканов или парафиновых углеводородов характеризуются формулой  Низшие алканы являются газами, промежуточные — жидкостями, высшие — твердыми веществами. Алканы в основном получают из природного газа, нефти и угля. Вследствие насыщенности и малополярного характера химических связей алканы при обычных условиях химически инертны, не вступают в реакции присоединения, не реагируют со щелочами и кислотами. Однако у них происходит замещение атома водорода галогенами и другими атомами. Такие реакции обычно идут по цепному радикальному механизму. Алканы широко используются в энергетике как составные части многих видов топлива.
Низшие алканы являются газами, промежуточные — жидкостями, высшие — твердыми веществами. Алканы в основном получают из природного газа, нефти и угля. Вследствие насыщенности и малополярного характера химических связей алканы при обычных условиях химически инертны, не вступают в реакции присоединения, не реагируют со щелочами и кислотами. Однако у них происходит замещение атома водорода галогенами и другими атомами. Такие реакции обычно идут по цепному радикальному механизму. Алканы широко используются в энергетике как составные части многих видов топлива.
Алкены
Алкены — непредельные углеводороды с общей формулой  имеющие одну двойную связь. Их называют также олефинами или этиленовыми углеводородами. Одним из основных методов их получения является крекинг нефти. Наличие двойной связи в молекуле алкенов обусловливает их высокую реакционную способность. Для алкенов характерна реакция присоединения, в процессе которой разрывается двойная химическая связь, например:
имеющие одну двойную связь. Их называют также олефинами или этиленовыми углеводородами. Одним из основных методов их получения является крекинг нефти. Наличие двойной связи в молекуле алкенов обусловливает их высокую реакционную способность. Для алкенов характерна реакция присоединения, в процессе которой разрывается двойная химическая связь, например:

Алкены относительно легко полимеризуются, это их свойство используют в технике для получения различных полимерных материалов. Алкены вступают и в реакцию замещения. При потере водорода в процессе замещения образуются радикалы, в названия которых входит суффикс -енил, например пропенил  Радикал этенил
Радикал этенил  называют также винилом. В название соединения, образуемого в результате реакции замещения, входит название радикала, например
называют также винилом. В название соединения, образуемого в результате реакции замещения, входит название радикала, например  (бромэтенил или бромвинил).
(бромэтенил или бромвинил).
Диены (алкадиены)
Диены (алкадиены) — углеводороды с двумя двойными связями с общей формулой  Диеновые углеводороды, как и алкины, относительно легко вступают в реакции присоединения. Значительное отличие в химических свойствах наблюдается между алкенами и диенами с сопряженными двойными связями, у которых двойные связи разделены ординарной связью. Вследствие эффекта сопряжения происходит делокализация
Диеновые углеводороды, как и алкины, относительно легко вступают в реакции присоединения. Значительное отличие в химических свойствах наблюдается между алкенами и диенами с сопряженными двойными связями, у которых двойные связи разделены ординарной связью. Вследствие эффекта сопряжения происходит делокализация  -электронов
-электронов
нов и более равномерное распределение электронной плотности по молекуле. Соответственно структуру молекулы можно записать в следующем виде:

Такая перестройка приводит к повышению устойчивости молекулы. Возникшие связи (по энергии и длине) занимают промежуточное положение между двойными и ординарными связями. В ходе реакции взаимодействия таких диенов с галогенами и другими электрофильными реагентами последние присоединяются в положения 1, 4 или 1, 2. Реакция сопровождается не только разрывом, но и перегруппировкой связей, например:

Алкадиены с сопряженными двойными связями легко вступают в реакцию полимеризации, на этом их свойстве основано получение каучуков.
Алкины
Алкины — углеводороды с тройной связью с общей формулой  Простейший алкин
Простейший алкин  называемый этином или ацетиленом, широко используется в кислородно-ацетиленовых горелках, в которых пламя имеет очень высокую температуру (3200 К). Алкины, будучи ненасыщенными соединениями, обладают высокой реакционной способностью. Они легко вступают в реакцию присоединения, превращаясь в алкены или алканы и их производные, например:
называемый этином или ацетиленом, широко используется в кислородно-ацетиленовых горелках, в которых пламя имеет очень высокую температуру (3200 К). Алкины, будучи ненасыщенными соединениями, обладают высокой реакционной способностью. Они легко вступают в реакцию присоединения, превращаясь в алкены или алканы и их производные, например:

Этины также могут полимеризоваться.
Ароматические углеводороды
Ароматические углеводороды — это планарные (плоские) циклические соединения, у которых образуется единая сопряженная система электронов. Типичным представителем ароматических углеводородов является бензол. Как было показано ранее, негибридизированные р-электроны атомов углерода в бензоле образуют систему сопряженных нелокализованных  -связей. Все связи между атомами углерода в бензоле равноценны, по энергии и длине они занимают промежуточное положение между ординарными и двойными связями. Поэтому бензол и его гомологи
-связей. Все связи между атомами углерода в бензоле равноценны, по энергии и длине они занимают промежуточное положение между ординарными и двойными связями. Поэтому бензол и его гомологи  достаточно устойчивы, реакции их окисления и присоединения протекают с трудом. Для ароматических углеводородов характерна реакция электрофильного замещения водорода на другие атомы или группы атомов, например:
достаточно устойчивы, реакции их окисления и присоединения протекают с трудом. Для ароматических углеводородов характерна реакция электрофильного замещения водорода на другие атомы или группы атомов, например:

Водород можно также заменить на сульфогруппы  гидрокси-группу
гидрокси-группу  алкильные радикалы. В результате реакции замещения образуются соединения, в названия которых входит название радикала фенила
алкильные радикалы. В результате реакции замещения образуются соединения, в названия которых входит название радикала фенила  Ароматические радикалы называют арильными
Ароматические радикалы называют арильными 
Наряду с моноциклическими существуют полициклические ароматические углеводороды, например:

Алициклические углеводороды.
Циклические углеводороды, не содержащие в своем составе ароматических циклов, получили название алициклических. Непредельные алициклические углеводороды называют циклоалканами или нафтенами. Их получают из некоторых видов нефти, например, из бакинской. Прочность циклов снижается с уменьшением числа атомов углерода в цикле из-за увеличения напряжения вследствие изменения валентных углов при образовании связей. Характерной для циклоалканов является реакция замещения. Малые циклы склонны к реакциям присоединения, сопровождающимся разрывом циклов.
При замещении водорода циклоалканов органическими углеводородными радикалами появляются боковые цепи. Поэтому наряду с гомологическим рядом циклоалканов с общей формулой  существуют гомологические ряды циклоалканов, образуемые за счет роста боковых цепей. При этом боковые цепи могут представлять собой как предельные, так и непредельные углеводороды.
существуют гомологические ряды циклоалканов, образуемые за счет роста боковых цепей. При этом боковые цепи могут представлять собой как предельные, так и непредельные углеводороды.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- § 1. ПРЕДМЕТ ХИМИИ
- § 2. ЗНАЧЕНИЕ ХИМИИ В ИЗУЧЕНИИ ПРИРОДЫ И РАЗВИТИИ ТЕХНИКИ
- 1. СТРОЕНИЕ ВЕЩЕСТВА
- Глава I. СТРОЕНИЕ АТОМА И СИСТЕМАТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- § 1.2. КВАНТОВО-МЕХАНИЧЕСКАЯ МОДЕЛЬ АТОМА
- § 1.3. КВАНТОВЫЕ ЧИСЛА И АТОМНЫЕ ОРБИТАЛИ
- § 1.4. МНОГОЭЛЕКТРОННЫЕ АТОМЫ
- § 1.5. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
- § 1.6. ПЕРИОДИЧЕСКОЕ ИЗМЕНЕНИЕ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- Глава II. ХИМИЧЕСКАЯ СВЯЗЬ
- § II.1. ОСНОВНЫЕ ВИДЫ И ХАРАКТЕРИСТИКИ ХИМИЧЕСКОЙ СВЯЗИ
- § II.2. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ. ВАЛЕНТНОСТЬ
- § II.3. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННАЯ СТРУКТУРА МОЛЕКУЛ
- § 11.4. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- § 11.5. ЭЛЕКТРОННАЯ СТРУКТУРА НЕКОТОРЫХ МОЛЕКУЛ
- Глава III. ТИПЫ ВЗАИМОДЕЙСТВИЯ МОЛЕКУЛ. КОНДЕНСИРОВАННОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- § III.1. ВЗАИМОДЕЙСТВИЕ МЕЖДУ МОЛЕКУЛАМИ
- § III.2. СВОЙСТВА ВЕЩЕСТВ В РАЗЛИЧНЫХ СОСТОЯНИЯХ
- § III.3. СТРОЕНИЕ КРИСТАЛЛОВ. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ТЕЛАХ
- § III.4. МЕТАЛЛЫ, ПОЛУПРОВОДНИКИ И ДИЭЛЕКТРИКИ
- § III.5. РЕАЛЬНЫЕ КРИСТАЛЛЫ
- 2. ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ
- Глава IV. ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ХИМИЧЕСКОЕ СРОДСТВО
- § IV.2. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ И ФАЗОВЫХ ПРЕВРАЩЕНИЙ. ТЕРМОХИМИЧЕСКИЕ ЗАКОНЫ
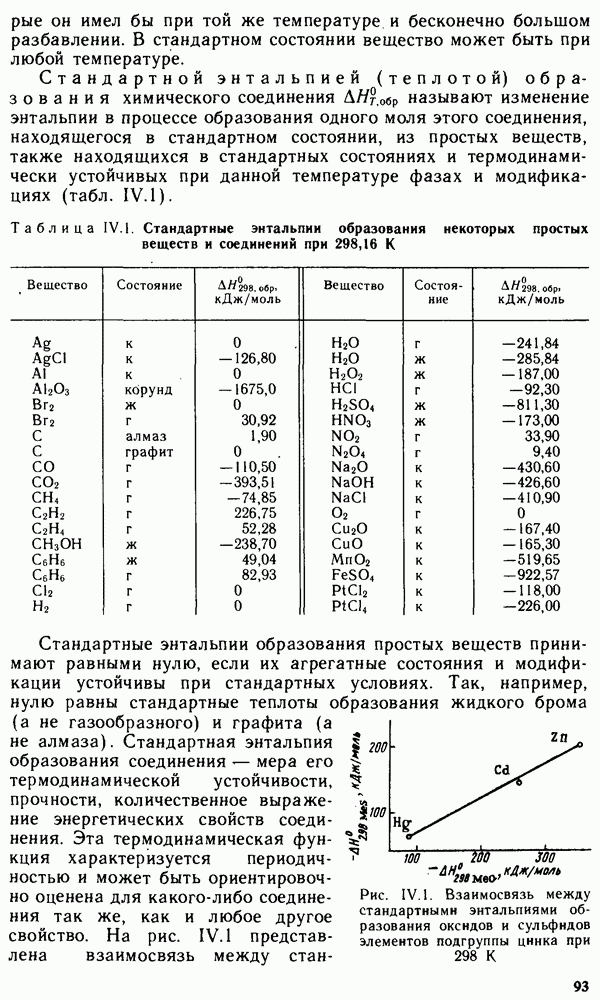
- § IV.3. ЭНТАЛЬПИЯ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СОЕДИНЕНИЙ. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
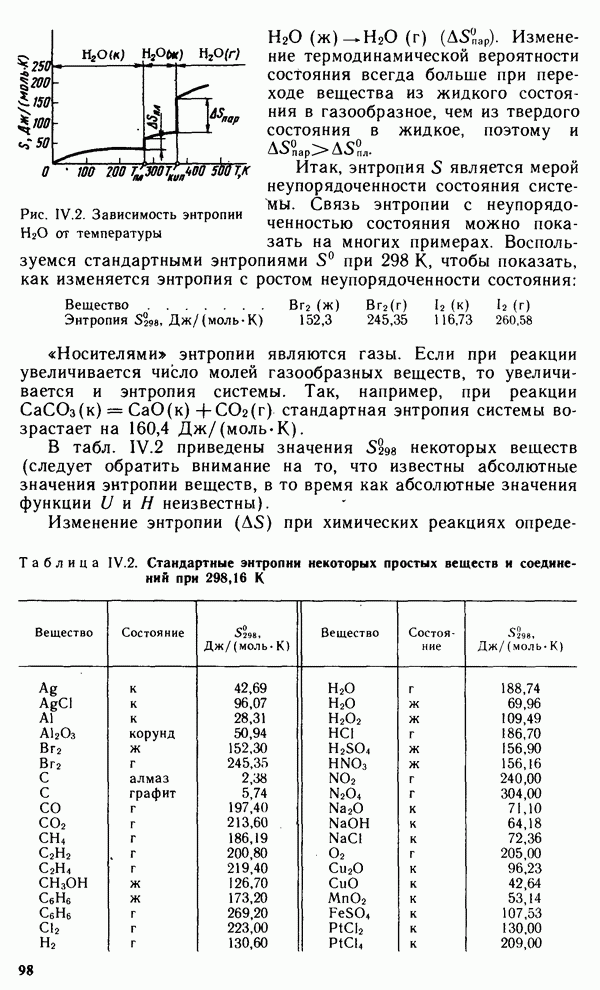
- § IV.4. ЭНТРОПИЯ. НАПРАВЛЕНИЕ И ПРЕДЕЛ ПРОТЕКАНИЯ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ СИСТЕМАХ
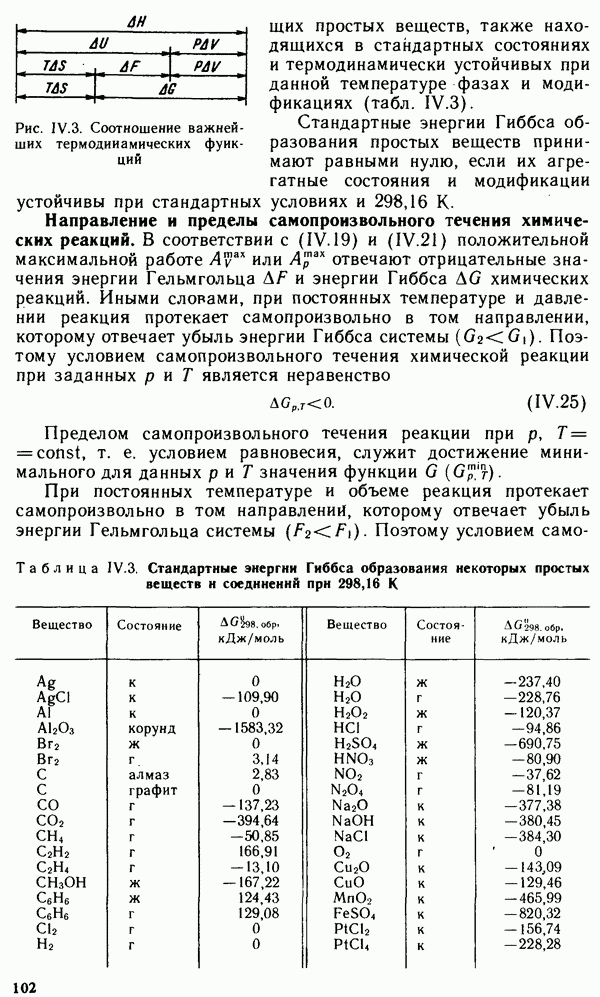
- § IV.5. ЭНЕРГИЯ ГИББСА И ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА ХИМИЧЕСКОЙ РЕАКЦИИ
- Глава V. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- § V.2. СКОРОСТЬ ГЕТЕРОГЕННЫХ ХИМИЧЕСКИХ РЕАКЦИЙ
- § V.3. ЗАВИСИМОСТЬ СКОРОСТИ ХИМИЧЕСКОЙ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
- § V.4. ФИЗИЧЕСКИЕ ВОЗДЕЙСТВИЯ НА ХИМИЧЕСКИЕ РЕАКЦИИ. ЦЕПНЫЕ РЕАКЦИИ
- § V.5. КИНЕТИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ О ХИМИЧЕСКОМ РАВНОВЕСИИ
- § V.6. ФАЗОВЫЕ РАВНОВЕСИЯ ПРАВИЛО ФАЗ
- § V.7. АДСОРБЦИОННОЕ РАВНОВЕСИЕ
- § V.8. КАТАЛИЗ
- 3. РАСТВОРЫ ДИСПЕРСНЫЕ СИСТЕМЫ ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- VI.1. ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
- § VI.2. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ЖИДКИХ РАСТВОРОВ
- § VI.3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ В РАСТВОРАХ
- § VI.4. ВОДНЫЕ РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- § VI.5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
- § VI.6. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- § VI.7. ДИСПЕРСНЫЕ СИСТЕМЫ. КОЛЛОИДНЫЕ РАСТВОРЫ
- § VI.8. УСТОЙЧИВОСТЬ И КОАГУЛЯЦИЯ КОЛЛОИДНЫХ СИСТЕМ
- Глава VII. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.1. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ
- § VII.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
- § VII.3. ПОТЕНЦИАЛЫ МЕТАЛЛИЧЕСКИХ И ГАЗОВЫХ ЭЛЕКТРОДОВ
- § VII.4. ПОТЕНЦИАЛЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ (РЕДОКСИ-) ЭЛЕКТРОДОВ
- § VII.5. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ. ПОЛЯРИЗАЦИЯ
- § VII.6. ЭЛЕКТРОЛИЗ
- Глава VIII. КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
- § VIII.1. ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ
- § VIII.2. ХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.3. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
- § VIII.4. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
- 4. ОБЩАЯ ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- Глава IX. ПРОСТЫЕ ВЕЩЕСТВА И ДВОЙНЫЕ СОЕДИНЕНИЯ. КРАТКИЙ ОБЗОР ХИМИЧЕСКИХ СВОЙСТВ s- И р-ЭЛЕМЕНТОВ
- § IX.2. МЕТАЛЛЫ И СПЛАВЫ. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА
- § IX.3. ДВОЙНЫЕ СОЕДИНЕНИЯ
- § IX.4. СВОЙСТВА МЕТАЛЛОВ ГЛАВНЫХ ПОДГРУПП I И II ГРУПП
- § IX.5. СВОЙСТВА р-ЭЛЕМЕНТОВ III ГРУППЫ
- § IX.6. СВОЙСТВА р-ЭЛЕМЕНТОВ IV ГРУППЫ
- § IX.7. СВОЙСТВА р-ЭЛЕМЕНТОВ V, VI И VII ГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ
- Глава Х. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- § Х.1. СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИИ
- § Х.2. КОМПЛЕКСООБРАЗОВАТЕЛИ И ЛИГАНДЫ
- § Х.3. НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- § Х.4. МЕТОДЫ РАСЧЕТА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
- § Х.5. УСТОЙЧИВОСТЬ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
- Глава XI. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- § XI.1. ОСОБЕННОСТИ. ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ И КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- § XI.2. УГЛЕВОДОРОДЫ
- § ХI.3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- 5. СПЕЦИАЛЬНЫЕ ВОПРОСЫ ХИМИИ
- Глава XII. ХИМИЯ КОНСТРУКЦИОННЫХ И ЭЛЕКТРОТЕХНИЧЕСКИХ МАТЕРИАЛОВ
- § XII.2. СВОЙСТВА ПЕРЕХОДНЫХ МЕТАЛЛОВ VIII ГРУППЫ
- § ХII.3. СВОЙСТВА ЭЛЕМЕНТОВ I И II ГРУПП
- § XII.4. ХИМИЯ ПОЛУПРОВОДНИКОВЫХ МАТЕРИАЛОВ
- § XII.5. МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛОВ ВЫСОКОЙ ЧИСТОТЫ
- Глава XIII. ПОЛИМЕРНЫЕ МАТЕРИАЛЫ И ИХ ПРИМЕНЕНИЕ В ЭНЕРГЕТИКЕ
- § XIII.1. МЕТОДЫ ПОЛУЧЕНИЯ ПОЛИМЕРОВ
- § XIII.2. СТРОЕНИЕ ПОЛИМЕРОВ
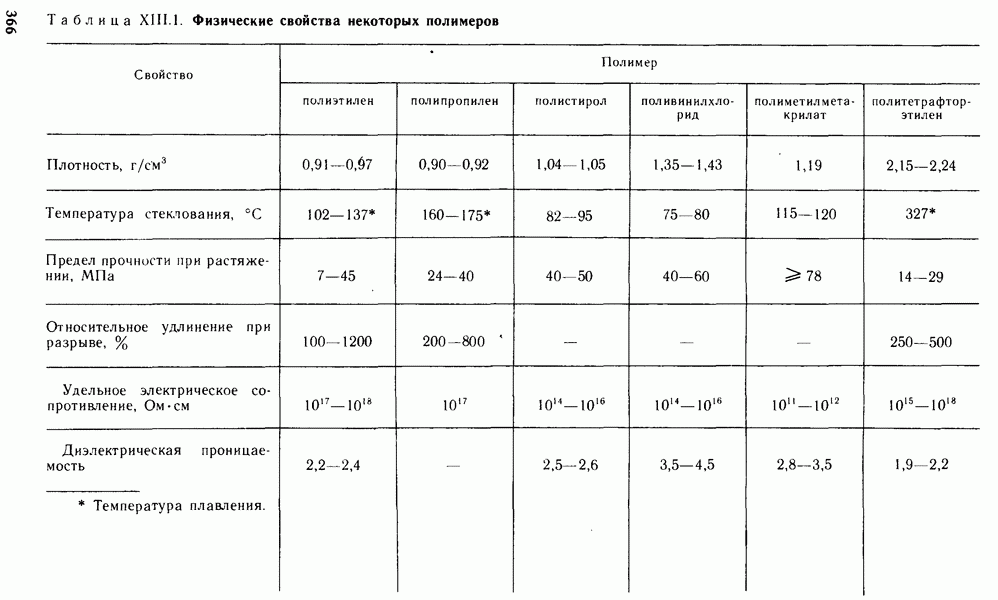
- § XIII.3. СВОЙСТВА ПОЛИМЕРОВ
- § XIII.4. ПРИМЕНЕНИЕ ПОЛИМЕРОВ
- Глава XIV. ХИМИЯ ВОДЫ И ТОПЛИВА. ХИМИЯ И ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
- § XIV.1. СТРОЕНИЕ И СВОЙСТВА ВОДЫ
- § XIV.2. ПРИРОДНЫЕ ВОДЫ
- § ХIV.3. ОСНОВНЫЕ МЕТОДЫ ОЧИСТКИ ВОДЫ
- § XIV.4. СОСТАВ И СВОЙСТВА ОРГАНИЧЕСКОГО ТОПЛИВА
- § XIV.5. ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ОБЩЕСТВА
- § XIV.6. ОХРАНА ВОЗДУШНОГО БАССЕЙНА
- § XIV.7. ОХРАНА ВОДНОГО БАССЕЙНА
- Глава XV. ЯДЕРНАЯ ХИМИЯ И РАДИОХИМИЯ
- § XV.1. АТОМНОЕ ЯДРО. РАДИОАКТИВНОСТЬ
- § XV.2. ЯДЕРНЫЕ РЕАКЦИИ
- § XV.3. ЯДЕРНАЯ ЭНЕРГЕТИКА
- § XV.4. ХИМИЧЕСКИЕ СВОЙСТВА РАДИОАКТИВНЫХ ЭЛЕМЕНТОВ
- Глава XVI. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ В ЭНЕРГЕТИКЕ, ЭЛЕКТРОНИКЕ И АВТОМАТИКЕ
- § ХVI.1. ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА. ЭЛЕКТРОХИМИЧЕСКИЕ ЭНЕРГОУСТАНОВКИ
- § XVI.2. ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ (ХЕМОТРОНЫ)
- § ХVI.3. ЭЛЕКТРОХИМИЧЕСКАЯ АНОДНАЯ ОБРАБОТКА МЕТАЛЛОВ И СПЛАВОВ
- § XVI.4. ПОЛУЧЕНИЕ И СВОЙСТВА ГАЛЬВАНОПОКРЫТИИ
- ЗАКЛЮЧЕНИЕ