| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
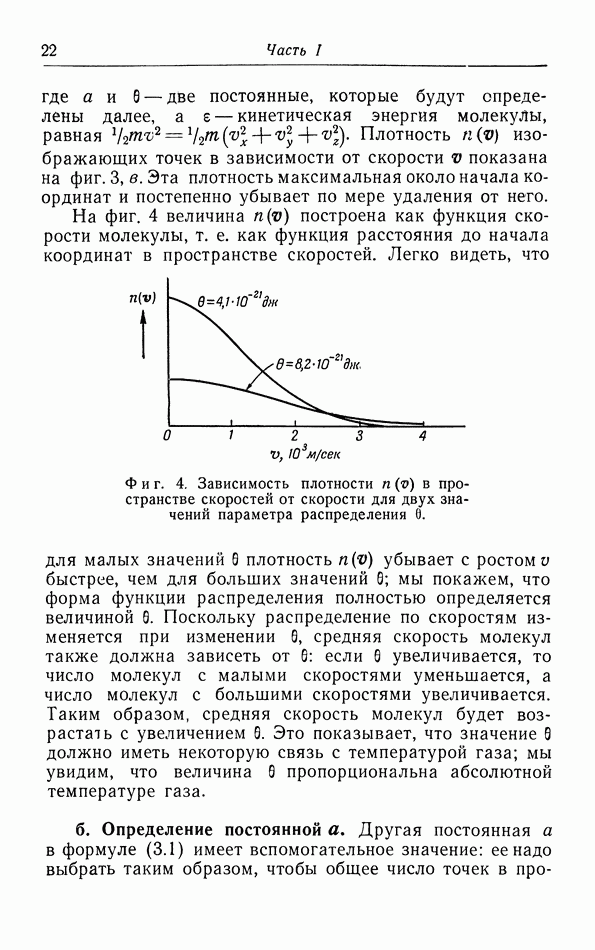
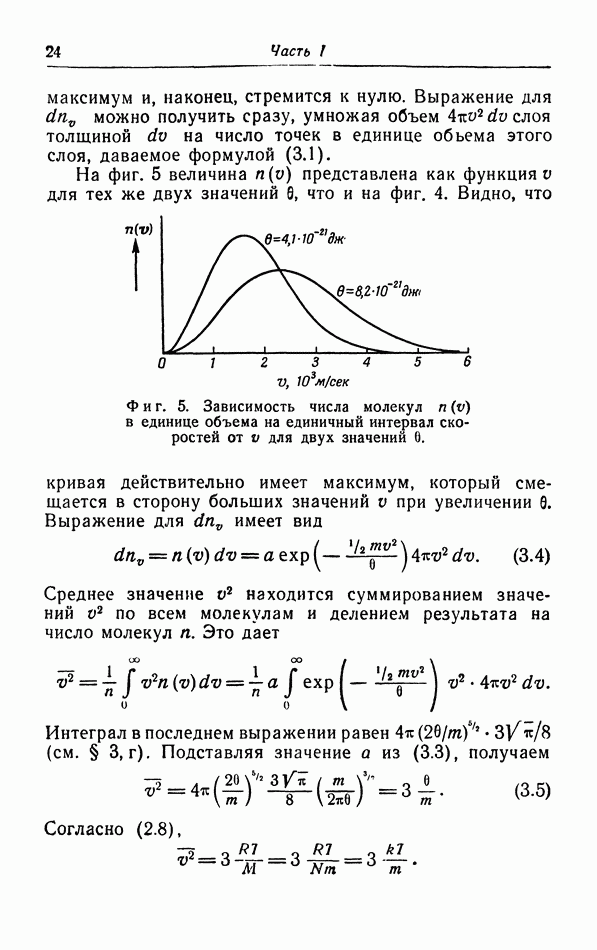
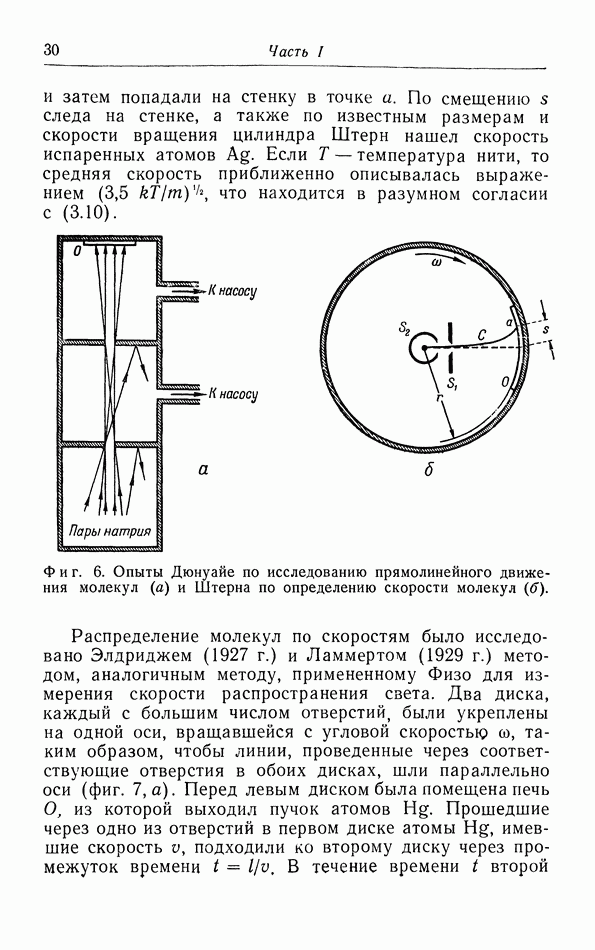
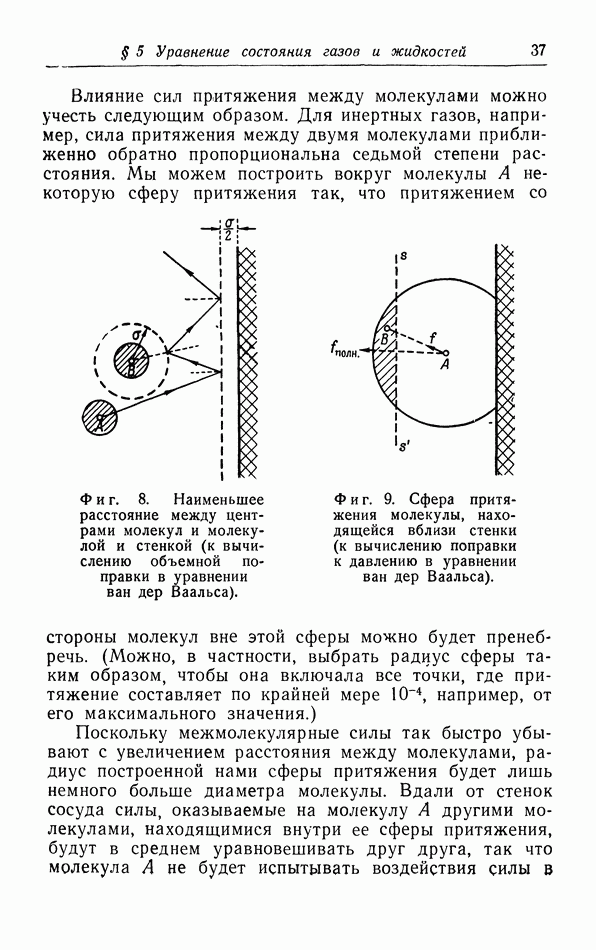
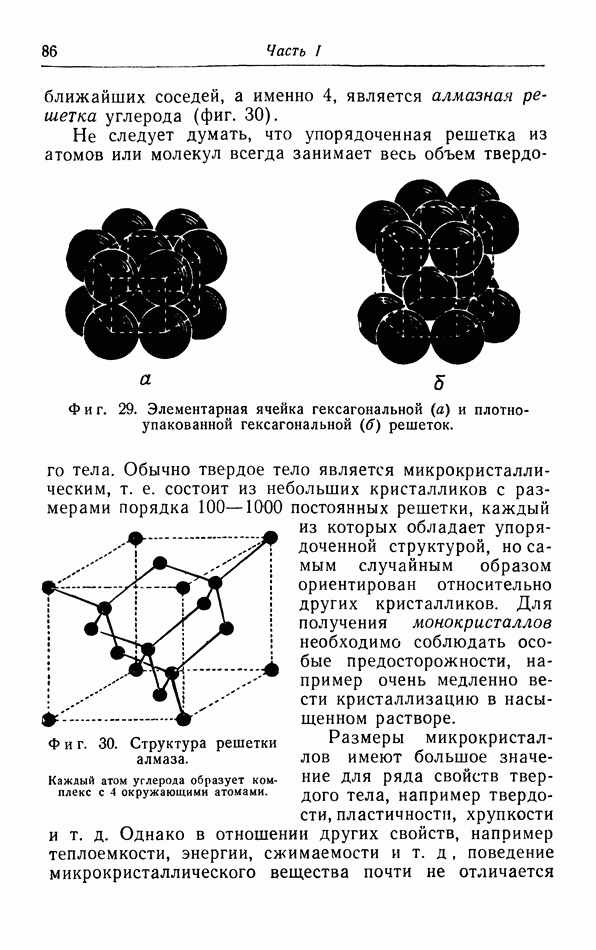
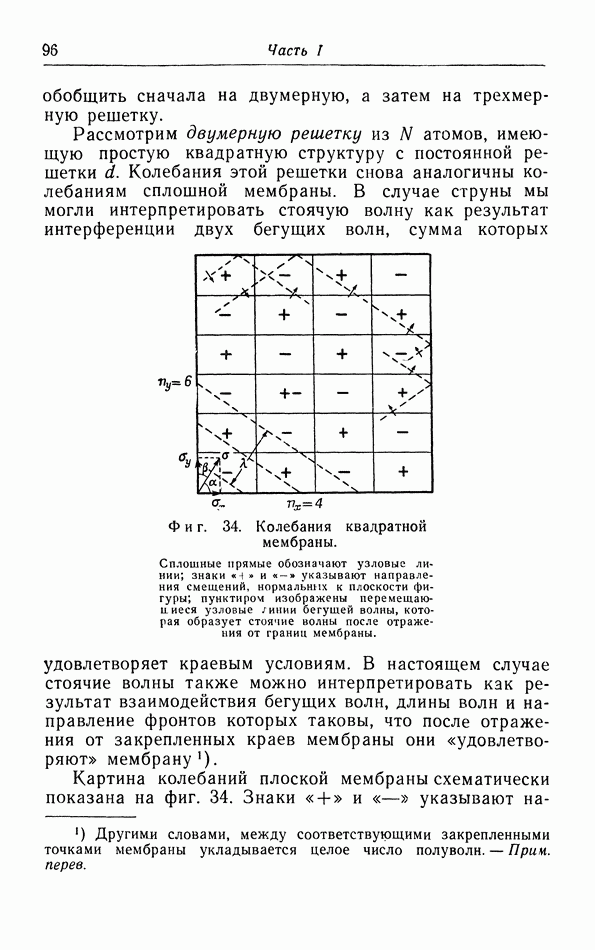
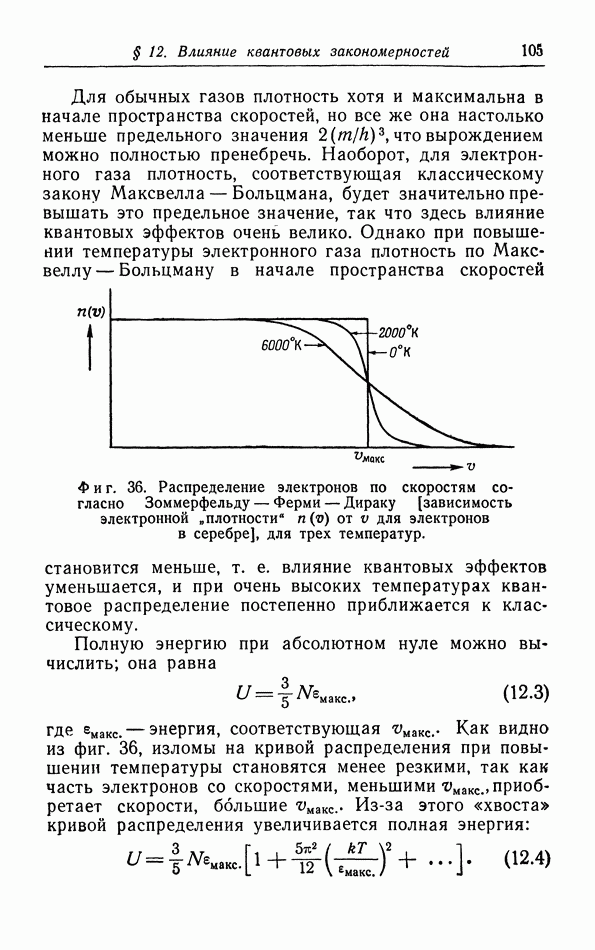
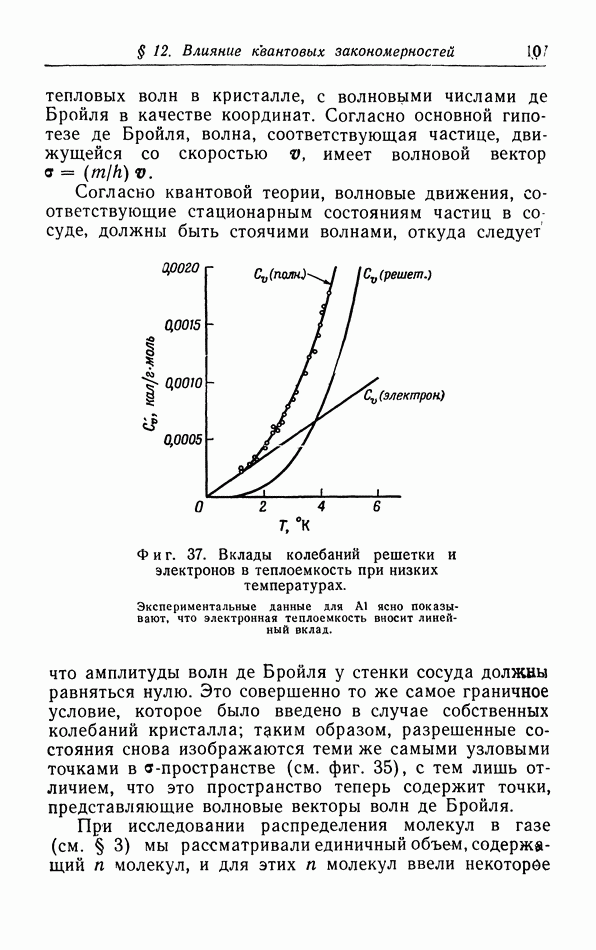
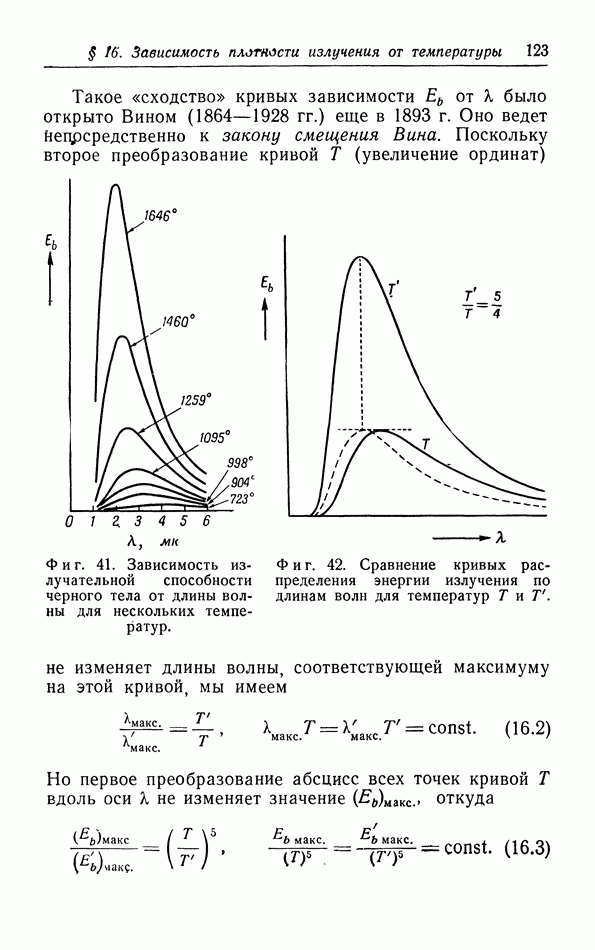
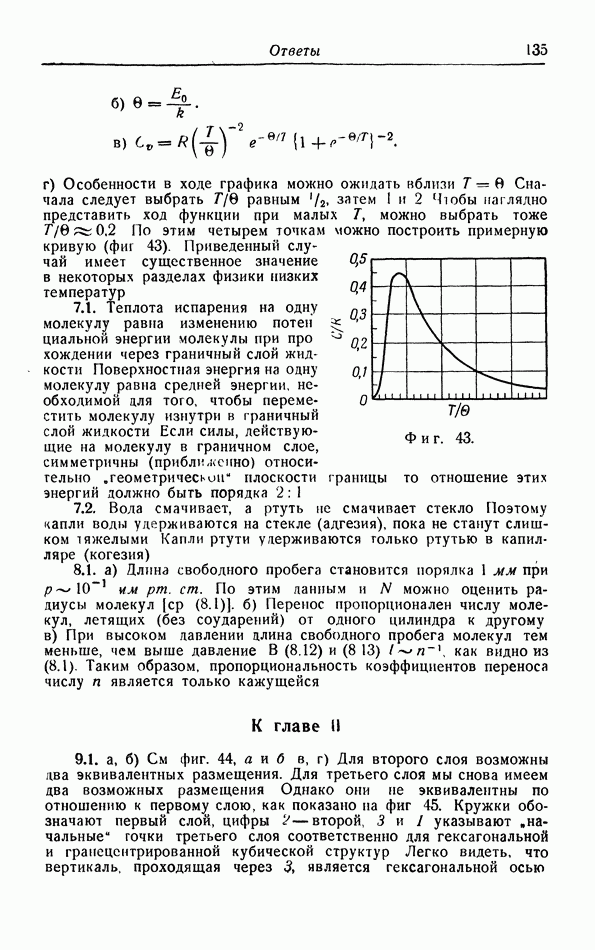
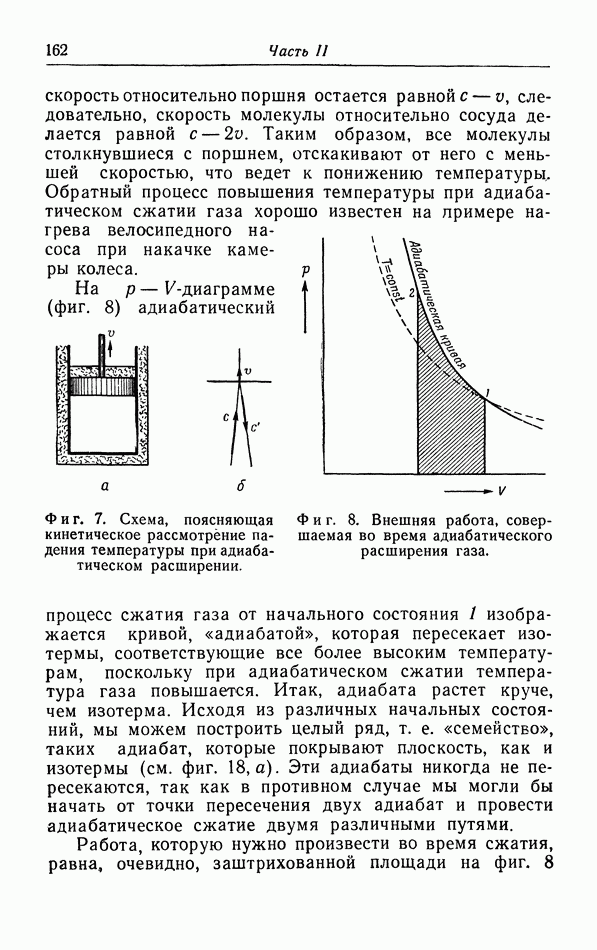
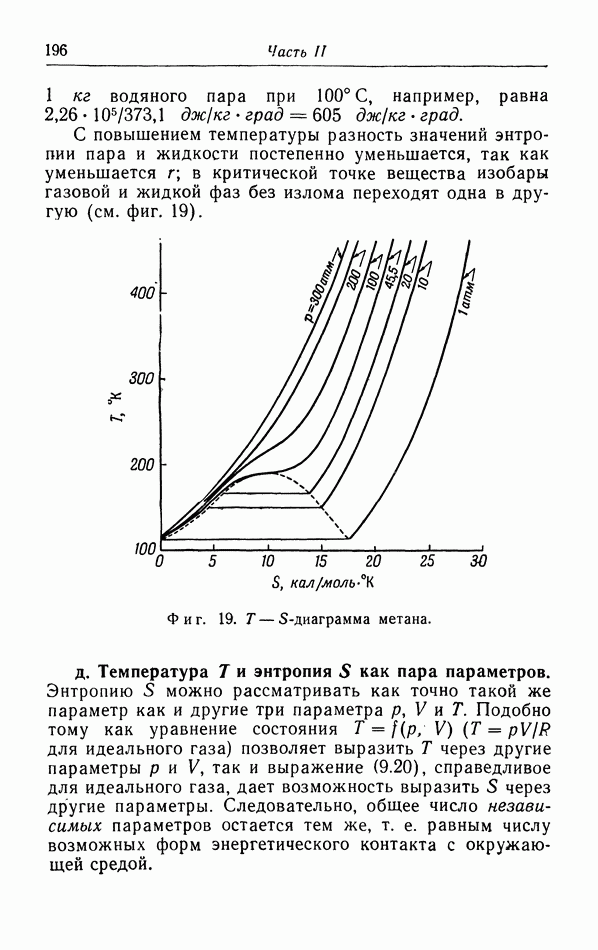
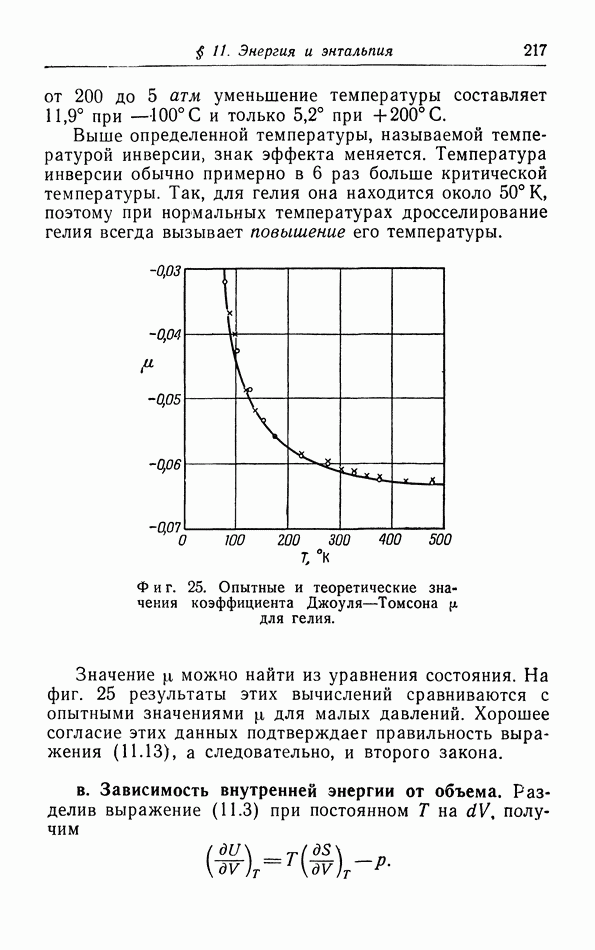
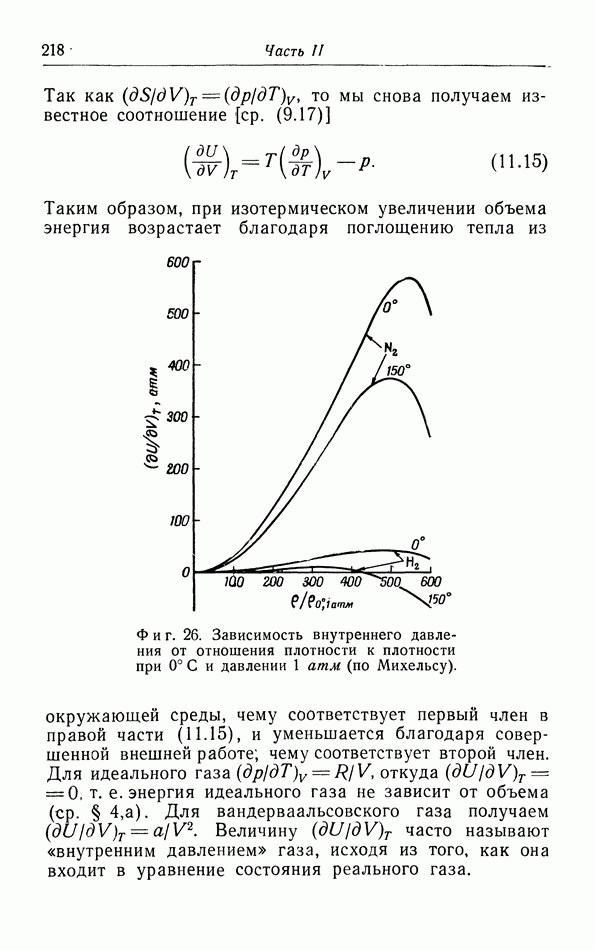
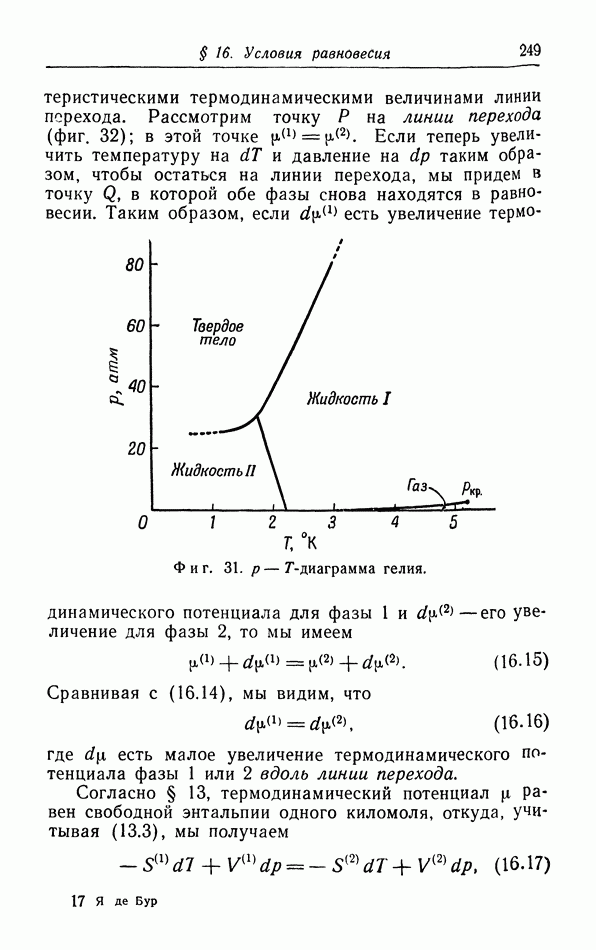
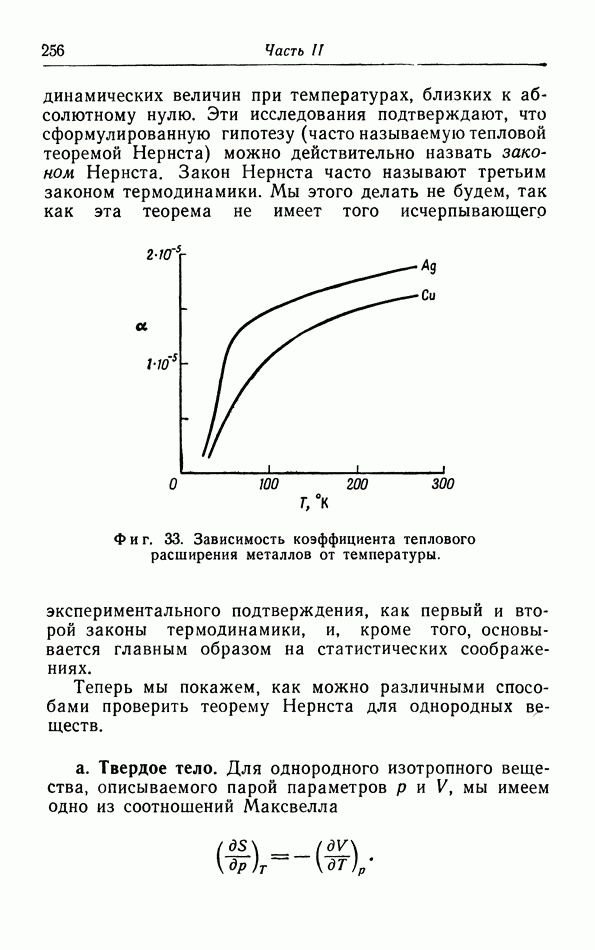
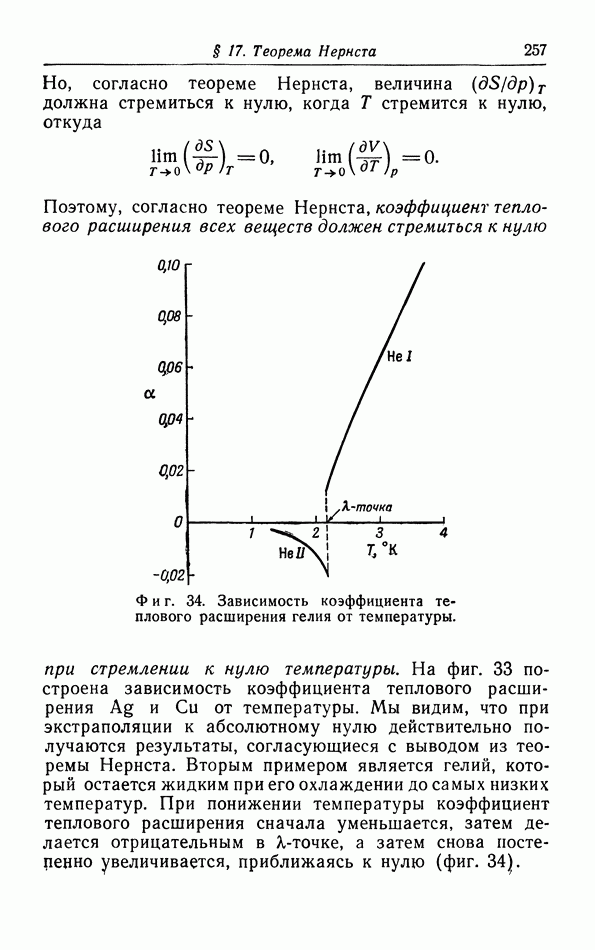
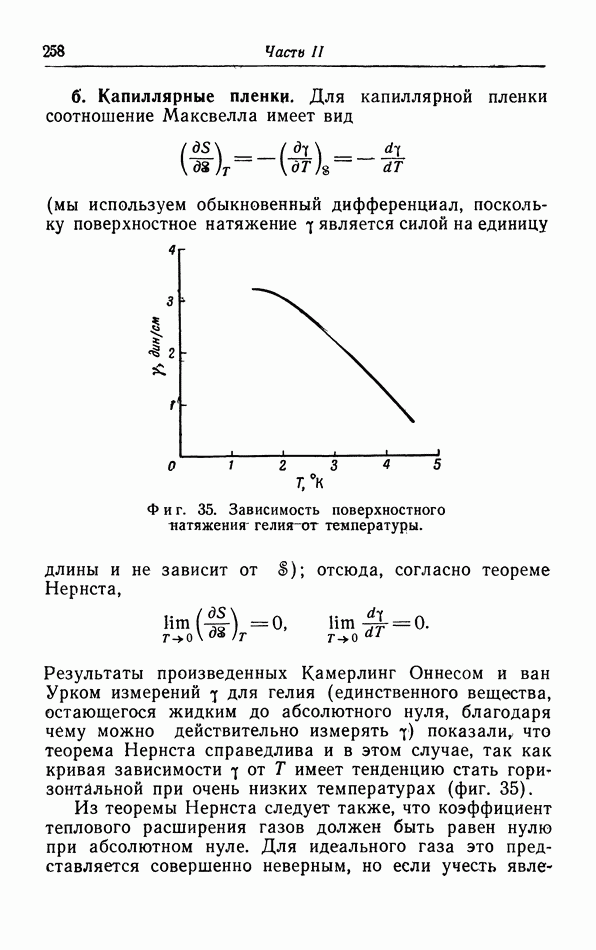
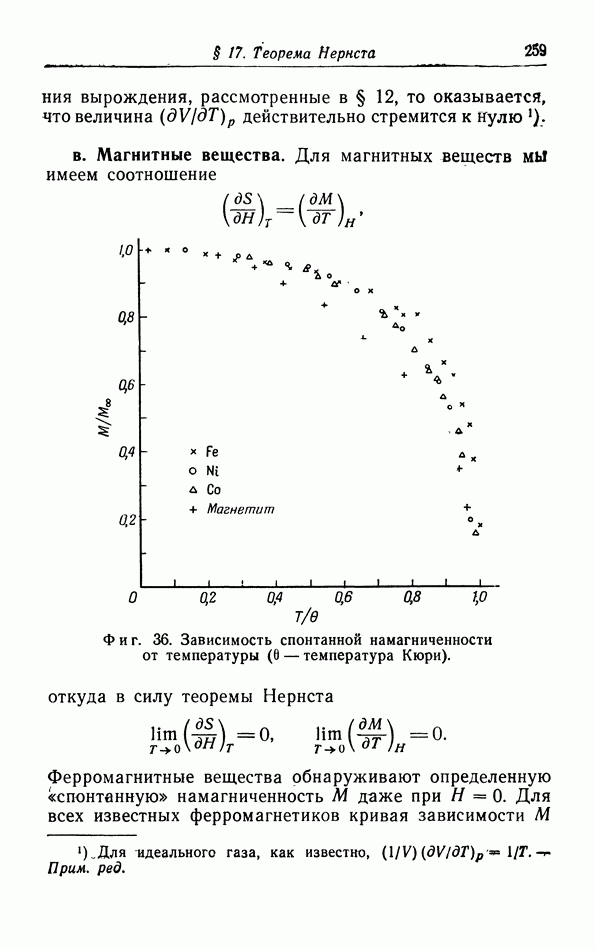
б. Обсуждение уравнения ван дер Ваальса.
Теперь мы исследуем изменения в изотермах, обусловленные двумя поправками, введенными ван дер Ваальсом в уравнение состояния  На фиг. 10 пунктиром
На фиг. 10 пунктиром
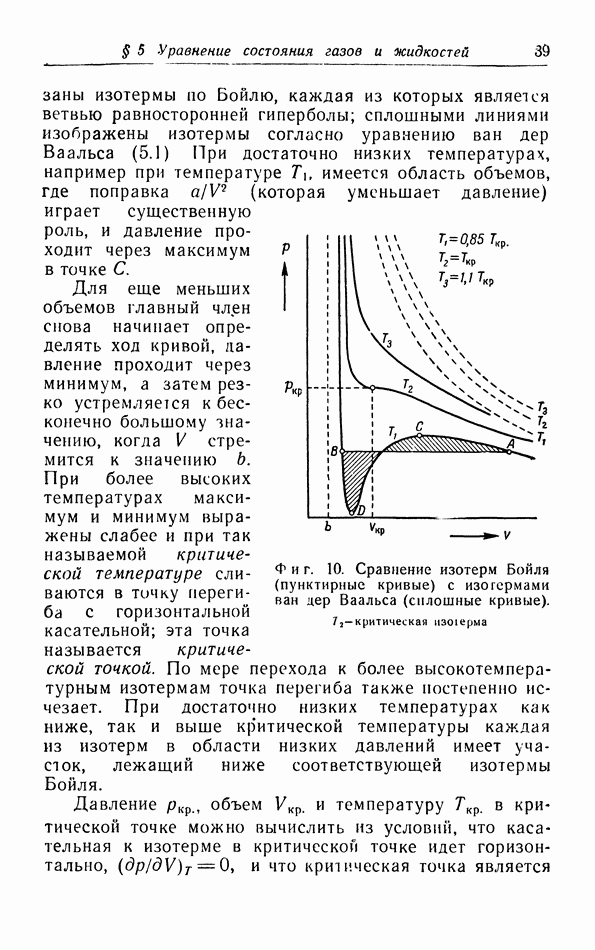
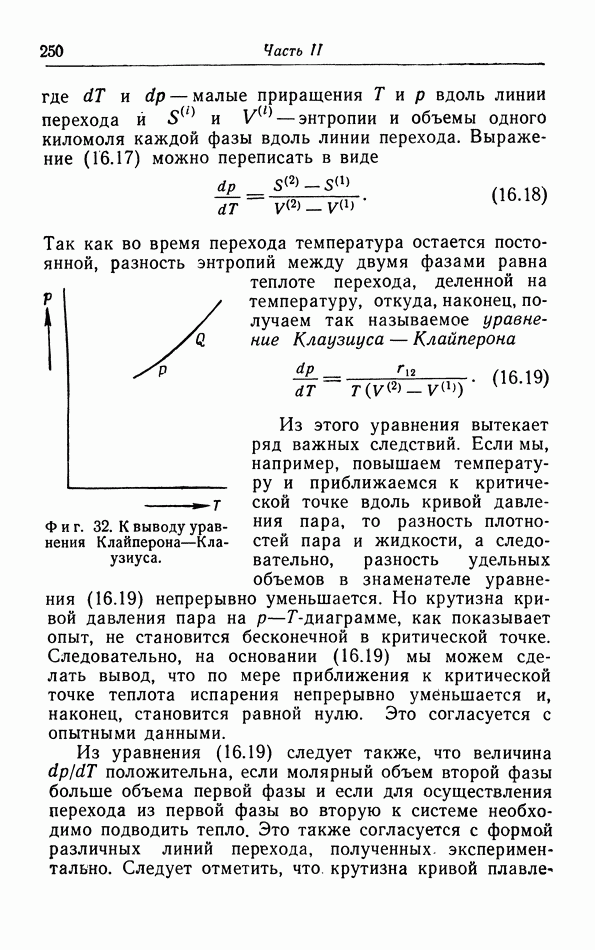
показаны изотермы по Бойлю, каждая из которых является ветвью равносторонней гиперболы; сплошными линиями изображены изотермы согласно уравнению ван дер Ваальса (5.1) При достаточно низких температурах, например при температуре  имеется область объемов, где поправка
имеется область объемов, где поправка  (которая уменьшает давление) играет существенную роль, и давление проходит через максимум в точке С.
(которая уменьшает давление) играет существенную роль, и давление проходит через максимум в точке С.

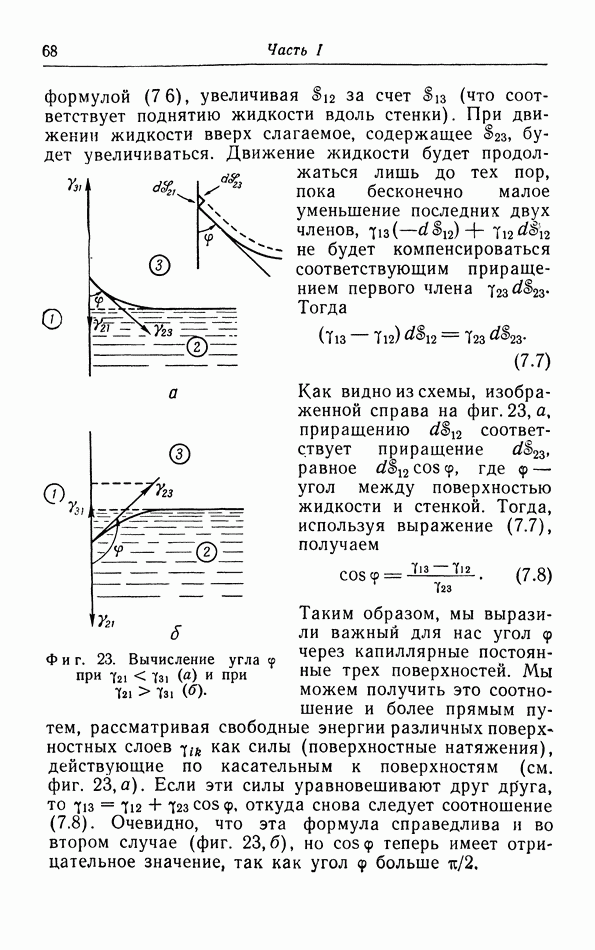
Фиг. 10. Сравнение изотерм Бойля (пунктирные кривые) с изотермами  Ваальса (сплошные кривые).
Ваальса (сплошные кривые).  - критическая изотерма.
- критическая изотерма.
Для еще меньших объемов главный член снова начинает определять ход кривой, давление проходит через минимум, а затем резко устремляется к бесконечно большому значению, когда V стремится к значению  . При более высоких температурах максимум и минимум выражены слабее и при так называемой критической температуре сливаются в точку перегиба с горизонтальной касательной; эта точка называется критической точкой. По мере перехода к более высокотемпературным изотермам точка перегиба также постепенно исчезает. При достаточно низких температурах как ниже, так и выше критической температуры каждая из изотерм в области низких давлений имеет участок, лежащий ниже соответствующей изотермы Бойля.
. При более высоких температурах максимум и минимум выражены слабее и при так называемой критической температуре сливаются в точку перегиба с горизонтальной касательной; эта точка называется критической точкой. По мере перехода к более высокотемпературным изотермам точка перегиба также постепенно исчезает. При достаточно низких температурах как ниже, так и выше критической температуры каждая из изотерм в области низких давлений имеет участок, лежащий ниже соответствующей изотермы Бойля.
Давление  объем
объем  и температуру
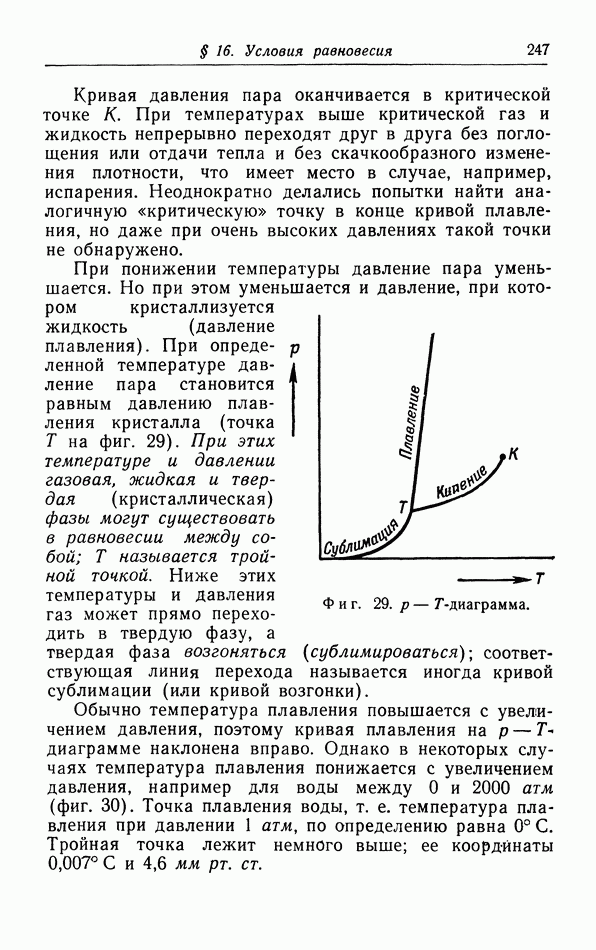
и температуру  в критической точке можно вычислить из условий, что касательная к изотерме в критической точке идет горизонтально,
в критической точке можно вычислить из условий, что касательная к изотерме в критической точке идет горизонтально,  и что критическая точка является
и что критическая точка является
точкой перегиба,  Отсюда получаем уравнения
Отсюда получаем уравнения

Температура  и объем
и объем  определяются из (5.2) и (5.3), а давление
определяются из (5.2) и (5.3), а давление  находится затем с помощью (5.1). В результате получаем
находится затем с помощью (5.1). В результате получаем

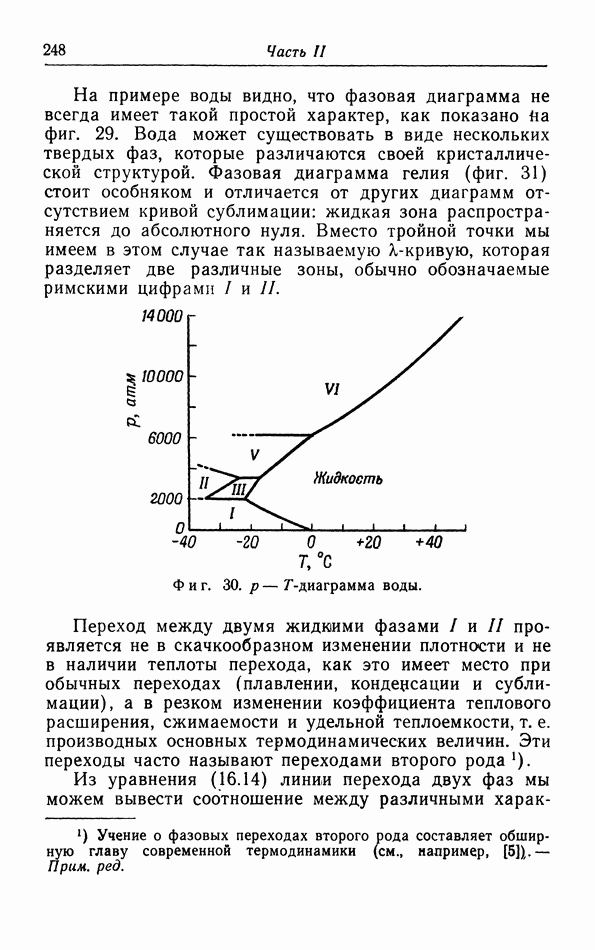
Максимумы и минимумы на изотермах экспериментально не наблюдаются, однако в определенной точке  начинается конденсация паров. Если продолжать далее уменьшать объем, то давление остается постоянным до тех пор, пока наконец в точке В весь пар полностью не превратится в жидкость В части II мы убедимся, что давление в области одновременного существования пара и жидкости таково, что две заштрихованные на фиг. 10 площади одинаковы по величине. Участки
начинается конденсация паров. Если продолжать далее уменьшать объем, то давление остается постоянным до тех пор, пока наконец в точке В весь пар полностью не превратится в жидкость В части II мы убедимся, что давление в области одновременного существования пара и жидкости таково, что две заштрихованные на фиг. 10 площади одинаковы по величине. Участки  и
и  на изотермах легко воспроизводятся экспериментально при использовании очень чистых газов и жидкостей, причем иногда бывает даже трудно вызвать конденсацию пересыщенных паров Пересыщенные пары и перегретые жидкости называются метастабильными. Состояния, соответствующие участку
на изотермах легко воспроизводятся экспериментально при использовании очень чистых газов и жидкостей, причем иногда бывает даже трудно вызвать конденсацию пересыщенных паров Пересыщенные пары и перегретые жидкости называются метастабильными. Состояния, соответствующие участку  теоретической изотермы, на опыте не реализуются и называются нестабильными 2).
теоретической изотермы, на опыте не реализуются и называются нестабильными 2).
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Предисловие к русскому изданию
- ГЛАВА I. Газы и жидкости
- § 1. Молекулярная структура газов и жидкостей
- § 2. Кинетическая теория идеального газа
- б. Расчет давления в кинетической теории газов.
- в. Расчет удельной теплоемкости в кинетической теории газов.
- § 3. Распределение молекул по скорости их движения
- г. Средняя квадратичная и средняя скорости.
- д. Броуновское движение.
- е. Опыты с молекулярными пучками.
- § 4. Общее распределение молекул по энергиям
- б. Возбужденные состояния.
- в. вращательная и колебательная энергии.
- г. Потенциальная энергия тяготения.
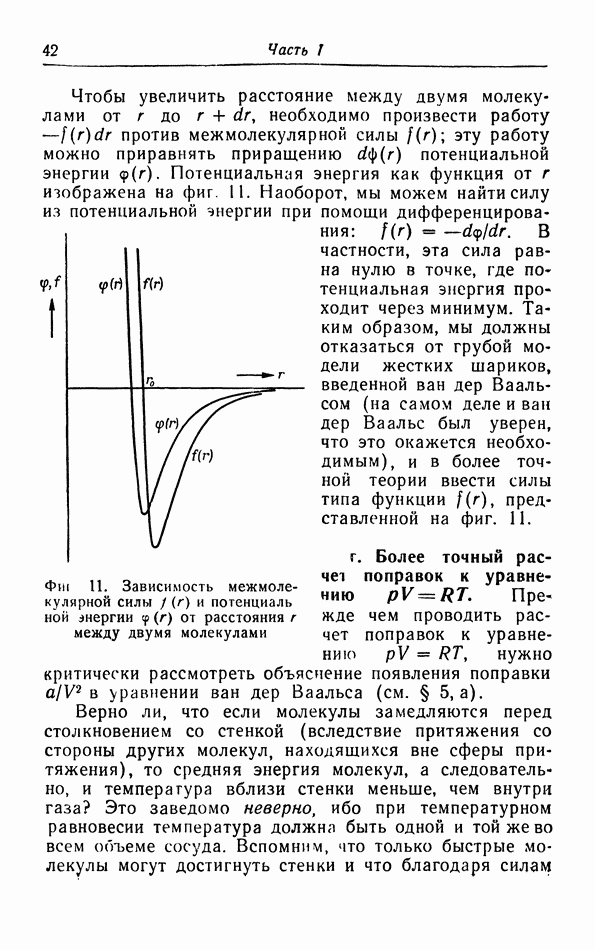
- д. Потенциальная энергия межмолекулярных сил.
- § 5. Уравнение состояния газов и жидкостей
- б. Обсуждение уравнения ван дер Ваальса.
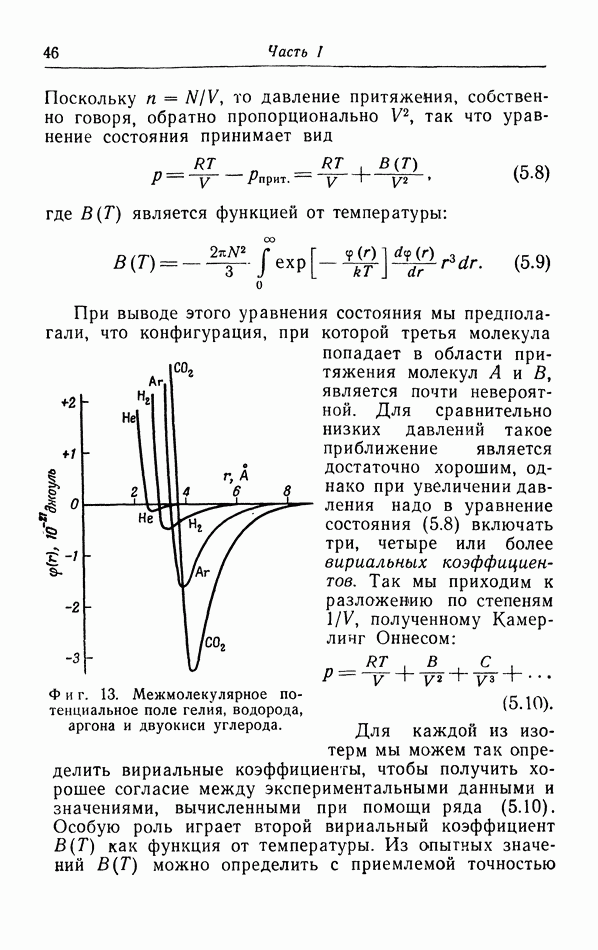
- в. Взаимодействие молекул.
- г. Более точный расчет поправок к уравнению pV=RT.
- д. Закон соответственных состояний.
- е. Жидкая фаза.
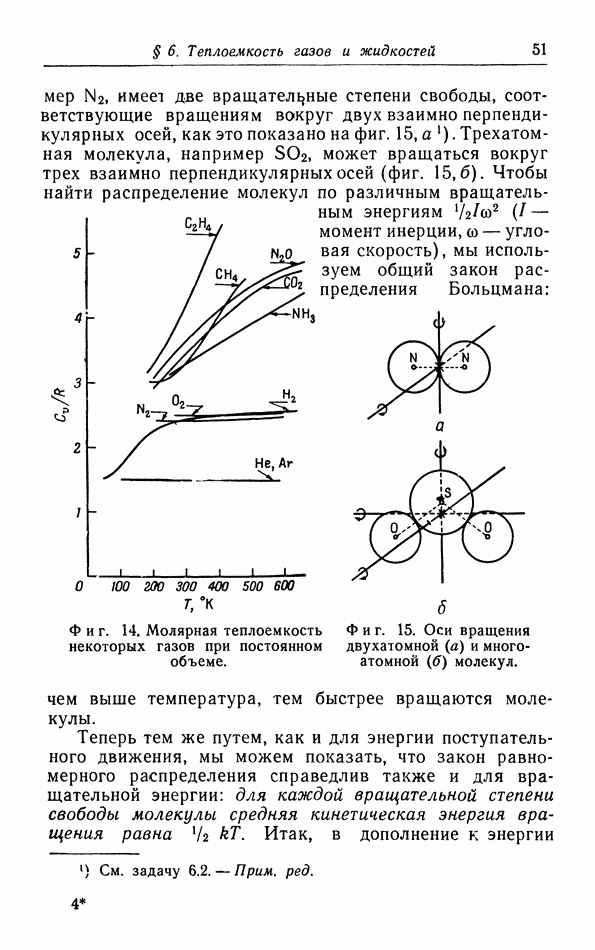
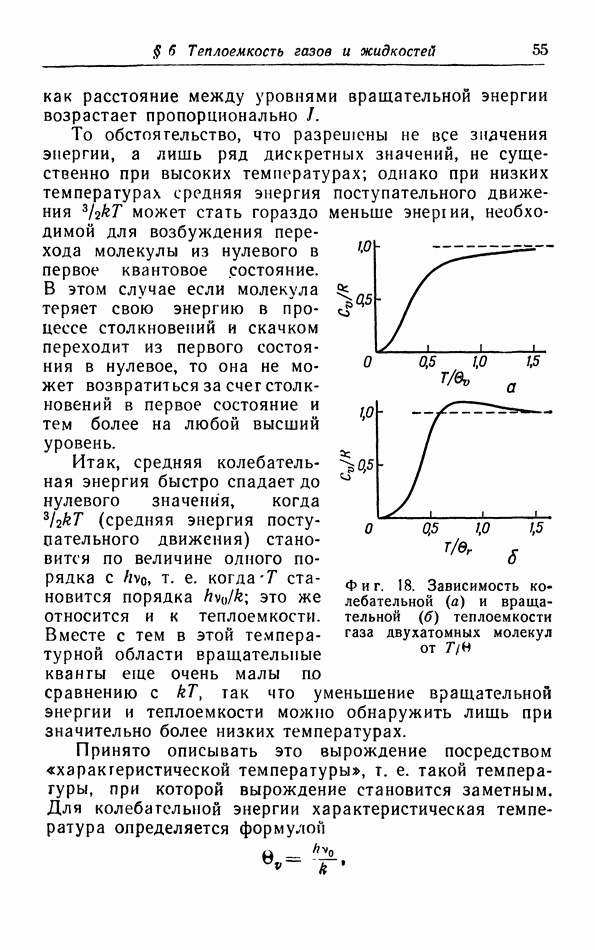
- § 6. Теплоемкость газов и жидкостей
- б. Классическая теория колебательной теплоемкости.
- в. Квантовая теория теплоемкости.
- г. Расчет колебательной теплоемкости двухатомной молекулы.
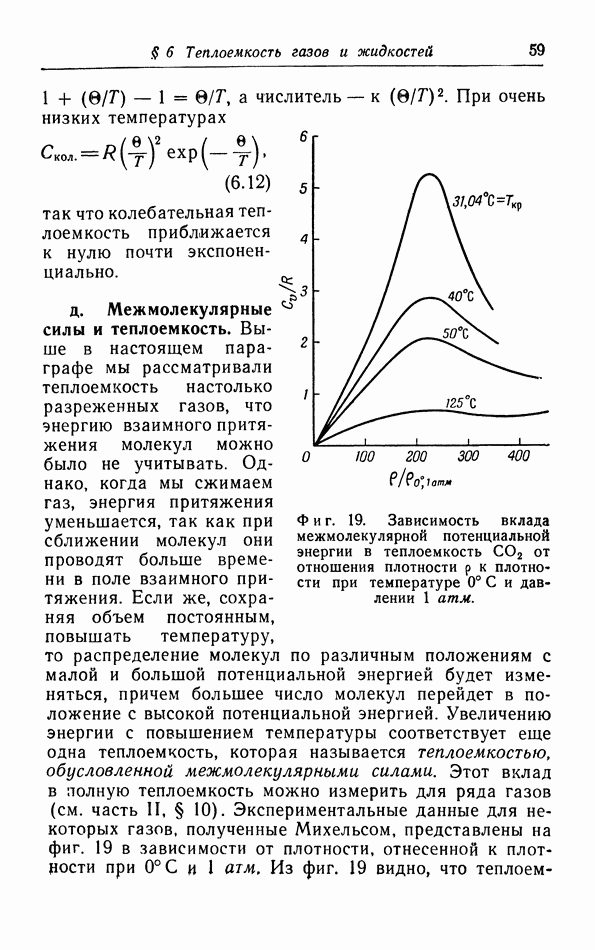
- д. Межмолекулярные силы и теплоемкость.
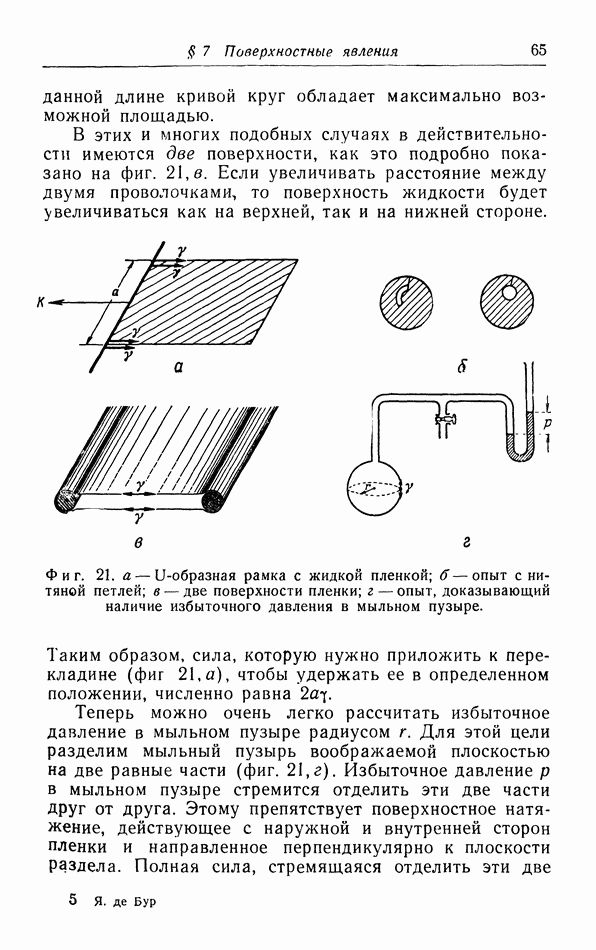
- § 7. Поверхностные явления
- б. Жидкие пленки.
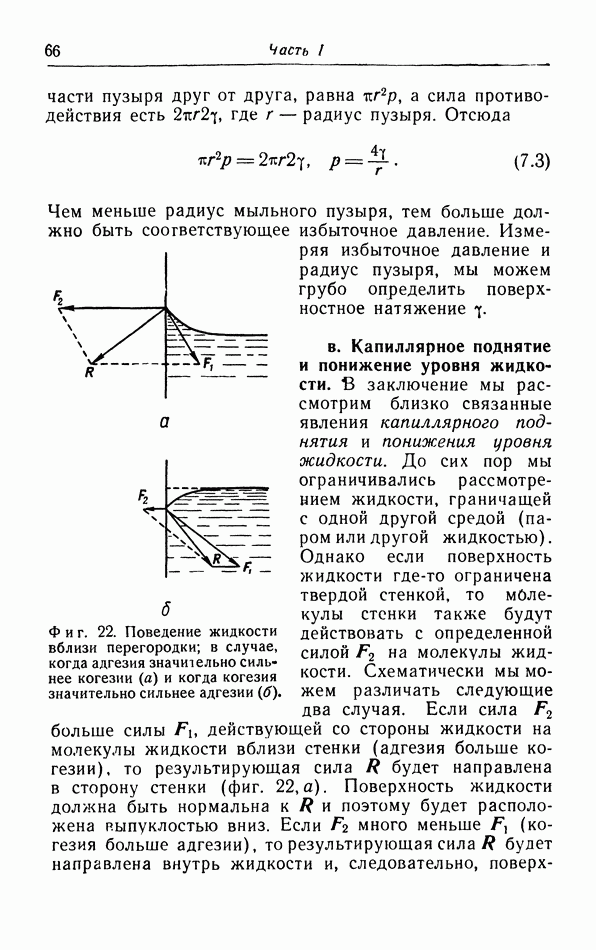
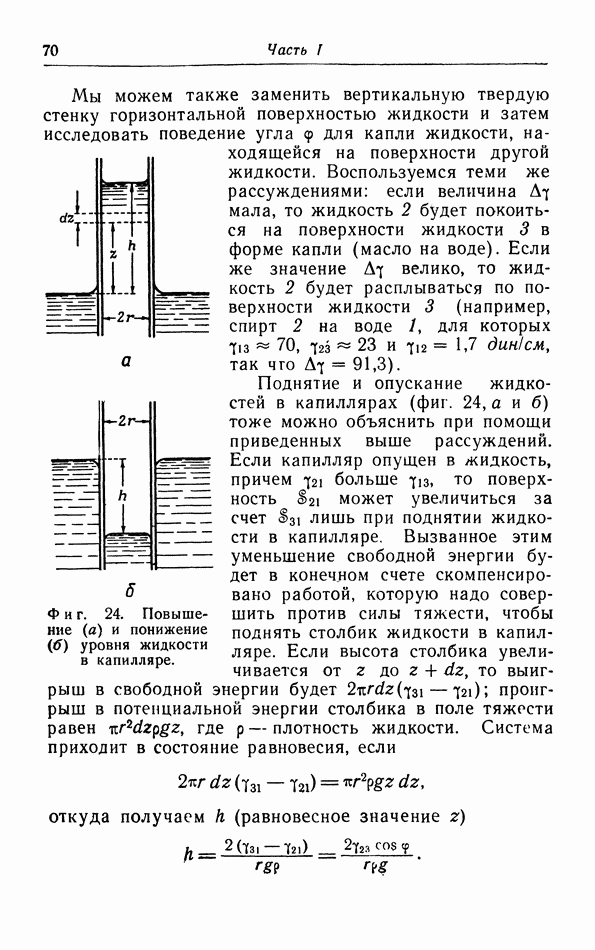
- в. Капиллярное поднятие и понижение уровня жидкости.
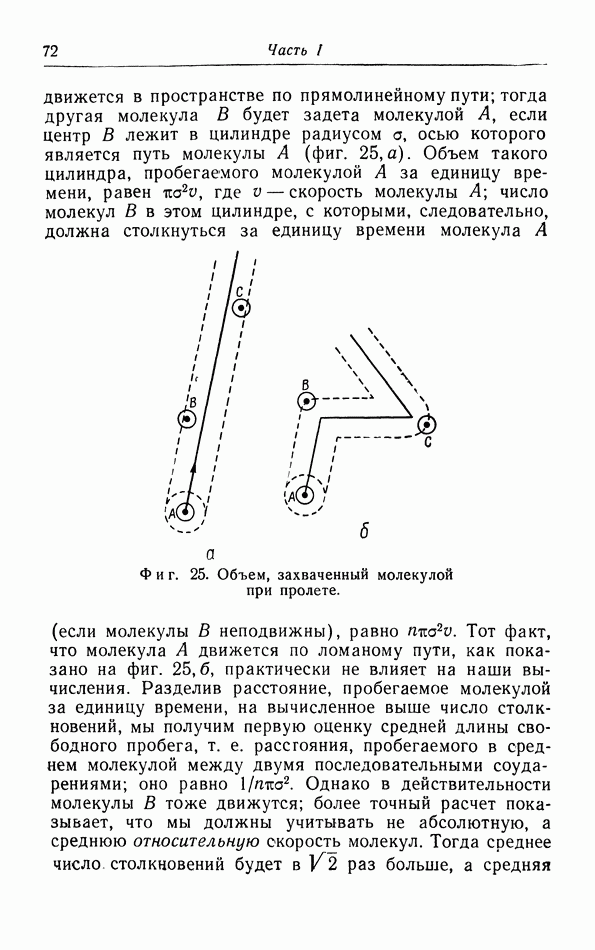
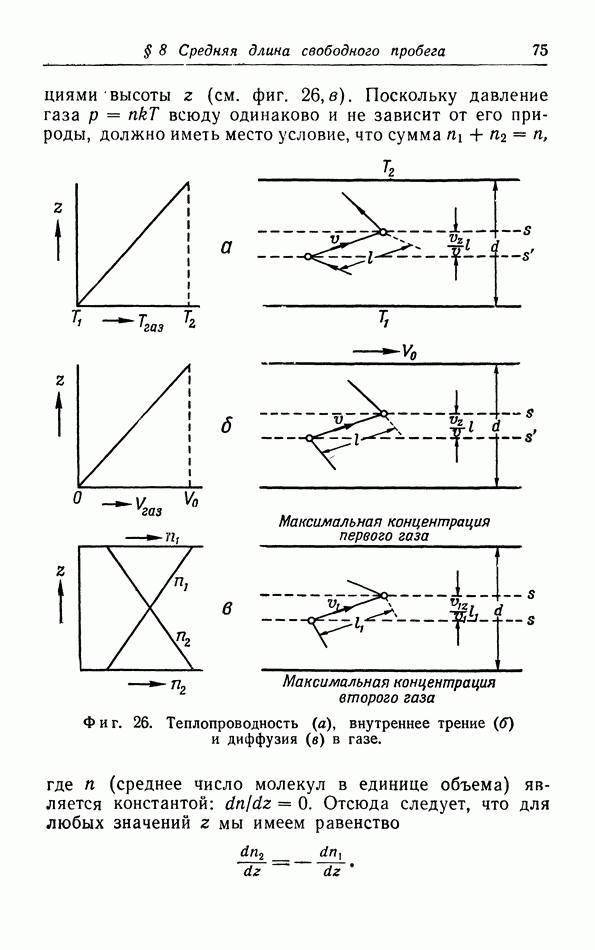
- § 8. Средняя длина свободного пробега, теплопроводность, вязкость и диффузия
- ГЛАВА II. Твердые тела
- § 9. Структура твердых тел
- § 10. Уравнение состояния твердых тел
- § 11. Теплоемкость твердых тел
- в. Колебания линейной цепочки.
- г. Колебания двумерной решетки.
- д. Колебания трехмерной решетки.
- е. Теория Дебая.
- § 12. Влияние квантовых закономерностей на распределение частиц по скоростям
- ГЛАВА III. Излучение
- § 13. Тепловое излучение и свет
- § 14. Испускание, поглощение и плотность излучения
- б. Яркость и излучательная способность.
- в. Плотность излучения.
- г. Закон Кирхгофа.
- § 15. Фотонная гипотеза. Давление излучения
- § 16. Зависимость плотности излучения от температуры и длины волны
- б. Закон смещения Вина.
- в. Закон излучения Релея — Джинса.
- г. Закон излучения Планка.
- ГЛАВА I. Первый закон термодинамики
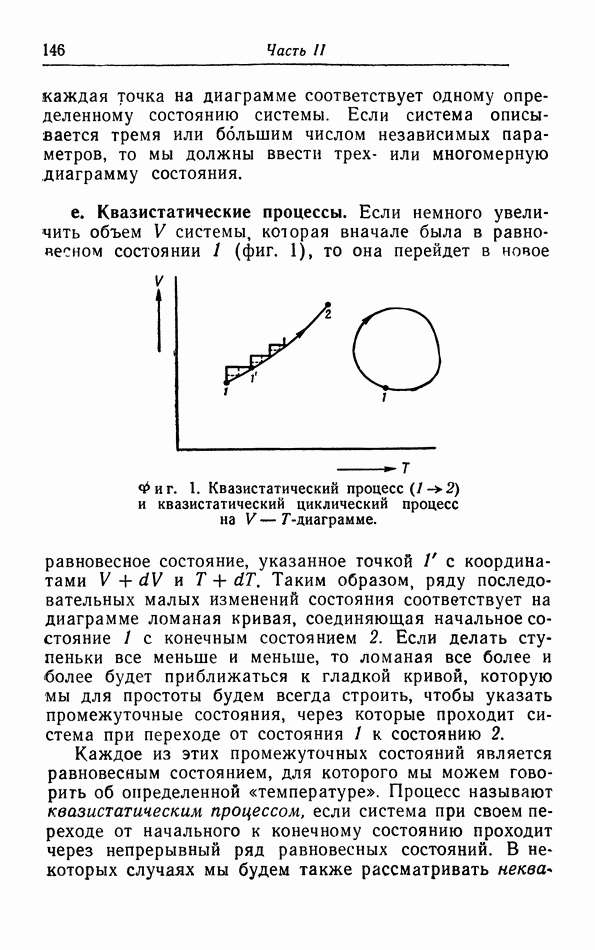
- § 1. Термодинамическое состояние и его изменения
- § 2. Работа при квазистатических процессах
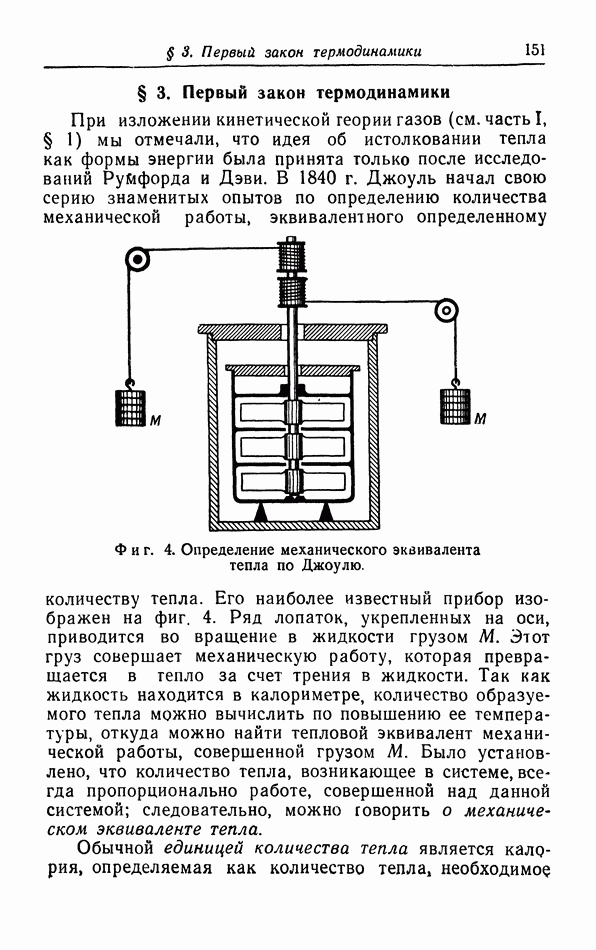
- § 3. Первый закон термодинамики
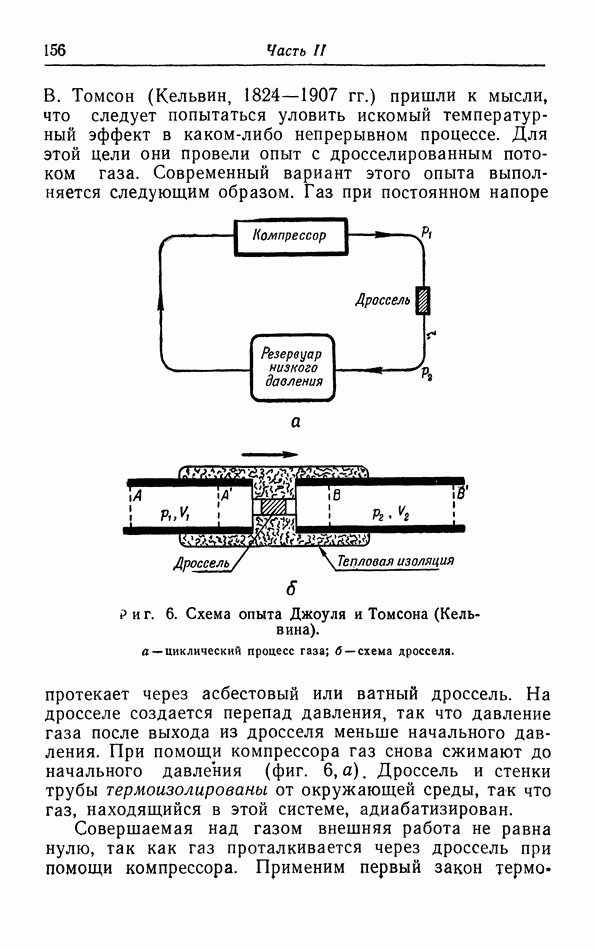
- § 4. Опыты Джоуля и Томсона
- § 5. Дальнейшие приложения первого закона
- б. Теплоемкость.
- в. Работа при адиабатических процессах.
- ГЛАВА II. Второй закон термодинамики
- § 6. Работа и теплота в циклических процессах
- § 7. Второе начало термодинамики и его различные формулировки
- § 8. Температура
- § 9. Энтропия и второй закон термодинамики
- § 10. Применения второго закона термодинамики
- в. Изэнтропические изменения состояния.
- г. Изэнтропические холодильные процессы (процесс Ж. Клода).
- д. Иззнтропические холодильные процессы (адиабатическое размагничивание).
- е. Коэффициент полезного действия технических циклических процессов.
- ГЛАВА III. Характеристические функции
- § 11. Энергия и энтальпия
- б. Расчет процессов Джоуля и Джоуля — Томсона (Кельвина).
- в. Зависимость внутренней энергии от объема.
- г. Вывод закона Стефана — Больцмана.
- д. Характеристические функции U и H.
- § 12. Свободная энергия
- б. Свободная энергия и поверхностное натяжение.
- в. Свободная энергия и гальванические элементы.
- § 13. Свободная энтальпия и термодинамический потенциал
- б. Термодинамический потенциал.
- в. Системы с более чем одним компонентом.
- § 14. Соотношения Максвелла
- ГЛАВА IV. Неквазистатические процессы. Равновесие
- § 15. Неквазистатические процессы
- б. Подвод тепла и изменение энтропии.
- в. Увеличение энтропии в адиабатических системах.
- г. Неквазистатический изотермический процесс.
- § 16. Условия равновесия
- б. Первое условие равновесия.
- в. Второе условие равновесия.
- г. Третье условие равновесия.
- д. p-T-диаграмма.
- е. Равновесие фаз в случае более чем одного компонента. Правило фаз.
- ГЛАВА V. Теорема Нернста
- § 17. Теорема Нернста
- § 18. Применение теоремы Нернста к фазовым переходам