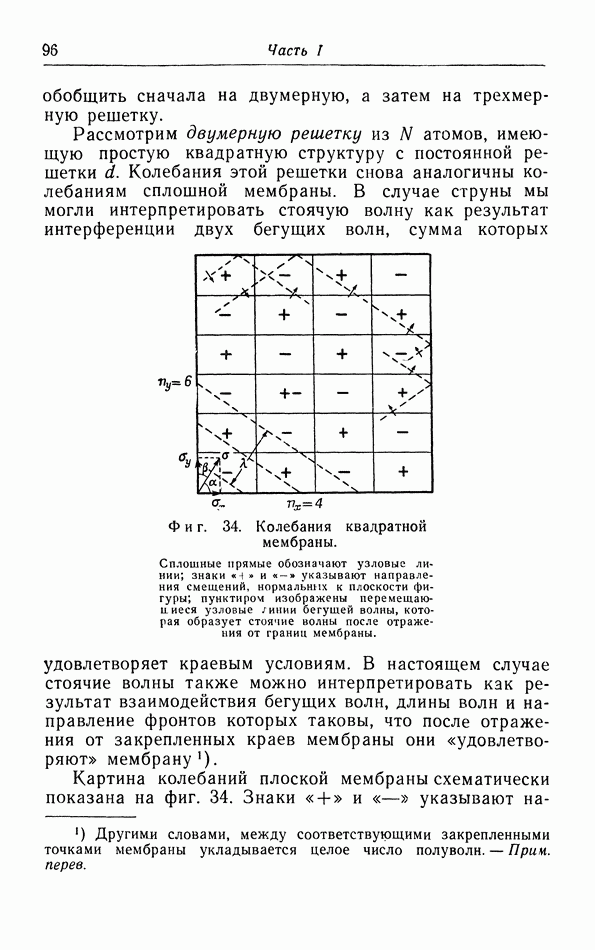
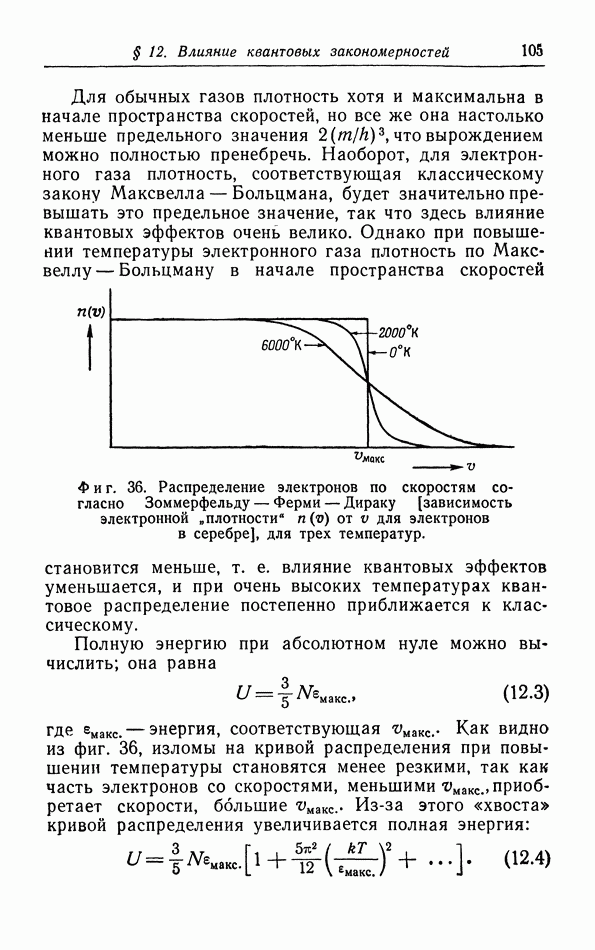
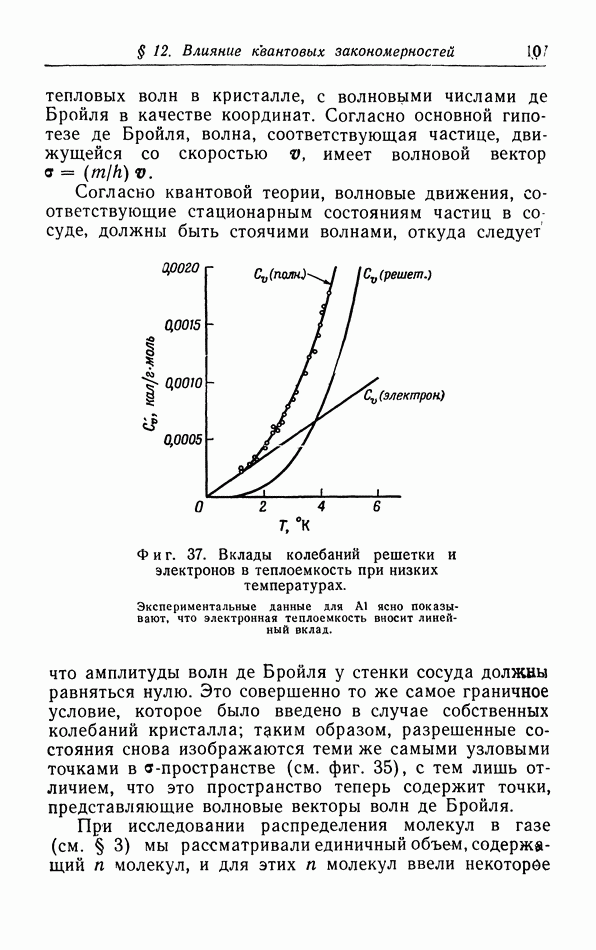
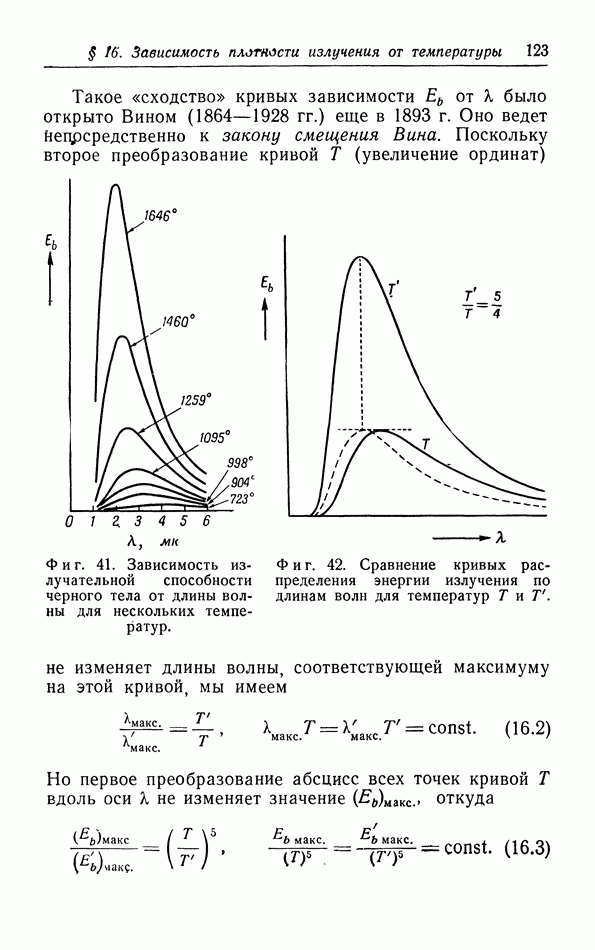
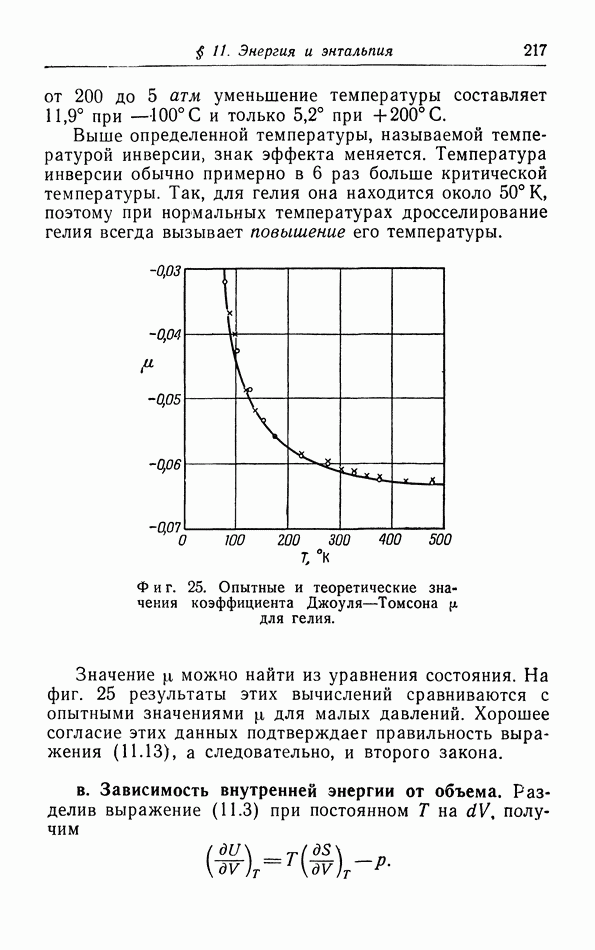
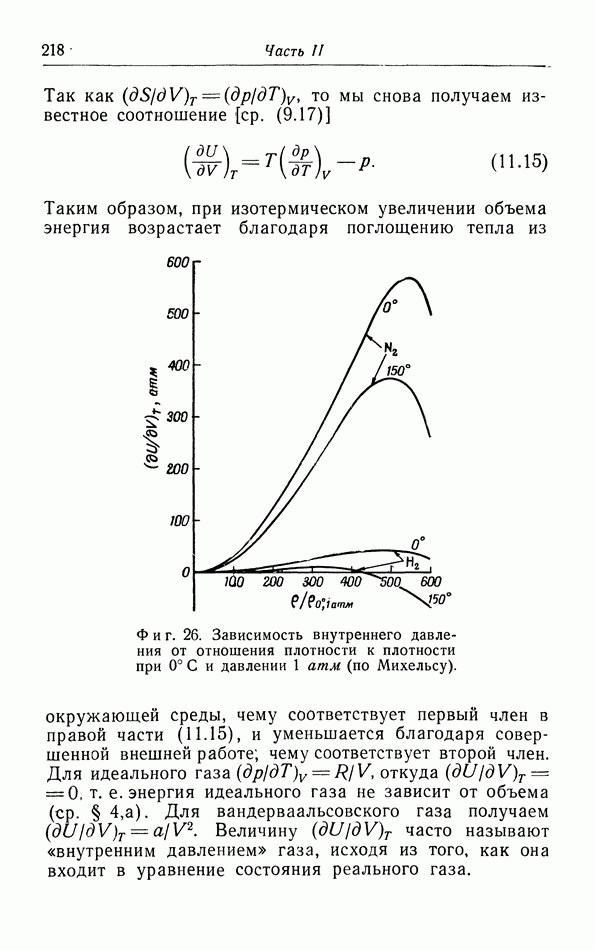
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ГЛАВА IV. Неквазистатические процессы. Равновесие
§ 15. Неквазистатические процессы
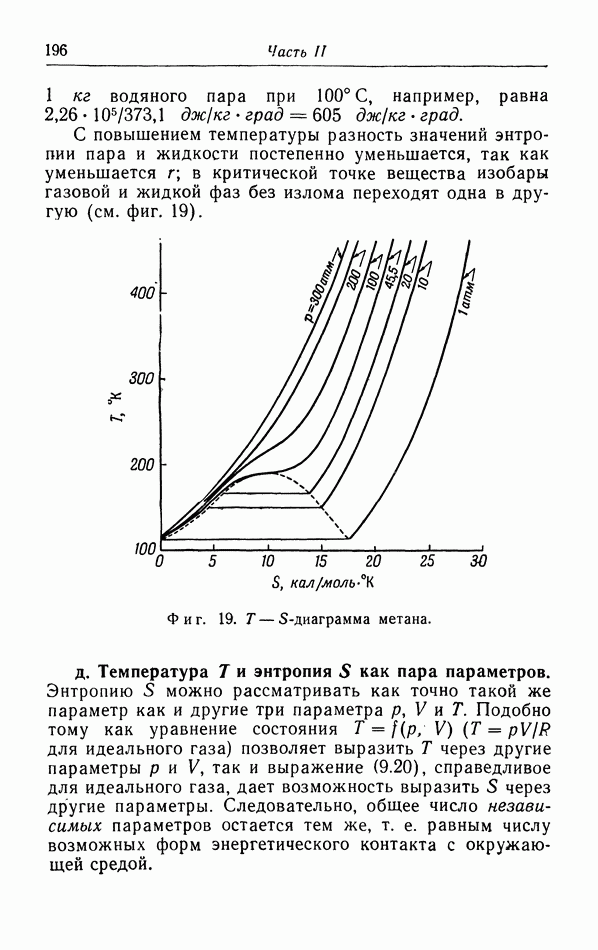
а. Естественные процессы.
В предыдущих параграфах мы ограничивались ргосыотртш квазистатических процессов. Такой процесс складывается из ряда последовательных очень малых изменений состояния, после каждого из которых система снова приходит в равновесие. Квазистатический процесс можно осуществить рядом очень малых и медленных изменений внешних параметров, описывающих систему.
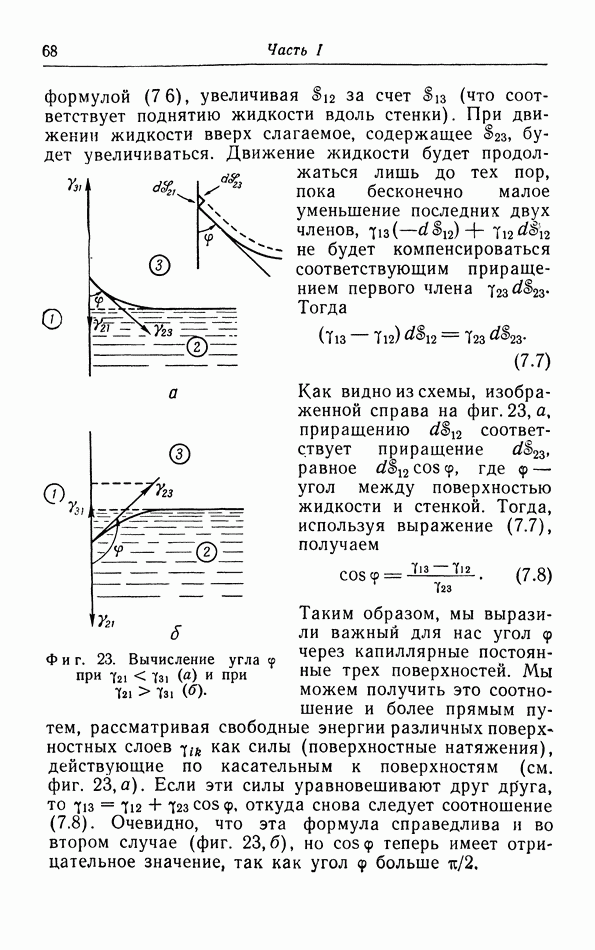
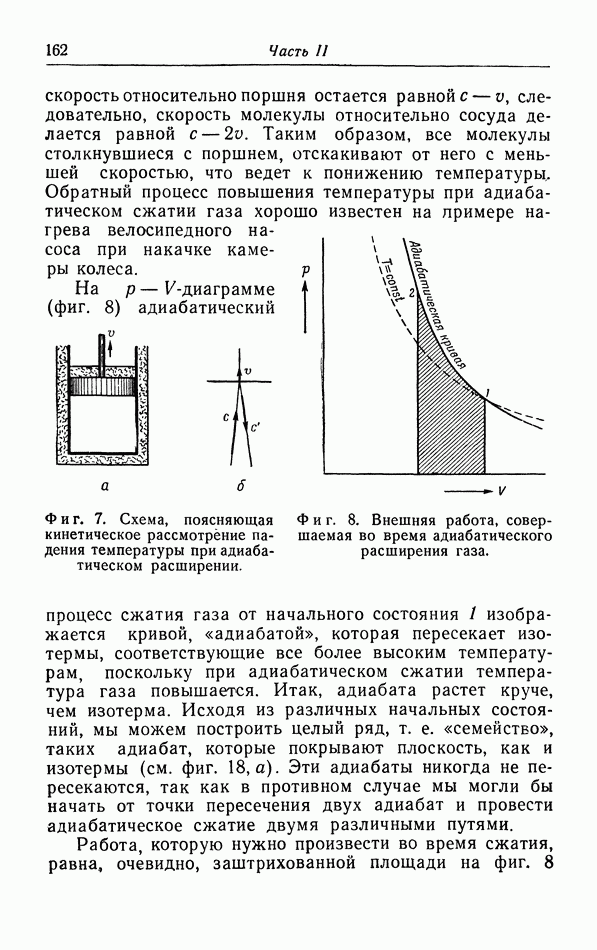
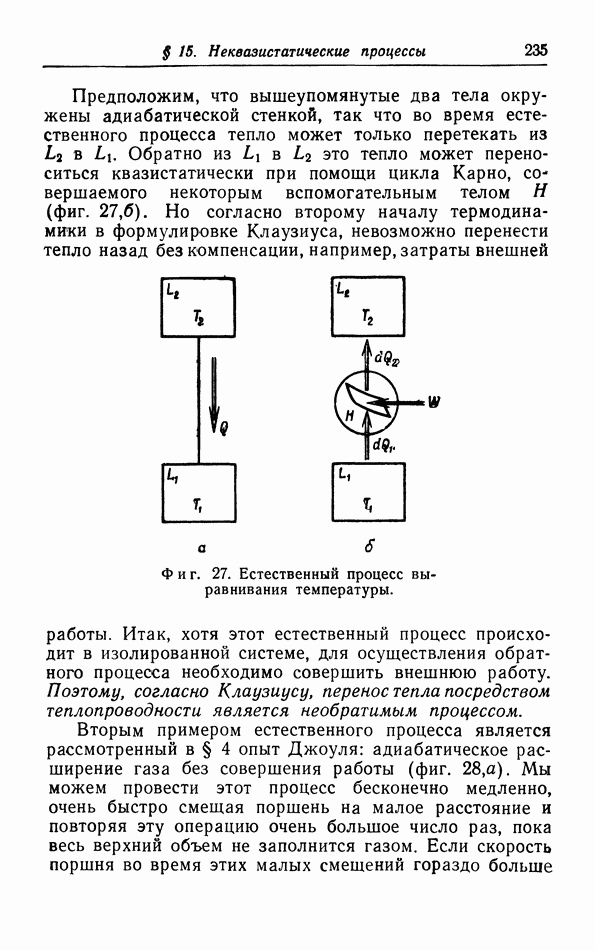
Общеизвестным типом неквазистатических процессов являются так называемые естественные процессы, т. е. процессы, которые действительно происходят в природе и которые, однажды начавшись, совершаются без дальнейшего внешнего воздейстйия. Рассмотрим два тела  с неодинаковыми температурами
с неодинаковыми температурами  Мы можем начать естественный процесс, соединив эти два тела теплопроводящей проволокой (фиг. 21,а). Тогда тепло само по себе будет переходить от
Мы можем начать естественный процесс, соединив эти два тела теплопроводящей проволокой (фиг. 21,а). Тогда тепло само по себе будет переходить от  пока температуры не станут равными. Даже если этот процесс совершается очень медленно (малая теплопроводность проволоки), все равно между этим естественным процессом и квазистатическим процессом остаются принципиальные различия: каждое из промежуточных состояний естественного процесса является неравновесным; кроме того, такой процесс совершается сам по себе (для его осуществления не нужно производить непрерывные малые изменения внешних параметров).
пока температуры не станут равными. Даже если этот процесс совершается очень медленно (малая теплопроводность проволоки), все равно между этим естественным процессом и квазистатическим процессом остаются принципиальные различия: каждое из промежуточных состояний естественного процесса является неравновесным; кроме того, такой процесс совершается сам по себе (для его осуществления не нужно производить непрерывные малые изменения внешних параметров).
Более того, очевидно, что естественный процесс является необратимым в противоположность квазистатическим процессам. Это можно видеть из различных примеров. Необратимость следует также из второго начала термодинамики.
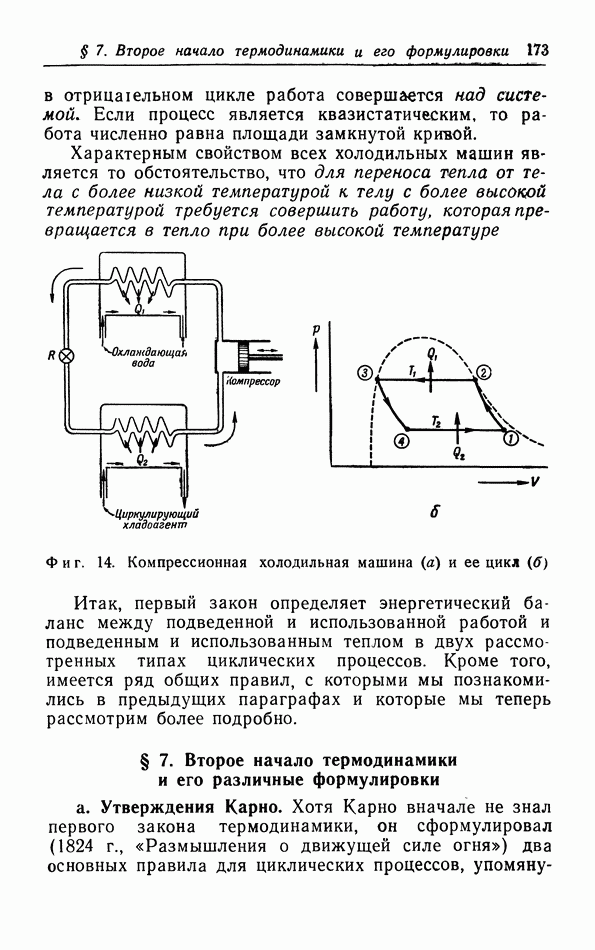
Предположим, что вышеупомянутые два тела окружены адиабатической стенкой, так что во время естественного процесса тепло может только перетекать из  Обратно из
Обратно из  это тепло может переноситься квазистатически при помощи цикла Карно, совершаемого некоторым вспомогательным телом Я (фиг. 27,б). Но согласно второму началу термодинамики в формулировке Клаузиуса, невозможно перенести тепло назад без компенсации, например, затраты внешней работы.
это тепло может переноситься квазистатически при помощи цикла Карно, совершаемого некоторым вспомогательным телом Я (фиг. 27,б). Но согласно второму началу термодинамики в формулировке Клаузиуса, невозможно перенести тепло назад без компенсации, например, затраты внешней работы.

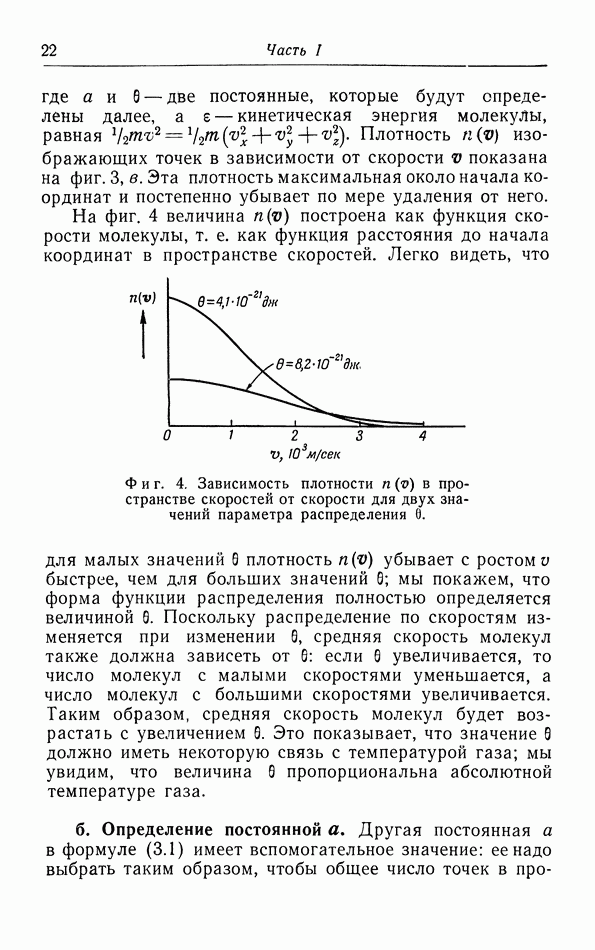
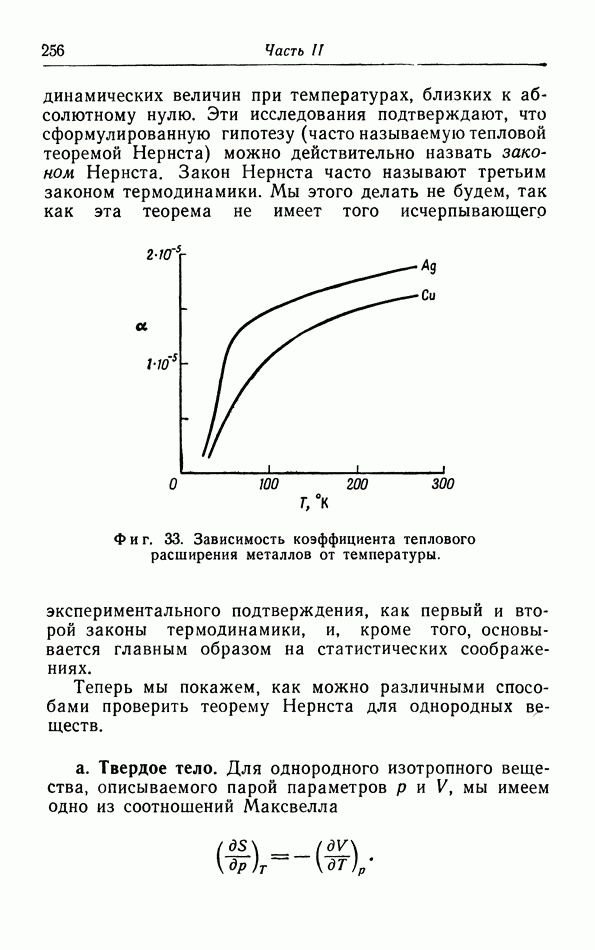
Фиг. 27. Естественный процесс выравнивания температуры.
Итак, хотя этот естественный процесс происходит в изолированной системе, для осуществления обратного процесса необходимо совершить внешнюю работу. Поэтому, согласно Клаузиусу, перенос тепла посредством теплопроводности является необратимым процессом.
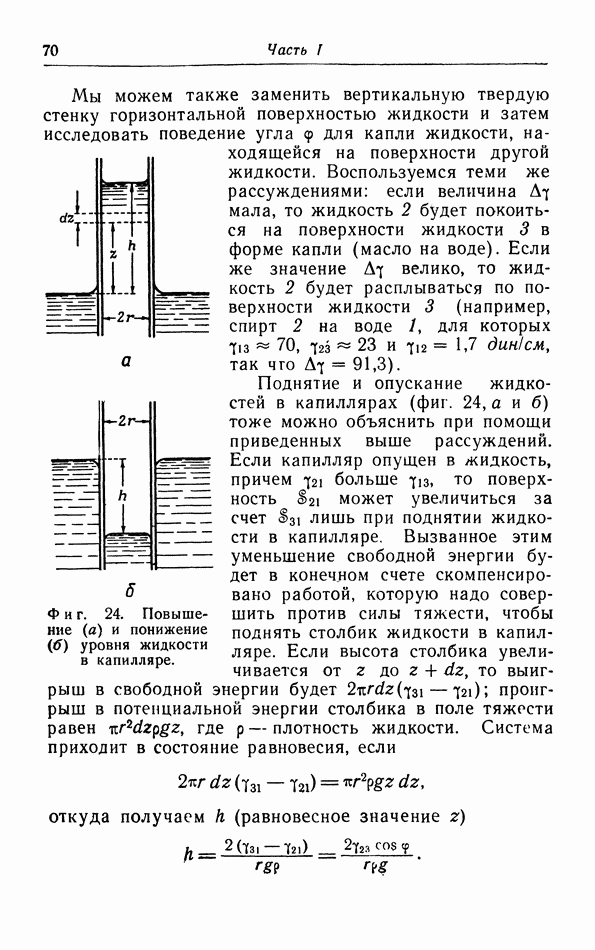
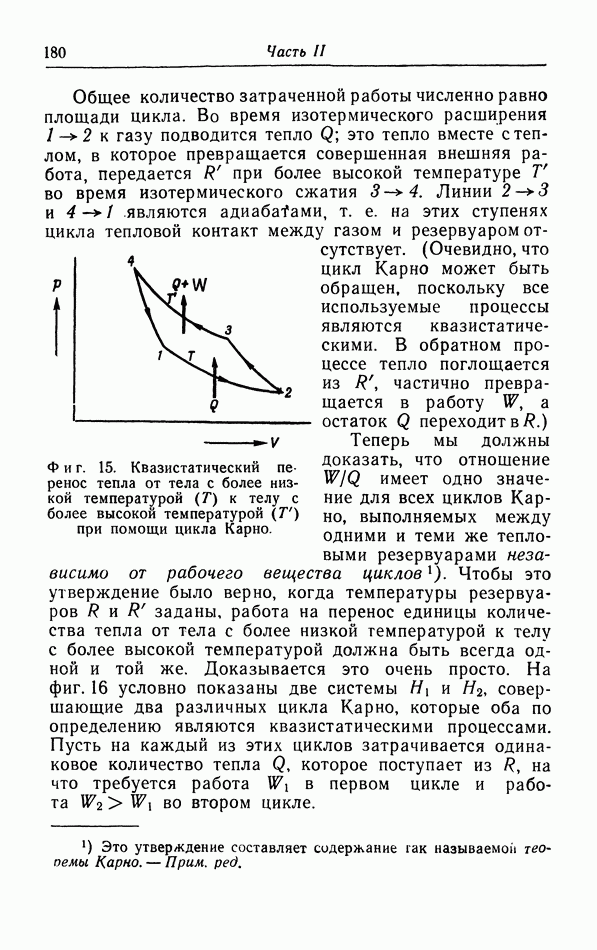
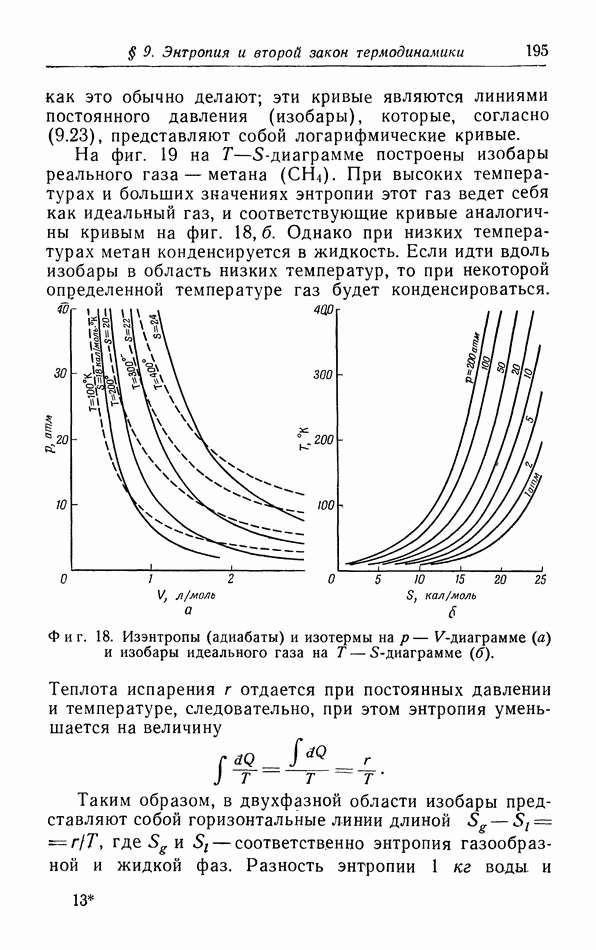
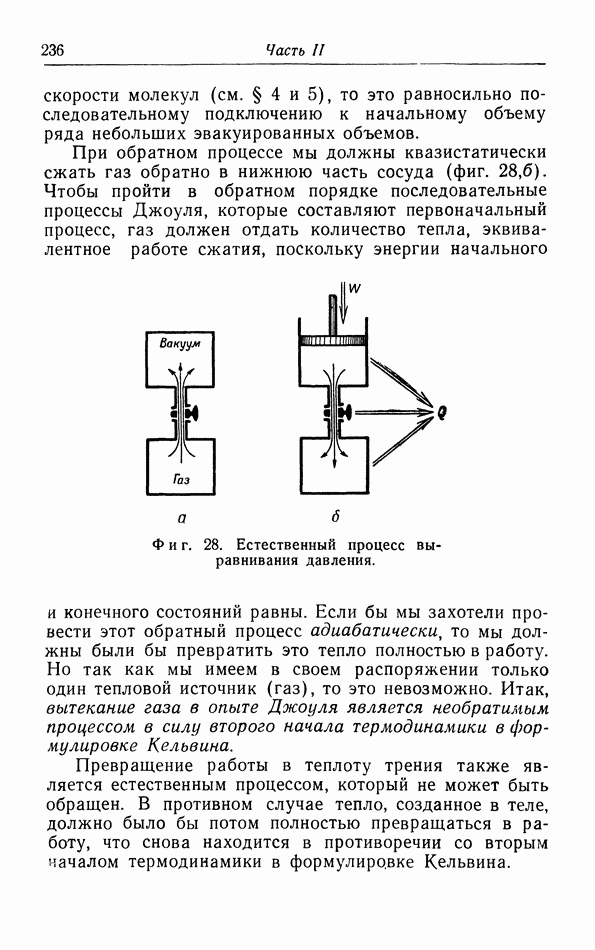
Вторым примером естественного процесса является рассмотренный в § 4 опыт Джоуля: адиабатическое расширение газа без совершения работы (фиг. 28,а). Мы можем провести этот процесс бесконечно медленно, очень быстро смещая поршень на малое расстояние и повторяя эту операцию очень большое число раз, пока весь верхний объем не заполнится газом. Если скорость поршня во время этих малых смещений гораздо больше
скорости молекул (см. § 4 и 5), то это равносильно последовательному подключению к начальному объему ряда небольших эвакуированных объемов.
При обратном процессе мы должны квазистатически сжать газ обратно в нижнюю часть сосуда (фиг. 28,б). Чтобы пройти в обратном порядке последовательные процессы Джоуля, которые составляют первоначальный процесс, газ должен отдать количество тепла, эквивалентное работе сжатия, поскольку энергии начального и конечного состояний равны.

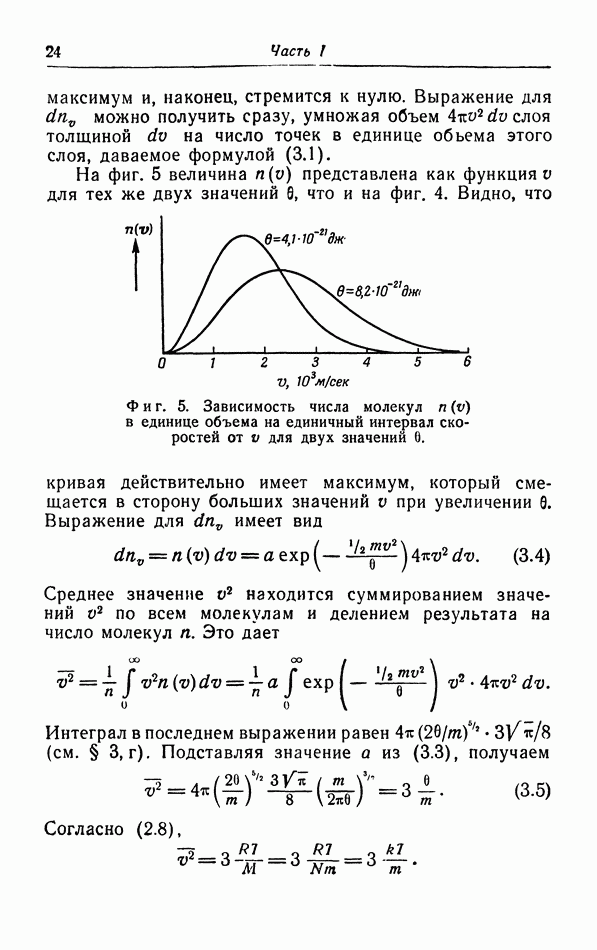
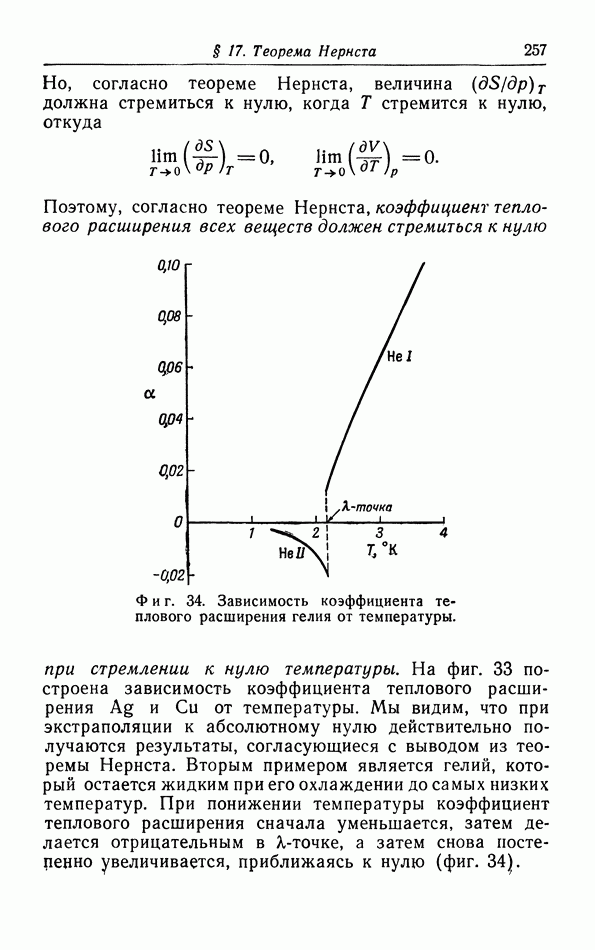
Фиг. 28. Естественный процесс выравнивания давления.
Если бы мы захотели провести этот обратный процесс адиабатически то мы должны были бы превратить это тепло полностью в работу. Но так как мы имеем в своем распоряжении только один тепловой источник (газ), то это невозможно. Итак, вытекание газа в опыте Джоуля является необратимым процессом в силу второго начала термодинамики в формулировке Кельвина.
Превращение работы в теплоту трения также является естественным процессом, который не может быть обращен. В противном случае тепло, созданное в теле, должно было бы потом полностью превращаться в работу, что снова находится в противоречии со вторым началом термодинамики в формулировке Кельвина.
Естественные процессы, приведенные выше, мы предполагали медленными. Таким путем мы хотели подчеркнуть, насколько существенно естественные процессы отличаются от квазистатических процессов, несмотря на то что все промежуточные состояния могут быть известными функциями времени. Для большинства естественных процессов, не являющихся медленными, различие будет еще больше. В качестве примера можно назвать опыт Джоуля, как он выполняется в действительности, или процесс обмена теплом между двумя телами с различной температурой. В этих примерах невозможно определить промежуточные состояния, и «необратимость» означает невозможность достижения начального состояния, исходя из конечного состояния, посредством квазистатического процесса, проводимого при тех же самых внешних условиях.
В каждом неквазистатическом процессе имеют место один или оба указанных выше типа естественных процессов. Так, когда система нагревается слишком быстро, возникает большая разность температур, которая исчезает сама по себе, т. е. в результате естественных процессов, подобно тому как исчезают турбулентные завихрения, появляющиеся при быстром сжатии. Поэтому мы можем сказать, что в общем случае неквазистатические процессы необратимы в силу второго начала термодинамики.
Прежде чем перейти к дальнейшему обсуждению свойств неквазистатических процессов, мы заметим, что вместо двух формулировок второго начала термодинамики, а именно формулировок Клаузиуса и Кельвина, мы могли бы ввести следующий основной принцип: естественный процесс является необратимым. Тогда формулировка Клаузиуса следует, в частности, из рассмотрения естественного потока тепла от тела с более высокой к телу с более низкой температурой, а формулировка Кельвина вытекает из необратимости непрерывного превращения работы в тепло.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие к русскому изданию
- ГЛАВА I. Газы и жидкости
- § 1. Молекулярная структура газов и жидкостей
- § 2. Кинетическая теория идеального газа
- б. Расчет давления в кинетической теории газов.
- в. Расчет удельной теплоемкости в кинетической теории газов.
- § 3. Распределение молекул по скорости их движения
- г. Средняя квадратичная и средняя скорости.
- д. Броуновское движение.
- е. Опыты с молекулярными пучками.
- § 4. Общее распределение молекул по энергиям
- б. Возбужденные состояния.
- в. вращательная и колебательная энергии.
- г. Потенциальная энергия тяготения.
- д. Потенциальная энергия межмолекулярных сил.
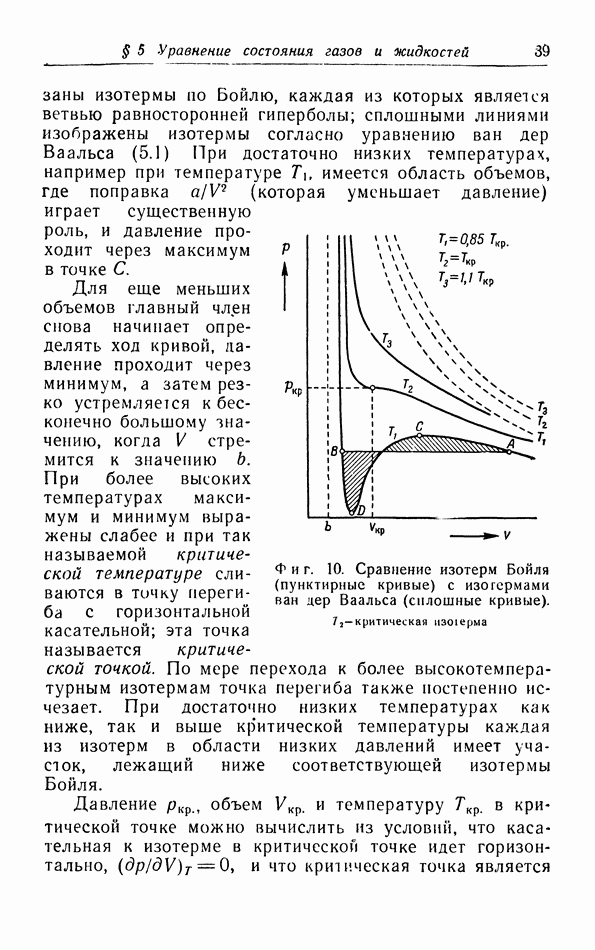
- § 5. Уравнение состояния газов и жидкостей
- б. Обсуждение уравнения ван дер Ваальса.
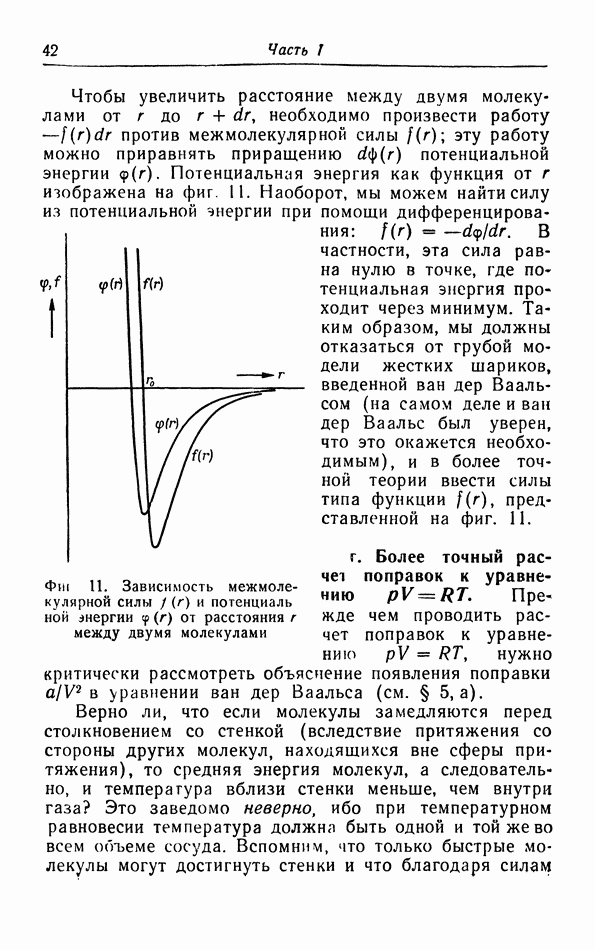
- в. Взаимодействие молекул.
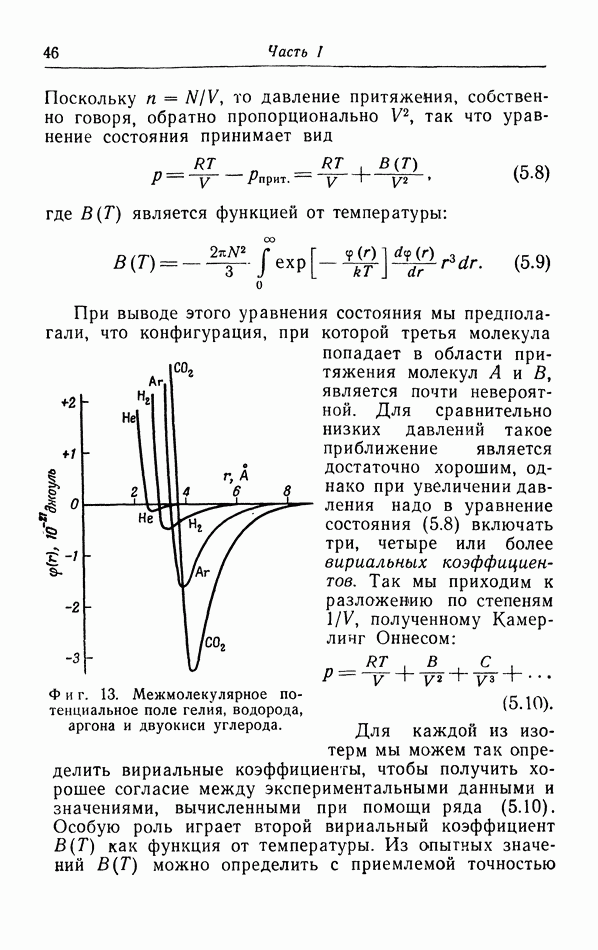
- г. Более точный расчет поправок к уравнению pV=RT.
- д. Закон соответственных состояний.
- е. Жидкая фаза.
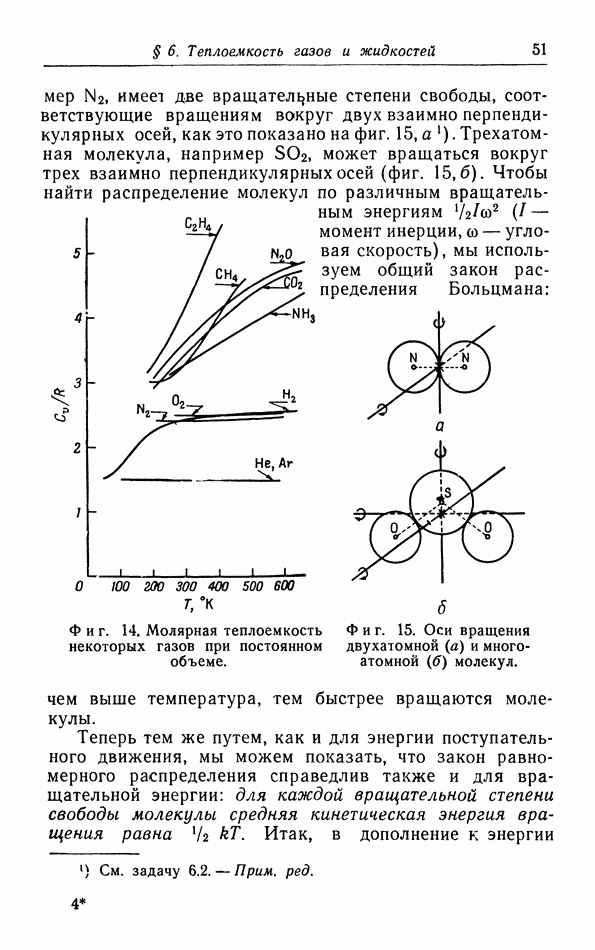
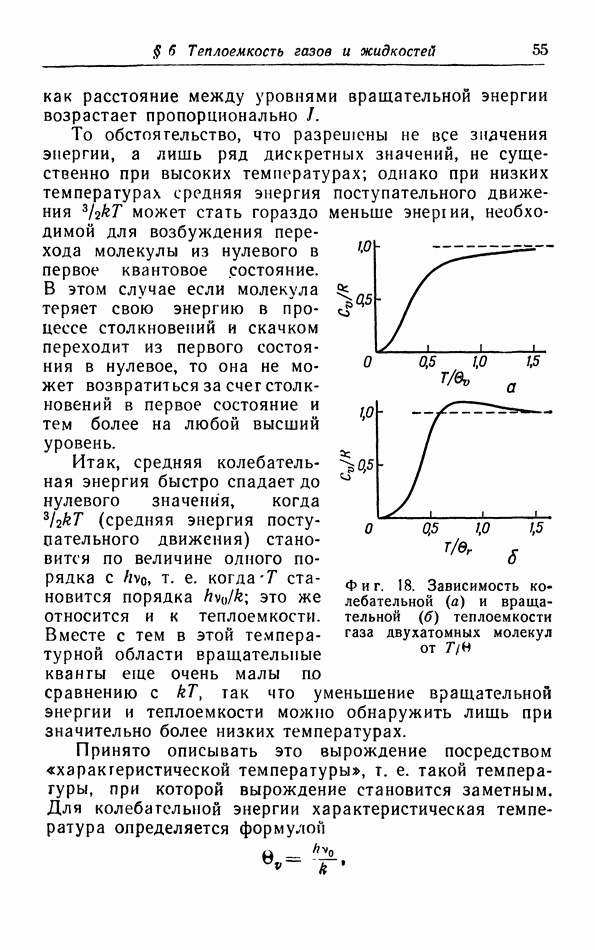
- § 6. Теплоемкость газов и жидкостей
- б. Классическая теория колебательной теплоемкости.
- в. Квантовая теория теплоемкости.
- г. Расчет колебательной теплоемкости двухатомной молекулы.
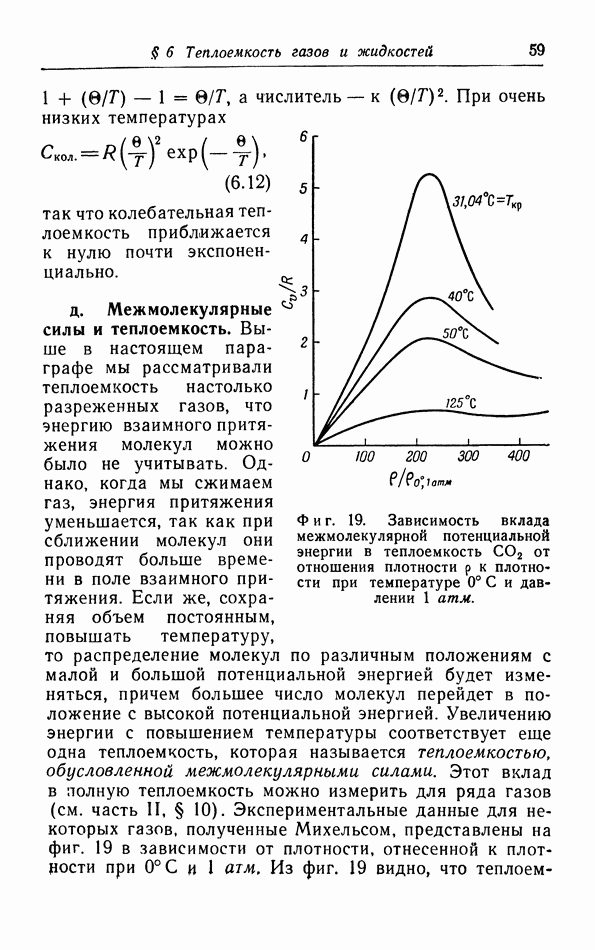
- д. Межмолекулярные силы и теплоемкость.
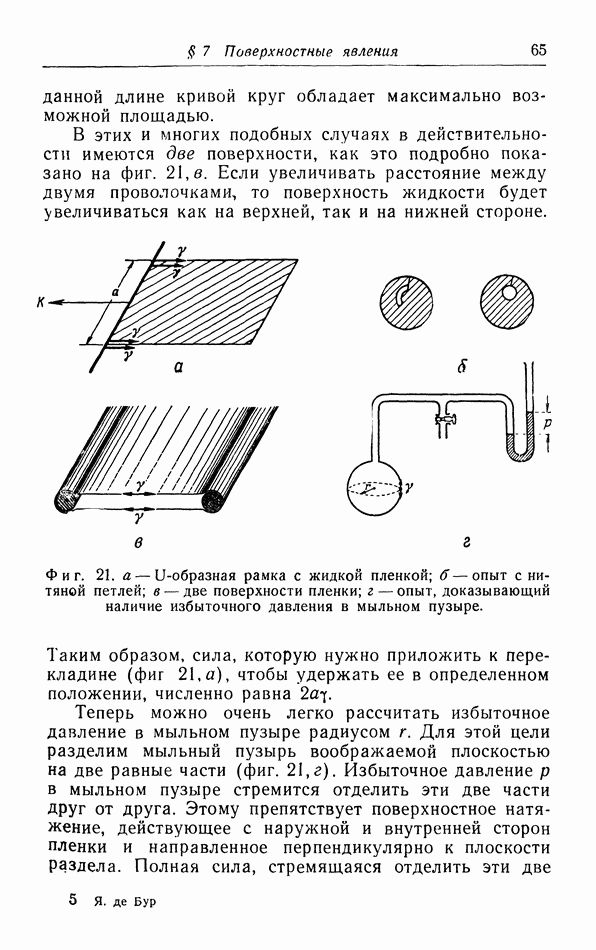
- § 7. Поверхностные явления
- б. Жидкие пленки.
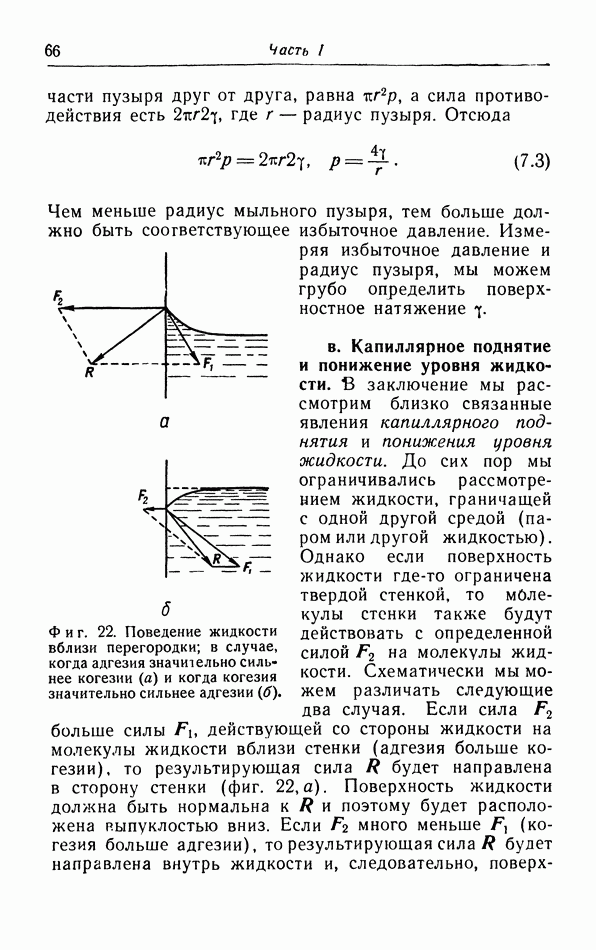
- в. Капиллярное поднятие и понижение уровня жидкости.
- § 8. Средняя длина свободного пробега, теплопроводность, вязкость и диффузия
- ГЛАВА II. Твердые тела
- § 9. Структура твердых тел
- § 10. Уравнение состояния твердых тел
- § 11. Теплоемкость твердых тел
- в. Колебания линейной цепочки.
- г. Колебания двумерной решетки.
- д. Колебания трехмерной решетки.
- е. Теория Дебая.
- § 12. Влияние квантовых закономерностей на распределение частиц по скоростям
- ГЛАВА III. Излучение
- § 13. Тепловое излучение и свет
- § 14. Испускание, поглощение и плотность излучения
- б. Яркость и излучательная способность.
- в. Плотность излучения.
- г. Закон Кирхгофа.
- § 15. Фотонная гипотеза. Давление излучения
- § 16. Зависимость плотности излучения от температуры и длины волны
- б. Закон смещения Вина.
- в. Закон излучения Релея — Джинса.
- г. Закон излучения Планка.
- ГЛАВА I. Первый закон термодинамики
- § 1. Термодинамическое состояние и его изменения
- § 2. Работа при квазистатических процессах
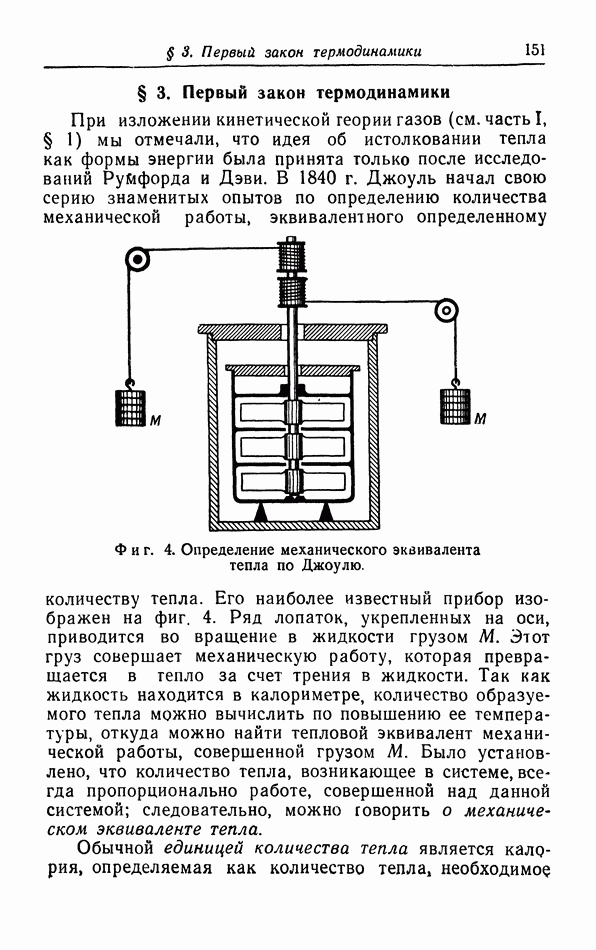
- § 3. Первый закон термодинамики
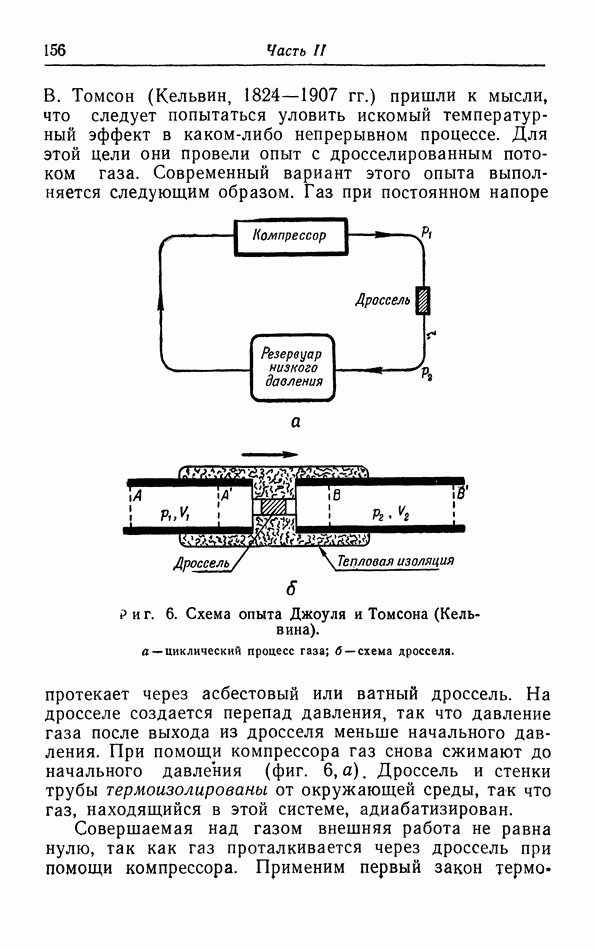
- § 4. Опыты Джоуля и Томсона
- § 5. Дальнейшие приложения первого закона
- б. Теплоемкость.
- в. Работа при адиабатических процессах.
- ГЛАВА II. Второй закон термодинамики
- § 6. Работа и теплота в циклических процессах
- § 7. Второе начало термодинамики и его различные формулировки
- § 8. Температура
- § 9. Энтропия и второй закон термодинамики
- § 10. Применения второго закона термодинамики
- в. Изэнтропические изменения состояния.
- г. Изэнтропические холодильные процессы (процесс Ж. Клода).
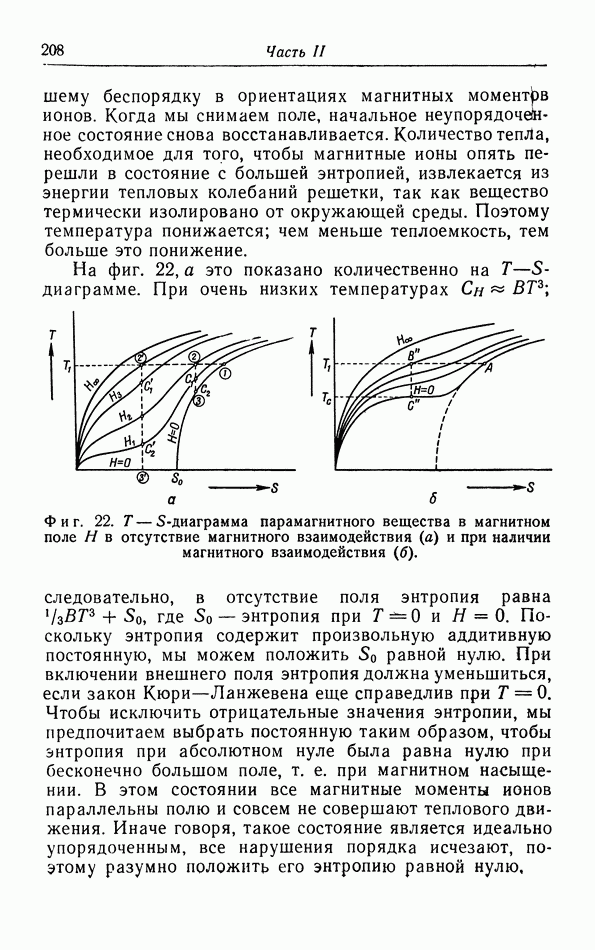
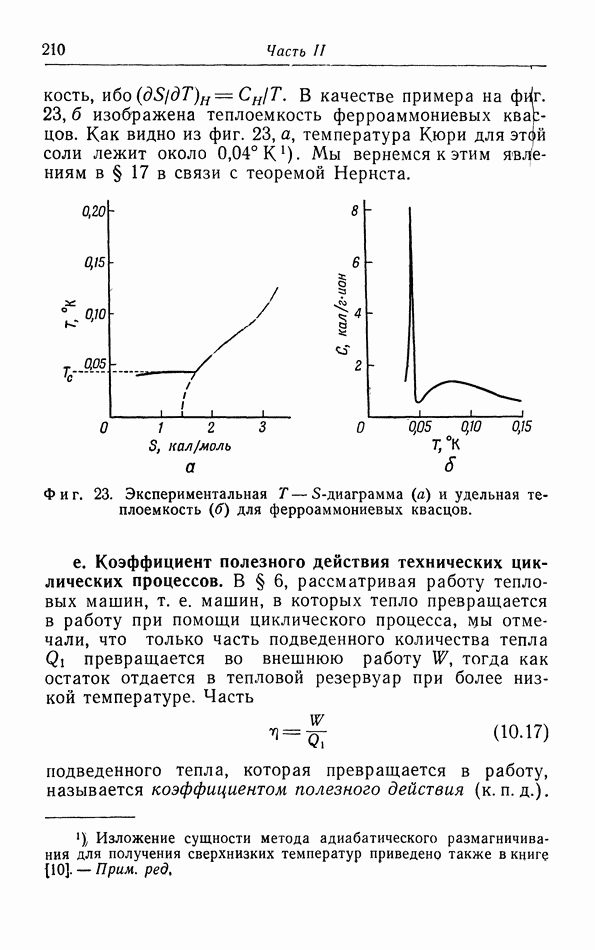
- д. Иззнтропические холодильные процессы (адиабатическое размагничивание).
- е. Коэффициент полезного действия технических циклических процессов.
- ГЛАВА III. Характеристические функции
- § 11. Энергия и энтальпия
- б. Расчет процессов Джоуля и Джоуля — Томсона (Кельвина).
- в. Зависимость внутренней энергии от объема.
- г. Вывод закона Стефана — Больцмана.
- д. Характеристические функции U и H.
- § 12. Свободная энергия
- б. Свободная энергия и поверхностное натяжение.
- в. Свободная энергия и гальванические элементы.
- § 13. Свободная энтальпия и термодинамический потенциал
- б. Термодинамический потенциал.
- в. Системы с более чем одним компонентом.
- § 14. Соотношения Максвелла
- ГЛАВА IV. Неквазистатические процессы. Равновесие
- § 15. Неквазистатические процессы
- б. Подвод тепла и изменение энтропии.
- в. Увеличение энтропии в адиабатических системах.
- г. Неквазистатический изотермический процесс.
- § 16. Условия равновесия
- б. Первое условие равновесия.
- в. Второе условие равновесия.
- г. Третье условие равновесия.
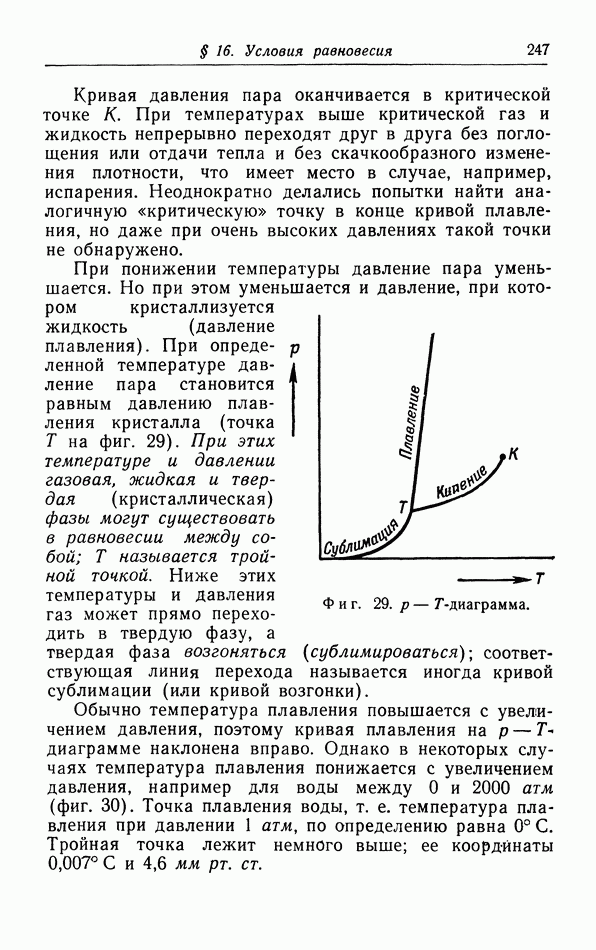
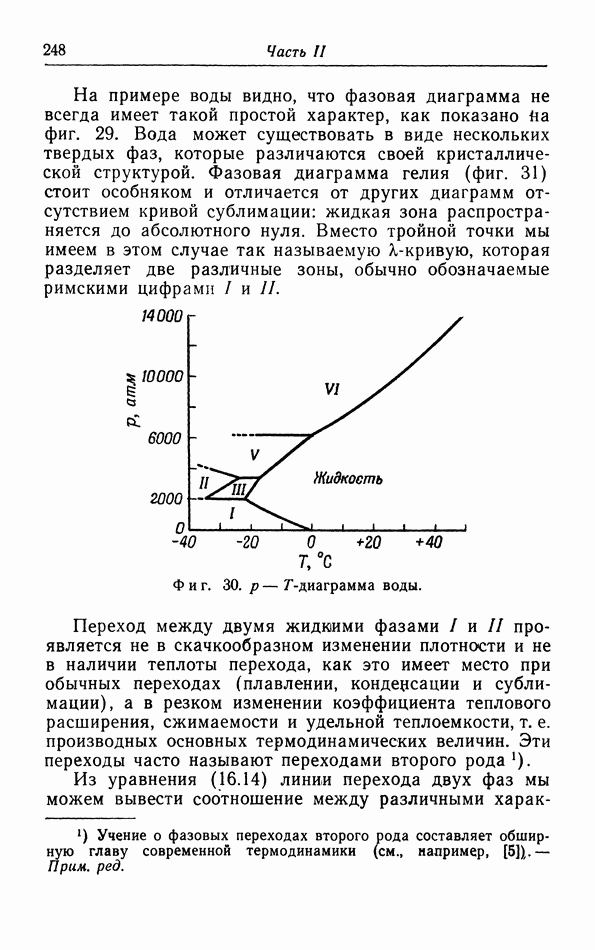
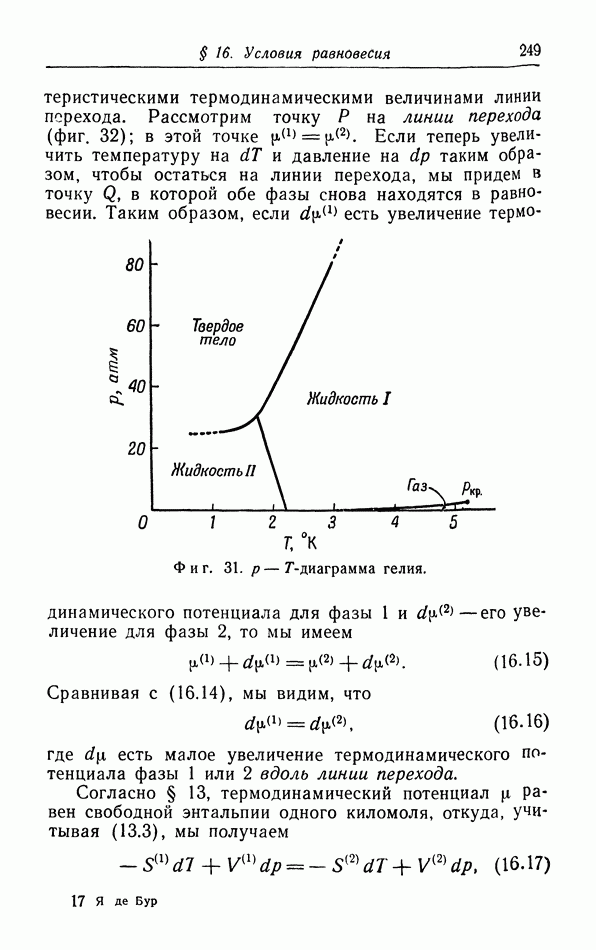
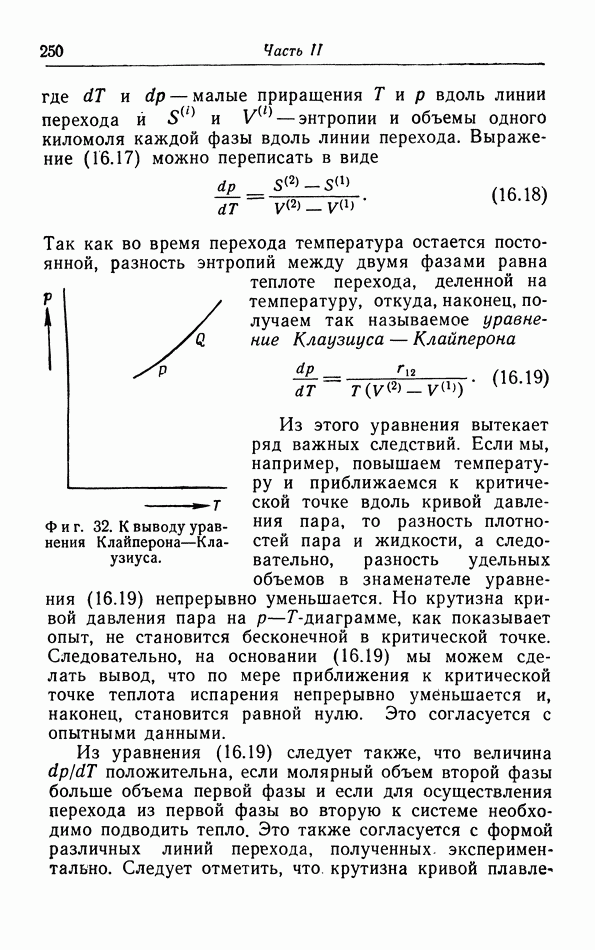
- д. p-T-диаграмма.
- е. Равновесие фаз в случае более чем одного компонента. Правило фаз.
- ГЛАВА V. Теорема Нернста
- § 17. Теорема Нернста
- § 18. Применение теоремы Нернста к фазовым переходам