| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
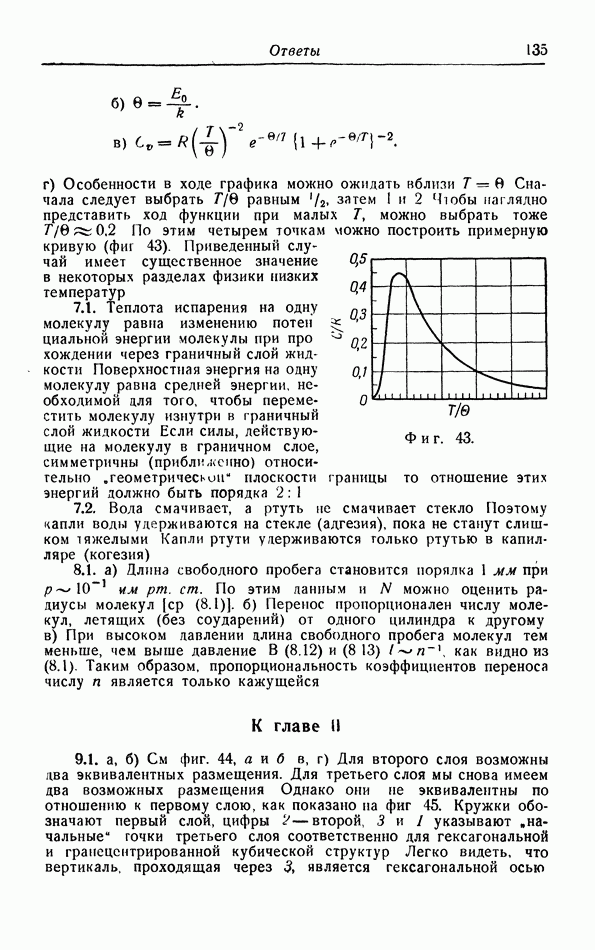
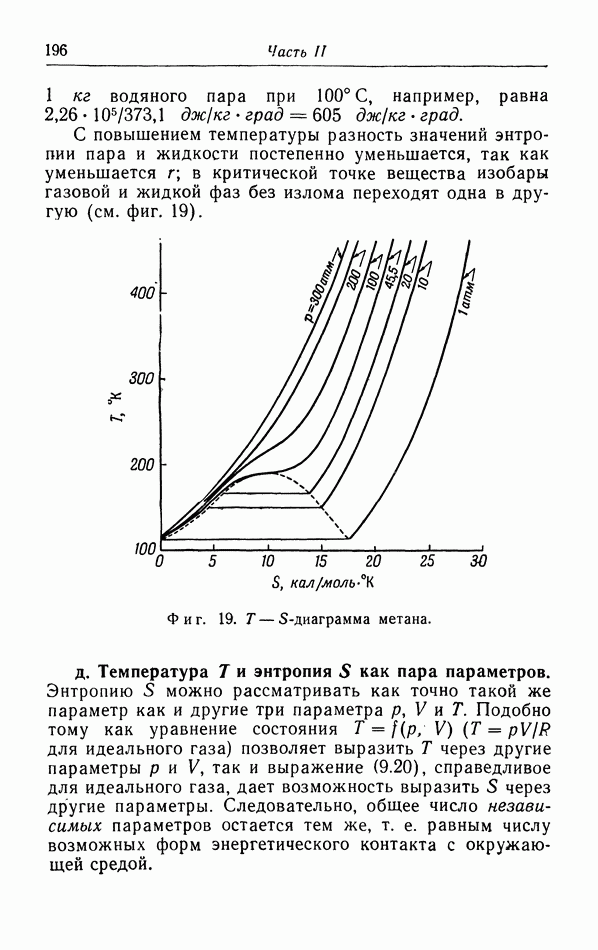
д. Закон соответственных состояний.
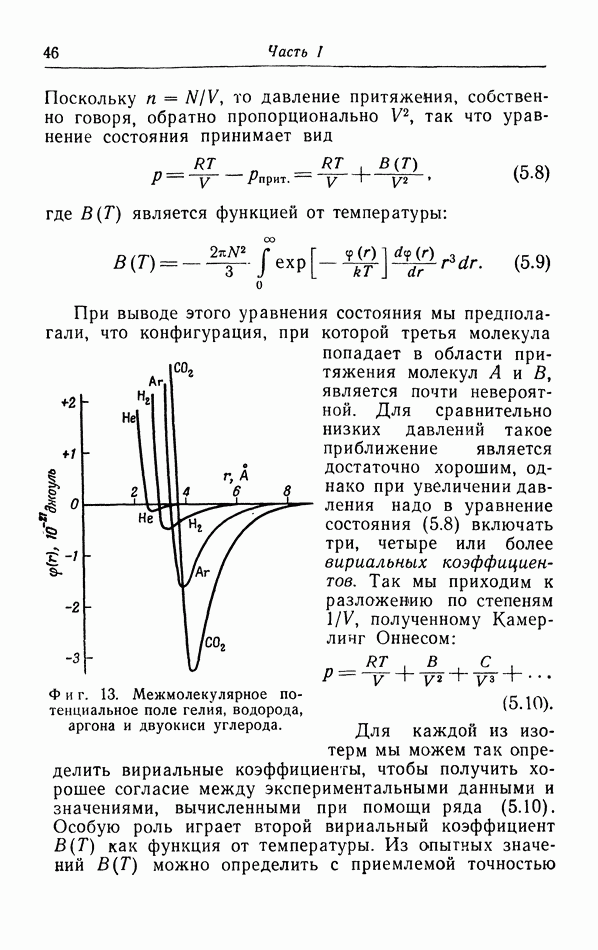
Как видно из фиг. 13, газы, которые могут быть ожижены при комнатной температуре и которые, таким образом, имеют сравнительно высокую критическую температуру, обладают глубокой потенциальной ямой в  это показывает, что силы притяжения особенно велики Наоборот, водород и гелий, обладающие чрезвычайно низкими критическими температурами (33,2 и 5,2° К), характеризуются гораздо меньшей энергией притяжения Таким образом, поведение газов и жидкостей сильно зависит от сил взаимодействия между молекулами.
это показывает, что силы притяжения особенно велики Наоборот, водород и гелий, обладающие чрезвычайно низкими критическими температурами (33,2 и 5,2° К), характеризуются гораздо меньшей энергией притяжения Таким образом, поведение газов и жидкостей сильно зависит от сил взаимодействия между молекулами.
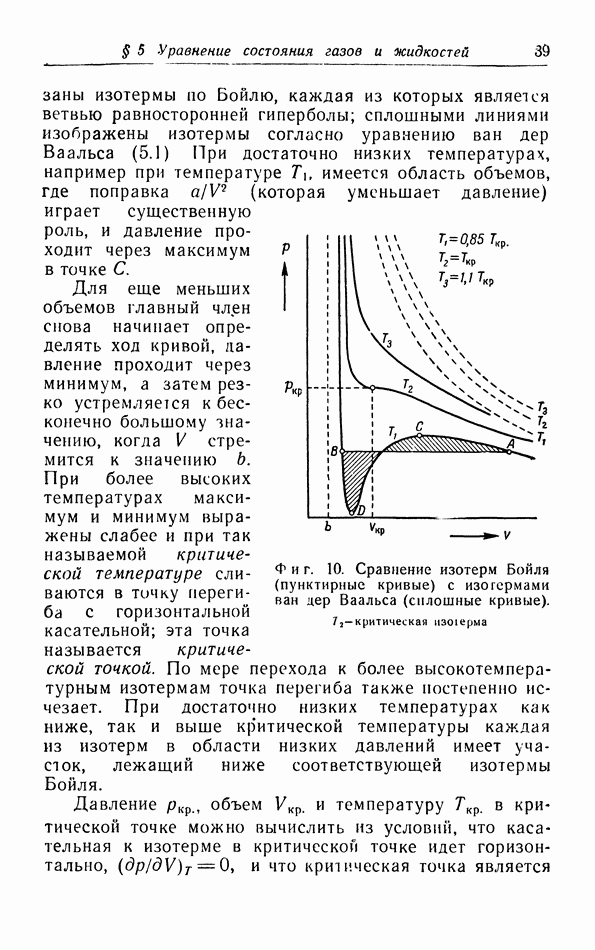
Если мы выразим давление, объем и температуру газа в единицах, более соответствующих его специфическим свойствам, то поведение различных газов окажется более схожим. Поэтому ван дер Ваальс выражал опытные значения давления, температуры и объема газа через соответствующие критические величины. Таким образом, параметры газа измерялись в единицах, которые являются характерными свойствами данного газа.
Изотермы для различных газов, вычерченные в функции от таких «приведенных» значений  действительно весьма похожи, а для газов, свойства которых различаются не слишком сильно, эти изотермы даже совпадают. При помощи этого закона соответственных состояний оказывается возможным вполне точно рассчитать неизвестные изотермы для различных газов, зная критические величины этих газов и имея измеренные изотермы для какого-то другого газа.
действительно весьма похожи, а для газов, свойства которых различаются не слишком сильно, эти изотермы даже совпадают. При помощи этого закона соответственных состояний оказывается возможным вполне точно рассчитать неизвестные изотермы для различных газов, зная критические величины этих газов и имея измеренные изотермы для какого-то другого газа.
Уравнение ван дер Ваальса можно также записать в форме закона соответственных состояний, если мы введем приведенные величины  и
и  определяемые формулами
определяемые формулами

Подстановка значений критических величин из (5.4) дает

Подставляя полученные значения в уравнение ван дер Ваальса и деля на постоянные  получаем уравнение
получаем уравнение

которое является уравнением ван дер Ваальса в приведенной форме.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Предисловие к русскому изданию
- ГЛАВА I. Газы и жидкости
- § 1. Молекулярная структура газов и жидкостей
- § 2. Кинетическая теория идеального газа
- б. Расчет давления в кинетической теории газов.
- в. Расчет удельной теплоемкости в кинетической теории газов.
- § 3. Распределение молекул по скорости их движения
- г. Средняя квадратичная и средняя скорости.
- д. Броуновское движение.
- е. Опыты с молекулярными пучками.
- § 4. Общее распределение молекул по энергиям
- б. Возбужденные состояния.
- в. вращательная и колебательная энергии.
- г. Потенциальная энергия тяготения.
- д. Потенциальная энергия межмолекулярных сил.
- § 5. Уравнение состояния газов и жидкостей
- б. Обсуждение уравнения ван дер Ваальса.
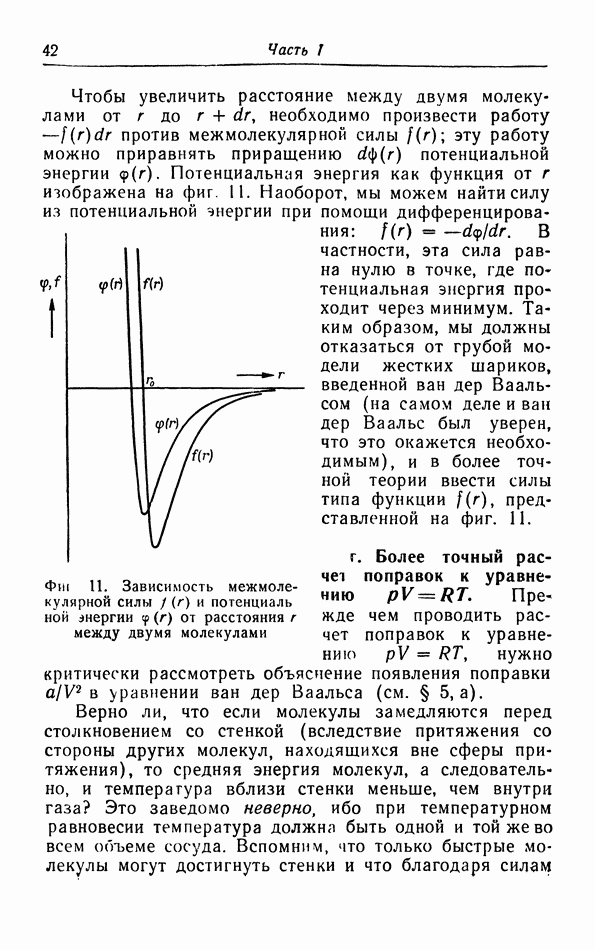
- в. Взаимодействие молекул.
- г. Более точный расчет поправок к уравнению pV=RT.
- д. Закон соответственных состояний.
- е. Жидкая фаза.
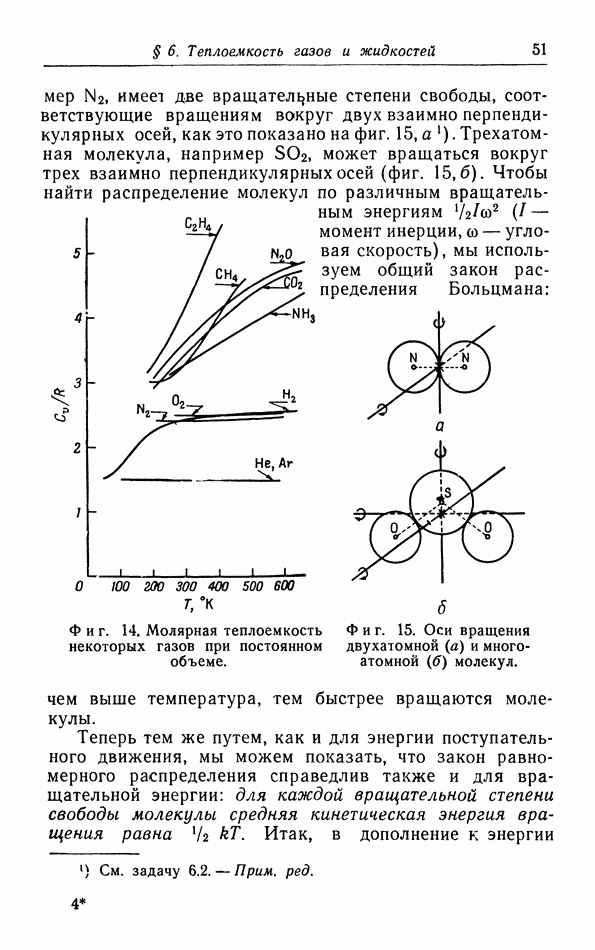
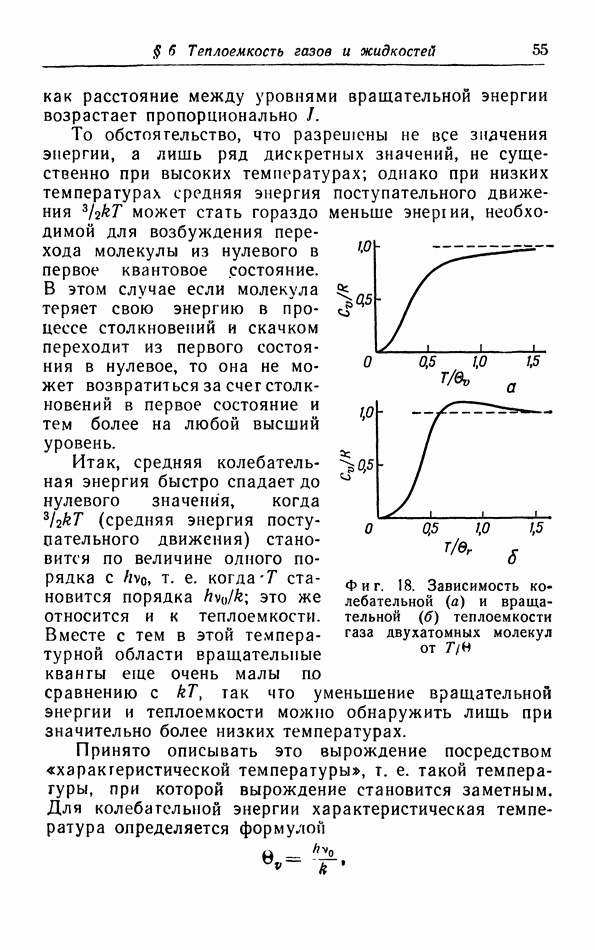
- § 6. Теплоемкость газов и жидкостей
- б. Классическая теория колебательной теплоемкости.
- в. Квантовая теория теплоемкости.
- г. Расчет колебательной теплоемкости двухатомной молекулы.
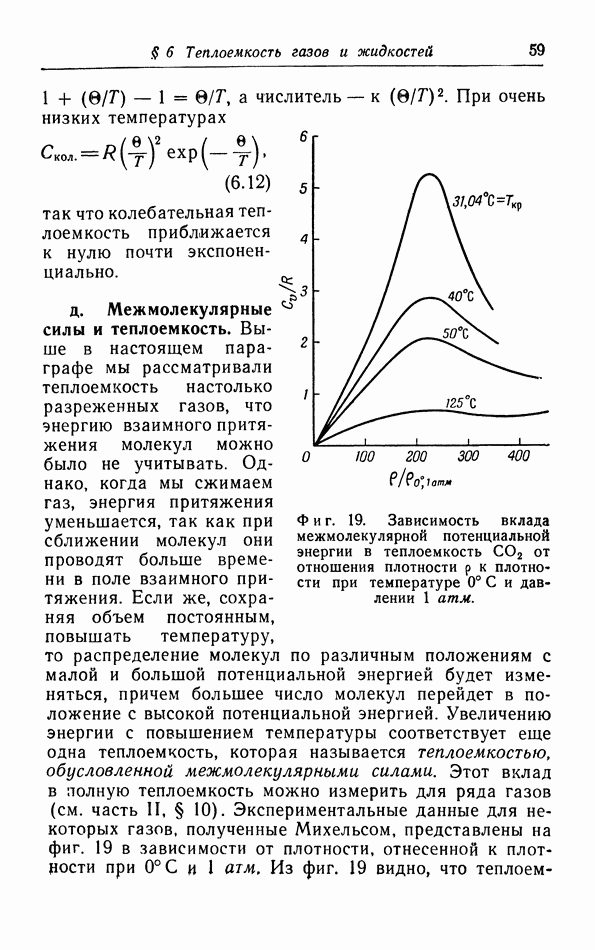
- д. Межмолекулярные силы и теплоемкость.
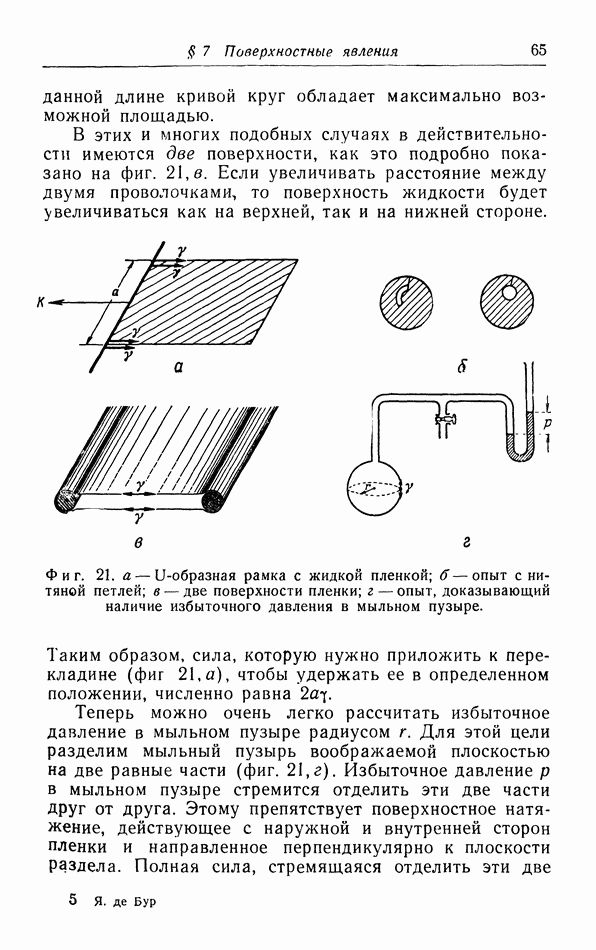
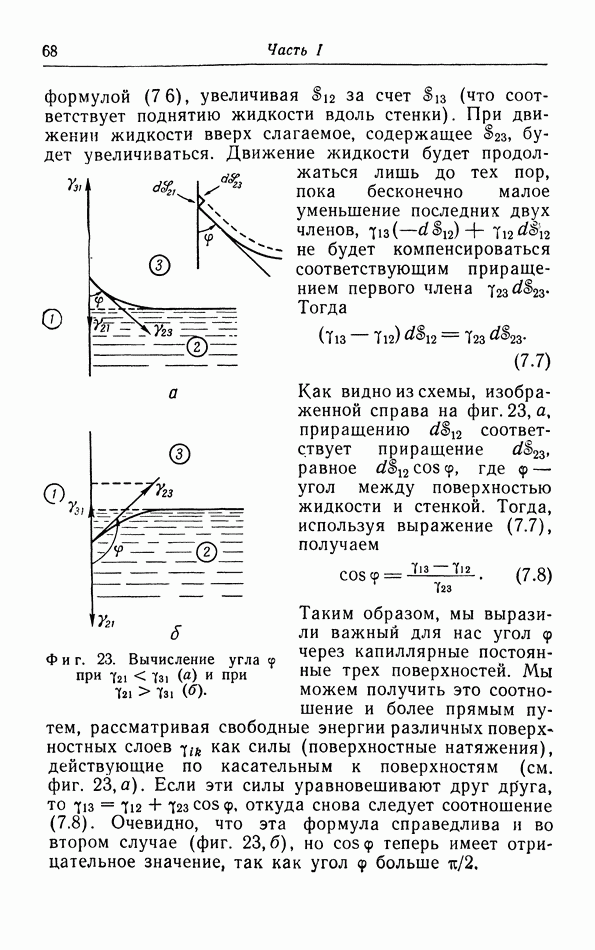
- § 7. Поверхностные явления
- б. Жидкие пленки.
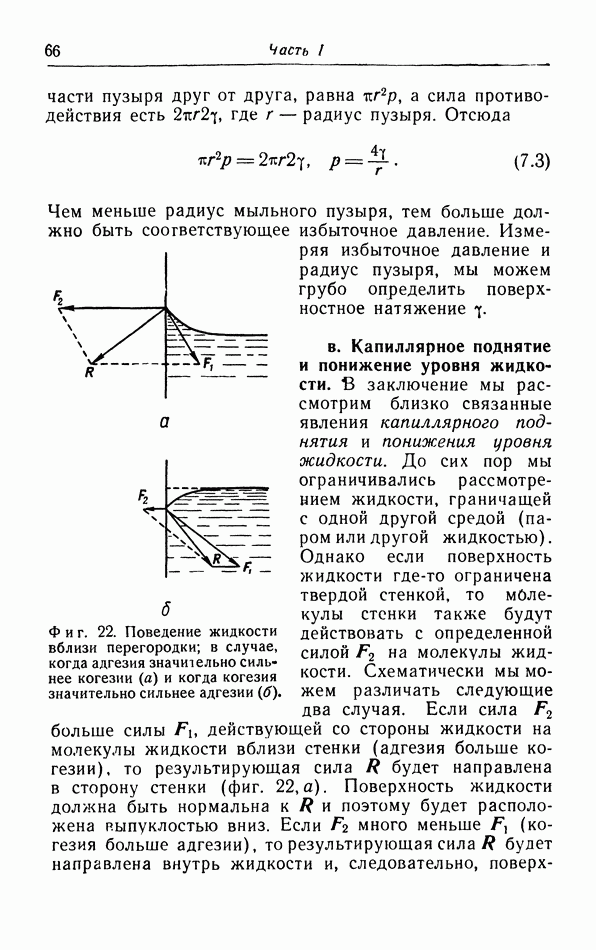
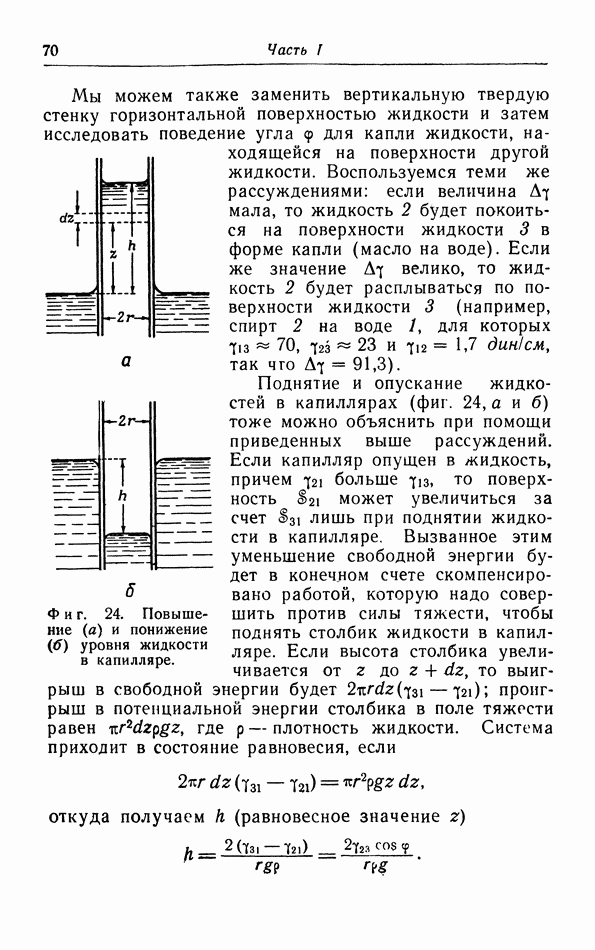
- в. Капиллярное поднятие и понижение уровня жидкости.
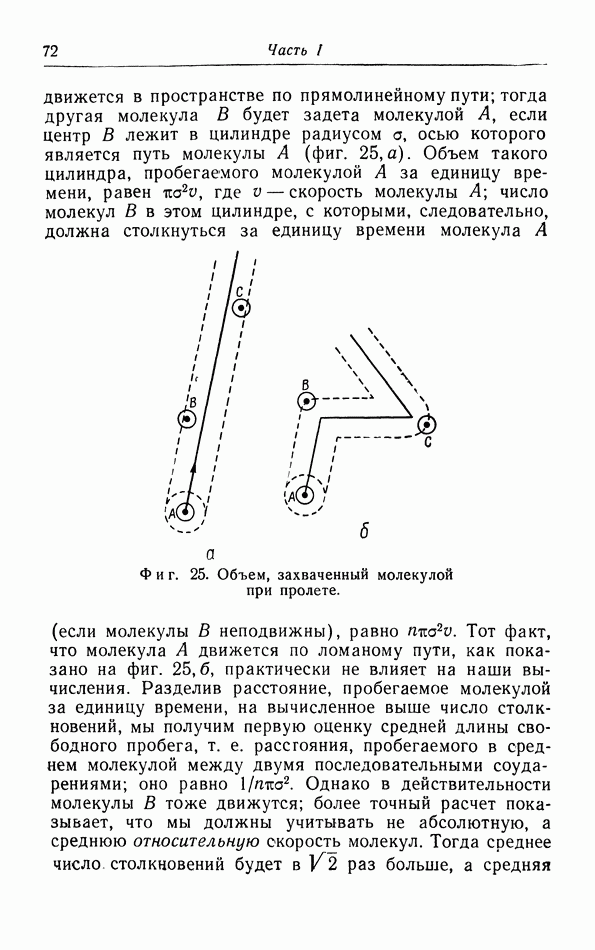
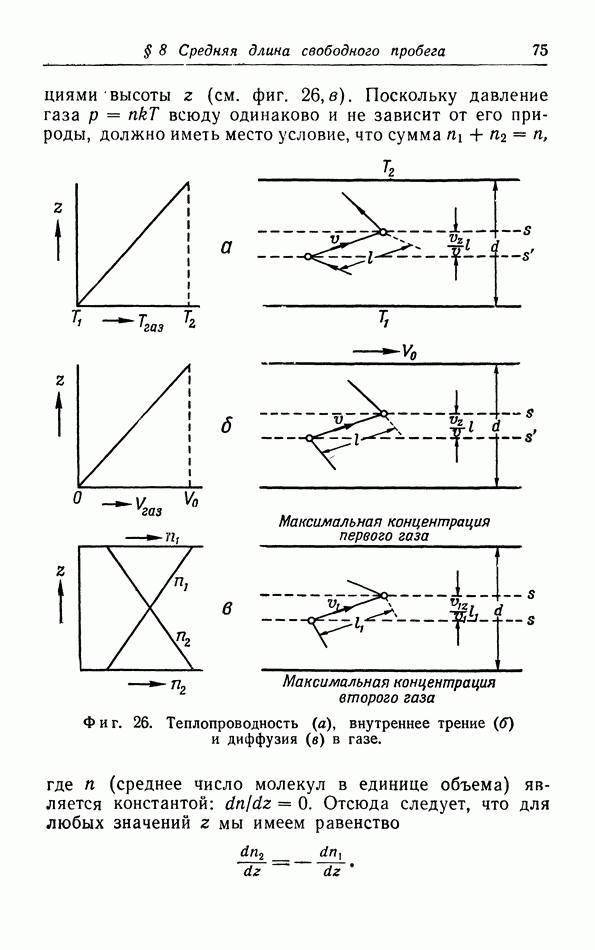
- § 8. Средняя длина свободного пробега, теплопроводность, вязкость и диффузия
- ГЛАВА II. Твердые тела
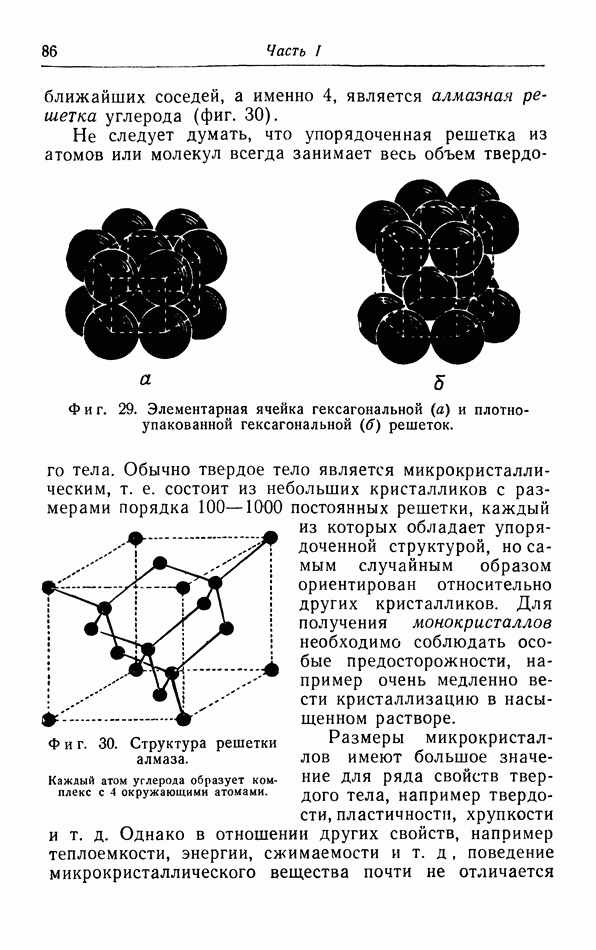
- § 9. Структура твердых тел
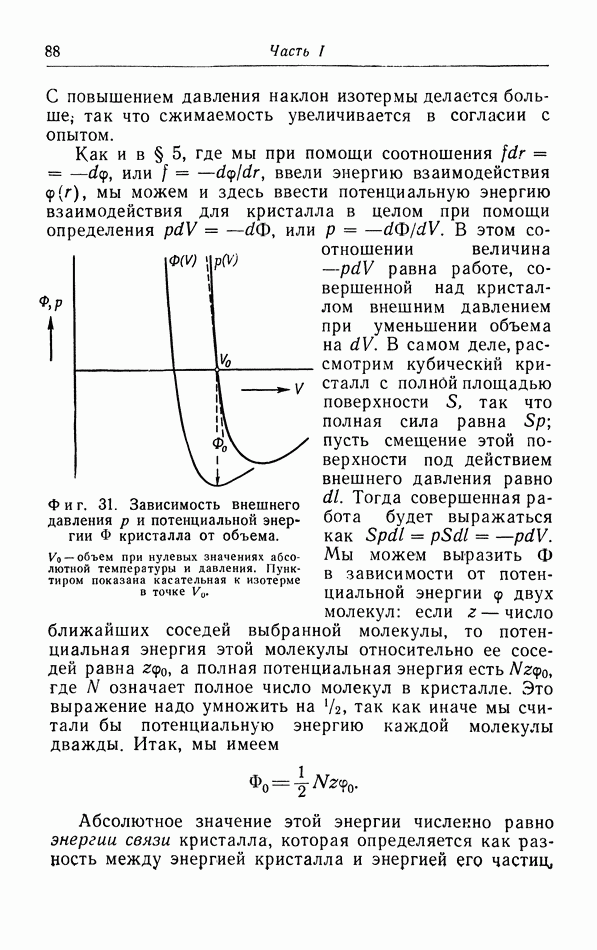
- § 10. Уравнение состояния твердых тел
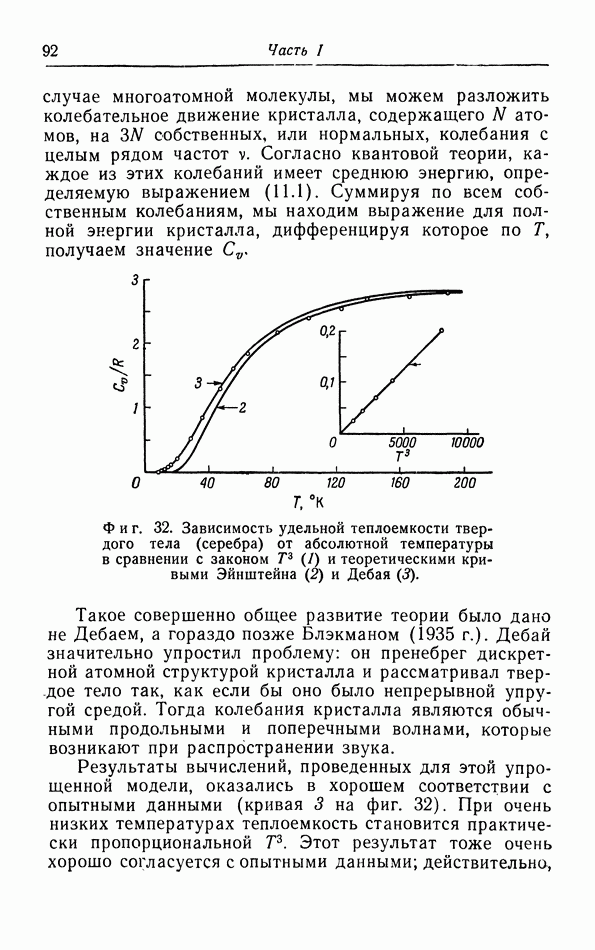
- § 11. Теплоемкость твердых тел
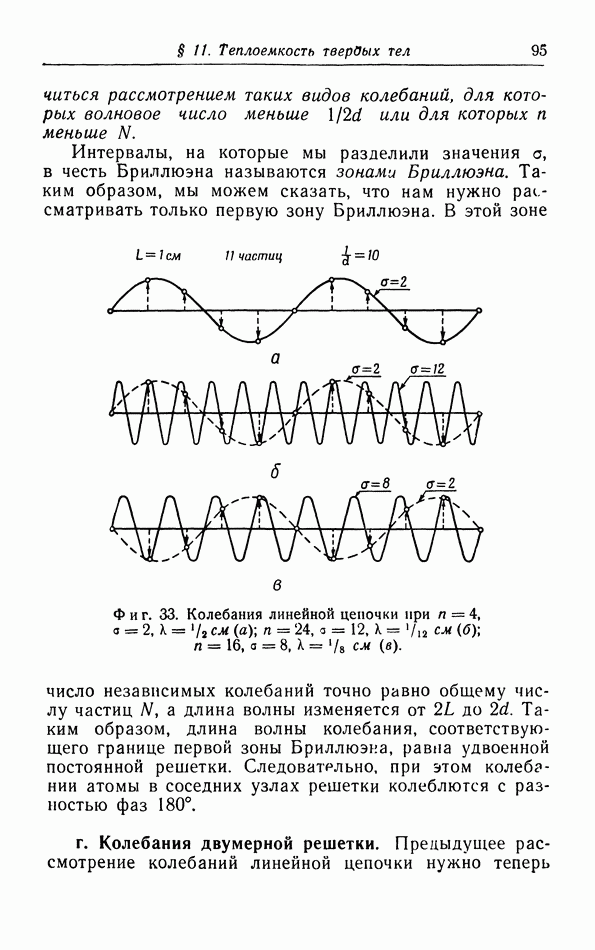
- в. Колебания линейной цепочки.
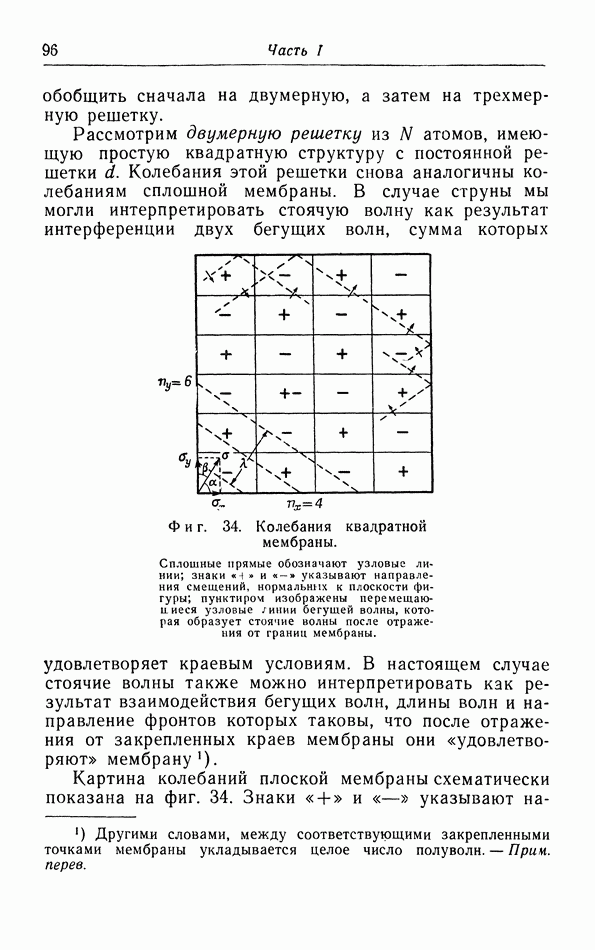
- г. Колебания двумерной решетки.
- д. Колебания трехмерной решетки.
- е. Теория Дебая.
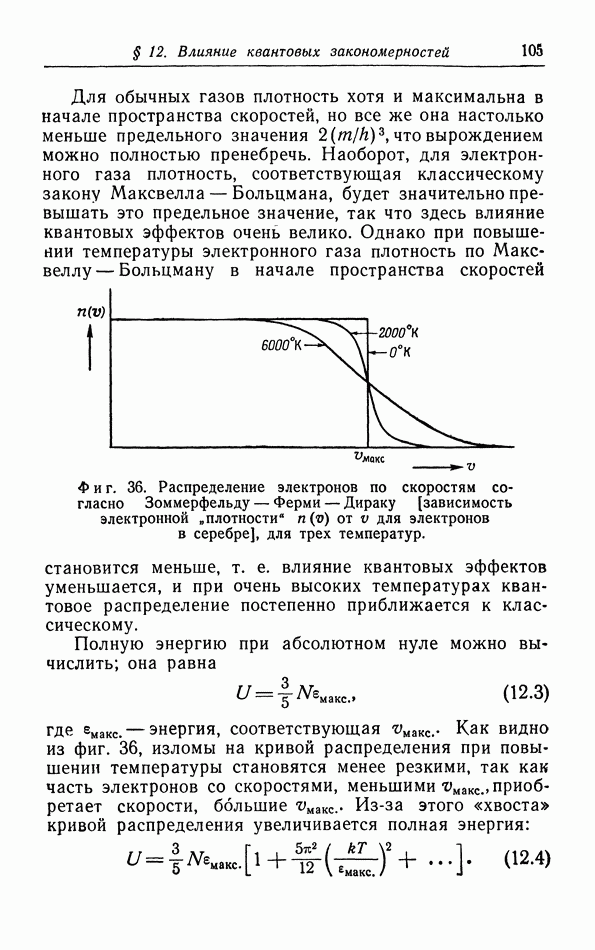
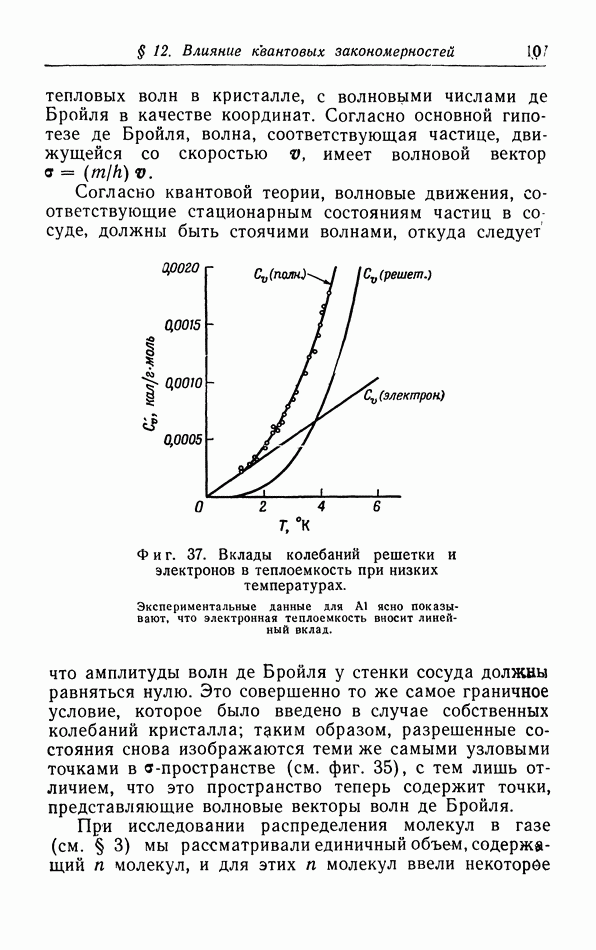
- § 12. Влияние квантовых закономерностей на распределение частиц по скоростям
- ГЛАВА III. Излучение
- § 13. Тепловое излучение и свет
- § 14. Испускание, поглощение и плотность излучения
- б. Яркость и излучательная способность.
- в. Плотность излучения.
- г. Закон Кирхгофа.
- § 15. Фотонная гипотеза. Давление излучения
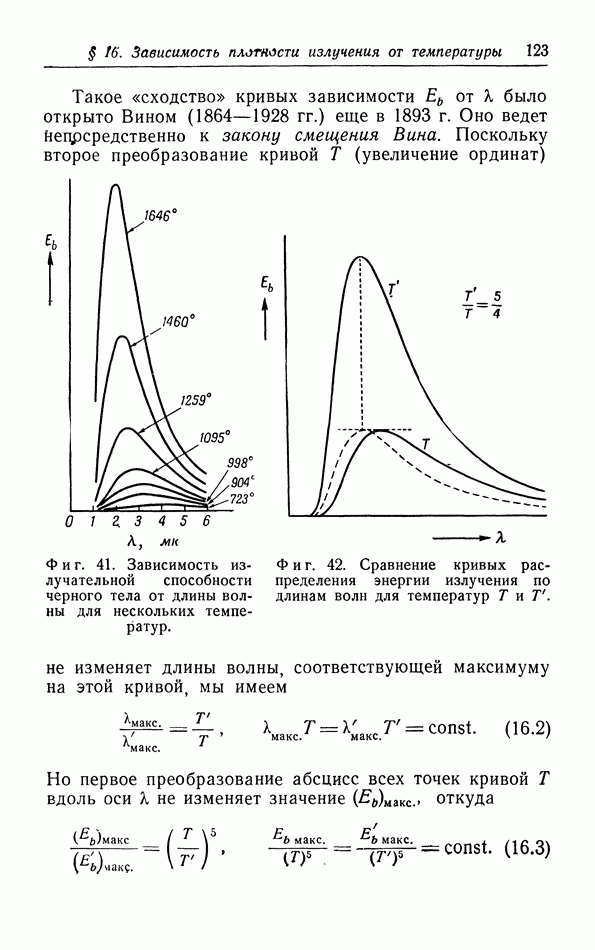
- § 16. Зависимость плотности излучения от температуры и длины волны
- б. Закон смещения Вина.
- в. Закон излучения Релея — Джинса.
- г. Закон излучения Планка.
- ГЛАВА I. Первый закон термодинамики
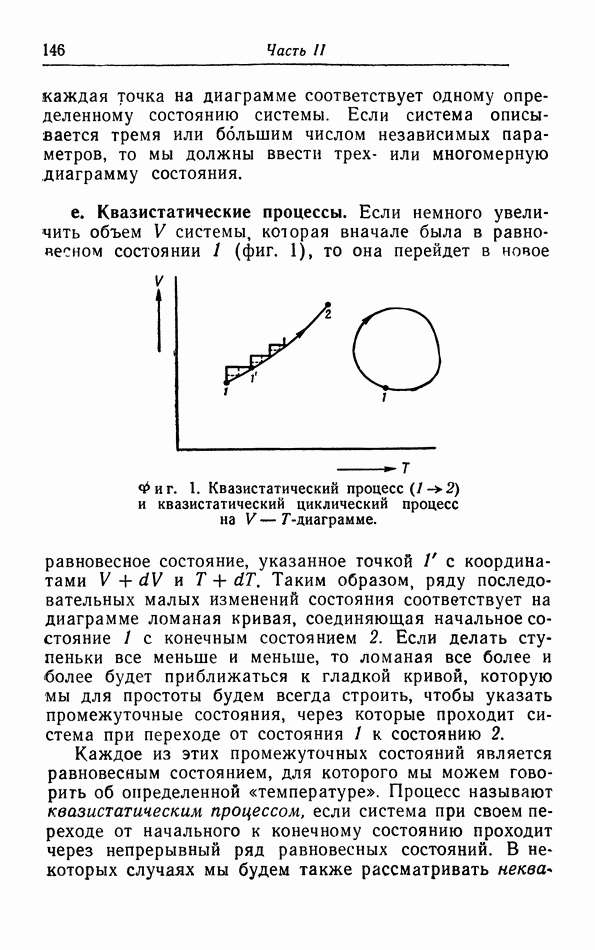
- § 1. Термодинамическое состояние и его изменения
- § 2. Работа при квазистатических процессах
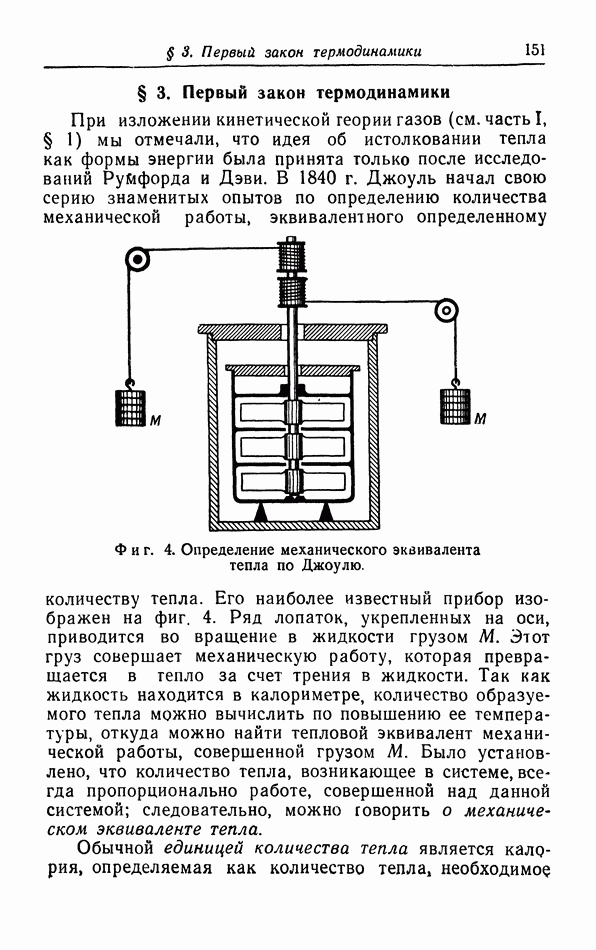
- § 3. Первый закон термодинамики
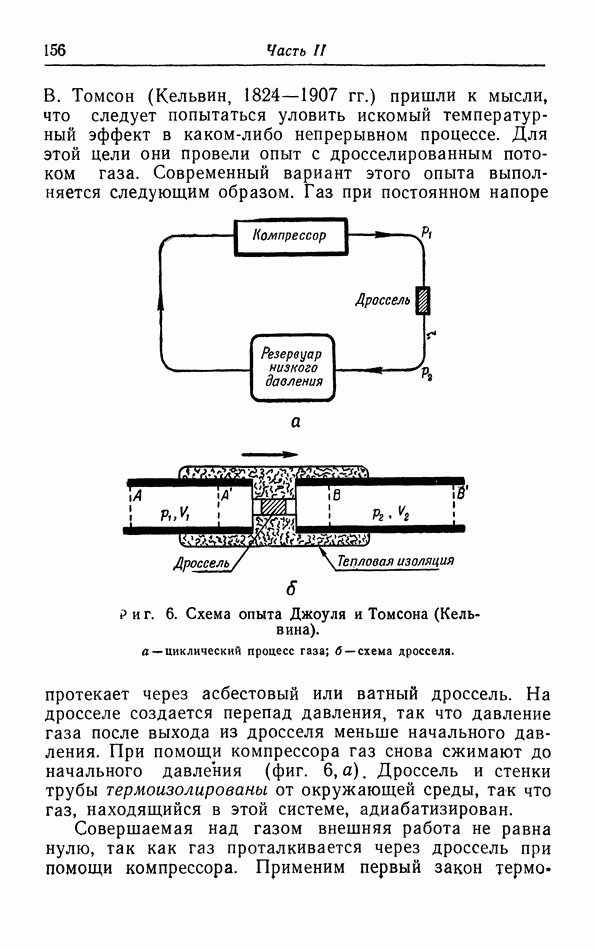
- § 4. Опыты Джоуля и Томсона
- § 5. Дальнейшие приложения первого закона
- б. Теплоемкость.
- в. Работа при адиабатических процессах.
- ГЛАВА II. Второй закон термодинамики
- § 6. Работа и теплота в циклических процессах
- § 7. Второе начало термодинамики и его различные формулировки
- § 8. Температура
- § 9. Энтропия и второй закон термодинамики
- § 10. Применения второго закона термодинамики
- в. Изэнтропические изменения состояния.
- г. Изэнтропические холодильные процессы (процесс Ж. Клода).
- д. Иззнтропические холодильные процессы (адиабатическое размагничивание).
- е. Коэффициент полезного действия технических циклических процессов.
- ГЛАВА III. Характеристические функции
- § 11. Энергия и энтальпия
- б. Расчет процессов Джоуля и Джоуля — Томсона (Кельвина).
- в. Зависимость внутренней энергии от объема.
- г. Вывод закона Стефана — Больцмана.
- д. Характеристические функции U и H.
- § 12. Свободная энергия
- б. Свободная энергия и поверхностное натяжение.
- в. Свободная энергия и гальванические элементы.
- § 13. Свободная энтальпия и термодинамический потенциал
- б. Термодинамический потенциал.
- в. Системы с более чем одним компонентом.
- § 14. Соотношения Максвелла
- ГЛАВА IV. Неквазистатические процессы. Равновесие
- § 15. Неквазистатические процессы
- б. Подвод тепла и изменение энтропии.
- в. Увеличение энтропии в адиабатических системах.
- г. Неквазистатический изотермический процесс.
- § 16. Условия равновесия
- б. Первое условие равновесия.
- в. Второе условие равновесия.
- г. Третье условие равновесия.
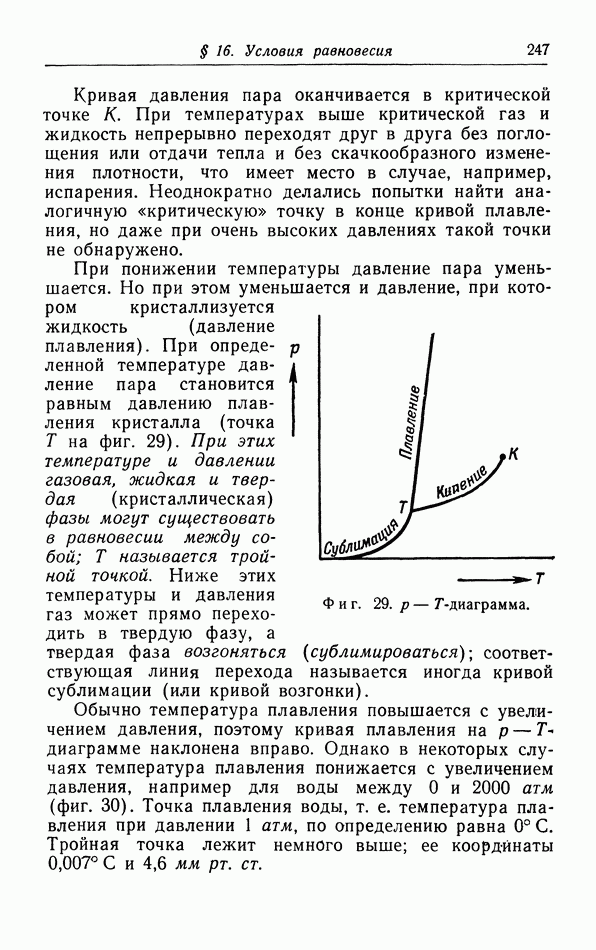
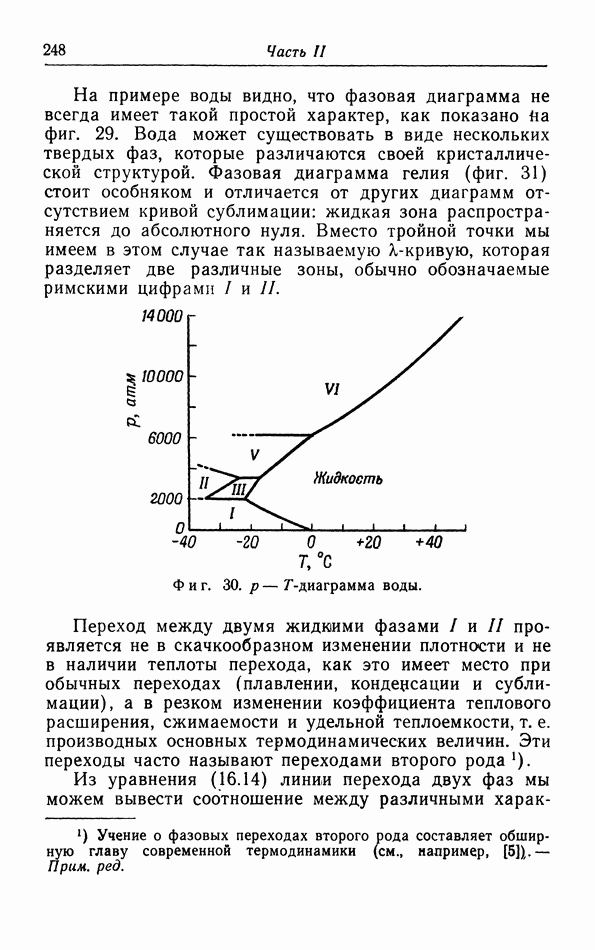
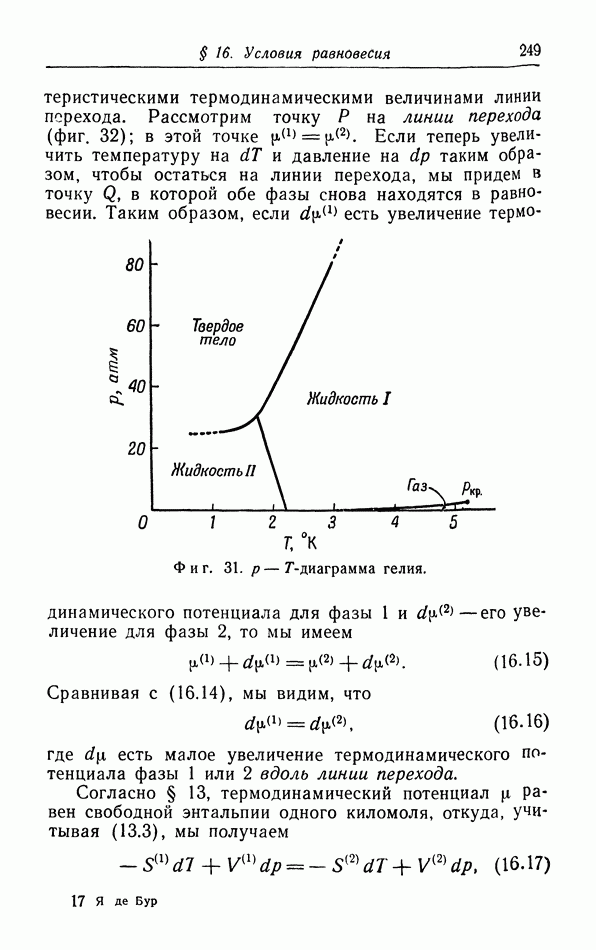
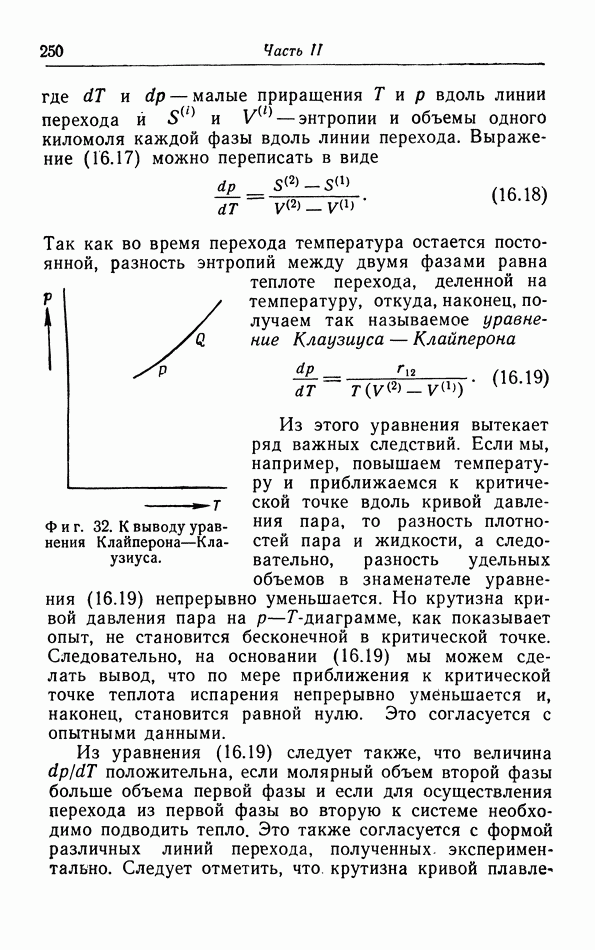
- д. p-T-диаграмма.
- е. Равновесие фаз в случае более чем одного компонента. Правило фаз.
- ГЛАВА V. Теорема Нернста
- § 17. Теорема Нернста
- § 18. Применение теоремы Нернста к фазовым переходам