| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
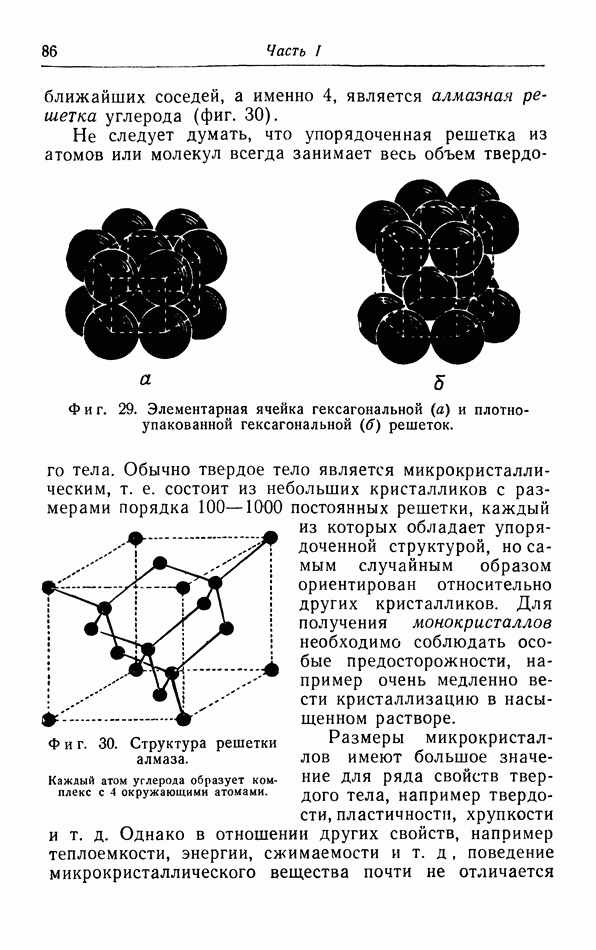
б. Расчет процессов Джоуля и Джоуля — Томсона (Кельвина).
В опыте Джоуля энергия идеального газа сохраняется постоянной,  Тогда из выражения (11.3) получаем
Тогда из выражения (11.3) получаем

Таким образом, увеличение объема газа обязательно сопровождается ростом энтропии. Это может показаться парадоксальным, ибо, поскольку во время опыта Джоуля тепло не подводится, из соотношения  можно было бы сделать ошибочный вывод, что энтропия газа должна оставаться постоянной. Но этот опыт в действительности является неквазистатическим процессом, так что, вопреки равенству
можно было бы сделать ошибочный вывод, что энтропия газа должна оставаться постоянной. Но этот опыт в действительности является неквазистатическим процессом, так что, вопреки равенству  энтропия газа может возрастать и
энтропия газа может возрастать и 
Перейдем к расчету в обпхем виде случая адиабатического расширения произвольного газа в пустоту без совершения внешней работы. Чтобы определить изменение температуры, выразим приращение энтропии обычным образом через приращение температуры и объема;
эти величины связаны между собой вторым законом термодинамики

Подстановка в (11.7) дает

или

Интегрируя это выражение от начального до конечного объема, получаем

Этот интеграл можно вычислить лишь в том случае, когда известно уравнение состояния. Если справедливо уравнение  то
то

откуда  как мы указывали в § 4. Если справедливо уравнение ван дер Ваальса, то
как мы указывали в § 4. Если справедливо уравнение ван дер Ваальса, то

откуда, предполагая теплоемкость  постоянной, получаем
постоянной, получаем

Итак, мы видим, что при наличии сил межмолекулярного притяжения увеличение объема должно вызывать понижение температуры. Однако подстановка экспериментальных данных показывает, что понижение температуры в опыте Джоуля имело слишком малую величину и не могло бцть обнаружено вследствие
сравнительно большой теплоемкости применявшегося калори метра.
Аналогичным образом можно рассчитать изменение температуры в опыте Джоуля — Томсона. Согласно § 4, энтальпия  во время этого процесса остается постоянной, так что выражение (11.4) принимает вид
во время этого процесса остается постоянной, так что выражение (11.4) принимает вид

Подставляя выражение для  в функции от
в функции от 

которое мы вывели в § 10, получаем

или

Интегрируя это соотношение от начального давления до более низкого конечного давления  находим
находим

Вместо этого выражения, описывающего «интегральный» эффект Джоуля — Томсона, часто используют величину, характеризующую «дифференциальный» эффект Джоуля-Томсона, так называемый коэффициент Джоуля — Томсона:

Этот коэффициент зависит от температуры и давления и является мерой величины изменения температуры, соответствующего очень малому изменению давления при определенных значениях  и
и  Когда коэффициент
Когда коэффициент  положителен, что имеет место в большинстве случаев, расширение вызывает понижение температуры. Если температура опыта повышается, то коэффициент Джоуля — Томсона уменьшается. При дросселировании азота
положителен, что имеет место в большинстве случаев, расширение вызывает понижение температуры. Если температура опыта повышается, то коэффициент Джоуля — Томсона уменьшается. При дросселировании азота
от 200 до 5 атм уменьшение температуры составляет 11,9° при —100° С и только 5,2° при +200° С.
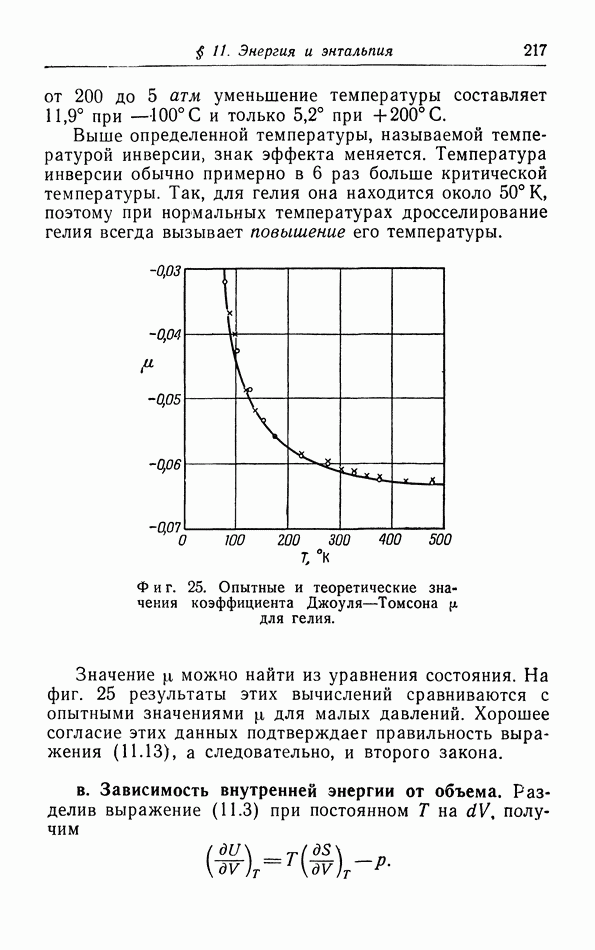
Выше определенной температуры, называемой температурой инверсии, знак эффекта меняется. Температура инверсии обычно примерно в 6 раз больше критической температуры. Так, для гелия она находится около 50° К, поэтому при нормальных температурах дросселирование гелия всегда вызывает повышение его температуры.

Фиг. 25. Опытные и теоретические значения коэффициента Джоуля-Томсона  для гелия.
для гелия.
Значение можно найти из уравнения состояния. На фиг. 25 результаты этих вычислений сравниваются с опытными значениями для малых давлений. Хорошее согласие этих данных подтверждает правильность выражения (11.13), а следовательно, и второго закона.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие к русскому изданию
- ГЛАВА I. Газы и жидкости
- § 1. Молекулярная структура газов и жидкостей
- § 2. Кинетическая теория идеального газа
- б. Расчет давления в кинетической теории газов.
- в. Расчет удельной теплоемкости в кинетической теории газов.
- § 3. Распределение молекул по скорости их движения
- г. Средняя квадратичная и средняя скорости.
- д. Броуновское движение.
- е. Опыты с молекулярными пучками.
- § 4. Общее распределение молекул по энергиям
- б. Возбужденные состояния.
- в. вращательная и колебательная энергии.
- г. Потенциальная энергия тяготения.
- д. Потенциальная энергия межмолекулярных сил.
- § 5. Уравнение состояния газов и жидкостей
- б. Обсуждение уравнения ван дер Ваальса.
- в. Взаимодействие молекул.
- г. Более точный расчет поправок к уравнению pV=RT.
- д. Закон соответственных состояний.
- е. Жидкая фаза.
- § 6. Теплоемкость газов и жидкостей
- б. Классическая теория колебательной теплоемкости.
- в. Квантовая теория теплоемкости.
- г. Расчет колебательной теплоемкости двухатомной молекулы.
- д. Межмолекулярные силы и теплоемкость.
- § 7. Поверхностные явления
- б. Жидкие пленки.
- в. Капиллярное поднятие и понижение уровня жидкости.
- § 8. Средняя длина свободного пробега, теплопроводность, вязкость и диффузия
- ГЛАВА II. Твердые тела
- § 9. Структура твердых тел
- § 10. Уравнение состояния твердых тел
- § 11. Теплоемкость твердых тел
- в. Колебания линейной цепочки.
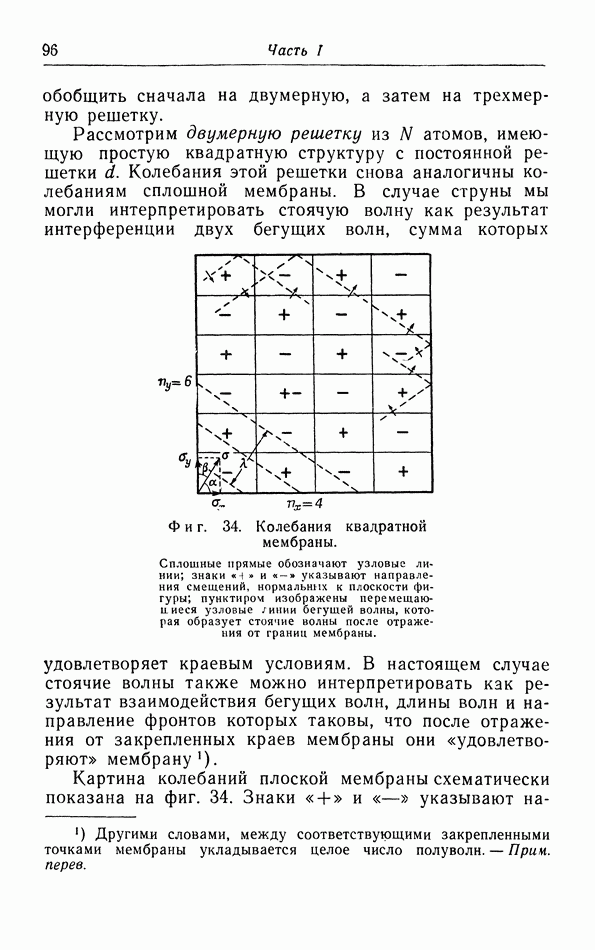
- г. Колебания двумерной решетки.
- д. Колебания трехмерной решетки.
- е. Теория Дебая.
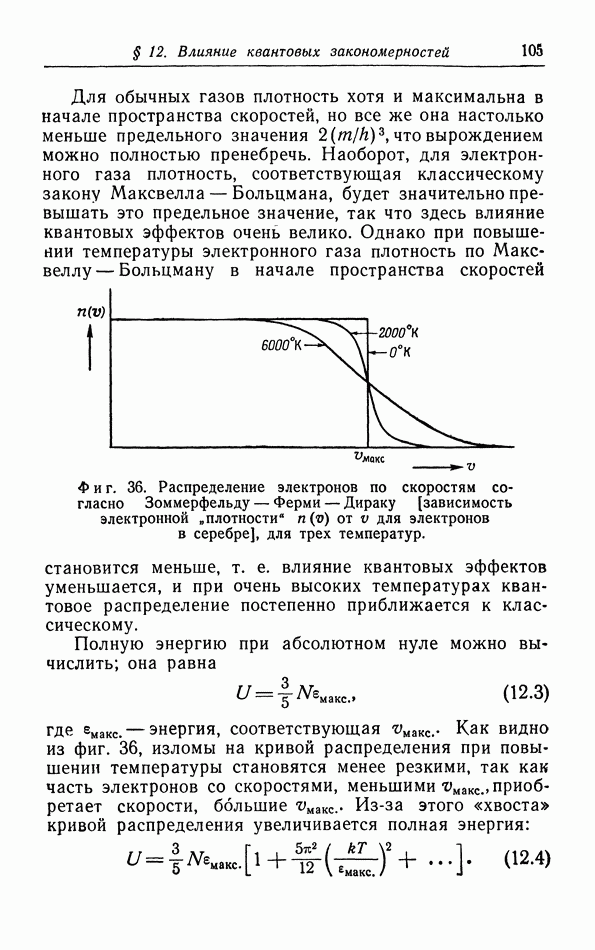
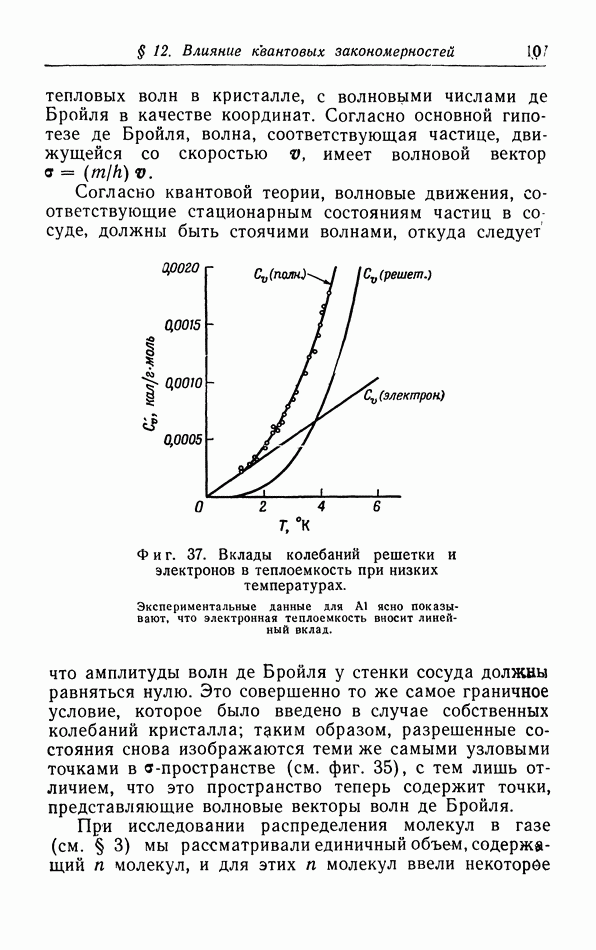
- § 12. Влияние квантовых закономерностей на распределение частиц по скоростям
- ГЛАВА III. Излучение
- § 13. Тепловое излучение и свет
- § 14. Испускание, поглощение и плотность излучения
- б. Яркость и излучательная способность.
- в. Плотность излучения.
- г. Закон Кирхгофа.
- § 15. Фотонная гипотеза. Давление излучения
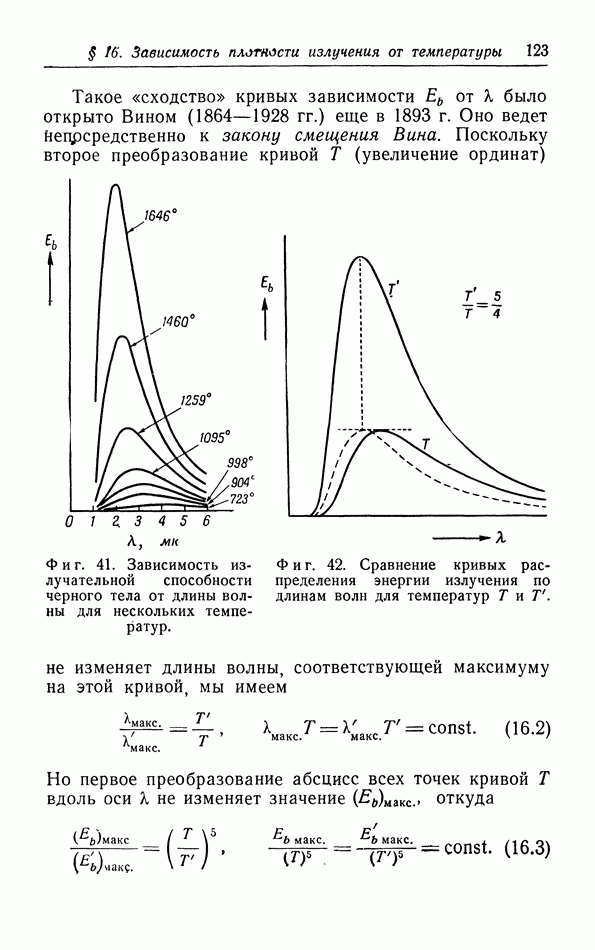
- § 16. Зависимость плотности излучения от температуры и длины волны
- б. Закон смещения Вина.
- в. Закон излучения Релея — Джинса.
- г. Закон излучения Планка.
- ГЛАВА I. Первый закон термодинамики
- § 1. Термодинамическое состояние и его изменения
- § 2. Работа при квазистатических процессах
- § 3. Первый закон термодинамики
- § 4. Опыты Джоуля и Томсона
- § 5. Дальнейшие приложения первого закона
- б. Теплоемкость.
- в. Работа при адиабатических процессах.
- ГЛАВА II. Второй закон термодинамики
- § 6. Работа и теплота в циклических процессах
- § 7. Второе начало термодинамики и его различные формулировки
- § 8. Температура
- § 9. Энтропия и второй закон термодинамики
- § 10. Применения второго закона термодинамики
- в. Изэнтропические изменения состояния.
- г. Изэнтропические холодильные процессы (процесс Ж. Клода).
- д. Иззнтропические холодильные процессы (адиабатическое размагничивание).
- е. Коэффициент полезного действия технических циклических процессов.
- ГЛАВА III. Характеристические функции
- § 11. Энергия и энтальпия
- б. Расчет процессов Джоуля и Джоуля — Томсона (Кельвина).
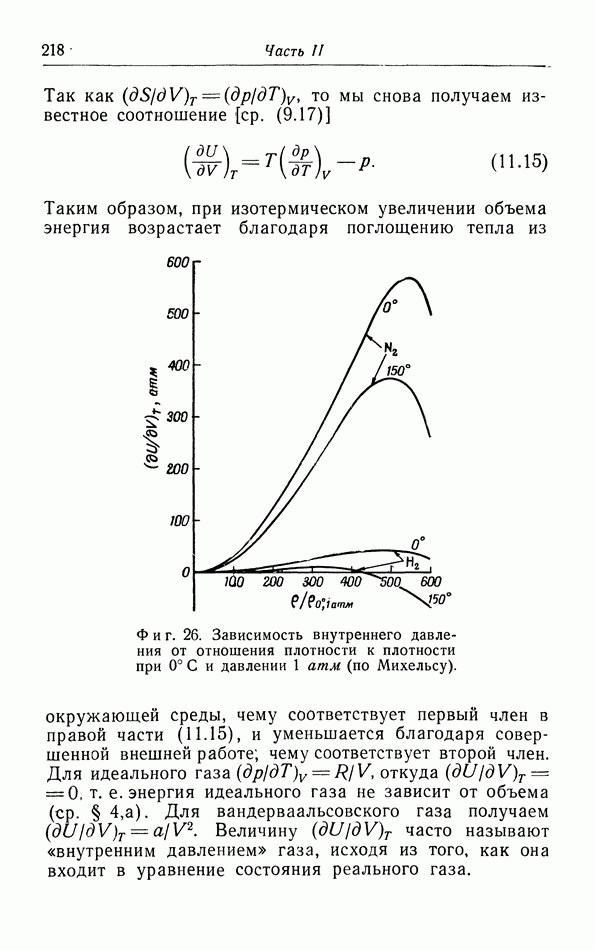
- в. Зависимость внутренней энергии от объема.
- г. Вывод закона Стефана — Больцмана.
- д. Характеристические функции U и H.
- § 12. Свободная энергия
- б. Свободная энергия и поверхностное натяжение.
- в. Свободная энергия и гальванические элементы.
- § 13. Свободная энтальпия и термодинамический потенциал
- б. Термодинамический потенциал.
- в. Системы с более чем одним компонентом.
- § 14. Соотношения Максвелла
- ГЛАВА IV. Неквазистатические процессы. Равновесие
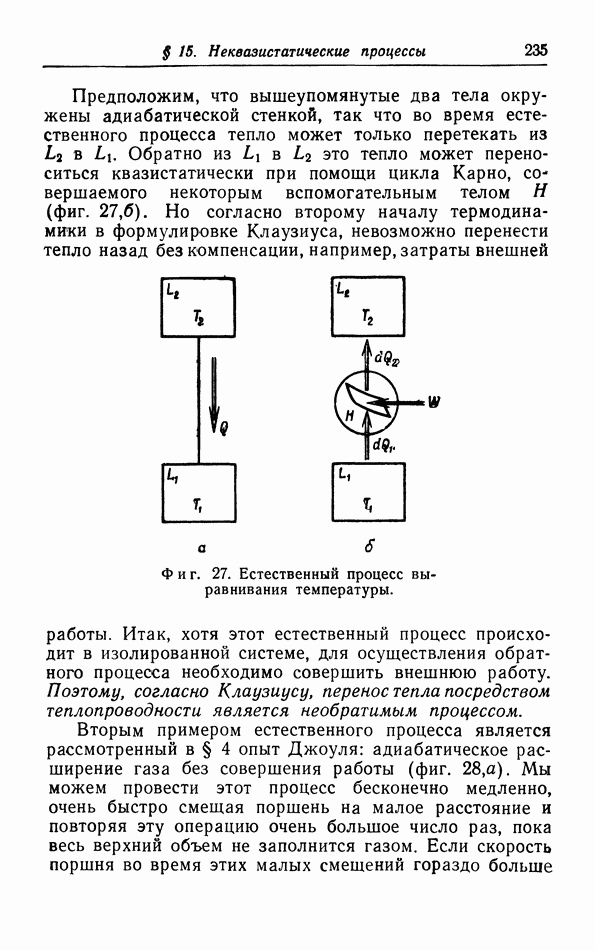
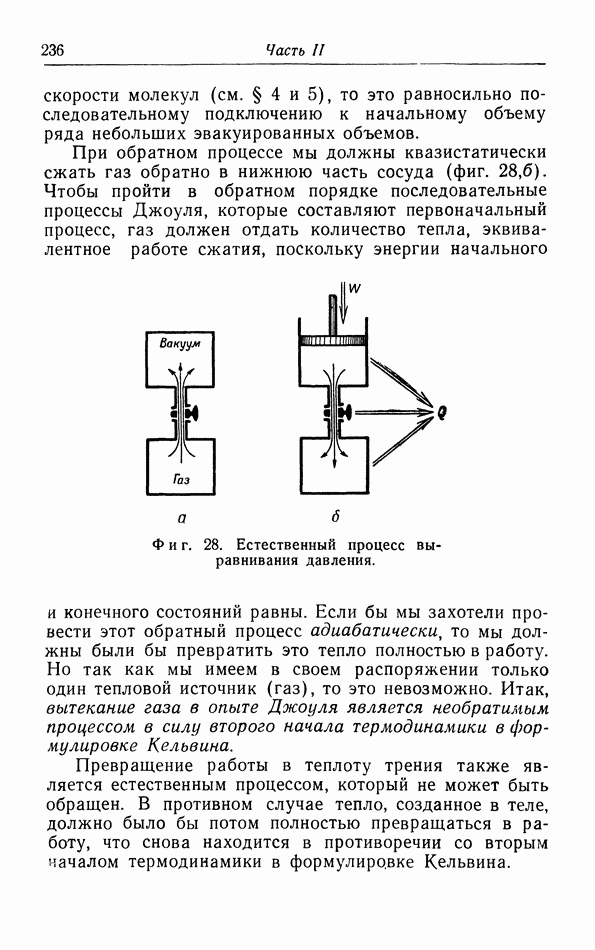
- § 15. Неквазистатические процессы
- б. Подвод тепла и изменение энтропии.
- в. Увеличение энтропии в адиабатических системах.
- г. Неквазистатический изотермический процесс.
- § 16. Условия равновесия
- б. Первое условие равновесия.
- в. Второе условие равновесия.
- г. Третье условие равновесия.
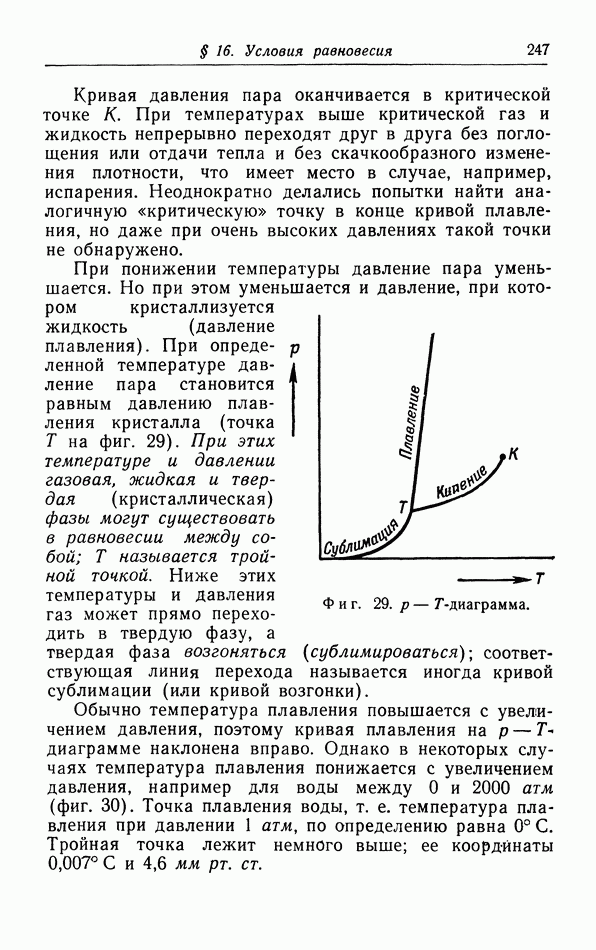
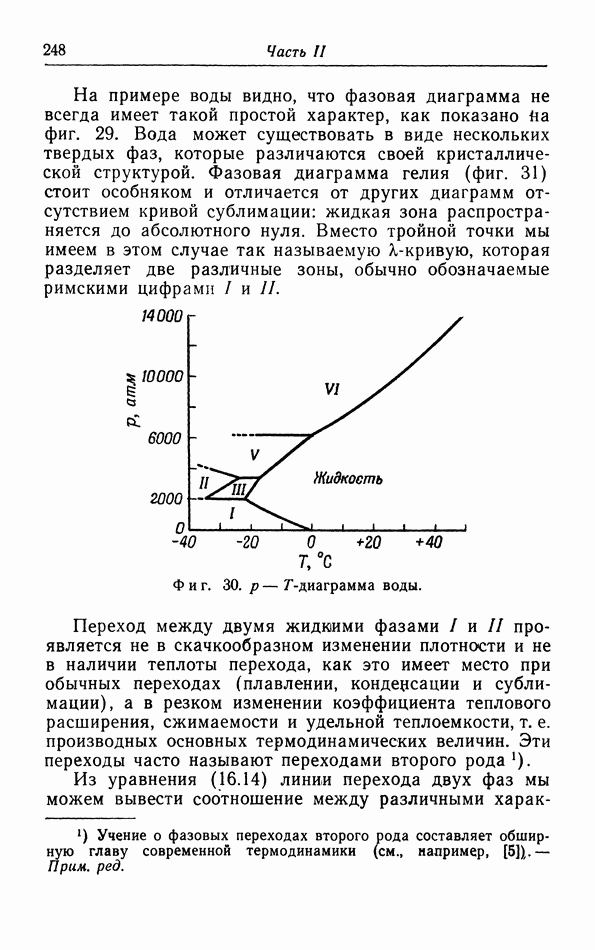
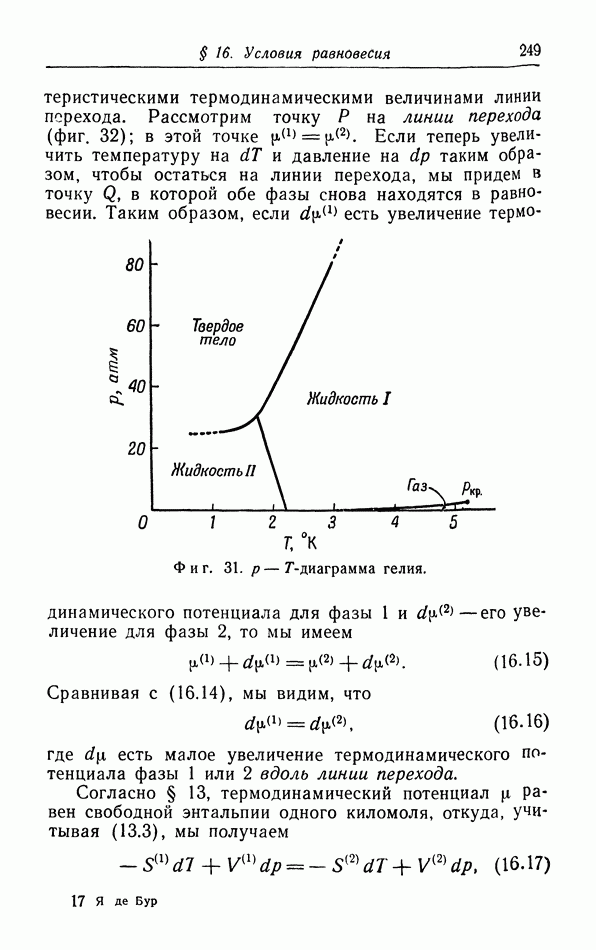
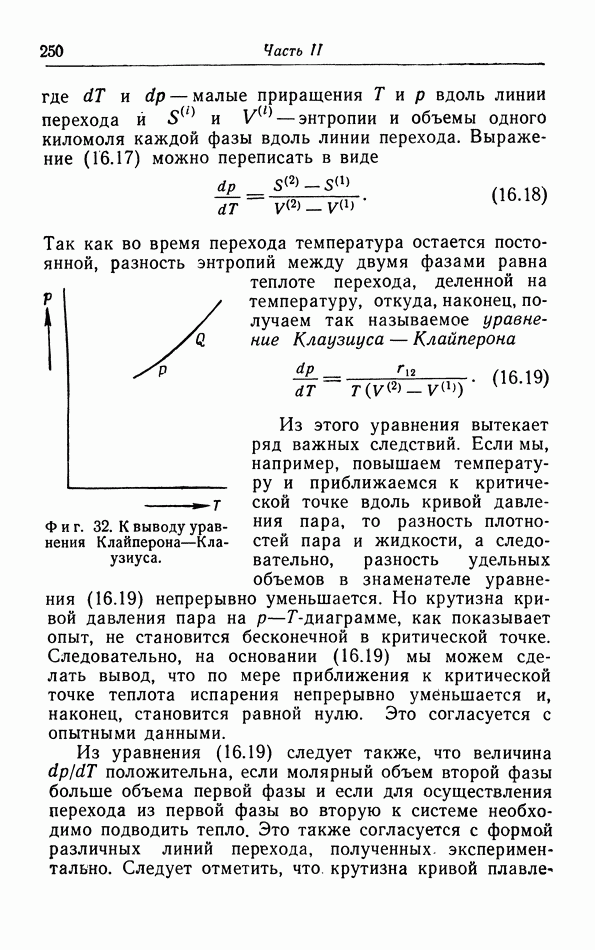
- д. p-T-диаграмма.
- е. Равновесие фаз в случае более чем одного компонента. Правило фаз.
- ГЛАВА V. Теорема Нернста
- § 17. Теорема Нернста
- § 18. Применение теоремы Нернста к фазовым переходам