| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
е. Равновесие фаз в случае более чем одного компонента. Правило фаз.
Когда две фазы, каждая из которых состоит из нескольких компонентов, находятся в равновесии между собой, мы можем найти условие равновесия, переведя небольшое количество компонента  из второй фазы в первук) при постоянных Тир, точно таким же образом, как мы это делали в случае единственного вещества. Изменение свободной энтальпии первой фазы будет тогда для второй фазы аналогично оно равно где
из второй фазы в первук) при постоянных Тир, точно таким же образом, как мы это делали в случае единственного вещества. Изменение свободной энтальпии первой фазы будет тогда для второй фазы аналогично оно равно где  есть число киломолей компонента перенесенных из второй фазы в первую. Отсюда
есть число киломолей компонента перенесенных из второй фазы в первую. Отсюда

так что в равновесии каждый компонент  удовлетворяет условию
удовлетворяет условию

В состоянии равновесия системы, в которой возможен перенос вещества между различными фазами, термодинамические потенциалы каждого из компонентов должны быть равны во всех фазах.
Когда система состоит из  различных фаз, мы получаем
различных фаз, мы получаем  уравнений
уравнений

для каждого компонента и Выражение  является уравнением, связывающим
является уравнением, связывающим  и концентрации в двух соответствующих фазах
и концентрации в двух соответствующих фазах  Если имеется с компонентов, то полное число соотношений между параметрами
Если имеется с компонентов, то полное число соотношений между параметрами  и концентрациями [Уавно
и концентрациями [Уавно  Полное число параметров, необходимых для однозначного
Полное число параметров, необходимых для однозначного
определения состояния, равно  этими параметрами являются
этими параметрами являются  концентраций
концентраций  в каждой из
в каждой из  фаз а.
фаз а.
Между этими  параметрами имеется
параметрами имеется  соотношений, откуда следует, что только
соотношений, откуда следует, что только

параметров являются независимыми переменными. Эта величина называется числом степеней свободы системы. Итак, мы получаем правило
Число степеней свободы 
Это правило фаз Гиббса: число степеней свободы системы равно числу компонентов плюс два минус число фаз.
Система с одним компонентом и одной фазой является бивариантной, т. е. имеет две степени свободы: давление и температура могут меняться произвольным образом. При наличии равновесия между двумя фазами система является моновариантной, т. е. имеет только одну степень свободы: если температура задана, то давление должно иметь определенное значение. Когда три фазы находятся в равновесии, система является инвариантной, т. е. какие-либо изменения невозможны; температура и давление фиксированы (тройная точка системы).
Если система содержит два компонента, то двухфазное равновесие является бивариантным. Иначе говоря, в двухфазном равновесии два из четырех параметров  и могут еще выбираться произвольно. Примером является раствор соли в воде. Если мы выбираем температуру и концентрацию соли в воде в качестве независимых параметров, то давление и концентрация в парах будут фиксированными: система бивариантна.
и могут еще выбираться произвольно. Примером является раствор соли в воде. Если мы выбираем температуру и концентрацию соли в воде в качестве независимых параметров, то давление и концентрация в парах будут фиксированными: система бивариантна.
Понижая температуру либо увеличивая концентрацию соли в растворе, можно достичь состояния, в котором соль начнет кристаллизоваться. В этом случае мы имеем три фазы в равновесии между собой: твердую соль, насыщенный раствор и пар. Система стала моновариантной, ибо концентрация в насыщенном растворе
и паре, а также давление пара определяются одним параметром — температурой. Если теперь понижать температуру, то при определенном ее значении образуется лед с очень малым содержанием соли. Тогда мы имеем в равновесии четыре фазы: твердую соль, лед, раствор и пар, и система станет инвариантной. Такая точка называется эвтектической. Она аналогична тройной точке системы с одним компонентом, где три фазы находятся в равновесии друг с другом.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие к русскому изданию
- ГЛАВА I. Газы и жидкости
- § 1. Молекулярная структура газов и жидкостей
- § 2. Кинетическая теория идеального газа
- б. Расчет давления в кинетической теории газов.
- в. Расчет удельной теплоемкости в кинетической теории газов.
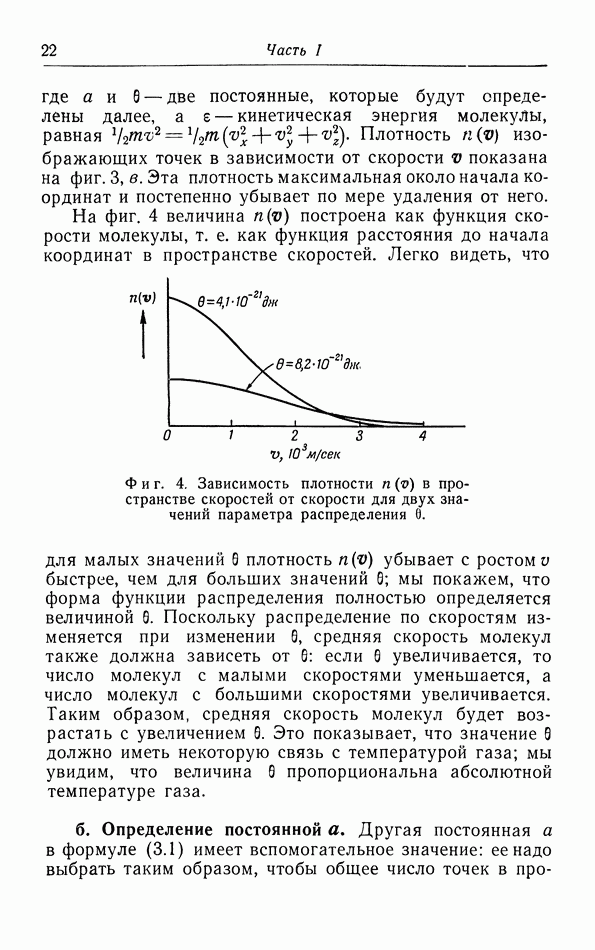
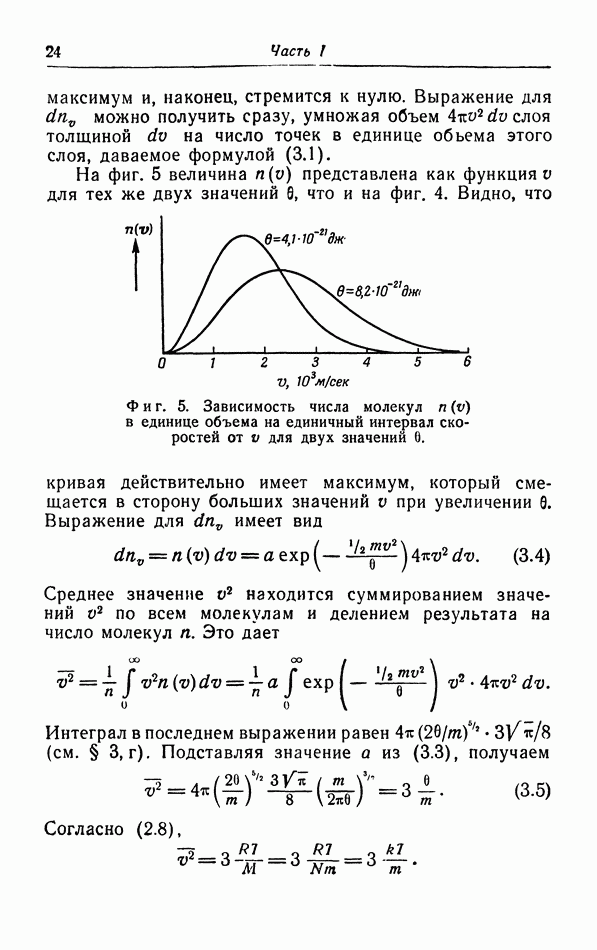
- § 3. Распределение молекул по скорости их движения
- г. Средняя квадратичная и средняя скорости.
- д. Броуновское движение.
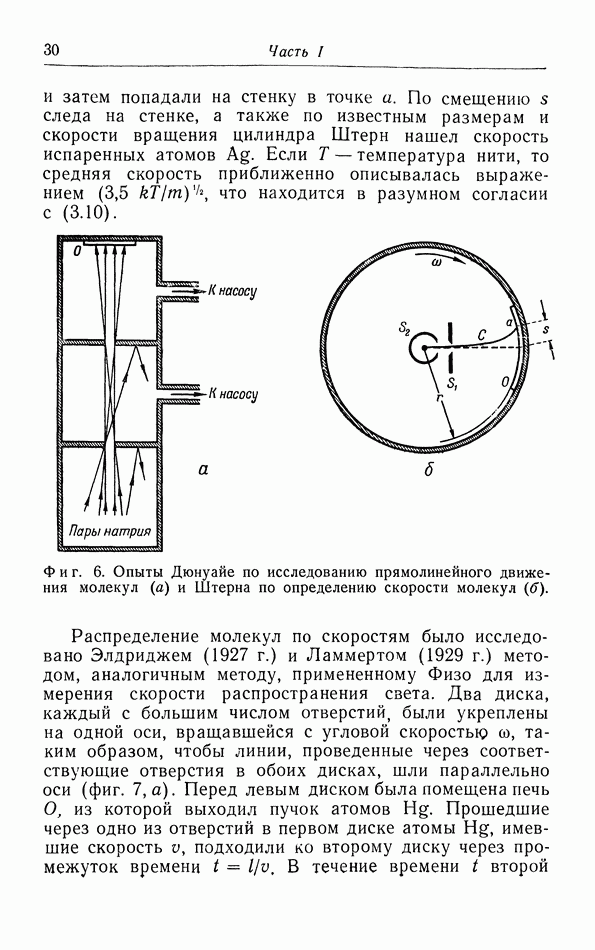
- е. Опыты с молекулярными пучками.
- § 4. Общее распределение молекул по энергиям
- б. Возбужденные состояния.
- в. вращательная и колебательная энергии.
- г. Потенциальная энергия тяготения.
- д. Потенциальная энергия межмолекулярных сил.
- § 5. Уравнение состояния газов и жидкостей
- б. Обсуждение уравнения ван дер Ваальса.
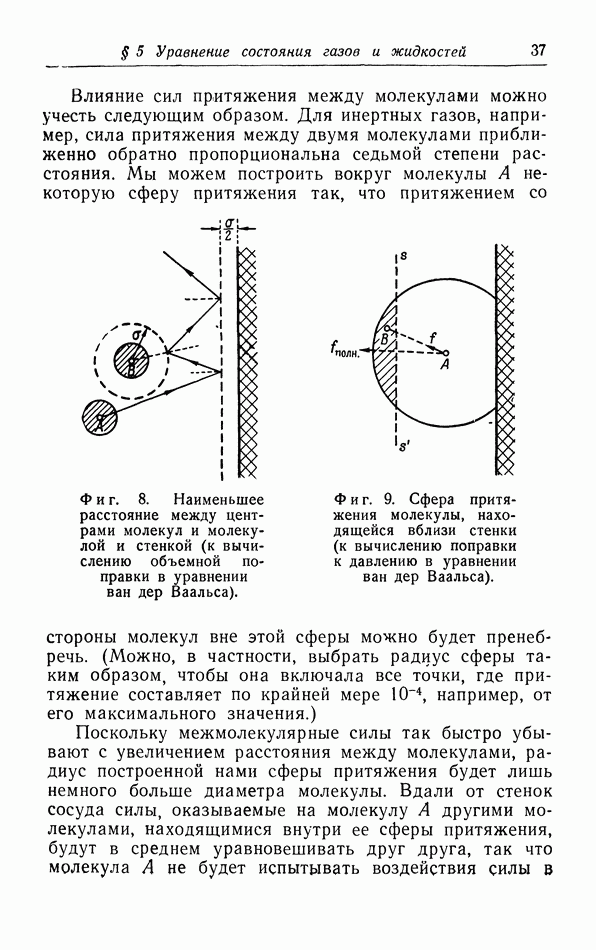
- в. Взаимодействие молекул.
- г. Более точный расчет поправок к уравнению pV=RT.
- д. Закон соответственных состояний.
- е. Жидкая фаза.
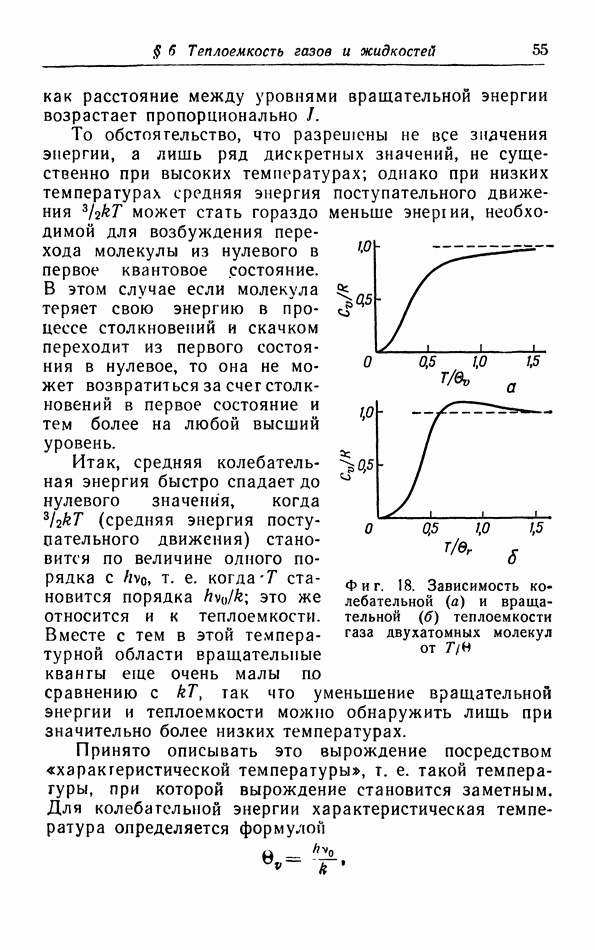
- § 6. Теплоемкость газов и жидкостей
- б. Классическая теория колебательной теплоемкости.
- в. Квантовая теория теплоемкости.
- г. Расчет колебательной теплоемкости двухатомной молекулы.
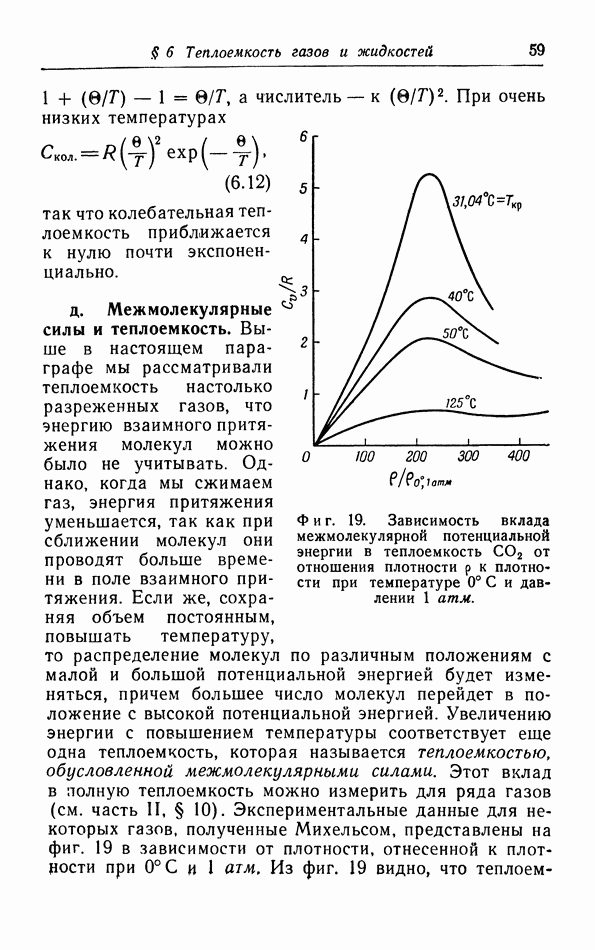
- д. Межмолекулярные силы и теплоемкость.
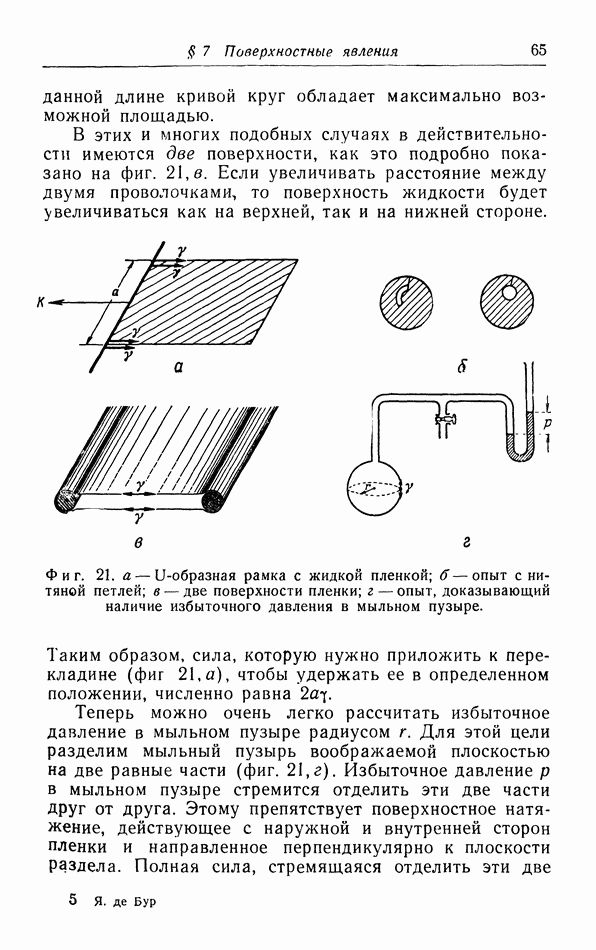
- § 7. Поверхностные явления
- б. Жидкие пленки.
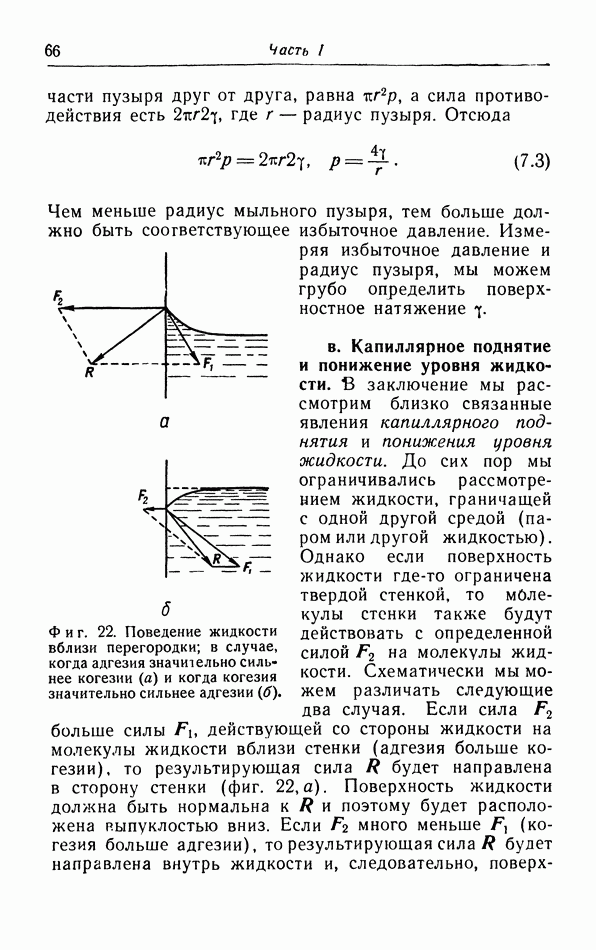
- в. Капиллярное поднятие и понижение уровня жидкости.
- § 8. Средняя длина свободного пробега, теплопроводность, вязкость и диффузия
- ГЛАВА II. Твердые тела
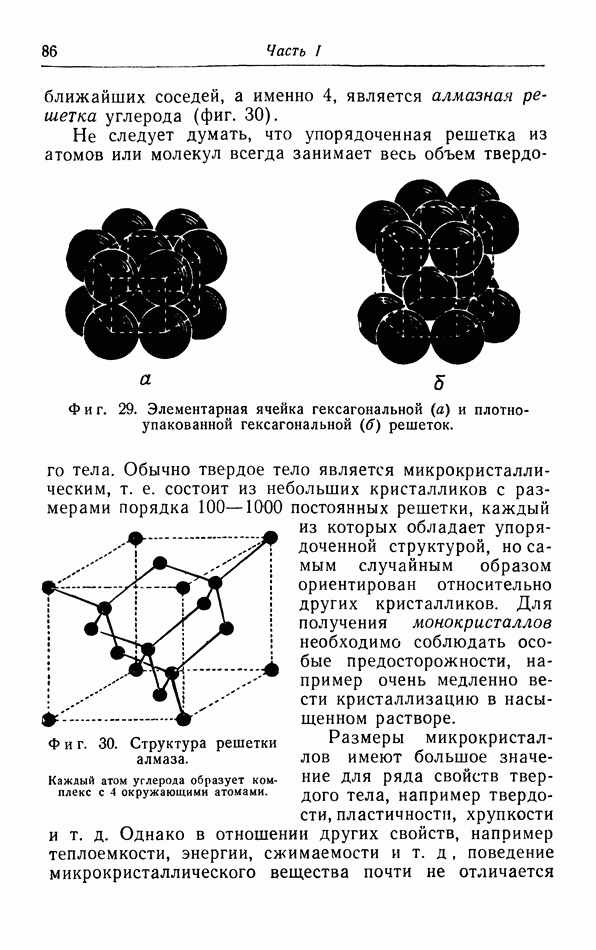
- § 9. Структура твердых тел
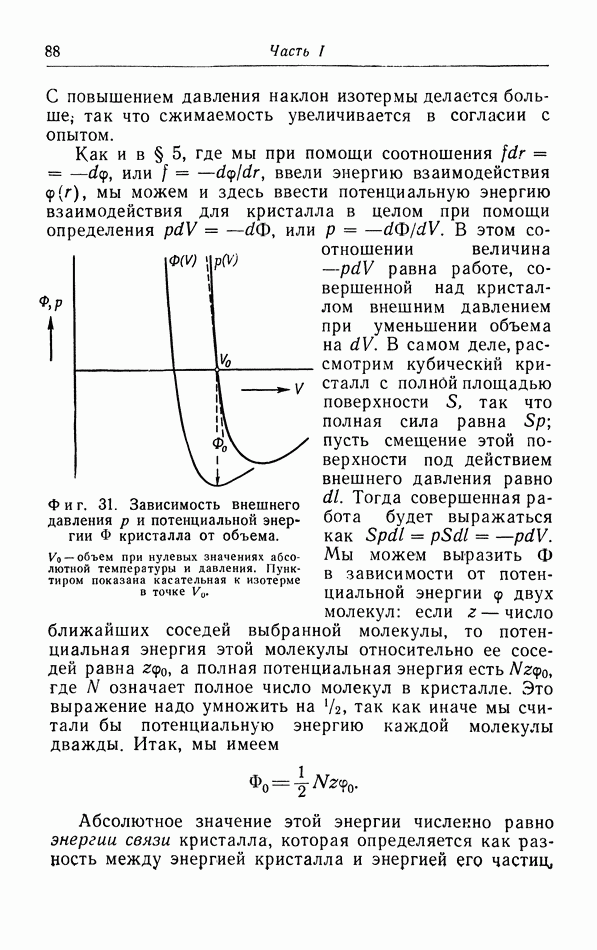
- § 10. Уравнение состояния твердых тел
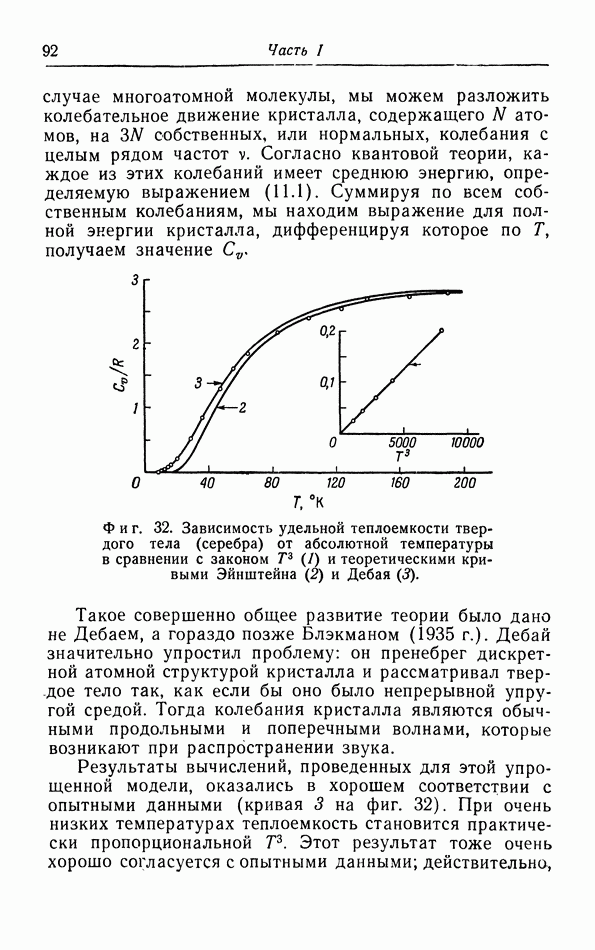
- § 11. Теплоемкость твердых тел
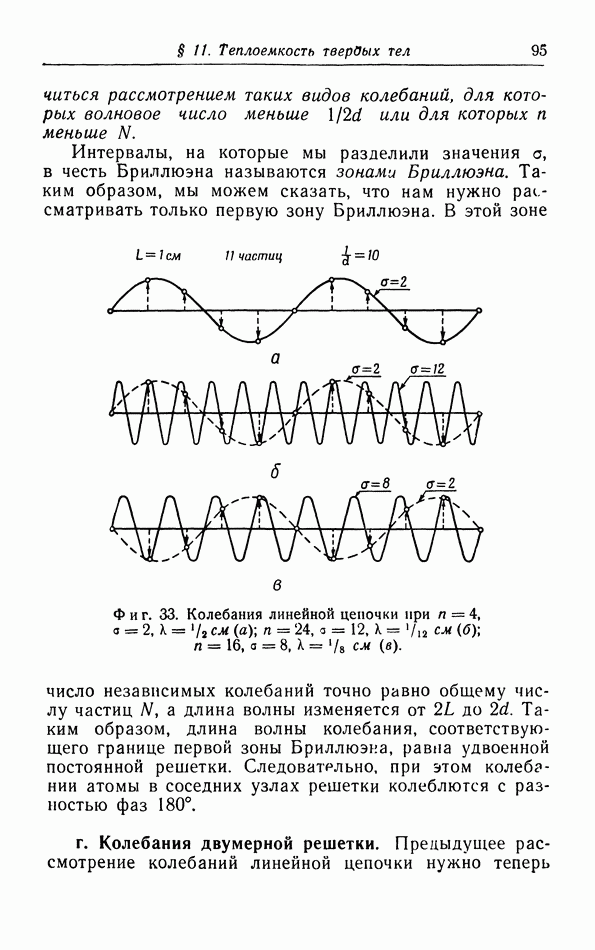
- в. Колебания линейной цепочки.
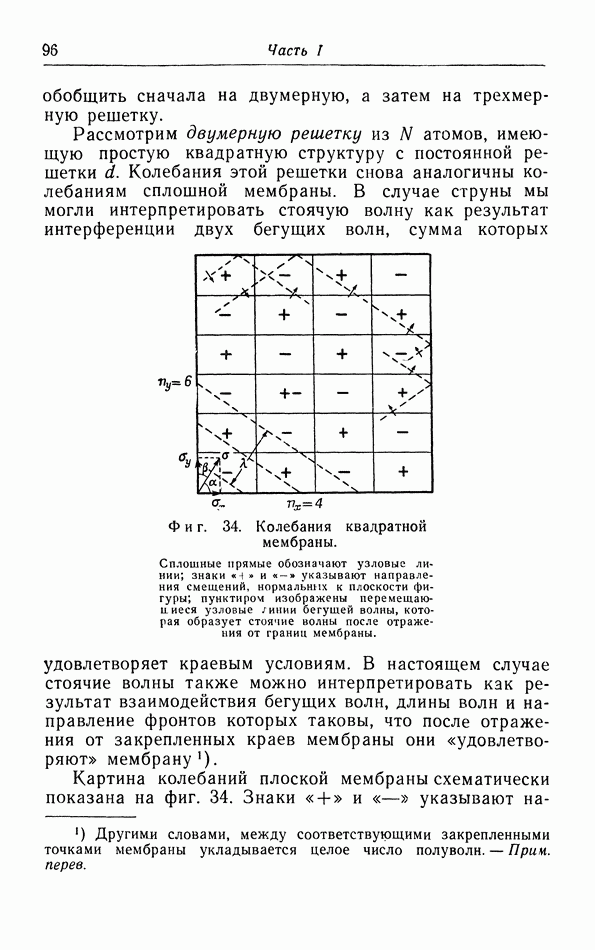
- г. Колебания двумерной решетки.
- д. Колебания трехмерной решетки.
- е. Теория Дебая.
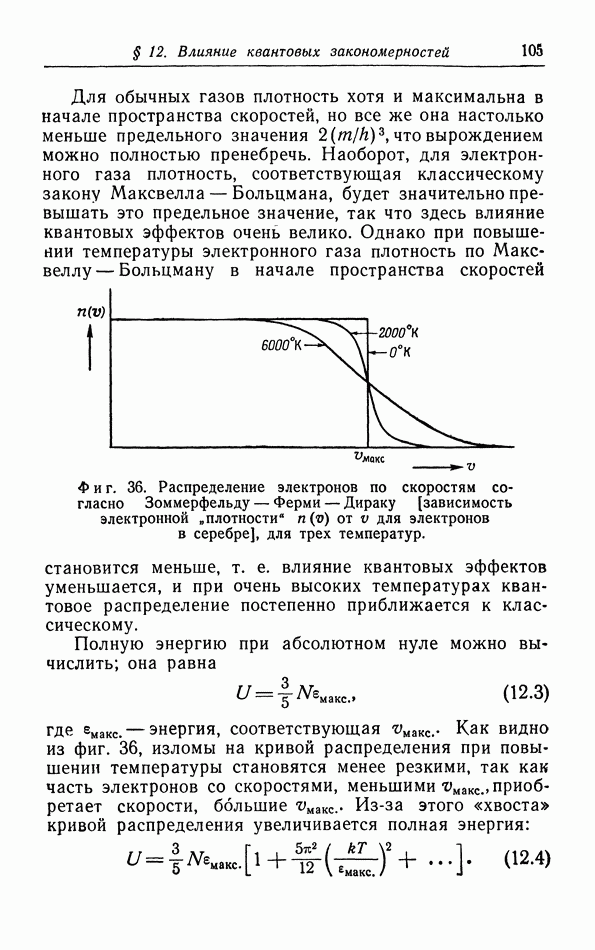
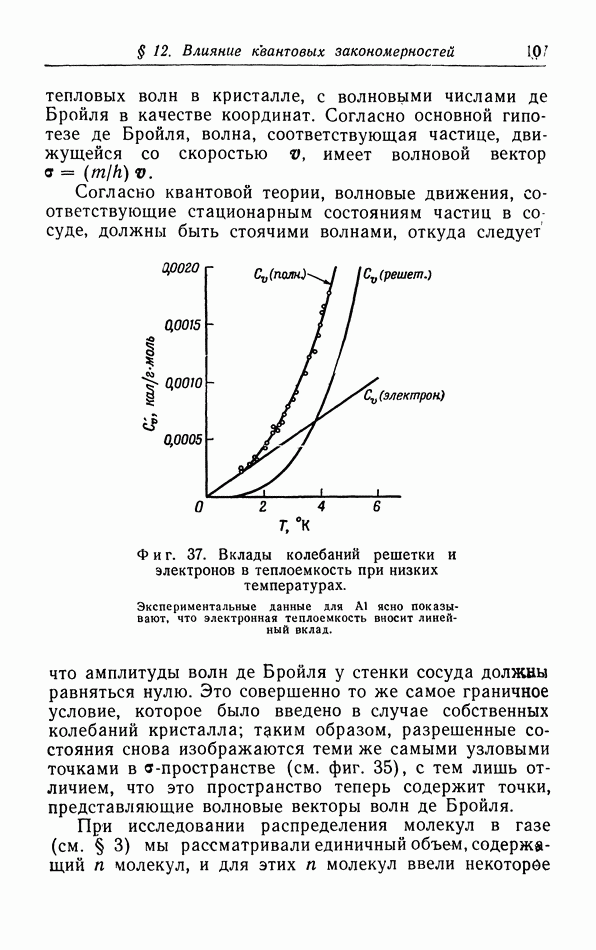
- § 12. Влияние квантовых закономерностей на распределение частиц по скоростям
- ГЛАВА III. Излучение
- § 13. Тепловое излучение и свет
- § 14. Испускание, поглощение и плотность излучения
- б. Яркость и излучательная способность.
- в. Плотность излучения.
- г. Закон Кирхгофа.
- § 15. Фотонная гипотеза. Давление излучения
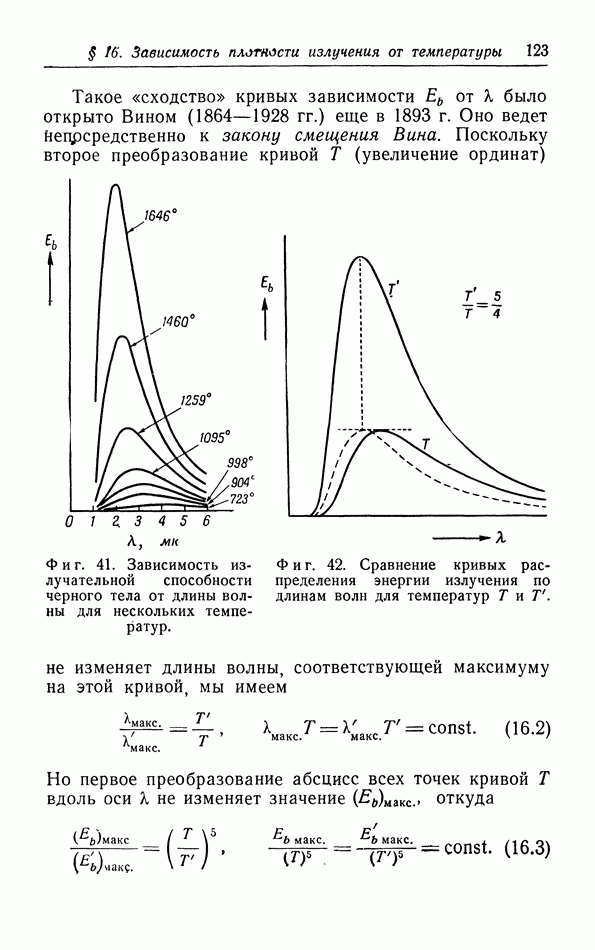
- § 16. Зависимость плотности излучения от температуры и длины волны
- б. Закон смещения Вина.
- в. Закон излучения Релея — Джинса.
- г. Закон излучения Планка.
- ГЛАВА I. Первый закон термодинамики
- § 1. Термодинамическое состояние и его изменения
- § 2. Работа при квазистатических процессах
- § 3. Первый закон термодинамики
- § 4. Опыты Джоуля и Томсона
- § 5. Дальнейшие приложения первого закона
- б. Теплоемкость.
- в. Работа при адиабатических процессах.
- ГЛАВА II. Второй закон термодинамики
- § 6. Работа и теплота в циклических процессах
- § 7. Второе начало термодинамики и его различные формулировки
- § 8. Температура
- § 9. Энтропия и второй закон термодинамики
- § 10. Применения второго закона термодинамики
- в. Изэнтропические изменения состояния.
- г. Изэнтропические холодильные процессы (процесс Ж. Клода).
- д. Иззнтропические холодильные процессы (адиабатическое размагничивание).
- е. Коэффициент полезного действия технических циклических процессов.
- ГЛАВА III. Характеристические функции
- § 11. Энергия и энтальпия
- б. Расчет процессов Джоуля и Джоуля — Томсона (Кельвина).
- в. Зависимость внутренней энергии от объема.
- г. Вывод закона Стефана — Больцмана.
- д. Характеристические функции U и H.
- § 12. Свободная энергия
- б. Свободная энергия и поверхностное натяжение.
- в. Свободная энергия и гальванические элементы.
- § 13. Свободная энтальпия и термодинамический потенциал
- б. Термодинамический потенциал.
- в. Системы с более чем одним компонентом.
- § 14. Соотношения Максвелла
- ГЛАВА IV. Неквазистатические процессы. Равновесие
- § 15. Неквазистатические процессы
- б. Подвод тепла и изменение энтропии.
- в. Увеличение энтропии в адиабатических системах.
- г. Неквазистатический изотермический процесс.
- § 16. Условия равновесия
- б. Первое условие равновесия.
- в. Второе условие равновесия.
- г. Третье условие равновесия.
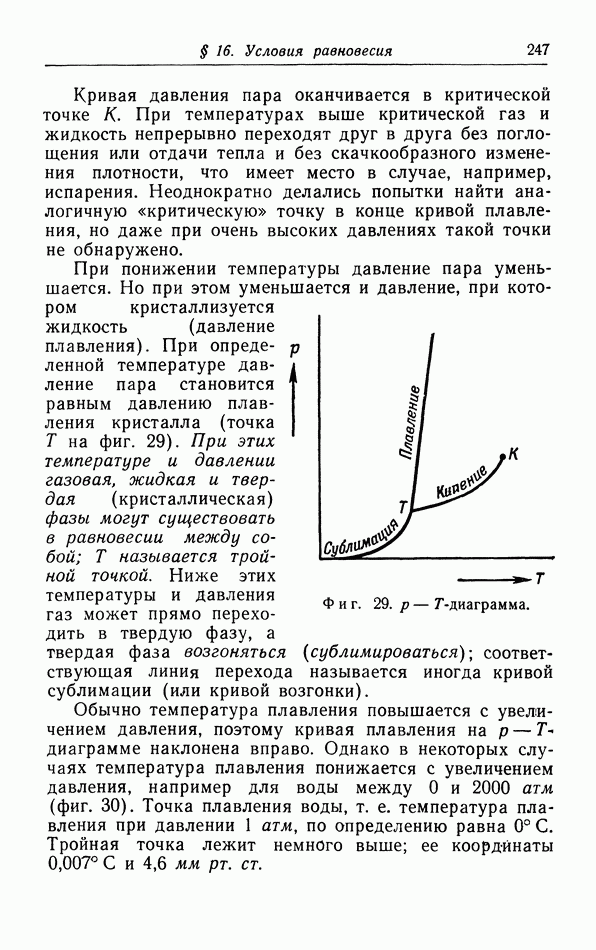
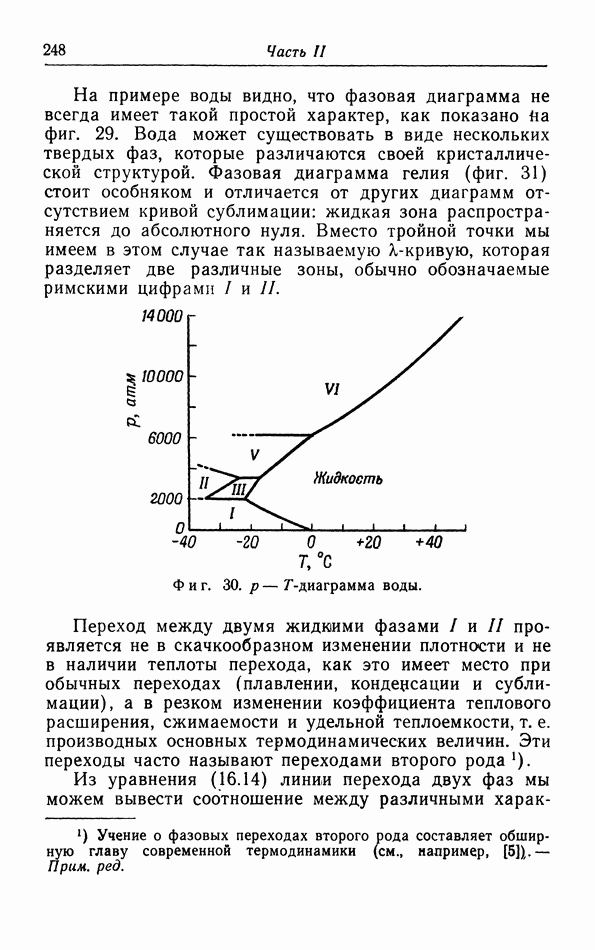
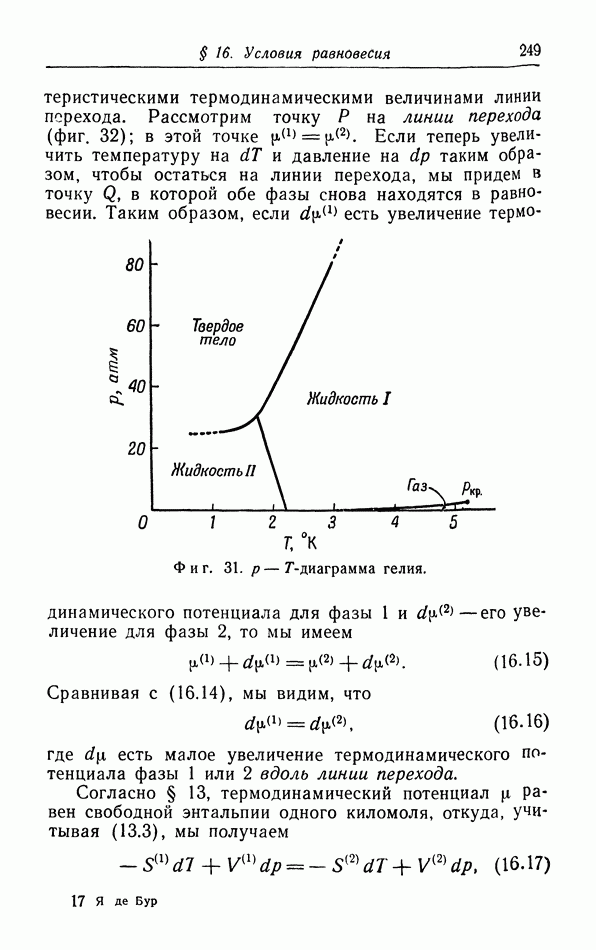
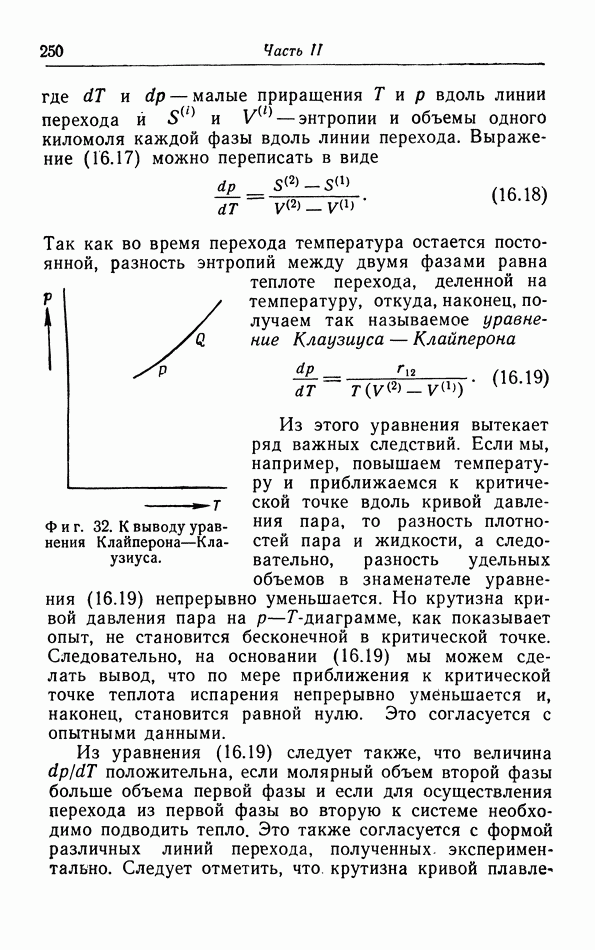
- д. p-T-диаграмма.
- е. Равновесие фаз в случае более чем одного компонента. Правило фаз.
- ГЛАВА V. Теорема Нернста
- § 17. Теорема Нернста
- § 18. Применение теоремы Нернста к фазовым переходам