| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
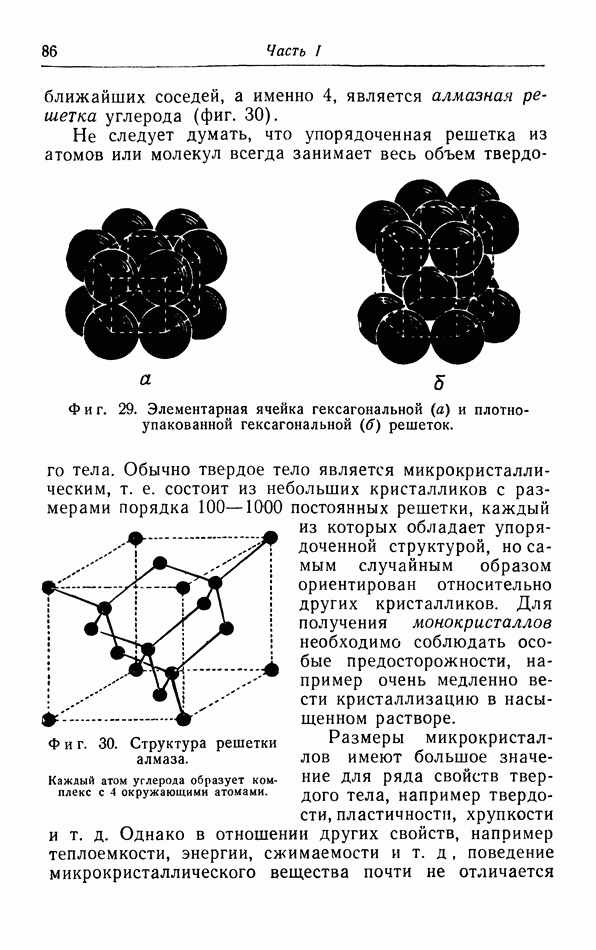
§ 3. Распределение молекул по скорости их движения
а. Распределение Максвелла.
В предыдущем параграфе мы не занимались подробным исследованием распределения молекул по скоростям, так как оказалось, что давление зависит только от среднего значения  Достаточно было лишь сделать предположение, что распределение скоростей является случайным в том смысле, что скорости молекул равномерно распределены по всем направлениям в пространстве. Теперь мы более подробно исследуем распределение молекул по различным скоростям; это распределение было выведено Максвеллом и Больцманом. Для этой цели введем понятие пространства скоростей, использованное Максвеллом: для каждой молекулы откладываем компоненты
Достаточно было лишь сделать предположение, что распределение скоростей является случайным в том смысле, что скорости молекул равномерно распределены по всем направлениям в пространстве. Теперь мы более подробно исследуем распределение молекул по различным скоростям; это распределение было выведено Максвеллом и Больцманом. Для этой цели введем понятие пространства скоростей, использованное Максвеллом: для каждой молекулы откладываем компоненты  ее скорости по трем взаимно перпендикулярным осям (фиг. 2). Таким образом, каждая точка в пространстве скоростей соответствует одной молекуле с определенной скоростью. Вектор скорости молекулы изображается, очевидно, вектором, идущим от начала координат к рассматриваемой точке.
ее скорости по трем взаимно перпендикулярным осям (фиг. 2). Таким образом, каждая точка в пространстве скоростей соответствует одной молекуле с определенной скоростью. Вектор скорости молекулы изображается, очевидно, вектором, идущим от начала координат к рассматриваемой точке.
Рассмотрим теперь распределение молекул, содержащихся в единице объема газа, по скоростям. Эти  молекул в пространстве скоростей будут изображаться совокупностью из
молекул в пространстве скоростей будут изображаться совокупностью из  точек. Вследствие непрерывного столкновения молекул точка в пространстве скоростей, характеризующая какую-то определенную молекулу, будет все время перемещаться. Следовательно, какие-то точки будут непрерывно выходить из выбранного в
точек. Вследствие непрерывного столкновения молекул точка в пространстве скоростей, характеризующая какую-то определенную молекулу, будет все время перемещаться. Следовательно, какие-то точки будут непрерывно выходить из выбранного в
пространстве скоростей элемента объема, - а некоторые другие входить извне в этот объем.
Если газ находится в стационарном состоянии, т. е. отсутствуют какие-либо макроскопические изменения, то число точек в выбранном элементе объема пространства скоростей будет сохранять свое среднее значение, не считая малых флуктуаций. Если объем этого элемента в пространстве скоростей, равный  достаточно мал, то среднее число точек в нем пропорционально его объему, т. е. равно
достаточно мал, то среднее число точек в нем пропорционально его объему, т. е. равно  .
.

Фиг. 2. Пространство скоростей молекул.
В этом выражении  есть среднее число точек в единице объема пространства скоростей, или, более строго, их «плотность» вблизи точки, определенной вектором скорости
есть среднее число точек в единице объема пространства скоростей, или, более строго, их «плотность» вблизи точки, определенной вектором скорости  с компонентами
с компонентами  . Величина
. Величина  есть число молекул газа, имеющих скорости с компонентами в пределах от
есть число молекул газа, имеющих скорости с компонентами в пределах от  до
до  от
от  до
до  и от
и от  до
до 
В предыдущем параграфе мы уже использовали тот факт, что для газа в стационарном состоянии имеет место изотропное распределение скоростей молекул по всем направлениям в пространстве. Отсюда следует, что и в пространстве скоростей не может быть преимущественных направлений, т. е. плотность должна быть сферически симметричной относительно начала координат.
Однако это условие еще не определяет вид распределения скоростей. На фиг. 3 показаны три различных распределения, удовлетворяющих условию сферической симметрии: на фиг. 3, а изображающие точки равномерно распределены по объему сферы радиусом  на фиг. 3,б эти точки равномерно распределены в пространстве между двумя сферами. В первом случае учитываются только скорости, меньшие
на фиг. 3,б эти точки равномерно распределены в пространстве между двумя сферами. В первом случае учитываются только скорости, меньшие  а во втором случае все скорости лежат в пределах от
а во втором случае все скорости лежат в пределах от  до
до 

Фиг. 3. Различные сферически симметричные распределения скоростей (в — стационарное распределение Максвелла).
Как мы уже отмечали, искомое распределение является средним распределением, поскольку имеет место непрерывное движение изображающих точек вследствие столкновений молекул. Поэтому распределение, представляющее данный газ «в среднем», не должно меняться в результате столкновений молекул: оно должно быть стационарным распределением, т. е. постоянным во времени. Распределения, представленные на фиг. 3, а и б, не удовлетворяют этому условию, так как столкновение двух молекул со скоростями  может легко вызвать большое увеличение или уменьшение их скоростей, что привело бы к непрерывному нарушению начального распределения. Распределение, которое удовлетворяет этому дополнительному требованию, было выведено Максвеллом; оно имеет вид
может легко вызвать большое увеличение или уменьшение их скоростей, что привело бы к непрерывному нарушению начального распределения. Распределение, которое удовлетворяет этому дополнительному требованию, было выведено Максвеллом; оно имеет вид

где  постоянные, которые будут определены далее,
постоянные, которые будут определены далее,  кинетическая энергия молекулы, равная
кинетическая энергия молекулы, равная  Плотность
Плотность  изображающих точек в зависимости от скорости
изображающих точек в зависимости от скорости  показана на фиг. 3, е. Эта плотность максимальная около начала координат и постепенно убывает по мере удаления от него.
показана на фиг. 3, е. Эта плотность максимальная около начала координат и постепенно убывает по мере удаления от него.

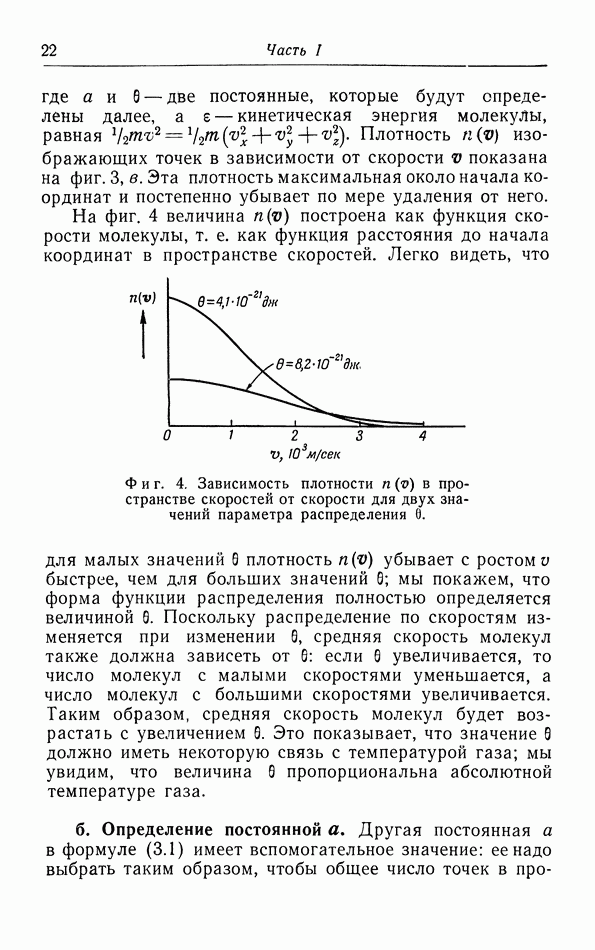
Фиг. 4. Зависимость плотности  в пространстве скоростей от скорости для двух значений параметра распределения 0.
в пространстве скоростей от скорости для двух значений параметра распределения 0.
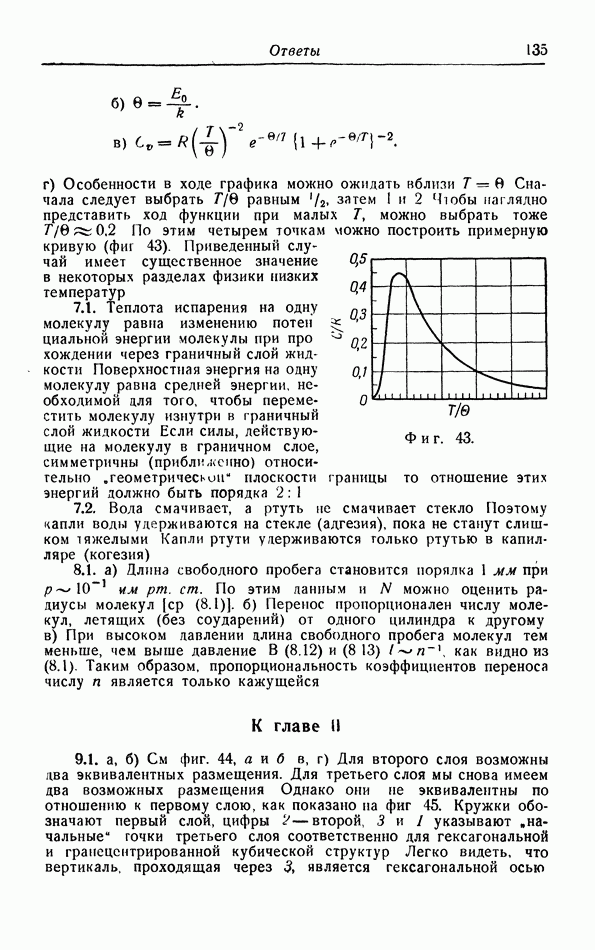
На фиг. 4 величина  построена как функция скорости молекулы, т. е. как функция расстояния до начала координат в пространстве скоростей. Легко видеть, что для малых значений
построена как функция скорости молекулы, т. е. как функция расстояния до начала координат в пространстве скоростей. Легко видеть, что для малых значений  плотность
плотность  убывает с ростом и быстрее, чем для больших значений
убывает с ростом и быстрее, чем для больших значений  ; мы покажем, что форма функции распределения полностью определяется величиной
; мы покажем, что форма функции распределения полностью определяется величиной  Поскольку распределение по скоростям изменяется при изменении
Поскольку распределение по скоростям изменяется при изменении  средняя скорость молекул также должна зависеть от
средняя скорость молекул также должна зависеть от  : если
: если  увеличивается, то число молекул с малыми скоростями уменьшается, а число молекул с большими скоростями увеличивается. Таким образом, средняя скорость молекул будет возрастать с увеличением
увеличивается, то число молекул с малыми скоростями уменьшается, а число молекул с большими скоростями увеличивается. Таким образом, средняя скорость молекул будет возрастать с увеличением  Это показывает, что значение
Это показывает, что значение  должно иметь некоторую связь с температурой газа; мы увидим, что величина
должно иметь некоторую связь с температурой газа; мы увидим, что величина  пропорциональна абсолютной температуре газа.
пропорциональна абсолютной температуре газа.
б. Определение постоянной а.
Другая постоянная а в формуле (3.1) имеет вспомогательное значение: ее надо выбрать таким образом, чтобы общее число точек
в пространстве скоростей, которое дается интегралом от  по всему пространству скоростей, было равно числу молекул в единице объема,
по всему пространству скоростей, было равно числу молекул в единице объема, 
Отсюда

Интеграл (3.2) можно записать как произведение трех интегралов, каждый из которых равен  (ср. § 3, г), откуда
(ср. § 3, г), откуда

Последняя формула выражает а через  . Мы уже использовали это соотношение на фиг. 4: для
. Мы уже использовали это соотношение на фиг. 4: для  Так как то число молекул с малыми скоростями уменьшается при увеличении 6.
Так как то число молекул с малыми скоростями уменьшается при увеличении 6.
в. Определение параметра ...
Чтобы найти связь между средним значением скорости и параметром  разделим пространство скоростей на сферические слои радиусом V и толщиной
разделим пространство скоростей на сферические слои радиусом V и толщиной  как показано на фиг. 3, е. Все изображающие точки в слое
как показано на фиг. 3, е. Все изображающие точки в слое  относятся к молекулам с одним значением модуля скорости, векторы скоростей которых равномерно распределены по всем направлениям. Как видно из фиг. 3, в, при изменении
относятся к молекулам с одним значением модуля скорости, векторы скоростей которых равномерно распределены по всем направлениям. Как видно из фиг. 3, в, при изменении  число точек в таком слое сначала возрастает вместе с
число точек в таком слое сначала возрастает вместе с  так как при увеличении
так как при увеличении  объем слоя увеличивается, а при малых значениях
объем слоя увеличивается, а при малых значениях  плотность убывает медленно. Однако при больших значениях
плотность убывает медленно. Однако при больших значениях  плотность убывает настолько быстро, что, несмотря на увеличение объема слоя, число точек в нем уменьшается. Итак, число молекул со скоростями в пределах
плотность убывает настолько быстро, что, несмотря на увеличение объема слоя, число точек в нем уменьшается. Итак, число молекул со скоростями в пределах  которое мы будем обозначать
которое мы будем обозначать  сначала возрастает, затем проходит через
сначала возрастает, затем проходит через
максимум и, наконец, стремится к нулю. Выражение для  можно получить сразу, умножая объем
можно получить сразу, умножая объем  толщиной
толщиной  на число точек в единице объема этого слоя, даваемое формулой (3.1).
на число точек в единице объема этого слоя, даваемое формулой (3.1).
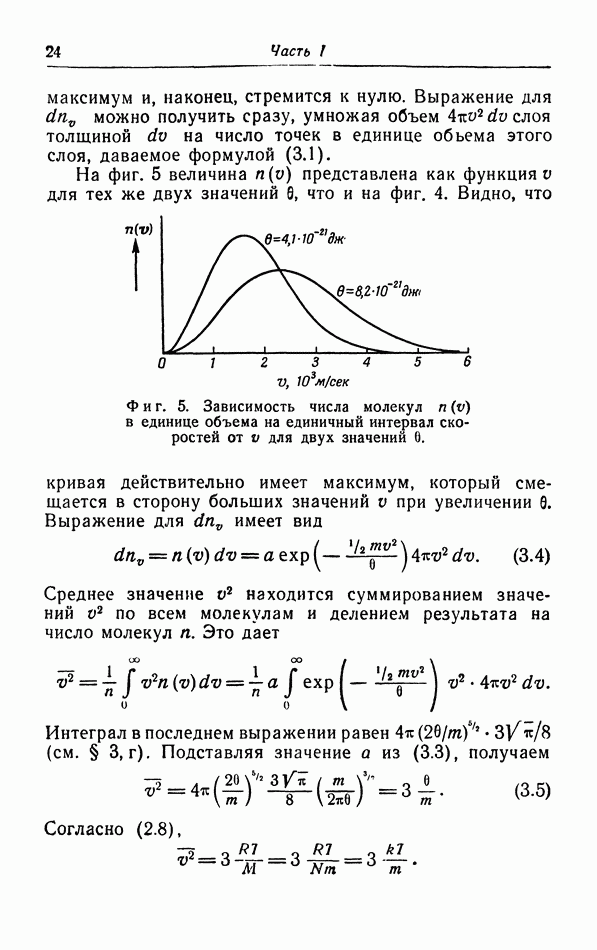
Фиг. 5. Зависимость числа молекул  в единице объема на единичный интервал скоростей от V для двух значений 6.
в единице объема на единичный интервал скоростей от V для двух значений 6.
На фиг. 5 величина  представлена как функциям для тех же двух значений 0, что и на фиг. 4. Видно, что кривая действительно имеет максимум, который смещается в сторону больших значений
представлена как функциям для тех же двух значений 0, что и на фиг. 4. Видно, что кривая действительно имеет максимум, который смещается в сторону больших значений  при увеличении 0. Выражение для
при увеличении 0. Выражение для  имеет вид
имеет вид

Среднее значение  находится суммированием значений
находится суммированием значений  по всем молекулам и делением результата на число молекул
по всем молекулам и делением результата на число молекул  Это дает
Это дает

Интеграл в последнем выражении равен  (см. § 3, г). Подставляя значение а из (3.3), получаем
(см. § 3, г). Подставляя значение а из (3.3), получаем

Согласно (2.8),


Из этих выкладок следует, что

Итак, мы показали, что параметр распределения, входящий в формулу Максвелла, пропорционален абсолютной температуре газа. Функции распределения (3.1) и (3.4) можно теперь записать в виде

и

Величину а в этих выражениях легко найти, подставляя  формулу (3.3). Это дает
формулу (3.3). Это дает

Значения  , использованные для вычисления распределений молекул по скоростям, представленным на фиг. 4 и 5, соответствуют температурам
, использованные для вычисления распределений молекул по скоростям, представленным на фиг. 4 и 5, соответствуют температурам 
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие к русскому изданию
- ГЛАВА I. Газы и жидкости
- § 1. Молекулярная структура газов и жидкостей
- § 2. Кинетическая теория идеального газа
- б. Расчет давления в кинетической теории газов.
- в. Расчет удельной теплоемкости в кинетической теории газов.
- § 3. Распределение молекул по скорости их движения
- г. Средняя квадратичная и средняя скорости.
- д. Броуновское движение.
- е. Опыты с молекулярными пучками.
- § 4. Общее распределение молекул по энергиям
- б. Возбужденные состояния.
- в. вращательная и колебательная энергии.
- г. Потенциальная энергия тяготения.
- д. Потенциальная энергия межмолекулярных сил.
- § 5. Уравнение состояния газов и жидкостей
- б. Обсуждение уравнения ван дер Ваальса.
- в. Взаимодействие молекул.
- г. Более точный расчет поправок к уравнению pV=RT.
- д. Закон соответственных состояний.
- е. Жидкая фаза.
- § 6. Теплоемкость газов и жидкостей
- б. Классическая теория колебательной теплоемкости.
- в. Квантовая теория теплоемкости.
- г. Расчет колебательной теплоемкости двухатомной молекулы.
- д. Межмолекулярные силы и теплоемкость.
- § 7. Поверхностные явления
- б. Жидкие пленки.
- в. Капиллярное поднятие и понижение уровня жидкости.
- § 8. Средняя длина свободного пробега, теплопроводность, вязкость и диффузия
- ГЛАВА II. Твердые тела
- § 9. Структура твердых тел
- § 10. Уравнение состояния твердых тел
- § 11. Теплоемкость твердых тел
- в. Колебания линейной цепочки.
- г. Колебания двумерной решетки.
- д. Колебания трехмерной решетки.
- е. Теория Дебая.
- § 12. Влияние квантовых закономерностей на распределение частиц по скоростям
- ГЛАВА III. Излучение
- § 13. Тепловое излучение и свет
- § 14. Испускание, поглощение и плотность излучения
- б. Яркость и излучательная способность.
- в. Плотность излучения.
- г. Закон Кирхгофа.
- § 15. Фотонная гипотеза. Давление излучения
- § 16. Зависимость плотности излучения от температуры и длины волны
- б. Закон смещения Вина.
- в. Закон излучения Релея — Джинса.
- г. Закон излучения Планка.
- ГЛАВА I. Первый закон термодинамики
- § 1. Термодинамическое состояние и его изменения
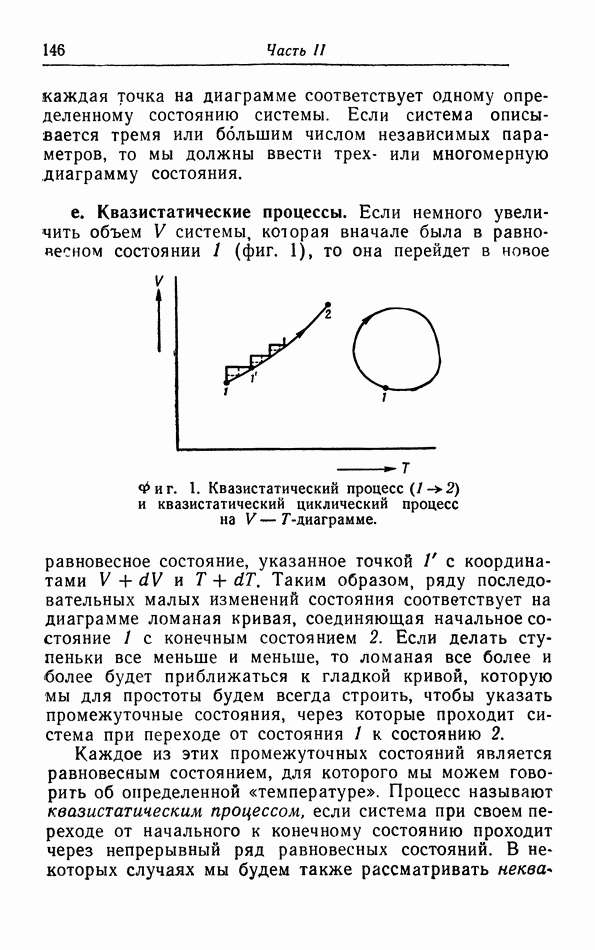
- § 2. Работа при квазистатических процессах
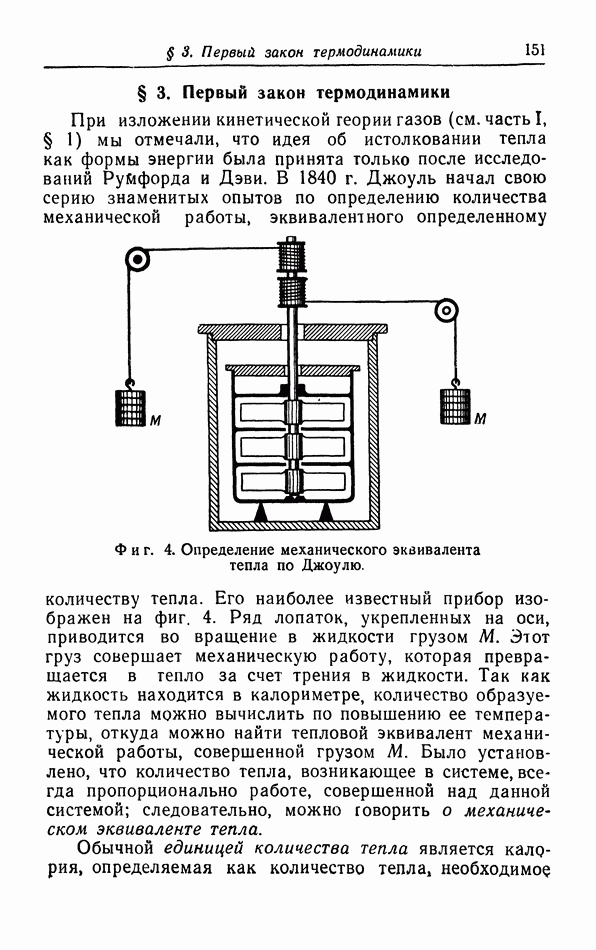
- § 3. Первый закон термодинамики
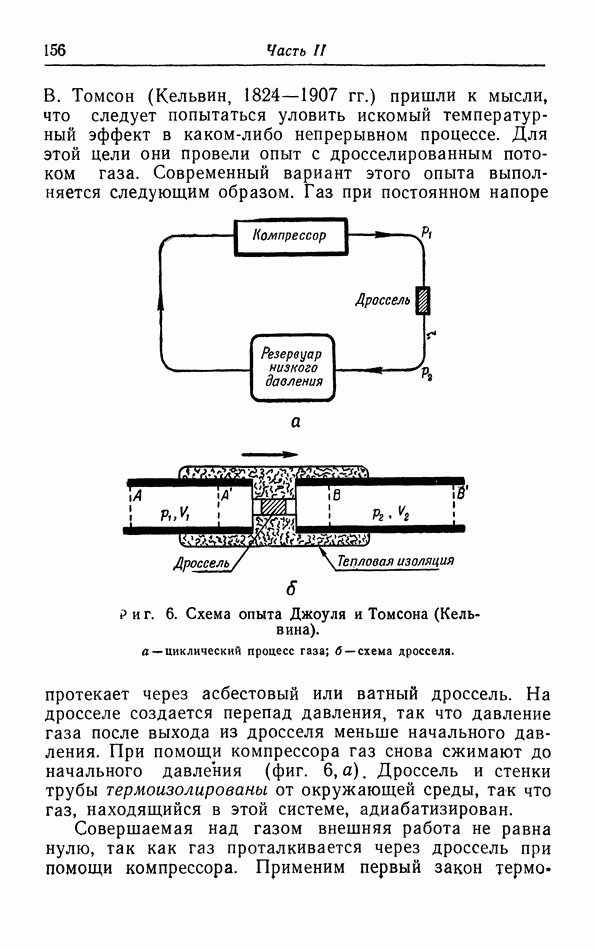
- § 4. Опыты Джоуля и Томсона
- § 5. Дальнейшие приложения первого закона
- б. Теплоемкость.
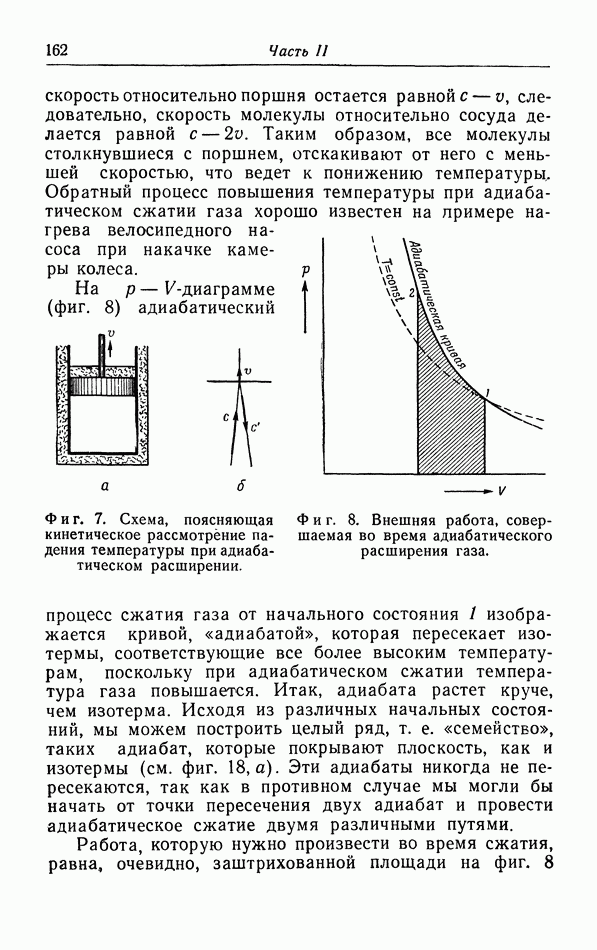
- в. Работа при адиабатических процессах.
- ГЛАВА II. Второй закон термодинамики
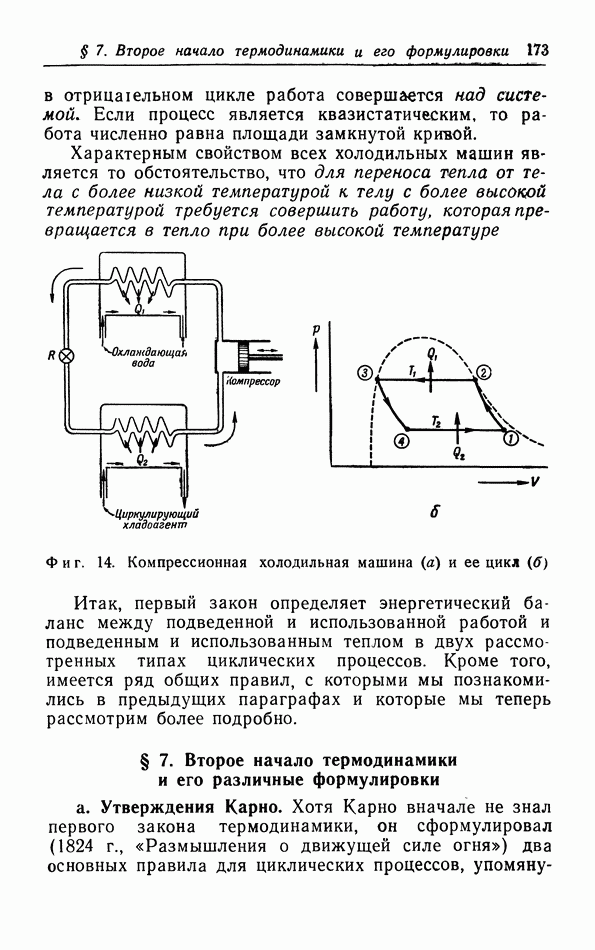
- § 6. Работа и теплота в циклических процессах
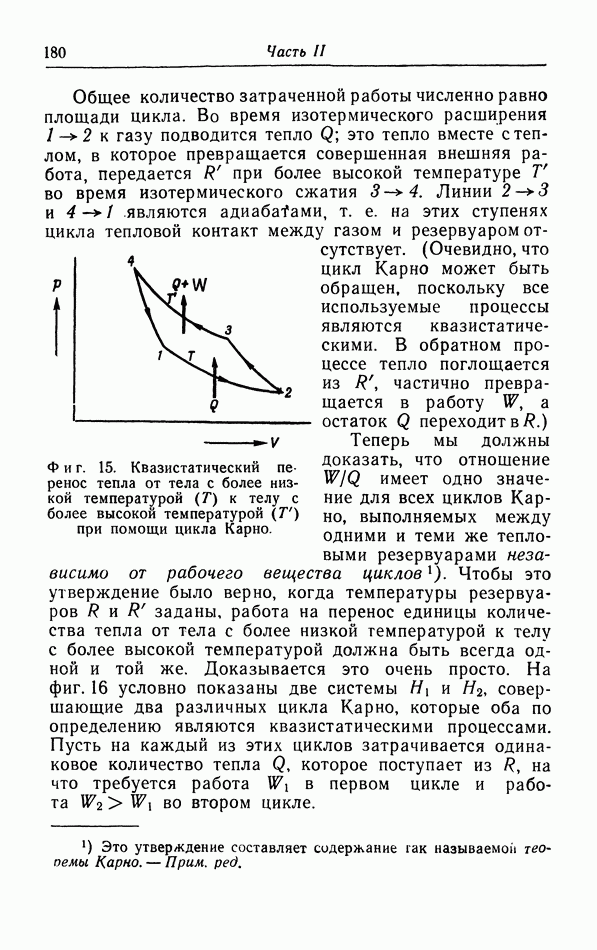
- § 7. Второе начало термодинамики и его различные формулировки
- § 8. Температура
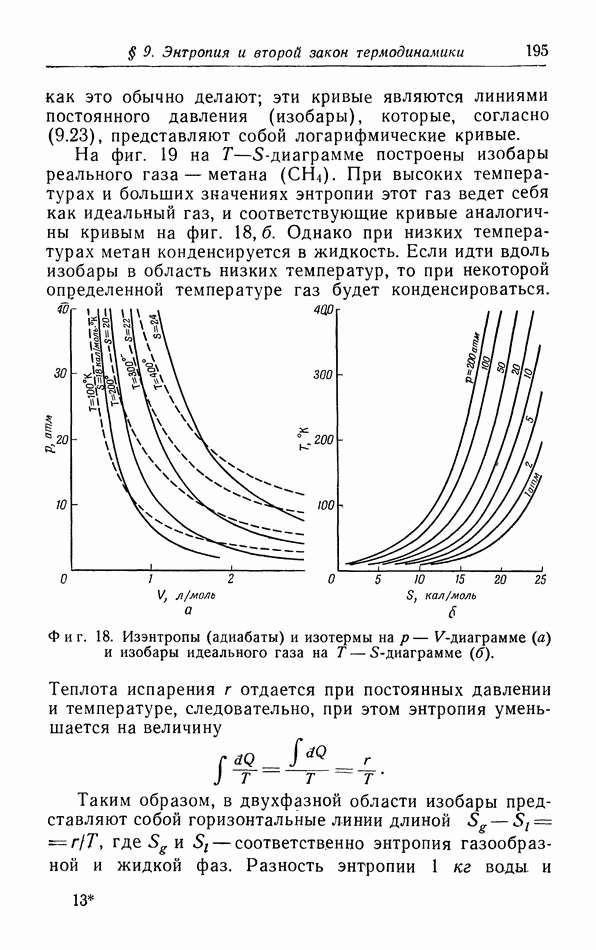
- § 9. Энтропия и второй закон термодинамики
- § 10. Применения второго закона термодинамики
- в. Изэнтропические изменения состояния.
- г. Изэнтропические холодильные процессы (процесс Ж. Клода).
- д. Иззнтропические холодильные процессы (адиабатическое размагничивание).
- е. Коэффициент полезного действия технических циклических процессов.
- ГЛАВА III. Характеристические функции
- § 11. Энергия и энтальпия
- б. Расчет процессов Джоуля и Джоуля — Томсона (Кельвина).
- в. Зависимость внутренней энергии от объема.
- г. Вывод закона Стефана — Больцмана.
- д. Характеристические функции U и H.
- § 12. Свободная энергия
- б. Свободная энергия и поверхностное натяжение.
- в. Свободная энергия и гальванические элементы.
- § 13. Свободная энтальпия и термодинамический потенциал
- б. Термодинамический потенциал.
- в. Системы с более чем одним компонентом.
- § 14. Соотношения Максвелла
- ГЛАВА IV. Неквазистатические процессы. Равновесие
- § 15. Неквазистатические процессы
- б. Подвод тепла и изменение энтропии.
- в. Увеличение энтропии в адиабатических системах.
- г. Неквазистатический изотермический процесс.
- § 16. Условия равновесия
- б. Первое условие равновесия.
- в. Второе условие равновесия.
- г. Третье условие равновесия.
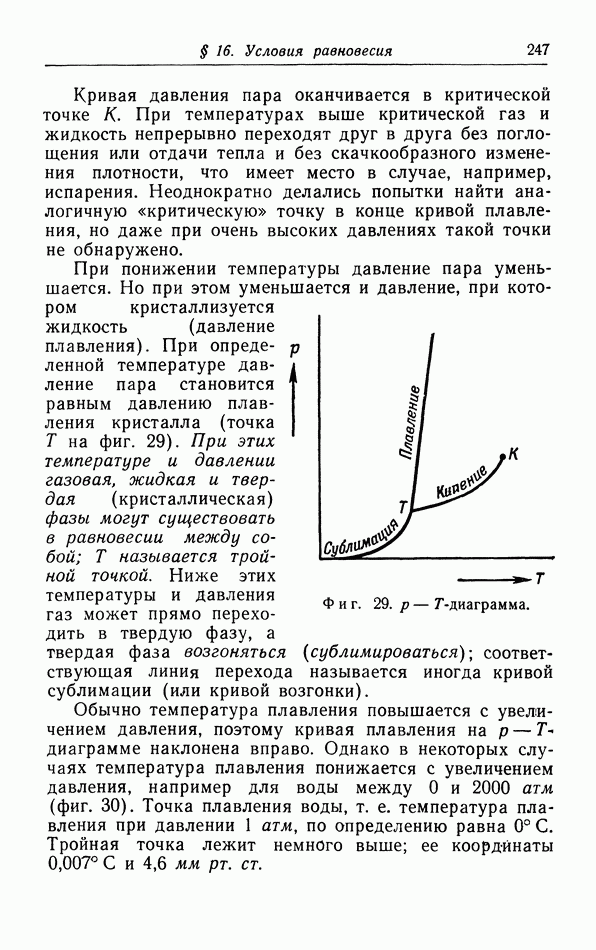
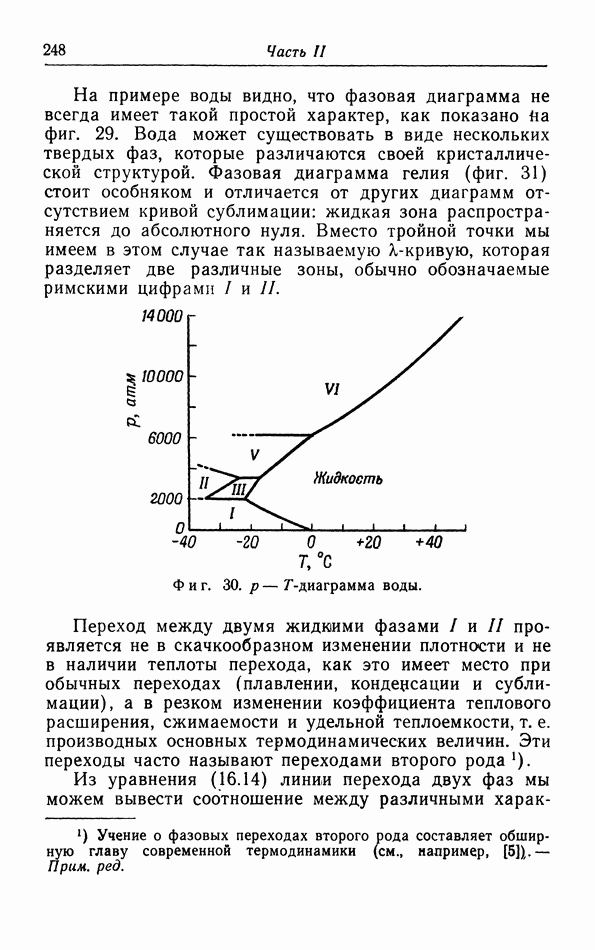
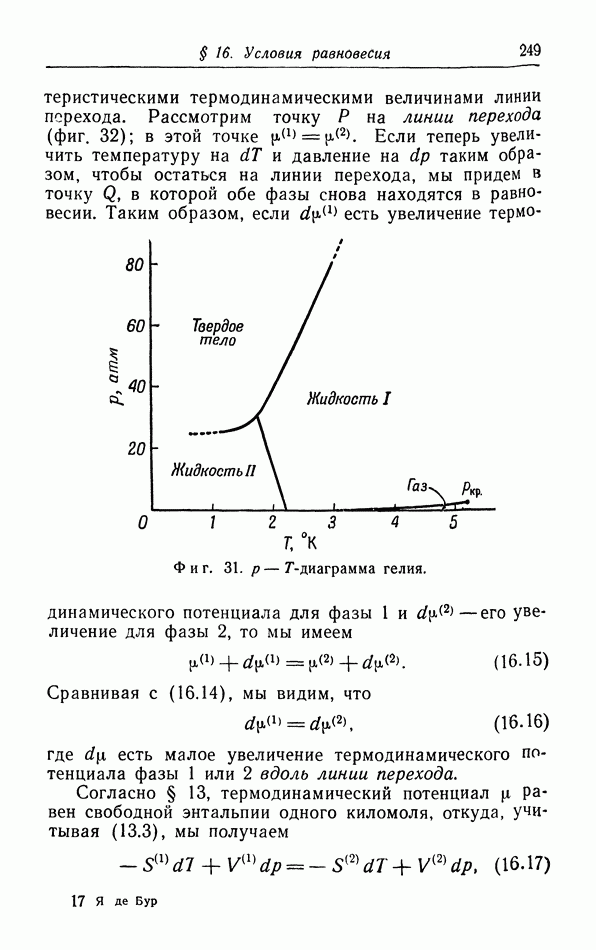
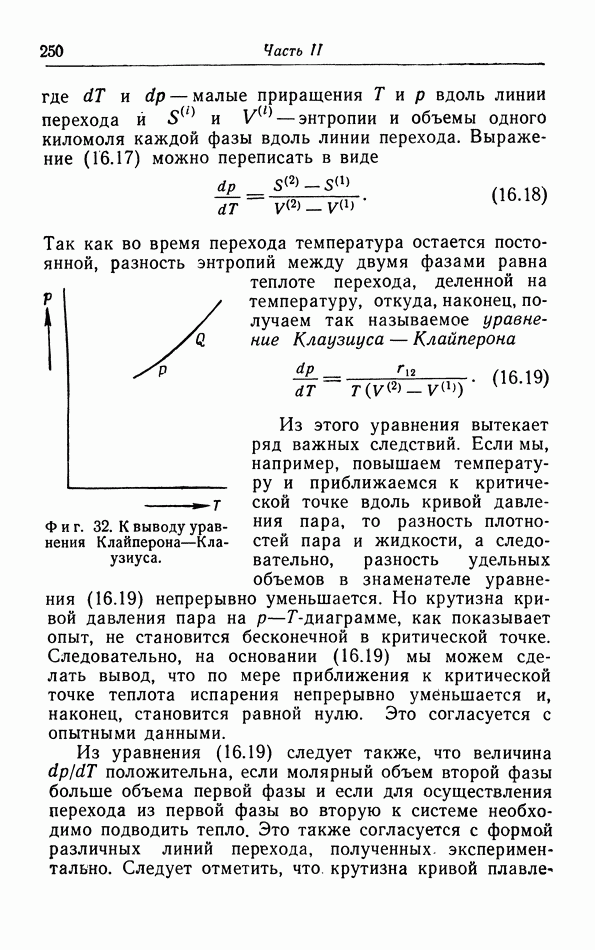
- д. p-T-диаграмма.
- е. Равновесие фаз в случае более чем одного компонента. Правило фаз.
- ГЛАВА V. Теорема Нернста
- § 17. Теорема Нернста
- § 18. Применение теоремы Нернста к фазовым переходам