| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
2. Молекулярные «сигма»-орбитали
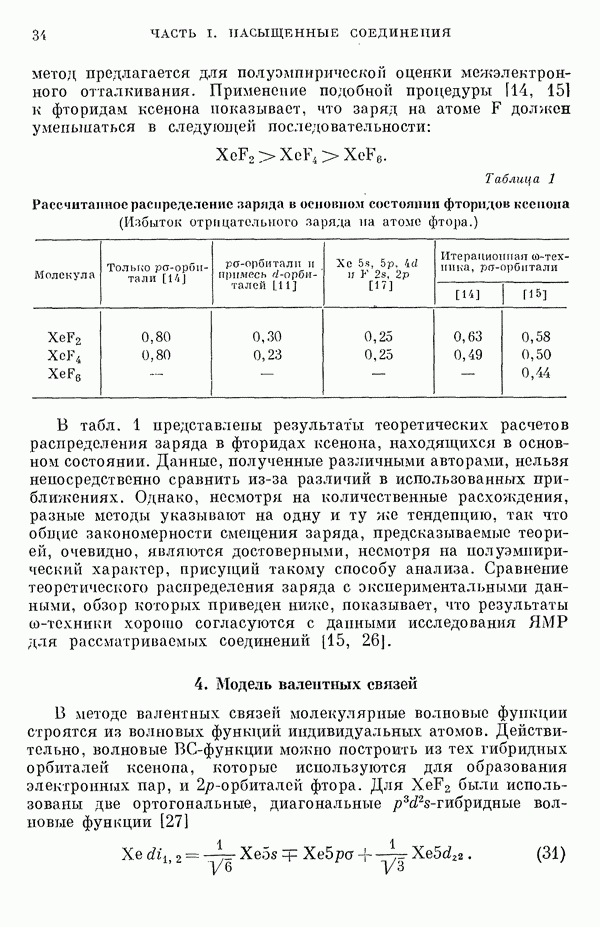
Для интерпретации свойств больших органических молекул в терминах квантовой механики мы вынуждены в общем случае использовать довольно смелые приближения. В связи с этим часто используют подход, в котором ищут и выделяют «инвариантные» составляющие системы. Известное рассмотрение сопряженных молекул в  -электронном приближении представляет собой один из таких примеров. В общем случае для насыщенных органических молекул «методы инвариантного разделения» не дают заметного упрощения, если не считать обычного исключения электронов внутренних оболочек из рассмотрения, что принято также и в этом разделе.
-электронном приближении представляет собой один из таких примеров. В общем случае для насыщенных органических молекул «методы инвариантного разделения» не дают заметного упрощения, если не считать обычного исключения электронов внутренних оболочек из рассмотрения, что принято также и в этом разделе.
Как хорошо известно,  -схема была предложена в связи с обсуждением двухатомных или линейных молекул, у которых
-схема была предложена в связи с обсуждением двухатомных или линейных молекул, у которых
проекция углового момента на ось молекулы имеет определенное значение, т. е. является хорошим квантовым числом. В нелинейных многоатомных молекулах можно использовать понятие  -электроных в приближенном смысле. В сопряженных органических молекулах понятие
-электроных в приближенном смысле. В сопряженных органических молекулах понятие  -электроны» имеет особое значение. В плоской молекуле, если мы используем подходящее приближение,
-электроны» имеет особое значение. В плоской молекуле, если мы используем подходящее приближение,  и
и  -части волновой функции отделены друг от друга. Физические причины применимости
-части волновой функции отделены друг от друга. Физические причины применимости  -электронного приближения в плоских сопряженных молекулах детально обсуждаются Ликосом и Парром
-электронного приближения в плоских сопряженных молекулах детально обсуждаются Ликосом и Парром  Кроме того, по аналогии со случаем двухатомных молекул в насыщенных органических молекулах одинарная связь, в которой распределение связывающих электронов обладает аксиальной симметрией относительно направления связи, обозначается обычно как
Кроме того, по аналогии со случаем двухатомных молекул в насыщенных органических молекулах одинарная связь, в которой распределение связывающих электронов обладает аксиальной симметрией относительно направления связи, обозначается обычно как  -связь.
-связь.
Для обсуждения электронной структуры молекул в рамках приближения Борна — Оппенгеймера мы выберем многоэлектронный гамильтониан (в атомных единицах) для органической молекулы в виде

где

 — заряд остова, связанный с атомом а, у которого удалены все валентные электроны;
— заряд остова, связанный с атомом а, у которого удалены все валентные электроны;  — расстояние между ядром а и электроном
— расстояние между ядром а и электроном  — расстояние между электронами
— расстояние между электронами  и
и  Суммирование в формуле (1) проводится по всем валентным электронам. Волновая функция основного состояния
Суммирование в формуле (1) проводится по всем валентным электронам. Волновая функция основного состояния  определяется как функция, которая минимизирует следующее выражение:
определяется как функция, которая минимизирует следующее выражение:

Мы не знаем, каков аналитический вид функции  за исключением того, что она во всяком случае является функцией
за исключением того, что она во всяком случае является функцией  координат, где
координат, где  — число валентных электронов. В качестве приближенного многоэлектронного рассмотрения мы используем метод Хартри—Фока, в котором для образования полной волновой функции
— число валентных электронов. В качестве приближенного многоэлектронного рассмотрения мы используем метод Хартри—Фока, в котором для образования полной волновой функции  вводится понятие об одноэлектронной волновой функции (орбитали). В этом приближении принято, что электроны движутся независимо, если не считать эффекта взаимного влияния, обусловленного усредненным полем. Даже «наилучшая» хартри-фоковская волновая функция для молекулы приводит к так
вводится понятие об одноэлектронной волновой функции (орбитали). В этом приближении принято, что электроны движутся независимо, если не считать эффекта взаимного влияния, обусловленного усредненным полем. Даже «наилучшая» хартри-фоковская волновая функция для молекулы приводит к так
называемым «корреляционным» ошибкам, которые в основном обусловлены пренебрежением столкновениями электронов. Такие ошибки мы не будем пока учитывать; о корреляционных эффектах см. в т. 2 настоящей книги.
В одноэлектронном приближении функция  аппроксимируется линейной комбинацией слэтеровских детерминантов
аппроксимируется линейной комбинацией слэтеровских детерминантов

причем правая часть представляет собой детерминант  характеризующийся своими диагональными элементами; образуют некоторый подходящий набор ортонормированных одноэлектронных орбиталей, состоящих из координатной части
характеризующийся своими диагональными элементами; образуют некоторый подходящий набор ортонормированных одноэлектронных орбиталей, состоящих из координатной части  и спиновой части
и спиновой части  . В качестве первого приближения мы рассмотрим случай, когда
. В качестве первого приближения мы рассмотрим случай, когда  аппроксимируется одним детерминантом. Устойчивые органические молекулы, вообще говоря, обладают электронной структурой, в которой каждая пара электронов занимает две орбитали
аппроксимируется одним детерминантом. Устойчивые органические молекулы, вообще говоря, обладают электронной структурой, в которой каждая пара электронов занимает две орбитали  с одинаковыми координатными и противоположными спиновыми функциями. Такая «замкнутая оболочка» описывается волновой функцией вида
с одинаковыми координатными и противоположными спиновыми функциями. Такая «замкнутая оболочка» описывается волновой функцией вида

где  Для энергии
Для энергии  имеем выражение
имеем выражение

где

Во всем предыдущем рассмотрении мы не задавались определенной формой каждой молекулярной орбитали  Так же, как и при расчетах атомов, можно найти наилучшие
Так же, как и при расчетах атомов, можно найти наилучшие  решив уравнения Фока. Соответствующая процедура решения системы нелинейных дифференциальных уравнений всегда является трудной задачей, поэтому воспользуемся приближенными выражениями для
решив уравнения Фока. Соответствующая процедура решения системы нелинейных дифференциальных уравнений всегда является трудной задачей, поэтому воспользуемся приближенными выражениями для  . В качестве приближения мы используем «липейиый вариационный метод», в котором
. В качестве приближения мы используем «липейиый вариационный метод», в котором  представляют в виде линейной комбинации
представляют в виде линейной комбинации
определенного числа известных функций 

Для минимизации энергии коэффициенты линейных комбинаций должны удовлетворять уравнениям Фока, которые в этом случае сводятся к виду

где  число взятых орбиталей
число взятых орбиталей  — число занятых орбиталей
— число занятых орбиталей  как было отмечено выше, и, кроме того,
как было отмечено выше, и, кроме того,

Выражение для энергии принимает вид

Далее можно принять три вида линейных комбинаций.
1. Метод ЛKAO:  — все атомные орбитали, скажем орбитали всех атомов, слэтеровского типа
— все атомные орбитали, скажем орбитали всех атомов, слэтеровского типа  которые связаны с химической валентностью.
которые связаны с химической валентностью.
2. Метод ЛКВО:  — содержит валентные орбитали, ассоциируемые со связывающими электронами, включая обособленные электронные пары; например, орбиталь
— содержит валентные орбитали, ассоциируемые со связывающими электронами, включая обособленные электронные пары; например, орбиталь  и гибридные орбитали атома углерода и орбиталь
и гибридные орбитали атома углерода и орбиталь  атома водорода в углеводородах; гибридными орбиталями углерода могут быть
атома водорода в углеводородах; гибридными орбиталями углерода могут быть  орбитали.
орбитали.
3. Метод ЛКСО:  — орбитали связи, выбранные соответствующим образом и локализованные на каждой связи.
— орбитали связи, выбранные соответствующим образом и локализованные на каждой связи.
При необходимости можно использовать при дальнейшем решении также метод конфигурационного взаимодействия, как это обычно делается в  -электронном приближении. Для краткости мы предлагаем называть три метода, упомянутые выше, как
-электронном приближении. Для краткости мы предлагаем называть три метода, упомянутые выше, как
ЛКАО-ССП, ЛКВО-ССП и ЛКСО-ССП соответственно. Применению метода ЛКАО-ССП для простых молекул посвящено большое число работ, которые отражены в обзоре Аллена и Каро [2]. Метод ЛКВО-ССП применялся только для специфических простых случаев 13, 4]. Кроме того, Имамура и др. [5] выполнили расчет по методу ЛКВО-АСМО для метана.
Леннард-Джонс и др.  показали, что для симметричной молекулы набор
показали, что для симметричной молекулы набор  полученных по методу ЛКАО, можно при помощи унитарного преобразования перевести в другой набор эквивалентных орбиталей
полученных по методу ЛКАО, можно при помощи унитарного преобразования перевести в другой набор эквивалентных орбиталей  в основном локализованных на каждой связи или на каждой орбитали обособленной пары. Орбитали, полученные таким образом, называются «эквивалентными орбиталями», и разумно ожидать, что они будут сходны с базисными функциями, входящими в линейные комбинации в методе ЛКСО. Другими словами, неопределенность понятия связи в методе ЛКАО исключается, согласно концепции Леннард-Джонса, при введении понятия об эквивалентных орбиталях. Метод Леннард-Джонса позволил дать физическое обоснование для понятия «орбитали связи» при обсуждении свойств насыщенных молекул и вызвал появление ряда более упрощенных методов
в основном локализованных на каждой связи или на каждой орбитали обособленной пары. Орбитали, полученные таким образом, называются «эквивалентными орбиталями», и разумно ожидать, что они будут сходны с базисными функциями, входящими в линейные комбинации в методе ЛКСО. Другими словами, неопределенность понятия связи в методе ЛКАО исключается, согласно концепции Леннард-Джонса, при введении понятия об эквивалентных орбиталях. Метод Леннард-Джонса позволил дать физическое обоснование для понятия «орбитали связи» при обсуждении свойств насыщенных молекул и вызвал появление ряда более упрощенных методов  .
.
В некоторых из этих методов  представляют в виде линейной комбинации орбиталей связи, так же как в методе ЛKCO. При этом, однако, используется гамильтониан не вида (1), а следующий:
представляют в виде линейной комбинации орбиталей связи, так же как в методе ЛKCO. При этом, однако, используется гамильтониан не вида (1), а следующий:

где  — определенный оператор, включающий члены отталкивания, содержащиеся в выражении (1) в усредненной форме. В этой схеме для энергии замкнутой оболочки выражение (4) сводится квиду
— определенный оператор, включающий члены отталкивания, содержащиеся в выражении (1) в усредненной форме. В этой схеме для энергии замкнутой оболочки выражение (4) сводится квиду

Наилучшие функции, даваемые линейной комбинацией вида (5), можно определить путем решения системы линейных уравнений относительно коэффициентов 

где  — одноэлектронная энергия
— одноэлектронная энергия  орбитали, определяемая из хорошо известного секулярного уравнения
орбитали, определяемая из хорошо известного секулярного уравнения

 соответственно кулоновский, резонансный интеграл и интеграл перекрывания
соответственно кулоновский, резонансный интеграл и интеграл перекрывания

Интегралы  оцениваются полуэмпирически. Уравнение для энергии принимает вид
оцениваются полуэмпирически. Уравнение для энергии принимает вид

Это упрощение можно применять не только в методе ЛКСО-ССП, но также и в методах ЛКАО-ССП и ЛКВО-ССП.
Упрощенные методы, упомянутые выше, мы предлагаем называть ЛКАО-ХМО (молекулярная орбиталь Хюккеля), ЛКВО-ХМО и ЛКСО-ХМО соответственно, поскольку сходный метод, в котором в качестве  берут
берут  -атомные орбитали углерода, был введен ранее в
-атомные орбитали углерода, был введен ранее в  -электронном приближении Хюккелем. Первые два из указанных методов при условии соответствующей параметризации в основном эквивалентны.
-электронном приближении Хюккелем. Первые два из указанных методов при условии соответствующей параметризации в основном эквивалентны.
Во всех методах ЛКСО-ХМО [7а-з] в качестве базисных функций в линейной комбинации применяются только связывающие орбитали для каждой связи и не принимаются во внимание разрыхляющие орбитали. В рамках этой схемы мы не можем рассматривать высшие одноэлектронные уровни, поскольку линейная комбинация орбиталей связи дает только общее число орбиталей, заполненных электронами. Это обстоятельство оказывается серьезным недостатком такого метода при обсуждении, ианример, проблем химической реакционной способности.
Для того чтобы избежать этого недостатка,  должны использовать методы ЛКАО или ЛКВО, в которых обычно число
должны использовать методы ЛКАО или ЛКВО, в которых обычно число  равно числу валентных электронов. Это число орбиталей является необходимым и достаточным для построения почти такого числа незанятых молекулярных орбиталей (помимо занятых
равно числу валентных электронов. Это число орбиталей является необходимым и достаточным для построения почти такого числа незанятых молекулярных орбиталей (помимо занятых  чтобы мы могли рассматривать более высокие одноэлектронные уровни так же, как в методе Хюккеля для
чтобы мы могли рассматривать более высокие одноэлектронные уровни так же, как в методе Хюккеля для  -электронных систем.
-электронных систем.
Метод ЛКАО-ХМО был нредложен для практического использования Гофманом [8а, б] при рассмотрении углеводородов с большим молекулярным весом. Для вычислений подобного типа первоначально Малликеп и др.  а затем еще несколько авторов
а затем еще несколько авторов  предложили различные способы приближенной оценки
предложили различные способы приближенной оценки
резонансного интеграла 

Если необходимо рассмотрение, выходящее за рамки приближения Хюккеля, то мы можем вернуться к антисимметризованному выражению (3) и с помощью метода Хартри — Фока получить более точные сведения о занятых одноэлектронных уровнях.
Такая процедура чрезвычайно эффективна, поскольку она позволяет получить определенную информацию об изменении молекулярной энергии при любом изменении конформации молекулярной системы. Таким образом, в принципе мы можем определить наиболее устойчивую конфигурацию молекулы. Это особенно важно также для теории химических реакций в связи с выбором конфигурации «активированного комплекса» и «промежуточных продуктов реакции».
Однако указанный подход все же не совершенен, поскольку понятие «связи», которое восстанавливается в методе ЛКАО, благодаря идее об эквивалентной орбитали становится еще более неясным. (При использовании представления о «заселенности связи» [14а] указанное понятие несколько уточняется. Но однозначное вычисление заселенности связи вызывает затруднения.) Нам не нужно строго сохранять консервативное классическое понятие о связи; однако при сопоставлении теории с химической практикой мы еще часто вынуждены к нему обращаться.
При этом лучше воспользоваться методом ЛКВО, в котором валентные орбитали вытянуты в направлении  -связей. Таким образом, мы получим метод, в котором все еще применяется понятие связи и который в то же время удобен для обсуждения химического взаимодействия насыщенных молекул.
-связей. Таким образом, мы получим метод, в котором все еще применяется понятие связи и который в то же время удобен для обсуждения химического взаимодействия насыщенных молекул.
В этом направлении выполнено несколько работ [15а-г]. По ряду причин здесь остановимся на методе, предложенном в работе Фукуи и др. [15г], в которой главное внимание уделено
рассмотрению углеводородов. Базисные функции в линейной комбинации, т. е.  в формуле (5), выбраны в следующем виде:
в формуле (5), выбраны в следующем виде:

где  — соответственно
— соответственно  и
и  -слэтеровские орбитали атома углерода, расположенные в направлении а-связи.
-слэтеровские орбитали атома углерода, расположенные в направлении а-связи.
Оценка различных интегралов проводится полуэмпирически.
Кулоновские интегралы

Резонансные интегралы

Все другие, пренебрежимо малые резонапсные интегралы не учитывались.
Интегралы перекрывания
Сандорфи [15а] принял во внимание интегралы перекрывания, но Фукуи и др. [15г] не стали учитывать их, из-за чего получили картину со смещенными уровнями энергии, на распределении  электронов это почти не отразилось. При обсуждении химической реакционной способности можно ввести это упрощающее предложение.
электронов это почти не отразилось. При обсуждении химической реакционной способности можно ввести это упрощающее предложение.
Для  -параметров, относящихся к аналитической форме орбиталей Слэтера и теоретической
-параметров, относящихся к аналитической форме орбиталей Слэтера и теоретической
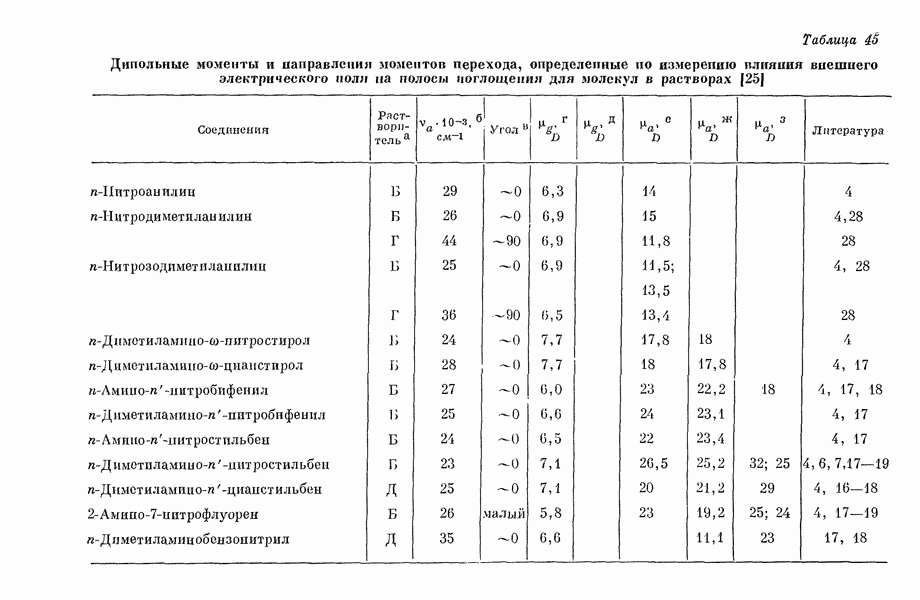
Таблица 5  -Дипольные моменты,
-Дипольные моменты, 

оценке интегралов перекрывания, Фукуи и др. [15а] приняли следующие численные значения, согласующиеся с различными эмпирическими результатами:
(см. скан)
Интегралы для других типов атомов также определялись аналогичным путем  Этим методом исследовались сг-электронные структуры и а-дипольные моменты (табл. 5) сопряженных молекул [15д].
Этим методом исследовались сг-электронные структуры и а-дипольные моменты (табл. 5) сопряженных молекул [15д].
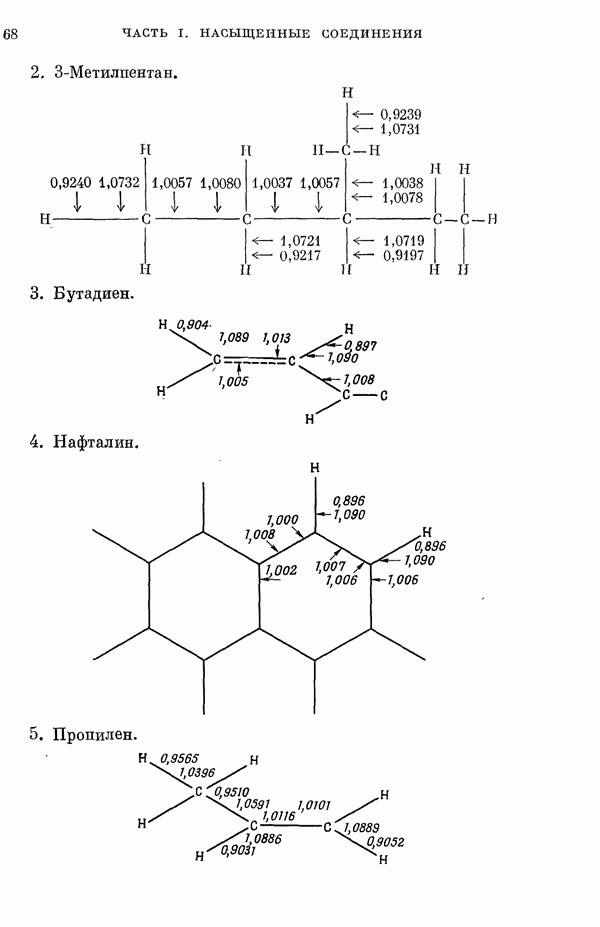
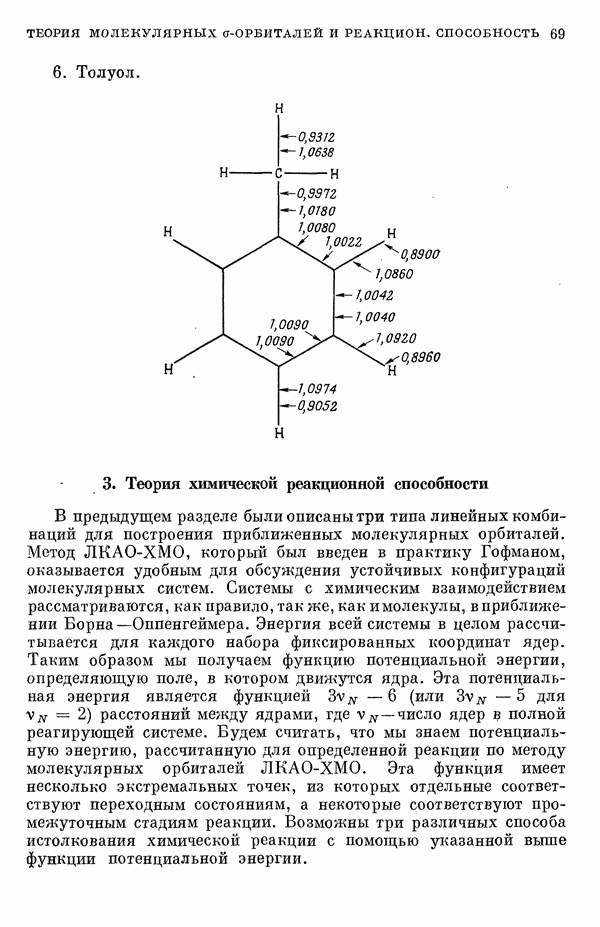
Примеры: Полная плотность а-электронов на каждой валентной атомной орбитали


(кликните для просмотра скана)
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие редакторов русского издания
- Из предисловия редактора английского издания
- Часть 1. Насыщенные соединения
- 1-1. Современное состояние теории электронной структуры молекул
- 2. Одно- и двухэлектронные системы
- 3. Предварительные замечания для многоэлектронных систем
- 4. Задачи для многоэлектронных систем
- 5. Применение теории
- 6. Заключение
- 1-2. Химическое приложение теории молекулярных орбиталей. Галогениды инертных газов
- 2. Модель электронных корреляций
- 3. Модель молекулярных орбиталей
- 4. Модель валентных связей
- 5. Интерпретация физических свойств
- 6. Возбужденные электронные состояния
- 7. Обсуждение теоретических моделей
- 1-3. Теория молекулярных «сигма»-орбиталей и реакционная способность
- 2. Молекулярные «сигма»-орбитали
- 3. Теория химической реакционной способности
- 4. Делокализация электронов в переходном состоянии
- 5. Простая интерпретация реакционной способности насыщенных соединений
- 6. Заключение
- 1-4. Локализованные ССП-орбитали в атомах и молекулах
- 2. Различные возможности в выборе хартри-фоковских орбиталей
- 3. Конкретный выбор хартри-фоковских орбиталей
- 4. Канонические ССП-орбитали
- 5. Внешне локализованные ССП-орбитали
- 6. Внутренне локализованные ССП-орбитали
- 7. Выбор функции разделения
- 8. Построение локализованных орбиталей из произвольной системы ССП-орбиталей
- 9. Локализованные орбитали и симметрия молекул
- 10. Локализованные орбитали при отсутствии симметрии
- 11. Локализованные молекулярные орбитали в системах с делокализованными электронами
- 1-5. Интегральная теорема Гельмана—Фейнмана. Барьеры для внутреннего вращения и изоэлектронные процессы
- 2. Барьеры для внутреннего вращения
- 3. Изоэлектронные процессы
- Чаешь II. «пи»-Электронные системы
- II-1. Общий обзор методов и проблем теории «пи»-электронов
- 2. «пи»-Электронные методы
- 3. Нерешенные вопросы теории «пи»-электронов
- II-2. Трехмерные и одномерные молекулярные орбитали свободных электронов
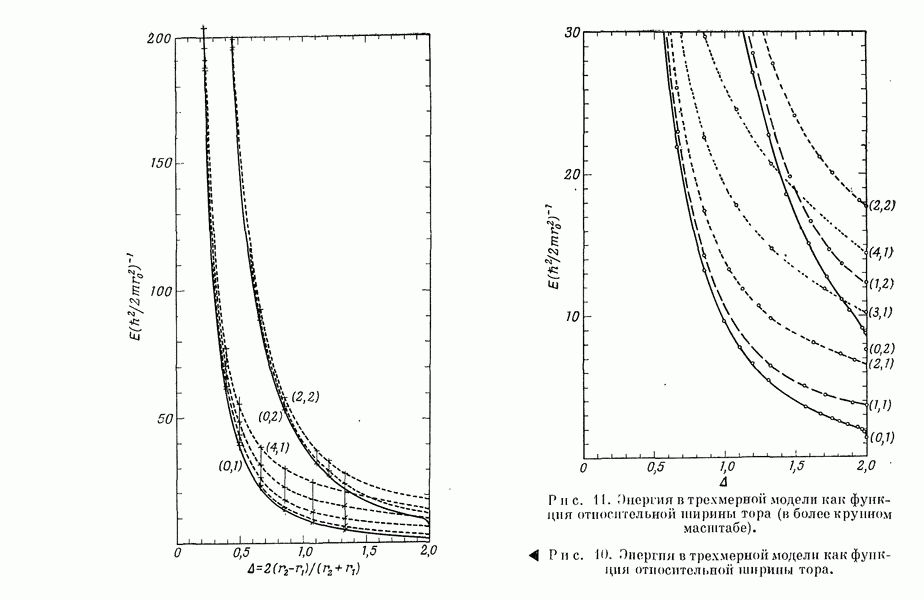
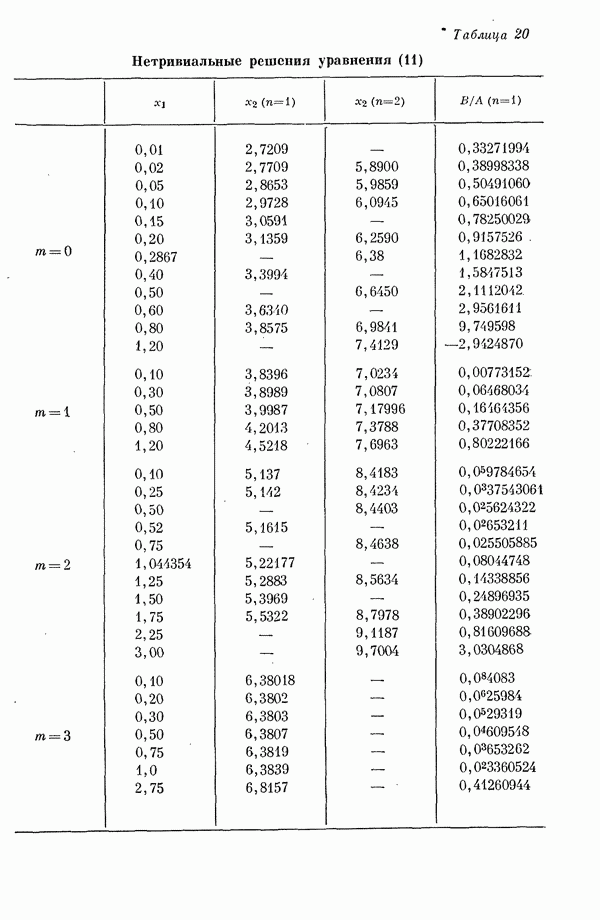
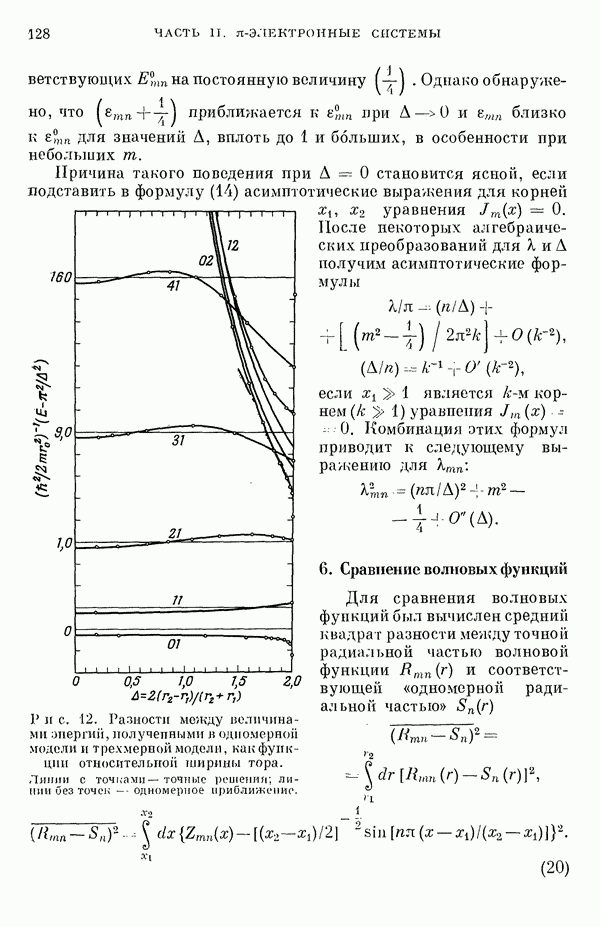
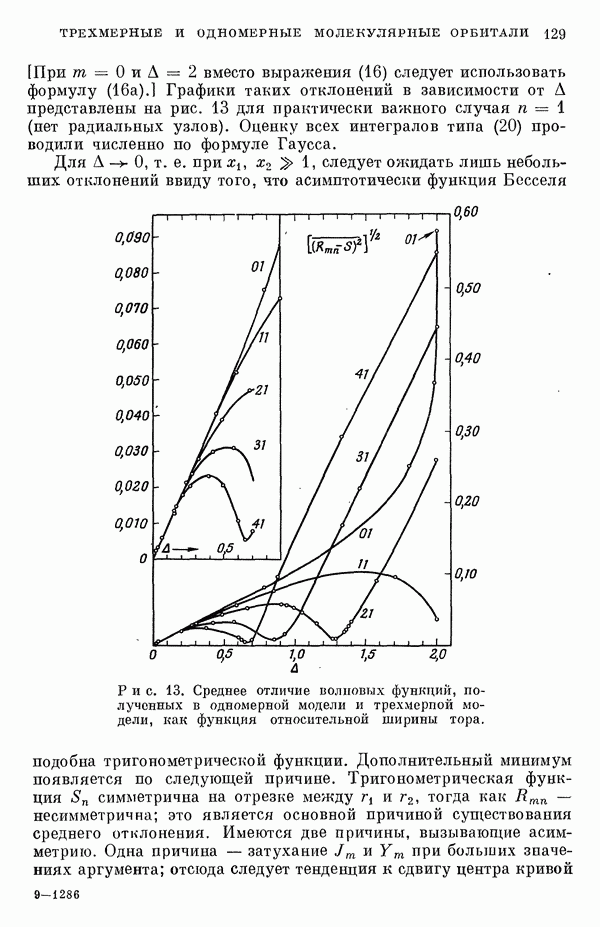
- 3. Определение собственных значений как функций А
- II-3. Теория самосогласованного поля для открытых оболочек и применение ее к «пи»-электронным системам
- 2. Уравнения в методе ССП для систем с замкнутыми оболочками. Теорема Бриллюэна
- 3. Условия самосогласования для систем с одной открытой оболочкой, находящихся в дублетных состояниях
- 4. Условия самосогласования для систем, находящихся в триплетных состояниях с двумя открытыми оболочками
- 5. Энергии низших триплетных возбужденных состояний для некоторых четных альтернантных углеводородов, вычисленные с различной степенью самосогласования
- II-4. Перенос заряда и ион-радикалы
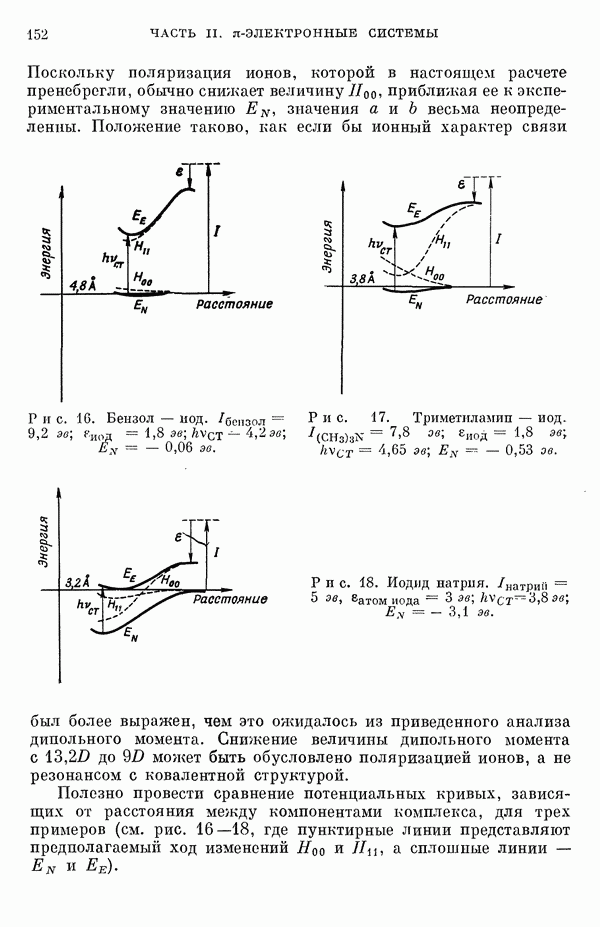
- 3. Слабосвязанные и полунонные комплексы: бензол — иод и триметиламин — иод
- 4. Ионные соединения: иодид натрия
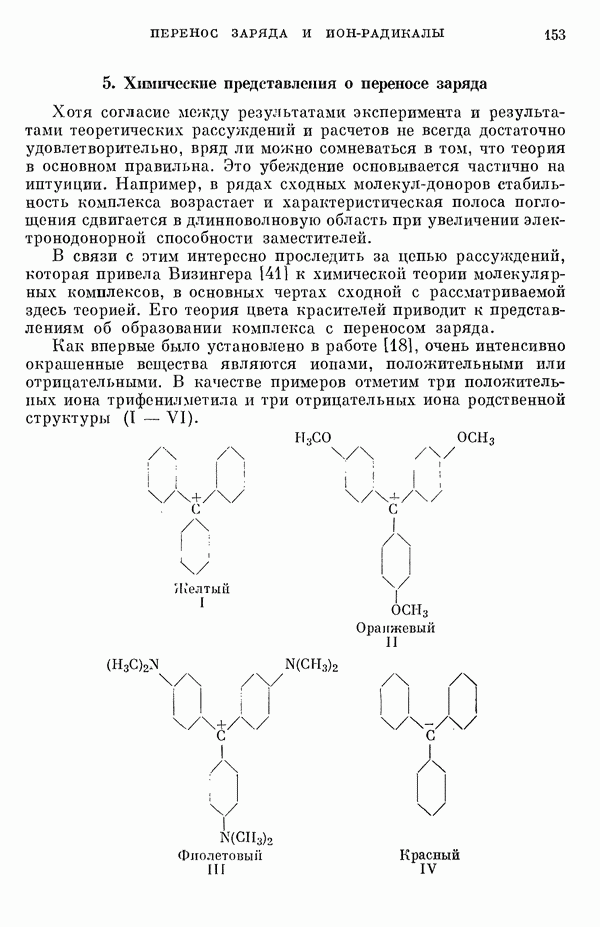
- 5. Химические представления о переносе заряда
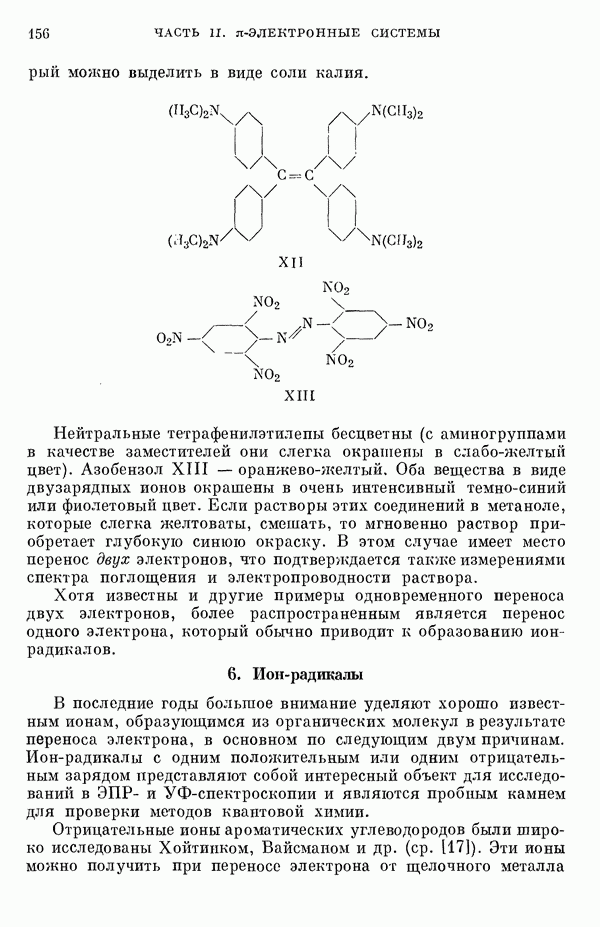
- 6. Ион-радикалы
- 7. Фотоионизация
- II-5. Некоторые свойства «пи»-ионов и триплетных состояний
- 2. Ограниченный метод Хартри — Фока
- 3. Неограниченный метод Хартри — Фока
- 4. Энергии и плотности заряда
- 5. Трансформационные свойства орбиталей
- 6. Спиновые свойства функции
- 7. Расщепление триплетных состояний в нулевом поле
- 8. Заключение
- II-6. Критическое обсуждение «пи»-электронных теорий
- II-6A. ПРЕДЕЛЫ ПРИМЕНИМОСТИ МЕТОДОВ ТИПА МЕТОДОВ ХЮККЕЛЯ И ПАРИЗЕРА — ПАРРА
- II-6Б. БАЗИСНЫЕ ОРБИТАЛИ И ПРИБЛИЖЕНИЕ НУЛЕВОГО ДИФФЕРЕНЦИАЛЬНОГО ПЕРЕКРЫВАНИЯ
- 2. Разложение по малому параметру
- 3. Преобразование оператора Фока
- 4. Другая формулировка исходных допущений приближения НДП
- II-6B. ЭЛЕКТРОННОЕ РАСПРЕДЕЛЕНИЕ В ГЕТЕРОЦИКЛИЧЕСКИХ МОЛЕКУЛАХ
- 2. Приближения Паризера — Парра и Хюккеля (Полинга — Уэланда)
- 3. Приближение Паризера — Парра
- 4. Влияние перехода к базису ОАО на распределение зарядов «пи»-электронов на атомах
- 5. Сравнение методов Паризера — Парра — Попла и Хюккеля
- 11-6Г. ПОЛУЭМПИРИЧЕСКИЕ ПАРАМЕТРЫ В ТЕОРИИ МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- 2. Одноцентровые интегралы
- 3. Двухцентровые интегралы
- II-6Д. РАСЧЕТ СОСТОЯНИЙ МОЛЕКУЛЫ БЕНЗОЛА С УЧЕТОМ КОНФИГУРАЦИОННОГО ВЗАИМОДЕЙСТВИЯ
- II-6E. «пи»-ЭЛЕКТРОННОЕ ПРИБЛИЖЕНИЕ И ПАРАМЕТРЫ ДЛЯ ИНТЕГРАЛОВ КУЛОНОВСКОГО ОТТАЛКИВАНИЯ
- 2. Параметры, связанные с интегралами кулоновского отталкивания
- Часть III. Молекулы и излучение
- III-1. Взаимодействие света с веществом и теория оптической вращающей способности
- 2. Распространение света в прозрачных средах
- 3. Распространение света в среде большого числа отдельных частиц
- 4. Переход от молекулярной теории к феноменологической теории
- 5. Усреднение по физическим элементам объема
- 6. Усреднение микроскопических уравнений Максвелла
- 7. Определение индуцированных молекулярных моментов
- 8. Определение внутреннего поля
- 9. Статистический вывод волнового уравнения
- 10. Квантовохимические аспекты
- III-2. Две теоремы, применяемые в расчетах оптической активности молекул
- III-3. Дипольные моменты в возбужденных состояниях молекул и влияние внешнего электрического поля на оптическое поглощение молекул в растворе
- 2. Средние вероятности переходов для молекулы с определенной ориентацией
- 3. Локальное электрическое поле в месте расположения молекулы, находящейся в растворе
- 4. Сдвиг волнового числа
- 5. Зависимость момента перехода от поля
- 6. Средние вероятности перехода для молекулы в статистическом ансамбле при наличии электрического поля
- 7. Приложения
- 8. Приложение. Расчет средних вероятностей перехода
- III-4. Энергии синглет-триплетных переходов
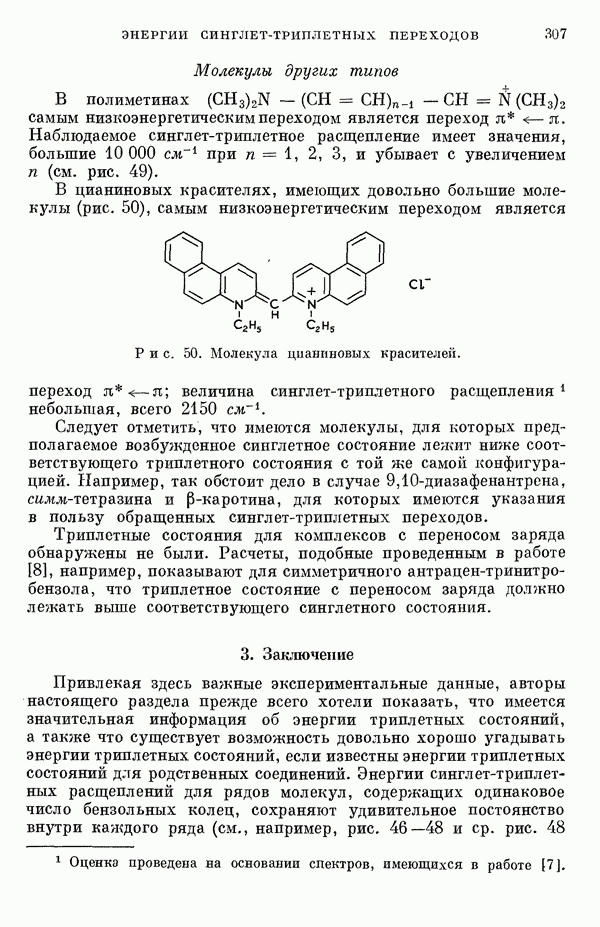
- 2. Обзор теоретических и экспериментальных данных
- 3. Заключение
- III-5. Моменты переходов и анизотропия флуоресценции и фосфоресценции
- 2. Степень анизотропии излучения
- 3. Приложения степени анизотропии
- 4. Обсуждение
- Дополнение. Вариационные оценки энергий сверху и снизу