| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
II-4. Перенос заряда и ион-радикалы
Л. Остерхоф
1. Введение
Представления о переносе заряженных частиц весьма часто встречаются в химии. Так, перенос электронов считают характерной чертой окислительно-восстановительных реакций. Переносом протонов объясняют известные свойства кислот и оснований. Если, следуя взглядам Лыоиса, обобщить эти представления и называть молекулу кислотной при наличии у нее вакансии для электронов и основной при наличии у нее электронной пары, которой она способна делиться с электронодефицитной молекулой, то понятия окисление — восстановление и кислота — основание оказываются взаимоперескающимися и обобщенное понятие переноса заряда становится весьма широким, настолько широким, что мы не можем воспользоваться им в наших последующих рассуждениях.
В настоящем разделе будет рассмотрен только очень специальный вид переноса заряда, с помощью которого объяспяют образование молекулярных комплексов и который может привести к образованию ион-радикалов. Однако даже для данного ограниченного круга вопросов трудно дать полное представление о том, насколько новые исследования в этой области были стимулированы замечательными фундаментальными идеями, высказанными Малликеном в 1950 г. [34], или сделать полный обзор, подобный приведенному в книге Бриглеба [9].
Вместо этого здесь будет дан обзор тех аспектов, с которыми автор достаточно близко знаком и которые кажутся ему наиболее интересными. При этом необходимо подчеркнуть значение тех идей, которые были сформулированы около 35 лет назад Робертом Визингером и на которые, к сожалению, не всегда обращают должное внимание.
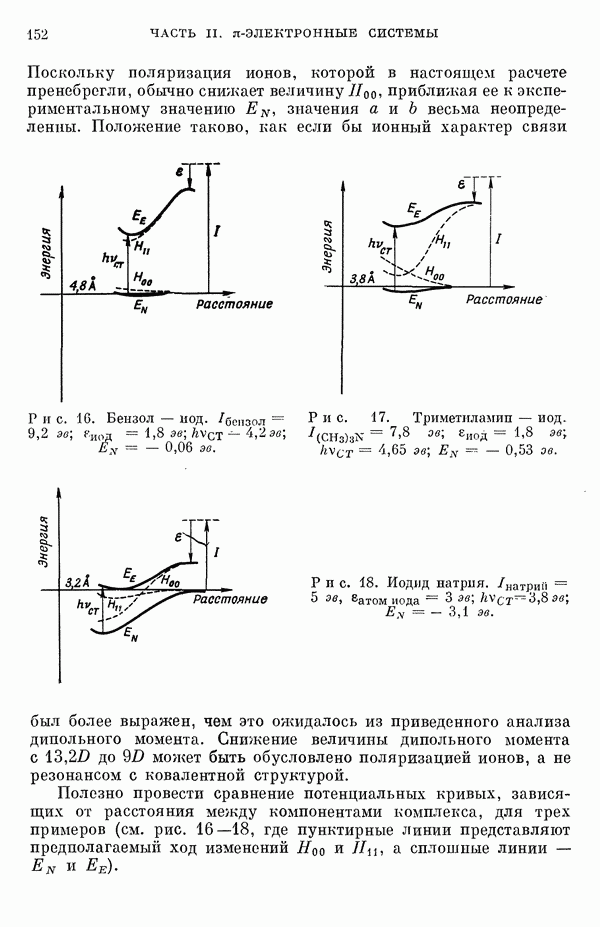
Сопоставим сначала три классических примера переноса заряда: слабосвязанный комплекс бензола и иода, полуионный комплекс триметиламина и иода и ионную молекулу иодида натрия.
Раствор иода в бензоле или иода и бензола вместе в неполярных растворителях обнаруживает следующие черты специфического взаимодействия между молекулами бензола и иода:
а) Фэйрбразер [19] обнаружил неожиданно большую диэлектрическую поляризацию, которую он приписал существованию дипольного момента  молекулы иода (позже Кортюм и Вальц [32] определили значение дипольного момента комплекса бензол — иод, равное
молекулы иода (позже Кортюм и Вальц [32] определили значение дипольного момента комплекса бензол — иод, равное 
б) Бенеши и Хильдебранд [2] наблюдали сильную полосу поглощения в ультрафиолетовой части спектра  , которая появлялась для этих растворов дополнительно лишь к слегка искаженным спектрам чистых соединений.
, которая появлялась для этих растворов дополнительно лишь к слегка искаженным спектрам чистых соединений.
Вскоре после этого были выполнены более обширные эксперименты, на оспове которых Малликен [34] дал объяснение происхождения и свойств этих молекулярных соединений. Основная идея (см. также [7]) состояла в том, чтобы рассматривать одну молекулу (например, бензол) как донор электронов  а другую (иод) — как акцептор электронов
а другую (иод) — как акцептор электронов  и две вместе — как мезомерную структуру
и две вместе — как мезомерную структуру

На языке квантовой химии указанная ситуация описывается волновой функцией основного состояния

и волновой функцией возбужденного состояния

Для слабосвязанных молекул, аналогичных бензолу и иоду,  Это означает, что возбужденное состояние является в основном ионным, тогда как в основном состояпии составляющие структуры почти нейтральны. Следовательно, переход из основного состояния в возбужденное, обусловленный поглощением кванта, заключается в переходе электрона от молекулы-донора к молекуле-акцептору. Поэтому полоса поглощения в дальнем ультрафиолете, появляющаяся дополнительно к известным полосам, которые по-прежнему можно приписывать переходам, локализованным внутри компонентов, получила название полосы «переноса заряда».
Это означает, что возбужденное состояние является в основном ионным, тогда как в основном состояпии составляющие структуры почти нейтральны. Следовательно, переход из основного состояния в возбужденное, обусловленный поглощением кванта, заключается в переходе электрона от молекулы-донора к молекуле-акцептору. Поэтому полоса поглощения в дальнем ультрафиолете, появляющаяся дополнительно к известным полосам, которые по-прежнему можно приписывать переходам, локализованным внутри компонентов, получила название полосы «переноса заряда».
Примесь состояния  к основному состоянию объясняет полярность молекулярного комплекса.
к основному состоянию объясняет полярность молекулярного комплекса.
Взаимодействие между  и
и  приводит к понижению энергии основного состояния ниже уровня
приводит к понижению энергии основного состояния ниже уровня  и таким образом — к стабилизации молекулярного комплекса. (Согласно известному правилу, энергетические уровни основного
и таким образом — к стабилизации молекулярного комплекса. (Согласно известному правилу, энергетические уровни основного  и возбужденного
и возбужденного  состояний при учете указанного взаимодействия стремятся «оттолкнуть» друг друга.)
состояний при учете указанного взаимодействия стремятся «оттолкнуть» друг друга.)
2. Основные формулы
Рассмотрим существенные для нас формулы. Поставим задачу определить в волновой функции типа

коэффициенты Яиц вариационным методом, который состоит в том, чтобы сделать среднее значение энергии

стационарным по отношению к вариациям  Рассматривая только вариации
Рассматривая только вариации  , известным способом получаем секулярные уравнения
, известным способом получаем секулярные уравнения

Как обычно,  Имеем два решения
Имеем два решения  которые мы обозначим следующим образом:
которые мы обозначим следующим образом:

Из условия ортогональности двух волновых функций и условий нормировки получаем

Далее из уравнения (5) следует, что

Частота полосы «переноса заряда»  связана с разностью энергий
связана с разностью энергий  обычным соотношением
обычным соотношением

Из уравнений  находим
находим

причем  определяет энергетическую устойчивость комплекса. Она равна
определяет энергетическую устойчивость комплекса. Она равна  — изменению энтальпии при его образовании, если уровень энергии для разделенных компонентов считать равным нулю. Во многих случаях определены как
— изменению энтальпии при его образовании, если уровень энергии для разделенных компонентов считать равным нулю. Во многих случаях определены как  так и
так и  [2, 26, 27]. Тем не менее величины
[2, 26, 27]. Тем не менее величины  и
и  нельзя определить из уравпепий (9) и (10) до тех пор, пока неизвестны значения
нельзя определить из уравпепий (9) и (10) до тех пор, пока неизвестны значения  и
и  Последние значения очень часто могут быть получены из величины дипольного момента который в данной области теории является существенной характеристикой. Диполъный момент комплекса дается следующим выражением:
Последние значения очень часто могут быть получены из величины дипольного момента который в данной области теории является существенной характеристикой. Диполъный момент комплекса дается следующим выражением:

где

Теперь, по-видимому, полезно ввести орбитали для представления  Если имеет место перенос электрона с орбитали
Если имеет место перенос электрона с орбитали  молекулы-донора на орбиталь А молекулы-акцептора, то соответствующие части
молекулы-донора на орбиталь А молекулы-акцептора, то соответствующие части  можно записать в виде
можно записать в виде

где

Для дипольных моментов, содержащихся в выражении  получаем следующие представления: диполъный момент несвязанного комплекса
получаем следующие представления: диполъный момент несвязанного комплекса  по-видимому, равен векторной сумме дипольных моментов компонентов. Его можно рассматривать как сумму постоянной части
по-видимому, равен векторной сумме дипольных моментов компонентов. Его можно рассматривать как сумму постоянной части  которая остается неизменной при образовании комплекса, и величины
которая остается неизменной при образовании комплекса, и величины  обусловленной вкладом электронов, находящихся на
обусловленной вкладом электронов, находящихся на  -орбиталях. Для
-орбиталях. Для  имеем
имеем

Для удобства введем обозначение  Подстановка этих выражений в формулу (11) приводит после перегруппировки членов к следующему выражению:
Подстановка этих выражений в формулу (11) приводит после перегруппировки членов к следующему выражению:

Поступая аналогично, находим

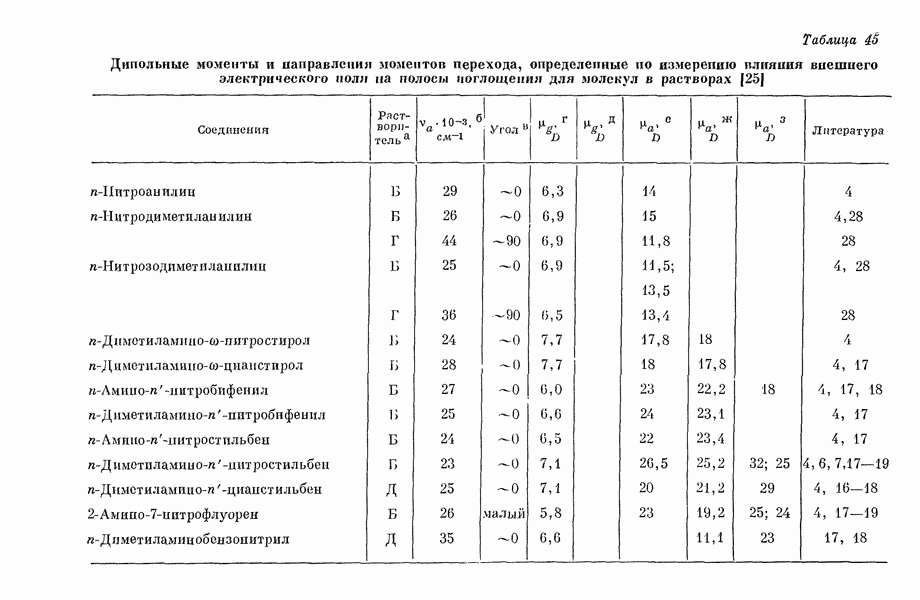
Величину дипольного момента  можно получить по величине диэлектрической проницаемости. Иногда можно определить дипольный момент возбужденного состояния, если полоса «переноса заряда» наблюдается при флюоресценции. При этом в принципе возможно применить два метода. В одном методе используется зависимость длины волны флюоресценции от полярности растворителя, в другом — влияние сильного электрического поля на поляризацию света. Эти методы более детально будут освещены в разд. III-3 т. 1 и разд. II-5 т. 2.
можно получить по величине диэлектрической проницаемости. Иногда можно определить дипольный момент возбужденного состояния, если полоса «переноса заряда» наблюдается при флюоресценции. При этом в принципе возможно применить два метода. В одном методе используется зависимость длины волны флюоресценции от полярности растворителя, в другом — влияние сильного электрического поля на поляризацию света. Эти методы более детально будут освещены в разд. III-3 т. 1 и разд. II-5 т. 2.
Дипольпый момент перехода можно получить из величины площади под кривой поглощения, которая пропорциональна силе осциллятора

Таким образом, для проверки применимости модели можно использовать обширные экспериментальные данные.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие редакторов русского издания
- Из предисловия редактора английского издания
- Часть 1. Насыщенные соединения
- 1-1. Современное состояние теории электронной структуры молекул
- 2. Одно- и двухэлектронные системы
- 3. Предварительные замечания для многоэлектронных систем
- 4. Задачи для многоэлектронных систем
- 5. Применение теории
- 6. Заключение
- 1-2. Химическое приложение теории молекулярных орбиталей. Галогениды инертных газов
- 2. Модель электронных корреляций
- 3. Модель молекулярных орбиталей
- 4. Модель валентных связей
- 5. Интерпретация физических свойств
- 6. Возбужденные электронные состояния
- 7. Обсуждение теоретических моделей
- 1-3. Теория молекулярных «сигма»-орбиталей и реакционная способность
- 2. Молекулярные «сигма»-орбитали
- 3. Теория химической реакционной способности
- 4. Делокализация электронов в переходном состоянии
- 5. Простая интерпретация реакционной способности насыщенных соединений
- 6. Заключение
- 1-4. Локализованные ССП-орбитали в атомах и молекулах
- 2. Различные возможности в выборе хартри-фоковских орбиталей
- 3. Конкретный выбор хартри-фоковских орбиталей
- 4. Канонические ССП-орбитали
- 5. Внешне локализованные ССП-орбитали
- 6. Внутренне локализованные ССП-орбитали
- 7. Выбор функции разделения
- 8. Построение локализованных орбиталей из произвольной системы ССП-орбиталей
- 9. Локализованные орбитали и симметрия молекул
- 10. Локализованные орбитали при отсутствии симметрии
- 11. Локализованные молекулярные орбитали в системах с делокализованными электронами
- 1-5. Интегральная теорема Гельмана—Фейнмана. Барьеры для внутреннего вращения и изоэлектронные процессы
- 2. Барьеры для внутреннего вращения
- 3. Изоэлектронные процессы
- Чаешь II. «пи»-Электронные системы
- II-1. Общий обзор методов и проблем теории «пи»-электронов
- 2. «пи»-Электронные методы
- 3. Нерешенные вопросы теории «пи»-электронов
- II-2. Трехмерные и одномерные молекулярные орбитали свободных электронов
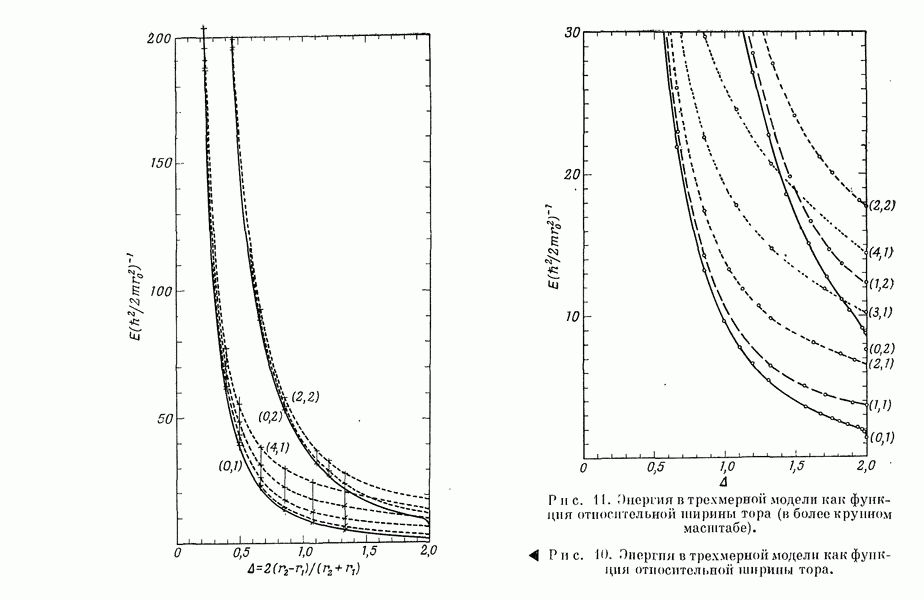
- 3. Определение собственных значений как функций А
- II-3. Теория самосогласованного поля для открытых оболочек и применение ее к «пи»-электронным системам
- 2. Уравнения в методе ССП для систем с замкнутыми оболочками. Теорема Бриллюэна
- 3. Условия самосогласования для систем с одной открытой оболочкой, находящихся в дублетных состояниях
- 4. Условия самосогласования для систем, находящихся в триплетных состояниях с двумя открытыми оболочками
- 5. Энергии низших триплетных возбужденных состояний для некоторых четных альтернантных углеводородов, вычисленные с различной степенью самосогласования
- II-4. Перенос заряда и ион-радикалы
- 3. Слабосвязанные и полунонные комплексы: бензол — иод и триметиламин — иод
- 4. Ионные соединения: иодид натрия
- 5. Химические представления о переносе заряда
- 6. Ион-радикалы
- 7. Фотоионизация
- II-5. Некоторые свойства «пи»-ионов и триплетных состояний
- 2. Ограниченный метод Хартри — Фока
- 3. Неограниченный метод Хартри — Фока
- 4. Энергии и плотности заряда
- 5. Трансформационные свойства орбиталей
- 6. Спиновые свойства функции
- 7. Расщепление триплетных состояний в нулевом поле
- 8. Заключение
- II-6. Критическое обсуждение «пи»-электронных теорий
- II-6A. ПРЕДЕЛЫ ПРИМЕНИМОСТИ МЕТОДОВ ТИПА МЕТОДОВ ХЮККЕЛЯ И ПАРИЗЕРА — ПАРРА
- II-6Б. БАЗИСНЫЕ ОРБИТАЛИ И ПРИБЛИЖЕНИЕ НУЛЕВОГО ДИФФЕРЕНЦИАЛЬНОГО ПЕРЕКРЫВАНИЯ
- 2. Разложение по малому параметру
- 3. Преобразование оператора Фока
- 4. Другая формулировка исходных допущений приближения НДП
- II-6B. ЭЛЕКТРОННОЕ РАСПРЕДЕЛЕНИЕ В ГЕТЕРОЦИКЛИЧЕСКИХ МОЛЕКУЛАХ
- 2. Приближения Паризера — Парра и Хюккеля (Полинга — Уэланда)
- 3. Приближение Паризера — Парра
- 4. Влияние перехода к базису ОАО на распределение зарядов «пи»-электронов на атомах
- 5. Сравнение методов Паризера — Парра — Попла и Хюккеля
- 11-6Г. ПОЛУЭМПИРИЧЕСКИЕ ПАРАМЕТРЫ В ТЕОРИИ МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- 2. Одноцентровые интегралы
- 3. Двухцентровые интегралы
- II-6Д. РАСЧЕТ СОСТОЯНИЙ МОЛЕКУЛЫ БЕНЗОЛА С УЧЕТОМ КОНФИГУРАЦИОННОГО ВЗАИМОДЕЙСТВИЯ
- II-6E. «пи»-ЭЛЕКТРОННОЕ ПРИБЛИЖЕНИЕ И ПАРАМЕТРЫ ДЛЯ ИНТЕГРАЛОВ КУЛОНОВСКОГО ОТТАЛКИВАНИЯ
- 2. Параметры, связанные с интегралами кулоновского отталкивания
- Часть III. Молекулы и излучение
- III-1. Взаимодействие света с веществом и теория оптической вращающей способности
- 2. Распространение света в прозрачных средах
- 3. Распространение света в среде большого числа отдельных частиц
- 4. Переход от молекулярной теории к феноменологической теории
- 5. Усреднение по физическим элементам объема
- 6. Усреднение микроскопических уравнений Максвелла
- 7. Определение индуцированных молекулярных моментов
- 8. Определение внутреннего поля
- 9. Статистический вывод волнового уравнения
- 10. Квантовохимические аспекты
- III-2. Две теоремы, применяемые в расчетах оптической активности молекул
- III-3. Дипольные моменты в возбужденных состояниях молекул и влияние внешнего электрического поля на оптическое поглощение молекул в растворе
- 2. Средние вероятности переходов для молекулы с определенной ориентацией
- 3. Локальное электрическое поле в месте расположения молекулы, находящейся в растворе
- 4. Сдвиг волнового числа
- 5. Зависимость момента перехода от поля
- 6. Средние вероятности перехода для молекулы в статистическом ансамбле при наличии электрического поля
- 7. Приложения
- 8. Приложение. Расчет средних вероятностей перехода
- III-4. Энергии синглет-триплетных переходов
- 2. Обзор теоретических и экспериментальных данных
- 3. Заключение
- III-5. Моменты переходов и анизотропия флуоресценции и фосфоресценции
- 2. Степень анизотропии излучения
- 3. Приложения степени анизотропии
- 4. Обсуждение
- Дополнение. Вариационные оценки энергий сверху и снизу