| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
2. Одно- и двухэлектронные системы
Для атома водорода возможно точное решение уравнения (9), в результате которого могут быть найдены водородные орбитали

с собственными значениями энергии

Эти орбитали полезны и при рассмотрении более сложных вопросов. Явный вид  -орбитали, например, таков:
-орбитали, например, таков:

Часто используются водородоподобные орбитали более общего вида. Они являются решениями задачи для одноэлектропной системы, в которой заряд ядра равен  Например,
Например,

Если же радиальные функции  выразить следующим образом:
выразить следующим образом:

то получим так называемые орбитали (или функции) Слэтера. Именно такие одноэлектронные орбитали наиболее часто используются при расчетах многоэлектронных систем.
Для расчета двухэлектронных систем необходимо использовать приближенные методы, или, более точно, методы последовательных приближений, сходящиеся к точным решениям. Методы теории возмущений сыграли в свое время важную роль. Они вновь приобрели свое значепие совсем недавно благодаря существенному прогрессу, достигнутому в работах Далгарно и других, а также появлепию новых экспериментальных методов исследования молекул с помощью магнитного резонанса. Здесь, однако, мы не будем подробно останавливаться на методах теории возмущений.
Для отыскания волновых функций молекул наиболее распространен вариационпый метод. Он базируется на том, что для данной молекулы с данным  при любой волновой функции Ф имеет место неравенство
при любой волновой функции Ф имеет место неравенство

где  — истинная эпергия основного состояния. Задаваясь различными пробными функциями Ф, можно вычислить
— истинная эпергия основного состояния. Задаваясь различными пробными функциями Ф, можно вычислить  повторяя эту процедуру до тех пор, пока не будет найден минимум
повторяя эту процедуру до тех пор, пока не будет найден минимум  Такой подход определяет наилучшее возможное приближение на взятом классе пробных функций; если в этот класс пробных функций включить все возможные функции (удовлетворяющие принципу Паули), то результат должен быть точно равен
Такой подход определяет наилучшее возможное приближение на взятом классе пробных функций; если в этот класс пробных функций включить все возможные функции (удовлетворяющие принципу Паули), то результат должен быть точно равен  а соответствующая волновая функция точно совпадает с
а соответствующая волновая функция точно совпадает с 
Для атома гелия наиболее простой пробной функцией (без учета спиновой части, о которой будет сказано ниже), очевидно, является следующая:

При оптимальном  однако, получается значение
однако, получается значение  превышающее истинное на 35 ккал/молъ. Лучший результат получается, если взять произведение функций в форме
превышающее истинное на 35 ккал/молъ. Лучший результат получается, если взять произведение функций в форме

где на радиальную зависимость  не накладывается никаких ограничений. Это волновая функция Хартри — Фока. Получающееся при этом превышение, которое все еще равно 26 ккал/моль, возникает из-за того, что функция, взятая в виде произведения, исключает из рассмотрения эффекты мгновенного электронного отталкивания. Величина этого превышения называется корреляционной энергией.
не накладывается никаких ограничений. Это волновая функция Хартри — Фока. Получающееся при этом превышение, которое все еще равно 26 ккал/моль, возникает из-за того, что функция, взятая в виде произведения, исключает из рассмотрения эффекты мгновенного электронного отталкивания. Величина этого превышения называется корреляционной энергией.
Точное решение для атома гелия может быть получено тремя методами. Можно сделать вполне определенный выбор подходящих вариационных форм, включающих межэлектронную координату  и обеспечивающих сколь угодно высокую степень точности. Существуют классические расчетные методы решения такой задачи, предложенные Хиллерасом. До высокой точности, как это недавно показал Шер, могут быть доведены также методы теории возмущений. Кроме того, можно использовать метод конфигурационного взаимодействия, причем этот метод наиболее просто обобщается на сложные молекулы. Сущность его заключается в том, что составляются линейные комбинации функций типа
и обеспечивающих сколь угодно высокую степень точности. Существуют классические расчетные методы решения такой задачи, предложенные Хиллерасом. До высокой точности, как это недавно показал Шер, могут быть доведены также методы теории возмущений. Кроме того, можно использовать метод конфигурационного взаимодействия, причем этот метод наиболее просто обобщается на сложные молекулы. Сущность его заключается в том, что составляются линейные комбинации функций типа  с функциями, соответствующими «возбуждению» других атомных орбиталей
с функциями, соответствующими «возбуждению» других атомных орбиталей  например:
например:

При этом в различных функциях надо брать различные значения параметра  , иначе сходимость ряда оказывается очень плохой.
, иначе сходимость ряда оказывается очень плохой.
Для молекулы водорода положение весьма сходно. Вводя зависимость от координаты  можно достигнуть высокой степени точности; это доказано расчетами Джеймса и Кулиджа, а также Колоса и Рутана. Метод конфигурационного взаимодействия представляет собой другой возможный путь расчета. В результате получается снова значение корреляционной энергии, равное
можно достигнуть высокой степени точности; это доказано расчетами Джеймса и Кулиджа, а также Колоса и Рутана. Метод конфигурационного взаимодействия представляет собой другой возможный путь расчета. В результате получается снова значение корреляционной энергии, равное 
Спины электронов в двухэлектронных системах можно учесть с помощью введения специальных множителей в волновые
функции. Для основного синглетпого состояния в приближении Хартри — Фока, например, получаем

где  — обычные одноэлектронные спиновые функции.
— обычные одноэлектронные спиновые функции.
После подстановки выражений вида (16) в уравнение (15) для ожидаемой величины энергии задача нахождения приближенных значений волновых функций сводится, очевидно, по существу лишь к алгебраическим операциям и вычислению интегралов. При этом сразу видно, что для самых сложных молекул интегрирования сведутся к задачам вычисления и оценки интегралов только четырех видов. Если через  обозначить четыре различные атомные орбитали (обычно локализованные на различных ядрах или других центрах), то нам придется иметь дело с вычислением интегралов перекрывания
обозначить четыре различные атомные орбитали (обычно локализованные на различных ядрах или других центрах), то нам придется иметь дело с вычислением интегралов перекрывания  интегралов кинетической энергии
интегралов кинетической энергии  интегралов притяжения ядер
интегралов притяжения ядер  и интегралов взаимного отталкивания электронов
и интегралов взаимного отталкивания электронов  Здесь и далее мы будем считать все орбитали действительными.
Здесь и далее мы будем считать все орбитали действительными.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Предисловие редакторов русского издания
- Из предисловия редактора английского издания
- Часть 1. Насыщенные соединения
- 1-1. Современное состояние теории электронной структуры молекул
- 2. Одно- и двухэлектронные системы
- 3. Предварительные замечания для многоэлектронных систем
- 4. Задачи для многоэлектронных систем
- 5. Применение теории
- 6. Заключение
- 1-2. Химическое приложение теории молекулярных орбиталей. Галогениды инертных газов
- 2. Модель электронных корреляций
- 3. Модель молекулярных орбиталей
- 4. Модель валентных связей
- 5. Интерпретация физических свойств
- 6. Возбужденные электронные состояния
- 7. Обсуждение теоретических моделей
- 1-3. Теория молекулярных «сигма»-орбиталей и реакционная способность
- 2. Молекулярные «сигма»-орбитали
- 3. Теория химической реакционной способности
- 4. Делокализация электронов в переходном состоянии
- 5. Простая интерпретация реакционной способности насыщенных соединений
- 6. Заключение
- 1-4. Локализованные ССП-орбитали в атомах и молекулах
- 2. Различные возможности в выборе хартри-фоковских орбиталей
- 3. Конкретный выбор хартри-фоковских орбиталей
- 4. Канонические ССП-орбитали
- 5. Внешне локализованные ССП-орбитали
- 6. Внутренне локализованные ССП-орбитали
- 7. Выбор функции разделения
- 8. Построение локализованных орбиталей из произвольной системы ССП-орбиталей
- 9. Локализованные орбитали и симметрия молекул
- 10. Локализованные орбитали при отсутствии симметрии
- 11. Локализованные молекулярные орбитали в системах с делокализованными электронами
- 1-5. Интегральная теорема Гельмана—Фейнмана. Барьеры для внутреннего вращения и изоэлектронные процессы
- 2. Барьеры для внутреннего вращения
- 3. Изоэлектронные процессы
- Чаешь II. «пи»-Электронные системы
- II-1. Общий обзор методов и проблем теории «пи»-электронов
- 2. «пи»-Электронные методы
- 3. Нерешенные вопросы теории «пи»-электронов
- II-2. Трехмерные и одномерные молекулярные орбитали свободных электронов
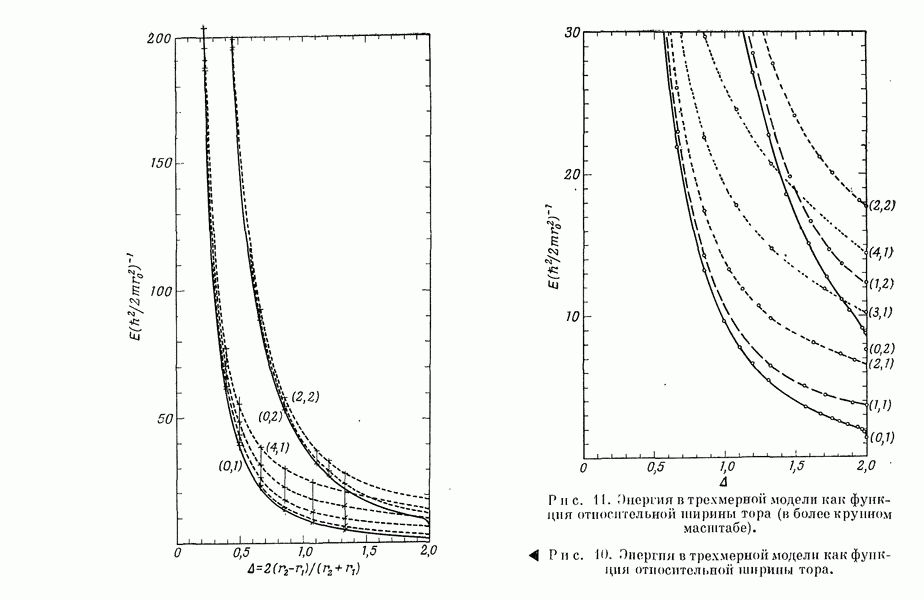
- 3. Определение собственных значений как функций А
- II-3. Теория самосогласованного поля для открытых оболочек и применение ее к «пи»-электронным системам
- 2. Уравнения в методе ССП для систем с замкнутыми оболочками. Теорема Бриллюэна
- 3. Условия самосогласования для систем с одной открытой оболочкой, находящихся в дублетных состояниях
- 4. Условия самосогласования для систем, находящихся в триплетных состояниях с двумя открытыми оболочками
- 5. Энергии низших триплетных возбужденных состояний для некоторых четных альтернантных углеводородов, вычисленные с различной степенью самосогласования
- II-4. Перенос заряда и ион-радикалы
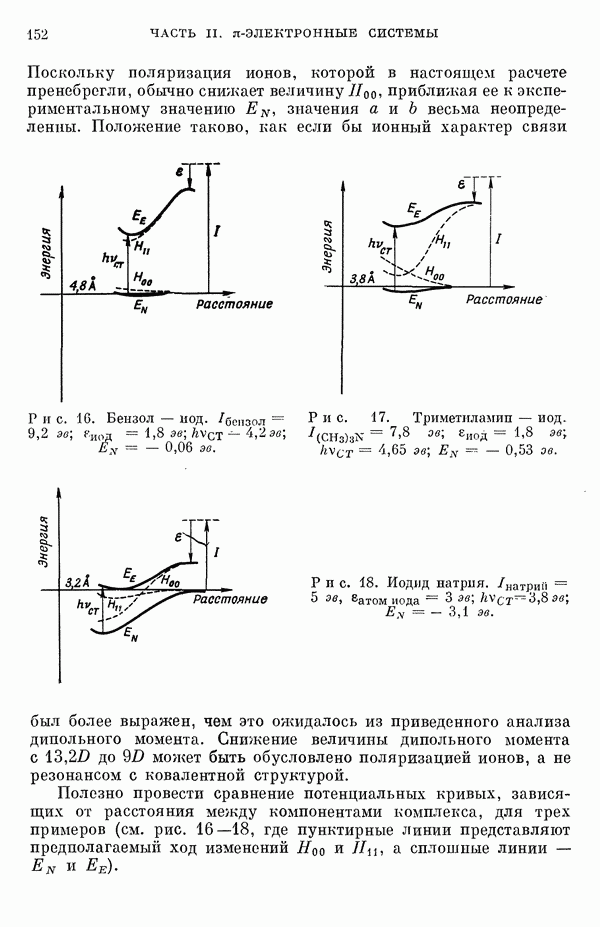
- 3. Слабосвязанные и полунонные комплексы: бензол — иод и триметиламин — иод
- 4. Ионные соединения: иодид натрия
- 5. Химические представления о переносе заряда
- 6. Ион-радикалы
- 7. Фотоионизация
- II-5. Некоторые свойства «пи»-ионов и триплетных состояний
- 2. Ограниченный метод Хартри — Фока
- 3. Неограниченный метод Хартри — Фока
- 4. Энергии и плотности заряда
- 5. Трансформационные свойства орбиталей
- 6. Спиновые свойства функции
- 7. Расщепление триплетных состояний в нулевом поле
- 8. Заключение
- II-6. Критическое обсуждение «пи»-электронных теорий
- II-6A. ПРЕДЕЛЫ ПРИМЕНИМОСТИ МЕТОДОВ ТИПА МЕТОДОВ ХЮККЕЛЯ И ПАРИЗЕРА — ПАРРА
- II-6Б. БАЗИСНЫЕ ОРБИТАЛИ И ПРИБЛИЖЕНИЕ НУЛЕВОГО ДИФФЕРЕНЦИАЛЬНОГО ПЕРЕКРЫВАНИЯ
- 2. Разложение по малому параметру
- 3. Преобразование оператора Фока
- 4. Другая формулировка исходных допущений приближения НДП
- II-6B. ЭЛЕКТРОННОЕ РАСПРЕДЕЛЕНИЕ В ГЕТЕРОЦИКЛИЧЕСКИХ МОЛЕКУЛАХ
- 2. Приближения Паризера — Парра и Хюккеля (Полинга — Уэланда)
- 3. Приближение Паризера — Парра
- 4. Влияние перехода к базису ОАО на распределение зарядов «пи»-электронов на атомах
- 5. Сравнение методов Паризера — Парра — Попла и Хюккеля
- 11-6Г. ПОЛУЭМПИРИЧЕСКИЕ ПАРАМЕТРЫ В ТЕОРИИ МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- 2. Одноцентровые интегралы
- 3. Двухцентровые интегралы
- II-6Д. РАСЧЕТ СОСТОЯНИЙ МОЛЕКУЛЫ БЕНЗОЛА С УЧЕТОМ КОНФИГУРАЦИОННОГО ВЗАИМОДЕЙСТВИЯ
- II-6E. «пи»-ЭЛЕКТРОННОЕ ПРИБЛИЖЕНИЕ И ПАРАМЕТРЫ ДЛЯ ИНТЕГРАЛОВ КУЛОНОВСКОГО ОТТАЛКИВАНИЯ
- 2. Параметры, связанные с интегралами кулоновского отталкивания
- Часть III. Молекулы и излучение
- III-1. Взаимодействие света с веществом и теория оптической вращающей способности
- 2. Распространение света в прозрачных средах
- 3. Распространение света в среде большого числа отдельных частиц
- 4. Переход от молекулярной теории к феноменологической теории
- 5. Усреднение по физическим элементам объема
- 6. Усреднение микроскопических уравнений Максвелла
- 7. Определение индуцированных молекулярных моментов
- 8. Определение внутреннего поля
- 9. Статистический вывод волнового уравнения
- 10. Квантовохимические аспекты
- III-2. Две теоремы, применяемые в расчетах оптической активности молекул
- III-3. Дипольные моменты в возбужденных состояниях молекул и влияние внешнего электрического поля на оптическое поглощение молекул в растворе
- 2. Средние вероятности переходов для молекулы с определенной ориентацией
- 3. Локальное электрическое поле в месте расположения молекулы, находящейся в растворе
- 4. Сдвиг волнового числа
- 5. Зависимость момента перехода от поля
- 6. Средние вероятности перехода для молекулы в статистическом ансамбле при наличии электрического поля
- 7. Приложения
- 8. Приложение. Расчет средних вероятностей перехода
- III-4. Энергии синглет-триплетных переходов
- 2. Обзор теоретических и экспериментальных данных
- 3. Заключение
- III-5. Моменты переходов и анизотропия флуоресценции и фосфоресценции
- 2. Степень анизотропии излучения
- 3. Приложения степени анизотропии
- 4. Обсуждение
- Дополнение. Вариационные оценки энергий сверху и снизу