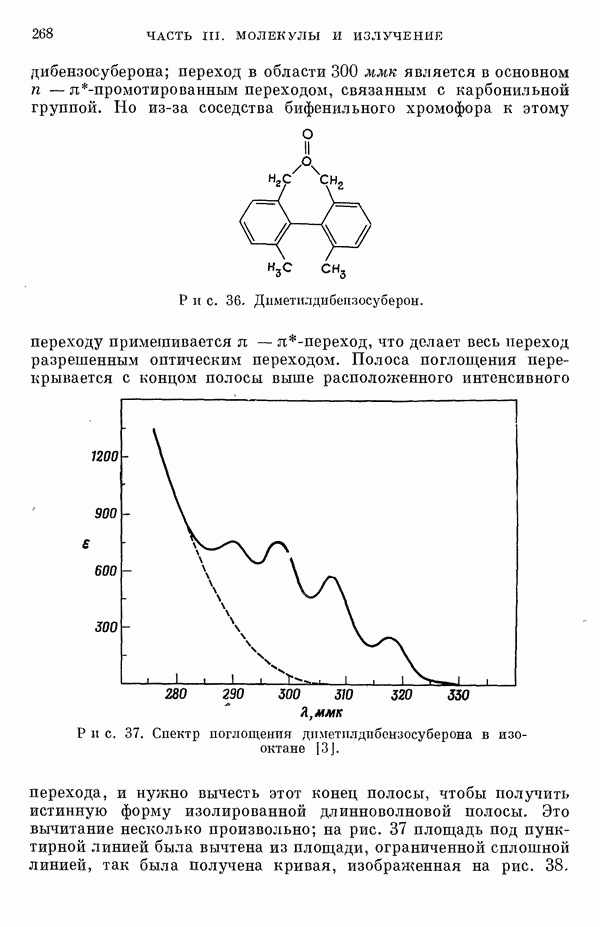
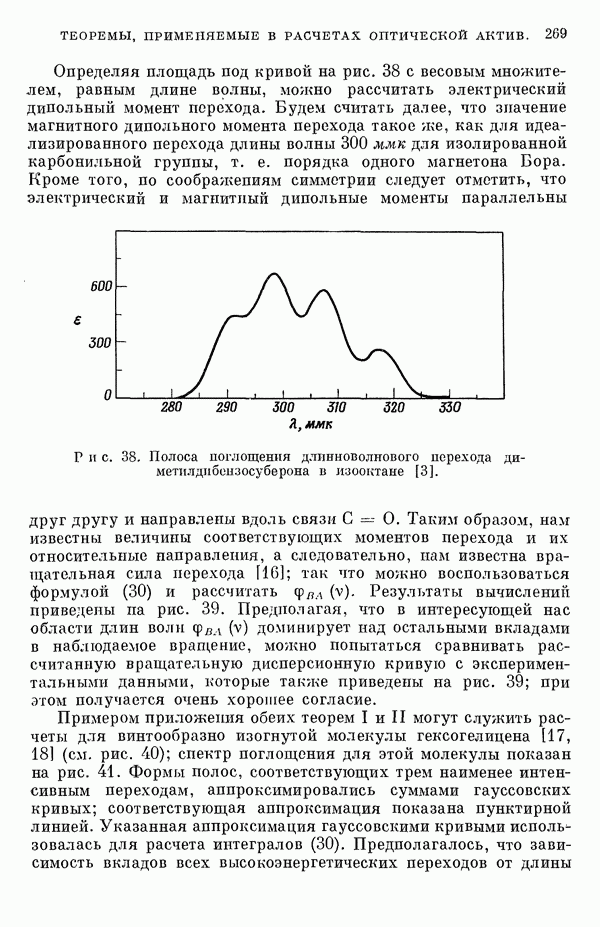
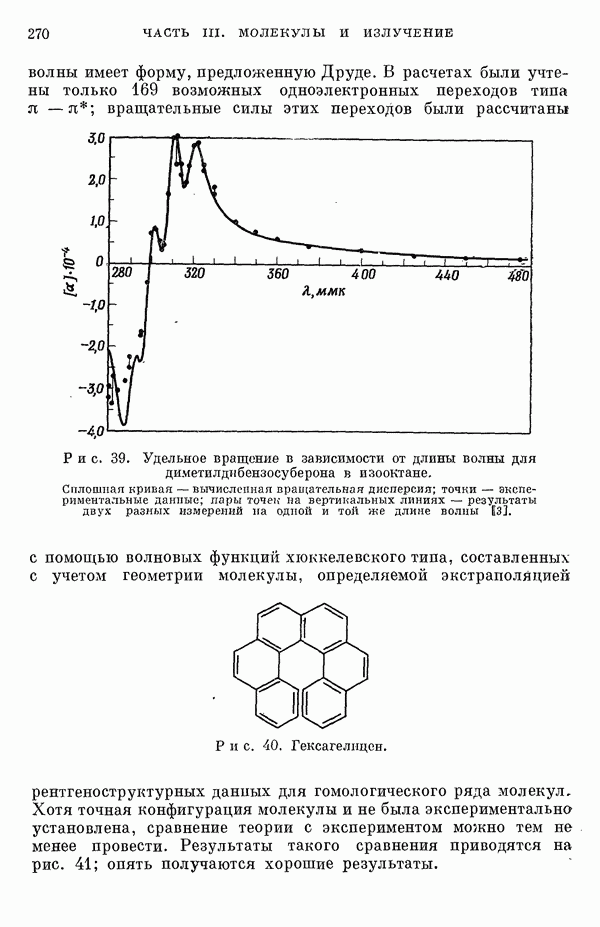
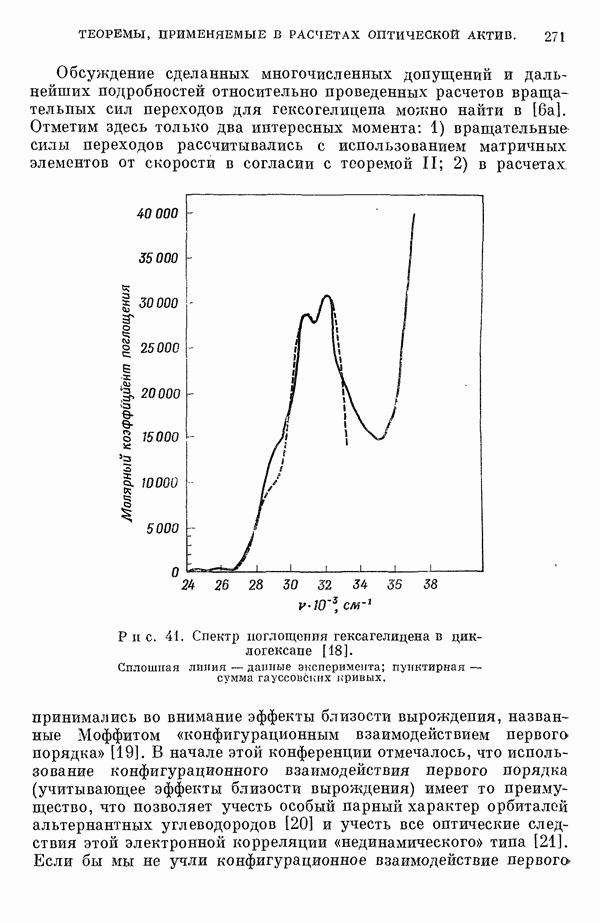
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Из предисловия редактора английского издания
Среди различных способов описания молекулярных орбиталей метод Хартри — Фока является наиболее точным. Волновые функции типа хартри-фоковских молекулярных орбиталей можно использовать для расчета как насыщенных, так и ненасыщенных молекул, стабильных и неустойчивых молекулярных систем. Эти орбитали обычно хорошо воспроизводят распределение электронного заряда и, кроме того, существенно упрощают дальнейшее рассмотрение корреляционных эффектов. То обстоятельство, что расчет достаточно точных хартри-фоковских орбиталей для любой сколько-нибудь большой молекулы еще является делом будущего, не уменьшает общую полезность этого метода. Исходя из хартри-фоковских орбиталей и вводя систематические упрощения, можно получить дальнейшие приближения, такие, как теорию молекулярных орбиталей Хюккеля.
Для расчета основных состояний большинства устойчивых молекул нужно знать хартри-фоковские орбитали замкнутых оболочек. При расчете возбужденных электронных состояний молекул, свободных радикалов, ион-радикалов и в том числе триплетных состояний, а также для предсказания вида поверхностей потенциальной энергии в химической кинетике можно использовать теорию Хартри—Фока о молекулярных орбиталях для открытых оболочек. Первый том книги посвящен в основном теории молекулярных орбиталей. В разд 1-2 и 1-3 первого тома рассматривается применение молекулярных орбиталей (МО) к системам с локализованными и делокализованными а-электронами. Теория МО, главным образом в приближении Хюккеля, используется также для рассмотрения влияния а-электронов на  -электроны в ароматических соединениях.
-электроны в ароматических соединениях.
Для насыщенных молекул преобразование МО волновых функций по Леннард-Джонсу приводит к описанию локализованных связей. Хотя в молекулах, подобных  такое преобразование определяется исключительно свойствами симметрии, в общем случае
такое преобразование определяется исключительно свойствами симметрии, в общем случае  необходимо проводить вычисления, в которых учитывается взаимное влияние электронов. В разд. 1-4 т. 1 обсуждается локализация хартри-фоковских орбиталей, исходя из минимизации обменного взаимодействия (максимизации самоотталкивания). Менее точные
необходимо проводить вычисления, в которых учитывается взаимное влияние электронов. В разд. 1-4 т. 1 обсуждается локализация хартри-фоковских орбиталей, исходя из минимизации обменного взаимодействия (максимизации самоотталкивания). Менее точные  -орбитали, полученные посредством одного из приближений Хюккеля, можно преобразовать в локализованные орбитали с помощью критериев, позволяющих заменить интегралы электронного отталкивания другими интегралами со сходным пространственным поведением [1].
-орбитали, полученные посредством одного из приближений Хюккеля, можно преобразовать в локализованные орбитали с помощью критериев, позволяющих заменить интегралы электронного отталкивания другими интегралами со сходным пространственным поведением [1].
При описании больших молекул, основанном только на представлениях о валентных электронах, необходимо учитывать ортогональность орбиталей валентных электронов внутренним орбиталям. Метод «псевдопотенциала», развитый в физике твердого тела, позволяет учесть условие ортогональности путем введения потенциала, который удерживает валентные электроны за пределами внутренних оболочек. Этот метод может оказаться полезным при построении молекулярных орбиталей больших молекул (см. т. 2, разд. II-1-II-3, III-5).
Для расчета молекулярных фрагментов с  -электронами нужна теория молекулярных орбиталей Хартри — Фока для открытых оболочек. В недавних работах (см., например, [3]) показано, что при учете открытых оболочек в рамках метода МО достигается также улучшение точности расчета
-электронами нужна теория молекулярных орбиталей Хартри — Фока для открытых оболочек. В недавних работах (см., например, [3]) показано, что при учете открытых оболочек в рамках метода МО достигается также улучшение точности расчета  -электронных спектров. Формально одинаковые хартри-фоковские орбитали могут существенно изменяться от состояния к состоянию. Некоторые варианты теории Хартри — Фока для открытых оболочек излагаются в разд. II-3 и II-5 т. 1 и в разд. 1-7 т. 2 [4].
-электронных спектров. Формально одинаковые хартри-фоковские орбитали могут существенно изменяться от состояния к состоянию. Некоторые варианты теории Хартри — Фока для открытых оболочек излагаются в разд. II-3 и II-5 т. 1 и в разд. 1-7 т. 2 [4].
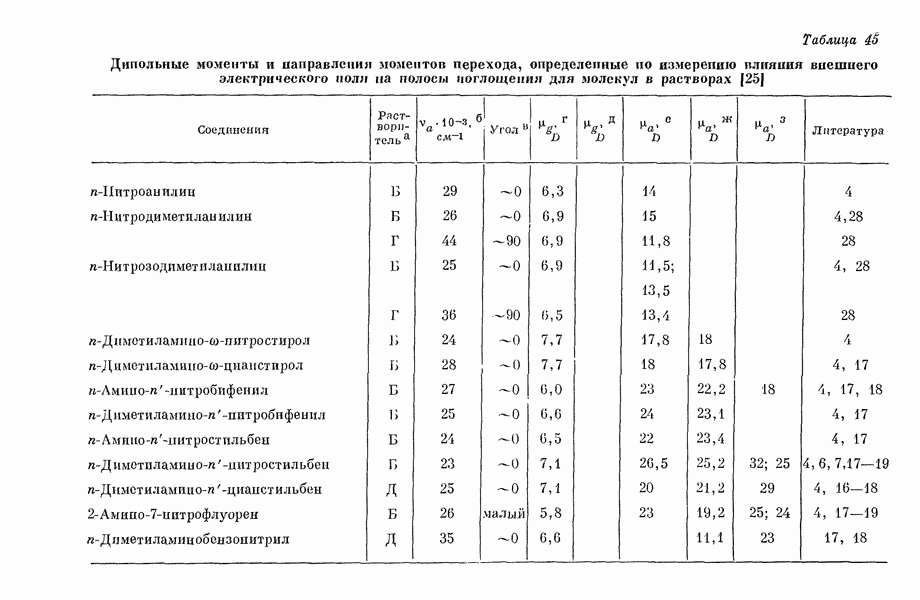
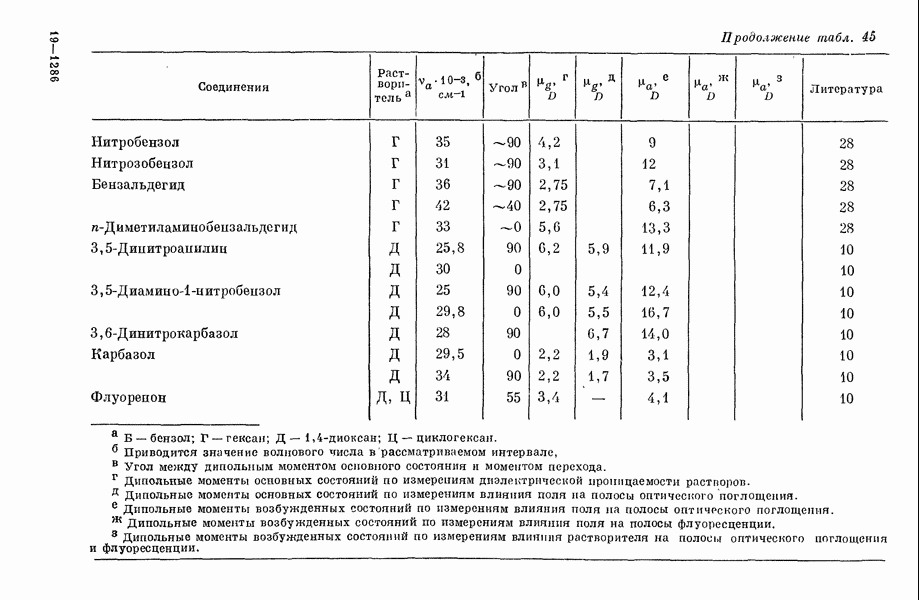
В первом томе (см. разд. II-6A— Е) рассматриваются формальное обоснование и экспериментальное подтверждение теорий, основанных на представлениях о  -электронах; обсуждаются природа n-электронного приближения, предсказания электропных спектров и распределение заряда в гетеромолекулах. Эффекты сольватации рассматриваются в т. 2. В разд. III-4 т. 1 дан обзор экспериментальных данных по синглет-тринлетному разделению и их теоретическое рассмотрение. Экспериментальное определение дипольных моментов органических молекул, находящихся в возбужденных состояниях, обсуждается в разд. III-3 т. 1. Эти величины могут быть использованы для сравнения с результатами расчетов возбужденных состояний по методу МО с открытыми оболочками. Экспериментальные данные приведены для растворов. Кроме того, недавно для газообразного состояния были измерены дипольные моменты сравнительно небольших молекул (подобных формальдегиду), находящихся в возбужденном состоянии.
-электронах; обсуждаются природа n-электронного приближения, предсказания электропных спектров и распределение заряда в гетеромолекулах. Эффекты сольватации рассматриваются в т. 2. В разд. III-4 т. 1 дан обзор экспериментальных данных по синглет-тринлетному разделению и их теоретическое рассмотрение. Экспериментальное определение дипольных моментов органических молекул, находящихся в возбужденных состояниях, обсуждается в разд. III-3 т. 1. Эти величины могут быть использованы для сравнения с результатами расчетов возбужденных состояний по методу МО с открытыми оболочками. Экспериментальные данные приведены для растворов. Кроме того, недавно для газообразного состояния были измерены дипольные моменты сравнительно небольших молекул (подобных формальдегиду), находящихся в возбужденном состоянии.
Окончательное подтверждение теории молекулярных орбиталей может быть получено, кроме проверки экспериментом, только из сравнения орбитальной волновой функции и соответствующей энергии с точными волновой функцией г|) и энергией Е (см. т. 1, разд. II-6E, и т. 2, разд. 1). Если орбитали найдены по теории Хартри—Фока, то остаются неучтенными эффекты корреляции электронов. Корреляция может сдвигать энергетические уровни в электронных спектрах и искажать хартри-фоковские орбитали, но наиболее сильное влияние оказывает она на энергии связен и силы взаимодействия в газах и конденсированных средах. Обзор этих эффектов дан в т. 2. При этом особое внимание уделено случаям, когда корреляция может изменить даже качественную картину, получающуюся, если исходить только из орбиталей. Работы последних лет освещены достаточно подробно 1.
Взаимодействие между электронами и конденсированной средой, а также силы, действующие между молекулами в газе, жидкости или твердом теле, сильно зависят от корреляции. Они рассматриваются в т. 2, разд. 11 и III. Электронные корреляции в металлах и системах бесконечной протяженности обсуждаются
в т. 2, разд. III-4 и III-5. В разд. III-4 т. 2 содержится компактное изложение зонной и хартри-фоковской орбитальной теории металлов. В разд. III-5 т. 2 рассмотрены сплавы жидких щелочных металлов. Общее описание методов теории и их приложений читатель найдет в разд. 1-4, III-4 и III-5 т. 2. В разд. III т. 1 рассматриваются некоторые эффекты взаимодействия света с молекулами и средой.
ЛИТЕРАТУРА
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие редакторов русского издания
- Из предисловия редактора английского издания
- Часть 1. Насыщенные соединения
- 1-1. Современное состояние теории электронной структуры молекул
- 2. Одно- и двухэлектронные системы
- 3. Предварительные замечания для многоэлектронных систем
- 4. Задачи для многоэлектронных систем
- 5. Применение теории
- 6. Заключение
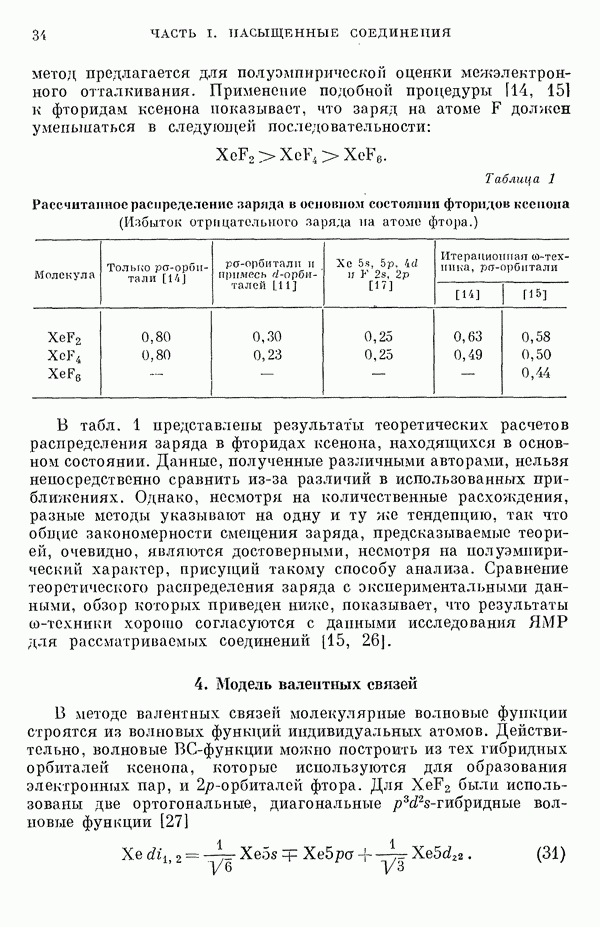
- 1-2. Химическое приложение теории молекулярных орбиталей. Галогениды инертных газов
- 2. Модель электронных корреляций
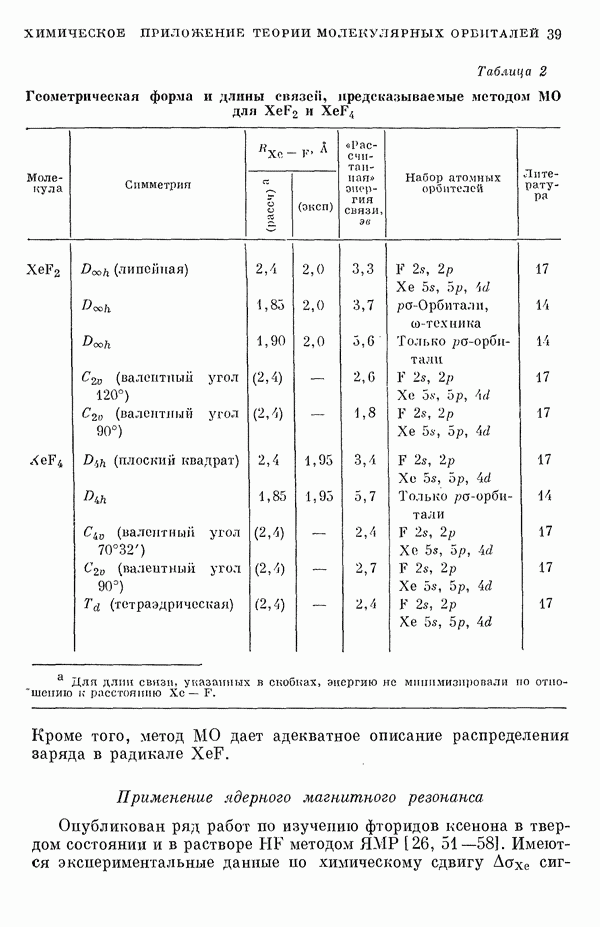
- 3. Модель молекулярных орбиталей
- 4. Модель валентных связей
- 5. Интерпретация физических свойств
- 6. Возбужденные электронные состояния
- 7. Обсуждение теоретических моделей
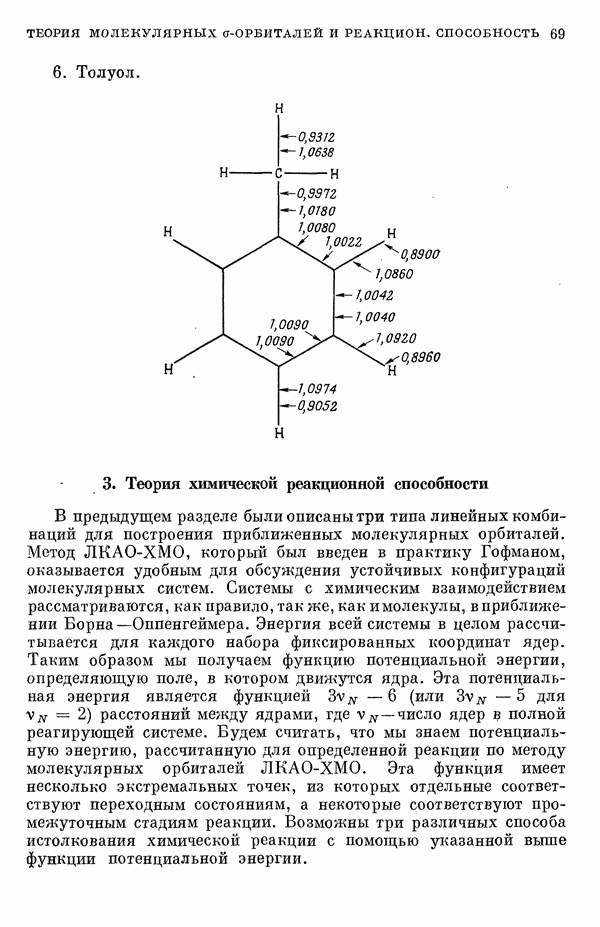
- 1-3. Теория молекулярных «сигма»-орбиталей и реакционная способность
- 2. Молекулярные «сигма»-орбитали
- 3. Теория химической реакционной способности
- 4. Делокализация электронов в переходном состоянии
- 5. Простая интерпретация реакционной способности насыщенных соединений
- 6. Заключение
- 1-4. Локализованные ССП-орбитали в атомах и молекулах
- 2. Различные возможности в выборе хартри-фоковских орбиталей
- 3. Конкретный выбор хартри-фоковских орбиталей
- 4. Канонические ССП-орбитали
- 5. Внешне локализованные ССП-орбитали
- 6. Внутренне локализованные ССП-орбитали
- 7. Выбор функции разделения
- 8. Построение локализованных орбиталей из произвольной системы ССП-орбиталей
- 9. Локализованные орбитали и симметрия молекул
- 10. Локализованные орбитали при отсутствии симметрии
- 11. Локализованные молекулярные орбитали в системах с делокализованными электронами
- 1-5. Интегральная теорема Гельмана—Фейнмана. Барьеры для внутреннего вращения и изоэлектронные процессы
- 2. Барьеры для внутреннего вращения
- 3. Изоэлектронные процессы
- Чаешь II. «пи»-Электронные системы
- II-1. Общий обзор методов и проблем теории «пи»-электронов
- 2. «пи»-Электронные методы
- 3. Нерешенные вопросы теории «пи»-электронов
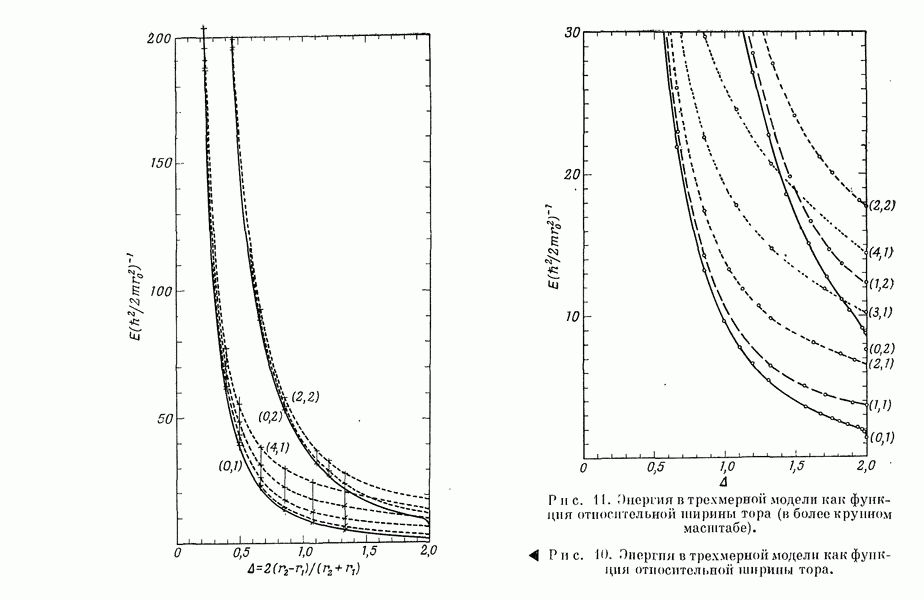
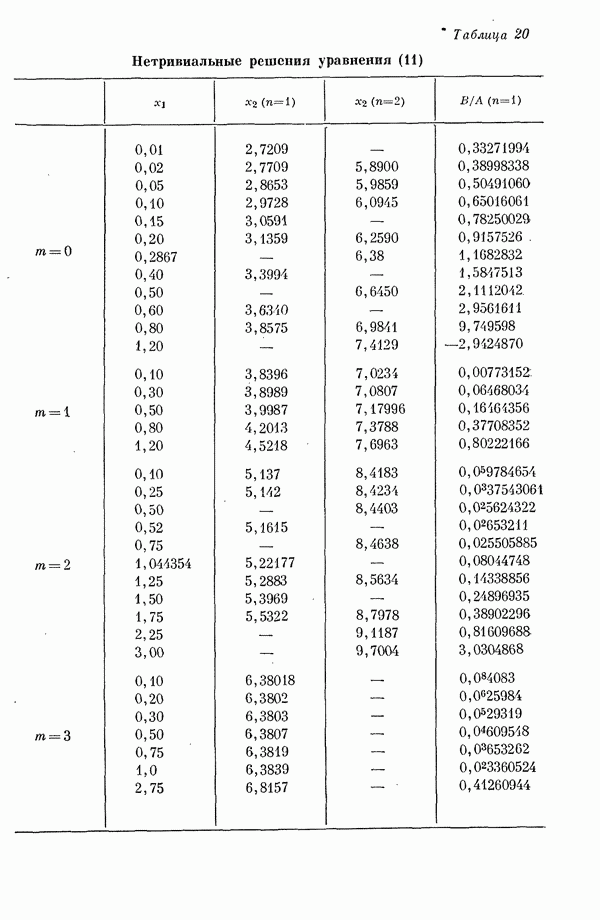
- II-2. Трехмерные и одномерные молекулярные орбитали свободных электронов
- 3. Определение собственных значений как функций А
- II-3. Теория самосогласованного поля для открытых оболочек и применение ее к «пи»-электронным системам
- 2. Уравнения в методе ССП для систем с замкнутыми оболочками. Теорема Бриллюэна
- 3. Условия самосогласования для систем с одной открытой оболочкой, находящихся в дублетных состояниях
- 4. Условия самосогласования для систем, находящихся в триплетных состояниях с двумя открытыми оболочками
- 5. Энергии низших триплетных возбужденных состояний для некоторых четных альтернантных углеводородов, вычисленные с различной степенью самосогласования
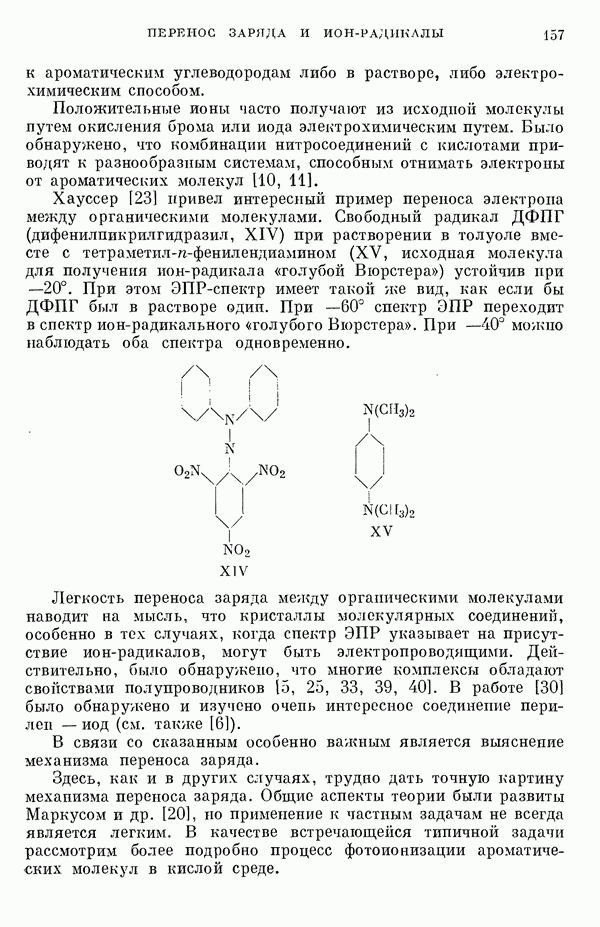
- II-4. Перенос заряда и ион-радикалы
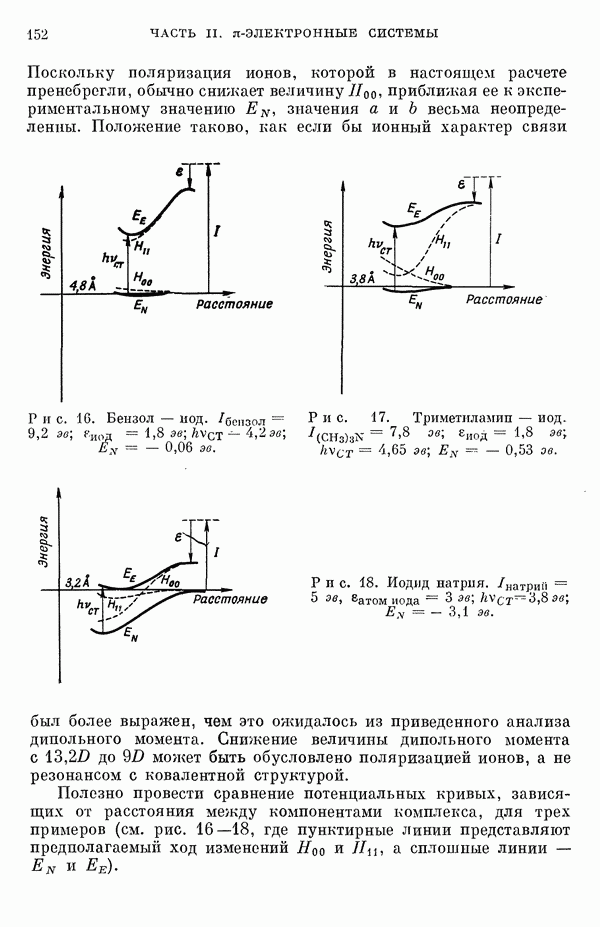
- 3. Слабосвязанные и полунонные комплексы: бензол — иод и триметиламин — иод
- 4. Ионные соединения: иодид натрия
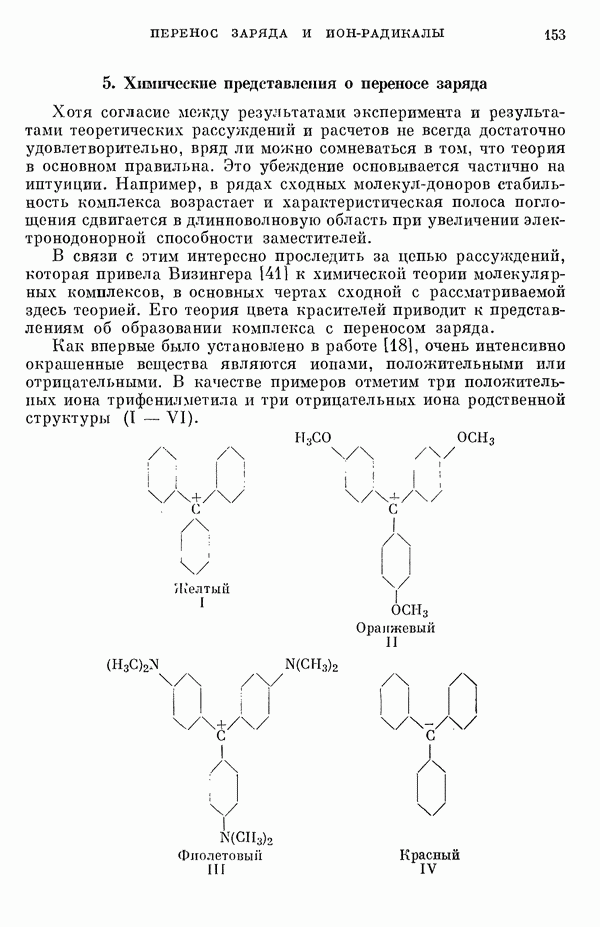
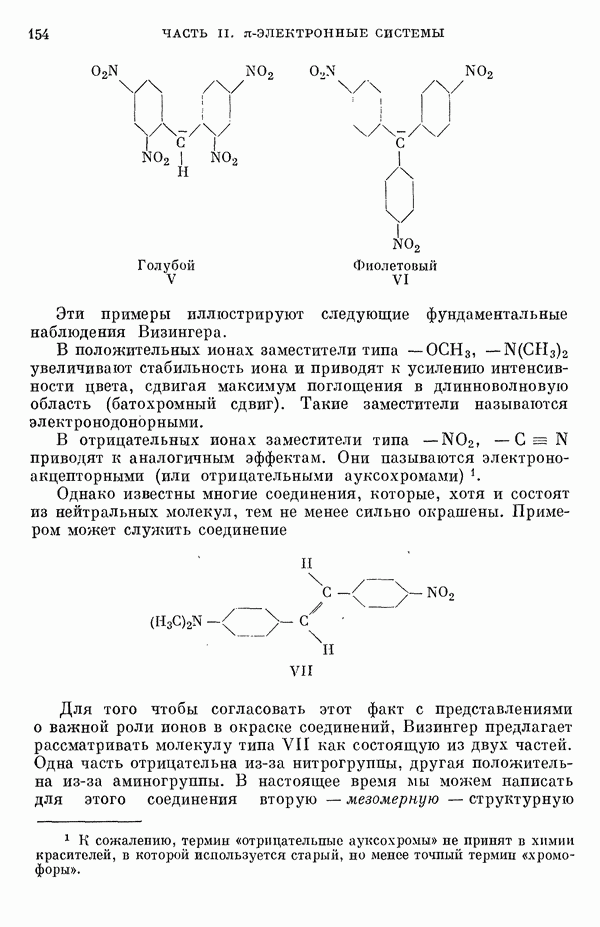
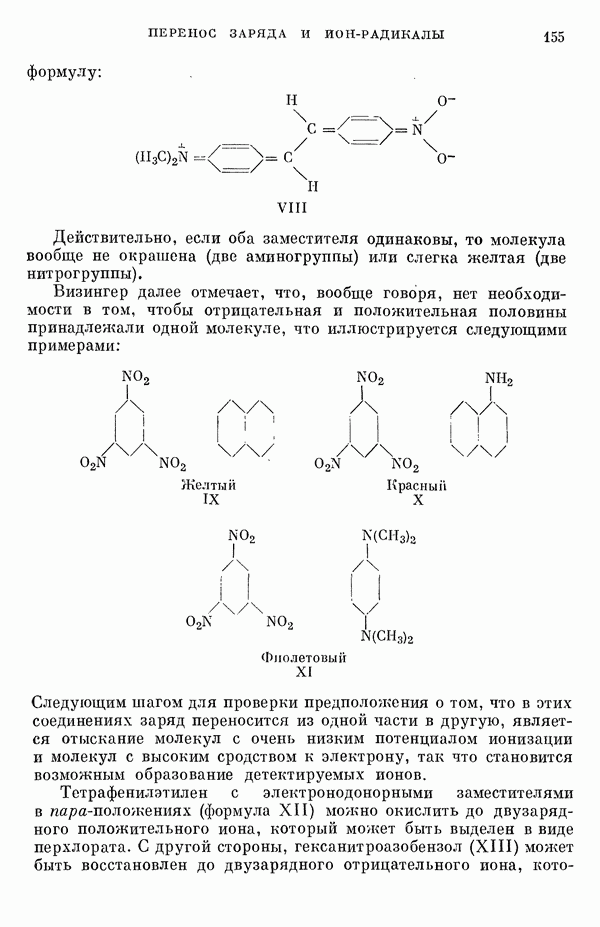
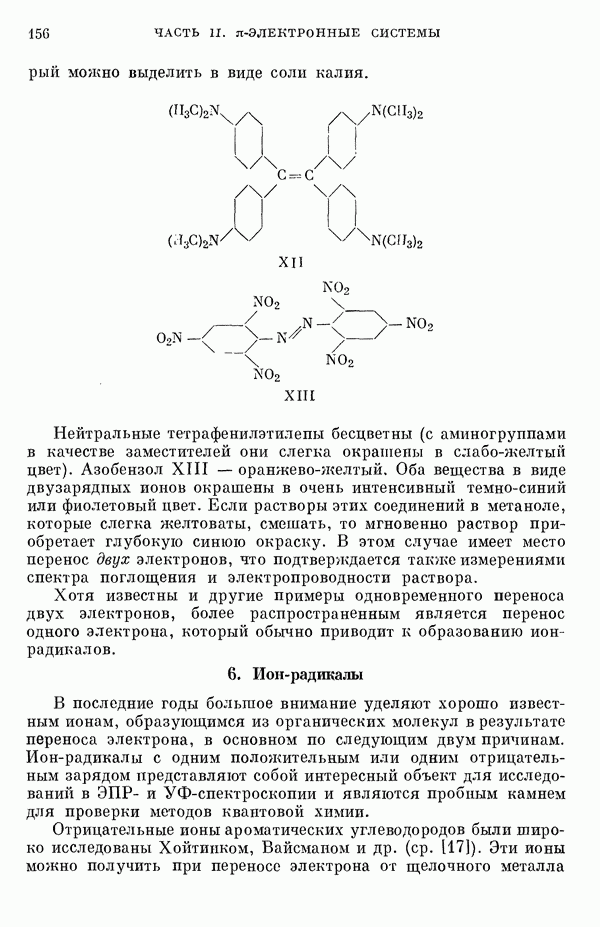
- 5. Химические представления о переносе заряда
- 6. Ион-радикалы
- 7. Фотоионизация
- II-5. Некоторые свойства «пи»-ионов и триплетных состояний
- 2. Ограниченный метод Хартри — Фока
- 3. Неограниченный метод Хартри — Фока
- 4. Энергии и плотности заряда
- 5. Трансформационные свойства орбиталей
- 6. Спиновые свойства функции
- 7. Расщепление триплетных состояний в нулевом поле
- 8. Заключение
- II-6. Критическое обсуждение «пи»-электронных теорий
- II-6A. ПРЕДЕЛЫ ПРИМЕНИМОСТИ МЕТОДОВ ТИПА МЕТОДОВ ХЮККЕЛЯ И ПАРИЗЕРА — ПАРРА
- II-6Б. БАЗИСНЫЕ ОРБИТАЛИ И ПРИБЛИЖЕНИЕ НУЛЕВОГО ДИФФЕРЕНЦИАЛЬНОГО ПЕРЕКРЫВАНИЯ
- 2. Разложение по малому параметру
- 3. Преобразование оператора Фока
- 4. Другая формулировка исходных допущений приближения НДП
- II-6B. ЭЛЕКТРОННОЕ РАСПРЕДЕЛЕНИЕ В ГЕТЕРОЦИКЛИЧЕСКИХ МОЛЕКУЛАХ
- 2. Приближения Паризера — Парра и Хюккеля (Полинга — Уэланда)
- 3. Приближение Паризера — Парра
- 4. Влияние перехода к базису ОАО на распределение зарядов «пи»-электронов на атомах
- 5. Сравнение методов Паризера — Парра — Попла и Хюккеля
- 11-6Г. ПОЛУЭМПИРИЧЕСКИЕ ПАРАМЕТРЫ В ТЕОРИИ МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- 2. Одноцентровые интегралы
- 3. Двухцентровые интегралы
- II-6Д. РАСЧЕТ СОСТОЯНИЙ МОЛЕКУЛЫ БЕНЗОЛА С УЧЕТОМ КОНФИГУРАЦИОННОГО ВЗАИМОДЕЙСТВИЯ
- II-6E. «пи»-ЭЛЕКТРОННОЕ ПРИБЛИЖЕНИЕ И ПАРАМЕТРЫ ДЛЯ ИНТЕГРАЛОВ КУЛОНОВСКОГО ОТТАЛКИВАНИЯ
- 2. Параметры, связанные с интегралами кулоновского отталкивания
- Часть III. Молекулы и излучение
- III-1. Взаимодействие света с веществом и теория оптической вращающей способности
- 2. Распространение света в прозрачных средах
- 3. Распространение света в среде большого числа отдельных частиц
- 4. Переход от молекулярной теории к феноменологической теории
- 5. Усреднение по физическим элементам объема
- 6. Усреднение микроскопических уравнений Максвелла
- 7. Определение индуцированных молекулярных моментов
- 8. Определение внутреннего поля
- 9. Статистический вывод волнового уравнения
- 10. Квантовохимические аспекты
- III-2. Две теоремы, применяемые в расчетах оптической активности молекул
- III-3. Дипольные моменты в возбужденных состояниях молекул и влияние внешнего электрического поля на оптическое поглощение молекул в растворе
- 2. Средние вероятности переходов для молекулы с определенной ориентацией
- 3. Локальное электрическое поле в месте расположения молекулы, находящейся в растворе
- 4. Сдвиг волнового числа
- 5. Зависимость момента перехода от поля
- 6. Средние вероятности перехода для молекулы в статистическом ансамбле при наличии электрического поля
- 7. Приложения
- 8. Приложение. Расчет средних вероятностей перехода
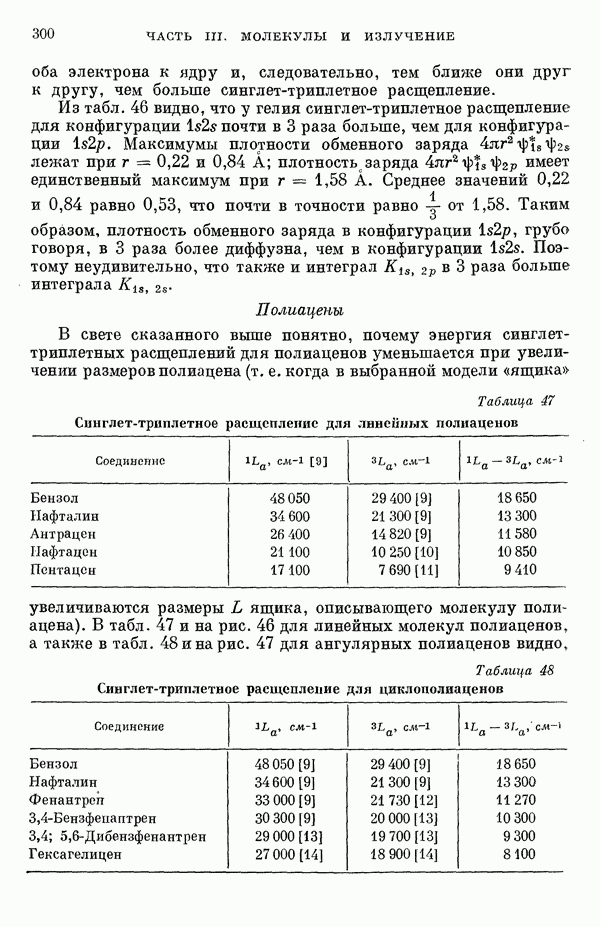
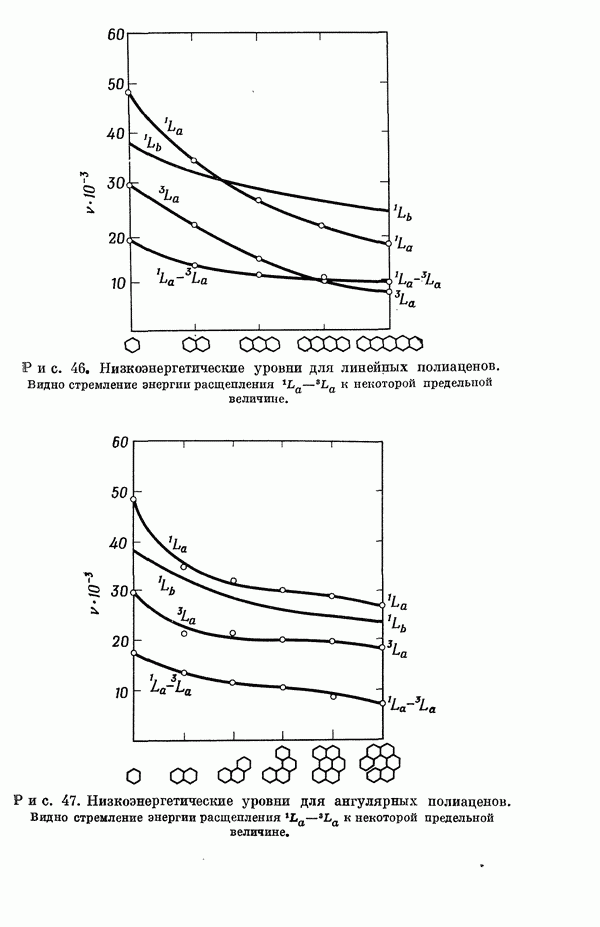
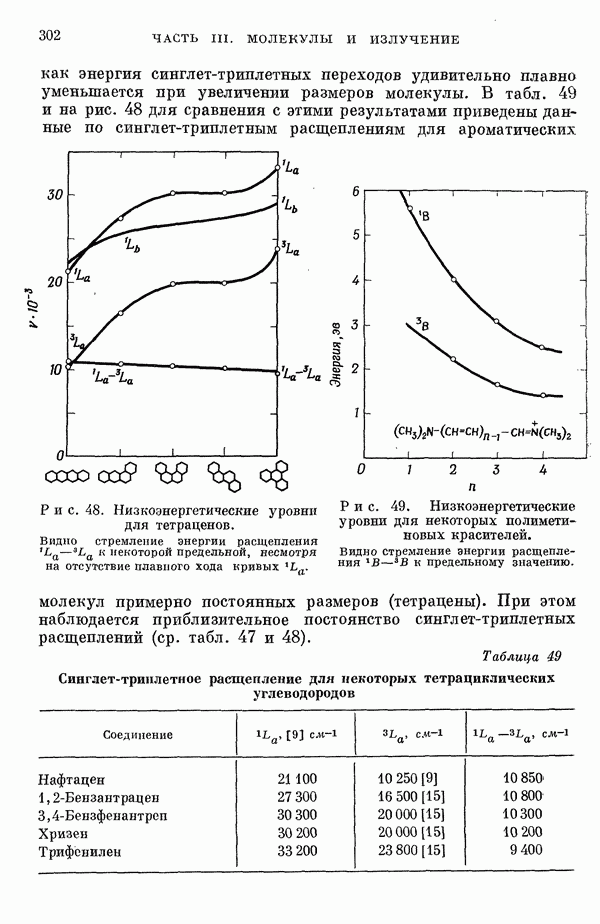
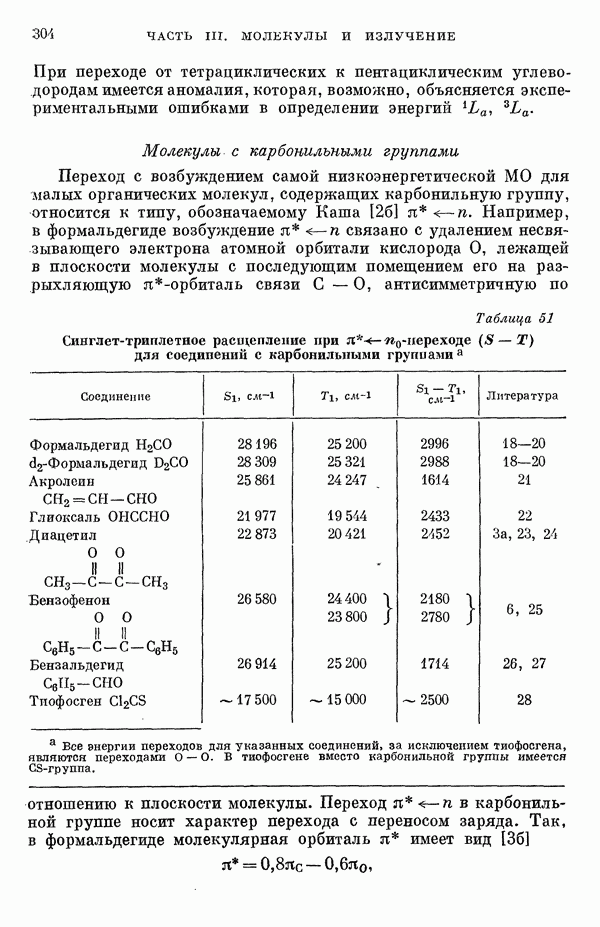
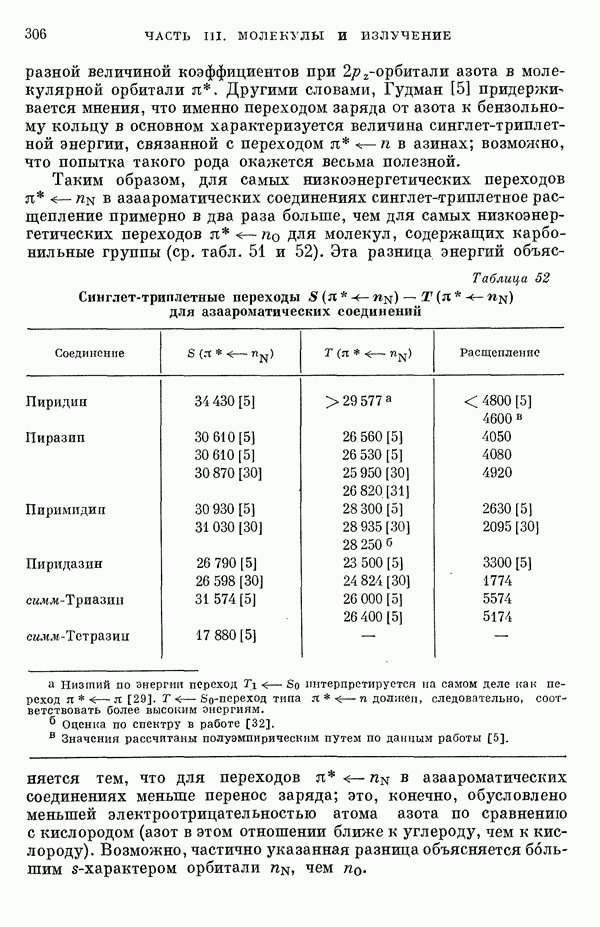
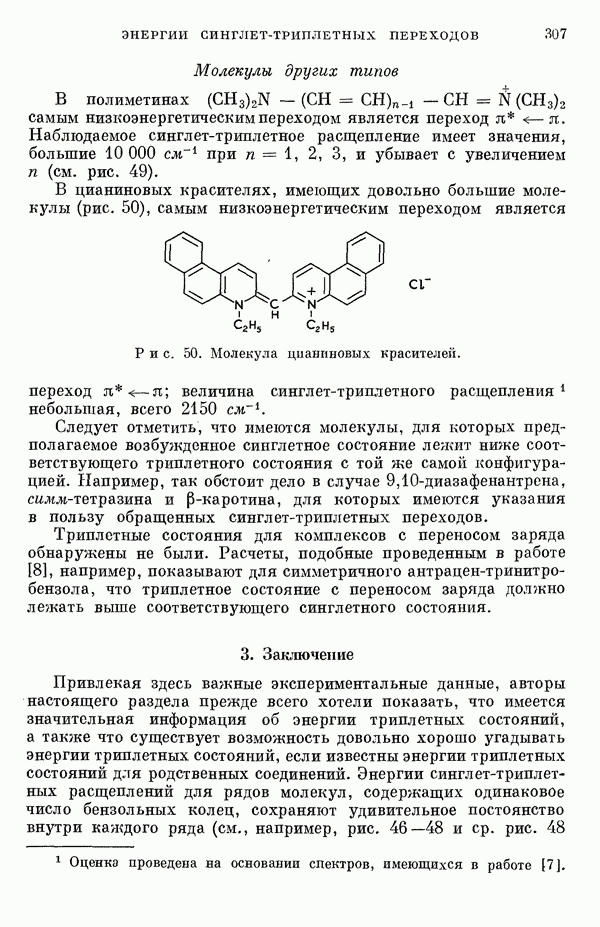
- III-4. Энергии синглет-триплетных переходов
- 2. Обзор теоретических и экспериментальных данных
- 3. Заключение
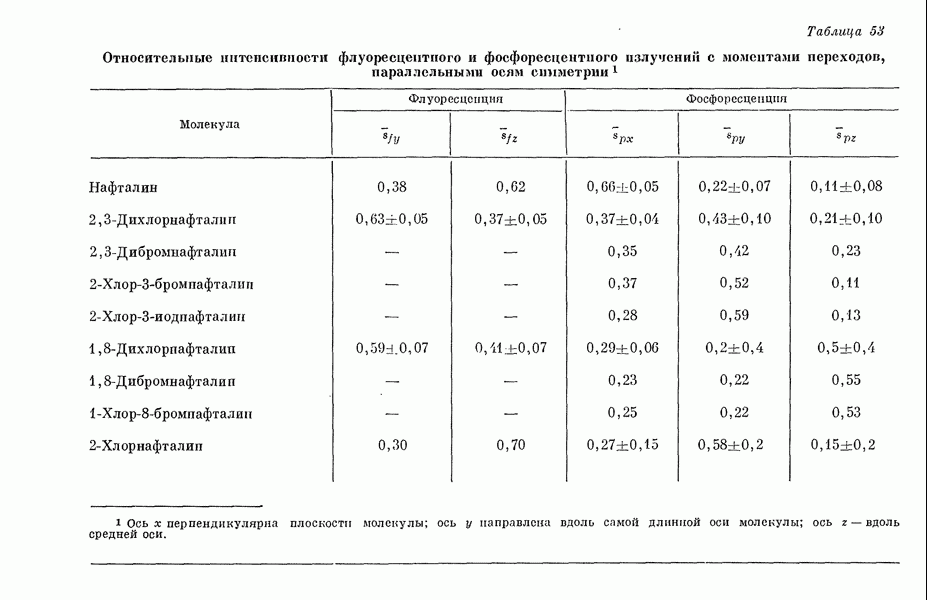
- III-5. Моменты переходов и анизотропия флуоресценции и фосфоресценции
- 2. Степень анизотропии излучения
- 3. Приложения степени анизотропии
- 4. Обсуждение
- Дополнение. Вариационные оценки энергий сверху и снизу