| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
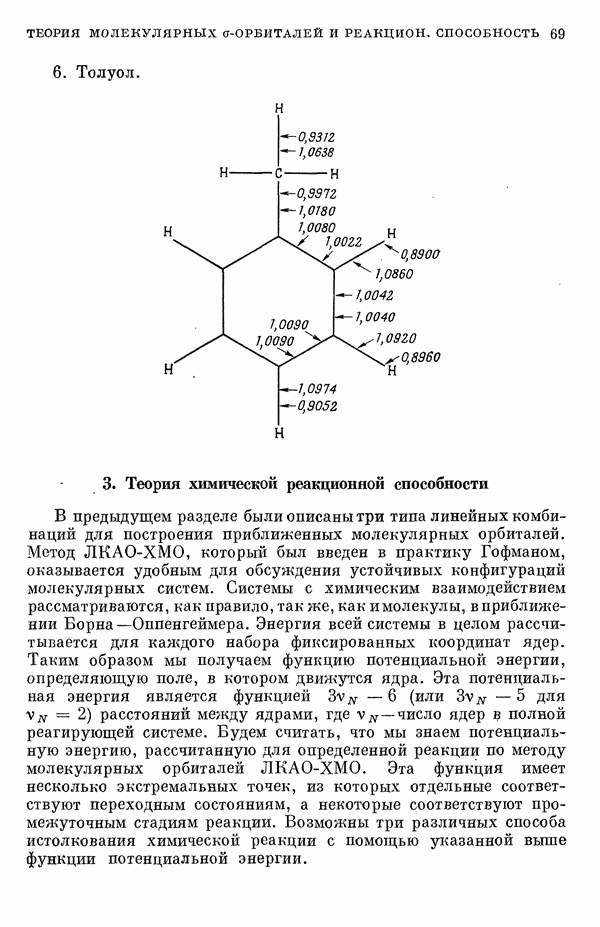
10. Локализованные орбитали при отсутствии симметрии
Если при определенной симметрии молекулы локализованные орбитали легко построить в виде эквивалентных орбиталей, то в отсутствие симметрии необходимо конкретное численное определение.
Простейшим примером является конфигурация  где
где  -орбиталь ортогонализована по отношению к
-орбиталь ортогонализована по отношению к  Для всех элементов второго периода (от
Для всех элементов второго периода (от  до
до  ) периодической таблицы можно обнаружить весьма близкие локализованные «внутренние» и «внешние»
) периодической таблицы можно обнаружить весьма близкие локализованные «внутренние» и «внешние»  -орбитали, а именно (см. [6а]):
-орбитали, а именно (см. [6а]):

Нетрудно видеть, что внутренняя орбиталь больше стянута к ядру, чем  -орбиталь, и ортогональная внешняя орбиталь имеет меньшую примесь
-орбиталь, и ортогональная внешняя орбиталь имеет меньшую примесь  -орбитали, чем ортогонализованная
-орбитали, чем ортогонализованная  -орбиталь.
-орбиталь.
Обменный интеграл между двумя орбиталями уменьшается приблизительно в 5 раз. Например, для кислорода он уменьшается с  до
до 

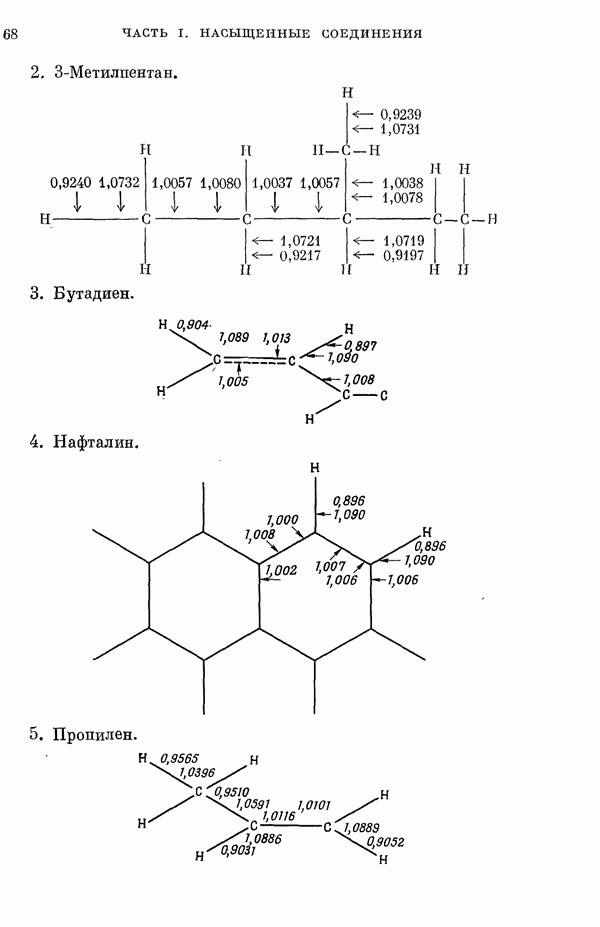
Рис. 8. Схематические диаграммы локализованных орбиталей.
Молекула  также дает простой пример рассматриваемого явления. Если локализовать три канонические орбитали
также дает простой пример рассматриваемого явления. Если локализовать три канонические орбитали  то получим орбиталь внутренней оболочки
то получим орбиталь внутренней оболочки  на атоме бора, неподеленную пару
на атоме бора, неподеленную пару  на боре и связывающую орбиталь
на боре и связывающую орбиталь 
Исключение локализации в методе ЛКАО-ССП-МО по Рзисилу дает результаты, приведенные в табл.
15—18 [66]. При этом можно видеть, что сумма шести недиагональных обменных интегралов уменьшается от  до примерно
до примерно 
Для большинства молекул, конечно, ситуация смешанная: локализованные орбитали определяются частично соображениями симметрии, частично дальнейшей численной локализацией. В качестве

(кликните для просмотра скана)

(кликните для просмотра скана)
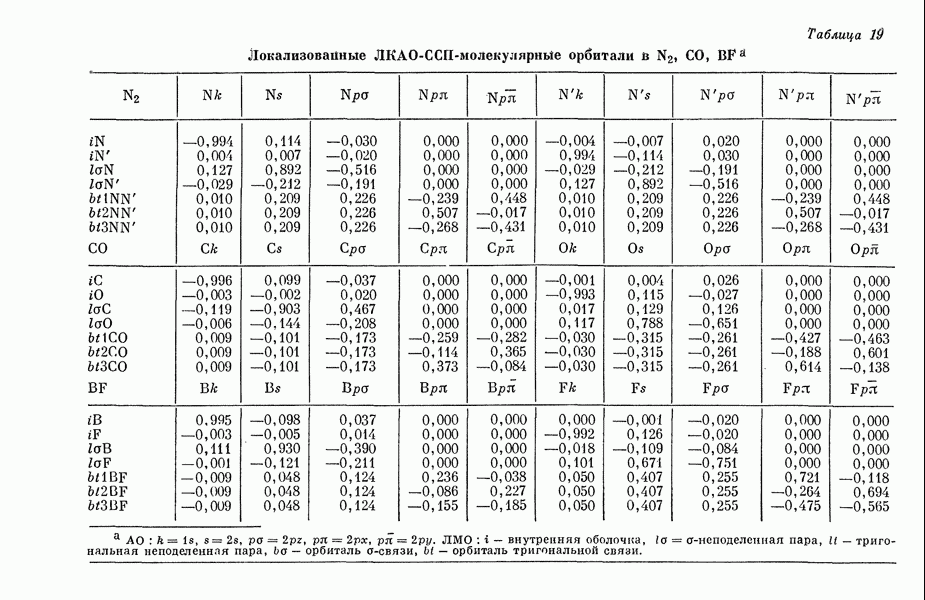
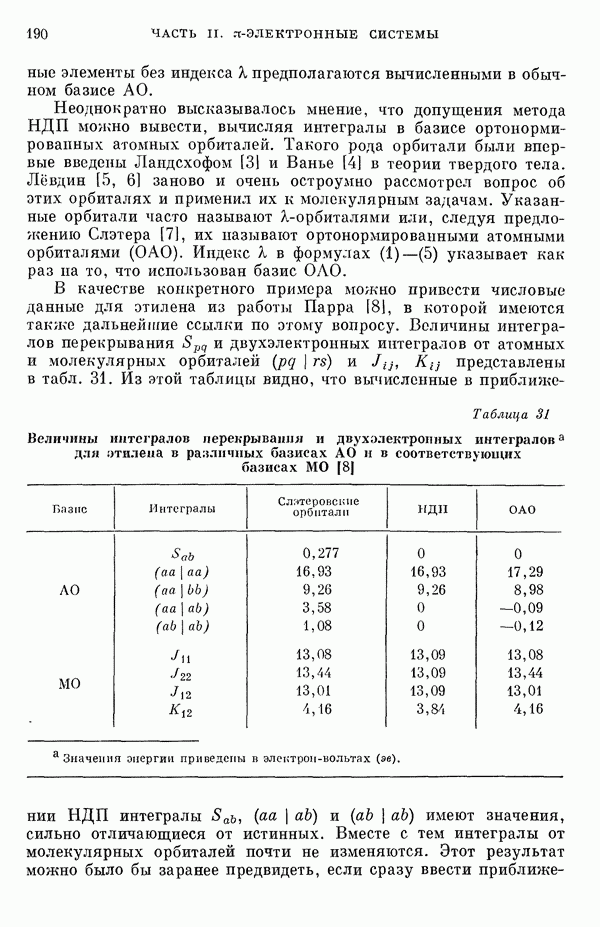
примеров в табл. 19 приводятся локализованные орбитали для изозлектронных рядов 
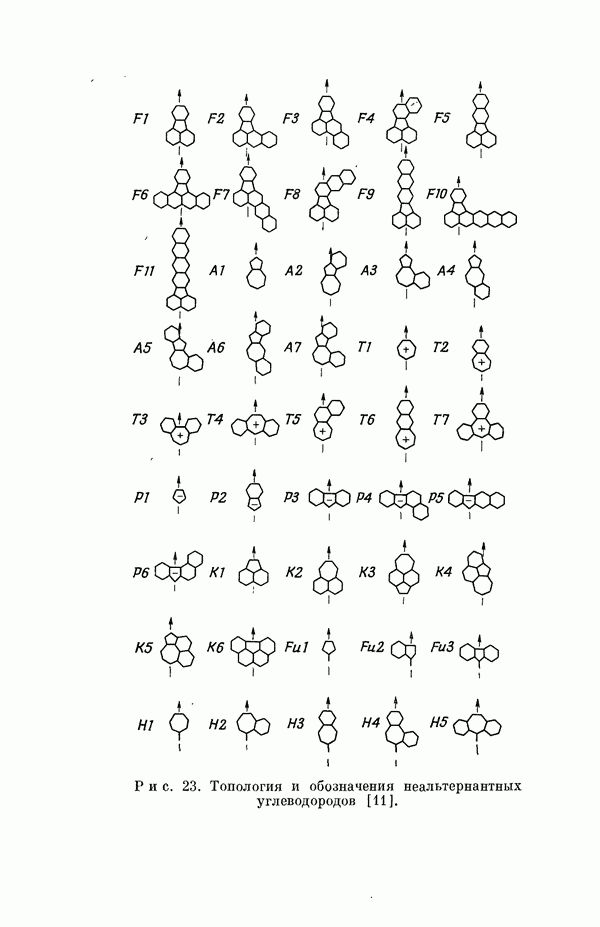
Из табл. 19 видно, что состав внутренних оболочек этих молекул приблизительно постояпен,  -гибридизация неподеленных пар и связывающих орбиталей систематическим образом меняется с изменением отношения числа неподеленных электронных пар к числу связывающих электронов. На рис. 8 приведены схемы, поясняющие природу локализованных молекулярных орбиталей в некоторых молекулах. Более детальное обсуждение свойств этих и других молекул дано в работах [66, 13].
-гибридизация неподеленных пар и связывающих орбиталей систематическим образом меняется с изменением отношения числа неподеленных электронных пар к числу связывающих электронов. На рис. 8 приведены схемы, поясняющие природу локализованных молекулярных орбиталей в некоторых молекулах. Более детальное обсуждение свойств этих и других молекул дано в работах [66, 13].
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Предисловие редакторов русского издания
- Из предисловия редактора английского издания
- Часть 1. Насыщенные соединения
- 1-1. Современное состояние теории электронной структуры молекул
- 2. Одно- и двухэлектронные системы
- 3. Предварительные замечания для многоэлектронных систем
- 4. Задачи для многоэлектронных систем
- 5. Применение теории
- 6. Заключение
- 1-2. Химическое приложение теории молекулярных орбиталей. Галогениды инертных газов
- 2. Модель электронных корреляций
- 3. Модель молекулярных орбиталей
- 4. Модель валентных связей
- 5. Интерпретация физических свойств
- 6. Возбужденные электронные состояния
- 7. Обсуждение теоретических моделей
- 1-3. Теория молекулярных «сигма»-орбиталей и реакционная способность
- 2. Молекулярные «сигма»-орбитали
- 3. Теория химической реакционной способности
- 4. Делокализация электронов в переходном состоянии
- 5. Простая интерпретация реакционной способности насыщенных соединений
- 6. Заключение
- 1-4. Локализованные ССП-орбитали в атомах и молекулах
- 2. Различные возможности в выборе хартри-фоковских орбиталей
- 3. Конкретный выбор хартри-фоковских орбиталей
- 4. Канонические ССП-орбитали
- 5. Внешне локализованные ССП-орбитали
- 6. Внутренне локализованные ССП-орбитали
- 7. Выбор функции разделения
- 8. Построение локализованных орбиталей из произвольной системы ССП-орбиталей
- 9. Локализованные орбитали и симметрия молекул
- 10. Локализованные орбитали при отсутствии симметрии
- 11. Локализованные молекулярные орбитали в системах с делокализованными электронами
- 1-5. Интегральная теорема Гельмана—Фейнмана. Барьеры для внутреннего вращения и изоэлектронные процессы
- 2. Барьеры для внутреннего вращения
- 3. Изоэлектронные процессы
- Чаешь II. «пи»-Электронные системы
- II-1. Общий обзор методов и проблем теории «пи»-электронов
- 2. «пи»-Электронные методы
- 3. Нерешенные вопросы теории «пи»-электронов
- II-2. Трехмерные и одномерные молекулярные орбитали свободных электронов
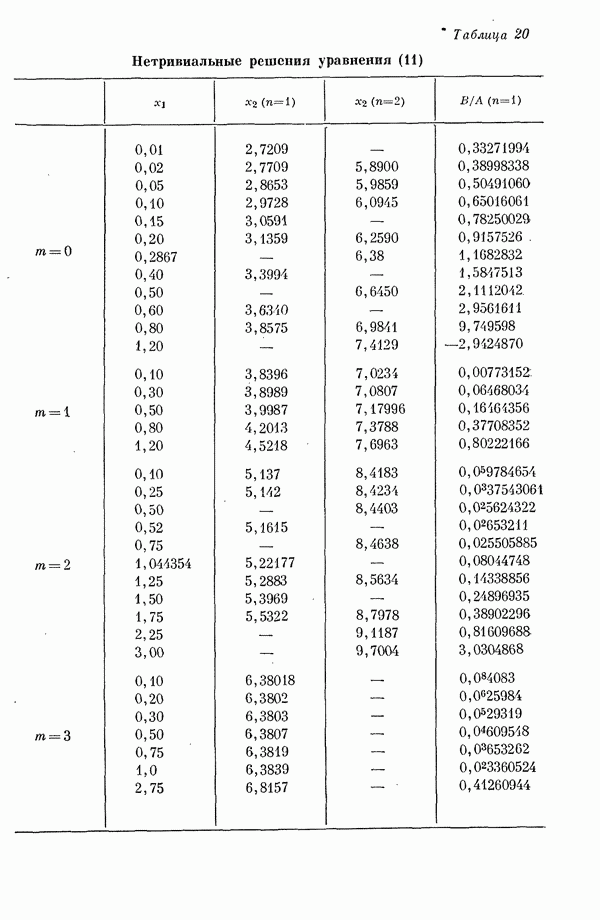
- 3. Определение собственных значений как функций А
- II-3. Теория самосогласованного поля для открытых оболочек и применение ее к «пи»-электронным системам
- 2. Уравнения в методе ССП для систем с замкнутыми оболочками. Теорема Бриллюэна
- 3. Условия самосогласования для систем с одной открытой оболочкой, находящихся в дублетных состояниях
- 4. Условия самосогласования для систем, находящихся в триплетных состояниях с двумя открытыми оболочками
- 5. Энергии низших триплетных возбужденных состояний для некоторых четных альтернантных углеводородов, вычисленные с различной степенью самосогласования
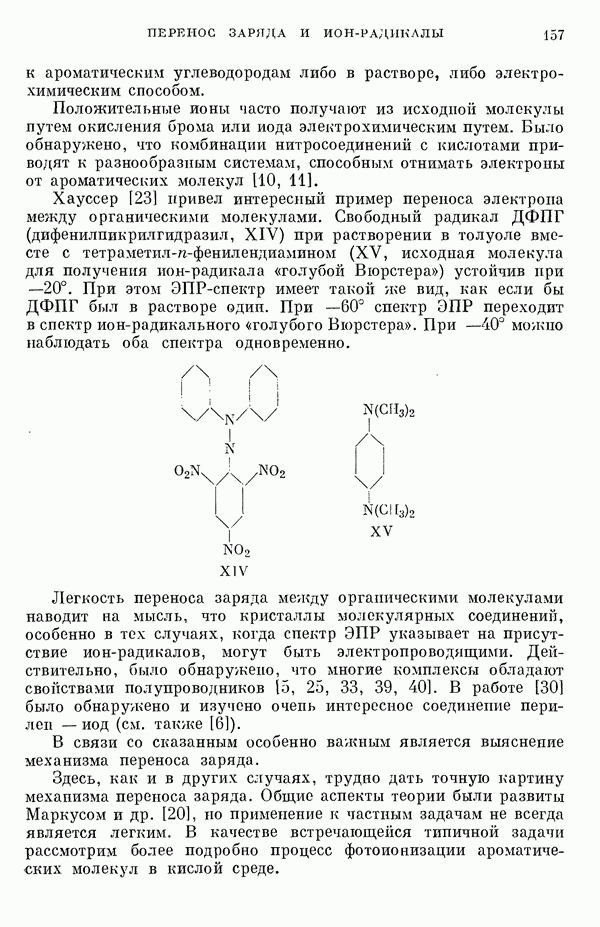
- II-4. Перенос заряда и ион-радикалы
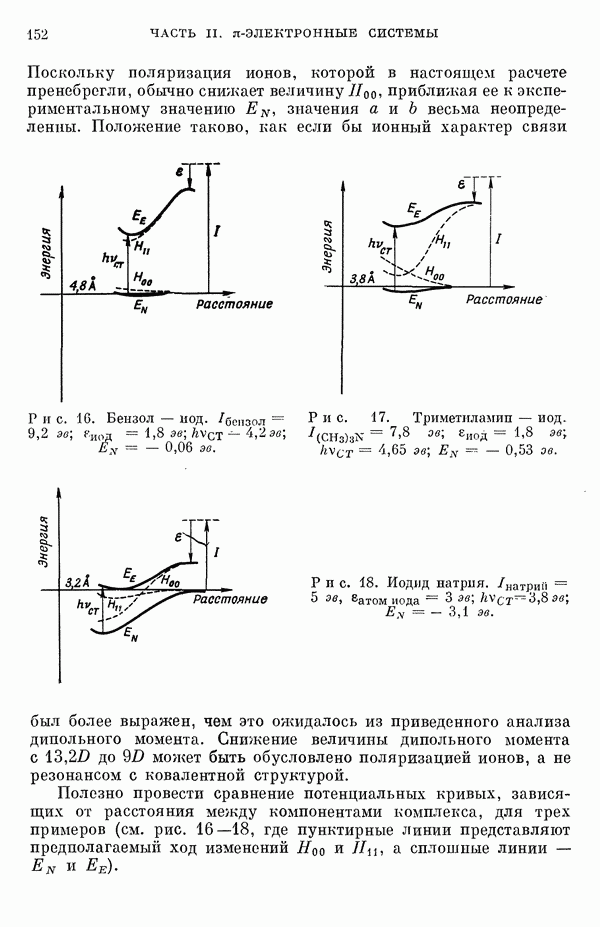
- 3. Слабосвязанные и полунонные комплексы: бензол — иод и триметиламин — иод
- 4. Ионные соединения: иодид натрия
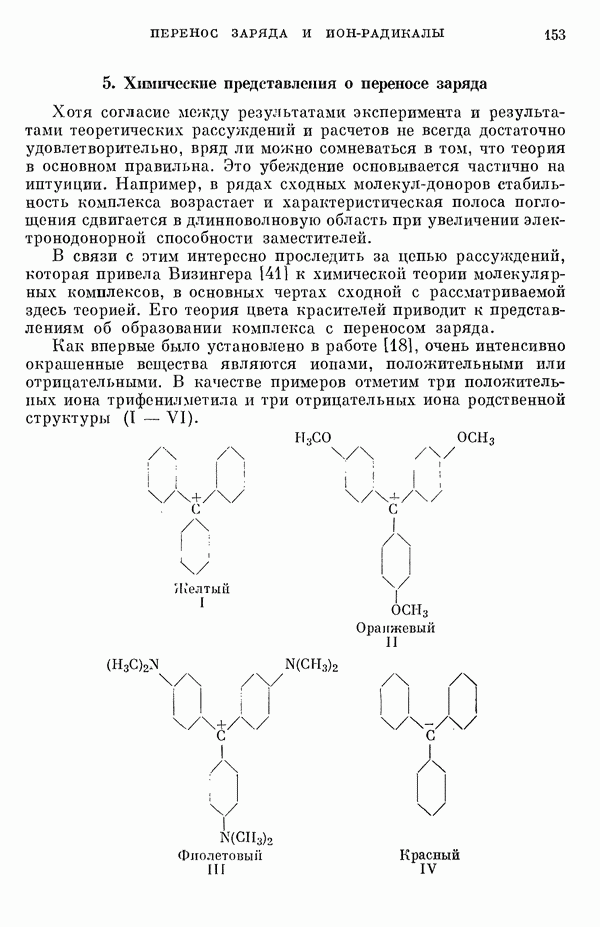
- 5. Химические представления о переносе заряда
- 6. Ион-радикалы
- 7. Фотоионизация
- II-5. Некоторые свойства «пи»-ионов и триплетных состояний
- 2. Ограниченный метод Хартри — Фока
- 3. Неограниченный метод Хартри — Фока
- 4. Энергии и плотности заряда
- 5. Трансформационные свойства орбиталей
- 6. Спиновые свойства функции
- 7. Расщепление триплетных состояний в нулевом поле
- 8. Заключение
- II-6. Критическое обсуждение «пи»-электронных теорий
- II-6A. ПРЕДЕЛЫ ПРИМЕНИМОСТИ МЕТОДОВ ТИПА МЕТОДОВ ХЮККЕЛЯ И ПАРИЗЕРА — ПАРРА
- II-6Б. БАЗИСНЫЕ ОРБИТАЛИ И ПРИБЛИЖЕНИЕ НУЛЕВОГО ДИФФЕРЕНЦИАЛЬНОГО ПЕРЕКРЫВАНИЯ
- 2. Разложение по малому параметру
- 3. Преобразование оператора Фока
- 4. Другая формулировка исходных допущений приближения НДП
- II-6B. ЭЛЕКТРОННОЕ РАСПРЕДЕЛЕНИЕ В ГЕТЕРОЦИКЛИЧЕСКИХ МОЛЕКУЛАХ
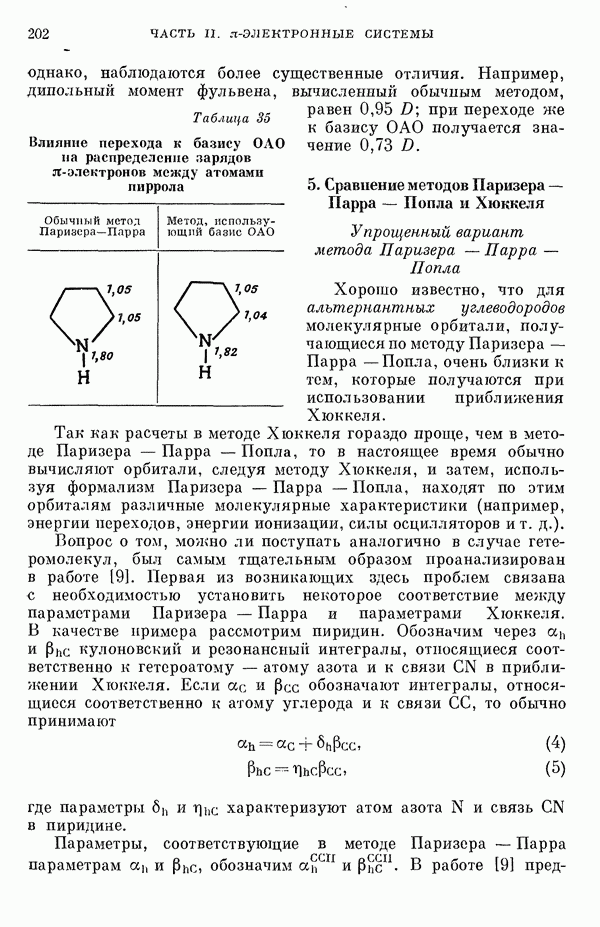
- 2. Приближения Паризера — Парра и Хюккеля (Полинга — Уэланда)
- 3. Приближение Паризера — Парра
- 4. Влияние перехода к базису ОАО на распределение зарядов «пи»-электронов на атомах
- 5. Сравнение методов Паризера — Парра — Попла и Хюккеля
- 11-6Г. ПОЛУЭМПИРИЧЕСКИЕ ПАРАМЕТРЫ В ТЕОРИИ МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
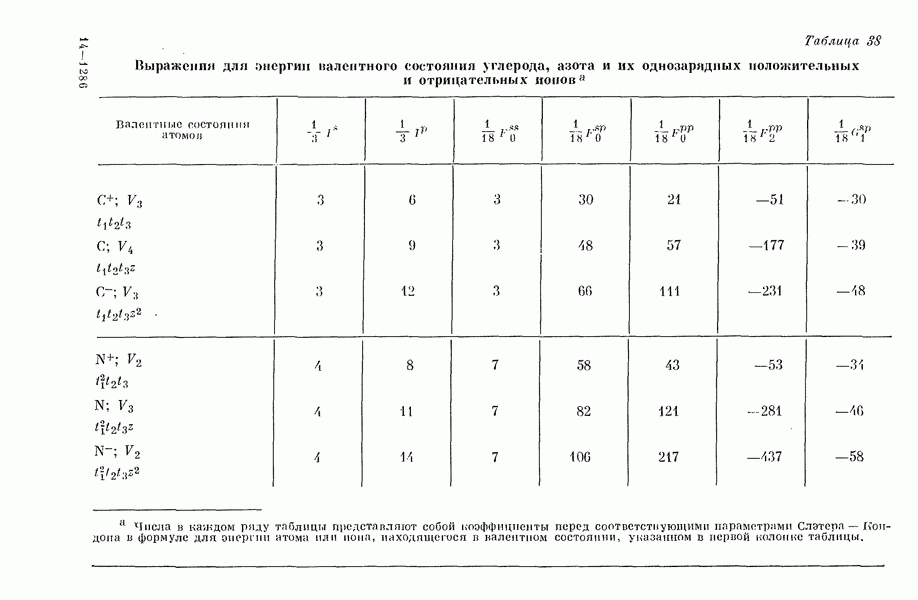
- 2. Одноцентровые интегралы
- 3. Двухцентровые интегралы
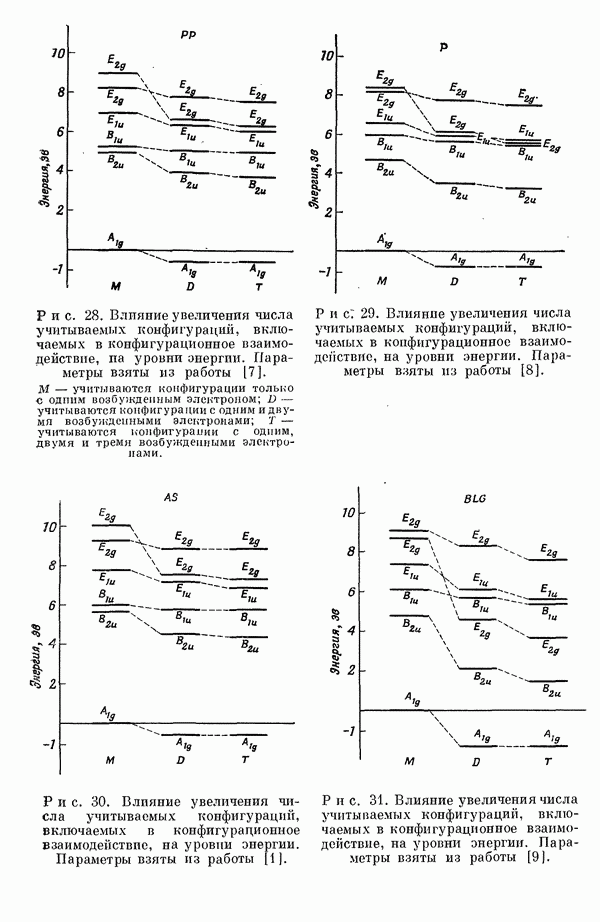
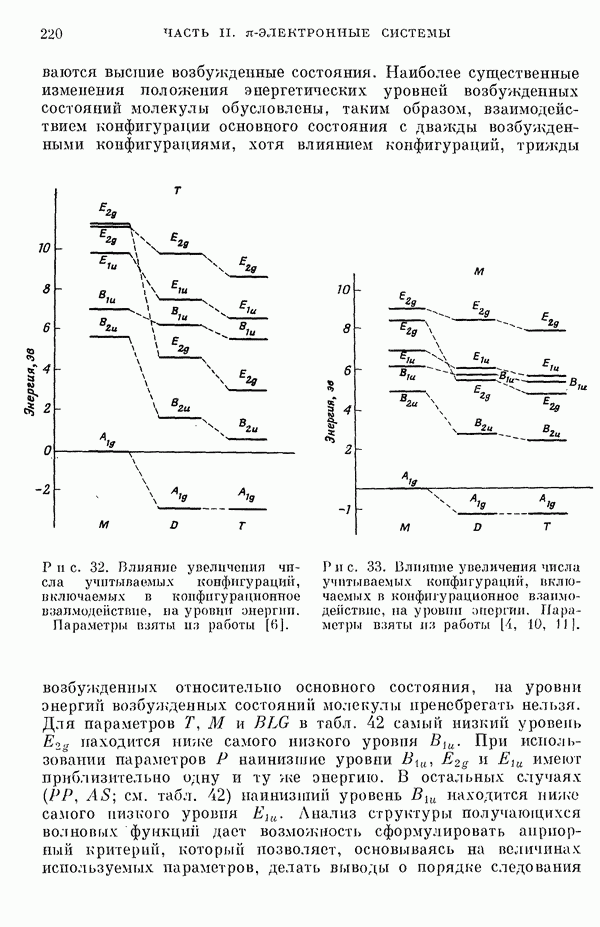
- II-6Д. РАСЧЕТ СОСТОЯНИЙ МОЛЕКУЛЫ БЕНЗОЛА С УЧЕТОМ КОНФИГУРАЦИОННОГО ВЗАИМОДЕЙСТВИЯ
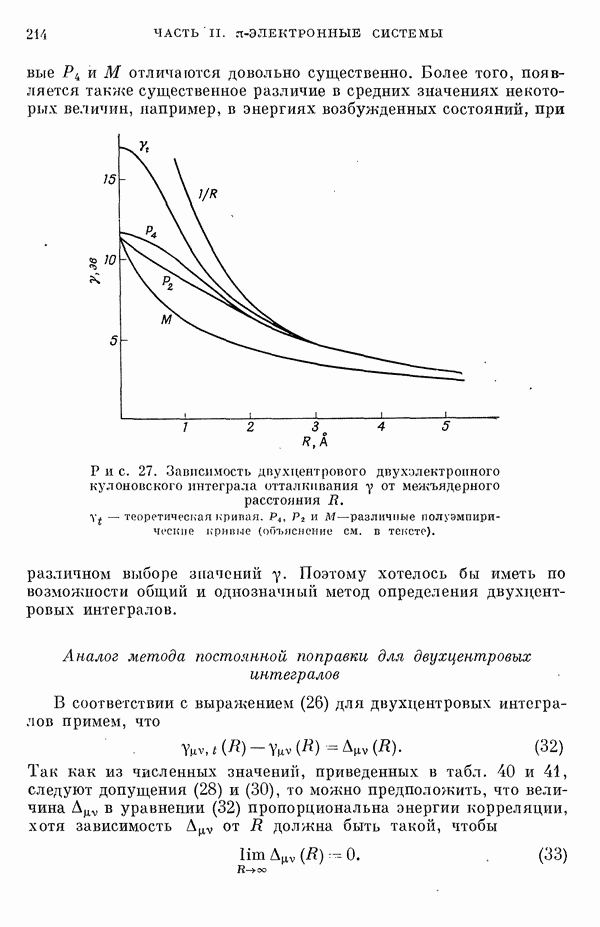
- II-6E. «пи»-ЭЛЕКТРОННОЕ ПРИБЛИЖЕНИЕ И ПАРАМЕТРЫ ДЛЯ ИНТЕГРАЛОВ КУЛОНОВСКОГО ОТТАЛКИВАНИЯ
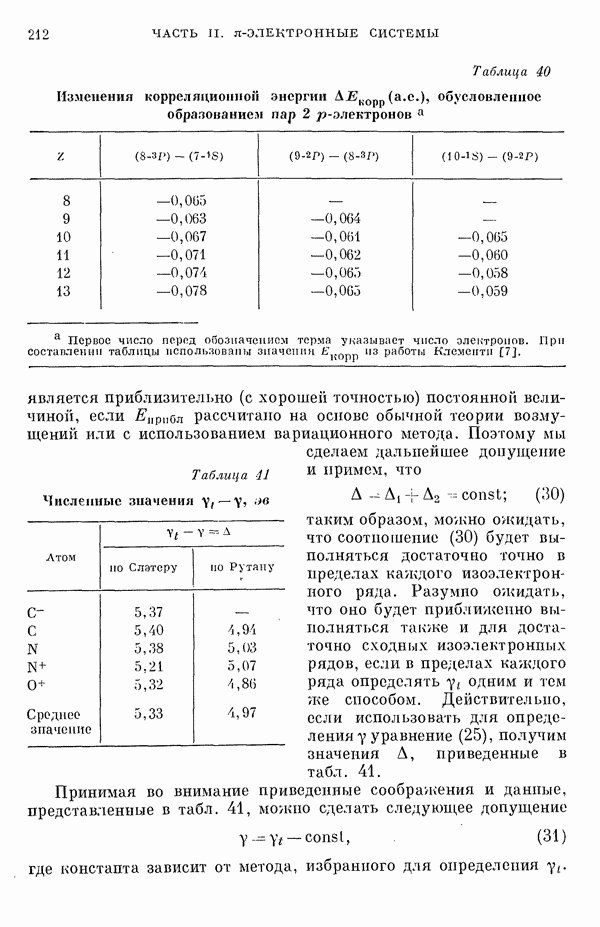
- 2. Параметры, связанные с интегралами кулоновского отталкивания
- Часть III. Молекулы и излучение
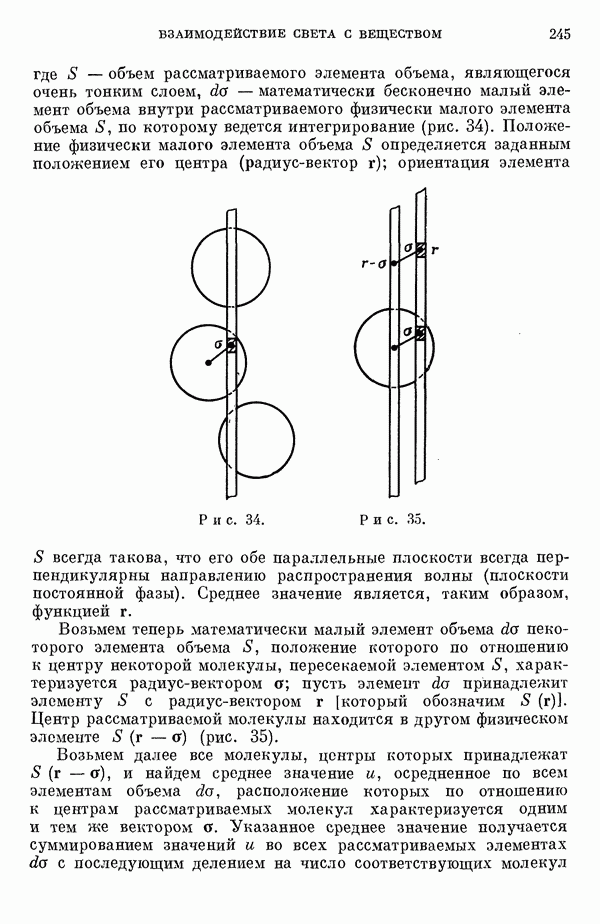
- III-1. Взаимодействие света с веществом и теория оптической вращающей способности
- 2. Распространение света в прозрачных средах
- 3. Распространение света в среде большого числа отдельных частиц
- 4. Переход от молекулярной теории к феноменологической теории
- 5. Усреднение по физическим элементам объема
- 6. Усреднение микроскопических уравнений Максвелла
- 7. Определение индуцированных молекулярных моментов
- 8. Определение внутреннего поля
- 9. Статистический вывод волнового уравнения
- 10. Квантовохимические аспекты
- III-2. Две теоремы, применяемые в расчетах оптической активности молекул
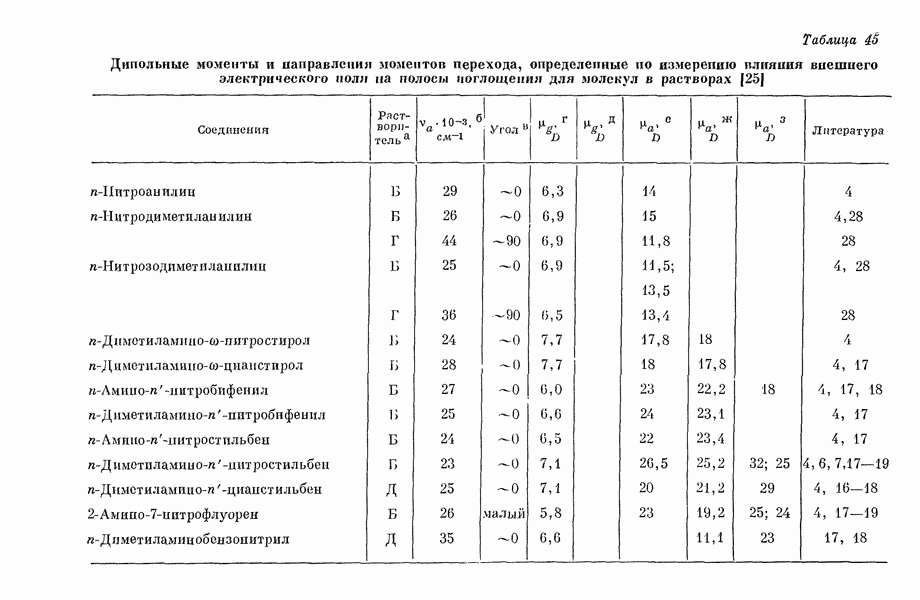
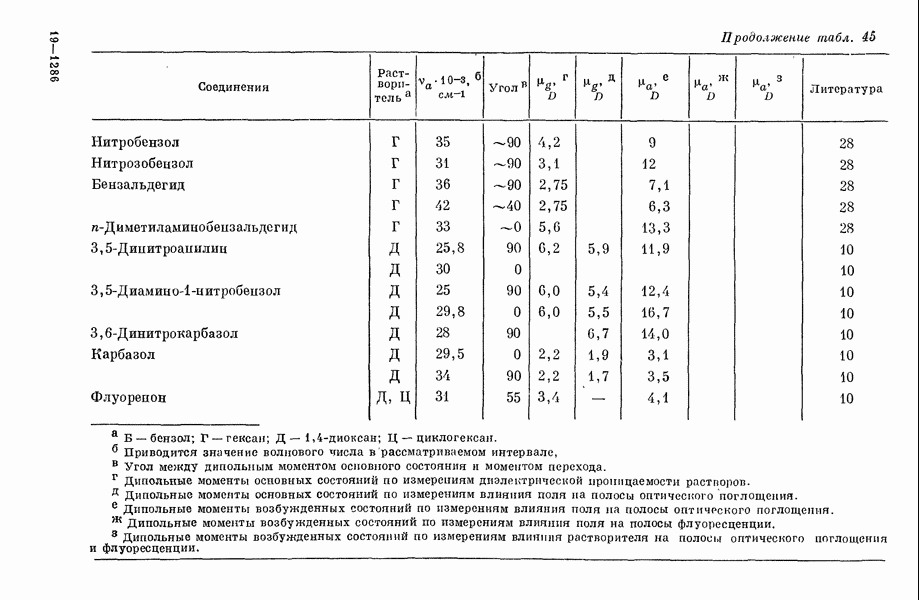
- III-3. Дипольные моменты в возбужденных состояниях молекул и влияние внешнего электрического поля на оптическое поглощение молекул в растворе
- 2. Средние вероятности переходов для молекулы с определенной ориентацией
- 3. Локальное электрическое поле в месте расположения молекулы, находящейся в растворе
- 4. Сдвиг волнового числа
- 5. Зависимость момента перехода от поля
- 6. Средние вероятности перехода для молекулы в статистическом ансамбле при наличии электрического поля
- 7. Приложения
- 8. Приложение. Расчет средних вероятностей перехода
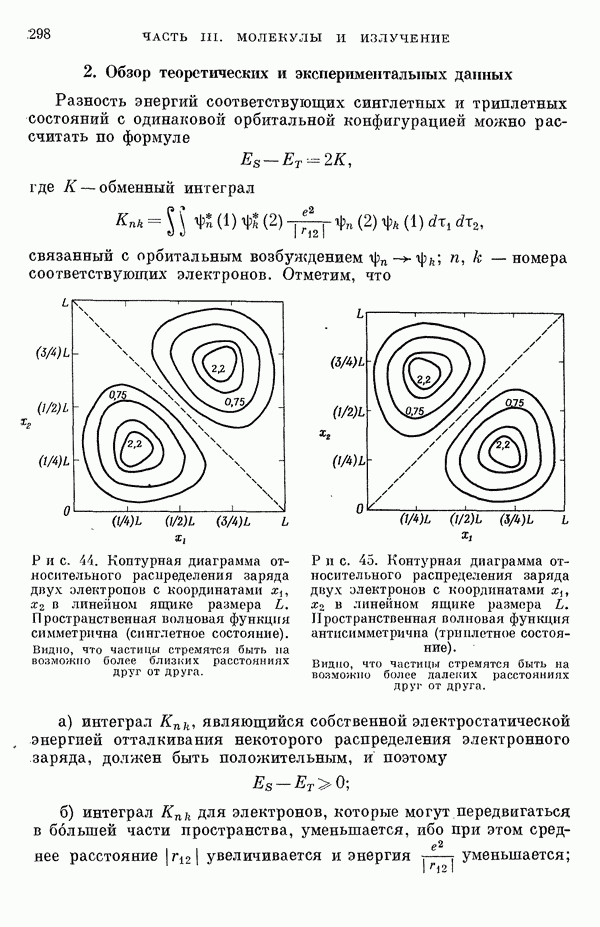
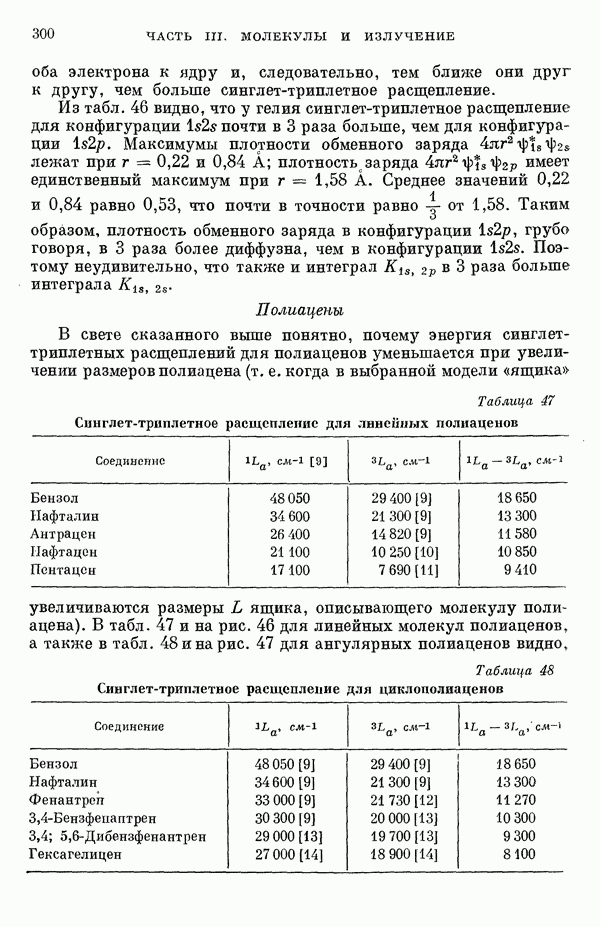
- III-4. Энергии синглет-триплетных переходов
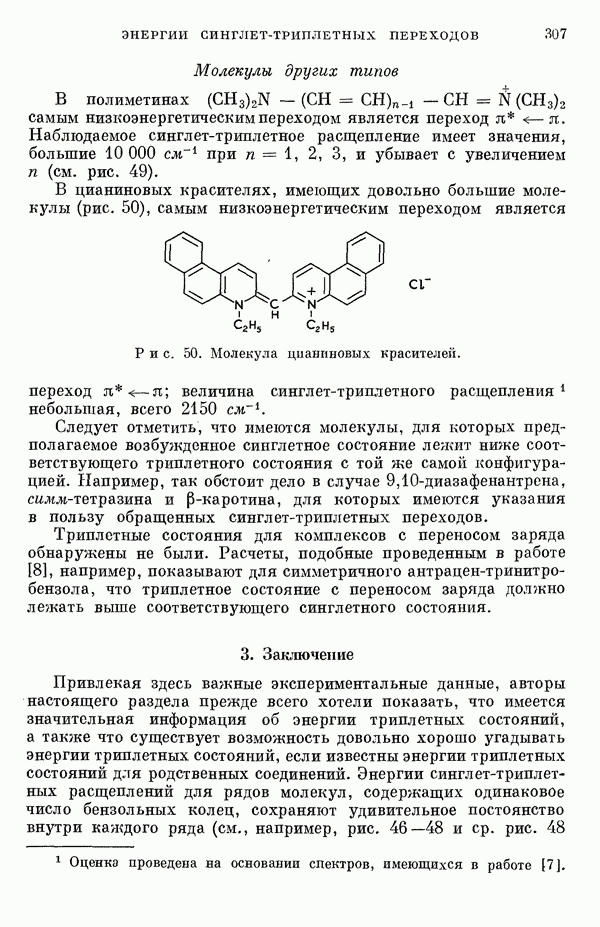
- 2. Обзор теоретических и экспериментальных данных
- 3. Заключение
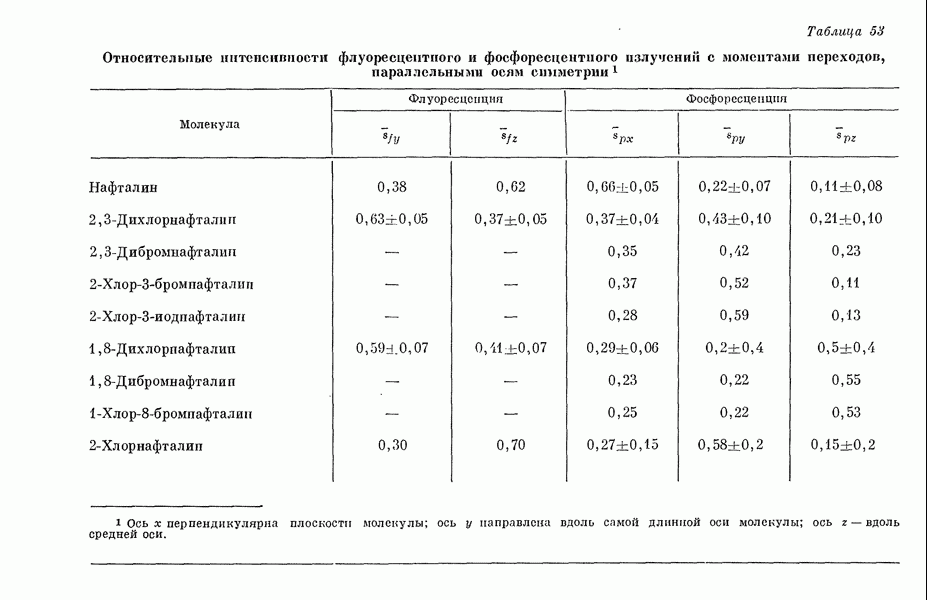
- III-5. Моменты переходов и анизотропия флуоресценции и фосфоресценции
- 2. Степень анизотропии излучения
- 3. Приложения степени анизотропии
- 4. Обсуждение
- Дополнение. Вариационные оценки энергий сверху и снизу