| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
2. Одноцентровые интегралы
Оценки по методу ионизационного потенциала и сродства к электрону
Хорошо известно, что интегралы у легко вычислить для слэтеровских атомных орбиталей

Известно также, что использование этих теоретических значений у в расчетах, проводимых без учета конфигурационного взаимодействия, приводит к результатам, не согласующимся с экспериментом, см. [3]. Это расхождение наиболее существенно в случае одноцентрового интеграла

В связи с тем, что в дальнейшем будут обсуждаться как полуэмпирические, так и теоретические значения интегралов, введем для обозначения теоретических значений индекс  Используя атомные орбитали (3), получим
Используя атомные орбитали (3), получим

Приняв для атома углерода, по Слэтеру, значение  получим для углерода
получим для углерода

Согласно Паризеру и Парру [1], энергетический эффект реакции

для которой предполагается, что атомы и ионы находятся в соответствующих валентных состояниях, определяется выражением

Согласно определениям, для потенциала ионизации I и эпергии сродства к электрону А имеем

Следовательно, обобщая рассуждения тривиальным образом на произвольный атом  из формул (8) — (10) получаем
из формул (8) — (10) получаем

Подстановка в последнее соотношение экспериментальных значений I и А для атома углерода дает

Можно видеть, что между значениями (6) и (12) имеется большое различие. Паризер и Парр [1] высказали мнение, что в рамках  -электронного приближения полуомпирическое значение (12) следует предпочесть теоретическому значению (6).
-электронного приближения полуомпирическое значение (12) следует предпочесть теоретическому значению (6).
В течение последних десяти лет выбор у по Паризеру — Парру успешно применялся в многочисленных расчетах конкретных  -электронных систем, включая как углеводороды, так и молекулы с гетероатомами. Однако определение достаточно точных экспериментальных значений потенциала ионизации и сродства к электрону во многих случаях является затруднительным. Еще труднее бывает выяснить, с какими именно атомными состояниями нужно иметь дело в данном эксперименте и как сопоставить экспериментальные данные соответствующим валентным состояниям.
-электронных систем, включая как углеводороды, так и молекулы с гетероатомами. Однако определение достаточно точных экспериментальных значений потенциала ионизации и сродства к электрону во многих случаях является затруднительным. Еще труднее бывает выяснить, с какими именно атомными состояниями нужно иметь дело в данном эксперименте и как сопоставить экспериментальные данные соответствующим валентным состояниям.
Для критического разбора соотношения (11) воспользуемся хорошо известным выражением

которое является точным для  -орбиталей самого общего вида
-орбиталей самого общего вида

в выражении  — параметры Слэтера — Кондона (см., например, [4])
— параметры Слэтера — Кондона (см., например, [4])

где  — знаменатель, появляющийся в результате интегрирования
— знаменатель, появляющийся в результате интегрирования  и
и 
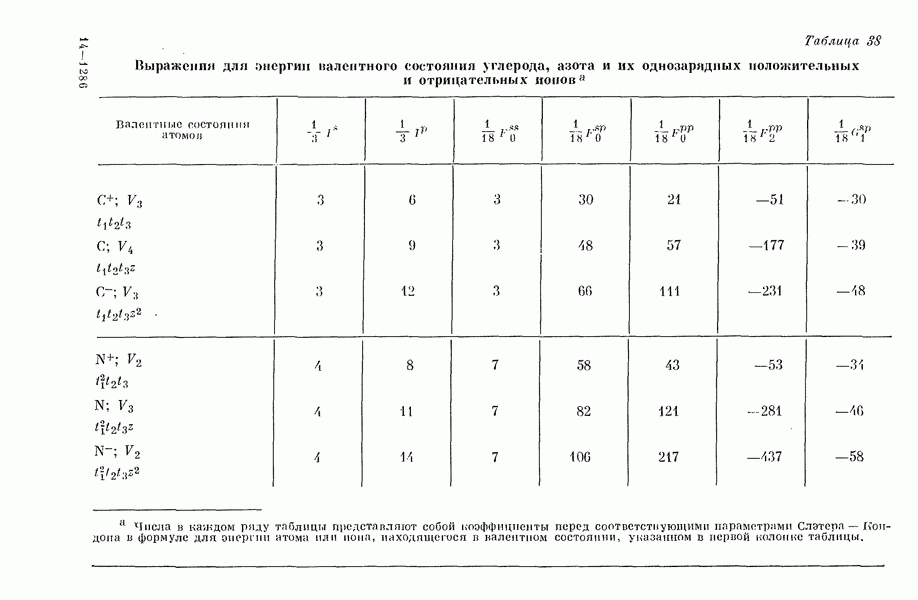
Можно показать, что выражение (13) может быть получено из (11), если последнее подвергнуть приближенному преобразованию. Энергию валентного состояния всегда можно выразить через параметры Слэтера — Кондона. Действительно, энергию любого атомного состояния (см. табл. 38) можно представить в виде

Используя предположение о тригоналъных валентных состояниях углеродного атома, получаем

где  — гибридные
— гибридные  -орбитали, a z - перпендикулярная к плоскости углеродных атомов чистая
-орбитали, a z - перпендикулярная к плоскости углеродных атомов чистая  -орбиталь. Считая, что любой параметр Р Слэтера — Кондона удовлетворяет условию
-орбиталь. Считая, что любой параметр Р Слэтера — Кондона удовлетворяет условию

(что является достаточно точным приближением), для атома углерода (ср. табл. 38) находим

Вводя далее гораздо более грубое приближение

получим окончательно


(кликните для просмотра скана)
Грубо приближенный характер этого последнего соотношения проиллюстрирован в табл. 39 (значения эмпирических параметров взяты по Пилчеру и Скиннеру [5]).
Таблица 39 (см. скан)
Оценки параметров по методу Слэтера — Кондона
Как было только что показано, параметры у из соотношения (11) можно интерпретировать как величины, зависящие от параметров Слэтера — Кондона, усредненных по различным состояниям ионизации  Наличие процедуры усреднения можно было бы рассматривать как преимущество метода определения параметров
Наличие процедуры усреднения можно было бы рассматривать как преимущество метода определения параметров  Мы считаем, однако, что нам нужно знать значение
Мы считаем, однако, что нам нужно знать значение  для нейтрального атома (конечно, если атом в молекуле действительно нейтрален).
для нейтрального атома (конечно, если атом в молекуле действительно нейтрален).
С целыо отыскания у  несколько лет назад в работе [6] было предложено использовать непосредственно соотношение (13), подставив в него эмпирические значения параметров Слэтера — Кондона
несколько лет назад в работе [6] было предложено использовать непосредственно соотношение (13), подставив в него эмпирические значения параметров Слэтера — Кондона  Недавно были проведены тщательные исследования спектроскопических данных для параметра
Недавно были проведены тщательные исследования спектроскопических данных для параметра  (см., например, [5]). Однако получить значения параметра
(см., например, [5]). Однако получить значения параметра  из спектров нейтральных атомов, к сожалению, невозможно. Поэтому приходится прибегать к следующему приему.
из спектров нейтральных атомов, к сожалению, невозможно. Поэтому приходится прибегать к следующему приему.
Мы знаем, что использование обычных слэтеровских  -орби-талей приводит к значениям параметров Слэтера — Кондона
-орби-талей приводит к значениям параметров Слэтера — Кондона

и

Предположим, что

Тогда получим

и отсюда, используя значения (22) и (5), имеем

Соотношение (25) имеет два недостатка: 1) допущение (23) совершенно произвольно; 2) появляющийся большой множитель  сильно увеличивает неточность эмпирического значения
сильно увеличивает неточность эмпирического значения  Поэтому обратимся еще к одному методу определения параметра
Поэтому обратимся еще к одному методу определения параметра 
Оценки по методу постоянной поправки
Синаноглу и Орлов (см. разд. II-6E) коротко изложили возможные теоретические предпосылки для исправления теоретических значений 7. Делается предположение, что

где  — поправка от учета корреляционных эффектов, а
— поправка от учета корреляционных эффектов, а  — поправка от учета того, что значение
— поправка от учета того, что значение  рассчитано с использованием простых слэтеровских орбиталей, а не орбиталей Хартри — Фока.
рассчитано с использованием простых слэтеровских орбиталей, а не орбиталей Хартри — Фока.
Начнем с обсуждения поправки  Для этого воспользуемся данными недавней работы Клементи [7], который вычислил хартри-фоковскую энергию для целого ряда атомных систем. Эти вычисления, проводимые с учетом релятивистских поправок, позволили Клементи получить численные значения
Для этого воспользуемся данными недавней работы Клементи [7], который вычислил хартри-фоковскую энергию для целого ряда атомных систем. Эти вычисления, проводимые с учетом релятивистских поправок, позволили Клементи получить численные значения  Для нескольких рядов изоэлектронных систем. По самому определению,
Для нескольких рядов изоэлектронных систем. По самому определению,

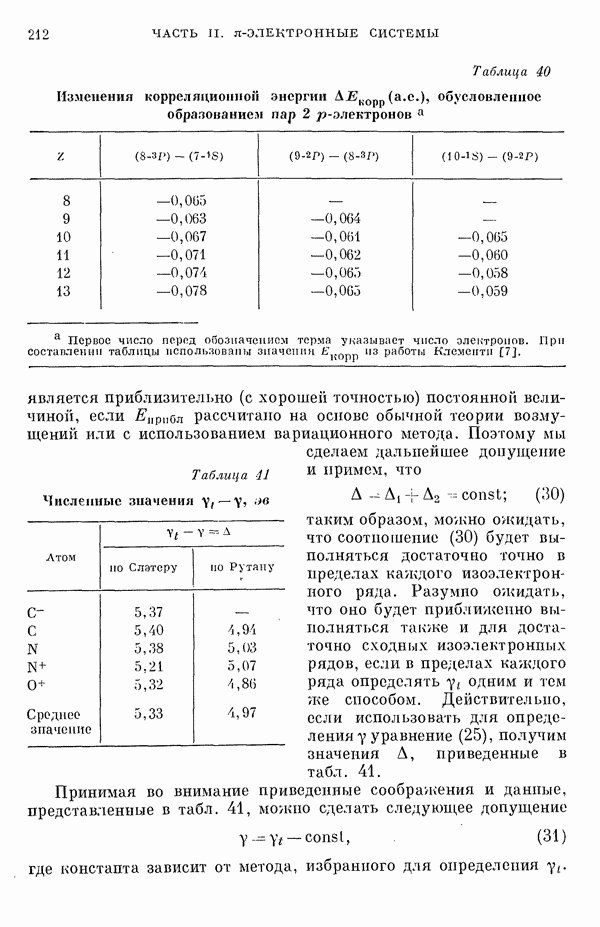
В табл. 40 приведены изменения корреляционной энергии  происходящие при образовании пар
происходящие при образовании пар  -электронов. Легко видеть, что Дкорр примерно постоянна;
-электронов. Легко видеть, что Дкорр примерно постоянна;  Разумно ожидать
Разумно ожидать  что образование пар именно
что образование пар именно  -электронов дает главный вклад в
-электронов дает главный вклад в  Таким образом, из табл. 40 следует, что
Таким образом, из табл. 40 следует, что

Для обсуждения второй поправки  напомним некоторые результаты расчетов двухэлектронных ионов с конфигурацией
напомним некоторые результаты расчетов двухэлектронных ионов с конфигурацией  Хорошо известно, что для таких систем условие (28) выполняется [8]. Более того, величина
Хорошо известно, что для таких систем условие (28) выполняется [8]. Более того, величина  из уравнения
из уравнения

Таблица 40 (см. скан) Изменения корреляционной энергии  (а.е.), обусловленное образованием пар
(а.е.), обусловленное образованием пар  -электронов
-электронов
является приблизительно (с хорошей точностью) постоянной величиной, если  рассчитано на основе обычной теории возмущений или с использованием вариационного метода. Поэтому мы сделаем дальнейшее допущение и примем, что
рассчитано на основе обычной теории возмущений или с использованием вариационного метода. Поэтому мы сделаем дальнейшее допущение и примем, что

таким образом, можно ожидать, что соотношение (30) будет выполняться достаточно точно в пределах каждого изоэлектронного ряда. Разумно ожидать, что оно будет приближенно выполняться также и для достаточно сходных изоэлектронпых рядов, если в пределах каждого ряда определять  одним и тем же способом. Действительно, если использовать для определения у уравнение (25), получим значения
одним и тем же способом. Действительно, если использовать для определения у уравнение (25), получим значения  приведенные в табл. 41.
приведенные в табл. 41.
Принимая во внимание приведенные соображения и данные, представленные в табл. 41, можно сделать следующее допущение

где константа зависит от метода, избранного для определения 
Таблица 41 (см. скан) Численные значения — 
Если для значений параметров  появятся более точные данные, то соотношение (31), возможно, несколько изменится. Для атомов, указанных в табл. 41, эти изменения, вероятно, составят всего несколько десятых электрон-вольт.
появятся более точные данные, то соотношение (31), возможно, несколько изменится. Для атомов, указанных в табл. 41, эти изменения, вероятно, составят всего несколько десятых электрон-вольт.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие редакторов русского издания
- Из предисловия редактора английского издания
- Часть 1. Насыщенные соединения
- 1-1. Современное состояние теории электронной структуры молекул
- 2. Одно- и двухэлектронные системы
- 3. Предварительные замечания для многоэлектронных систем
- 4. Задачи для многоэлектронных систем
- 5. Применение теории
- 6. Заключение
- 1-2. Химическое приложение теории молекулярных орбиталей. Галогениды инертных газов
- 2. Модель электронных корреляций
- 3. Модель молекулярных орбиталей
- 4. Модель валентных связей
- 5. Интерпретация физических свойств
- 6. Возбужденные электронные состояния
- 7. Обсуждение теоретических моделей
- 1-3. Теория молекулярных «сигма»-орбиталей и реакционная способность
- 2. Молекулярные «сигма»-орбитали
- 3. Теория химической реакционной способности
- 4. Делокализация электронов в переходном состоянии
- 5. Простая интерпретация реакционной способности насыщенных соединений
- 6. Заключение
- 1-4. Локализованные ССП-орбитали в атомах и молекулах
- 2. Различные возможности в выборе хартри-фоковских орбиталей
- 3. Конкретный выбор хартри-фоковских орбиталей
- 4. Канонические ССП-орбитали
- 5. Внешне локализованные ССП-орбитали
- 6. Внутренне локализованные ССП-орбитали
- 7. Выбор функции разделения
- 8. Построение локализованных орбиталей из произвольной системы ССП-орбиталей
- 9. Локализованные орбитали и симметрия молекул
- 10. Локализованные орбитали при отсутствии симметрии
- 11. Локализованные молекулярные орбитали в системах с делокализованными электронами
- 1-5. Интегральная теорема Гельмана—Фейнмана. Барьеры для внутреннего вращения и изоэлектронные процессы
- 2. Барьеры для внутреннего вращения
- 3. Изоэлектронные процессы
- Чаешь II. «пи»-Электронные системы
- II-1. Общий обзор методов и проблем теории «пи»-электронов
- 2. «пи»-Электронные методы
- 3. Нерешенные вопросы теории «пи»-электронов
- II-2. Трехмерные и одномерные молекулярные орбитали свободных электронов
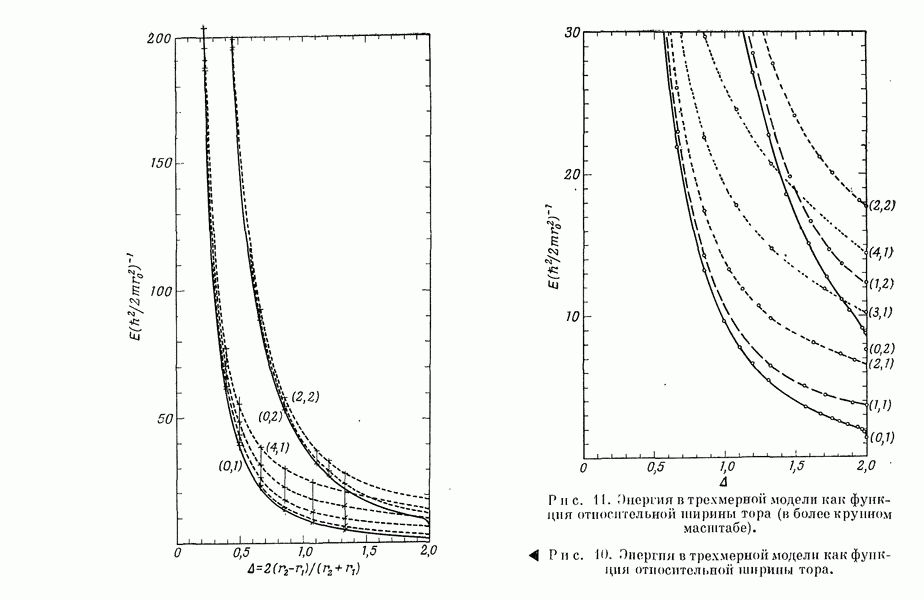
- 3. Определение собственных значений как функций А
- II-3. Теория самосогласованного поля для открытых оболочек и применение ее к «пи»-электронным системам
- 2. Уравнения в методе ССП для систем с замкнутыми оболочками. Теорема Бриллюэна
- 3. Условия самосогласования для систем с одной открытой оболочкой, находящихся в дублетных состояниях
- 4. Условия самосогласования для систем, находящихся в триплетных состояниях с двумя открытыми оболочками
- 5. Энергии низших триплетных возбужденных состояний для некоторых четных альтернантных углеводородов, вычисленные с различной степенью самосогласования
- II-4. Перенос заряда и ион-радикалы
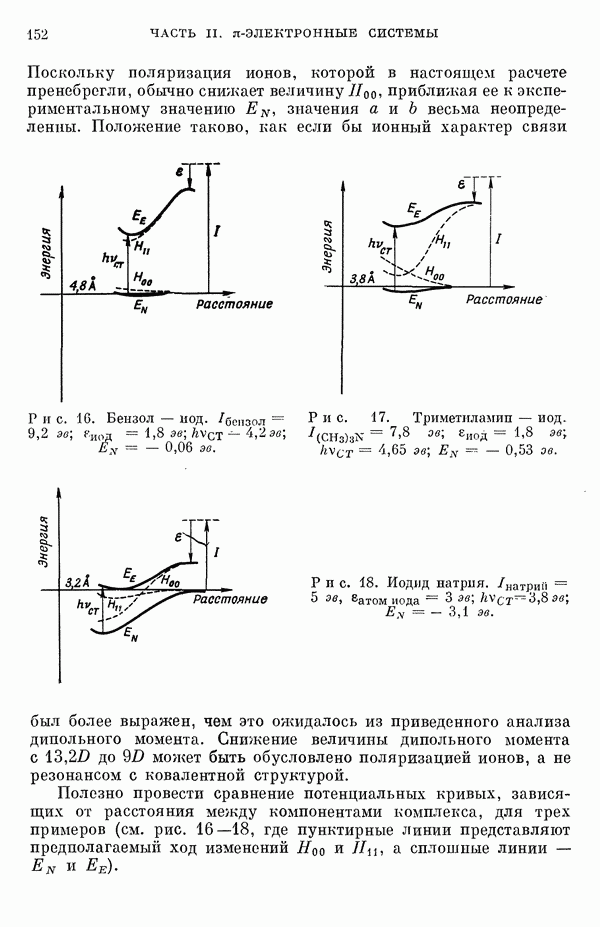
- 3. Слабосвязанные и полунонные комплексы: бензол — иод и триметиламин — иод
- 4. Ионные соединения: иодид натрия
- 5. Химические представления о переносе заряда
- 6. Ион-радикалы
- 7. Фотоионизация
- II-5. Некоторые свойства «пи»-ионов и триплетных состояний
- 2. Ограниченный метод Хартри — Фока
- 3. Неограниченный метод Хартри — Фока
- 4. Энергии и плотности заряда
- 5. Трансформационные свойства орбиталей
- 6. Спиновые свойства функции
- 7. Расщепление триплетных состояний в нулевом поле
- 8. Заключение
- II-6. Критическое обсуждение «пи»-электронных теорий
- II-6A. ПРЕДЕЛЫ ПРИМЕНИМОСТИ МЕТОДОВ ТИПА МЕТОДОВ ХЮККЕЛЯ И ПАРИЗЕРА — ПАРРА
- II-6Б. БАЗИСНЫЕ ОРБИТАЛИ И ПРИБЛИЖЕНИЕ НУЛЕВОГО ДИФФЕРЕНЦИАЛЬНОГО ПЕРЕКРЫВАНИЯ
- 2. Разложение по малому параметру
- 3. Преобразование оператора Фока
- 4. Другая формулировка исходных допущений приближения НДП
- II-6B. ЭЛЕКТРОННОЕ РАСПРЕДЕЛЕНИЕ В ГЕТЕРОЦИКЛИЧЕСКИХ МОЛЕКУЛАХ
- 2. Приближения Паризера — Парра и Хюккеля (Полинга — Уэланда)
- 3. Приближение Паризера — Парра
- 4. Влияние перехода к базису ОАО на распределение зарядов «пи»-электронов на атомах
- 5. Сравнение методов Паризера — Парра — Попла и Хюккеля
- 11-6Г. ПОЛУЭМПИРИЧЕСКИЕ ПАРАМЕТРЫ В ТЕОРИИ МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- 2. Одноцентровые интегралы
- 3. Двухцентровые интегралы
- II-6Д. РАСЧЕТ СОСТОЯНИЙ МОЛЕКУЛЫ БЕНЗОЛА С УЧЕТОМ КОНФИГУРАЦИОННОГО ВЗАИМОДЕЙСТВИЯ
- II-6E. «пи»-ЭЛЕКТРОННОЕ ПРИБЛИЖЕНИЕ И ПАРАМЕТРЫ ДЛЯ ИНТЕГРАЛОВ КУЛОНОВСКОГО ОТТАЛКИВАНИЯ
- 2. Параметры, связанные с интегралами кулоновского отталкивания
- Часть III. Молекулы и излучение
- III-1. Взаимодействие света с веществом и теория оптической вращающей способности
- 2. Распространение света в прозрачных средах
- 3. Распространение света в среде большого числа отдельных частиц
- 4. Переход от молекулярной теории к феноменологической теории
- 5. Усреднение по физическим элементам объема
- 6. Усреднение микроскопических уравнений Максвелла
- 7. Определение индуцированных молекулярных моментов
- 8. Определение внутреннего поля
- 9. Статистический вывод волнового уравнения
- 10. Квантовохимические аспекты
- III-2. Две теоремы, применяемые в расчетах оптической активности молекул
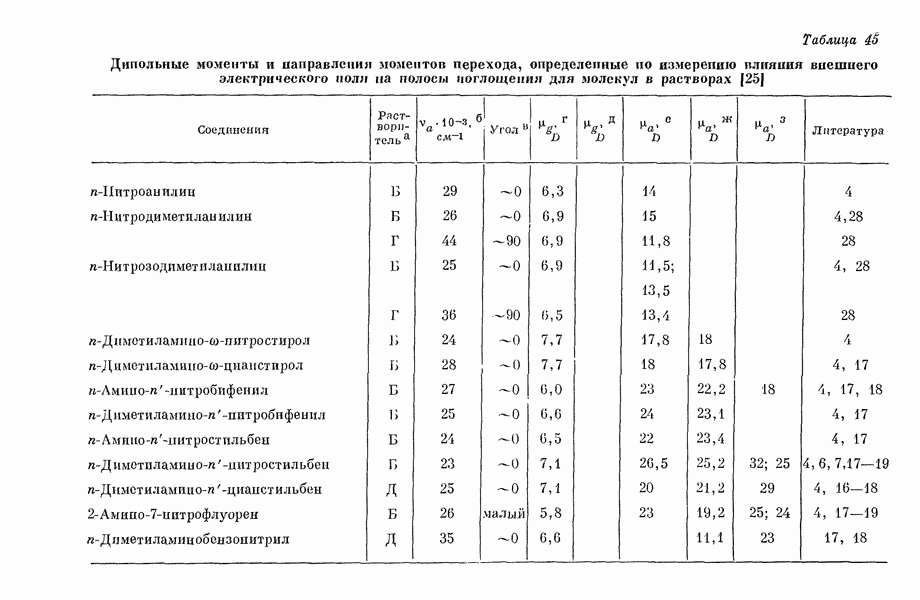
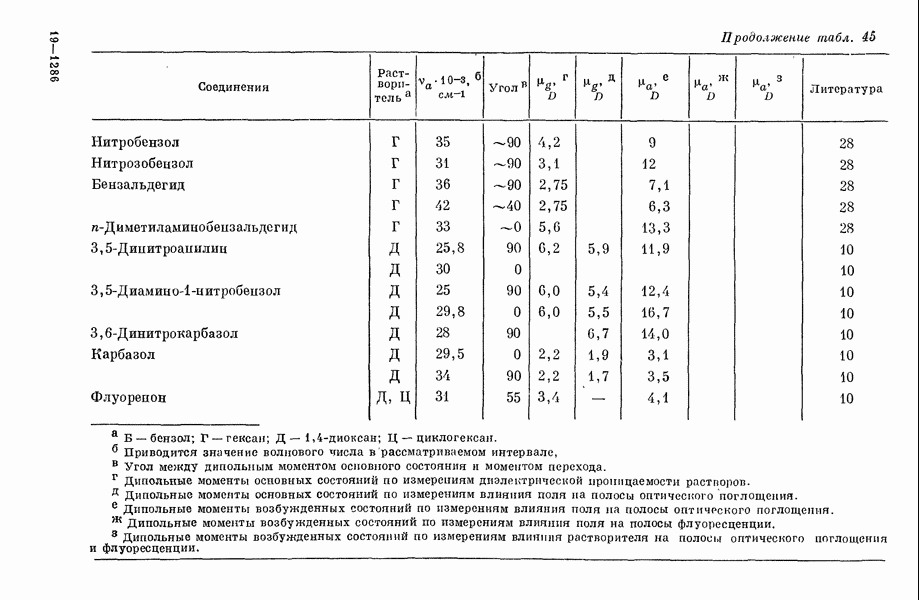
- III-3. Дипольные моменты в возбужденных состояниях молекул и влияние внешнего электрического поля на оптическое поглощение молекул в растворе
- 2. Средние вероятности переходов для молекулы с определенной ориентацией
- 3. Локальное электрическое поле в месте расположения молекулы, находящейся в растворе
- 4. Сдвиг волнового числа
- 5. Зависимость момента перехода от поля
- 6. Средние вероятности перехода для молекулы в статистическом ансамбле при наличии электрического поля
- 7. Приложения
- 8. Приложение. Расчет средних вероятностей перехода
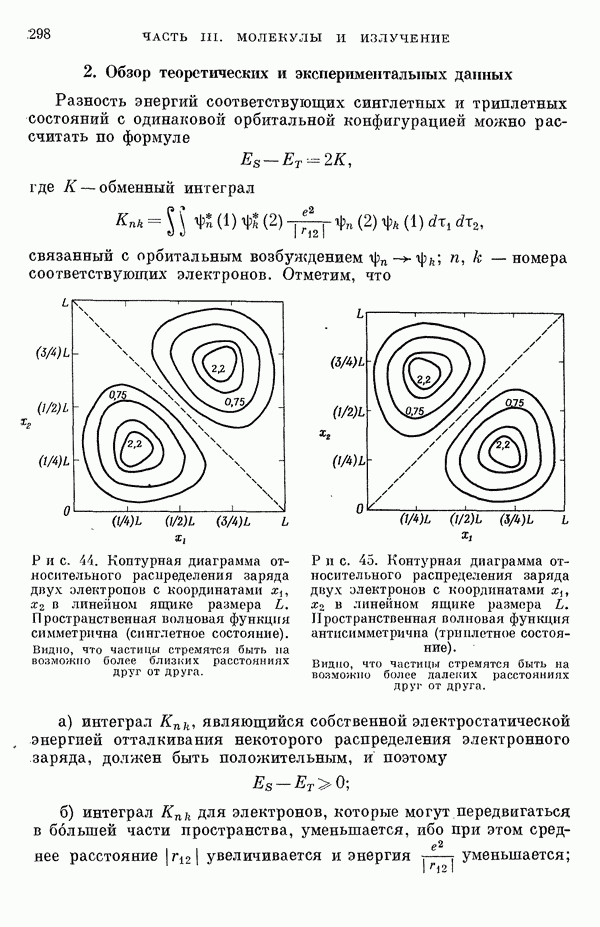
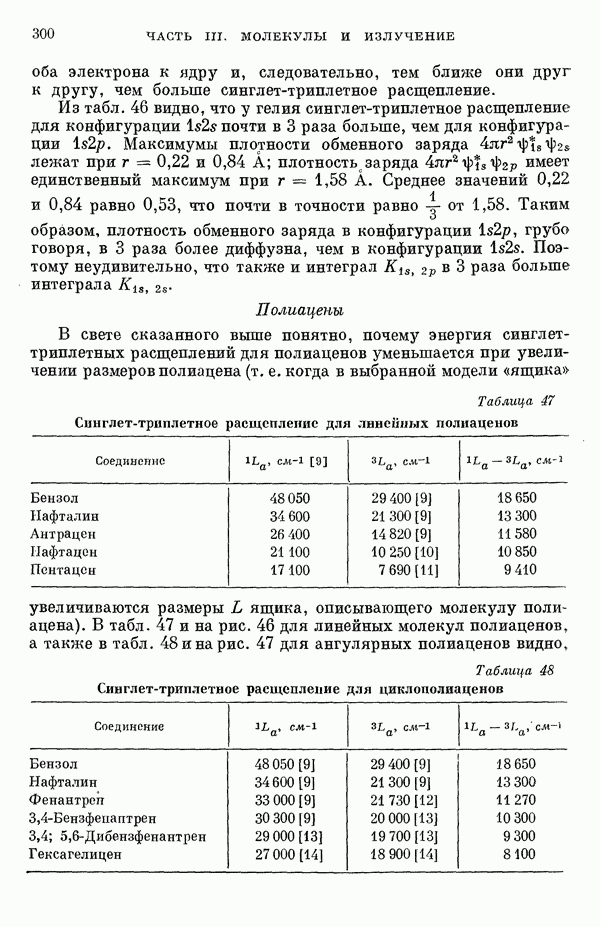
- III-4. Энергии синглет-триплетных переходов
- 2. Обзор теоретических и экспериментальных данных
- 3. Заключение
- III-5. Моменты переходов и анизотропия флуоресценции и фосфоресценции
- 2. Степень анизотропии излучения
- 3. Приложения степени анизотропии
- 4. Обсуждение
- Дополнение. Вариационные оценки энергий сверху и снизу