| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
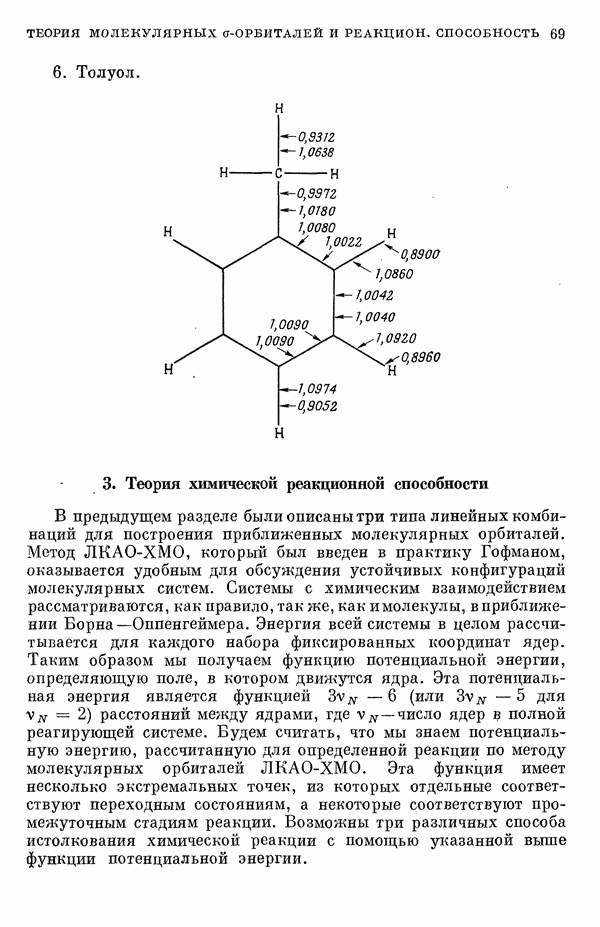
7. Обсуждение теоретических моделей
Удовлетворительное качественное описание свойств соединений ксенона дает как полуэмпирический метод молекулярных орбиталей, так и метод валентных связей. В первом методе схема связи включает в основном  -атомные орбитали. Однако для интерпретации многих физических свойств (сверхтонкое взаимодействие, константы взаимодействия с ядерным спином, магнитная восприимчивость и эффекты взаимодействия колебаний) существенна небольшая примесь s- и d-орбиталей. Против применения полуэмпирического метода МО можно выдвинуть следующие возражения:
-атомные орбитали. Однако для интерпретации многих физических свойств (сверхтонкое взаимодействие, константы взаимодействия с ядерным спином, магнитная восприимчивость и эффекты взаимодействия колебаний) существенна небольшая примесь s- и d-орбиталей. Против применения полуэмпирического метода МО можно выдвинуть следующие возражения:
1. Нельзя сделать надежных предсказаний об энергии связи и устойчивости ввиду использованных приближений, касающихся взаимного уничтожения эффектов притяжения к ядру и межэлектронного отталкивания различных атомов. Этот недостаток является, конечно, главным дефектом любых полуэмпирических моделей.
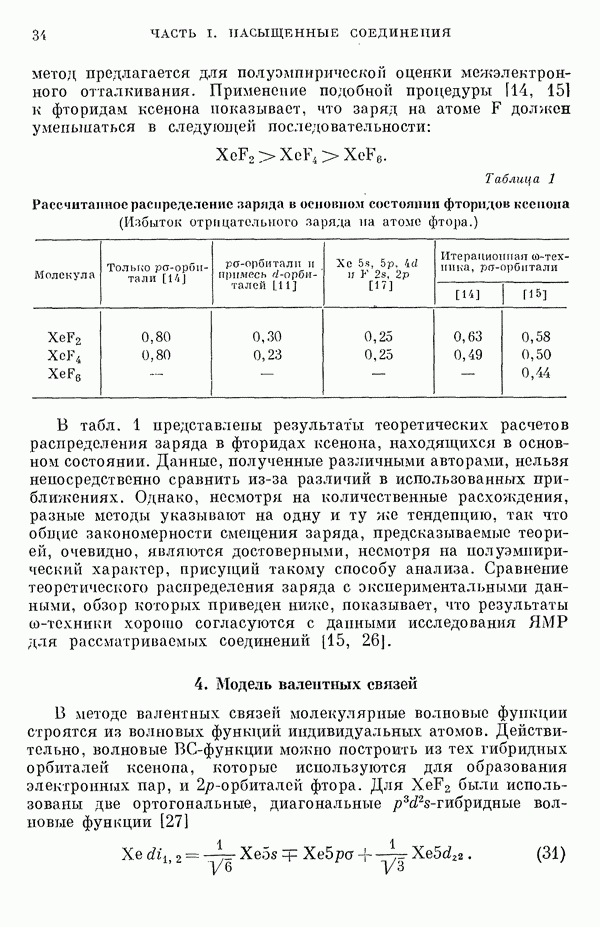
2. Распределение заряда, предсказанное на основе простейшей модели (при учете  -орбиталей), переоценивает смещение заряда. Это распределение можно уточнить, если использовать большее количество базисных волновых функций, метод конфигурационного взаимодействия или полуэмпирическую итерационную
-орбиталей), переоценивает смещение заряда. Это распределение можно уточнить, если использовать большее количество базисных волновых функций, метод конфигурационного взаимодействия или полуэмпирическую итерационную  -технику.
-технику.
3. Количественные численные предсказания полуэмпирического метода о порядке энергетических уровней некоторых возбужденных состояний можно принимать лишь с оговорками. Сходный полуэмпирический метод МО [23], использованный для изучения переходов в тетраэдрических комплексах переходных металлов, приводит к неправильной картине расположения некоторых энергетических уровней, указывая тем самым на трудности применения
дедуктивного подхода к исследованиям структуры неорганических соединений.
Однако в настоящее время полуэмпирический метод МО обеспечивает наиболее разносторонний и полезный подход к проблеме корреляций и классификации свойств соединений ксенона в основном и в возбужденных состояниях.
Применимость метода валентных связей к интерпретации экспериментальных данных пока все еще весьма ограничена. Этот подход позволяет, однако, значительно лучше понять физическую природу связи в соединениях инертных газов. Распределения заряда в основном состоянии фторидов ксенона, найденные как методом МО, так и методом ВС, весьма близки. Оба метода предсказывают значительное смещение заряда от ксенона к фтору. В методе МО этот результат обусловлен низким потенциалом ионизации (т. е. кулоновским интегралом) центрального атома инертного газа [14, 19]. В методе ВС определяющими являются ионные структуры; действительно, ионные структуры  вполне устойчивы [30]. Электростатическая энергия образования
вполне устойчивы [30]. Электростатическая энергия образования  (приближенно равная
(приближенно равная  по-видимому, возмещается энергией образования связи
по-видимому, возмещается энергией образования связи  Это общее соображение показывает важность низкого потенциала ионизации центрального атома, электроотрицательности лигандов и небольших размеров лигандов при образовании соединений инертных газов. Преимущество фтора по сравнению с другими галогенами обусловлено не только величиной его сродства к электрону, но и меньшими его размерами [30]. К сожалению, в настоящее время нельзя сделать более обоснованных заключений.
Это общее соображение показывает важность низкого потенциала ионизации центрального атома, электроотрицательности лигандов и небольших размеров лигандов при образовании соединений инертных газов. Преимущество фтора по сравнению с другими галогенами обусловлено не только величиной его сродства к электрону, но и меньшими его размерами [30]. К сожалению, в настоящее время нельзя сделать более обоснованных заключений.
Такое описание основного состояния фторидов ксенона в терминах представления о вкладе ионных структур соответствует тому, что правило октета в некотором смысле сохраняет силу, что согласуется с обычными химическими представлениями. Аналогичная ситуация возникает и в случае ионов полигалогенидов. Эти ионы служили прототипами при качественной интерпретации связи в фторидах ксенона [14, 17—19]. Отметим, что схема связи, включающая делокализованные  -орбитали и впервые примененная к молекулам с небольшим числом электронов, таким, как гидрид бора, очевидно, чрезвычайно полезна также для описания молекул с большим числом электронов, таких, как ионы полигалогенидов и соединения инертных газов [30].
-орбитали и впервые примененная к молекулам с небольшим числом электронов, таким, как гидрид бора, очевидно, чрезвычайно полезна также для описания молекул с большим числом электронов, таких, как ионы полигалогенидов и соединения инертных газов [30].
Несомненно, что связь в соединениях инертных газов можно понять в рамках обычных полуэмпирических методов квантовой химии. Для понимания природы химической связи в таких молекулах не требуется привлечения новых принципов. В настоящее время невозможно полное априорное теоретическое рассмотрение
этих соединений, но эта трудность является общей проблемой, внутренне присущей квантовомеханическому рассмотрению всех сложных молекулярных систем.
ЛИТЕРАТУРА
(см. скан)
(см. скан)
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Предисловие редакторов русского издания
- Из предисловия редактора английского издания
- Часть 1. Насыщенные соединения
- 1-1. Современное состояние теории электронной структуры молекул
- 2. Одно- и двухэлектронные системы
- 3. Предварительные замечания для многоэлектронных систем
- 4. Задачи для многоэлектронных систем
- 5. Применение теории
- 6. Заключение
- 1-2. Химическое приложение теории молекулярных орбиталей. Галогениды инертных газов
- 2. Модель электронных корреляций
- 3. Модель молекулярных орбиталей
- 4. Модель валентных связей
- 5. Интерпретация физических свойств
- 6. Возбужденные электронные состояния
- 7. Обсуждение теоретических моделей
- 1-3. Теория молекулярных «сигма»-орбиталей и реакционная способность
- 2. Молекулярные «сигма»-орбитали
- 3. Теория химической реакционной способности
- 4. Делокализация электронов в переходном состоянии
- 5. Простая интерпретация реакционной способности насыщенных соединений
- 6. Заключение
- 1-4. Локализованные ССП-орбитали в атомах и молекулах
- 2. Различные возможности в выборе хартри-фоковских орбиталей
- 3. Конкретный выбор хартри-фоковских орбиталей
- 4. Канонические ССП-орбитали
- 5. Внешне локализованные ССП-орбитали
- 6. Внутренне локализованные ССП-орбитали
- 7. Выбор функции разделения
- 8. Построение локализованных орбиталей из произвольной системы ССП-орбиталей
- 9. Локализованные орбитали и симметрия молекул
- 10. Локализованные орбитали при отсутствии симметрии
- 11. Локализованные молекулярные орбитали в системах с делокализованными электронами
- 1-5. Интегральная теорема Гельмана—Фейнмана. Барьеры для внутреннего вращения и изоэлектронные процессы
- 2. Барьеры для внутреннего вращения
- 3. Изоэлектронные процессы
- Чаешь II. «пи»-Электронные системы
- II-1. Общий обзор методов и проблем теории «пи»-электронов
- 2. «пи»-Электронные методы
- 3. Нерешенные вопросы теории «пи»-электронов
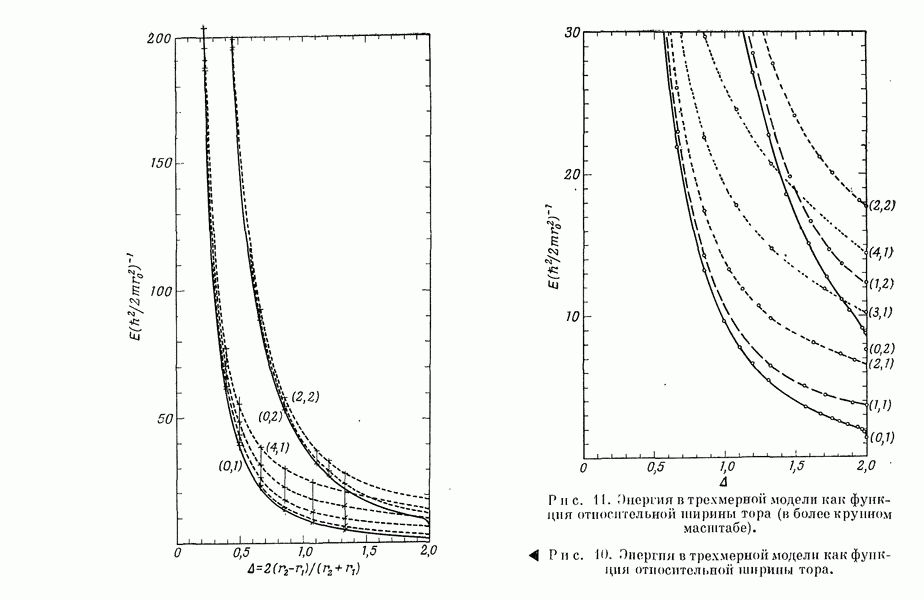
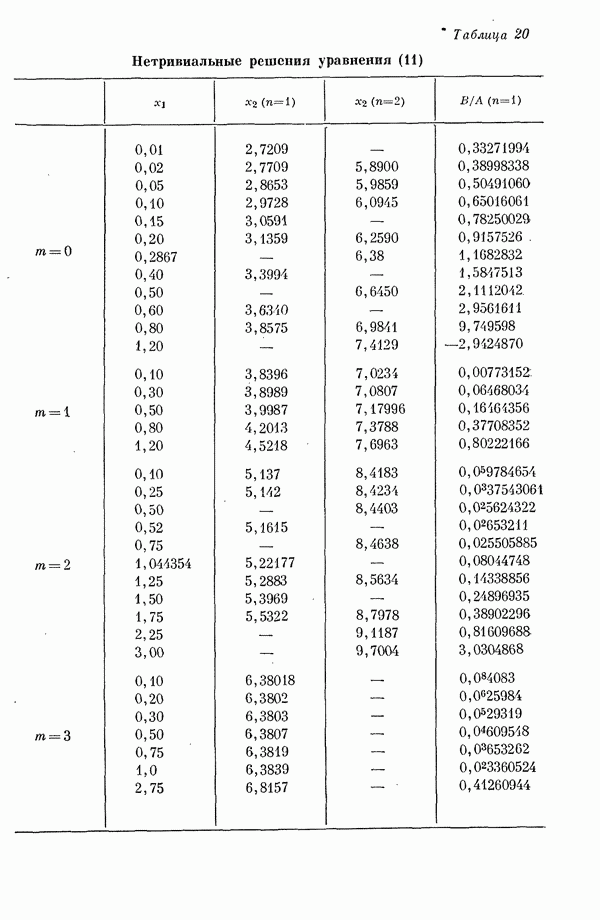
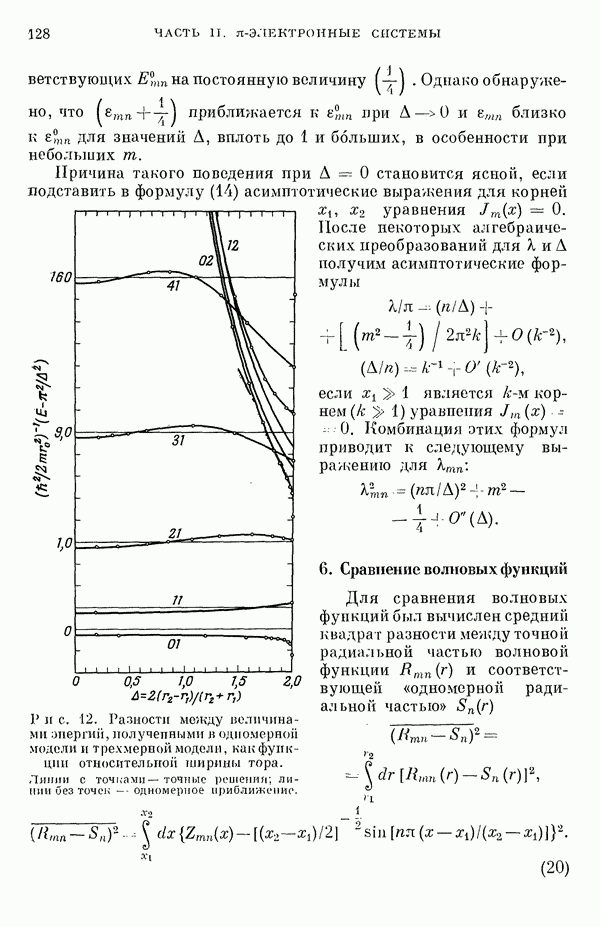
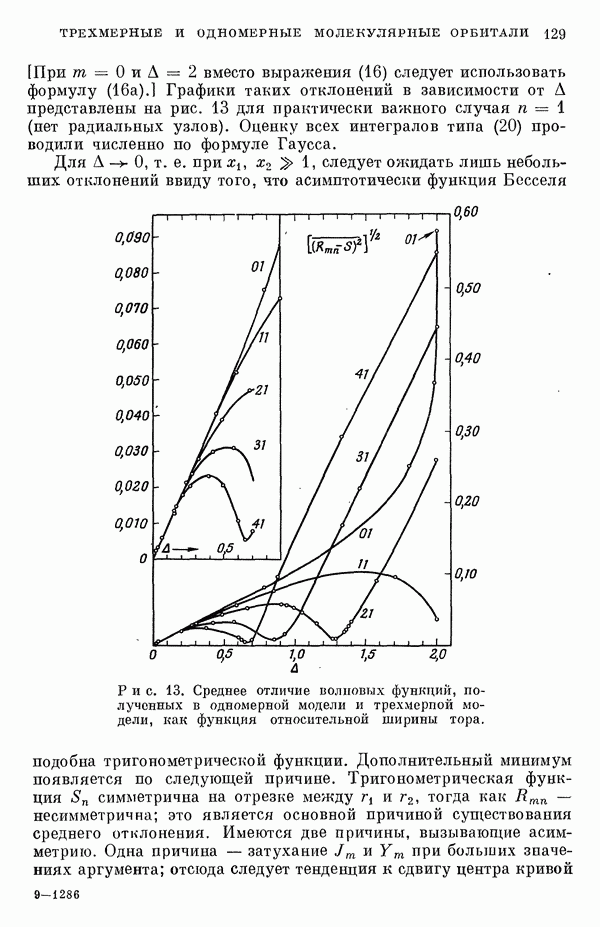
- II-2. Трехмерные и одномерные молекулярные орбитали свободных электронов
- 3. Определение собственных значений как функций А
- II-3. Теория самосогласованного поля для открытых оболочек и применение ее к «пи»-электронным системам
- 2. Уравнения в методе ССП для систем с замкнутыми оболочками. Теорема Бриллюэна
- 3. Условия самосогласования для систем с одной открытой оболочкой, находящихся в дублетных состояниях
- 4. Условия самосогласования для систем, находящихся в триплетных состояниях с двумя открытыми оболочками
- 5. Энергии низших триплетных возбужденных состояний для некоторых четных альтернантных углеводородов, вычисленные с различной степенью самосогласования
- II-4. Перенос заряда и ион-радикалы
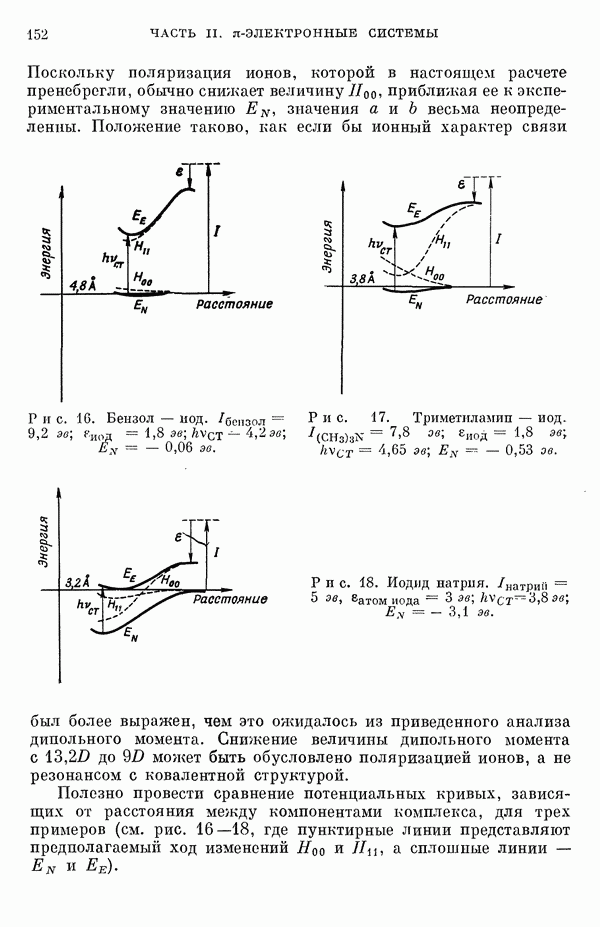
- 3. Слабосвязанные и полунонные комплексы: бензол — иод и триметиламин — иод
- 4. Ионные соединения: иодид натрия
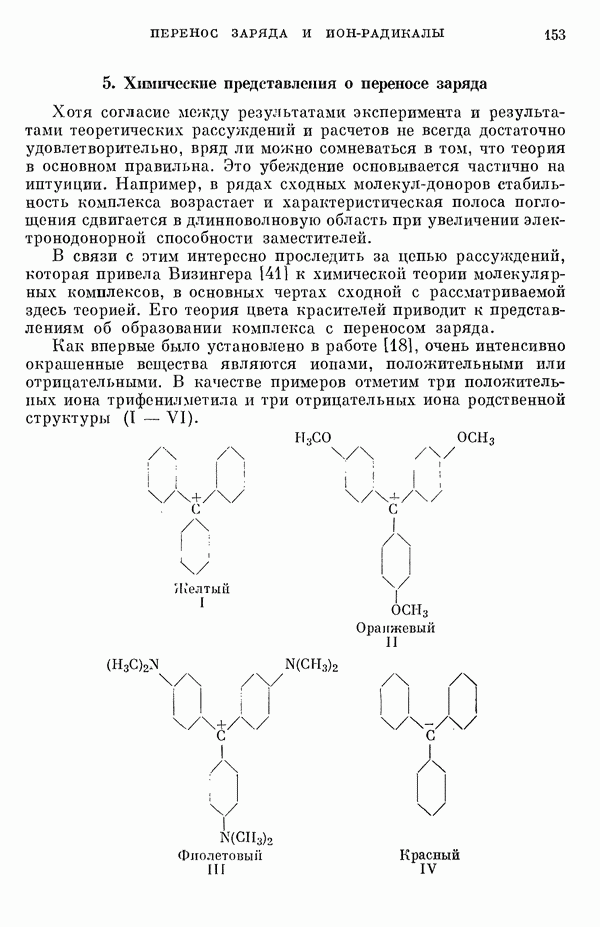
- 5. Химические представления о переносе заряда
- 6. Ион-радикалы
- 7. Фотоионизация
- II-5. Некоторые свойства «пи»-ионов и триплетных состояний
- 2. Ограниченный метод Хартри — Фока
- 3. Неограниченный метод Хартри — Фока
- 4. Энергии и плотности заряда
- 5. Трансформационные свойства орбиталей
- 6. Спиновые свойства функции
- 7. Расщепление триплетных состояний в нулевом поле
- 8. Заключение
- II-6. Критическое обсуждение «пи»-электронных теорий
- II-6A. ПРЕДЕЛЫ ПРИМЕНИМОСТИ МЕТОДОВ ТИПА МЕТОДОВ ХЮККЕЛЯ И ПАРИЗЕРА — ПАРРА
- II-6Б. БАЗИСНЫЕ ОРБИТАЛИ И ПРИБЛИЖЕНИЕ НУЛЕВОГО ДИФФЕРЕНЦИАЛЬНОГО ПЕРЕКРЫВАНИЯ
- 2. Разложение по малому параметру
- 3. Преобразование оператора Фока
- 4. Другая формулировка исходных допущений приближения НДП
- II-6B. ЭЛЕКТРОННОЕ РАСПРЕДЕЛЕНИЕ В ГЕТЕРОЦИКЛИЧЕСКИХ МОЛЕКУЛАХ
- 2. Приближения Паризера — Парра и Хюккеля (Полинга — Уэланда)
- 3. Приближение Паризера — Парра
- 4. Влияние перехода к базису ОАО на распределение зарядов «пи»-электронов на атомах
- 5. Сравнение методов Паризера — Парра — Попла и Хюккеля
- 11-6Г. ПОЛУЭМПИРИЧЕСКИЕ ПАРАМЕТРЫ В ТЕОРИИ МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
- 2. Одноцентровые интегралы
- 3. Двухцентровые интегралы
- II-6Д. РАСЧЕТ СОСТОЯНИЙ МОЛЕКУЛЫ БЕНЗОЛА С УЧЕТОМ КОНФИГУРАЦИОННОГО ВЗАИМОДЕЙСТВИЯ
- II-6E. «пи»-ЭЛЕКТРОННОЕ ПРИБЛИЖЕНИЕ И ПАРАМЕТРЫ ДЛЯ ИНТЕГРАЛОВ КУЛОНОВСКОГО ОТТАЛКИВАНИЯ
- 2. Параметры, связанные с интегралами кулоновского отталкивания
- Часть III. Молекулы и излучение
- III-1. Взаимодействие света с веществом и теория оптической вращающей способности
- 2. Распространение света в прозрачных средах
- 3. Распространение света в среде большого числа отдельных частиц
- 4. Переход от молекулярной теории к феноменологической теории
- 5. Усреднение по физическим элементам объема
- 6. Усреднение микроскопических уравнений Максвелла
- 7. Определение индуцированных молекулярных моментов
- 8. Определение внутреннего поля
- 9. Статистический вывод волнового уравнения
- 10. Квантовохимические аспекты
- III-2. Две теоремы, применяемые в расчетах оптической активности молекул
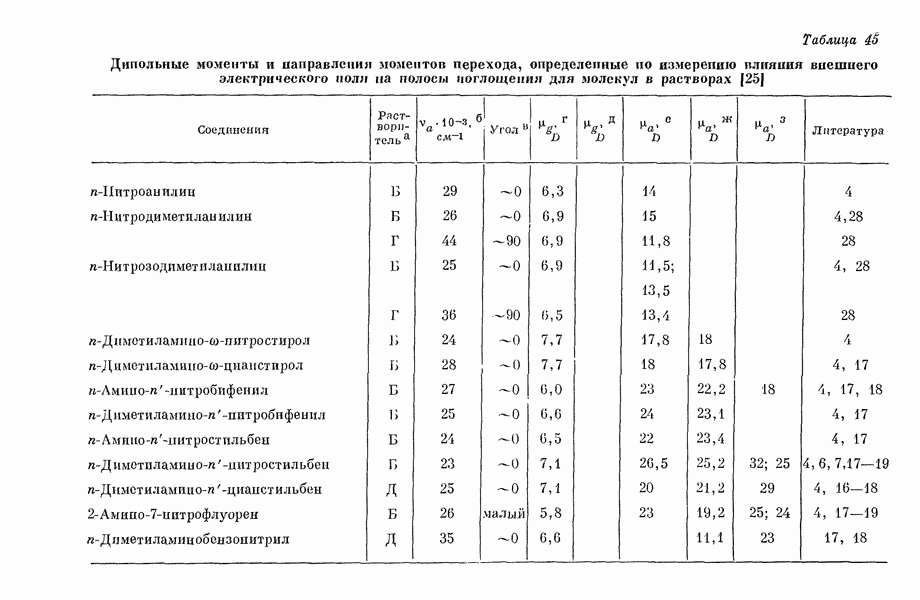
- III-3. Дипольные моменты в возбужденных состояниях молекул и влияние внешнего электрического поля на оптическое поглощение молекул в растворе
- 2. Средние вероятности переходов для молекулы с определенной ориентацией
- 3. Локальное электрическое поле в месте расположения молекулы, находящейся в растворе
- 4. Сдвиг волнового числа
- 5. Зависимость момента перехода от поля
- 6. Средние вероятности перехода для молекулы в статистическом ансамбле при наличии электрического поля
- 7. Приложения
- 8. Приложение. Расчет средних вероятностей перехода
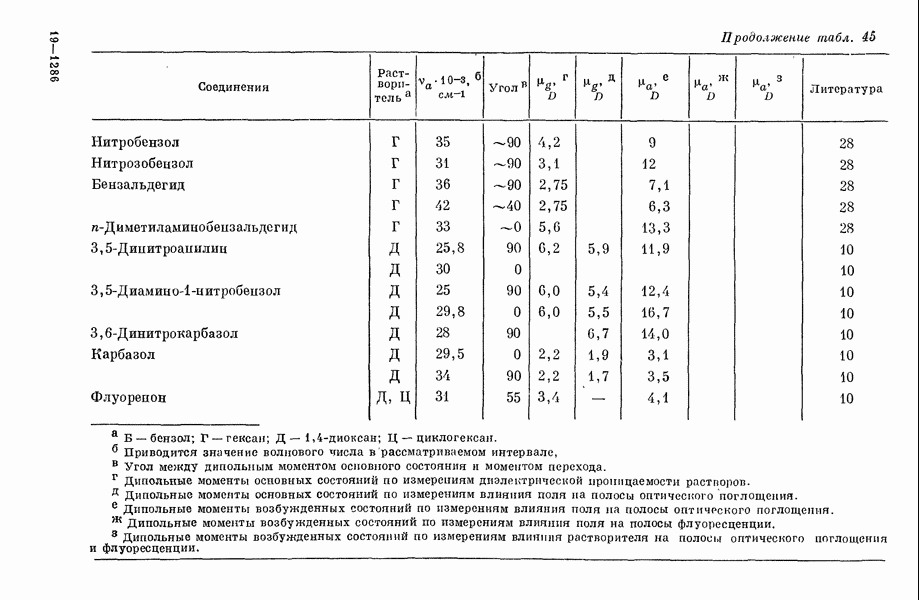
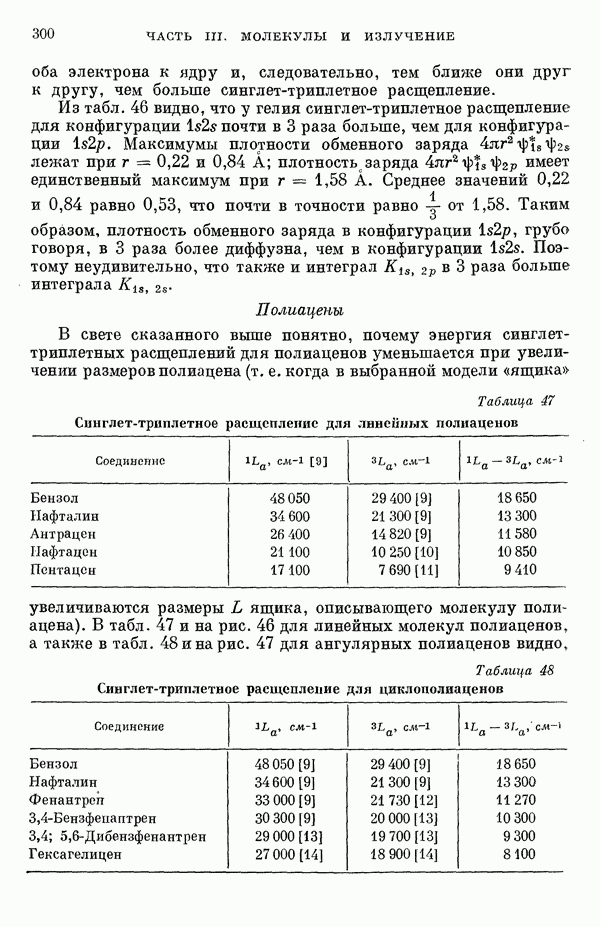
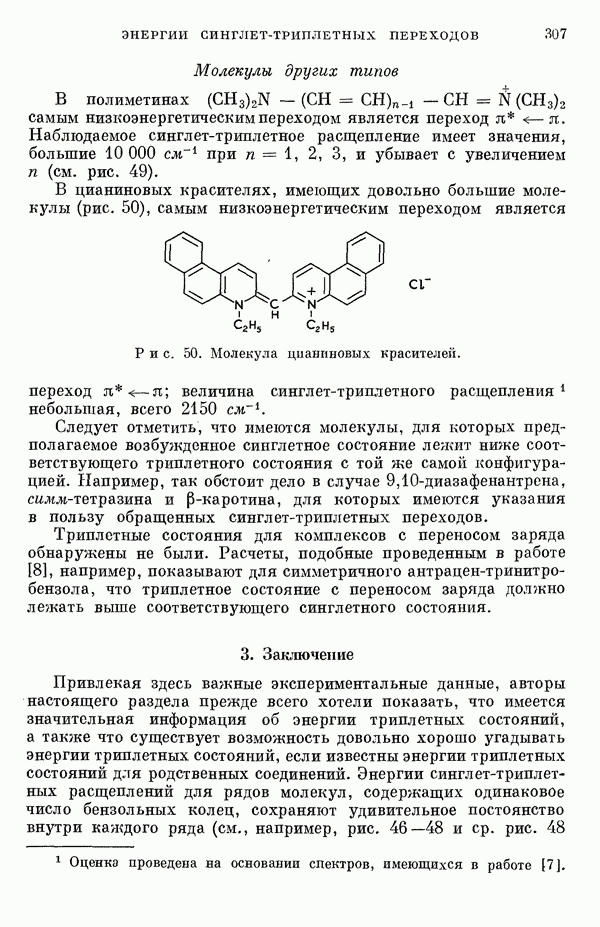
- III-4. Энергии синглет-триплетных переходов
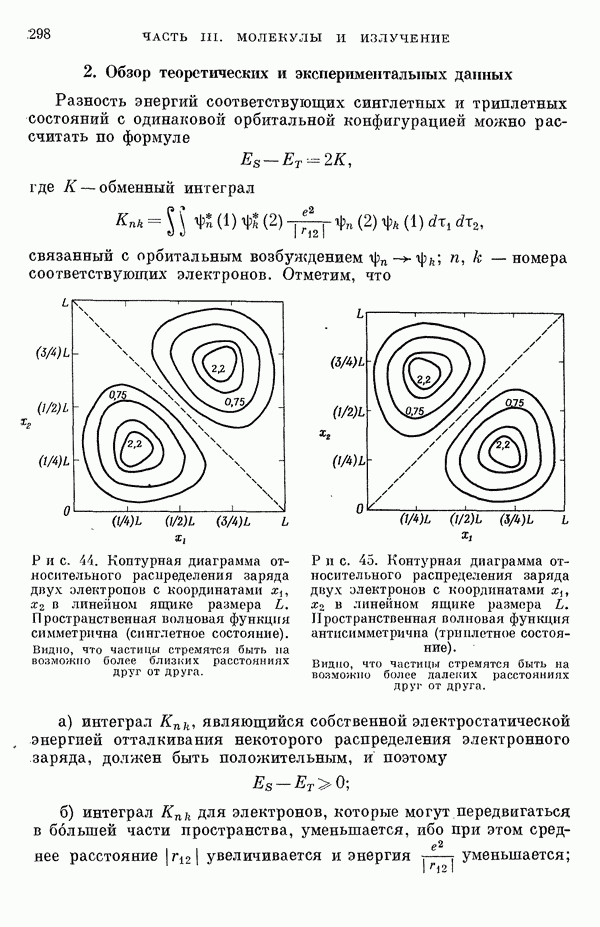
- 2. Обзор теоретических и экспериментальных данных
- 3. Заключение
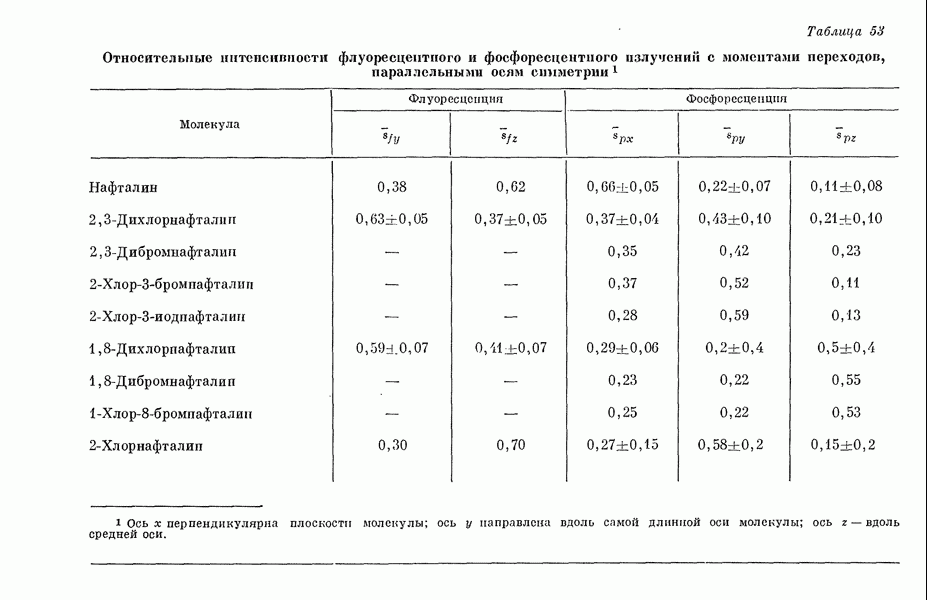
- III-5. Моменты переходов и анизотропия флуоресценции и фосфоресценции
- 2. Степень анизотропии излучения
- 3. Приложения степени анизотропии
- 4. Обсуждение
- Дополнение. Вариационные оценки энергий сверху и снизу