| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 3. Направление аналитических реакций; правила обменного разложения
Протекание аналитических реакций в растворах подчиняется правилам Бертолле. Предложенные более 150 лет тому назад правила Бертолле обычно формулировались следующим образом.
Если смешать две соли АВ и DE, то начавшаяся реакция обменного разложения скоро останавливается, в растворе оказываются четыре соли АВ, DE, АЕ и BD, составляющие равновесную систему:

Этот случай наблюдается, если исходные и образующиеся соли растворимы в воде. Если же хотя бы одно из веществ нерастворимо и, выделяясь в виде газа или в виде осадка, выходит из сферы реакции, то реакция идет до конца в сторону образования этого вещества, т. е. пока не будет исчерпан весь материал для его образования.
На самом деле вещества, образующиеся в процессе реакции, не выходят из сферы реакции, как предполагал Бертолле, так как все реакции в той или иной мере обратимы:

На основе теории электролитической диссоциации, предложенной С. А. Аррениусом, Я. И. Михайленко дал более точную формулировку правилам обменного разложения.
1. Если из пришедших в соприкосновение ионов не могут образоваться неэлектролиты, то реакция не идет — в растворе находятся только одни ионы.
2. Если из пришедших в соприкосновение ионов образуются неэлектролиты, слабые электролиты, или малорастворимые вещества, то:
а) Реакция идет в сторону образования очень слабого электролита практически до конца, например:

или в ионной форме

Здесь направляет реакцию слабый электролит — вода.
б) Реакция идет в сторону образования растворимого в воде слабого электролита не до конца, если «направляющие» вещества имеются как среди конечных, так и среди исходных соединений:

или в ионной форме

Здесь направляющими реакцию веществами являются слабый электролит — вода (в правую сторону) и слабый электролит— уксусная кислота (в левую сторону).
в) Если из пришедших в соприкосновение ионов могут образоваться малорастворимые соединения, то реакция идет в сторону образования этих малорастворимых соединений практически до конца, например:

С. А. Арренаус (1859-1927).

Здесь направляет реакцию малорастворимый в воде хромат бария  , выделяющийся в осадок.
, выделяющийся в осадок.
г) Если из пришедших в соприкосновение ионов образуется малорастворимый в воде газ, то реакция идет в сторону образования этого газа практически до конца, например:

или в ионной форме

Здесь направляет реакцию малорастворимый в воде газ — сероводород.
д) Если из пришедших в соприкосновение частиц образуются слабо диссоциирующие комплексные ионы, то реакция идет в сторону образования этих (комплексных) ионов практически до конца, например:

Здесь направляют реакцию слабо диссоциирующие молекулы  (в левую сторону) и комплексы
(в левую сторону) и комплексы  (в правую сторону).
(в правую сторону).
Таким образом, теория электролитической диссоциации дала возможность понять смысл положений Бертолле, обобщила их и прибавила к ним еще цовое: практически реакция идет до конца, если из ионов может образоваться очень слабый, растворимый в воде электролит (нейтральная молекула или комплексный ион). Высказанные Бертолле более 100 лет назад положения получили новое развитие.
В настоящее время правила Бертолле — Михайленко формулируют следующим образом.
Обменная реакция идет в сторону образования малорастворимого вещества (осадка или газа), нейтральных молекул слабых электролитов и комплексных или сложных ионов.
Примеры обменных аналитических реакций. а) Реакции, идущие с образованием малорастворимых веществ. Например:

или в ионной форме

б) Реакции, идущие с образованием газов. К числу газообразных веществ, образующихся в процессе аналитических реакций, относятся  и некоторые другие.
и некоторые другие.

Я. И. Михайленко (1864—1943).
В случае получения в процессе какой-либо аналитической реакции одного из указанных газов реакция направляется в сторону образования этого газа. Например:

или в ионной форме

в) Реакции, идущие с образованием слабых электролитов. К числу слабых электролитов, образующихся в процессе аналитических реакций, относятся: вода, слабые кислоты и основания и некоторые соли, например  и некоторые другие.
и некоторые другие.
Если в процессе аналитической реакции образуется какой-либо из слабых электролитов, реакция направляется в сторону образования этого электролита. Например:

или в ионной форме

г) Реакции, идущие с образованием комплексных ионов типа  и многие другие.
и многие другие.
Указанные комплексные ионы можно рассматривать как составные части комплексных соединений:  и т. п. В формулах подобных комплексных соединений в квадратные скобки заключают внутреннюю сферу, представляющую собой комплексообразова-тель, и непосредственно связанные с ним ионы и нейтральные молекулы:
и т. п. В формулах подобных комплексных соединений в квадратные скобки заключают внутреннюю сферу, представляющую собой комплексообразова-тель, и непосредственно связанные с ним ионы и нейтральные молекулы:

или в ионной форме

д) Реакции, идущие в сторону образования комплексных ионов, типа  и др. В настоящее время по ряду соображений сложные ионы типа
и др. В настоящее время по ряду соображений сложные ионы типа  и т. п. рассматриваются как комплексные ионы. Например:
и т. п. рассматриваются как комплексные ионы. Например:

В большинстве случаев при смешивании растворов реагирующих веществ протекают обратимые обменные реакции. Например:

 — осадок, растворимый в растворе
— осадок, растворимый в растворе  . Поэтому гидроокись магния неколичественно (не полностью) осаждается гидроокисью аммония.
. Поэтому гидроокись магния неколичественно (не полностью) осаждается гидроокисью аммония.
В процессе, казалось бы, самых разнообразных реакций очень часто образуются одни и те же химические продукты. Например:

Это объясняется тем, что реакции протекают не между отдельными электролитами, а между образующимися при их диссоциации ионами. В рассмотренных случаях — между  и
и  -ионами:
-ионами:

Примечание. Следует иметь в виду, что в водных растворах аммиака не существует недиссоциированных молекул гидроокиси аммония, т. е. молекул состава  . Это объясняется тем, что атом азота
. Это объясняется тем, что атом азота  -слой
-слой  характеризуется наличием лишь четырех валентных орбиталей, принимающих участие в образовании ковалентных связей. В состав недиссоциированных молекул гидроокиси аммония должен был бы входить азот, окруженный десятью электронами (пять ковалентных связей), что противоречит данным теории строения атомов и положению азота в периодической системе элементов Д. И. Менделеева. При растворении аммиака в воде образуется его гидрат
характеризуется наличием лишь четырех валентных орбиталей, принимающих участие в образовании ковалентных связей. В состав недиссоциированных молекул гидроокиси аммония должен был бы входить азот, окруженный десятью электронами (пять ковалентных связей), что противоречит данным теории строения атомов и положению азота в периодической системе элементов Д. И. Менделеева. При растворении аммиака в воде образуется его гидрат  или
или  , который выделен в виде кристаллов, существующих при низкой температуре .
, который выделен в виде кристаллов, существующих при низкой температуре .
Образование ионов аммония в водном растворе можно представить уравнением:

Однако указанное равновесие сильно сдвинуто влево. Поэтому в водных растворах  имеется относительно небольшая концентрация гидроксильных ионов. Вот почему водные растворы аммиака отличаются слабой щелочной реакцией, т. е. ведут себя как растворы слабых оснований.
имеется относительно небольшая концентрация гидроксильных ионов. Вот почему водные растворы аммиака отличаются слабой щелочной реакцией, т. е. ведут себя как растворы слабых оснований.
В дальнейшем ради простоты и для удобства написания уравнений некоторых реакций вместо формулы гидрата аммиака мы будем иногда писать формулу гидроокиси аммония  . Однако еще раз подчеркиваем, что такого рода формула условна.
. Однако еще раз подчеркиваем, что такого рода формула условна.
Для полной характеристики направления аналитических реакций дополним этот раздел примерами реакций, протекающих под влиянием изменения зарядов реагирующих веществ. Например, некоторые сульфиды металлов ( и др.) не растворяются в воде и хлористоводородной кислоте, но стоит только обработать сульфид окислителем, способным окислить сульфидную серу в элементарную или сульфатную серу, как под влиянием изменения заряда сульфидной серы сульфид растворяется:
и др.) не растворяются в воде и хлористоводородной кислоте, но стоит только обработать сульфид окислителем, способным окислить сульфидную серу в элементарную или сульфатную серу, как под влиянием изменения заряда сульфидной серы сульфид растворяется:

| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Анализ и синтез
- § 2. Предмет аналитической химии
- § 3. Развитие аналитической химии
- § 4. Качественный и количественный анализ
- ГЛАВА I. ПРИМЕНЕНИЕ ЗАКОНА ДЕЙСТВИЯ МАСС В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Влияние среды на состояние ионов в растворах
- § 2. Обратимые и необратимые аналитические реакции
- § 3. Направление аналитических реакций; правила обменного разложения
- § 4. Закон действия масс и следствие из него
- § 5. Границы применимости закона действия масс
- § 6. Сильные и слабые электролиты
- § 7. Активность
- § 8. Коэффициент активности и ионная сила
- Б. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ (В ГОМОГЕННЫХ СИСТЕМАХ)
- § 9. Гомогенные и гетерогенные системы
- § 10. Ионное произведение воды
- § 11. Ионы гидроксония
- § 12. Равновесие ионов в водных растворах; понятие о pH
- § 13. Равновесие в водных растворах слабых электролитов
- § 14. Влияние сильных кислот или сильных оснований на степень электролитической диссоциации слабых электролитов
- § 15. Приближенные формулы для расчета [H+] и [OH-] в водных растворах кислот и оснований
- В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
- § 16. Буферные растворы
- § 17. Применение буферных растворов в химическом анализе
- Г. РАВНОВЕСИЯ В РАСТВОРАХ ГИДРОЛИЗУЮЩИХСЯ СОЛЕЙ
- § 18. Теоретические основы гидролиза
- § 19. Механизм гидролитического расщепления
- § 20. Подавление и усиление гидролиза солей
- Д. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ТИПИЧНО АМФОТЕРНЫХ ЭЛЕКТРОЛИТОВ
- § 21. Поведение амфотерных гидроокисей в водных растворах
- § 22. Константы электролитической диссоциации амфотерных гидроокисей
- Е. РАВНОВЕСИЯ В СИСТЕМАХ: ОСАДОК-НАСЫЩЕННЫЙ РАСТВОР
- § 23. Осаждение как один из основных методов химического анализа
- § 24. Произведение растворимости
- § 25. Произведение активностей
- § 26. Вычисление растворимости электролитов в воде по величине произведения растворимости
- § 27. Влияние различных факторов на растворимость малорастворимых электролитов
- Ж. ОСНОВЫ ТЕОРИИ ОБРАЗОВАНИЯ И РАЗЛОЖЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИИ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 28. Характеристика комплексных соединений, имеющих значение в химическом анализе
- § 29. Квантовомеханические представления о строении комплексов
- § 30. Равновесия в растворах комплексных соединений
- § 31. Константы нестойкости комплексов
- § 32. Внутрикомплексные соединения
- § 33. Методы разложения и образования комплексов, применяемых в аналитической химии
- § 34. Применение метода комплексообразования в химическом анализе
- ГЛАВА II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Окисление—восстановление как один из основных методов химического анализа
- § 2. Направление реакций окисления—восстановления
- § 3. Окислительно-восстановительные потенциалы
- § 4. Зависимость между величинами окислительно-восстановительных потенциалов и условиями, в которых протекают реакции окисления—восстановления
- § 5. Вычисление окислительно-восстановительных потенциалов
- § 6. Вычисление окислительно-восстановительных потенциалов с учетом коэффициентов активности
- ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
- § 1. Обнаружение отдельных элементов
- § 2. Анализ мокрым и сухим путем
- § 3. Химические и физические методы качественного анализа
- § 4. Макро-, полумикро- и микрометоды
- § 5. Капельный анализ
- § 6. Микрокристаллоскопический анализ
- § 7. Метод растирания порошков
- § 8. Методы анализа, основанные на нагревании и сплавлении веществ
- § 9. Спектральный качественный анализ
- § 10. Хроматографический метод анализа
- § 11. Кинетические методы анализа
- Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
- § 12. Специфичность и чувствительность реакций
- § 13. Максимальная чувствительность аналитических реактивов
- § 14. Способы повышения чувствительности реакций
- § 15. Маскировка мешающих ионов
- § 16. Определение pH среды
- § 17. Регулирование pH среды в процессе аналитических определений
- В. РЕАКТИВЫ
- § 18. Понятие о химических реактивах
- § 19. Концентрация применяемых реактивов
- § 20. Техника пользования реактивами
- Г. ПОСУДА И ПРИБОРЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕННОМ АНАЛИЗЕ
- § 21. Химическая посуда
- § 22. Приборы
- Д. АНАЛИТИЧЕСКИЕ ГРУППЫ
- § 23. Дробный и систематический анализ
- § 24. Аналитическая классификация катионов
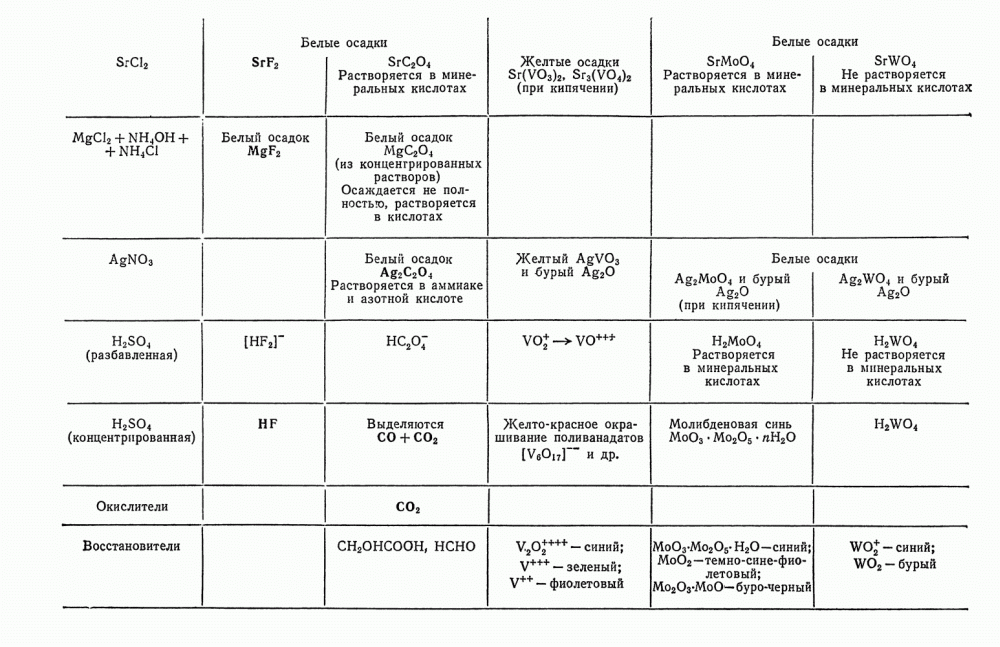
- § 25. Сводные таблицы действия реактивов на катионы и анионы
- Е. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ ИОНОВ
- § 26. Значение периодического закона в аналитической химии
- § 27. Периодическая система элементов Д. И. Менделеева как классификация атомов по их строению
- § 28. Зависимость некоторых химических свойств элементов от положения их в периодической системе Д. И. Менделеева
- § 29. Растворимость химических соединений в связи с положением элементов в периодической системе Д. И. Менделеева
- § 30. Открытие новых аналитических реакций
- § 31. Аналитические группы и периодическая система элементов Д. И. Менделеева
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ КАТИОНОВ И АНАЛИЗ СМЕСЕЙ КАТИОНОВ
- § 1. Характеристика первой аналитической группы катионов
- § 2. Общие реакции катионов первой аналитической группы
- РЕАКЦИИ КАТИОНОВ 1-й ПОДГРУППЫ
- § 3. Обнаружение NН-ионов
- § 4. Методы разложения и удаления солей аммония
- § 5. Обнаружение K-ионов
- § 6. Обнаружение Rb-ионов
- § 7. Обнаружение Cs-ионов
- § 8. Анализ смеси катионов первой подгруппы
- РЕАКЦИИ КАТИОНОВ 2-й ПОДГРУППЫ
- § 9. Обнаружение Li-ионов
- § 10. Обнаружение Na-ионов
- § 11. Обнаружение Mg-ионов
- § 12. Обзор действия реактивов на катионы первой аналитической группы
- § 13. Анализ смеси катионов второй подгруппы
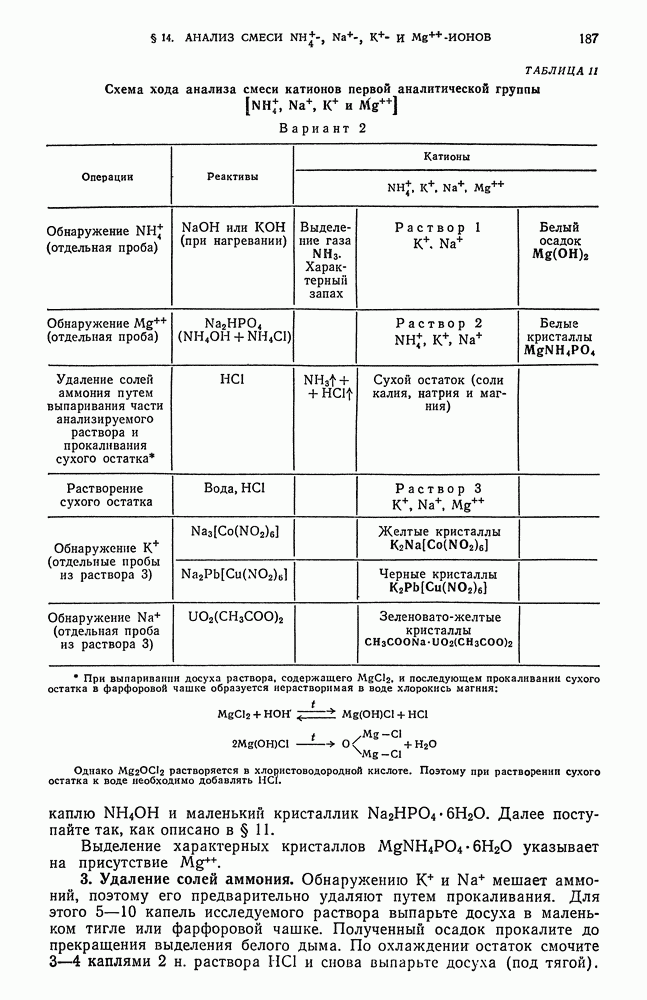
- § 14. Анализ смеси ионов
- § 15. Анализ смеси ионов
- ГЛАВА V. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика второй аналитической группы катионов
- § 2. Общие реакции катионов второй аналитической группы
- § 3. Обнаружение Ca-ионов
- § 4. Обнаружение Sr-ионов
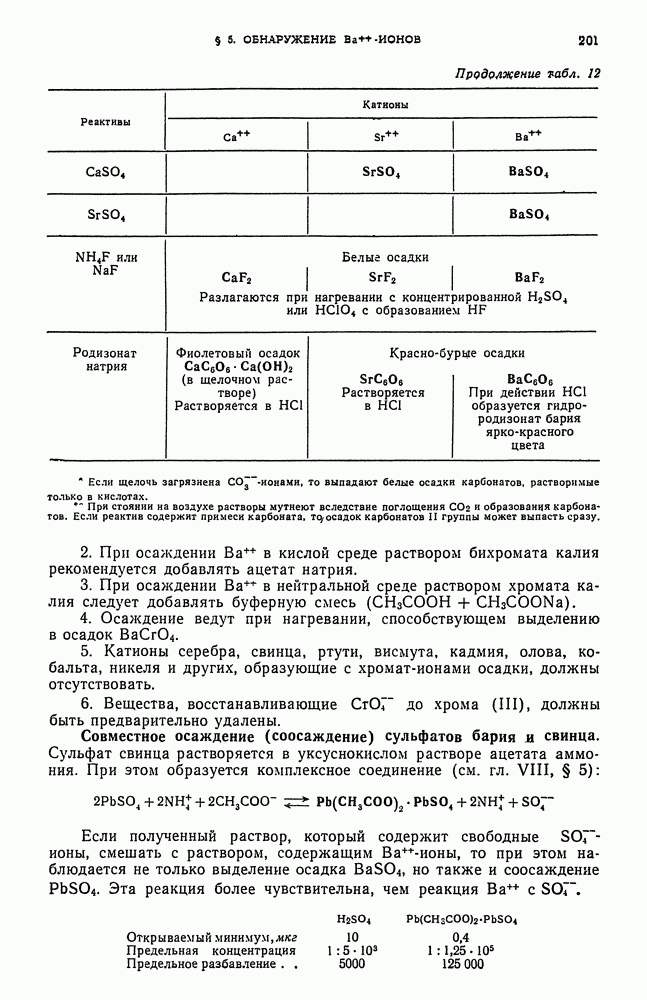
- § 5. Обнаружение Ba-ионов
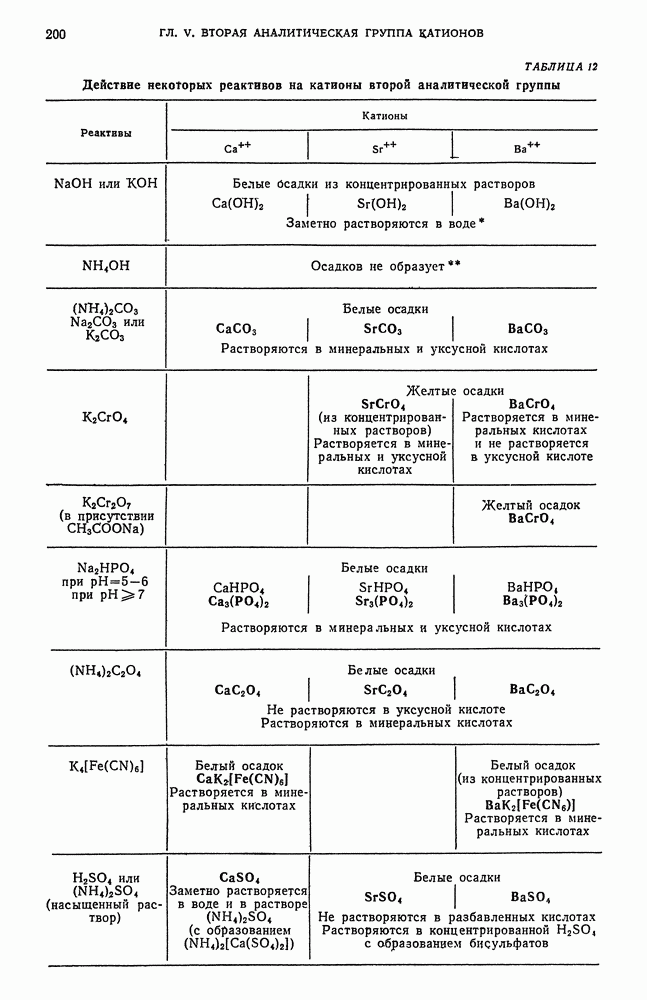
- § 6. Обзор действия реактивов на катионы второй аналитической группы
- § 7. Основы теории осаждения катионов второй аналитической группы групповым реактивом—карбонатом аммония
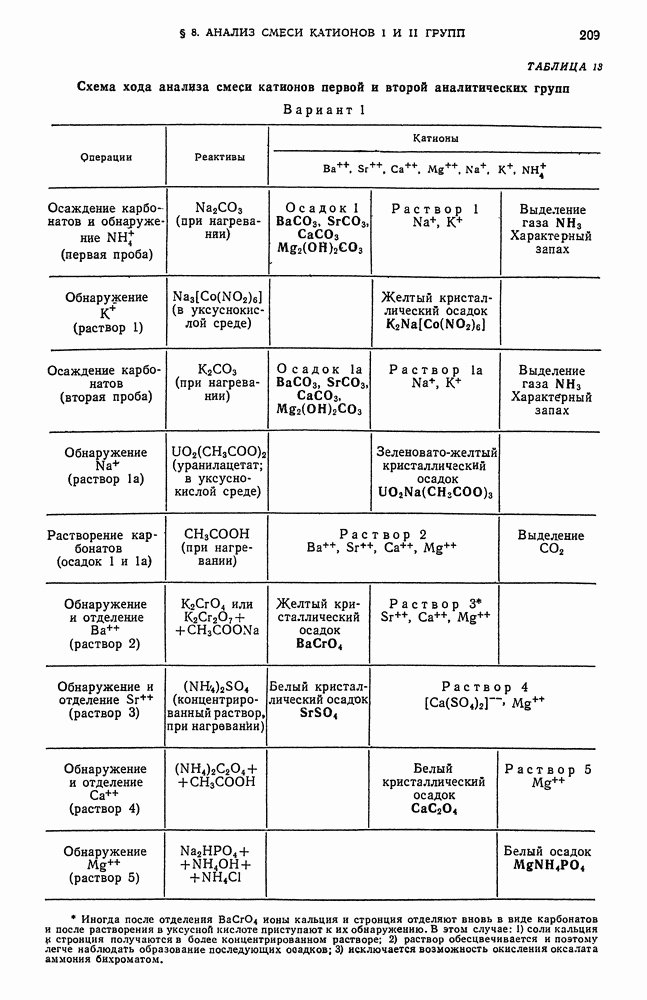
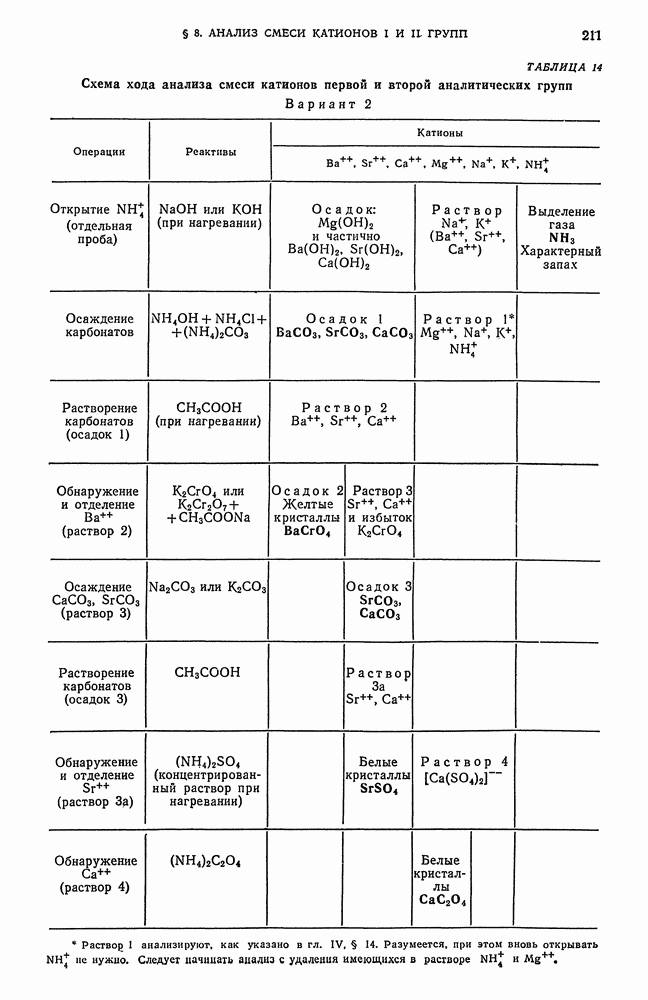
- § 8. Систематический ход анализа смеси катионов первой и второй аналитических групп
- § 9. Систематический ход анализа смеси катионов первой и второй аналитических групп в присутствии ионов
- § 10. Теоретические основы перевода сульфатов катионов второй аналитической группы в карбонаты
- ГЛАВА VI. ТРЕТЬЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика третьей аналитической группы катионов
- § 2. Общие реакции катионов третьей аналитической группы
- § 3. Обнаружение Be-ионов
- § 4. Обнаружение Al-ионов
- § 5. Обнаружение ионов титана (IV)
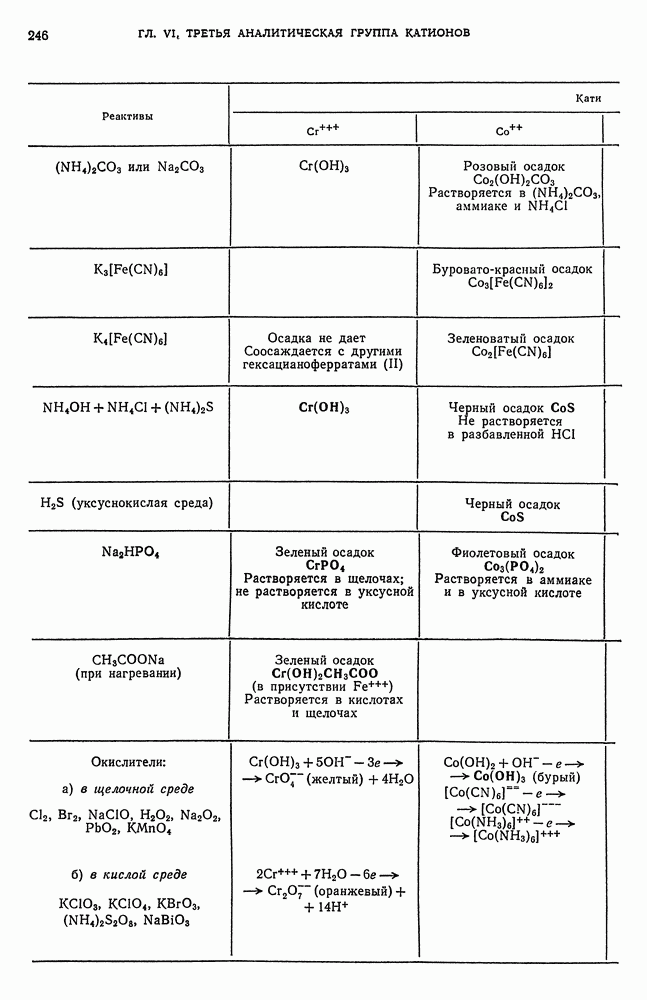
- § 6. Обнаружение Cr-ионов
- § 7. Обнаружение Mn-ионов
- § 8. Обнаружение Fe-ионов
- § 9. Обнаружение Fe-ионов
- § 10. Обнаружение Co-ионов
- § 13. Обнаружение ионов циркония (IV)
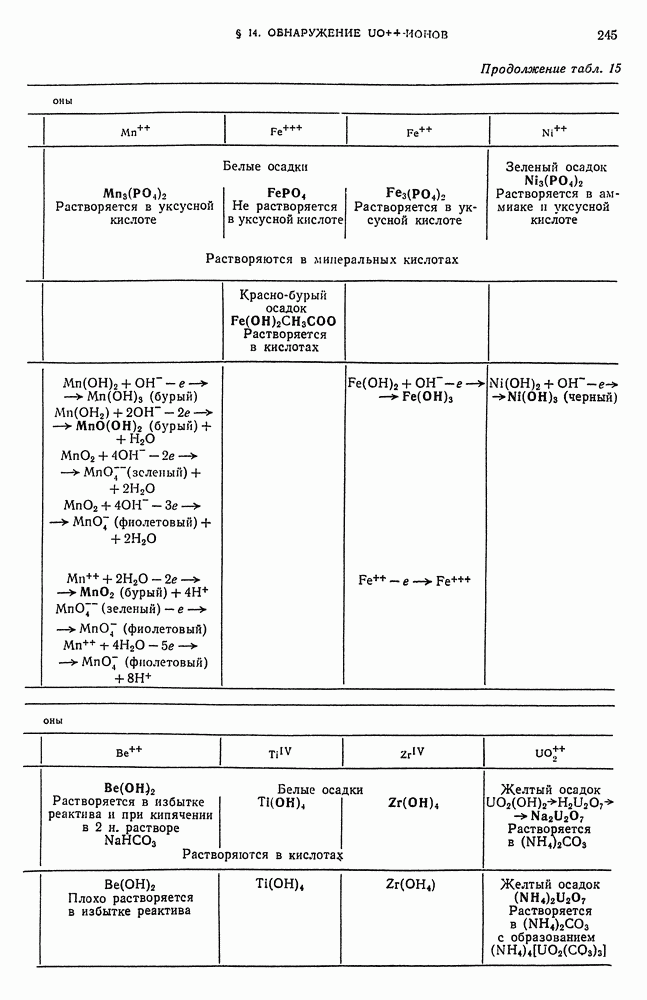
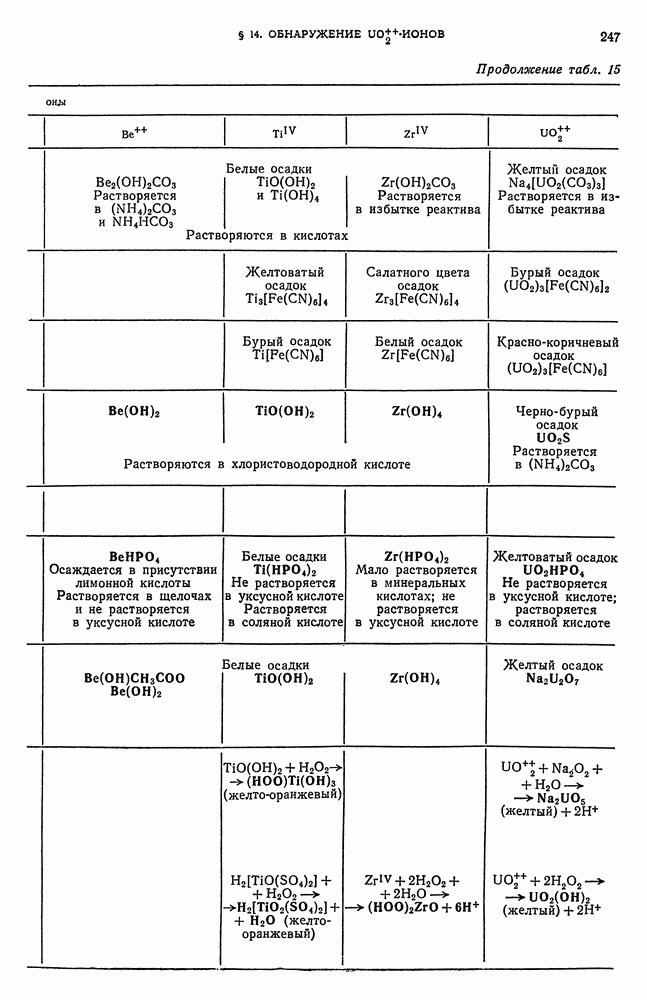
- § 14. Обнаружение UO-ионов
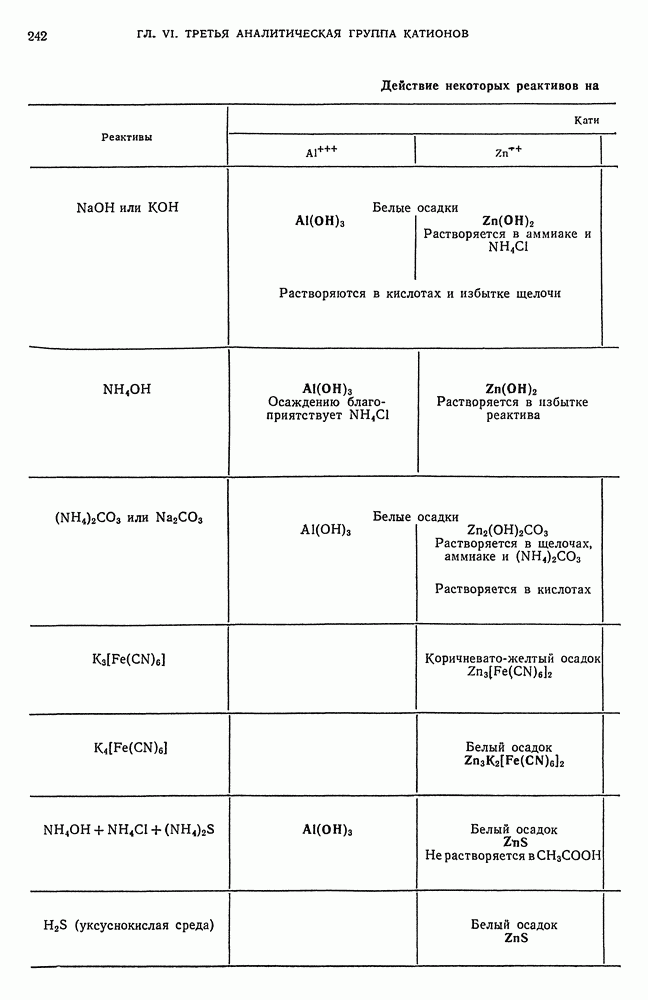
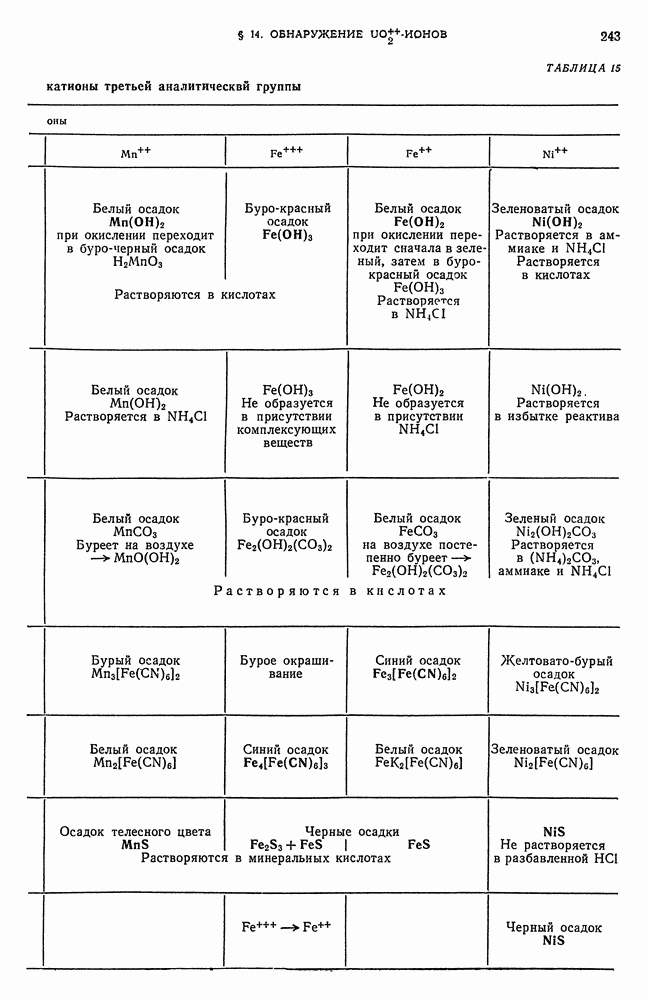
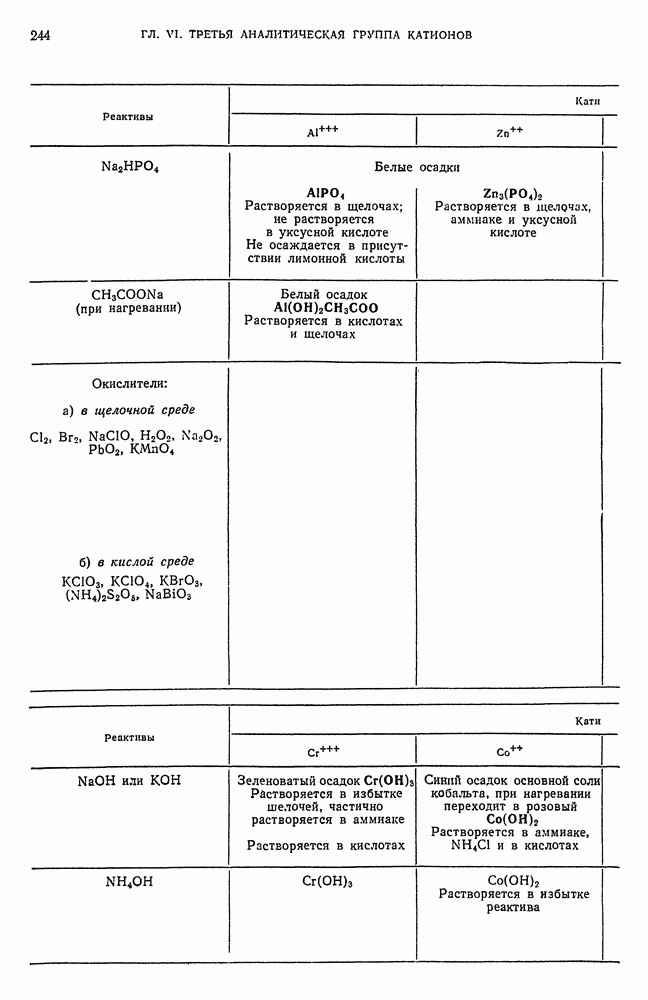
- § 15. Обзор действия реактивов на катионы третьей аналитической группы
- § 16. Использование коллоидных систем в химическом анализе
- § 17. Основы теории осаждения катионов третьей аналитической группы групповым реактивом — сульфидом аммония
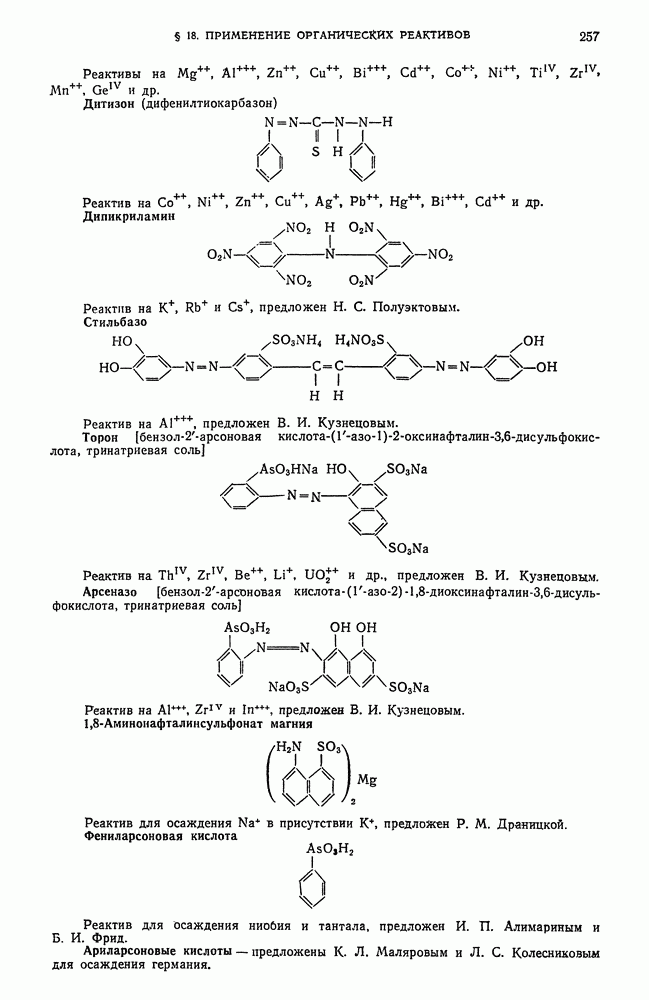
- § 18. Теоретические основы применения органических реактивов в качественном анализе неорганических веществ
- § 19. Методы разделения некоторых катионов третьей аналитической группы
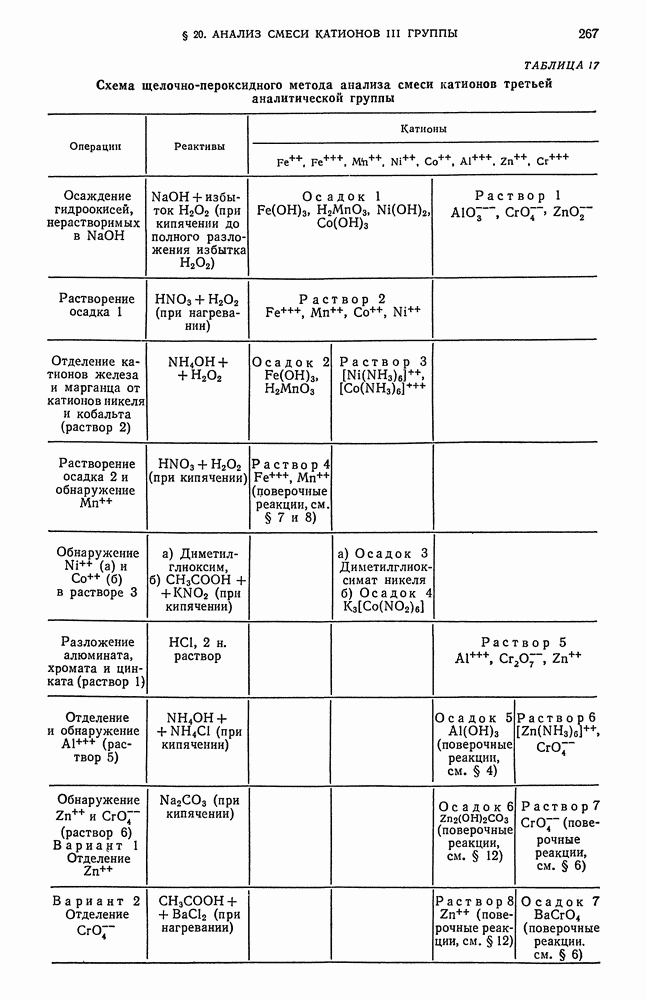
- § 20. Систематический ход анализа смеси катионов третьей аналитической группы
- § 21. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп
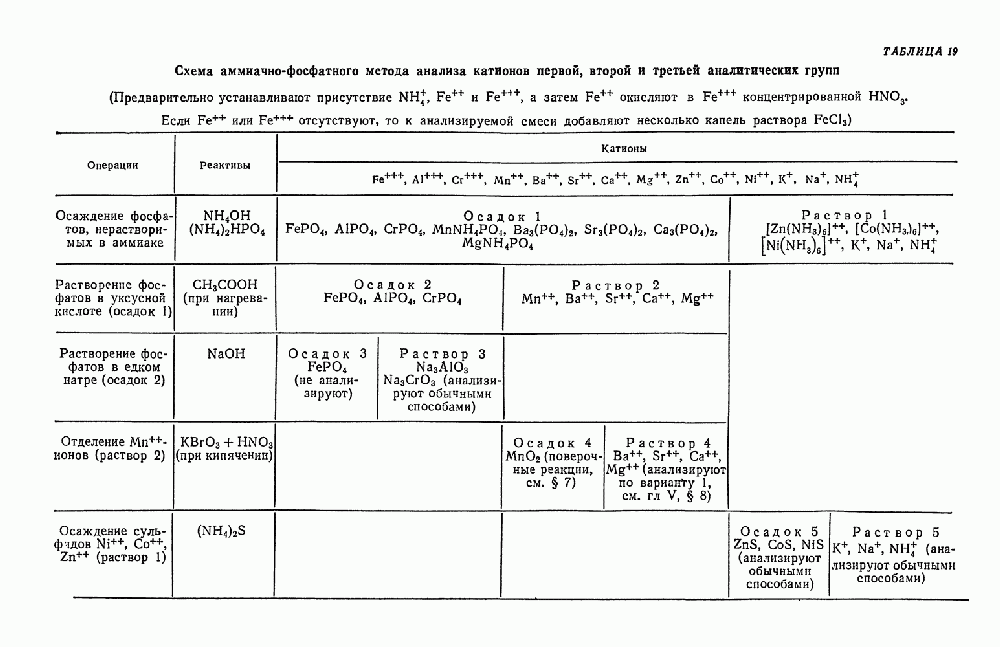
- § 22. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп в присутствии PO-ионов
- ГЛАВА VII. ЧЕТВЕРТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика четвертой аналитической группы катионов
- § 2. Общие реакции катионов четвертой аналитической группы
- РЕАКЦИИ КАТИОНОВ ПЕРВОЙ ПОДГРУППЫ (ПОДГРУППЫ МЕДИ)
- § 3. Обнаружение Hg-ионов
- § 4. Обнаружение Cu-ионов
- § 5. Обнаружение Cd-ионов
- § 6. Обнаружение Bi-ионов
- РЕАКЦИИ КАТИОНОВ ВТОРОЙ ПОДГРУППЫ (ПОДГРУППЫ МЫШЬЯКА)
- § 7. Обнаружение ионов мышьяка (III)
- § 8. Обнаружение ионов мышьяка (V)
- § 9. Общие реакции обнаружения
- § 10. Обнаружение ионов сурьмы (III)
- § 11. Обнаружение ионов сурьмы (V)
- § 12. Общие реакции обнаружения Sb
- § 13. Обнаружение ионов олова (II)
- § 14. Обнаружение ионов олова (IV)
- § 15. Общие реакции обнаружения ионов олова (II) и олова (IV)
- § 16. Отделение ионов олова от других ирнов четвертой аналитической группы
- § 17. Обнаружение ионов германия (IV)
- § 18. Отделение ионов германия от других ионов четвертой аналитической группы
- § 19. Обзор действия реактивов на катионы четвертой аналитической группы
- § 20. Основы теории осаждения сульфидов катионов четвертой аналитической группы групповым реактивом — сероводородом
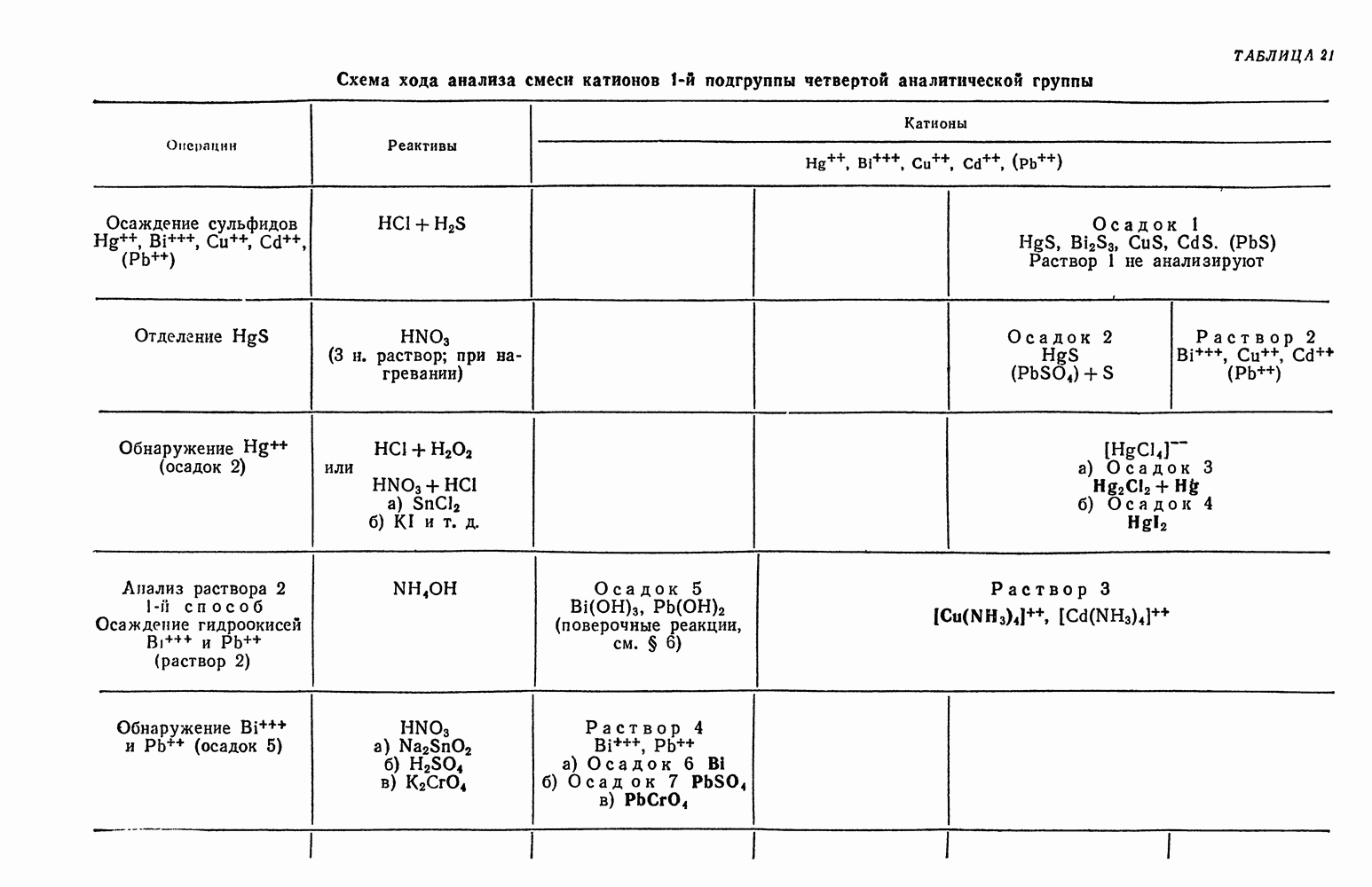
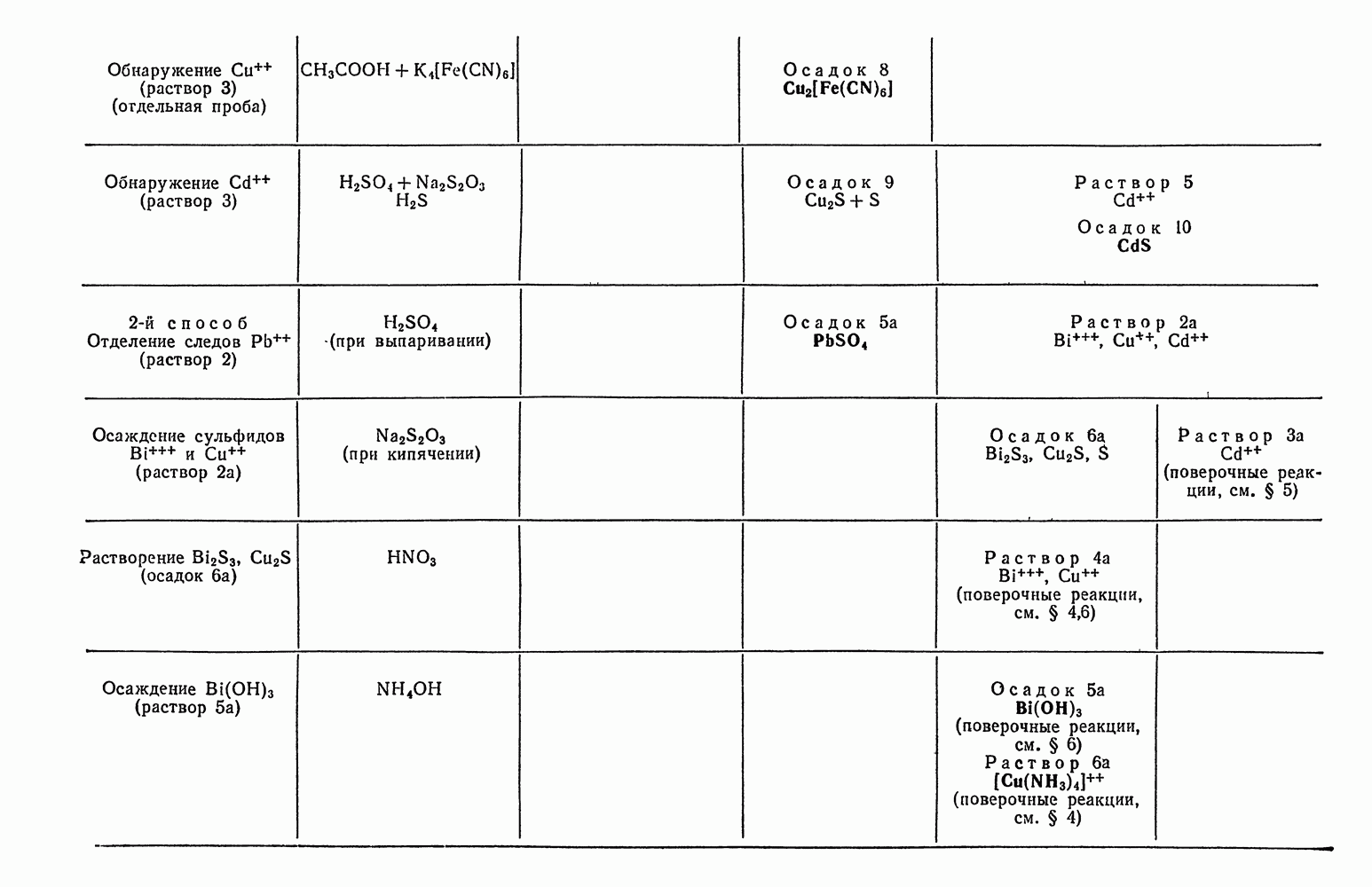
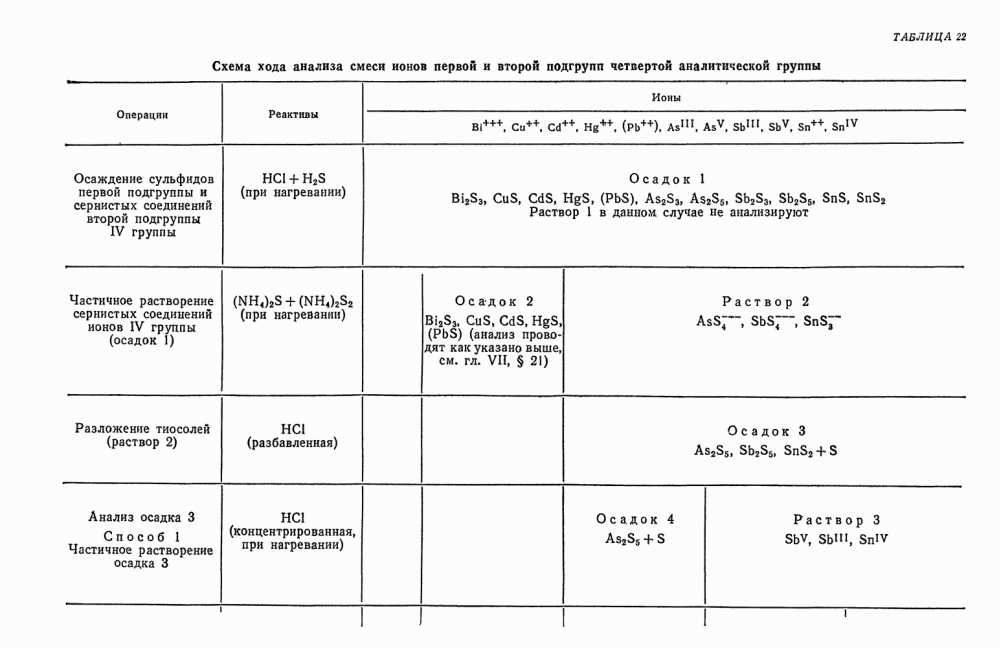
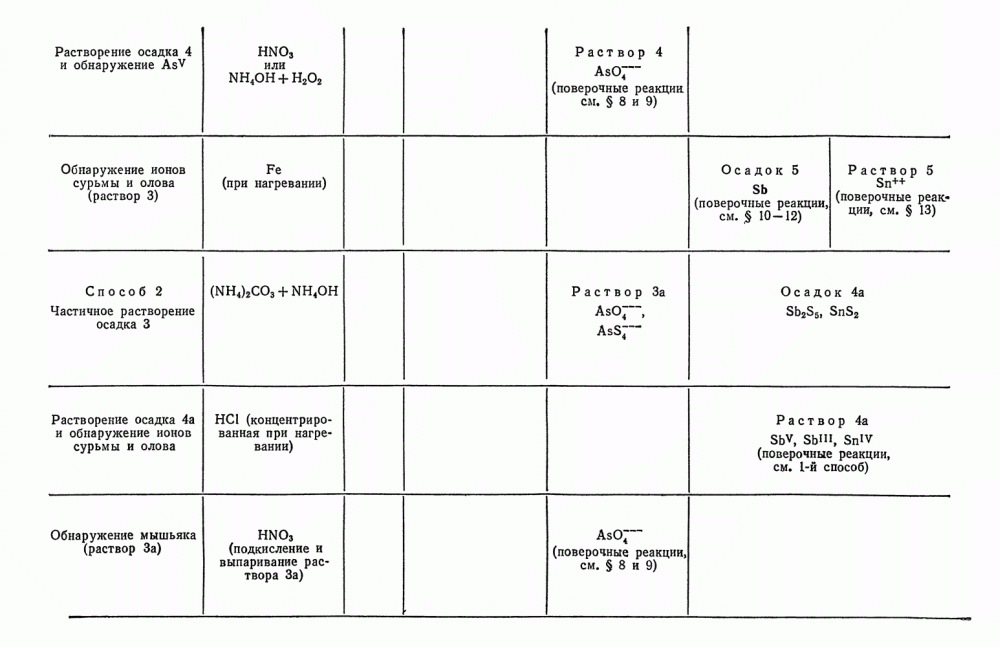
- § 21. Систематический ход анализа смеси катионов четвертой аналитической группы
- ГЛАВА VIII. ПЯТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ (ГРУППА СЕРЕБРА)
- § 1. Характеристика пятой аналитической группы катионов
- § 2. Общие реакции катионов пятой аналитической группы
- § 3. Обнаружение Ag-ионов
- § 4. Обнаружение [Hg]-ионов
- § 5. Обнаружение Pb-ионов
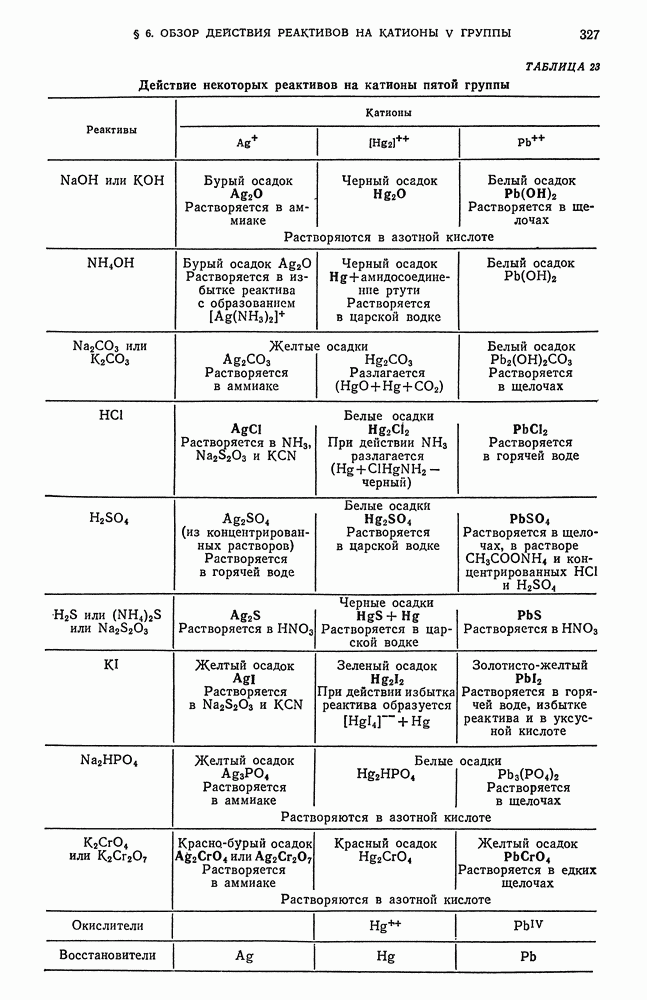
- § 6. Обзор действия реактивов на катионы пятой аналитической группы
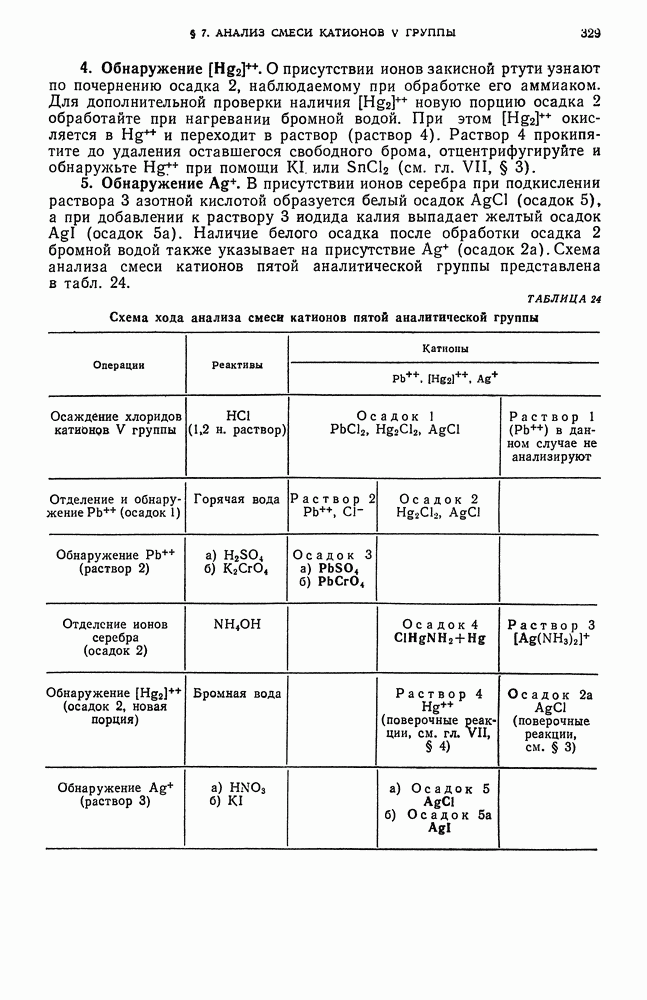
- § 7. Систематический ход анализа смеси катионов пятой аналитической группы
- ГЛАВА IX. АНАЛИЗ СМЕСИ ИОНОВ ВСЕХ ПЯТИ АНАЛИТИЧЕСКИХ ГРУПП
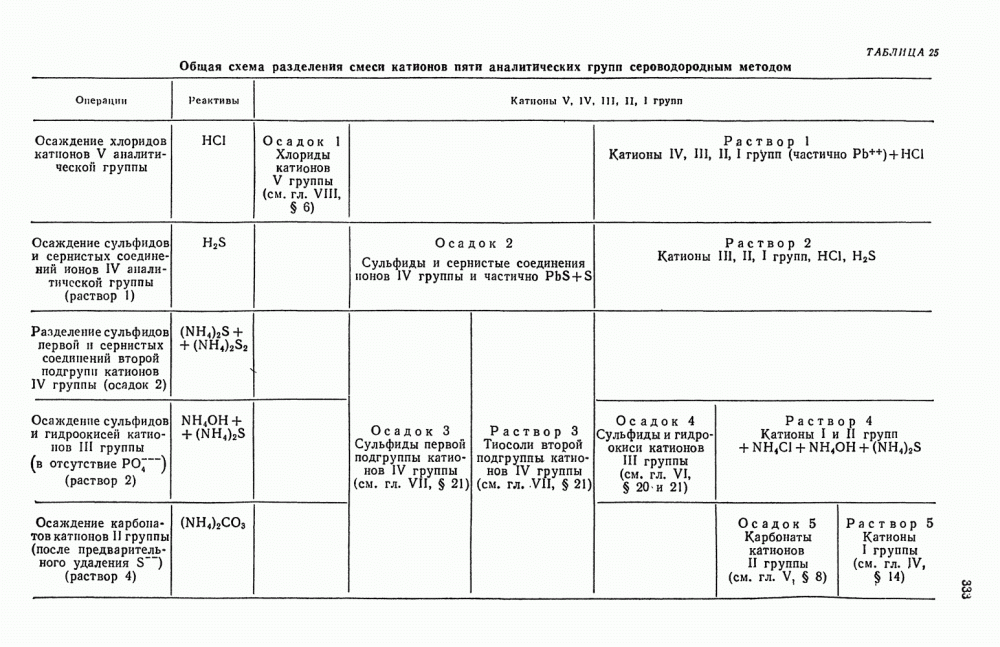
- § 1. Сероводородный метод анализа
- § 2. Недостатки сероводородного метода анализа
- § 3. Ошибки, возникающие при анализе смеси ионов пяти аналитических групп
- § 4. Бессероводородные методы анализа
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ АНИОНОВ И АНАЛИЗ СМЕСЕЙ АНИОНОВ
- § 1. Аналитическая классификация анионов
- § 2. Групповые реактивы на анионы
- § 3. Классификация методов анализа анионов
- ГЛАВА XI. ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика первой группы анионов
- § 2. Реакции анионов первой группы
- § 3. Обнаружение CI-ионов
- § 4. Обнаружение Br-ионов
- § 5. Обнаружение I-ионов
- § 6. Обнаружение CN-ионов
- § 7. Обнаружение SCN-ионов
- § 8. Обнаружение [Fe(CN)]-ионов
- § 9. Обнаружение Fe(CN)-ионов
- § 10. Обнаружение NO-ионов
- § 11. Обнаружение NO2-ионов
- § 12. Обнаружение S-ионов
- § 13. Обнаружение CH3COOO-ионов
- § 14. Обнаружение BrO3-ионов
- § 15. Обнаружение ClO3-ионов
- § 16. Обнаружение ClO4-ионов
- § 17. Обзор действия реактивов на анионы первой группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 18. Анализ смеси Cl, Br и I-ионов
- § 19. Анализ смеси Cl, Br, I и SCN-ионов
- § 20. Анализ смеси Cl, ClO3 и ClO4-ионов
- § 21. Анализ смеси NO2 и NO3-ионов
- § 22. Анализ смеси анионов первой группы
- ГЛАВА XII. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика второй группы анионов
- § 2. Общие реакции анионов второй группы
- § 3. Обнаружение SO3-ионов
- § 4. Обнаружение S2O3-ионов
- § 5. Обнаружение S2O3 в присутствии SO3-ионов
- § 6. Обнаружение SO4-ионов
- § 7. Обнаружение CO3-ионов
- § 8. Обнаружение CO3-ионов в присутствии SO3 и S2O3-ионов
- § 9. Обнаружение PO4-ионов
- § 10. Обнаружение CrO4-ионов
- § 11. Обнаружение AsO3-ионов
- § 12. Обнаружение AsO4-ионов
- § 13. Обнаружение BO2 и BO3-ионов
- § 14. Обнаружение SiO3-ионов
- § 15. Обнаружение F-ионов
- § 16. Обнаружение C2O4-ионов
- § 17. Обнаружение VO3-ионов
- § 18. Обнаружение MoO4-ионов
- § 19. Обнаружение WO4-ионов
- § 20. Обзор действия реактивов на анионы второй группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 21. Анализ смеси ионов
- § 22. Анализ смеси SO3, SO4, S2O3 и CO3-ионов
- § 23. Анализ смеси VO2, MoO4 и WO4-ионов
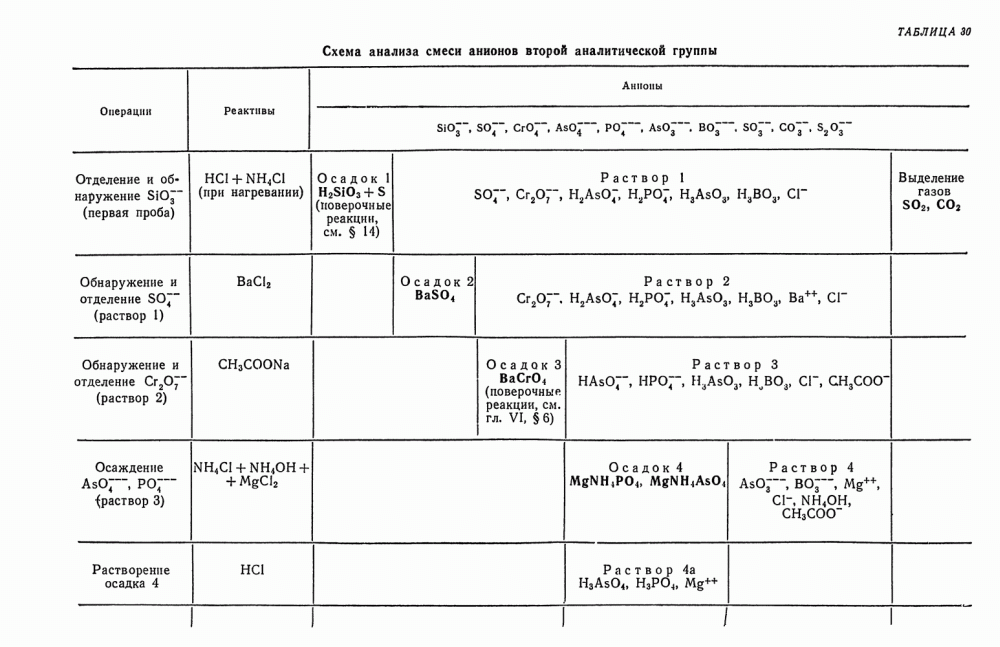
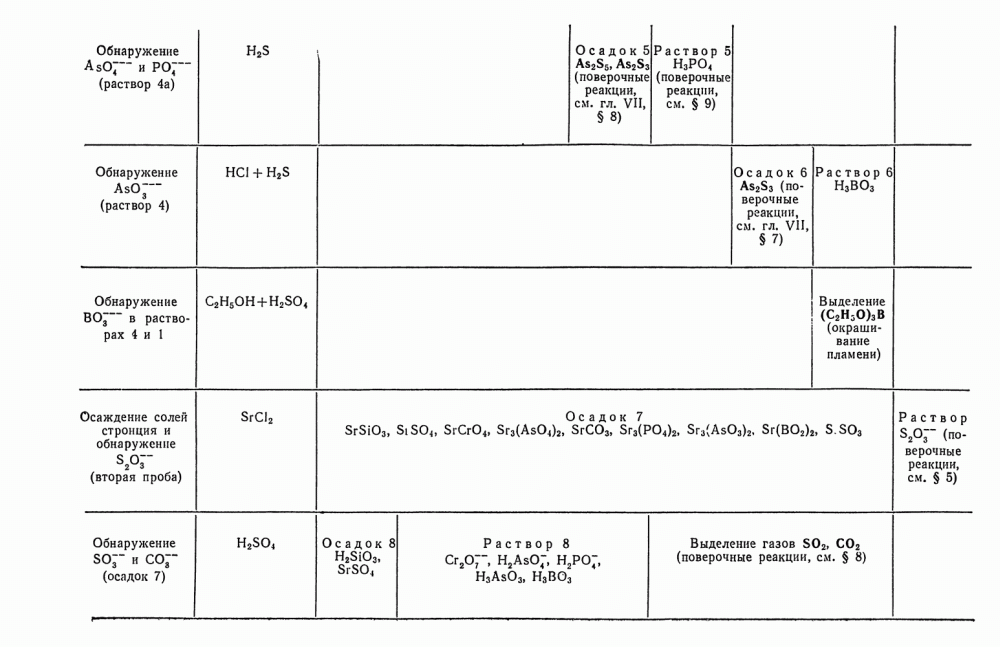
- § 24. Анализ смеси анионов второй группы
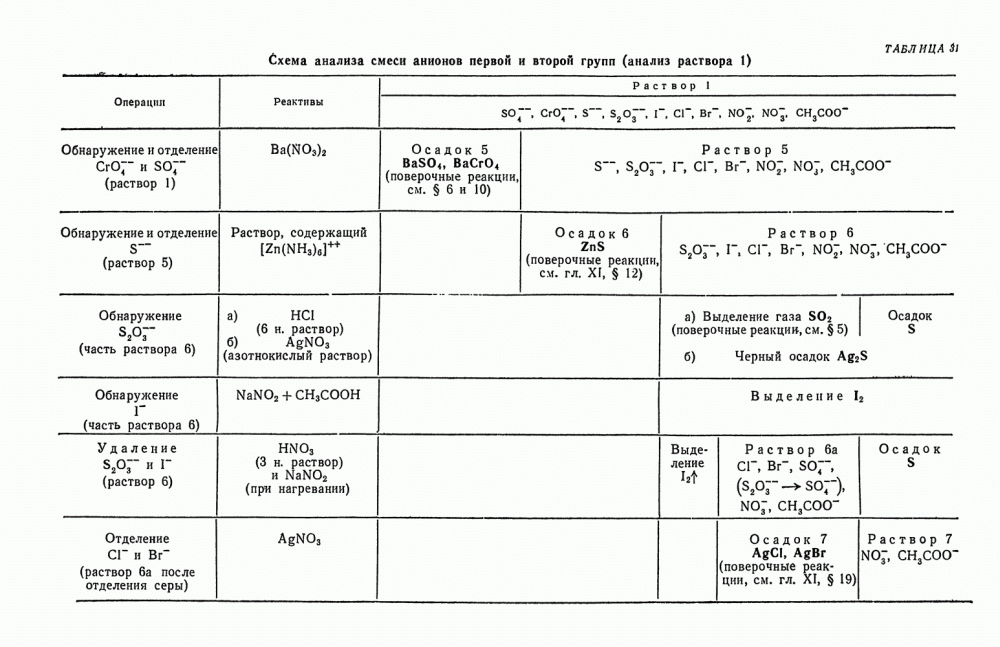
- § 25. Анализ смеси анионов первой и второй групп
- ГЛАВА XIII. ОБНАРУЖЕНИЕ СВОБОДНЫХ МЕТАЛЛОВ И НЕМЕТАЛЛОВ, ИДЕНТИФИЦИРОВАНИЕ СОЛЕЙ И ДРУГИХ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И АНАЛИЗ ИХ СМЕСЕЙ
- § 1. Подготовка вещества к анализу
- § 2. Предварительные испытания
- § 3. Растворение анализируемого вещества в воде, кислотах и щелочах
- § 4. Переведение в растворимое состояние веществ, нерастворимых в воде, кислотах и щелочах
- § 5. Анализ неизвестного вещества
- § 6. Обнаружение свободных элементов
- § 7. Идентифицирование солей и других индивидуальных соединений
- § 8. Обнаружение микропримесей
- § 9. Анализ сплавов
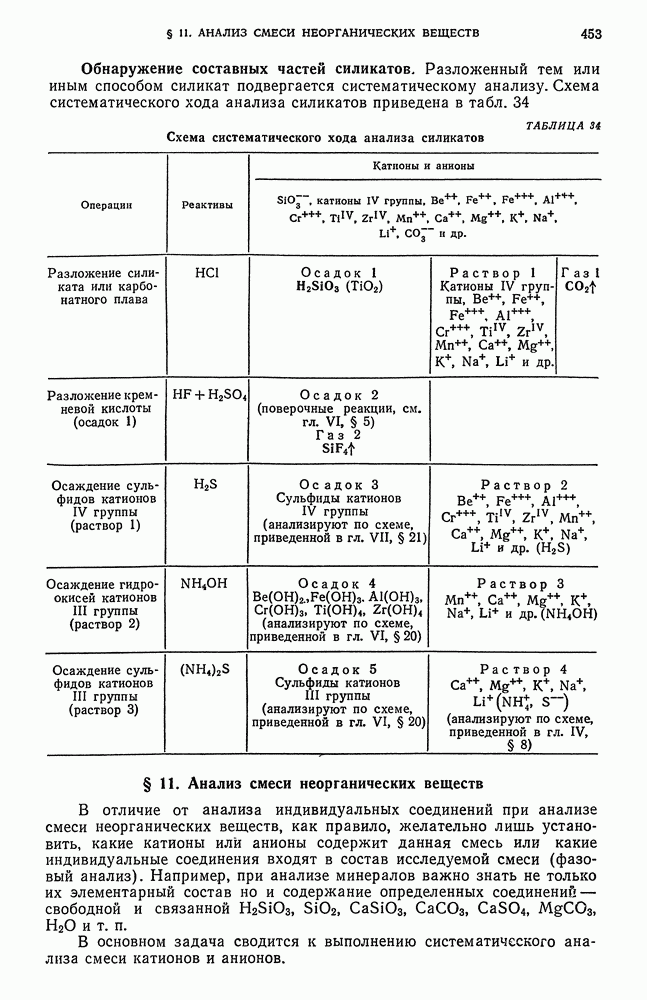
- § 10. Анализ силикатов и алюмосиликатов
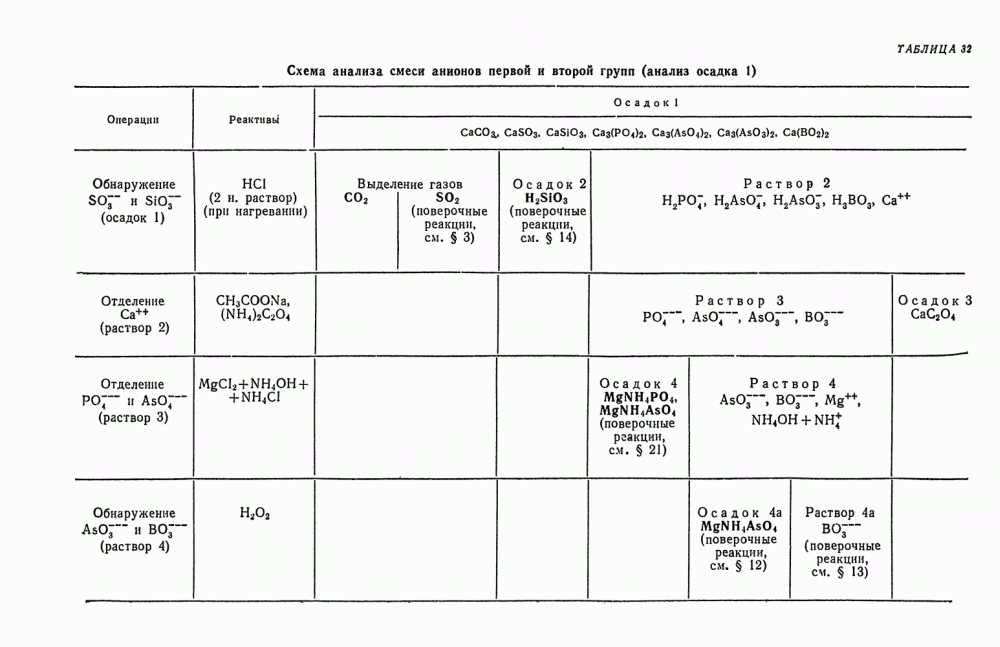
- § 11. Анализ смеси неорганических веществ
- § 12. Экспрессный метод анализа смесей катионов и анионов
- § 13. Идентифицирование нерастворимых веществ
- ЛИТЕРАТУРА