| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 11. Обнаружение Mg-ионов
Реакция с гидрофосфатом натрия  . а) Поместите в пробирку по
. а) Поместите в пробирку по  капли растворов
капли растворов  , прибавьте к полученной смеси 2—3 капли раствора
, прибавьте к полученной смеси 2—3 капли раствора  . Тщательно перемешайте содержимое пробирки стеклянной палочкой и затем добавьте к раствору
. Тщательно перемешайте содержимое пробирки стеклянной палочкой и затем добавьте к раствору  до щелочной реакции. Выпадает белый кристаллический осадок магний-аммоний фосфата
до щелочной реакции. Выпадает белый кристаллический осадок магний-аммоний фосфата  :
:

или в ионной форме:

б) Для микрокристаллоскопического обнаружения  в виде
в виде  поместите каплю анализируемого раствора на предметное стекло. К ней прибавьте из капиллярной пипетки сначала каплю раствора
поместите каплю анализируемого раствора на предметное стекло. К ней прибавьте из капиллярной пипетки сначала каплю раствора  , затем каплю концентрированного раствора
, затем каплю концентрированного раствора  . Наконец, внесите в раствор кристаллик гидрофосфата натрия
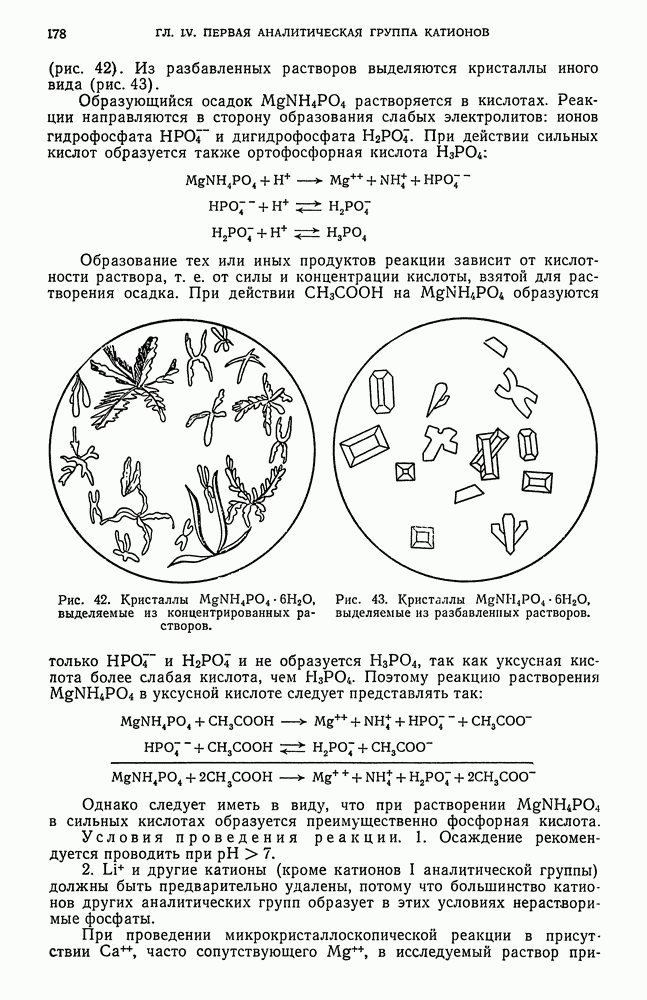
. Наконец, внесите в раствор кристаллик гидрофосфата натрия  . Предметное стекло рекомендуется осторожно нагреть на крышке водяной бани. При этом образуются кристаллы в виде шестилучевых звезд (рис. 42).
. Предметное стекло рекомендуется осторожно нагреть на крышке водяной бани. При этом образуются кристаллы в виде шестилучевых звезд (рис. 42).
Из разбавленных растворов выделяются кристаллы иного вида (рис. 43).

Рис. 42. Кристаллы  , выделяемые из концентрированных растворов.
, выделяемые из концентрированных растворов.

Рис. 43. Кристаллы  , выделяемые из разбавленных растворов.
, выделяемые из разбавленных растворов.
Образующийся осадок  растворяется в кислотах. Реакции направляются в сторону образования слабых электролитов: ионов гидрофосфата
растворяется в кислотах. Реакции направляются в сторону образования слабых электролитов: ионов гидрофосфата  и дигидрофосфата
и дигидрофосфата  . При действии сильных кислот образуется также ортофосфорная кислота
. При действии сильных кислот образуется также ортофосфорная кислота  :
:

Образование тех или иных продуктов реакции зависит от кислотности раствора, т. е. от силы и концентрации кислоты, взятой для растворения осадка. При действии  на
на  образуются только
образуются только  и
и  и не образуется
и не образуется  , так как уксусная кислота более слабая кислота, чем
, так как уксусная кислота более слабая кислота, чем  . Поэтому реакцию растворения
. Поэтому реакцию растворения  в уксусной кислоте следует представлять так:
в уксусной кислоте следует представлять так:

Однако следует иметь в виду, что при растворении  в сильных кислотах образуется преимущественно фосфорная кислота.
в сильных кислотах образуется преимущественно фосфорная кислота.
Условия проведения реакции. 1. Осаждение рекомендуется проводить при  .
.
2.  и другие катионы (кроме катионов I аналитической группы) должны быть предварительно удалены, потому что большинство катионов других аналитических групп образует в этих условиях нерастворимые фосфаты.
и другие катионы (кроме катионов I аналитической группы) должны быть предварительно удалены, потому что большинство катионов других аналитических групп образует в этих условиях нерастворимые фосфаты.
При проведении микрокристаллоскопической реакции в присутствии  , часто сопутствующего
, часто сопутствующего  , в исследуемый раствор прибавляют лимонную кислоту.
, в исследуемый раствор прибавляют лимонную кислоту.
Это дает возможность проводить реакцию в присутствии  .
.
3. При осаждении  следует добавлять небольшой избыток
следует добавлять небольшой избыток  во избежание выпадения в щелочной среде аморфного осадка
во избежание выпадения в щелочной среде аморфного осадка  . Однако большой избыток
. Однако большой избыток  препятствует осаждению
препятствует осаждению  вследствие образования комплексных ионов
вследствие образования комплексных ионов  :
:

4. Нагревание раствора до  благоприятствует образованию кристаллического осадка.
благоприятствует образованию кристаллического осадка.
5. Растворы  склонны к пересыщению, поэтому для ускорения выпадения осадка рекомендуется потереть стеклянной палочкой о стенки пробирки.
склонны к пересыщению, поэтому для ускорения выпадения осадка рекомендуется потереть стеклянной палочкой о стенки пробирки.
6. При малом содержании  или при работе с разбавленными растворами окончательный вывод о присутствии или отсутствии
или при работе с разбавленными растворами окончательный вывод о присутствии или отсутствии  можно сделать лишь через
можно сделать лишь через  после проведения реакции.
после проведения реакции.
Реакция с  -оксихинолином (оксином)
-оксихинолином (оксином)  . Поместите каплю раствора, содержащего
. Поместите каплю раствора, содержащего  , в пробирку или на фарфоровую пластинку, добавьте по капле растворов
, в пробирку или на фарфоровую пластинку, добавьте по капле растворов  и
и  -оксихинолина. При этом образуется зеленовато-желтый кристаллический осадок оксихинолята магния:
-оксихинолина. При этом образуется зеленовато-желтый кристаллический осадок оксихинолята магния:

Ионы  не дают осадков с
не дают осадков с  -оксихинолином.
-оксихинолином.
Эту реакцию применяют для отделения  от остальных катионов I группы, в том числе и от
от остальных катионов I группы, в том числе и от  , а также для количественного определения магния.
, а также для количественного определения магния.
Условия проведения реакции. 1. Осаждение рекомендуется проводить при 
Оксихиноляты других ионов осаждаются при различных значениях  :
:

2. Реактив осаждает катионы многих других элементов, поэтому катионы, помимо I и II аналитических групп, должны отсутствовать.
3. Если реакцию приходится вести в присутствии других катионов, осаждаемых оксихинолином, то применяют методы маскировки мешающих ионов (см. гл. III, § 14).
4. Осаждение лучше проводить при нагревании.
Реакция с  -нитробензолазорезорцином («магнезон»). Поместите 2—3 капли исследуемого нейтрального или слабокислого раствора на капельную пластинку, прибавьте 1—2 капли раствора магнезона, обладающего в щелочной среде красно-фиолетовой окраской. Если раствор окрашивается в желтый цвет (что указывает на кислый характер среды), добавьте 1—3 капли раствора
-нитробензолазорезорцином («магнезон»). Поместите 2—3 капли исследуемого нейтрального или слабокислого раствора на капельную пластинку, прибавьте 1—2 капли раствора магнезона, обладающего в щелочной среде красно-фиолетовой окраской. Если раствор окрашивается в желтый цвет (что указывает на кислый характер среды), добавьте 1—3 капли раствора  и КОН. В присутствии ионов магния раствор окрашивается в синий цвет или выпадает такого же цвета осадок.
и КОН. В присутствии ионов магния раствор окрашивается в синий цвет или выпадает такого же цвета осадок.
Механизм реакции основан на осаждении  , сопровождающемся явлением адсорбции красителя на поверхности гидроокиси магния. Адсорбция некоторых красителей так называемых
, сопровождающемся явлением адсорбции красителя на поверхности гидроокиси магния. Адсорбция некоторых красителей так называемых  и антрахинонового ряда сопровождается изменением первоначального цвета неадсорбированного красителя. Так как адсорбция красителя на поверхности
и антрахинонового ряда сопровождается изменением первоначального цвета неадсорбированного красителя. Так как адсорбция красителя на поверхности  протекает мгновенно, то это явление служит прекрасным средством для обнаружения ионов магния.
протекает мгновенно, то это явление служит прекрасным средством для обнаружения ионов магния.  не мешают этой реакции. Соли аммония препятствуют осаждению
не мешают этой реакции. Соли аммония препятствуют осаждению  , поэтому их необходимо предварительно удалить.
, поэтому их необходимо предварительно удалить.
Капельная реакция Н. А. Тананаева. Поместите на фильтровальную бумагу каплю раствора фенолфталеина, каплю нейтрального раствора испытуемого вещества и каплю раствора аммиака. При этом появляется красное пятно, обусловленное щелочностью аммиачного раствора и образующейся гидроокиси магния. Появление окрашивания еще не дает оснований сделать какие-либо выводы относительно присутствия  . При подсушивании мокрого пятна над пламенем горелки избыток
. При подсушивании мокрого пятна над пламенем горелки избыток  улетучивается, гидроокись магния обезвоживается и красное пятно обесцвечивается. Если затем смочить высушенное пятно дистиллированной водой, то вновь появляется красная окраска, обусловленная образованием
улетучивается, гидроокись магния обезвоживается и красное пятно обесцвечивается. Если затем смочить высушенное пятно дистиллированной водой, то вновь появляется красная окраска, обусловленная образованием  .
.
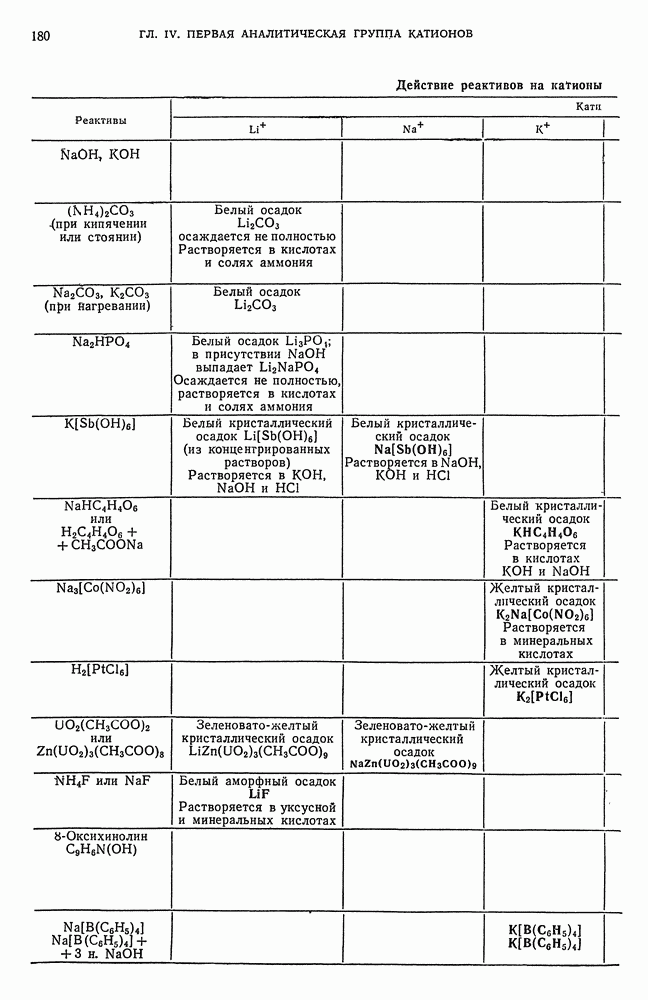
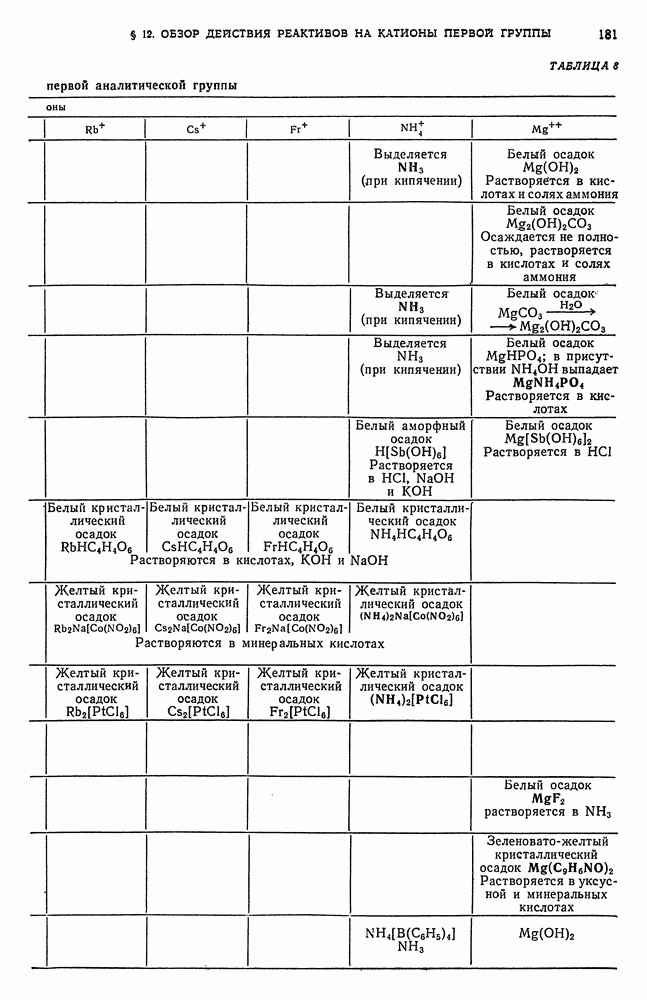
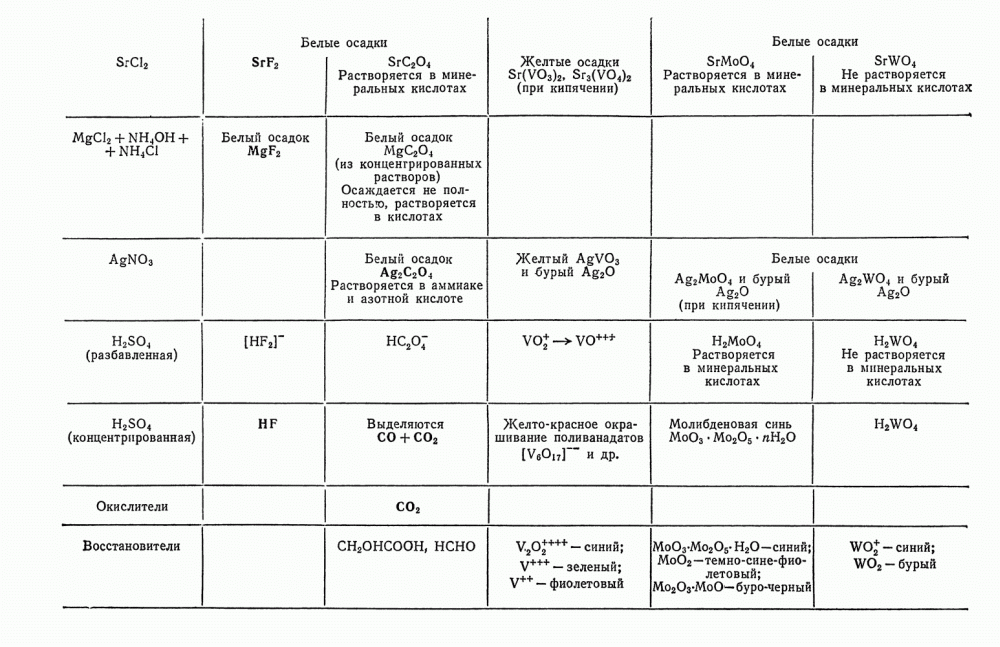
Таблица 8. Действие реактивов на катионы первой аналитической группы

Продолжение табл. 8.

Цветная реакция Тананаева дает возможность открывать  в присутствии
в присутствии  . Катионы других аналитических групп должны быть удалены. Выполнение реакции на фильтровальной бумаге показано на рис. 12 (см. гл. III, § 5).
. Катионы других аналитических групп должны быть удалены. Выполнение реакции на фильтровальной бумаге показано на рис. 12 (см. гл. III, § 5).
Реакция с гипоиодитом. Свежеосажденный белый осадок  окрашивается в красно-бурый цвет при действии гипоиодита вследствие адсорбции элементарного иода на поверхности осадка гидроокиси магния. Красно-бурая окраска обесцвечивается при обработке осадка иодидом или гидроокисью калия, спиртом и другими растворителями, растворяющими иод, а также при действии сульфита или тиосульфата, восстанавливающими элементарный иод.
окрашивается в красно-бурый цвет при действии гипоиодита вследствие адсорбции элементарного иода на поверхности осадка гидроокиси магния. Красно-бурая окраска обесцвечивается при обработке осадка иодидом или гидроокисью калия, спиртом и другими растворителями, растворяющими иод, а также при действии сульфита или тиосульфата, восстанавливающими элементарный иод.
При выполнении данной реакции реактивом служит раствор иода в иодиде калия, обесцвеченный добавлением возможно малого количества КОН или  . В образующемся растворе гипоиодита устанавливается подвижное равновесие:
. В образующемся растворе гипоиодита устанавливается подвижное равновесие:

или в ионной форме:

На фарфоровую пластинку поместите 5—10 капель 1 н. раствора иода, растворенного в  -ном растворе.
-ном растворе.  , добавьте по каплям 1 н. раствор КОН (или
, добавьте по каплям 1 н. раствор КОН (или  ) до появления лимонно-желтой окраски и затем 1—2 капли нейтрального или слегка подкисленного исследуемого раствора.
) до появления лимонно-желтой окраски и затем 1—2 капли нейтрального или слегка подкисленного исследуемого раствора.
В присутствии  появляются красно-бурые хлопья
появляются красно-бурые хлопья  .
.
При действии реактива на раствор, содержащий  , Ьыпадает
, Ьыпадает  , вследствие чего динамическое равновесие, установленное между иодом и щелочью, с одной стороны, и иодидом и гипоиодитом, с другой, нарушается. Реакция сдвигается справа налево и в растворе появляется некоторое количество иода, адсорбирующегося на поверхности выпадающей гидроокиси магния с образованием красно-бурого осадка.
, вследствие чего динамическое равновесие, установленное между иодом и щелочью, с одной стороны, и иодидом и гипоиодитом, с другой, нарушается. Реакция сдвигается справа налево и в растворе появляется некоторое количество иода, адсорбирующегося на поверхности выпадающей гидроокиси магния с образованием красно-бурого осадка.
Реакцию можно представить следующей схемой:

Условия проведения реакции. 1. Реакцию проводят в щелочной среде при  избыток щелочи вреден.
избыток щелочи вреден.
2. Соли аммония и ионы III, IV и V аналитических групп должны отсутствовать.
3. Восстановители мешают реакции.
4. Фосфаты и оксалаты также мешают реакции вследствие образования компактных осадков фосфата и оксалата магния, не способных адсорбировать элементарный иод в отличие от хорошо развитой поверхности аморфного осадка  .
.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Анализ и синтез
- § 2. Предмет аналитической химии
- § 3. Развитие аналитической химии
- § 4. Качественный и количественный анализ
- ГЛАВА I. ПРИМЕНЕНИЕ ЗАКОНА ДЕЙСТВИЯ МАСС В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Влияние среды на состояние ионов в растворах
- § 2. Обратимые и необратимые аналитические реакции
- § 3. Направление аналитических реакций; правила обменного разложения
- § 4. Закон действия масс и следствие из него
- § 5. Границы применимости закона действия масс
- § 6. Сильные и слабые электролиты
- § 7. Активность
- § 8. Коэффициент активности и ионная сила
- Б. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ (В ГОМОГЕННЫХ СИСТЕМАХ)
- § 9. Гомогенные и гетерогенные системы
- § 10. Ионное произведение воды
- § 11. Ионы гидроксония
- § 12. Равновесие ионов в водных растворах; понятие о pH
- § 13. Равновесие в водных растворах слабых электролитов
- § 14. Влияние сильных кислот или сильных оснований на степень электролитической диссоциации слабых электролитов
- § 15. Приближенные формулы для расчета [H+] и [OH-] в водных растворах кислот и оснований
- В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
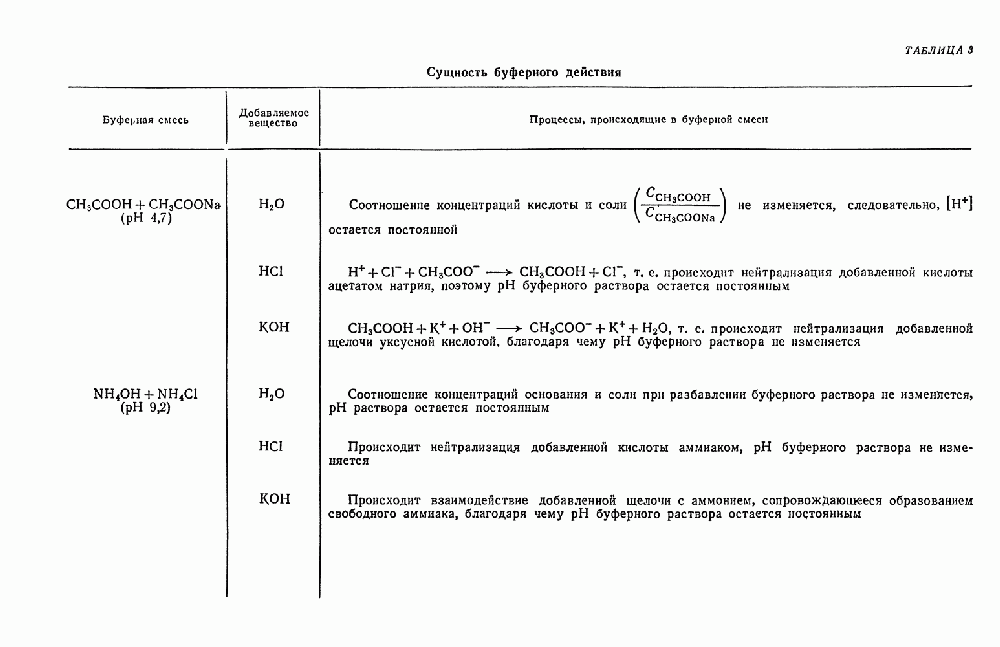
- § 16. Буферные растворы
- § 17. Применение буферных растворов в химическом анализе
- Г. РАВНОВЕСИЯ В РАСТВОРАХ ГИДРОЛИЗУЮЩИХСЯ СОЛЕЙ
- § 18. Теоретические основы гидролиза
- § 19. Механизм гидролитического расщепления
- § 20. Подавление и усиление гидролиза солей
- Д. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ТИПИЧНО АМФОТЕРНЫХ ЭЛЕКТРОЛИТОВ
- § 21. Поведение амфотерных гидроокисей в водных растворах
- § 22. Константы электролитической диссоциации амфотерных гидроокисей
- Е. РАВНОВЕСИЯ В СИСТЕМАХ: ОСАДОК-НАСЫЩЕННЫЙ РАСТВОР
- § 23. Осаждение как один из основных методов химического анализа
- § 24. Произведение растворимости
- § 25. Произведение активностей
- § 26. Вычисление растворимости электролитов в воде по величине произведения растворимости
- § 27. Влияние различных факторов на растворимость малорастворимых электролитов
- Ж. ОСНОВЫ ТЕОРИИ ОБРАЗОВАНИЯ И РАЗЛОЖЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИИ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 28. Характеристика комплексных соединений, имеющих значение в химическом анализе
- § 29. Квантовомеханические представления о строении комплексов
- § 30. Равновесия в растворах комплексных соединений
- § 31. Константы нестойкости комплексов
- § 32. Внутрикомплексные соединения
- § 33. Методы разложения и образования комплексов, применяемых в аналитической химии
- § 34. Применение метода комплексообразования в химическом анализе
- ГЛАВА II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Окисление—восстановление как один из основных методов химического анализа
- § 2. Направление реакций окисления—восстановления
- § 3. Окислительно-восстановительные потенциалы
- § 4. Зависимость между величинами окислительно-восстановительных потенциалов и условиями, в которых протекают реакции окисления—восстановления
- § 5. Вычисление окислительно-восстановительных потенциалов
- § 6. Вычисление окислительно-восстановительных потенциалов с учетом коэффициентов активности
- ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
- § 1. Обнаружение отдельных элементов
- § 2. Анализ мокрым и сухим путем
- § 3. Химические и физические методы качественного анализа
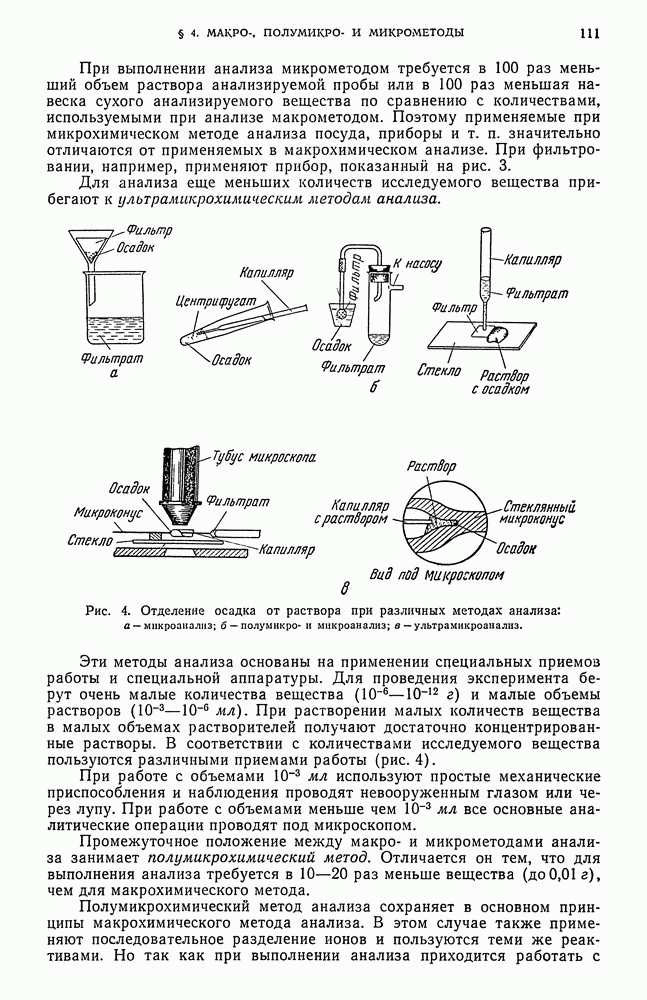
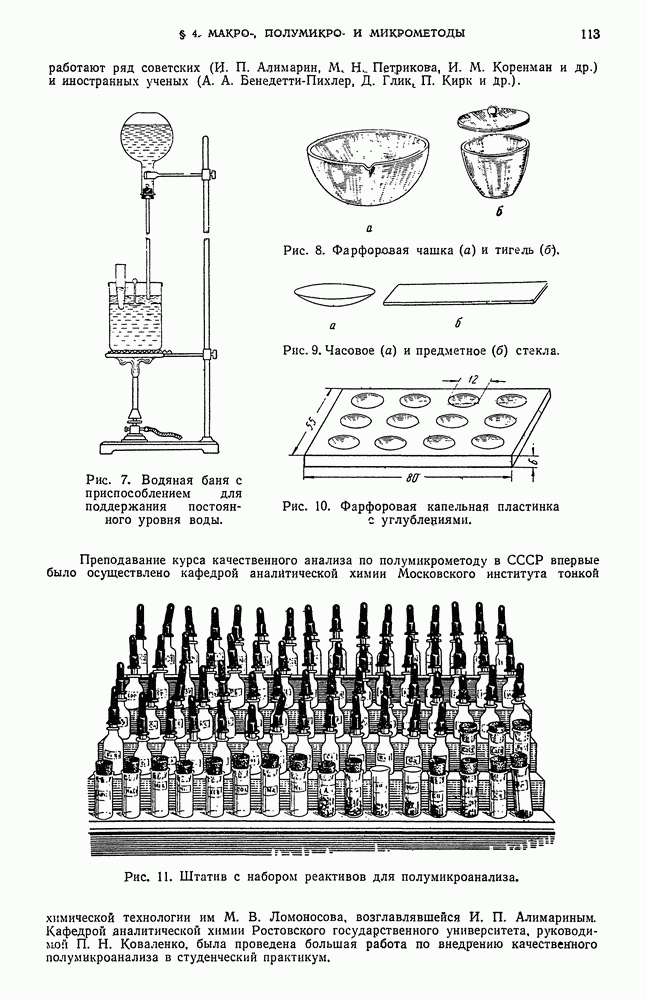
- § 4. Макро-, полумикро- и микрометоды
- § 5. Капельный анализ
- § 6. Микрокристаллоскопический анализ
- § 7. Метод растирания порошков
- § 8. Методы анализа, основанные на нагревании и сплавлении веществ
- § 9. Спектральный качественный анализ
- § 10. Хроматографический метод анализа
- § 11. Кинетические методы анализа
- Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
- § 12. Специфичность и чувствительность реакций
- § 13. Максимальная чувствительность аналитических реактивов
- § 14. Способы повышения чувствительности реакций
- § 15. Маскировка мешающих ионов
- § 16. Определение pH среды
- § 17. Регулирование pH среды в процессе аналитических определений
- В. РЕАКТИВЫ
- § 18. Понятие о химических реактивах
- § 19. Концентрация применяемых реактивов
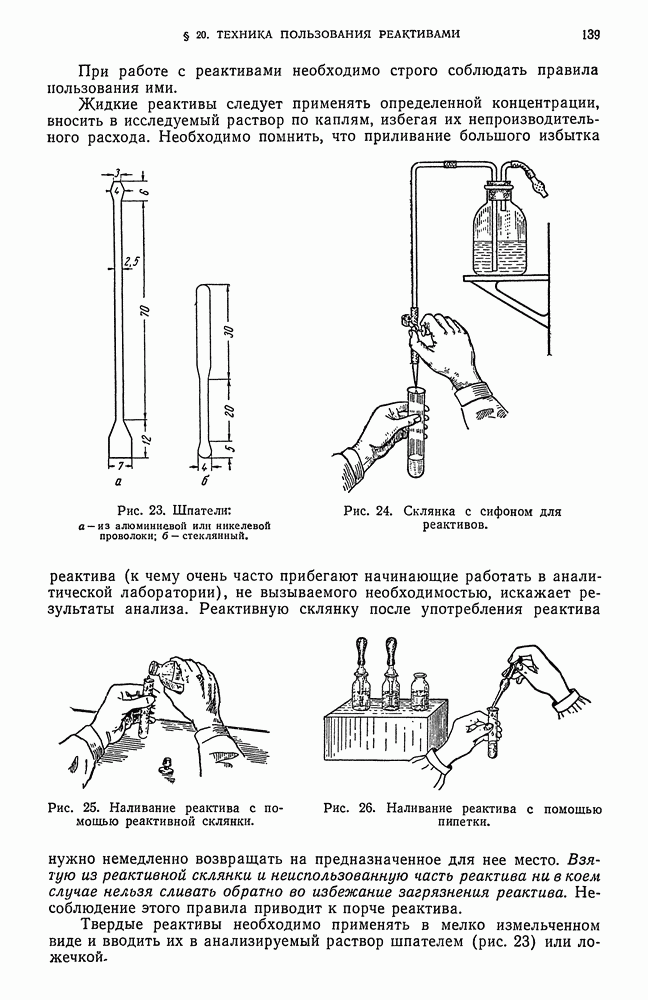
- § 20. Техника пользования реактивами
- Г. ПОСУДА И ПРИБОРЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕННОМ АНАЛИЗЕ
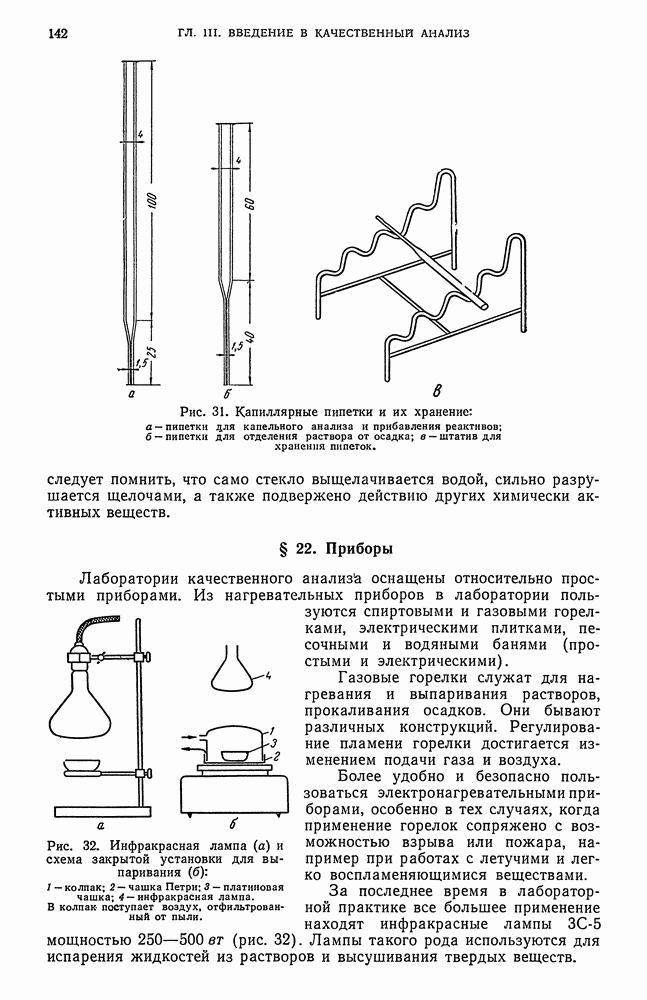
- § 21. Химическая посуда
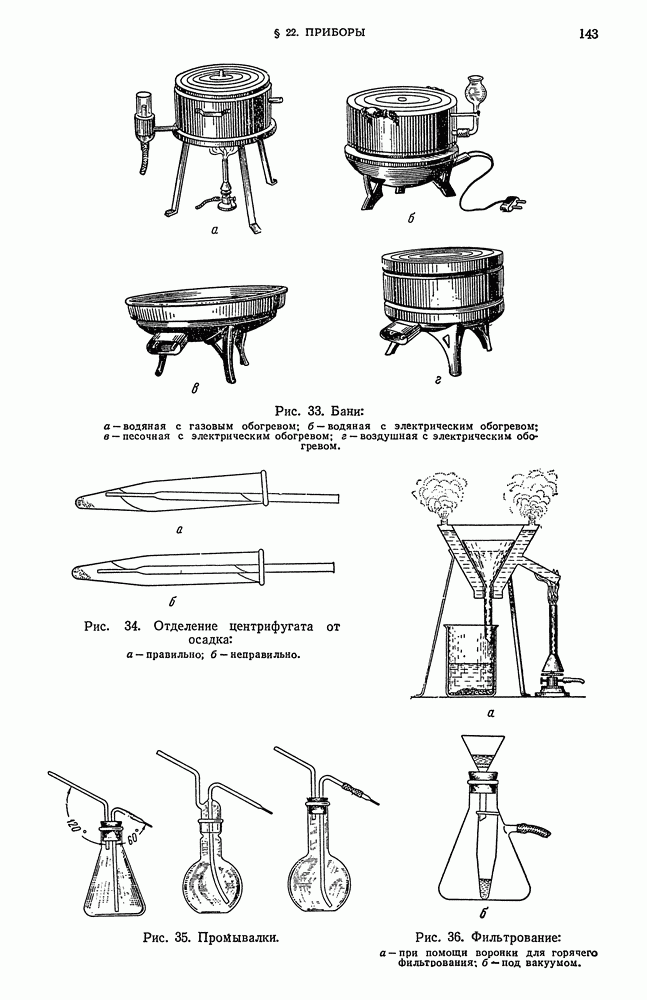
- § 22. Приборы
- Д. АНАЛИТИЧЕСКИЕ ГРУППЫ
- § 23. Дробный и систематический анализ
- § 24. Аналитическая классификация катионов
- § 25. Сводные таблицы действия реактивов на катионы и анионы
- Е. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ ИОНОВ
- § 26. Значение периодического закона в аналитической химии
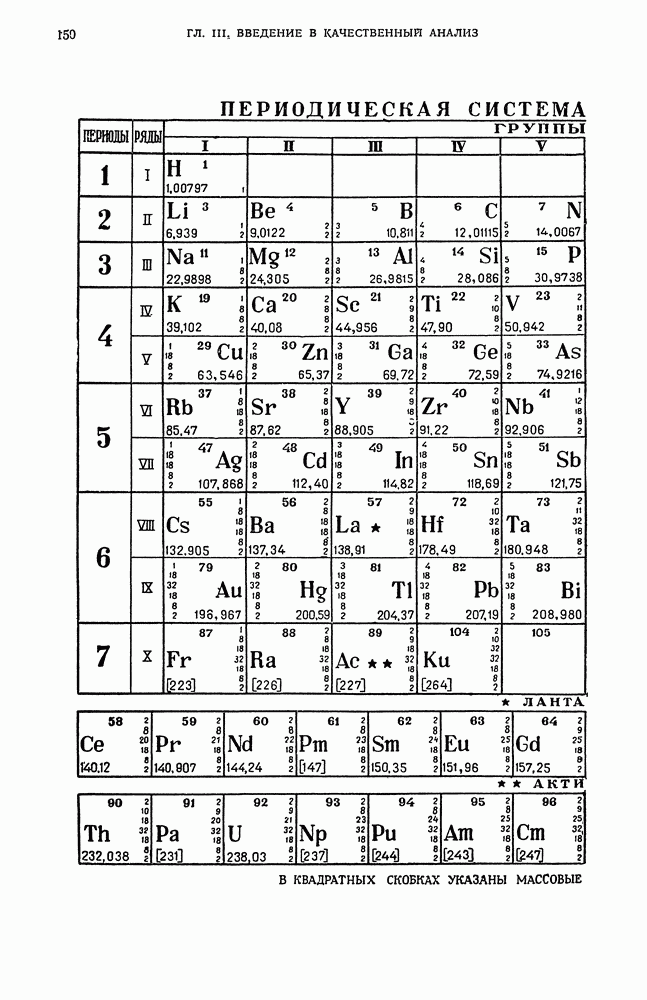
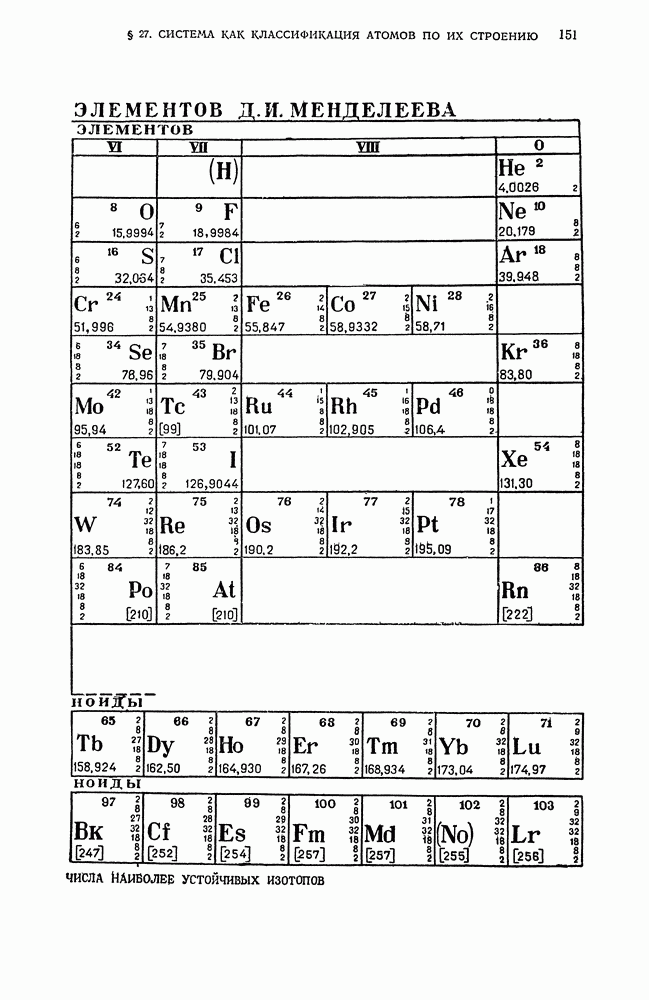
- § 27. Периодическая система элементов Д. И. Менделеева как классификация атомов по их строению
- § 28. Зависимость некоторых химических свойств элементов от положения их в периодической системе Д. И. Менделеева
- § 29. Растворимость химических соединений в связи с положением элементов в периодической системе Д. И. Менделеева
- § 30. Открытие новых аналитических реакций
- § 31. Аналитические группы и периодическая система элементов Д. И. Менделеева
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ КАТИОНОВ И АНАЛИЗ СМЕСЕЙ КАТИОНОВ
- § 1. Характеристика первой аналитической группы катионов
- § 2. Общие реакции катионов первой аналитической группы
- РЕАКЦИИ КАТИОНОВ 1-й ПОДГРУППЫ
- § 3. Обнаружение NН-ионов
- § 4. Методы разложения и удаления солей аммония
- § 5. Обнаружение K-ионов
- § 6. Обнаружение Rb-ионов
- § 7. Обнаружение Cs-ионов
- § 8. Анализ смеси катионов первой подгруппы
- РЕАКЦИИ КАТИОНОВ 2-й ПОДГРУППЫ
- § 9. Обнаружение Li-ионов
- § 10. Обнаружение Na-ионов
- § 11. Обнаружение Mg-ионов
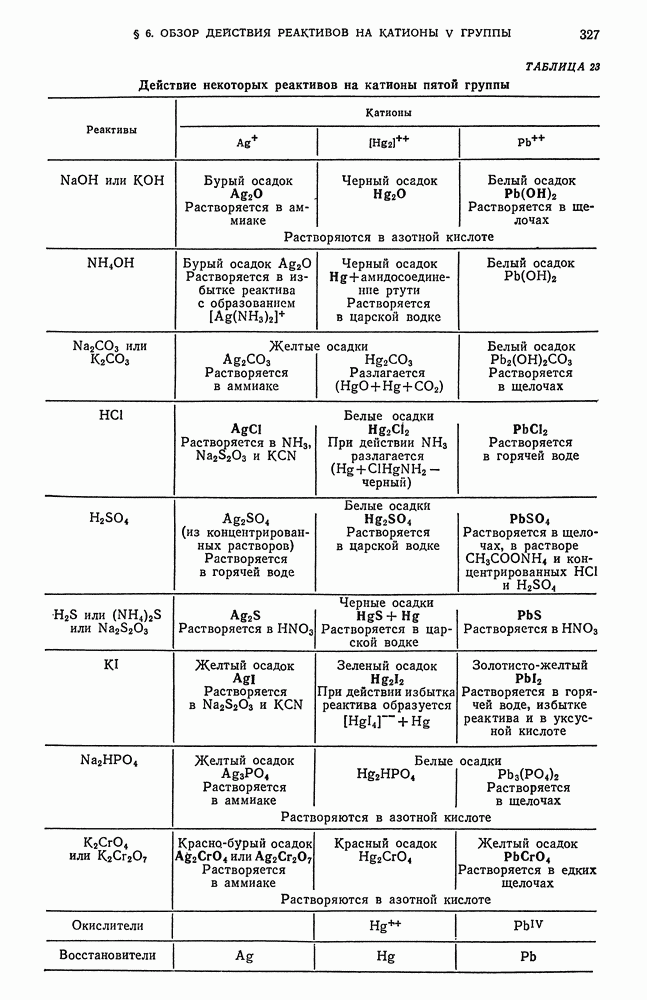
- § 12. Обзор действия реактивов на катионы первой аналитической группы
- § 13. Анализ смеси катионов второй подгруппы
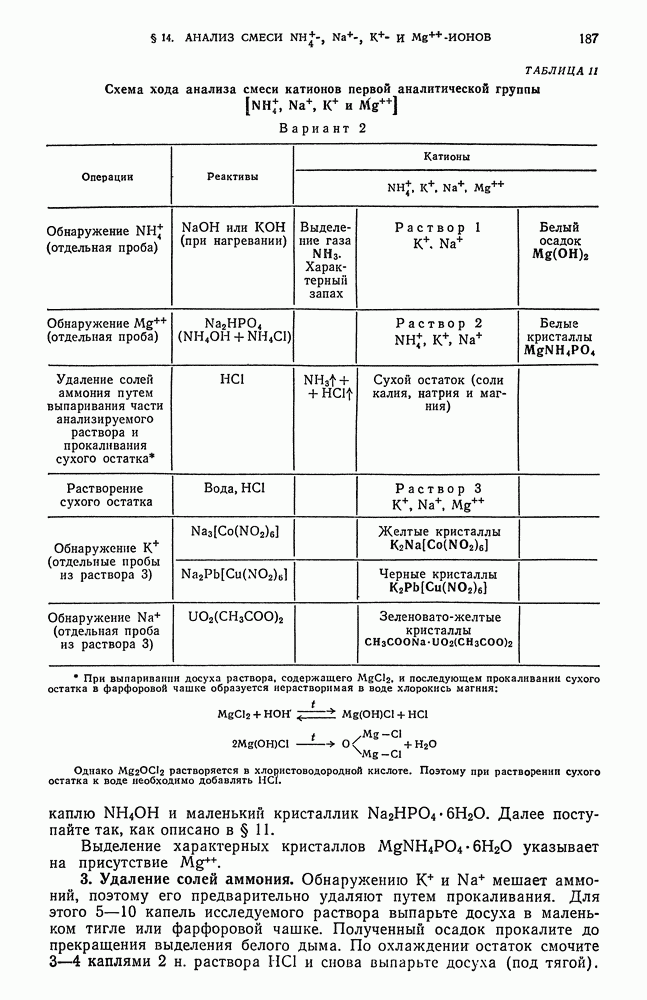
- § 14. Анализ смеси ионов
- § 15. Анализ смеси ионов
- ГЛАВА V. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика второй аналитической группы катионов
- § 2. Общие реакции катионов второй аналитической группы
- § 3. Обнаружение Ca-ионов
- § 4. Обнаружение Sr-ионов
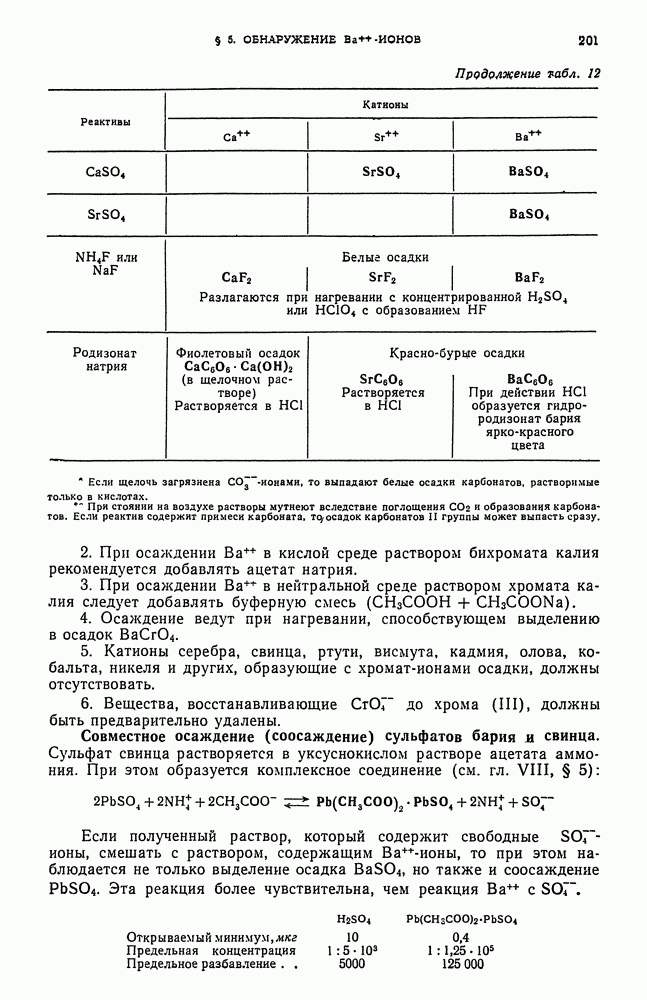
- § 5. Обнаружение Ba-ионов
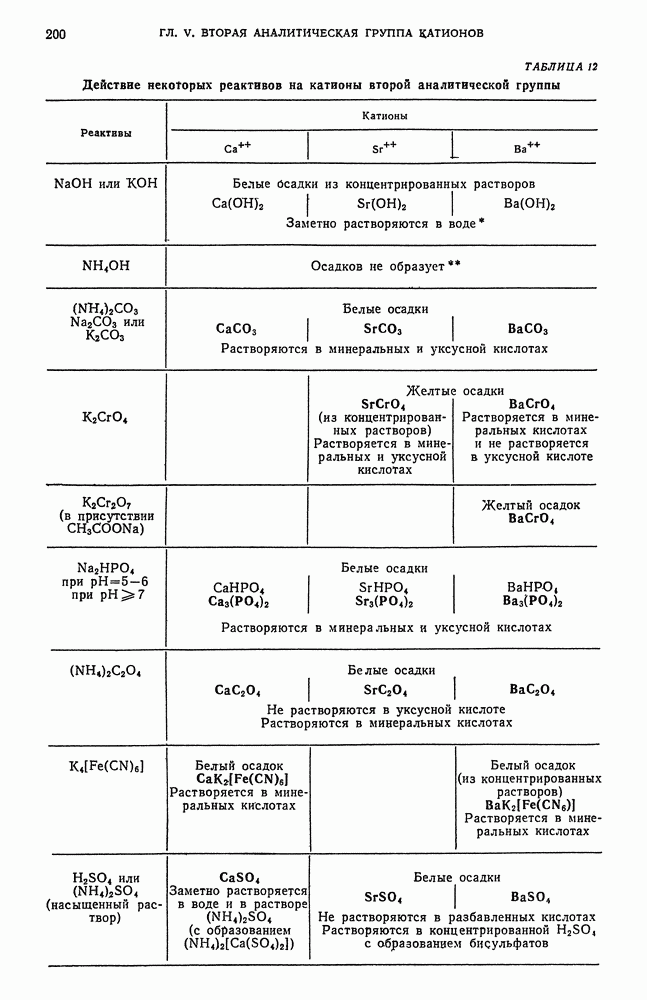
- § 6. Обзор действия реактивов на катионы второй аналитической группы
- § 7. Основы теории осаждения катионов второй аналитической группы групповым реактивом—карбонатом аммония
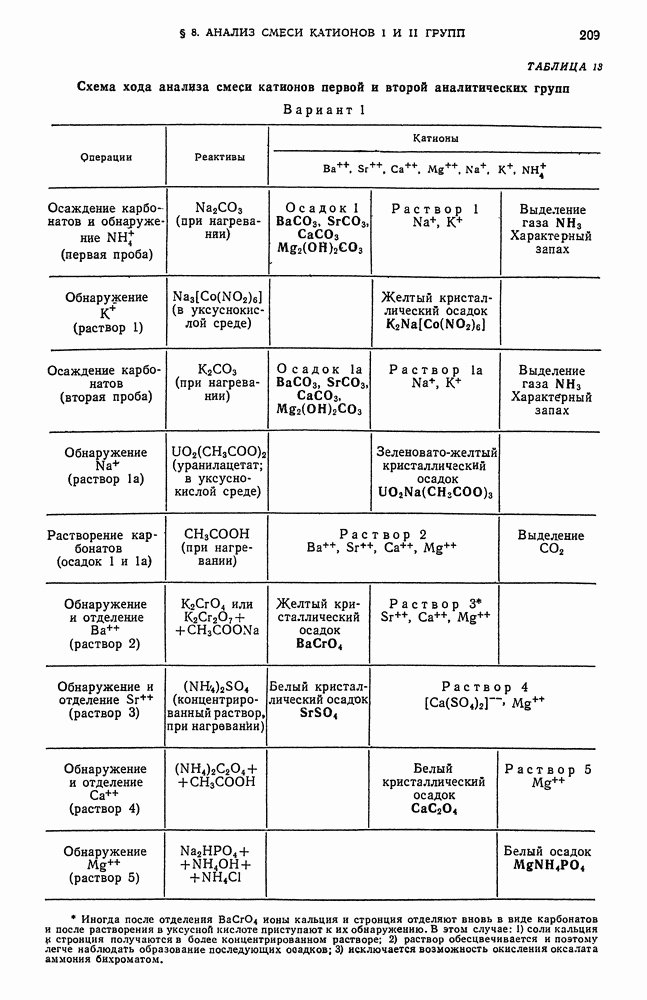
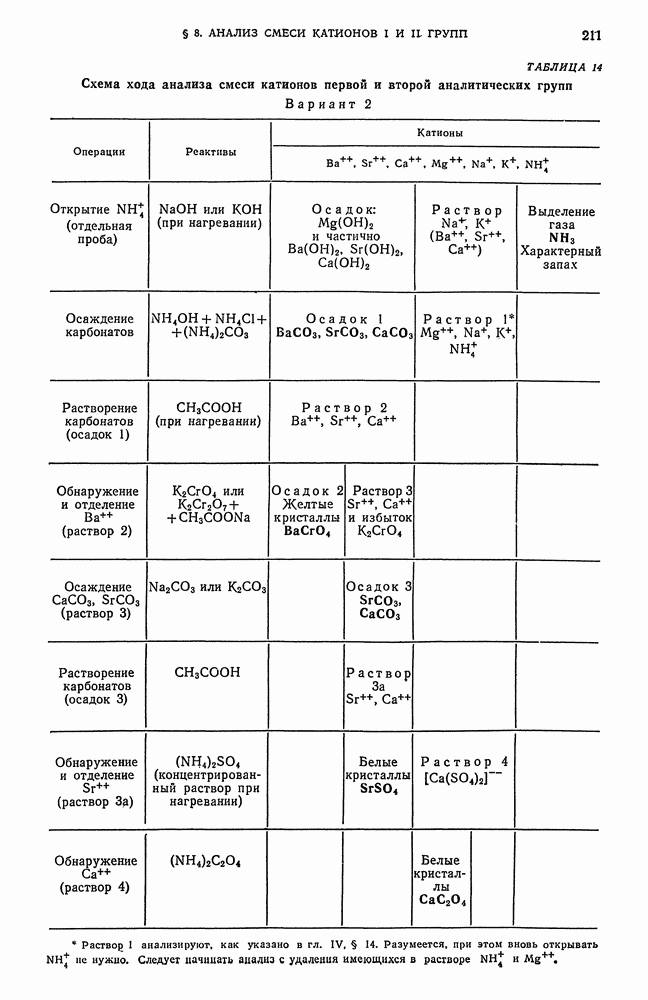
- § 8. Систематический ход анализа смеси катионов первой и второй аналитических групп
- § 9. Систематический ход анализа смеси катионов первой и второй аналитических групп в присутствии ионов
- § 10. Теоретические основы перевода сульфатов катионов второй аналитической группы в карбонаты
- ГЛАВА VI. ТРЕТЬЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика третьей аналитической группы катионов
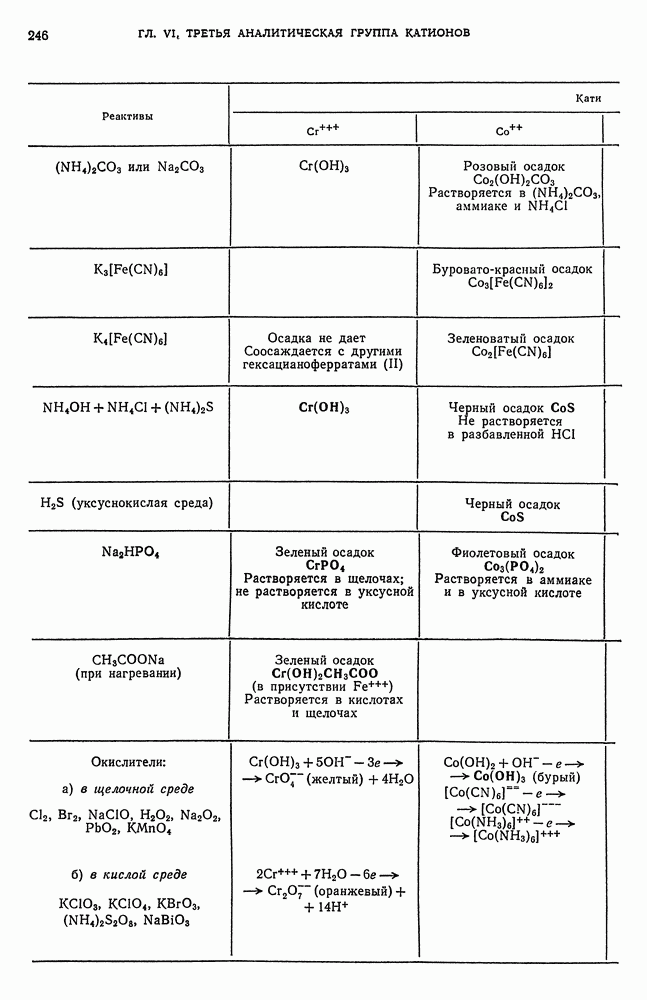
- § 2. Общие реакции катионов третьей аналитической группы
- § 3. Обнаружение Be-ионов
- § 4. Обнаружение Al-ионов
- § 5. Обнаружение ионов титана (IV)
- § 6. Обнаружение Cr-ионов
- § 7. Обнаружение Mn-ионов
- § 8. Обнаружение Fe-ионов
- § 9. Обнаружение Fe-ионов
- § 10. Обнаружение Co-ионов
- § 13. Обнаружение ионов циркония (IV)
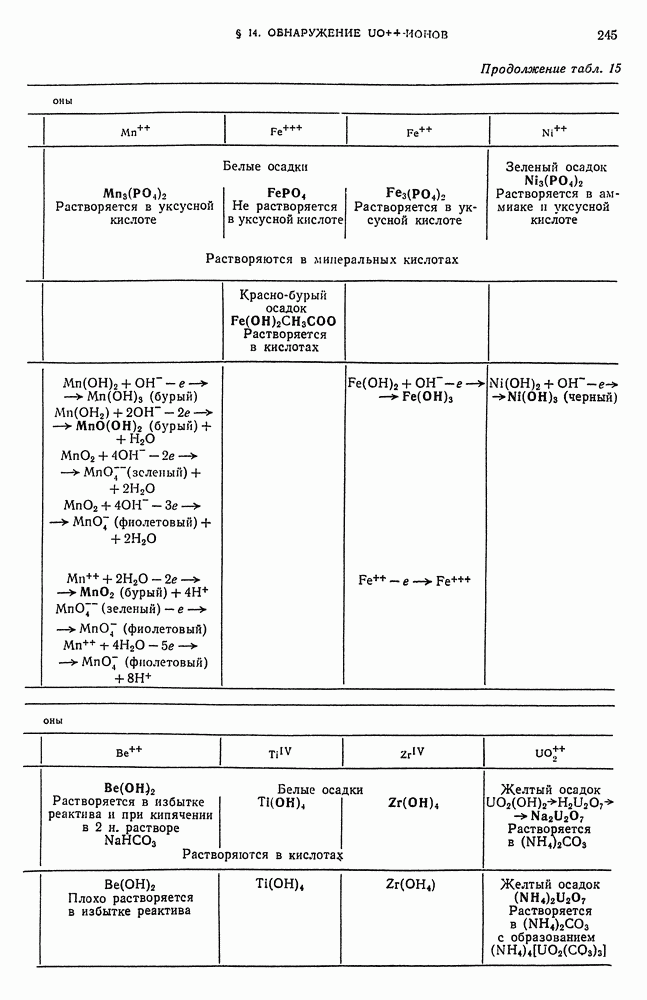
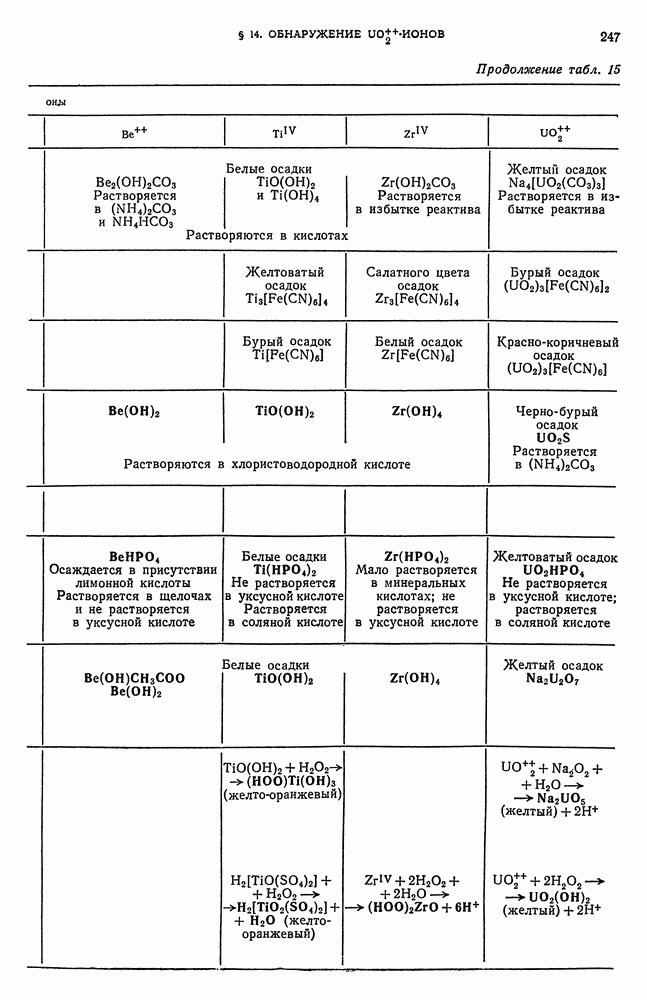
- § 14. Обнаружение UO-ионов
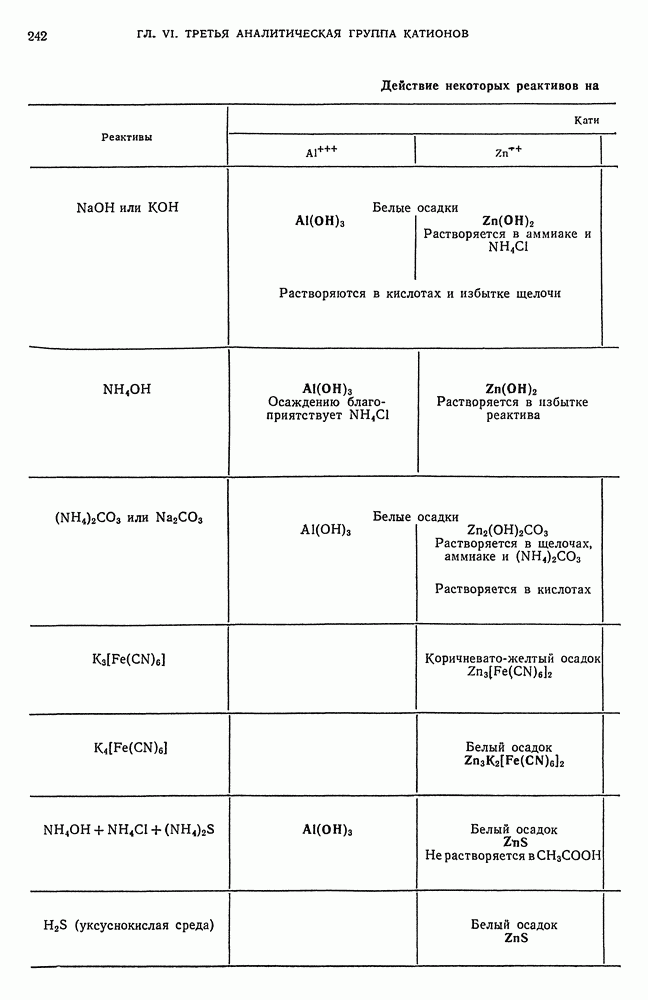
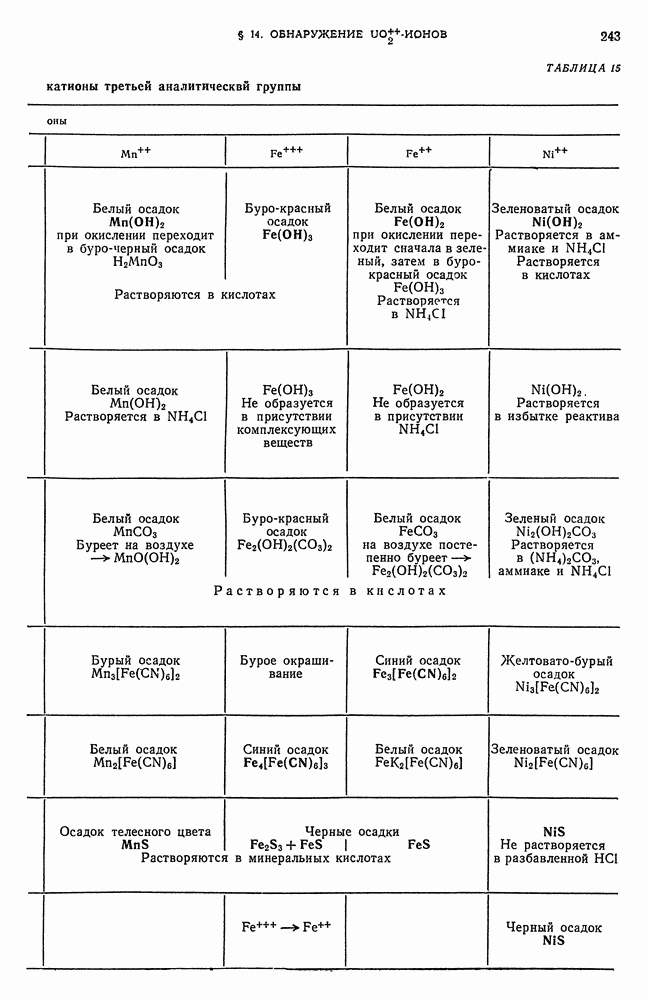
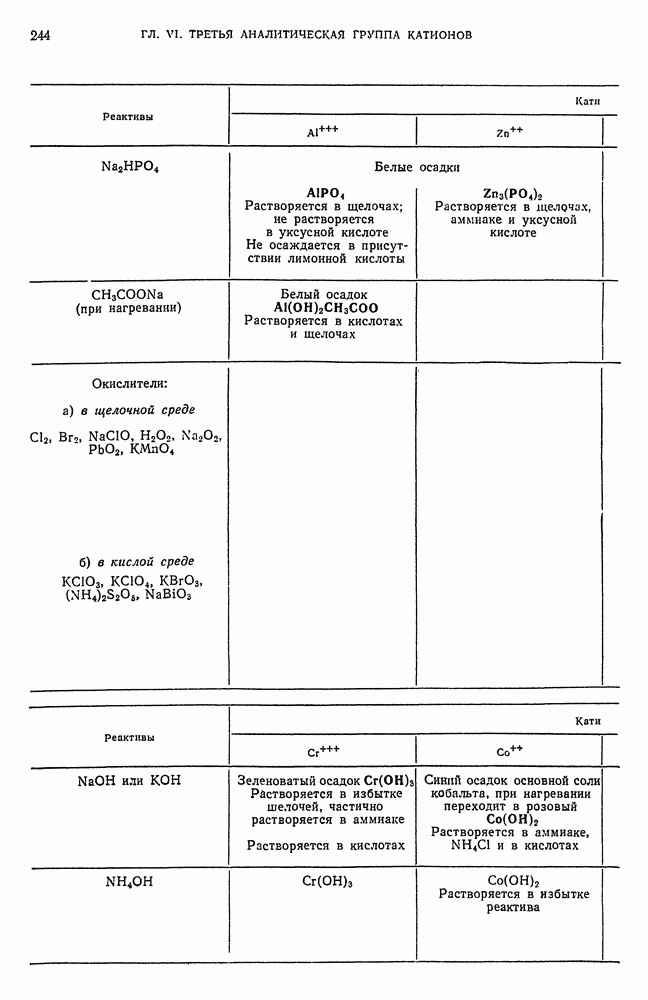
- § 15. Обзор действия реактивов на катионы третьей аналитической группы
- § 16. Использование коллоидных систем в химическом анализе
- § 17. Основы теории осаждения катионов третьей аналитической группы групповым реактивом — сульфидом аммония
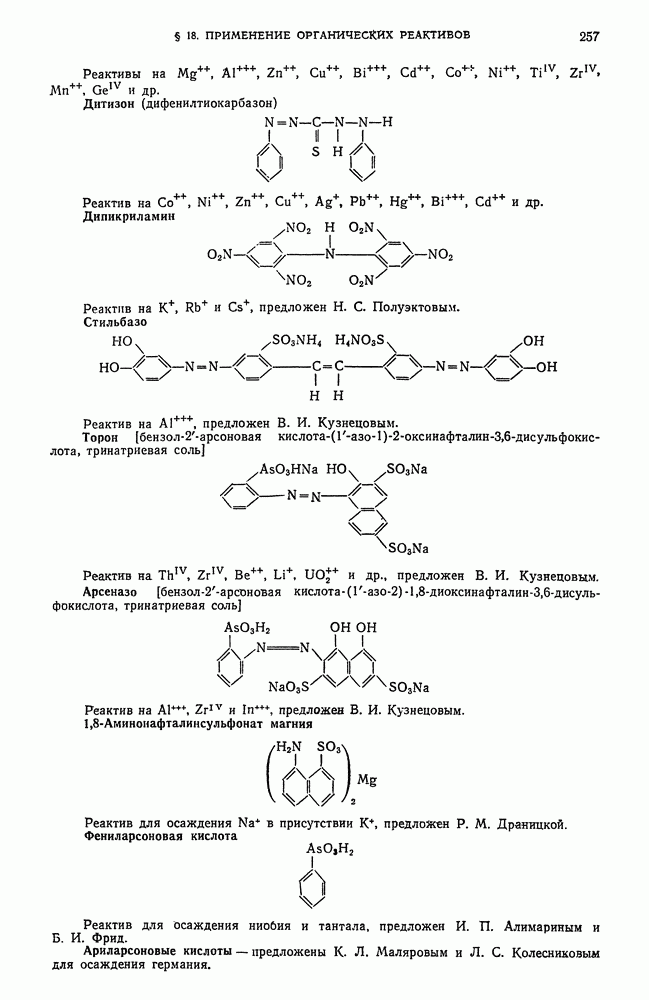
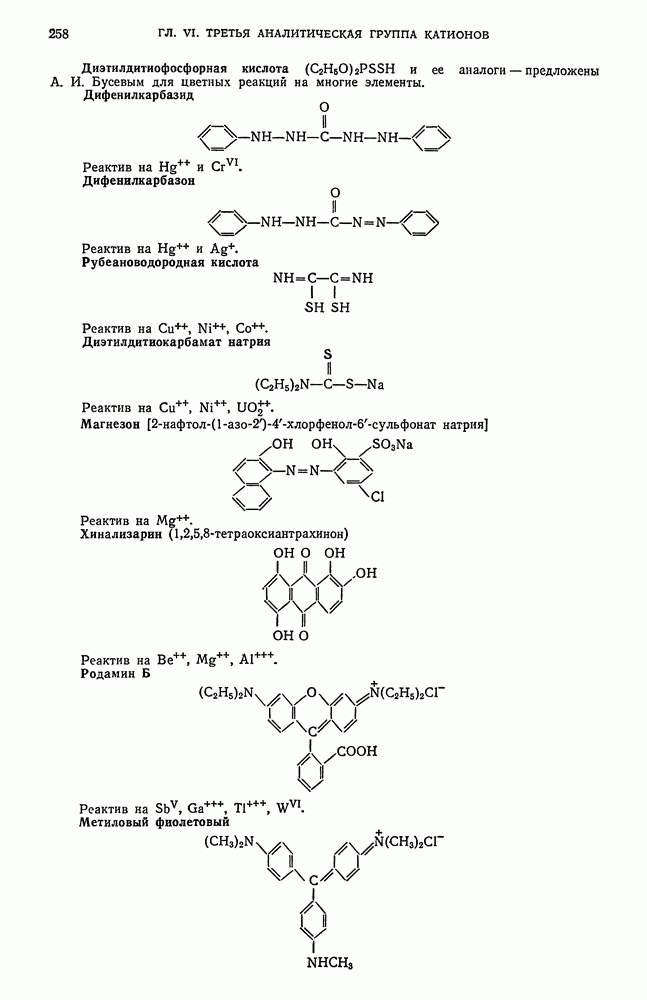
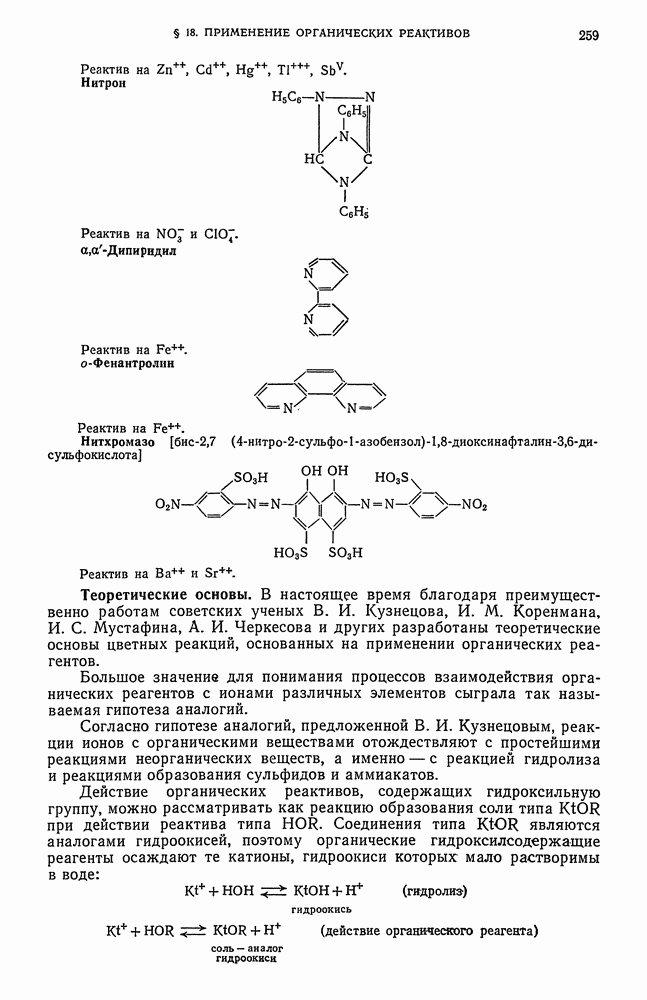
- § 18. Теоретические основы применения органических реактивов в качественном анализе неорганических веществ
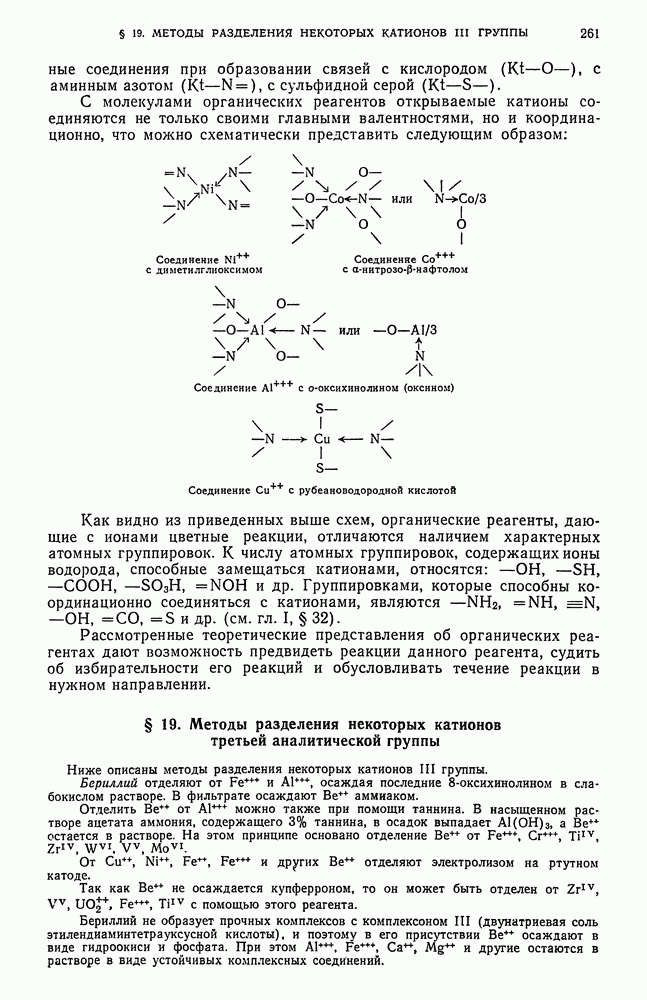
- § 19. Методы разделения некоторых катионов третьей аналитической группы
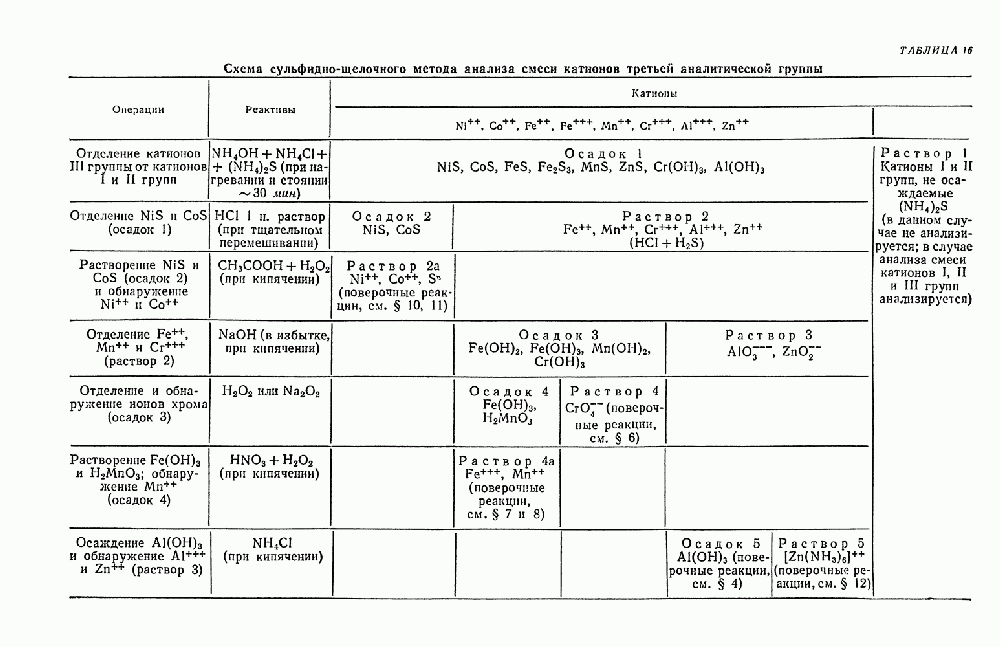
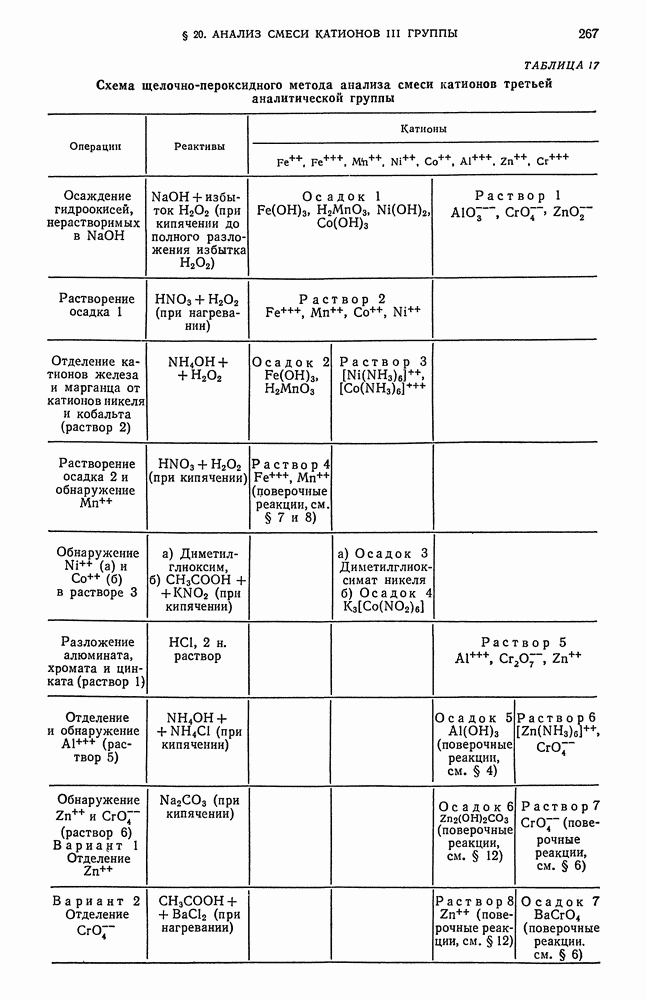
- § 20. Систематический ход анализа смеси катионов третьей аналитической группы
- § 21. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп
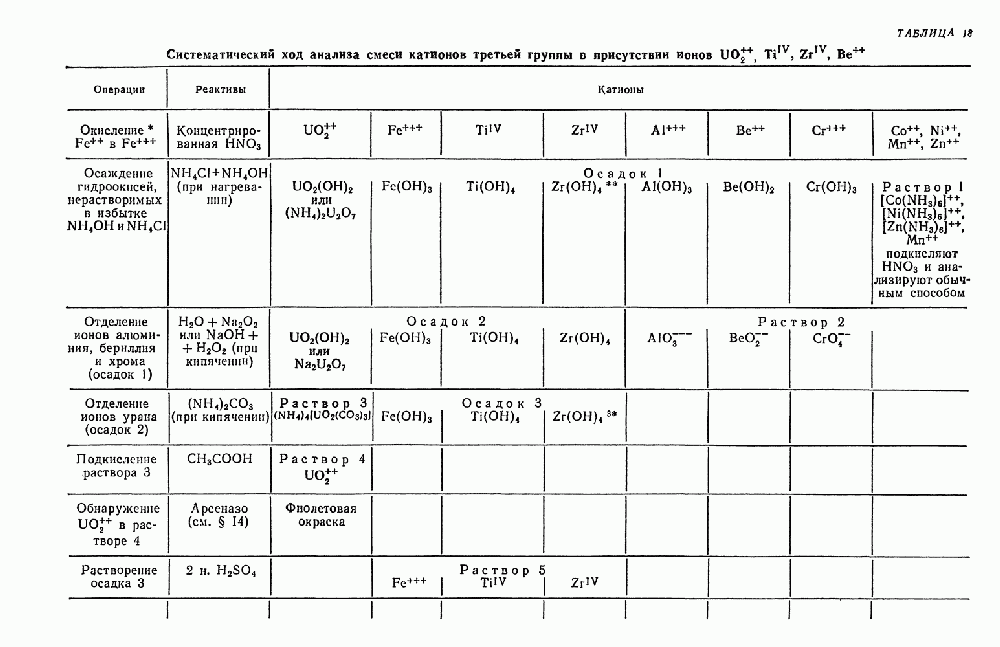
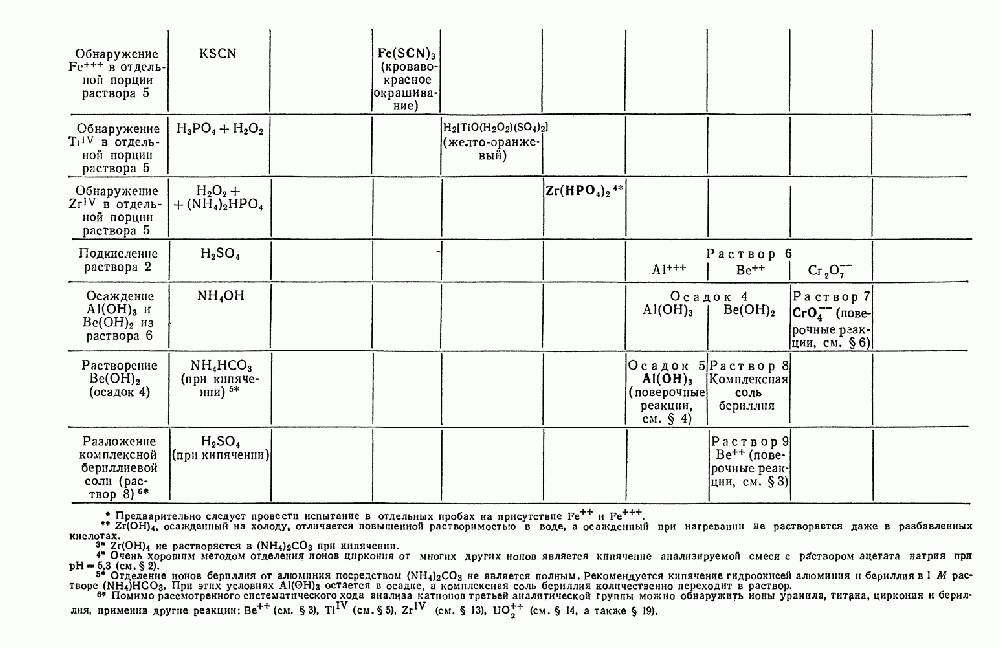
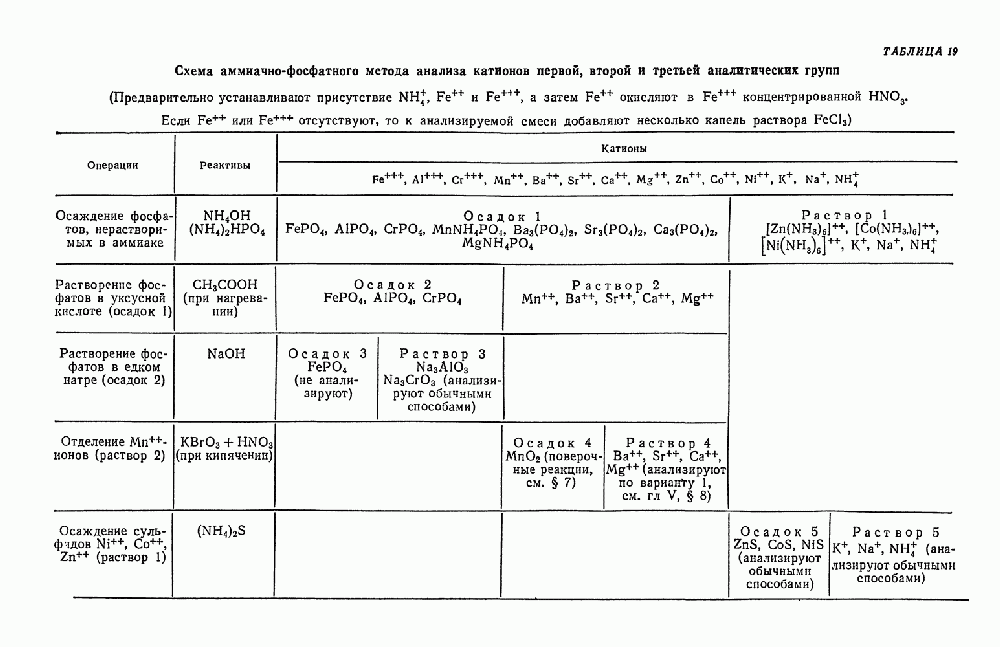
- § 22. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп в присутствии PO-ионов
- ГЛАВА VII. ЧЕТВЕРТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика четвертой аналитической группы катионов
- § 2. Общие реакции катионов четвертой аналитической группы
- РЕАКЦИИ КАТИОНОВ ПЕРВОЙ ПОДГРУППЫ (ПОДГРУППЫ МЕДИ)
- § 3. Обнаружение Hg-ионов
- § 4. Обнаружение Cu-ионов
- § 5. Обнаружение Cd-ионов
- § 6. Обнаружение Bi-ионов
- РЕАКЦИИ КАТИОНОВ ВТОРОЙ ПОДГРУППЫ (ПОДГРУППЫ МЫШЬЯКА)
- § 7. Обнаружение ионов мышьяка (III)
- § 8. Обнаружение ионов мышьяка (V)
- § 9. Общие реакции обнаружения
- § 10. Обнаружение ионов сурьмы (III)
- § 11. Обнаружение ионов сурьмы (V)
- § 12. Общие реакции обнаружения Sb
- § 13. Обнаружение ионов олова (II)
- § 14. Обнаружение ионов олова (IV)
- § 15. Общие реакции обнаружения ионов олова (II) и олова (IV)
- § 16. Отделение ионов олова от других ирнов четвертой аналитической группы
- § 17. Обнаружение ионов германия (IV)
- § 18. Отделение ионов германия от других ионов четвертой аналитической группы
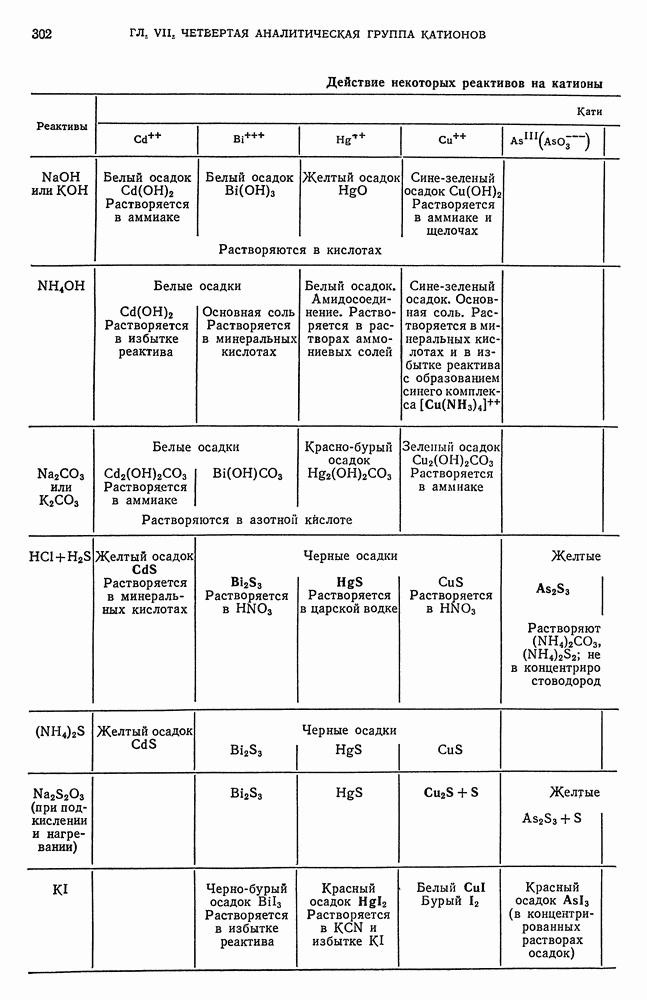
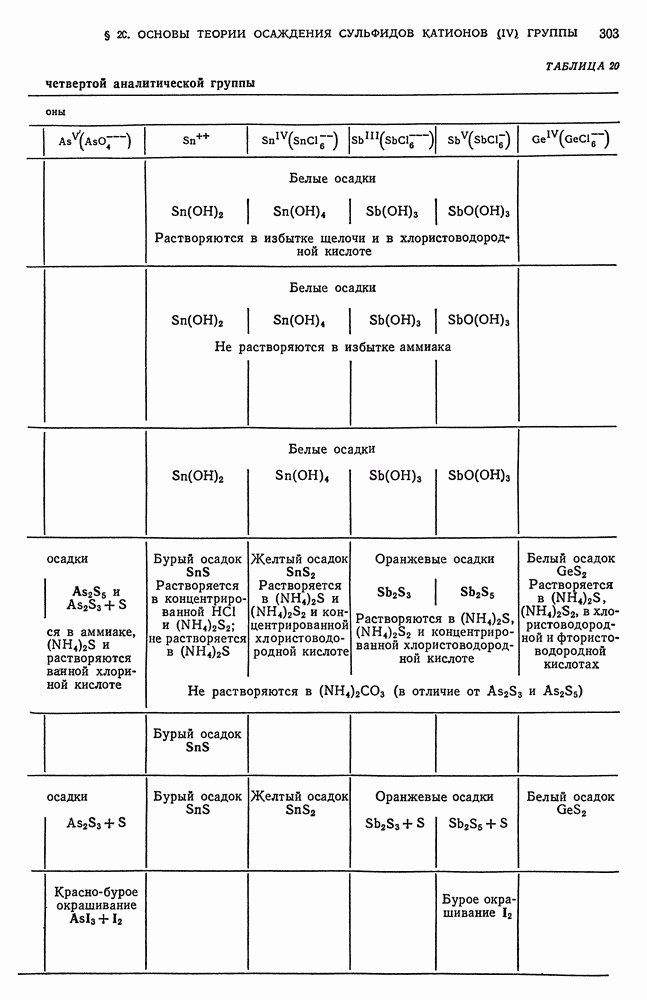
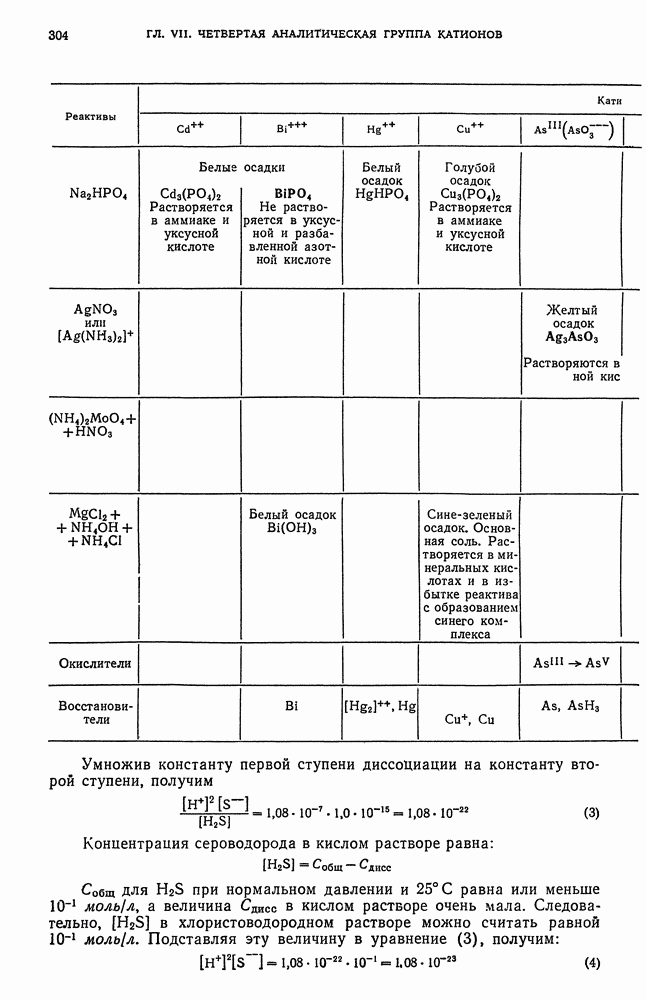
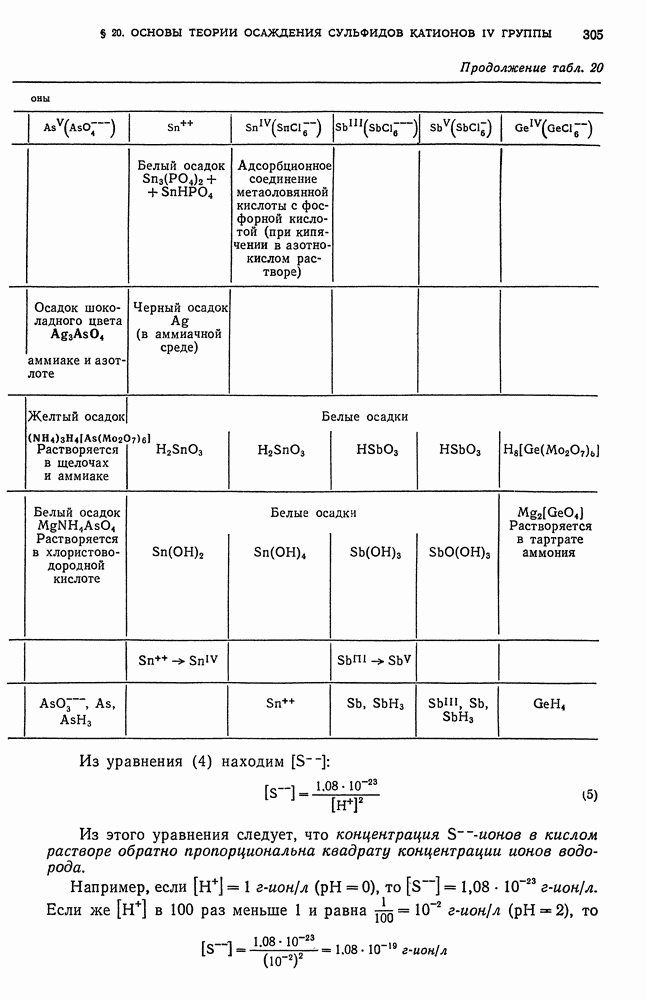
- § 19. Обзор действия реактивов на катионы четвертой аналитической группы
- § 20. Основы теории осаждения сульфидов катионов четвертой аналитической группы групповым реактивом — сероводородом
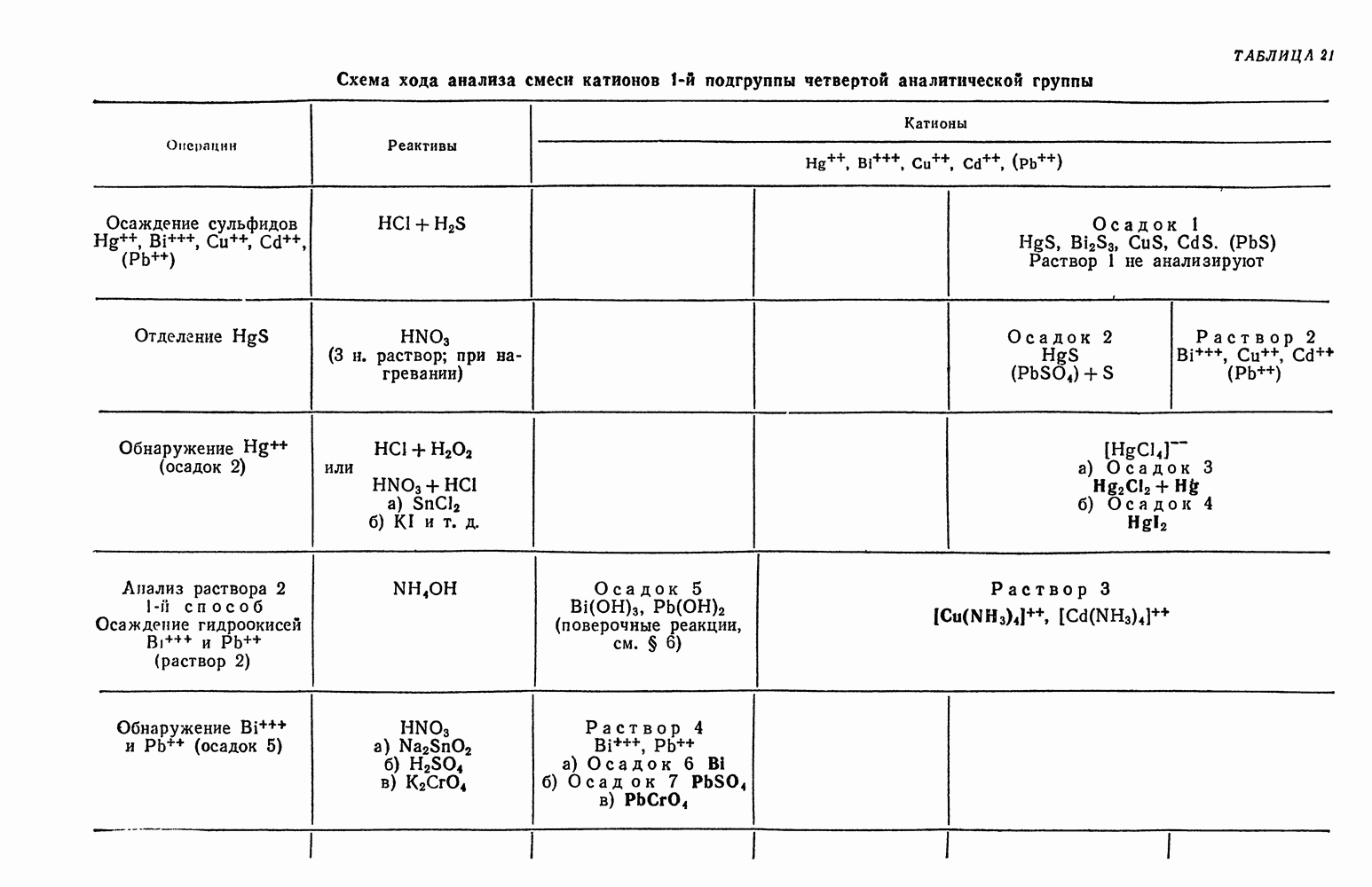
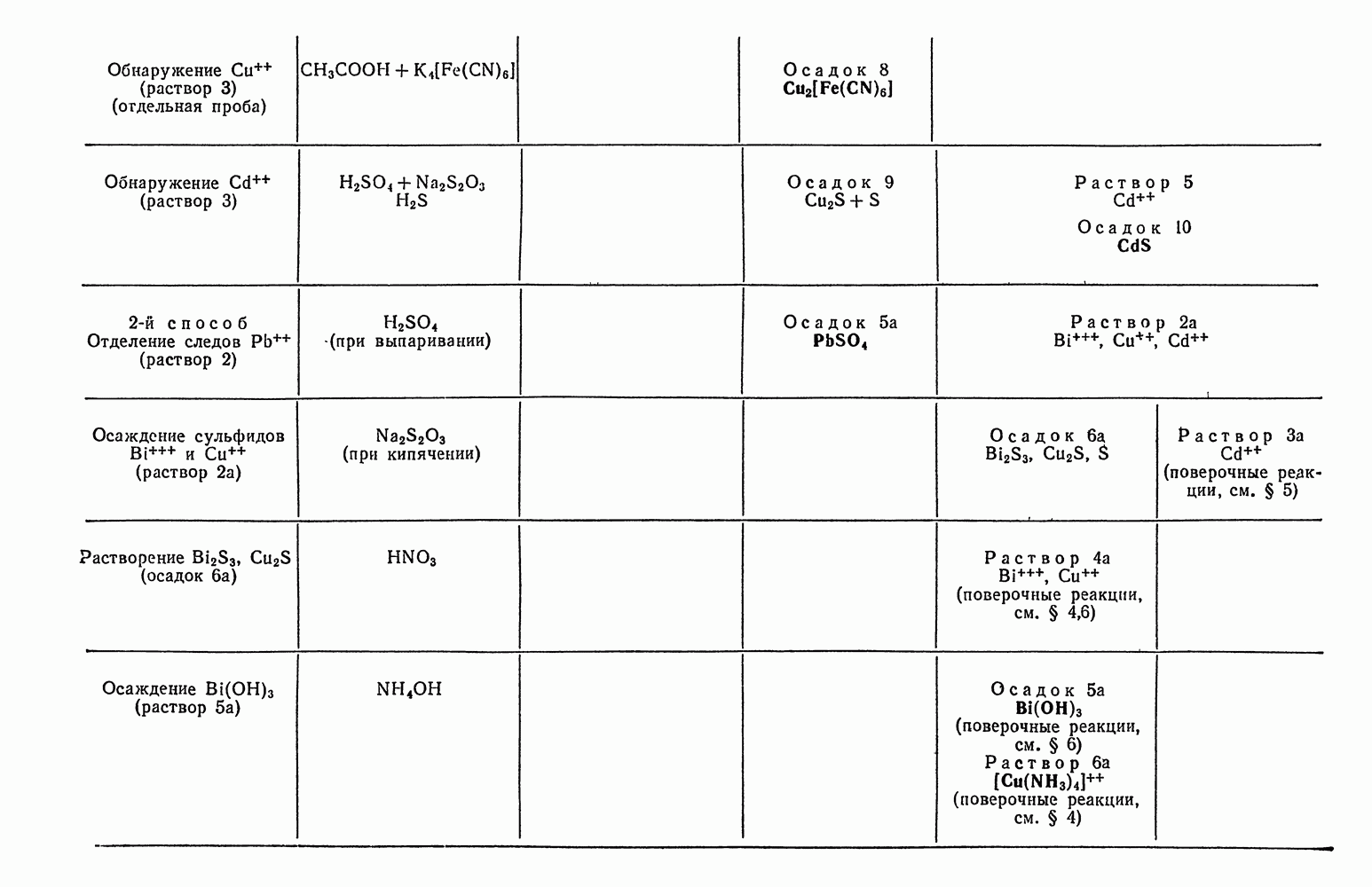
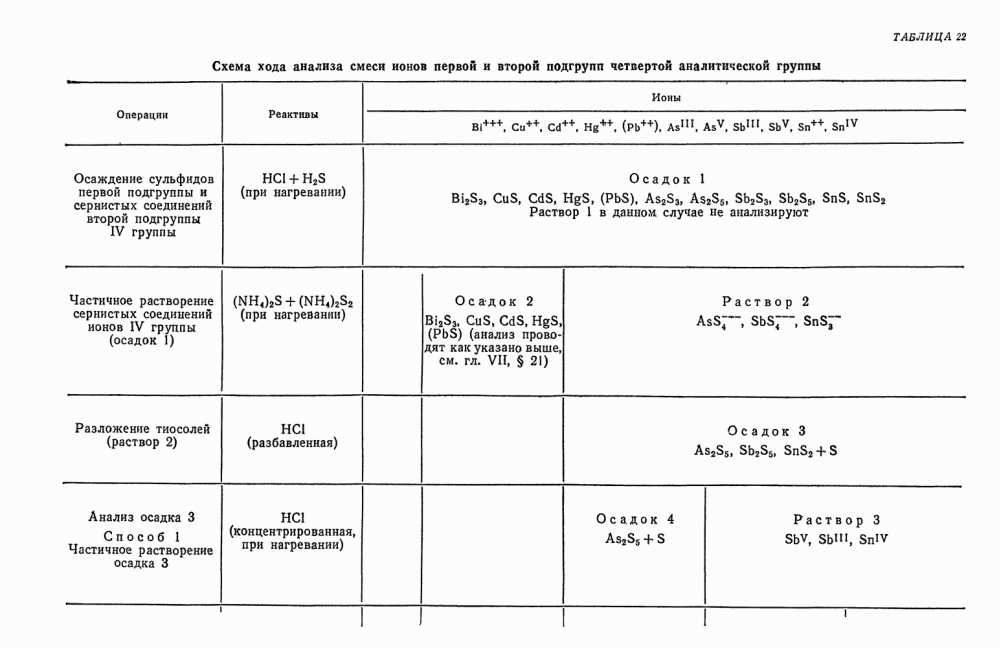
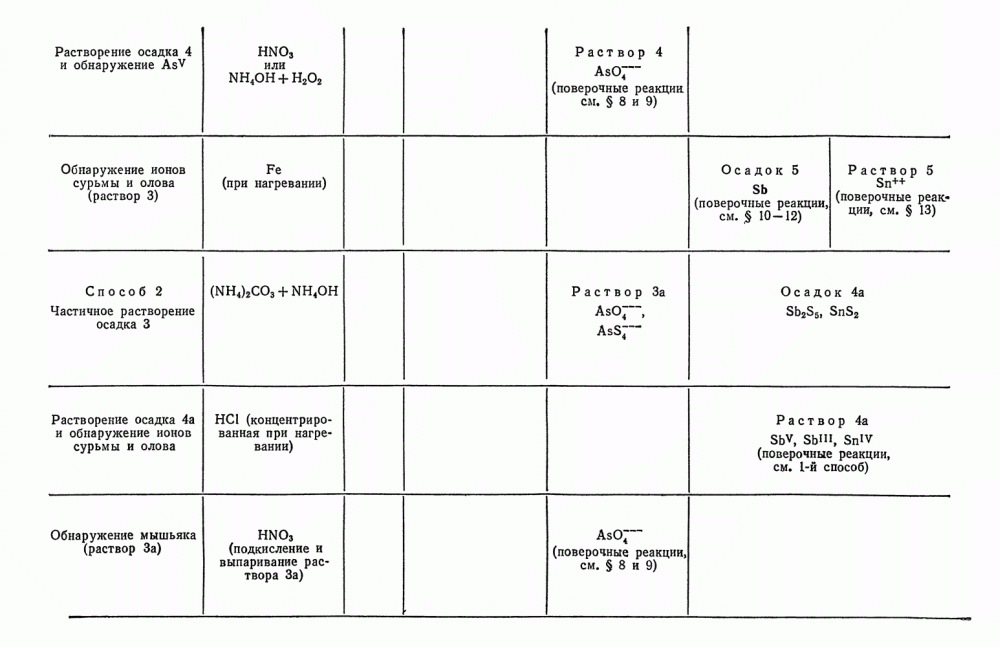
- § 21. Систематический ход анализа смеси катионов четвертой аналитической группы
- ГЛАВА VIII. ПЯТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ (ГРУППА СЕРЕБРА)
- § 1. Характеристика пятой аналитической группы катионов
- § 2. Общие реакции катионов пятой аналитической группы
- § 3. Обнаружение Ag-ионов
- § 4. Обнаружение [Hg]-ионов
- § 5. Обнаружение Pb-ионов
- § 6. Обзор действия реактивов на катионы пятой аналитической группы
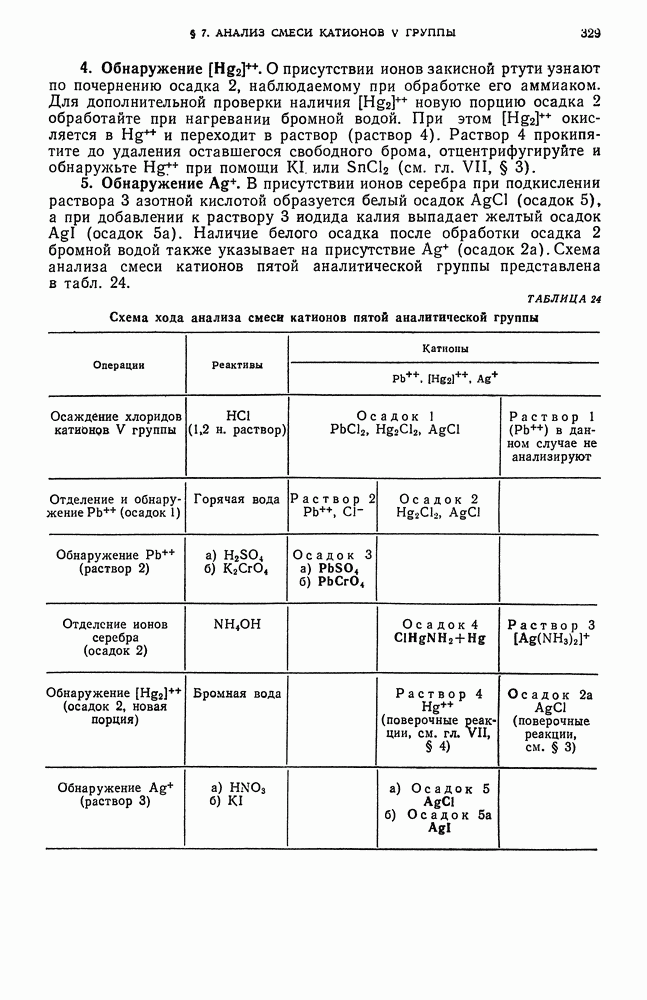
- § 7. Систематический ход анализа смеси катионов пятой аналитической группы
- ГЛАВА IX. АНАЛИЗ СМЕСИ ИОНОВ ВСЕХ ПЯТИ АНАЛИТИЧЕСКИХ ГРУПП
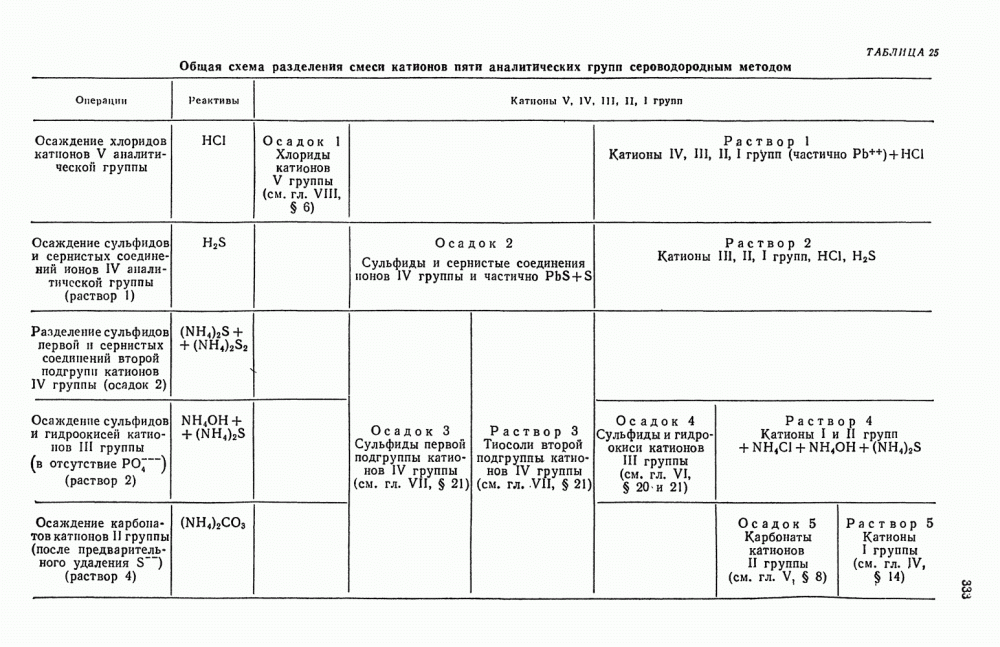
- § 1. Сероводородный метод анализа
- § 2. Недостатки сероводородного метода анализа
- § 3. Ошибки, возникающие при анализе смеси ионов пяти аналитических групп
- § 4. Бессероводородные методы анализа
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ АНИОНОВ И АНАЛИЗ СМЕСЕЙ АНИОНОВ
- § 1. Аналитическая классификация анионов
- § 2. Групповые реактивы на анионы
- § 3. Классификация методов анализа анионов
- ГЛАВА XI. ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика первой группы анионов
- § 2. Реакции анионов первой группы
- § 3. Обнаружение CI-ионов
- § 4. Обнаружение Br-ионов
- § 5. Обнаружение I-ионов
- § 6. Обнаружение CN-ионов
- § 7. Обнаружение SCN-ионов
- § 8. Обнаружение [Fe(CN)]-ионов
- § 9. Обнаружение Fe(CN)-ионов
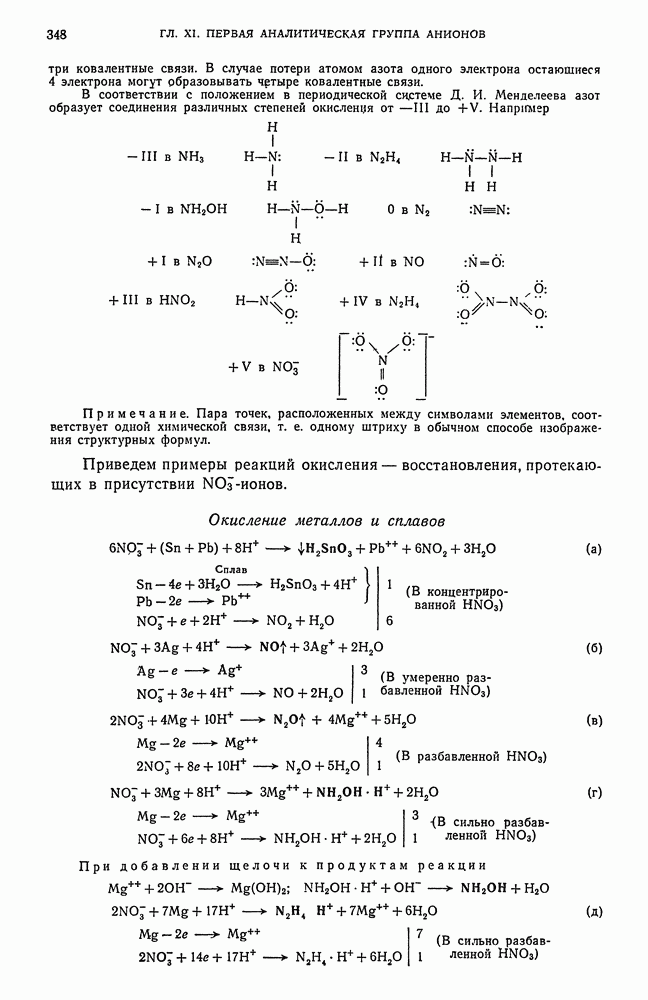
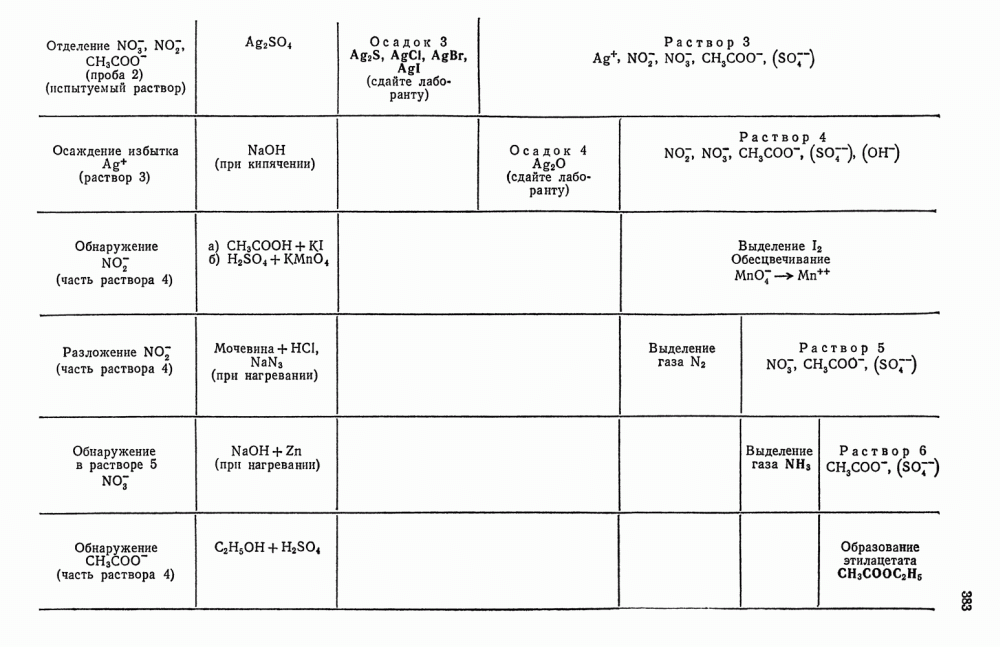
- § 10. Обнаружение NO-ионов
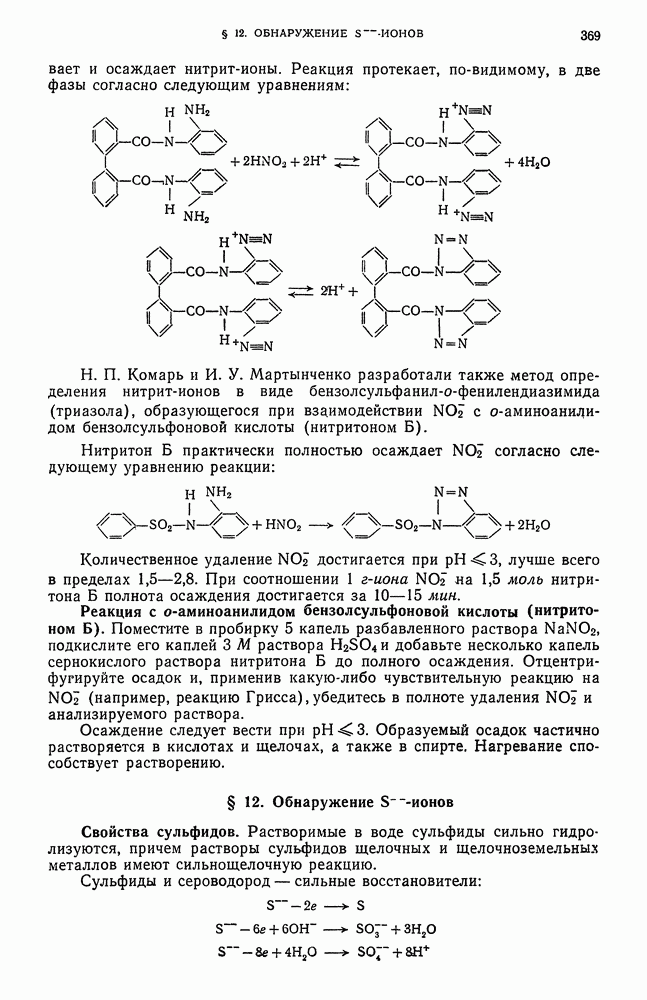
- § 11. Обнаружение NO2-ионов
- § 12. Обнаружение S-ионов
- § 13. Обнаружение CH3COOO-ионов
- § 14. Обнаружение BrO3-ионов
- § 15. Обнаружение ClO3-ионов
- § 16. Обнаружение ClO4-ионов
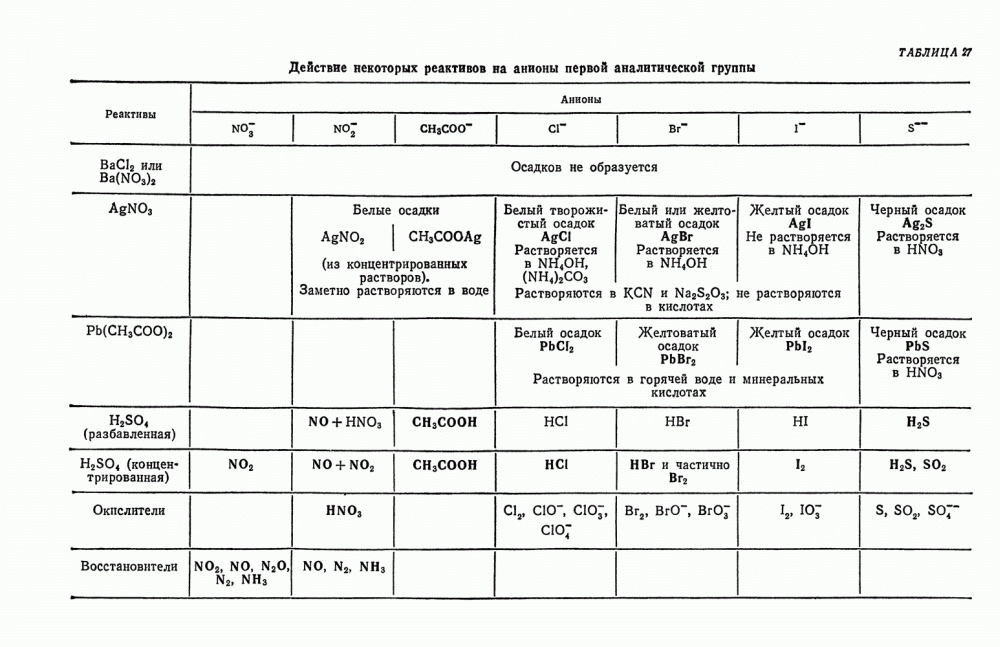
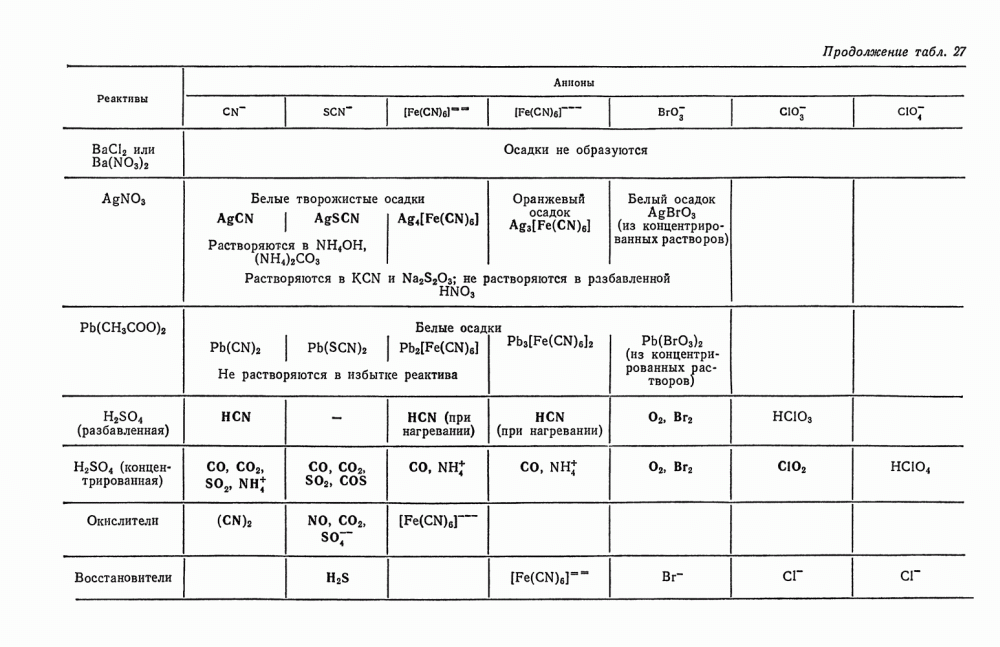
- § 17. Обзор действия реактивов на анионы первой группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 18. Анализ смеси Cl, Br и I-ионов
- § 19. Анализ смеси Cl, Br, I и SCN-ионов
- § 20. Анализ смеси Cl, ClO3 и ClO4-ионов
- § 21. Анализ смеси NO2 и NO3-ионов
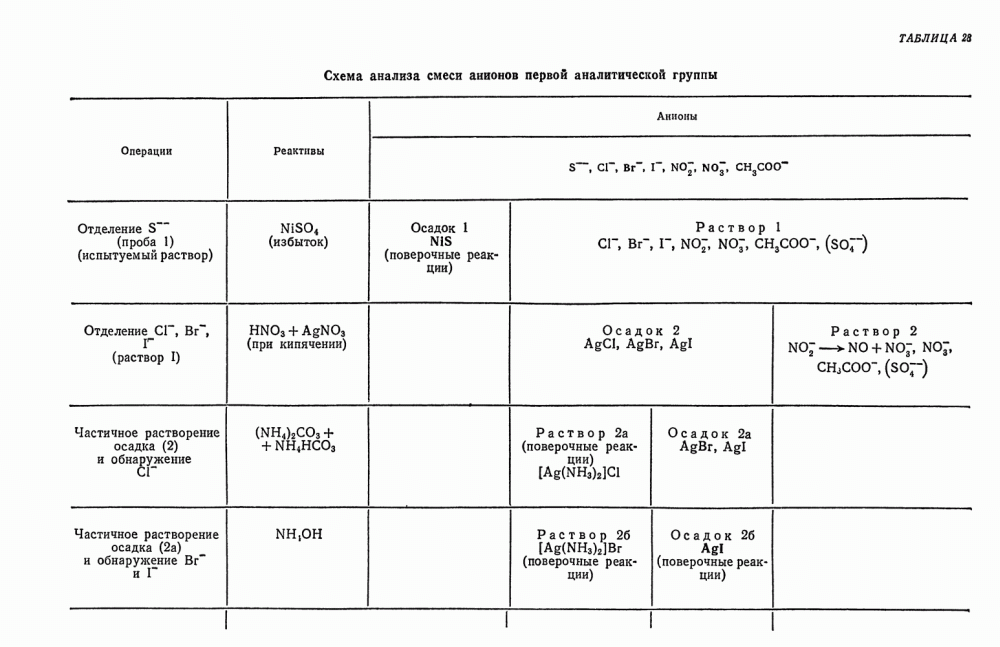
- § 22. Анализ смеси анионов первой группы
- ГЛАВА XII. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика второй группы анионов
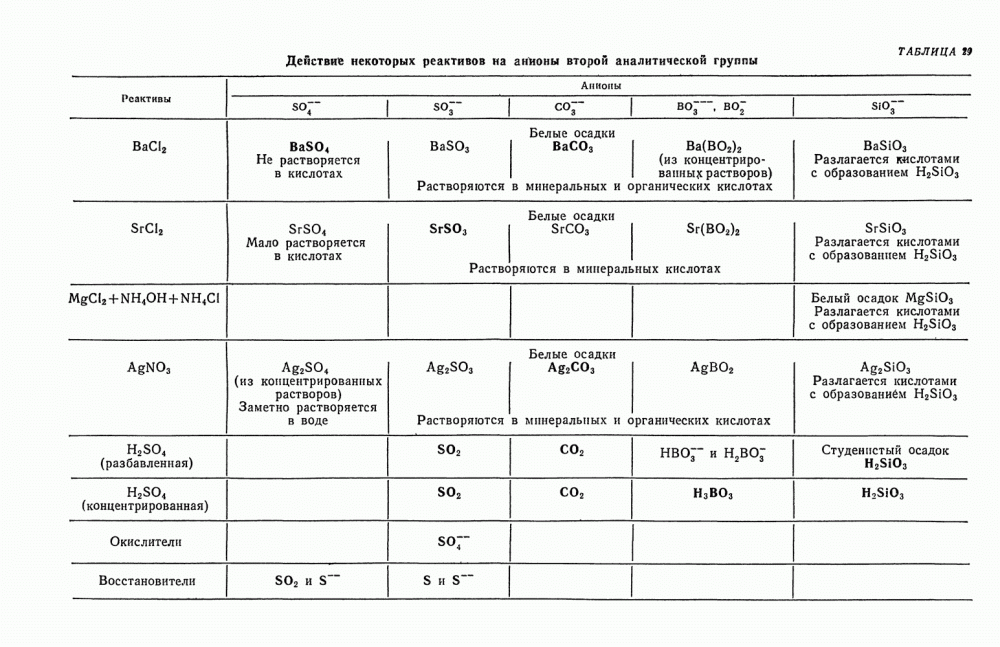
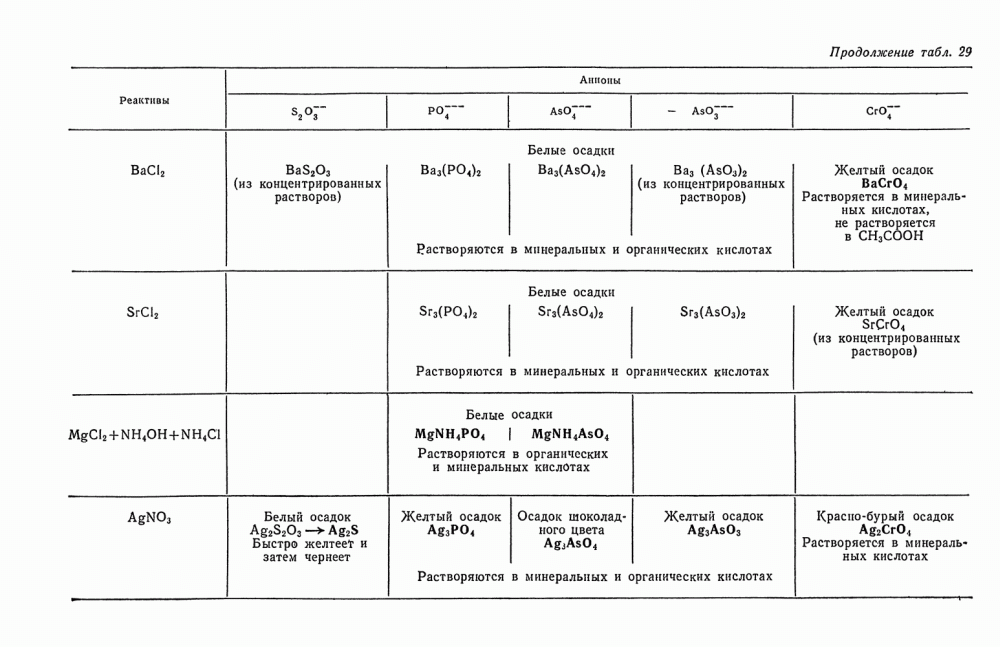
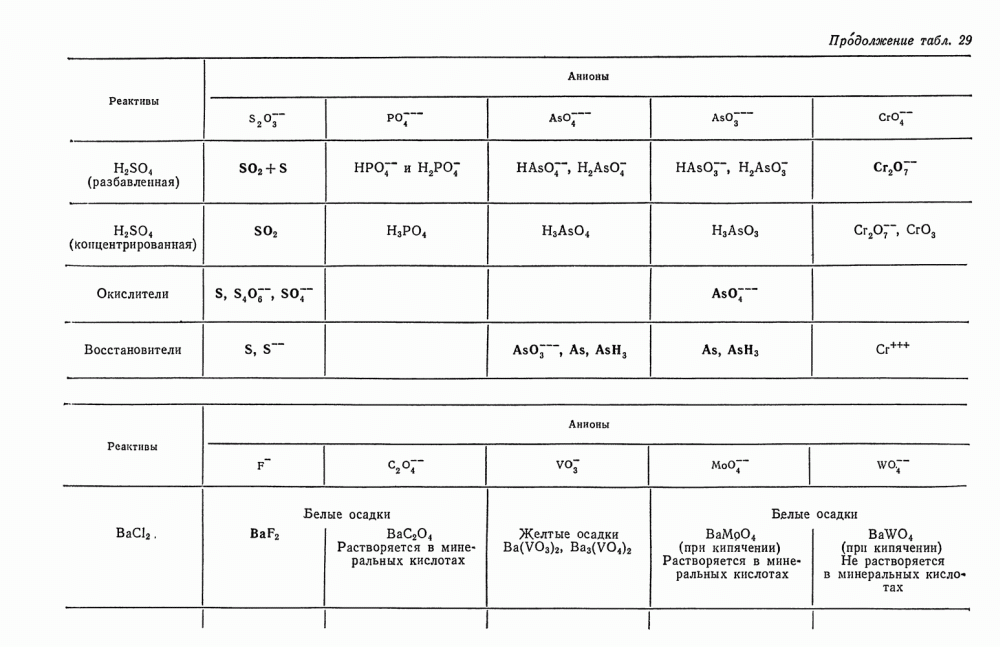
- § 2. Общие реакции анионов второй группы
- § 3. Обнаружение SO3-ионов
- § 4. Обнаружение S2O3-ионов
- § 5. Обнаружение S2O3 в присутствии SO3-ионов
- § 6. Обнаружение SO4-ионов
- § 7. Обнаружение CO3-ионов
- § 8. Обнаружение CO3-ионов в присутствии SO3 и S2O3-ионов
- § 9. Обнаружение PO4-ионов
- § 10. Обнаружение CrO4-ионов
- § 11. Обнаружение AsO3-ионов
- § 12. Обнаружение AsO4-ионов
- § 13. Обнаружение BO2 и BO3-ионов
- § 14. Обнаружение SiO3-ионов
- § 15. Обнаружение F-ионов
- § 16. Обнаружение C2O4-ионов
- § 17. Обнаружение VO3-ионов
- § 18. Обнаружение MoO4-ионов
- § 19. Обнаружение WO4-ионов
- § 20. Обзор действия реактивов на анионы второй группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 21. Анализ смеси ионов
- § 22. Анализ смеси SO3, SO4, S2O3 и CO3-ионов
- § 23. Анализ смеси VO2, MoO4 и WO4-ионов
- § 24. Анализ смеси анионов второй группы
- § 25. Анализ смеси анионов первой и второй групп
- ГЛАВА XIII. ОБНАРУЖЕНИЕ СВОБОДНЫХ МЕТАЛЛОВ И НЕМЕТАЛЛОВ, ИДЕНТИФИЦИРОВАНИЕ СОЛЕЙ И ДРУГИХ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И АНАЛИЗ ИХ СМЕСЕЙ
- § 1. Подготовка вещества к анализу
- § 2. Предварительные испытания
- § 3. Растворение анализируемого вещества в воде, кислотах и щелочах
- § 4. Переведение в растворимое состояние веществ, нерастворимых в воде, кислотах и щелочах
- § 5. Анализ неизвестного вещества
- § 6. Обнаружение свободных элементов
- § 7. Идентифицирование солей и других индивидуальных соединений
- § 8. Обнаружение микропримесей
- § 9. Анализ сплавов
- § 10. Анализ силикатов и алюмосиликатов
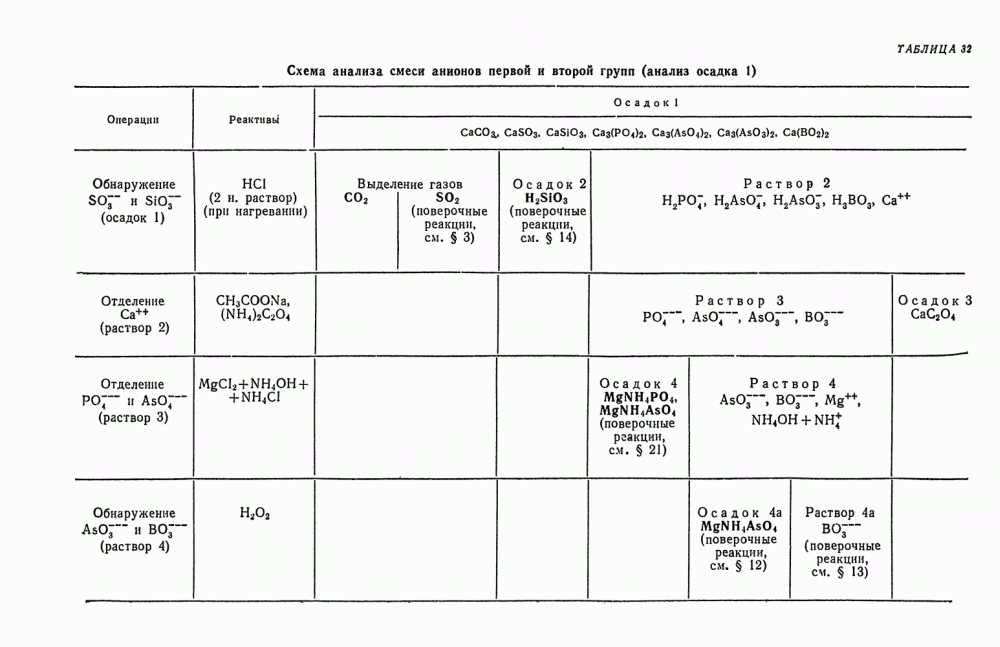
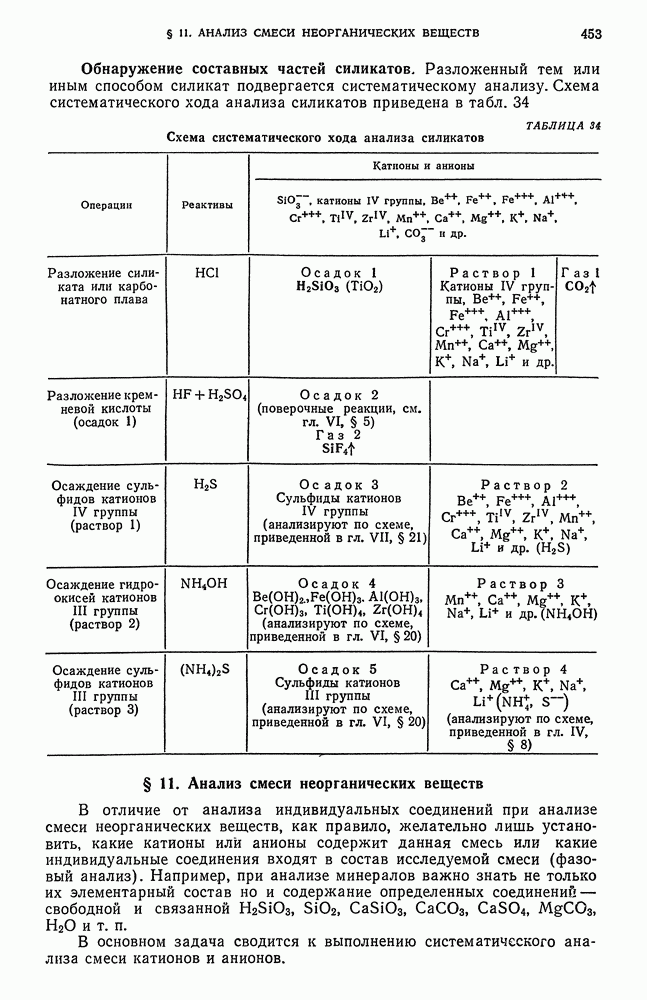
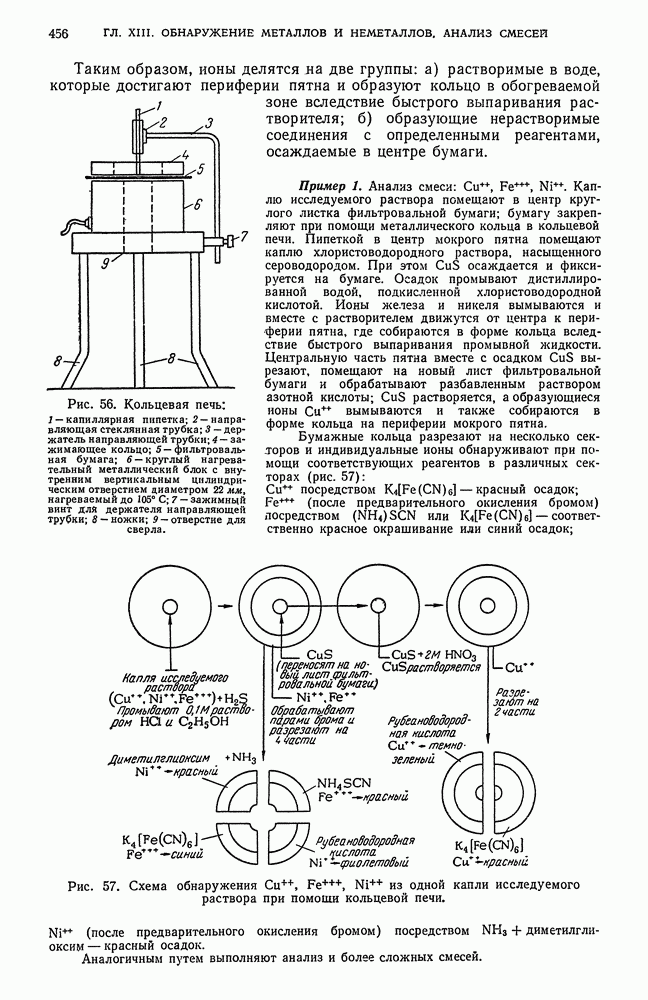
- § 11. Анализ смеси неорганических веществ
- § 12. Экспрессный метод анализа смесей катионов и анионов
- § 13. Идентифицирование нерастворимых веществ
- ЛИТЕРАТУРА