| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 2. Предварительные испытания
Предварительные испытания позволяют установить присутствие некоторых элементов, обнаружение которых затруднено при систематическом ходе анализа. Так, некоторые ионы не осаждаются полностью ни в одной группе, другие увлекаются в осадок в процессе осаждения отдельных катионов и анионов, некоторые разрушаются при подкислении, нагревании и т. п., наконец, ряд ионов приходится вводить в анализируемую смесь при систематическом анализе.
Поэтому их предварительно обнаруживают дробным методом в отдельных пробах исходного раствора.
В зависимости от физического состояния анализируемого вещества проводят различные предварительные испытания.
Для предварительных испытаний, связанных с нагреванием вещества, обычно достаточно небольшое количество сухого образца, размером от просяного до конопляного зерна. Твердый образец должен быть тщательно измельчен и хорошо смешан. Если анализу подвергается раствор, то его предварительно выпаривают и испытаниям подвергают сухой остаток.
Окрашивание пламени. При внесении в бесцветное пламя горелки летучих соединений некоторых элементов пламя окрашивается. Например:

Нагревание в фарфоровой чашке, микротигле или в калильной трубке. Образец анализируемого вещества помещают в фарфоровую чашку или тигель и затем нагревают на пламени горелки. Температуру повышают медленно и доводят ее до 600° С (температура красного каления). В процессе нагревания образца могут наблюдаться термическое разложение, окисление, возгонка и химические реакции между отдельными компонентами, входящими в состав испытуемого вещества.
При нагревании неизвестного вещества всегда нужно соблюдать крайнюю осторожность, так как это вещество при нагревании может воспламениться или даже взорваться. Поэтому сначала испытывают только очень небольшое количество исследуемого вещества. Иногда нагревание вещества проводят в калильной трубке.
Калильной трубкой называют пробирку из тугоплавкого стекла длиной около 5—6 см и диаметром 0,5 см.
Небольшое количество анализируемого вещества (около 0,1 г) насыпают на дно калильной трубки, закрепляют трубку в горизонтальном положении и медленно нагревают в пламени газовой горелки, внимательно наблюдая за происходящими изменениями вещества.
Испытуемое вещество может: а) полностью возгоняться; б) возгоняться частично; в) совсем не возгоняться.
Если вещество возгоняется полностью, то следует предположить, что нелетучие соединения отсутствуют; при частичной возгонке можно заключить, что вещество состоит лишь частично из летучих продуктов; если вещество не возгоняется, то летучие соединения отсутствуют.
Если вещество нелетуче, то это указывает на отсутствие солей ртути и аммония, карбонатрв, разлагающихся с образованием двуокиси углерода, органических и элементоорганических соединений, веществ, в состав которых входит кристаллизационная или адсорбированная вода (гели или гидраты) и т. д.
Если вещество возгоняется, то по окраске возгона (сублимата) также можно сделать ряд выводов:
Белый возгон свидетельствует о возможном присутствии солей аммония, хлорида и бромида ртути, окисей мышьяка и сурьмы;
Желтый — о присутствии сернистых соединений ртути, мышьяка иодида ртути и элементарной серы;
Серый или черный — о присутствии соединений ртути, мышьяка, иодидов, органических соединений и др.
При нагревании веществ в калильной трубке наряду с возгонкой может происходить выделение паров и газов. Так, образование капель воды указывает на присутствие солей, содержащих кристаллизационную воду, органических соединений, гидроокисей, основных или кислых солей.
Выделение кислорода свидетельствует о присутствии перекисных соединений, нитратов, хлоратов, перманганатов и других богатых кислородом соединений; двуокиси углерода — о присутствии карбонатов, оксалатов и органических соединений; окиси углерода — о присутствии оксалатов и органических соединений; окислов азота — о присутствии нитратов и нитритов; выделение хлора, брома и иода — о присутствии хлоридов, бромидов и иодидов, гипохлоритов, хлоратов, броматов, иодатов и других подобных соединений, разлагающихся при нагревании или вступающих в реакцию окисления — восстановления; выделение аммиака свидетельствует о присутствии солей аммония, цианидов, роданидов и т. п.
Если вещество плавится, то возможно присутствуют нитраты, нитриты, ацетаты, карбонаты и сульфаты щелочных металлов, квасцы, сульфаты железа, цинка, меди, а также  и т. п.
и т. п.
Если вещество изменяет свой цвет, то не исключена возможность присутствия солей тяжелых металлов, разлагающихся с образованием окислов (например,  и т. п.). Желтый хромат аммония (а) и оранжевый бихромат аммония (б) при нагревании разлагаются с образованием зеленой окиси хрома:
и т. п.). Желтый хромат аммония (а) и оранжевый бихромат аммония (б) при нагревании разлагаются с образованием зеленой окиси хрома:

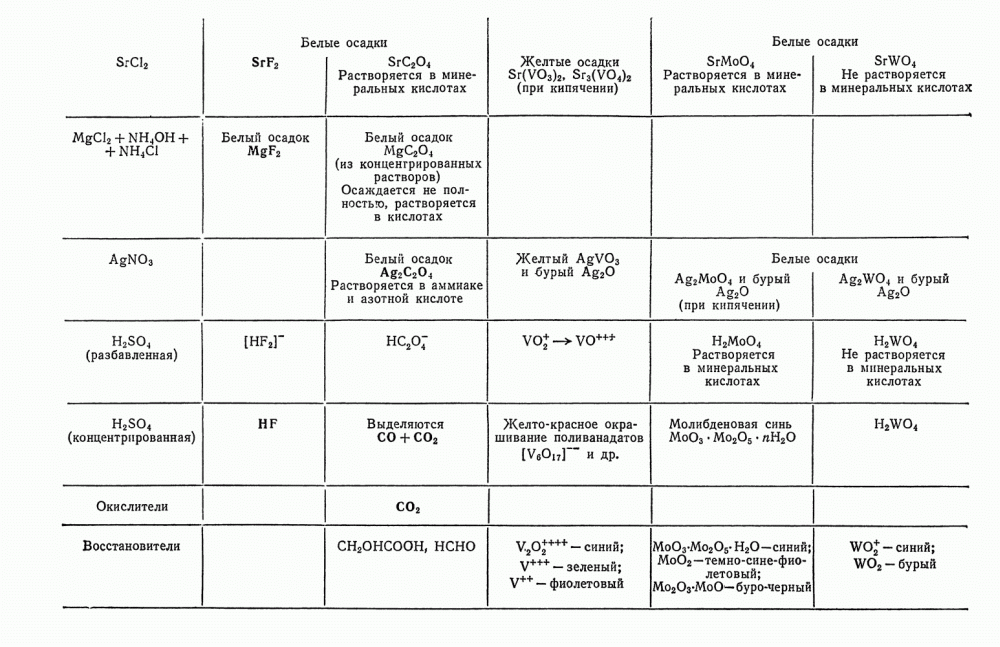
Желтый арсенит серебра становится темно-коричневым вследствие образования метаарсената серебра и металлического серебра:

Молибдаты и вольфраматы, реагируя с восстановителями, дают продукты реакции, окрашенные в синий цвет:

Соли кобальта и марганца при нагревании в смеси с нитратами, нитритами и хлоратами щелочных металлов окисляются до трех- и четырехвалентного состояния:

Получение окрашенных перлов. Очень часто в качестве предварительного испытания прибегают к получению окрашенных перлов буры или фосфорной соли.
Реакции окрашивания перлов не всегда надежны, так как окраска перлов меняется в зависимости от температуры нагревания и от концентрации испытуемого вещества.
Кроме того, при наличии в испытуемом веществе нескольких элементов, образующих окрашенные соединения, получаются перлы смешанной, трудноразличимой окраски (табл. 33).
ТАБЛИЦА 33. Окраска перлов буры некоторыми элементами

Действие разбавленной серной кислоты на испытуемое вещество.К части анализируемого вещества на холоду приливают 2 н. раствор серной кислоты и наблюдают выделение газов и паров:
 (газ без запаха) — выделяется в том случае, если в исходной смеси содержатся карбонаты;
(газ без запаха) — выделяется в том случае, если в исходной смеси содержатся карбонаты;
 (газ с запахом горящей серы) — при содержании сульфитов (без выделения серы) или тиосульфатов (с выделением серы);
(газ с запахом горящей серы) — при содержании сульфитов (без выделения серы) или тиосульфатов (с выделением серы);
 (газ с запахом тухлых яиц) — при содержании в испытуемом веществе сульфидов;
(газ с запахом тухлых яиц) — при содержании в испытуемом веществе сульфидов;
 (газ с запахом горького миндаля) — при содержании цианидов. Синильная кислота и ее водные растворы очень ядовиты. Незначительное содержание ее паров в воздухе (свыше
(газ с запахом горького миндаля) — при содержании цианидов. Синильная кислота и ее водные растворы очень ядовиты. Незначительное содержание ее паров в воздухе (свыше  ) опасно для жизни!
) опасно для жизни!
 (газ бурого цвета) — при содержании нитритов.
(газ бурого цвета) — при содержании нитритов.
При нагревании смеси испытуемого вещества с серной кислотой также наблюдают выделение газов:
 (зеленоватый газ со специфическим резким запахом) выделяется в том случае, если в исходном веществе содержались гипохлориты;
(зеленоватый газ со специфическим резким запахом) выделяется в том случае, если в исходном веществе содержались гипохлориты;
 — при содержании ацетатов;
— при содержании ацетатов;
 (газ без запаха, поддерживающий горение) выделяется при содержании в исходном веществе перекисных соединений.
(газ без запаха, поддерживающий горение) выделяется при содержании в исходном веществе перекисных соединений.
Более подробно о действии  см. гл. XI и XII.
см. гл. XI и XII.
Действие концентрированной серной кислоты. После действия разбавленной серной кислоты на анализируемое вещество (раствор) к той же пробе приливают концентрированную серную кислоту. Брать новую пробу анализируемого вещества для этого не следует. Если анализируемая смесь реагирует с разбавленной серной кислотой, то при добавлении концентрированной кислоты непосредственно к испытуемому веществу реакция протекает очень бурно, содержимое пробирки разбрызгивается. (Осторожно! Серная кислота может ожечь лицо и руки!)
При действии концентрированной серной кислоты могут дополнительно выделяться газы и пары:
 — при содержании хлоридов;
— при содержании хлоридов;
 (красно-бурые пары) — при совместном содержании бихроматов, хроматов и хлоридов;
(красно-бурые пары) — при совместном содержании бихроматов, хроматов и хлоридов;
 — при содержании в испытуемом веществе роданидов;
— при содержании в испытуемом веществе роданидов;
СО и  — при содержании оксалатов;
— при содержании оксалатов;
 (газ желтого цвета) —при содержании хлоратов;
(газ желтого цвета) —при содержании хлоратов;
 (желто-бурый газ) — при содержании бромидов;
(желто-бурый газ) — при содержании бромидов;
 (фиолетовые пары)-при содержании в исходной смеси иодидов;
(фиолетовые пары)-при содержании в исходной смеси иодидов;
 (бурые пары) — при содержании нитратов;
(бурые пары) — при содержании нитратов;
 — при содержании в исходной смеси кислородсодержащих соединений (перекисей, окисей, гидроокисей или кислородсодержащих солей высоковалентных элементов, хроматов, перманганатов и т. п.);
— при содержании в исходной смеси кислородсодержащих соединений (перекисей, окисей, гидроокисей или кислородсодержащих солей высоковалентных элементов, хроматов, перманганатов и т. п.);
 — при содержании фторидов и фторосиликатов.
— при содержании фторидов и фторосиликатов.
Растворение в воде. Небольшую пробу анализируемого вещества растворяют в дистиллированной воде. Проба на растворимость в воде имеет большое значение и дает возможность судить о составе исследуемого вещества (см. ниже).
Определение  раствора.
раствора.  раствора определяют при помощи шкалы стандартных растворов индикаторов или универсального индикатора (см. гл. III, § 16).
раствора определяют при помощи шкалы стандартных растворов индикаторов или универсального индикатора (см. гл. III, § 16).
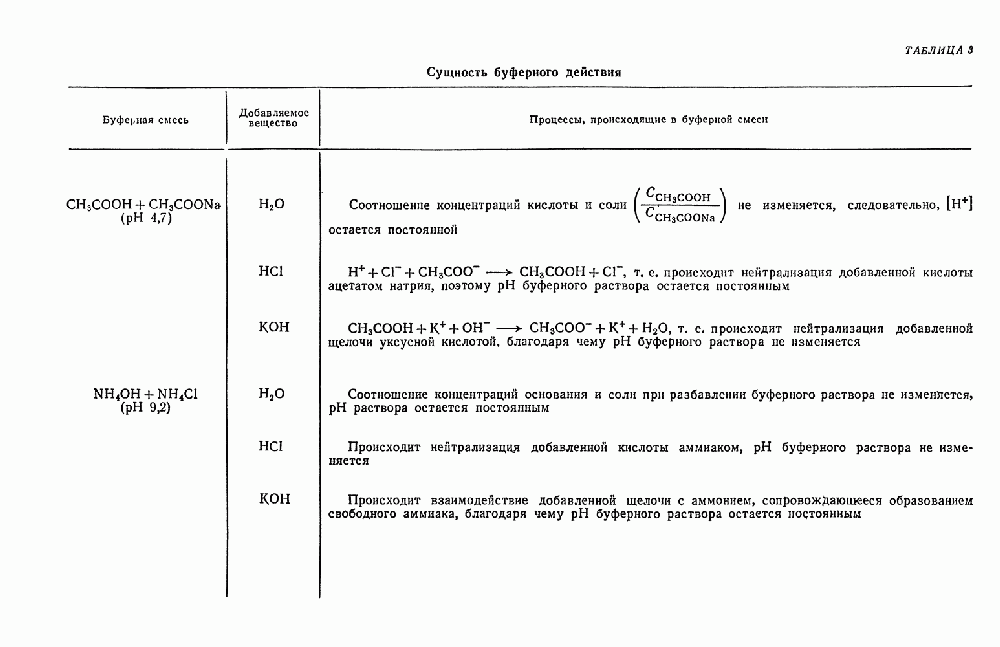
В кислом растворе (при низких значениях  ) не могут содержаться соли угольной, тиосерной, сернистой, сероводородной, азотистой кислот, так как они в сильнокислой среде разлагаются. В сильнокислом растворе не могут содержаться также соли щелочных и щелочноземельных металлов слабых кислот: уксусной, борной, кремневой, хлорноватистой, средние соли фосфорной, мышьяковистой и др., которые в такой среде разлагаются с образованием свободных кислот или моно- и дигидроанионов. Наконец, в кислом растворе несовместимо присутствие многих окислителей и восстановителей. Однако следует иметь в виду, что слабокислые растворы могут представлять собой буферные смеси (смесь растворов
) не могут содержаться соли угольной, тиосерной, сернистой, сероводородной, азотистой кислот, так как они в сильнокислой среде разлагаются. В сильнокислом растворе не могут содержаться также соли щелочных и щелочноземельных металлов слабых кислот: уксусной, борной, кремневой, хлорноватистой, средние соли фосфорной, мышьяковистой и др., которые в такой среде разлагаются с образованием свободных кислот или моно- и дигидроанионов. Наконец, в кислом растворе несовместимо присутствие многих окислителей и восстановителей. Однако следует иметь в виду, что слабокислые растворы могут представлять собой буферные смеси (смесь растворов  и т. д.) и, следовательно, могут содержать соли щелочных и щелочноземельных металлов.
и т. д.) и, следовательно, могут содержать соли щелочных и щелочноземельных металлов.
В щелочной среде отсутствуют соли слабых оснований и сильных кислот.
Обнаружение окислителей и восстановителей. Так как в процессе систематического хода анализа окислители или восстановители, входящие в состав анализируемого вещества, могут претерпевать различные изменения, вызываемые реакциями окисления — восстановления, то необходимо проводить предварительные пробы на присутствие окислителей (с помощью  и KI) и восстановителей с помощью
и KI) и восстановителей с помощью  .
.
Следует иметь в виду, что некоторые смеси окислителей и восстановителей при нагревании сухого вещества реагируют со взрывом. Поэтому, прежде чем проводить испытания на окрашивание пламени, с калильной трубкой и т. п., необходимо с самого начала установить, не входят ли в состав анализируемого вещества взрывчатые смеси. Для этого небольшое количество исследуемого вещества помещают в тигель, который устанавливают в штативе под тягой, защищают лицо щитом из органического стекла и нагревают тигель на пламени газовой горелки: В присутствии взрывчатых смесей наблюдается вспышка.
Если исследуемое вещество содержит б своем составе взрывчатые смеси, то его нельзя растирать в ступке и нагревать в калильной трубке. Такие смеси анализируют, применяя специальные методы.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Анализ и синтез
- § 2. Предмет аналитической химии
- § 3. Развитие аналитической химии
- § 4. Качественный и количественный анализ
- ГЛАВА I. ПРИМЕНЕНИЕ ЗАКОНА ДЕЙСТВИЯ МАСС В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Влияние среды на состояние ионов в растворах
- § 2. Обратимые и необратимые аналитические реакции
- § 3. Направление аналитических реакций; правила обменного разложения
- § 4. Закон действия масс и следствие из него
- § 5. Границы применимости закона действия масс
- § 6. Сильные и слабые электролиты
- § 7. Активность
- § 8. Коэффициент активности и ионная сила
- Б. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ (В ГОМОГЕННЫХ СИСТЕМАХ)
- § 9. Гомогенные и гетерогенные системы
- § 10. Ионное произведение воды
- § 11. Ионы гидроксония
- § 12. Равновесие ионов в водных растворах; понятие о pH
- § 13. Равновесие в водных растворах слабых электролитов
- § 14. Влияние сильных кислот или сильных оснований на степень электролитической диссоциации слабых электролитов
- § 15. Приближенные формулы для расчета [H+] и [OH-] в водных растворах кислот и оснований
- В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
- § 16. Буферные растворы
- § 17. Применение буферных растворов в химическом анализе
- Г. РАВНОВЕСИЯ В РАСТВОРАХ ГИДРОЛИЗУЮЩИХСЯ СОЛЕЙ
- § 18. Теоретические основы гидролиза
- § 19. Механизм гидролитического расщепления
- § 20. Подавление и усиление гидролиза солей
- Д. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ТИПИЧНО АМФОТЕРНЫХ ЭЛЕКТРОЛИТОВ
- § 21. Поведение амфотерных гидроокисей в водных растворах
- § 22. Константы электролитической диссоциации амфотерных гидроокисей
- Е. РАВНОВЕСИЯ В СИСТЕМАХ: ОСАДОК-НАСЫЩЕННЫЙ РАСТВОР
- § 23. Осаждение как один из основных методов химического анализа
- § 24. Произведение растворимости
- § 25. Произведение активностей
- § 26. Вычисление растворимости электролитов в воде по величине произведения растворимости
- § 27. Влияние различных факторов на растворимость малорастворимых электролитов
- Ж. ОСНОВЫ ТЕОРИИ ОБРАЗОВАНИЯ И РАЗЛОЖЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИИ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 28. Характеристика комплексных соединений, имеющих значение в химическом анализе
- § 29. Квантовомеханические представления о строении комплексов
- § 30. Равновесия в растворах комплексных соединений
- § 31. Константы нестойкости комплексов
- § 32. Внутрикомплексные соединения
- § 33. Методы разложения и образования комплексов, применяемых в аналитической химии
- § 34. Применение метода комплексообразования в химическом анализе
- ГЛАВА II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Окисление—восстановление как один из основных методов химического анализа
- § 2. Направление реакций окисления—восстановления
- § 3. Окислительно-восстановительные потенциалы
- § 4. Зависимость между величинами окислительно-восстановительных потенциалов и условиями, в которых протекают реакции окисления—восстановления
- § 5. Вычисление окислительно-восстановительных потенциалов
- § 6. Вычисление окислительно-восстановительных потенциалов с учетом коэффициентов активности
- ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
- § 1. Обнаружение отдельных элементов
- § 2. Анализ мокрым и сухим путем
- § 3. Химические и физические методы качественного анализа
- § 4. Макро-, полумикро- и микрометоды
- § 5. Капельный анализ
- § 6. Микрокристаллоскопический анализ
- § 7. Метод растирания порошков
- § 8. Методы анализа, основанные на нагревании и сплавлении веществ
- § 9. Спектральный качественный анализ
- § 10. Хроматографический метод анализа
- § 11. Кинетические методы анализа
- Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
- § 12. Специфичность и чувствительность реакций
- § 13. Максимальная чувствительность аналитических реактивов
- § 14. Способы повышения чувствительности реакций
- § 15. Маскировка мешающих ионов
- § 16. Определение pH среды
- § 17. Регулирование pH среды в процессе аналитических определений
- В. РЕАКТИВЫ
- § 18. Понятие о химических реактивах
- § 19. Концентрация применяемых реактивов
- § 20. Техника пользования реактивами
- Г. ПОСУДА И ПРИБОРЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕННОМ АНАЛИЗЕ
- § 21. Химическая посуда
- § 22. Приборы
- Д. АНАЛИТИЧЕСКИЕ ГРУППЫ
- § 23. Дробный и систематический анализ
- § 24. Аналитическая классификация катионов
- § 25. Сводные таблицы действия реактивов на катионы и анионы
- Е. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ ИОНОВ
- § 26. Значение периодического закона в аналитической химии
- § 27. Периодическая система элементов Д. И. Менделеева как классификация атомов по их строению
- § 28. Зависимость некоторых химических свойств элементов от положения их в периодической системе Д. И. Менделеева
- § 29. Растворимость химических соединений в связи с положением элементов в периодической системе Д. И. Менделеева
- § 30. Открытие новых аналитических реакций
- § 31. Аналитические группы и периодическая система элементов Д. И. Менделеева
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ КАТИОНОВ И АНАЛИЗ СМЕСЕЙ КАТИОНОВ
- § 1. Характеристика первой аналитической группы катионов
- § 2. Общие реакции катионов первой аналитической группы
- РЕАКЦИИ КАТИОНОВ 1-й ПОДГРУППЫ
- § 3. Обнаружение NН-ионов
- § 4. Методы разложения и удаления солей аммония
- § 5. Обнаружение K-ионов
- § 6. Обнаружение Rb-ионов
- § 7. Обнаружение Cs-ионов
- § 8. Анализ смеси катионов первой подгруппы
- РЕАКЦИИ КАТИОНОВ 2-й ПОДГРУППЫ
- § 9. Обнаружение Li-ионов
- § 10. Обнаружение Na-ионов
- § 11. Обнаружение Mg-ионов
- § 12. Обзор действия реактивов на катионы первой аналитической группы
- § 13. Анализ смеси катионов второй подгруппы
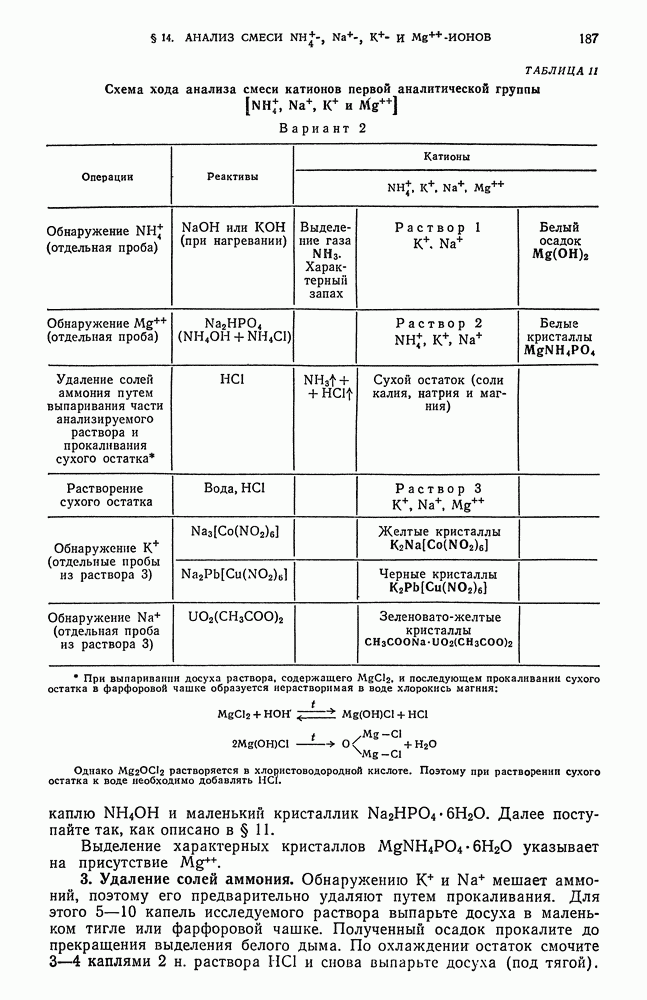
- § 14. Анализ смеси ионов
- § 15. Анализ смеси ионов
- ГЛАВА V. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика второй аналитической группы катионов
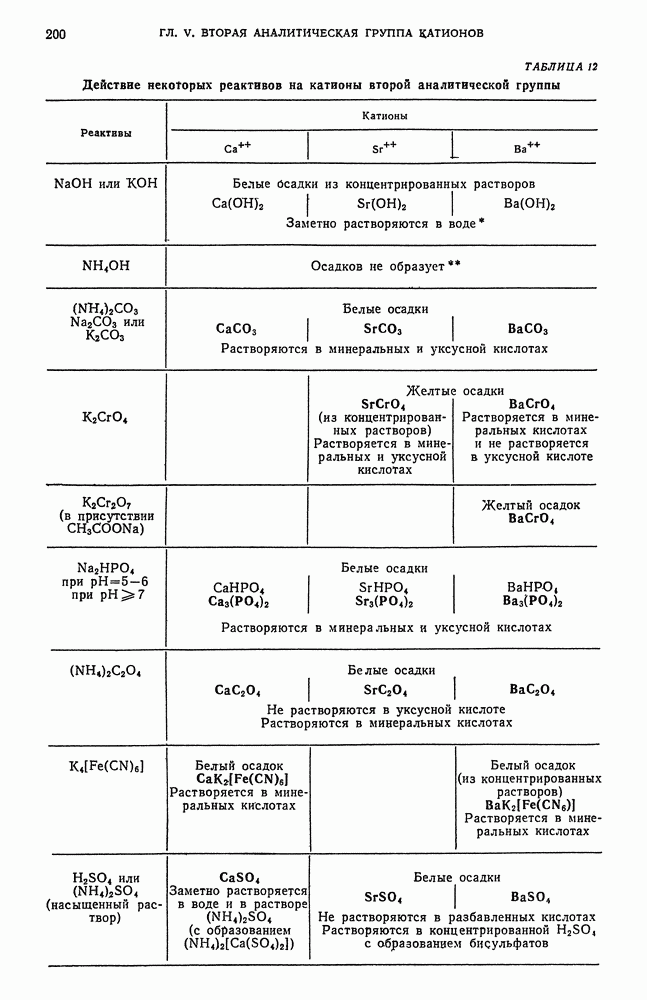
- § 2. Общие реакции катионов второй аналитической группы
- § 3. Обнаружение Ca-ионов
- § 4. Обнаружение Sr-ионов
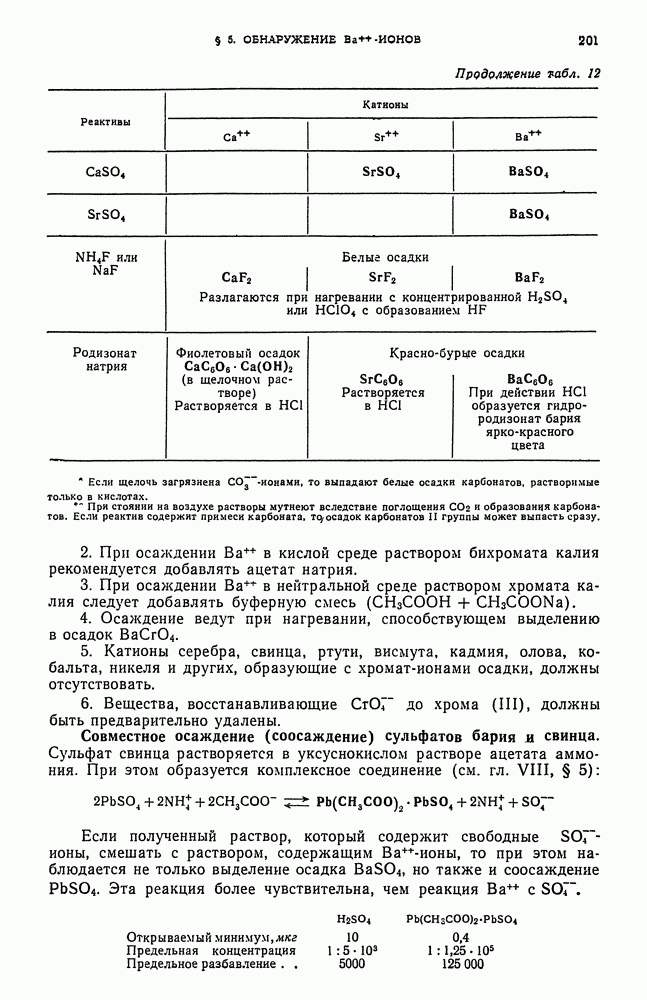
- § 5. Обнаружение Ba-ионов
- § 6. Обзор действия реактивов на катионы второй аналитической группы
- § 7. Основы теории осаждения катионов второй аналитической группы групповым реактивом—карбонатом аммония
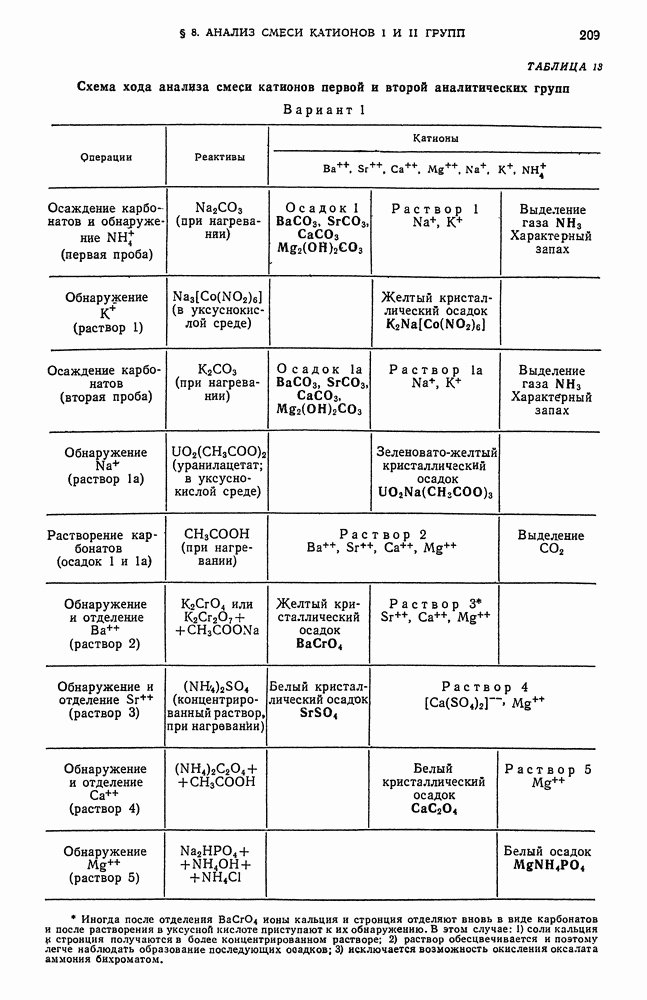
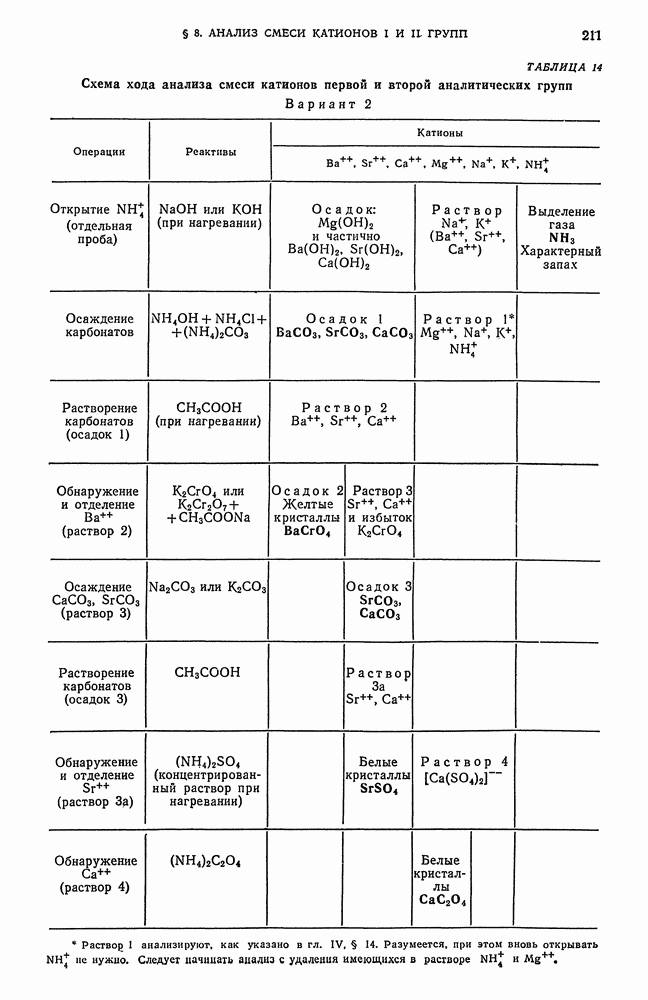
- § 8. Систематический ход анализа смеси катионов первой и второй аналитических групп
- § 9. Систематический ход анализа смеси катионов первой и второй аналитических групп в присутствии ионов
- § 10. Теоретические основы перевода сульфатов катионов второй аналитической группы в карбонаты
- ГЛАВА VI. ТРЕТЬЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика третьей аналитической группы катионов
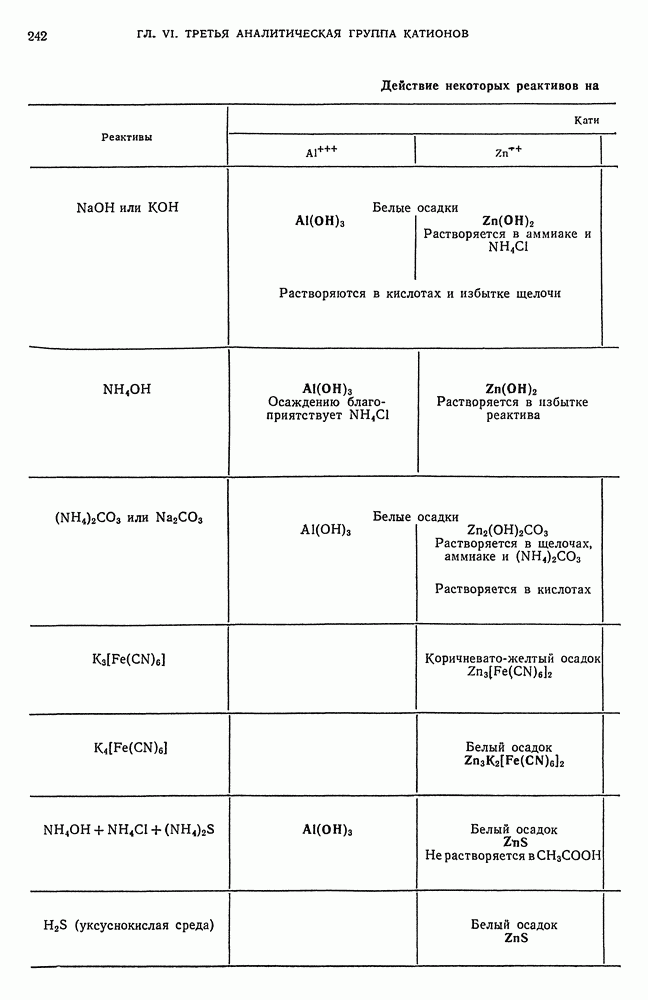
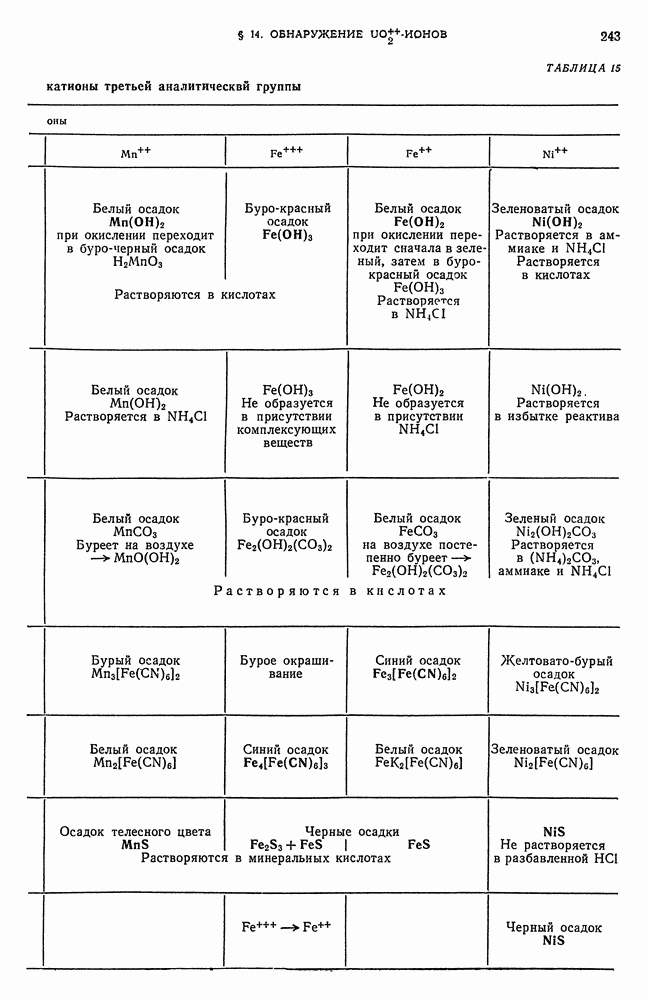
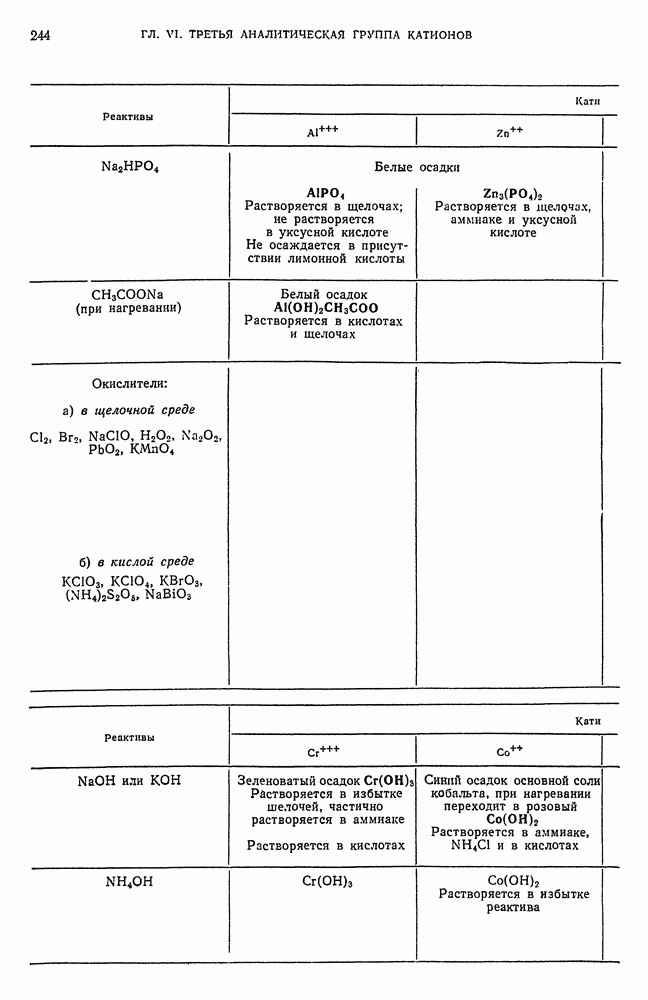
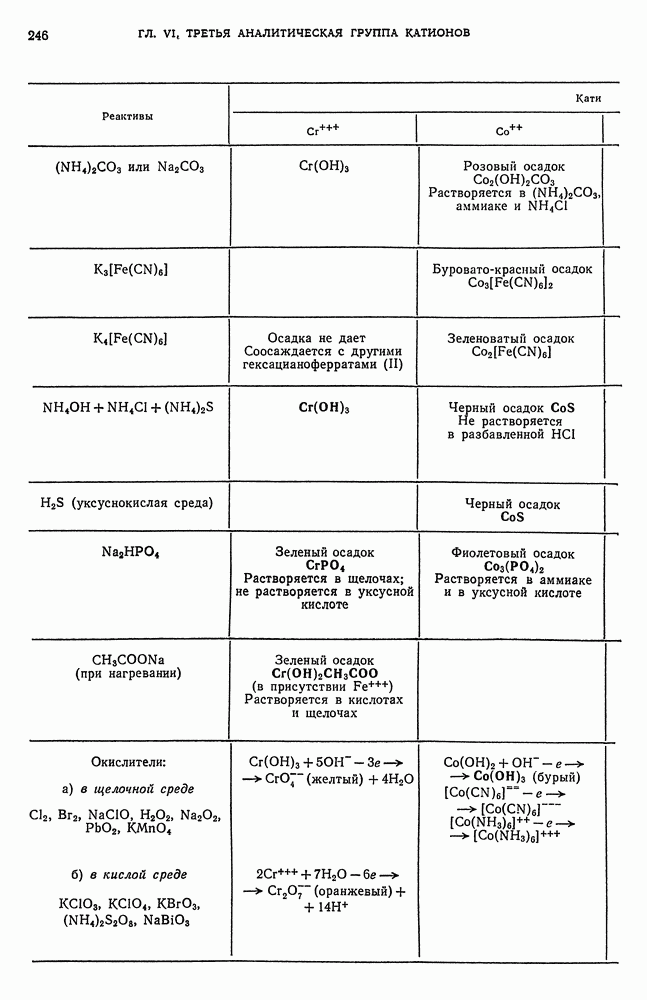
- § 2. Общие реакции катионов третьей аналитической группы
- § 3. Обнаружение Be-ионов
- § 4. Обнаружение Al-ионов
- § 5. Обнаружение ионов титана (IV)
- § 6. Обнаружение Cr-ионов
- § 7. Обнаружение Mn-ионов
- § 8. Обнаружение Fe-ионов
- § 9. Обнаружение Fe-ионов
- § 10. Обнаружение Co-ионов
- § 13. Обнаружение ионов циркония (IV)
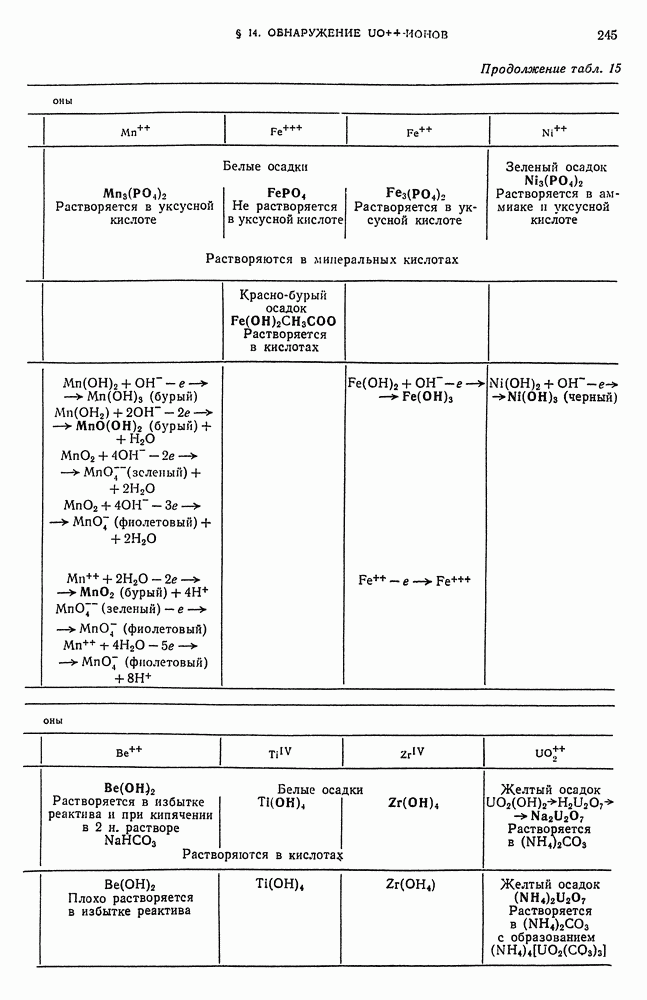
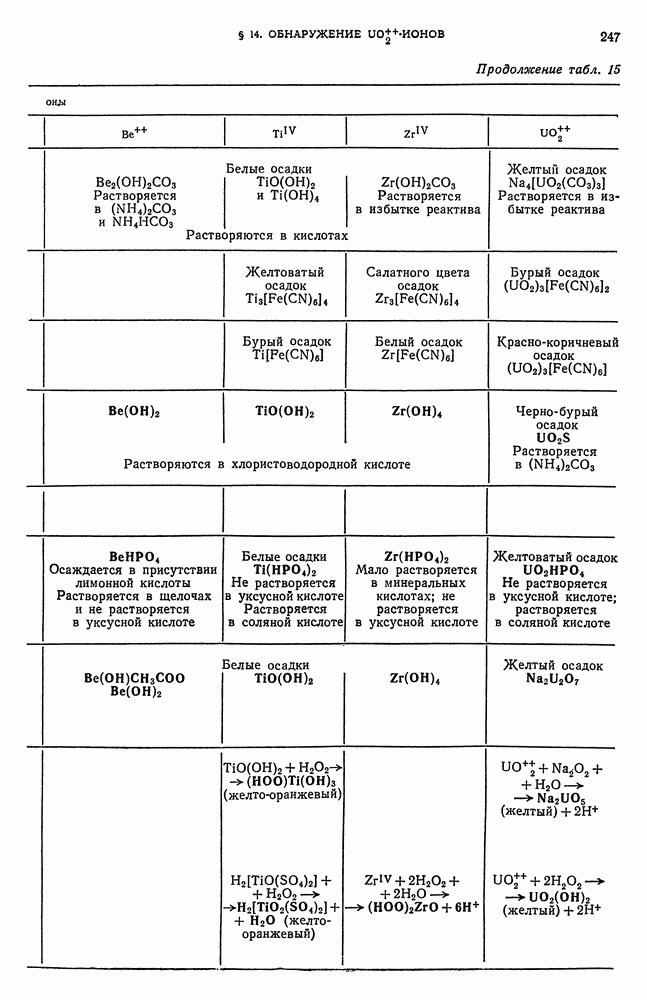
- § 14. Обнаружение UO-ионов
- § 15. Обзор действия реактивов на катионы третьей аналитической группы
- § 16. Использование коллоидных систем в химическом анализе
- § 17. Основы теории осаждения катионов третьей аналитической группы групповым реактивом — сульфидом аммония
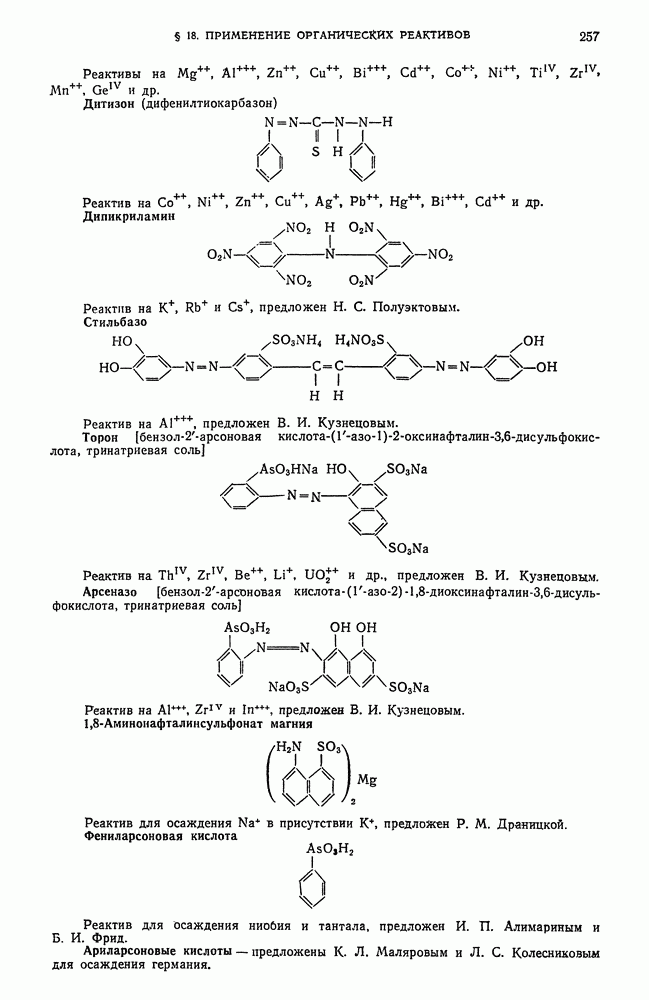
- § 18. Теоретические основы применения органических реактивов в качественном анализе неорганических веществ
- § 19. Методы разделения некоторых катионов третьей аналитической группы
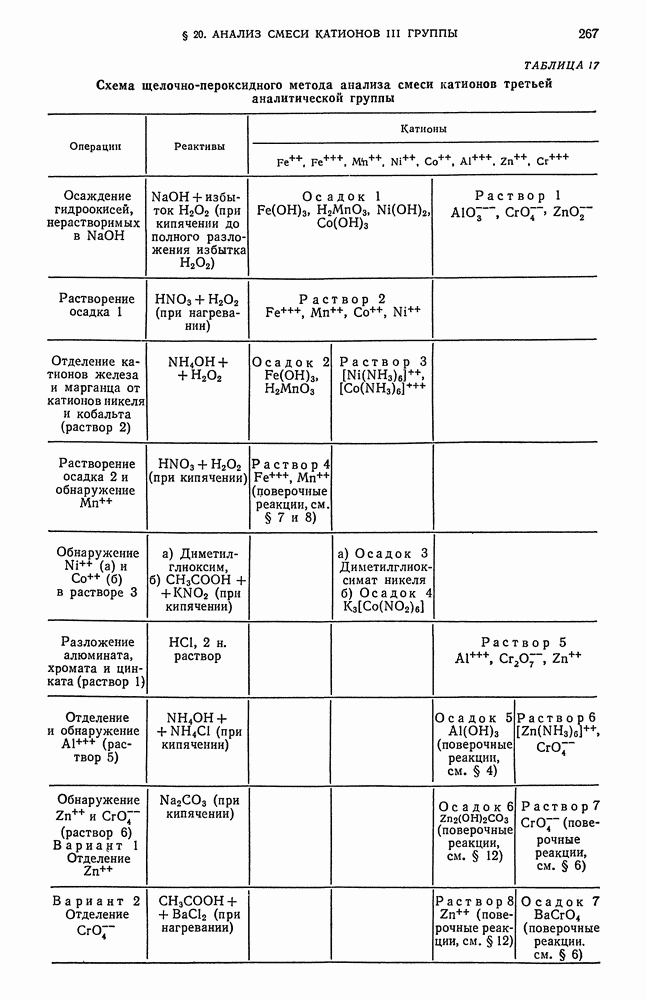
- § 20. Систематический ход анализа смеси катионов третьей аналитической группы
- § 21. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп
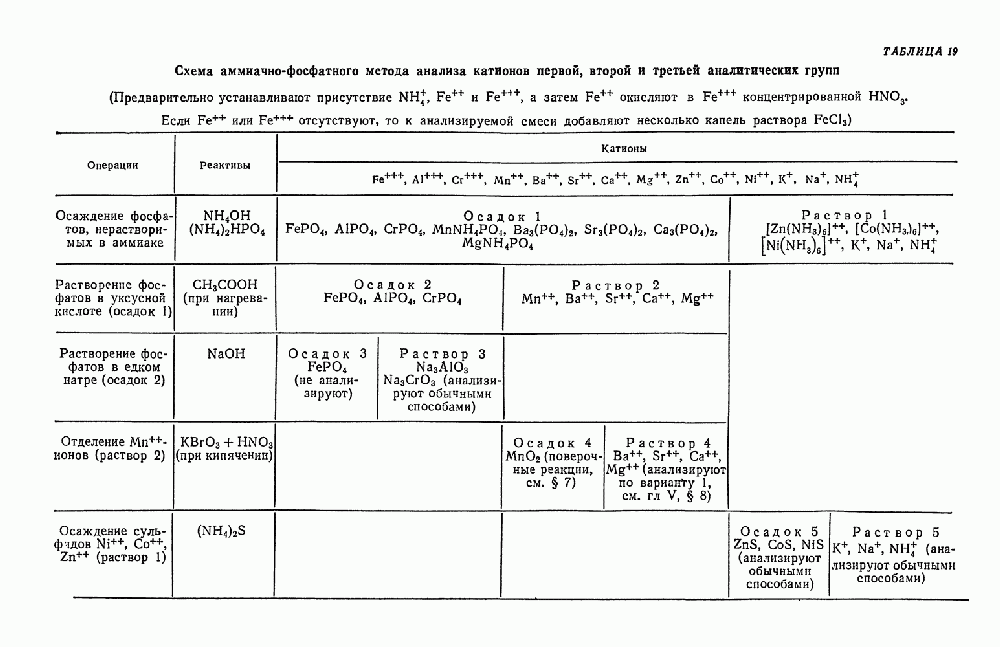
- § 22. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп в присутствии PO-ионов
- ГЛАВА VII. ЧЕТВЕРТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика четвертой аналитической группы катионов
- § 2. Общие реакции катионов четвертой аналитической группы
- РЕАКЦИИ КАТИОНОВ ПЕРВОЙ ПОДГРУППЫ (ПОДГРУППЫ МЕДИ)
- § 3. Обнаружение Hg-ионов
- § 4. Обнаружение Cu-ионов
- § 5. Обнаружение Cd-ионов
- § 6. Обнаружение Bi-ионов
- РЕАКЦИИ КАТИОНОВ ВТОРОЙ ПОДГРУППЫ (ПОДГРУППЫ МЫШЬЯКА)
- § 7. Обнаружение ионов мышьяка (III)
- § 8. Обнаружение ионов мышьяка (V)
- § 9. Общие реакции обнаружения
- § 10. Обнаружение ионов сурьмы (III)
- § 11. Обнаружение ионов сурьмы (V)
- § 12. Общие реакции обнаружения Sb
- § 13. Обнаружение ионов олова (II)
- § 14. Обнаружение ионов олова (IV)
- § 15. Общие реакции обнаружения ионов олова (II) и олова (IV)
- § 16. Отделение ионов олова от других ирнов четвертой аналитической группы
- § 17. Обнаружение ионов германия (IV)
- § 18. Отделение ионов германия от других ионов четвертой аналитической группы
- § 19. Обзор действия реактивов на катионы четвертой аналитической группы
- § 20. Основы теории осаждения сульфидов катионов четвертой аналитической группы групповым реактивом — сероводородом
- § 21. Систематический ход анализа смеси катионов четвертой аналитической группы
- ГЛАВА VIII. ПЯТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ (ГРУППА СЕРЕБРА)
- § 1. Характеристика пятой аналитической группы катионов
- § 2. Общие реакции катионов пятой аналитической группы
- § 3. Обнаружение Ag-ионов
- § 4. Обнаружение [Hg]-ионов
- § 5. Обнаружение Pb-ионов
- § 6. Обзор действия реактивов на катионы пятой аналитической группы
- § 7. Систематический ход анализа смеси катионов пятой аналитической группы
- ГЛАВА IX. АНАЛИЗ СМЕСИ ИОНОВ ВСЕХ ПЯТИ АНАЛИТИЧЕСКИХ ГРУПП
- § 1. Сероводородный метод анализа
- § 2. Недостатки сероводородного метода анализа
- § 3. Ошибки, возникающие при анализе смеси ионов пяти аналитических групп
- § 4. Бессероводородные методы анализа
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ АНИОНОВ И АНАЛИЗ СМЕСЕЙ АНИОНОВ
- § 1. Аналитическая классификация анионов
- § 2. Групповые реактивы на анионы
- § 3. Классификация методов анализа анионов
- ГЛАВА XI. ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика первой группы анионов
- § 2. Реакции анионов первой группы
- § 3. Обнаружение CI-ионов
- § 4. Обнаружение Br-ионов
- § 5. Обнаружение I-ионов
- § 6. Обнаружение CN-ионов
- § 7. Обнаружение SCN-ионов
- § 8. Обнаружение [Fe(CN)]-ионов
- § 9. Обнаружение Fe(CN)-ионов
- § 10. Обнаружение NO-ионов
- § 11. Обнаружение NO2-ионов
- § 12. Обнаружение S-ионов
- § 13. Обнаружение CH3COOO-ионов
- § 14. Обнаружение BrO3-ионов
- § 15. Обнаружение ClO3-ионов
- § 16. Обнаружение ClO4-ионов
- § 17. Обзор действия реактивов на анионы первой группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 18. Анализ смеси Cl, Br и I-ионов
- § 19. Анализ смеси Cl, Br, I и SCN-ионов
- § 20. Анализ смеси Cl, ClO3 и ClO4-ионов
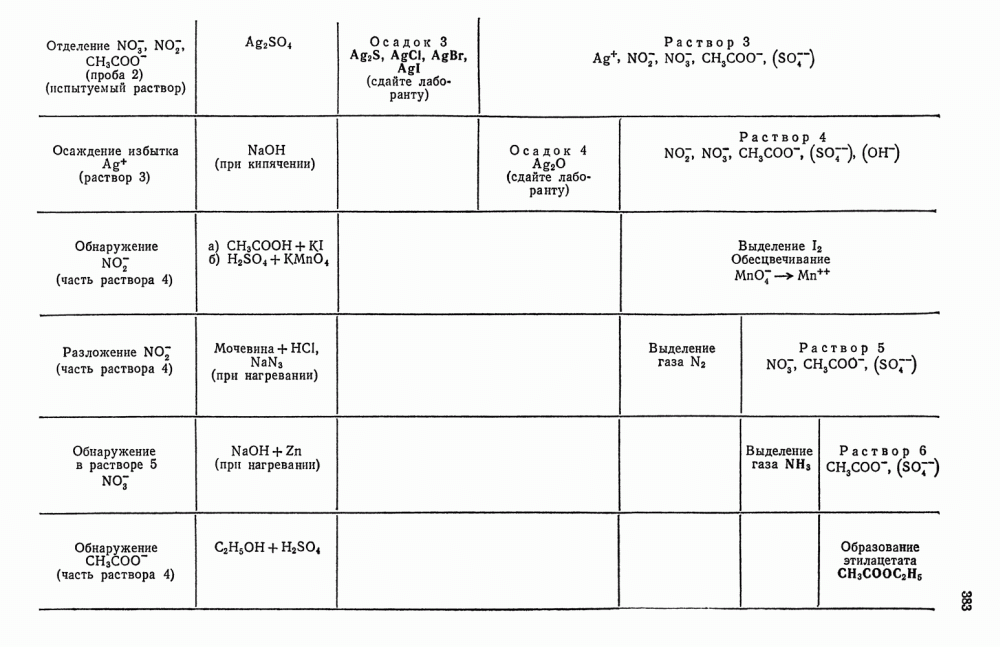
- § 21. Анализ смеси NO2 и NO3-ионов
- § 22. Анализ смеси анионов первой группы
- ГЛАВА XII. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика второй группы анионов
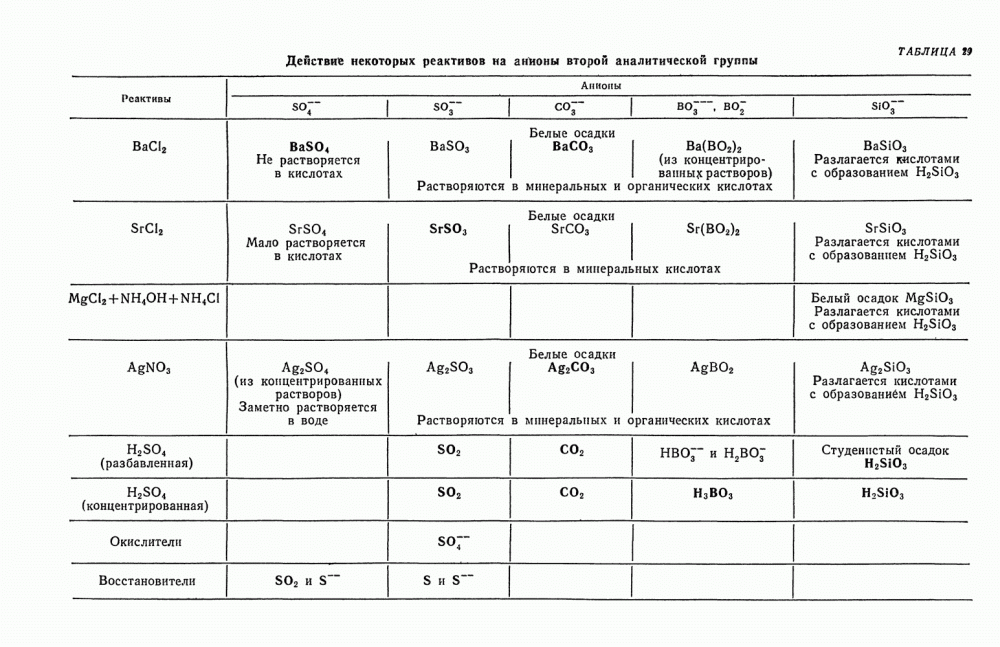
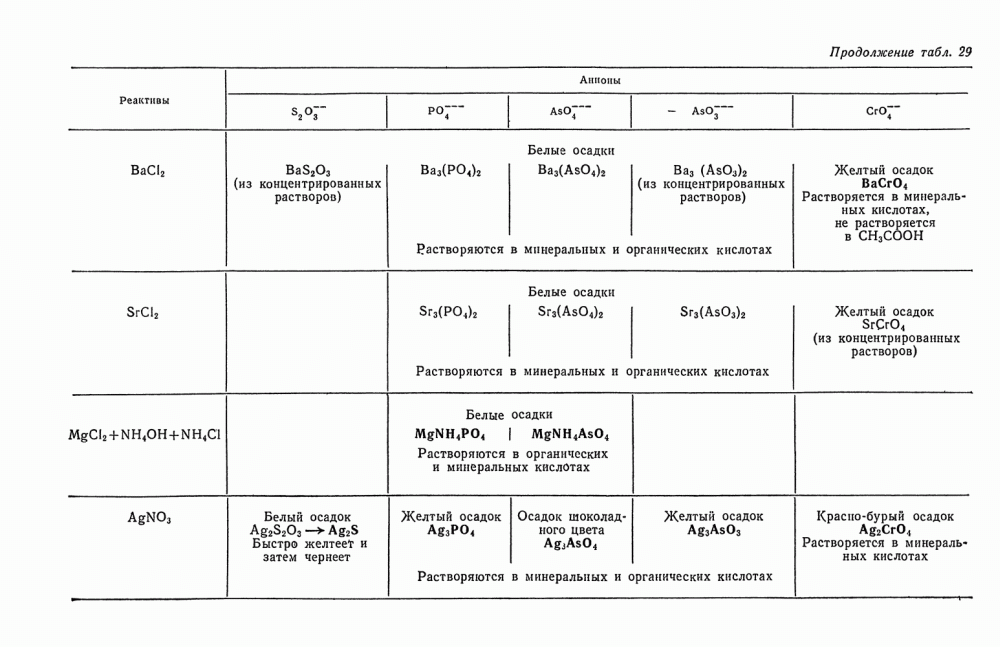
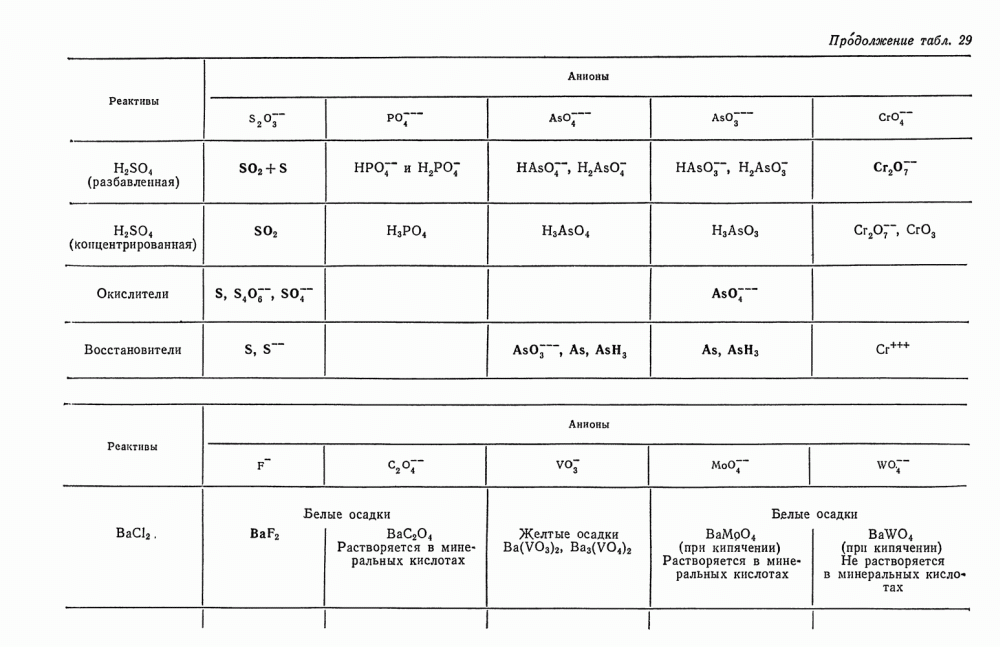
- § 2. Общие реакции анионов второй группы
- § 3. Обнаружение SO3-ионов
- § 4. Обнаружение S2O3-ионов
- § 5. Обнаружение S2O3 в присутствии SO3-ионов
- § 6. Обнаружение SO4-ионов
- § 7. Обнаружение CO3-ионов
- § 8. Обнаружение CO3-ионов в присутствии SO3 и S2O3-ионов
- § 9. Обнаружение PO4-ионов
- § 10. Обнаружение CrO4-ионов
- § 11. Обнаружение AsO3-ионов
- § 12. Обнаружение AsO4-ионов
- § 13. Обнаружение BO2 и BO3-ионов
- § 14. Обнаружение SiO3-ионов
- § 15. Обнаружение F-ионов
- § 16. Обнаружение C2O4-ионов
- § 17. Обнаружение VO3-ионов
- § 18. Обнаружение MoO4-ионов
- § 19. Обнаружение WO4-ионов
- § 20. Обзор действия реактивов на анионы второй группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 21. Анализ смеси ионов
- § 22. Анализ смеси SO3, SO4, S2O3 и CO3-ионов
- § 23. Анализ смеси VO2, MoO4 и WO4-ионов
- § 24. Анализ смеси анионов второй группы
- § 25. Анализ смеси анионов первой и второй групп
- ГЛАВА XIII. ОБНАРУЖЕНИЕ СВОБОДНЫХ МЕТАЛЛОВ И НЕМЕТАЛЛОВ, ИДЕНТИФИЦИРОВАНИЕ СОЛЕЙ И ДРУГИХ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И АНАЛИЗ ИХ СМЕСЕЙ
- § 1. Подготовка вещества к анализу
- § 2. Предварительные испытания
- § 3. Растворение анализируемого вещества в воде, кислотах и щелочах
- § 4. Переведение в растворимое состояние веществ, нерастворимых в воде, кислотах и щелочах
- § 5. Анализ неизвестного вещества
- § 6. Обнаружение свободных элементов
- § 7. Идентифицирование солей и других индивидуальных соединений
- § 8. Обнаружение микропримесей
- § 9. Анализ сплавов
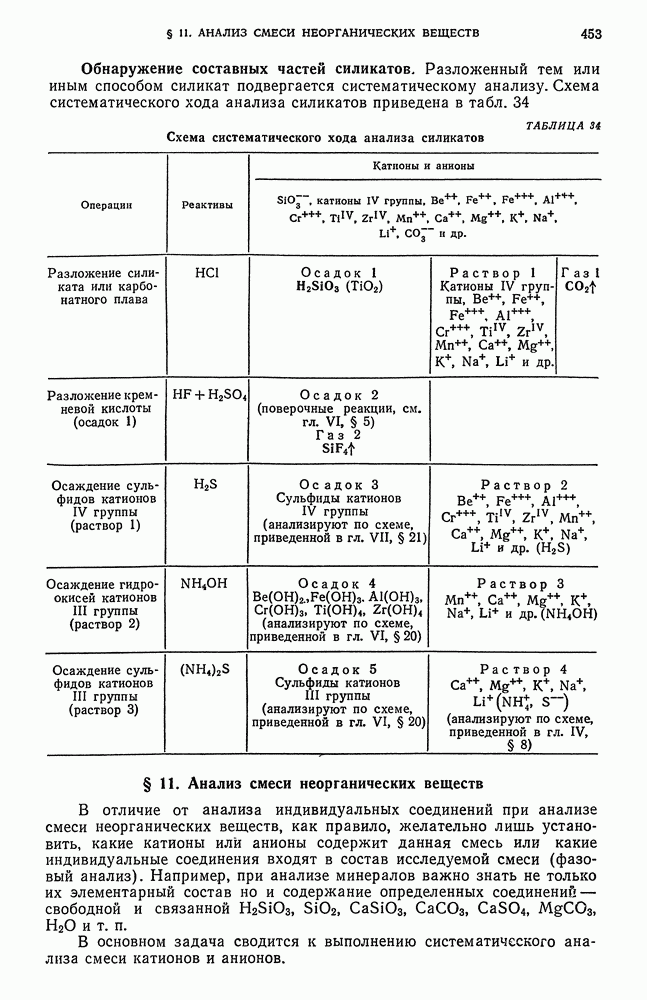
- § 10. Анализ силикатов и алюмосиликатов
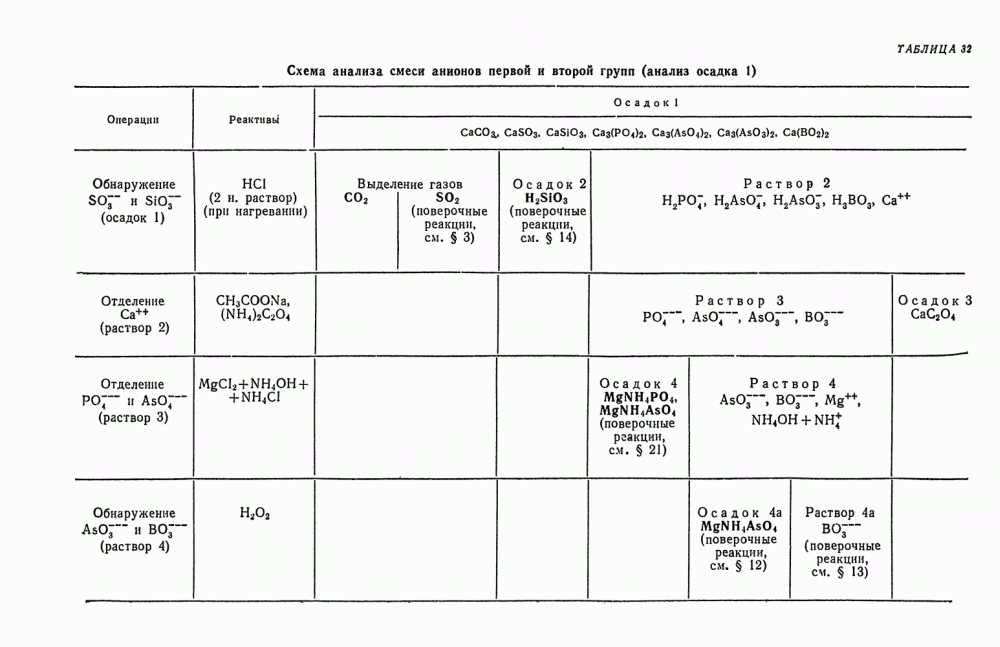
- § 11. Анализ смеси неорганических веществ
- § 12. Экспрессный метод анализа смесей катионов и анионов
- § 13. Идентифицирование нерастворимых веществ
- ЛИТЕРАТУРА