| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 7. Идентифицирование солей и других индивидуальных соединений
АНАЛИЗ ТВЕРДОГО ВЕЩЕСТВА
Перед систематическим исследованием данного соединения изучают под микроскопом его кристаллическую форму (если оно кристаллическое), отмечают его цвет, запах, отношение к нагреванию, прокаливанию, к воде, кислотам, щелочам и пр. (см. § 1). Далее приступают к систематическому ходу анализа.
Пример  . Дано кристаллическое слегка зеленоватое вещество [допустим,
. Дано кристаллическое слегка зеленоватое вещество [допустим,  ]. Требуется определить, какие элементы входят в состав исследуемого вещества.
]. Требуется определить, какие элементы входят в состав исследуемого вещества.
По внешнему виду вещества можно предположить, что в его состав не входят интенсивно окрашенные ионы [хромат, бйхромат, манганат, перманганат, гексанитрокобальтат (III), ионы кобальта и  .
.
Предварительные иодотания. 1. Окрашивание пламени. Испытуемое вещество не дает характерного окрашивания бесцветного пламени горелки. Следовательно, исключается содержание солей калия, кальция, стронция, бария, меди, свинца, сурьмы, мышьяка, бора и некоторых других соединений.
2. Нагревание в калильной трубке. При нагревании в калильной трубке вещество частично возгоняется, пахнет  кроме того, выделяются капельки воды. Следовательно, при нагревании испытуемое вещество разлагается с образованием как летучих, так и нелетучих продуктов, т. е. оно может быть солью аммония или ртути, в его состав могут входить мышьяк и сурьма. Выделение паров воды указывает на содержание в исходном веществе кристаллизационной воды. Однако нужно помнить, что вода выделяется также при нагреванин органических соединений, гидроокисей, основных и кислых солей.
кроме того, выделяются капельки воды. Следовательно, при нагревании испытуемое вещество разлагается с образованием как летучих, так и нелетучих продуктов, т. е. оно может быть солью аммония или ртути, в его состав могут входить мышьяк и сурьма. Выделение паров воды указывает на содержание в исходном веществе кристаллизационной воды. Однако нужно помнить, что вода выделяется также при нагреванин органических соединений, гидроокисей, основных и кислых солей.
3. Получение окрашенных перлов. Перл буры окрашивается исследуемым веществом в окислительном пламени в буровато-желтый цвет, а в восстановительном — в зеленый цвет. Отсюда можно заключить, что исследуемое вещество содержит соединения железа.
4. Действие разбавленной серной кислоты. При действии разбавленной серной кислоты каких-либо изменений не наблюдается. Следовательно, анализируемое вещество не является карбонатом, сульфитом, тиосульфатом, не является оно также и сульфидом, цианидом, нитритом, гипохлоритом, ацетатом, перекисью, которые легко разлагаются кислотами.
5. Действие концентрированной серной кислоты. При действии концентрированной серной кислоты тоже никаких видимых изменений не наблюдается. Следовательно, анализируемое вещество не представляет собой хлорида, бромида, иодида, фторида, роданида, оксалата, хлората, нитрата и т. п.
6. Растворение вещества. В данном случае испытуемое соединение растворимо в воде. Следовательно, оно не относится к числу нерастворимых в воде фосфатов, арсенитов, силикатов, оксалатов, карбонатов, гидроокисей, сульфидов (за исключением соответствующих солей щелочных и щелочноземельных металлов и аммония), хлоридов V группы, сульфатов бария, стронция, кальция, свинца и закиснои ртути, цианидов, образованных катионами III и IV аналитических групп [кроме цианида ртути (II)] и т. д.
7. Определение  раствора. Вещество растворяют в воде и определяют
раствора. Вещество растворяют в воде и определяют  среды. Если среда кислая, то анализируемое вещество может представлять собой кислоту или соль слабого основания и сильной кислоты. Если среда щелочная, то оно может быть основанием, основным окислом или солью сильного основания и слабой кислоты.
среды. Если среда кислая, то анализируемое вещество может представлять собой кислоту или соль слабого основания и сильной кислоты. Если среда щелочная, то оно может быть основанием, основным окислом или солью сильного основания и слабой кислоты.
Водный раствор взятого для исследования соединения имеет кислую реакцию — вещество может быть или свободной кислотой, или кислотным окислом, или солью, образованной катионами слабых оснований и анионами сильных кислот.
8. Обнаружение окислителей и восстановителей. В отдельной пробе проводят реакции на присутствие окислителей с помощью  . Иод не выделяется, что свидетельствует об отсутствии окислителей.
. Иод не выделяется, что свидетельствует об отсутствии окислителей.
В других пробах проводят реакции на присутствие восстановителей  перманганат калия обесцвечивается — имеются восстановители.
перманганат калия обесцвечивается — имеются восстановители.
Систематический ход анализа. 1. Обнаружение катионов:
а) Обнаруживают  , нагревая небольшое количество исследуемого раствора с едким натром; выделяющийся аммиак служит доказательством того, что в испытуемом веществе имеются
, нагревая небольшое количество исследуемого раствора с едким натром; выделяющийся аммиак служит доказательством того, что в испытуемом веществе имеются  .
.
б) В отдельной пробе обнаруживают железо (III) при помощи  осадок не образуется, следовательно ионы
осадок не образуется, следовательно ионы  отсутствуют.
отсутствуют.
в) В отдельной пробе делают реакцию на железо (II)  помощи
помощи  по образующемуся осадку турнбулевой сини можно заключить, что в растворе содерокится
по образующемуся осадку турнбулевой сини можно заключить, что в растворе содерокится  .
.
г) Осаждают хлористоводородной кислотой хлориды V группы. Осадок не образуется, значит отсутствуют  .
.
д) Пропускают в кислый раствор сероводород; осадок не образуется, это указывает на отсутствие ионов IV аналитической группы.
е) Действуют на раствор сульфидом аммония. При этом выпадает черный осадок (очевидно,  ); осадок отфильтровывают и исследуют, проверяя на
); осадок отфильтровывают и исследуют, проверяя на  .
.
ж) К фильтрату после отделения  и разрушения избытка
и разрушения избытка  приливают раствор карбоната аммония; осадок не образуется, что свидетельствует
приливают раствор карбоната аммония; осадок не образуется, что свидетельствует  отсутствии ионов бария, стронция и кальция.
отсутствии ионов бария, стронция и кальция.
з) С отдельными пробами фильтрата проводят поверочные реакции на  (предварительно удалив
(предварительно удалив  ). Отрицательные результаты свидетельствуют об отсутствии этих ионов.
). Отрицательные результаты свидетельствуют об отсутствии этих ионов.
Из проведенных испытаний можно сделать вывод, что в состав анализируемого вещества входят  .
.
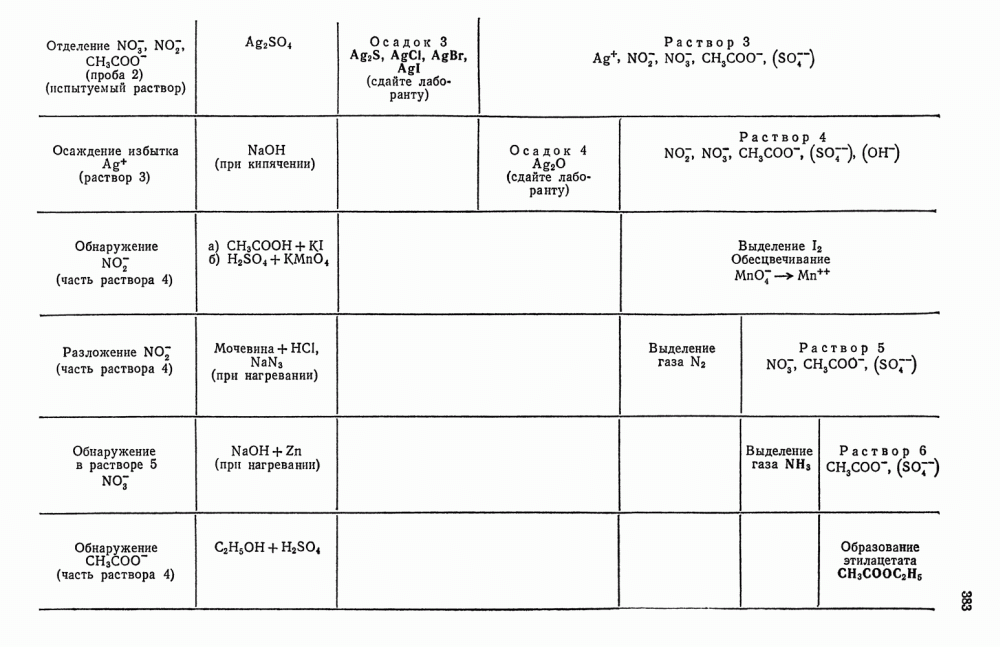
2. Обнаружение анионов. Затем приступают к открытию анионов.
а) На анализируемый раствор действуют нитратом бария; выпадает нерастворимый в кислотах осадок, следовательно в растворе имеется  .
.
б) На анализируемый раствор действуют раствором  . Осадок не образуется; анионов, осаждаемых в виде
. Осадок не образуется; анионов, осаждаемых в виде  солей, нет.
солей, нет.
Из проведенных опытов делают вывод, что в состав анализируемого вещества входят  и кристаллизационная вода.
и кристаллизационная вода.
И действительно,  кристаллическое, слегка зеленоватое вещество, растворимое в воде, не обладает запахом, не окрашивает бесцветного пламени горелки, частично возгоняется с выделением воды. Водный раствор данной соли имеет кислую реакцию, а при действии едкого натра выделяется аммиак и выпадает
кристаллическое, слегка зеленоватое вещество, растворимое в воде, не обладает запахом, не окрашивает бесцветного пламени горелки, частично возгоняется с выделением воды. Водный раствор данной соли имеет кислую реакцию, а при действии едкого натра выделяется аммиак и выпадает  с гексацнаноферратом (III) калия образует турнбулеву синь, с нитратом бария — нерастворимый в кислотах осадок
с гексацнаноферратом (III) калия образует турнбулеву синь, с нитратом бария — нерастворимый в кислотах осадок  оно не реагирует с нитратом серебра, иодидом калия и кислотами, обесцвечивает раствор перманганата и т. д.
оно не реагирует с нитратом серебра, иодидом калия и кислотами, обесцвечивает раствор перманганата и т. д.
Пример 2. Пусть для анализа дано неизвестное твердое вещество черного цвета. Требуется определить его состав.
Внешний вид испытуемого соединения: твердое вещество не имеет определенной кристаллической структуры; цвет вещества черный. Запах отсутствует.
По черному цвету вещества можно предположить, что оно представляет собой какой-либо сульфид ( и др.), окись или гидроокись трехвалентных кобальта, никеля, четырехвалентного марганца
и др.), окись или гидроокись трехвалентных кобальта, никеля, четырехвалентного марганца  или одно из следующих соединений:
или одно из следующих соединений:  и др.
и др.
Предварительные испытания. Соединение не окрашивает бесцветного пламени горелки в характерный цвет; при нагревании в калильной трубке выделяется вода; перл буры в окислительном пламени окрашивается в красно-бурый цвет, в восстановительном — в фиолетово-серый.
По-видимому, вещество не содержит солей, окрашивающих пламя в характерные цвета. Выделяющаяся при нагревании вода указывает на то, что в испытуемом веществе может содержаться кристаллизационная вода, органические соединения, гидроокиси, основные или кислые соли. По окрашиванию перла буры можно заключить о присутствии соединений никеля.
Испытуемое вещество не растворяется  воде и в разбавленной хлористоводородной кислоте, но растворяется в концентрированной хлористоводородной кислоте с выделением газообразного хлора. Получающийся раствор окрашен в зеленый цвет. При действии разбавленной серной кислоты никаких видимых изменений не наблюдается. В концентрированной серной кислбте исследуемое вещество растворяется, выделяя кислород. Полученный раствор окрашен в зеленый цвет.
воде и в разбавленной хлористоводородной кислоте, но растворяется в концентрированной хлористоводородной кислоте с выделением газообразного хлора. Получающийся раствор окрашен в зеленый цвет. При действии разбавленной серной кислоты никаких видимых изменений не наблюдается. В концентрированной серной кислбте исследуемое вещество растворяется, выделяя кислород. Полученный раствор окрашен в зеленый цвет.
По цвету раствора можно предположить, что анализируемое вещество содержит соединения  , меди или хрома (III). По выделению хлора можно заключить, что испытуемое вещество является окислителем, окисляющим
, меди или хрома (III). По выделению хлора можно заключить, что испытуемое вещество является окислителем, окисляющим  -ионы до элементарного хлора.
-ионы до элементарного хлора.
Выделяющийся при действии концентрированной серной кислоты кислород указывает на присутствие перекисей, окисей, гидроокисей, или кислородсодержащих солей высоко в аленшых элементов.
Систематический ход анализа. 1. Обнаружение катионов, а) Можно сделать вывод, что испытуемое вещество не содержит катионов V группы, так как при обработке его хлористоводородной кислотой осадок не образуется. Часть полученного солянокислого раствора разбавляют водой и наблюдают возможное образование осадка (разрушение комплексных соединений).
Отсутствие осадка служит окончательным доказательством того, что в испытуемом веществе нет катионов группы серебра (за исключением ионов свинца, которые все же могут остаться в растворе).
б) При действии на кислый раствор сероводородом осадок не образуется. Следовательно, отсутствуют катионы IV и V аналитических групп.
в) Кислый раствор, насыщенный сероводородом, подщелачивают гидроокисью аммония; при этом выпадает черный осадок. Следовательно, в растворе есть катионы III аналитической группы. Сульфиды и гидроокиси катионов III группы осаждают раствором  . Полученный осадок отделяют и анализируют (см. гл. VI, § 20). В результате анализа устанавливают присутствие ионов никеля.
. Полученный осадок отделяют и анализируют (см. гл. VI, § 20). В результате анализа устанавливают присутствие ионов никеля.
2. Обнаружение анионов. Оставшуюся от анализа катионов часть хлористоводородного раствора кипятят с  . Никель выпадает в осадок и его отделяют фильтрованием. Фильтрат нейтрализуют, и приготовленный таким образом раствор используют для обнаружения анионов.
. Никель выпадает в осадок и его отделяют фильтрованием. Фильтрат нейтрализуют, и приготовленный таким образом раствор используют для обнаружения анионов.
Сравнивая результаты исследований, приходят к выводу, что в растворе, кроме  , других анионов нет. Однако эти анионы были введены в раствор с хлористоводородной кислотой. Поэтому необходимо проверить, действительно ли исходное вещество содержит хлор-ионы. Для этого на испытуемое вещество действуют смесью растворов
, других анионов нет. Однако эти анионы были введены в раствор с хлористоводородной кислотой. Поэтому необходимо проверить, действительно ли исходное вещество содержит хлор-ионы. Для этого на испытуемое вещество действуют смесью растворов  (см. гл. XI, § 3) и по результатам анализа приходят к выводу, что испытуемое вещество не содержит
(см. гл. XI, § 3) и по результатам анализа приходят к выводу, что испытуемое вещество не содержит  .
.
Следовательно, анализируемый продукт представляет собой окись или гидроокись никеля. Гидроокись и окись никеля (II) растворимы в разбавленной хлористоводородной кислоте, но окрашены они не в черный, а в зеленый цвет.
На основании этого делают заключение, что исследуемый продукт представляет собой окись или гидроокись трехвалентного никеля. Действительно,  нерастворимы в разбавленной хлористоводородной кислоте и по окраске подходят к цвету данного анализируемого вещества. Весьма существенным доказательством такого заключения является тот факт, что окись и гидроокись никеля (III) действительно окисляют ионы хлора с образованием газообразного хлора и растворяются в концентрированной
нерастворимы в разбавленной хлористоводородной кислоте и по окраске подходят к цвету данного анализируемого вещества. Весьма существенным доказательством такого заключения является тот факт, что окись и гидроокись никеля (III) действительно окисляют ионы хлора с образованием газообразного хлора и растворяются в концентрированной  , выделяя кислород:
, выделяя кислород:

Образование на стенках калильной пробирки капелек воды убеждает аналитика в том, что испытуемое соединение представляет собой  .
.
АНАЛИЗ РАСТВОРА ИНДИВИДУАЛЬНОГО ВЕЩЕСТВА
Анализ раствора индивидуального вещества проще, чем анализ твердого вещества, так как отпадает операция перевода исследуемого соединения в раствор.
Например, дан раствор индивидуального вещества зеленого цвета. Требуется определить состав растворенного вещества.
По внешнему виду раствора можно предположить, что в состав исследуемого  входят окрашенные ионы
входят окрашенные ионы  .
.
Предварительные испытания. 1. Окрашивание пламени. Испытуемое вещество окрашивает бесцветное пламя горелки в фиолетовый цвет. Следовательно, можно предположить наличие в растворе ионов калия.
2. Получение окрашенных перлов. Перл буры окрашивается исследуемым веществом в зеленый цвет. Следовательно, возможно присутствие ионов хрома, меди, молибдена, ванадия, урана.
3. Определение  раствора. Допустим, что
раствора. Допустим, что  среды равен 13. Следовательно, среда сильнощелочная. При этом выделения
среды равен 13. Следовательно, среда сильнощелочная. При этом выделения  не наблюдается. В щелочном растворе должны отсутствовать катионы, образующие окиси и гидроокиси (
не наблюдается. В щелочном растворе должны отсутствовать катионы, образующие окиси и гидроокиси ( и т. п.). Возможно, присутствуют катионы, не образующие малорастворимых окисей и гидроокисей в щелочном растворе (
и т. п.). Возможно, присутствуют катионы, не образующие малорастворимых окисей и гидроокисей в щелочном растворе ( и др.), а также катионы, гидроокиси которых растворимы в избытке щелочи
и др.), а также катионы, гидроокиси которых растворимы в избытке щелочи  .
.
Систематический анализ. Обнаружение катионов. Обычно анализ катионов начинают с обнаружения  . В данном случае эти испытания следует опустить, так как среда исследуемого раствора сильнощелочная, раствор не пахнет аммиаком и не содержит осадка.
. В данном случае эти испытания следует опустить, так как среда исследуемого раствора сильнощелочная, раствор не пахнет аммиаком и не содержит осадка.
В присутствии  в сильнощелочной среде наблюдалось бы выделение аммиака, в присутствии
в сильнощелочной среде наблюдалось бы выделение аммиака, в присутствии  в щелочной среде был бы осадок. Следовательно, этих катионов в растворе исследуемого вещества нет.
в щелочной среде был бы осадок. Следовательно, этих катионов в растворе исследуемого вещества нет.
1. Поэтому в данном случае, приступая к анализу катионов, к небольшой пробе испытуемого раствора по каплям добавляют хлористоводородную кислоту для осаждения хлоридов группы серебра (катионов V группы). При осторожном подкислении раствора появляется муть, исчезающая при добавлении  . Следовательно, в анализируемом растворе содержатся катионы, образующие растворимые в избытке щелочи гидроокиси или разрушаемые кислотой комплексные соединения. По-видимому, отсутствуют катионы группы серебра, осаждаемые
. Следовательно, в анализируемом растворе содержатся катионы, образующие растворимые в избытке щелочи гидроокиси или разрушаемые кислотой комплексные соединения. По-видимому, отсутствуют катионы группы серебра, осаждаемые  в виде хлоридов, тиосоли, и растворимые силикаты, разлагающиеся кислотой с образованием осадков тиоангидридов и кремневой кислоты.
в виде хлоридов, тиосоли, и растворимые силикаты, разлагающиеся кислотой с образованием осадков тиоангидридов и кремневой кислоты.
2. В кислый раствор пропускают сероводород. Осадок не образуется, это указывает на отсутствие ионов IV и V аналитических групп.
3. Нейтрализуют кислый раствор аммиаком и приливают раствор  . При этом выпадает серо-зеленый осадок. Осадок отфильтровывают и исследуют, находят ионы хрома (III).
. При этом выпадает серо-зеленый осадок. Осадок отфильтровывают и исследуют, находят ионы хрома (III).
4. Фильтрат подкисляют и кипятят для удаления  . К свободному от
. К свободному от  раствору приливают смесь растворов
раствору приливают смесь растворов  . Осадок не образуется, что свидетельствует об отсутствии
. Осадок не образуется, что свидетельствует об отсутствии  в растворе.
в растворе.
5. С отдельными пробами фильтрата проводят поверочные реакции на катионы щелочных металлов. Находят ионы калия.
Обнаружение анионов. 1. При действии разбавленной и концентрированной серной кислоты видимых изменений не наблюдается.
2. Нейтрализуют раствор и приливают к нему раствор  . Осадка нет. Следовательно, нет анионов осаждаемых
. Осадка нет. Следовательно, нет анионов осаждаемых  .
.
3. Подкисляют исходный раствор азотной кислотой и добавляют раствор  . Осадка нет. При нейтрализации раствора осадок также
. Осадка нет. При нейтрализации раствора осадок также  образуется. Следовательно, отсутствуют анионы, осаждаемые
образуется. Следовательно, отсутствуют анионы, осаждаемые  .
.
4. Подкисляют отдельную пробу  и прибавляют раствор
и прибавляют раствор  . Иод не выделяется. Следовательно, в растворе нет окислителей.
. Иод не выделяется. Следовательно, в растворе нет окислителей.
5. Другую пробу подкисляют  , добавляют несколько капель раствора
, добавляют несколько капель раствора  и нагревают. Окраска раствора
и нагревают. Окраска раствора  исчезает, что указывает на присутствие восстановителя.
исчезает, что указывает на присутствие восстановителя.
При этом раствор также окрашивается в оранжевый цвет, что свидетельствует о наличии  окисляющегося до
окисляющегося до 
6. Проделывают частные реакции на анионы, неосаждаемые  . Реакции отрицательны.
. Реакции отрицательны.
Из проведенных опытов делают вывод, что в состав анализируемого вещества входят  . По-видимому, в исследуемом растворе находится хромит калия
. По-видимому, в исследуемом растворе находится хромит калия  .
.
Действительно,  растворимое в воде вещество зеленого цвета. Водный раствор
растворимое в воде вещество зеленого цвета. Водный раствор  имеет сильнощелочную реакцию. Калиевые соли
имеет сильнощелочную реакцию. Калиевые соли  бесцветное пламя горелки в фиолетовый цвет. Соединения хрома окрашивают перл буры в зеленый цвет. В состав
бесцветное пламя горелки в фиолетовый цвет. Соединения хрома окрашивают перл буры в зеленый цвет. В состав  никакие анионы, кроме
никакие анионы, кроме  , не входят. Соединения хрома (III) не выделяют 12 из раствора KI и обесцвечивают раствор
, не входят. Соединения хрома (III) не выделяют 12 из раствора KI и обесцвечивают раствор  с образованием соединений хрома (VI).
с образованием соединений хрома (VI).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Анализ и синтез
- § 2. Предмет аналитической химии
- § 3. Развитие аналитической химии
- § 4. Качественный и количественный анализ
- ГЛАВА I. ПРИМЕНЕНИЕ ЗАКОНА ДЕЙСТВИЯ МАСС В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Влияние среды на состояние ионов в растворах
- § 2. Обратимые и необратимые аналитические реакции
- § 3. Направление аналитических реакций; правила обменного разложения
- § 4. Закон действия масс и следствие из него
- § 5. Границы применимости закона действия масс
- § 6. Сильные и слабые электролиты
- § 7. Активность
- § 8. Коэффициент активности и ионная сила
- Б. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ (В ГОМОГЕННЫХ СИСТЕМАХ)
- § 9. Гомогенные и гетерогенные системы
- § 10. Ионное произведение воды
- § 11. Ионы гидроксония
- § 12. Равновесие ионов в водных растворах; понятие о pH
- § 13. Равновесие в водных растворах слабых электролитов
- § 14. Влияние сильных кислот или сильных оснований на степень электролитической диссоциации слабых электролитов
- § 15. Приближенные формулы для расчета [H+] и [OH-] в водных растворах кислот и оснований
- В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
- § 16. Буферные растворы
- § 17. Применение буферных растворов в химическом анализе
- Г. РАВНОВЕСИЯ В РАСТВОРАХ ГИДРОЛИЗУЮЩИХСЯ СОЛЕЙ
- § 18. Теоретические основы гидролиза
- § 19. Механизм гидролитического расщепления
- § 20. Подавление и усиление гидролиза солей
- Д. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ТИПИЧНО АМФОТЕРНЫХ ЭЛЕКТРОЛИТОВ
- § 21. Поведение амфотерных гидроокисей в водных растворах
- § 22. Константы электролитической диссоциации амфотерных гидроокисей
- Е. РАВНОВЕСИЯ В СИСТЕМАХ: ОСАДОК-НАСЫЩЕННЫЙ РАСТВОР
- § 23. Осаждение как один из основных методов химического анализа
- § 24. Произведение растворимости
- § 25. Произведение активностей
- § 26. Вычисление растворимости электролитов в воде по величине произведения растворимости
- § 27. Влияние различных факторов на растворимость малорастворимых электролитов
- Ж. ОСНОВЫ ТЕОРИИ ОБРАЗОВАНИЯ И РАЗЛОЖЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИИ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 28. Характеристика комплексных соединений, имеющих значение в химическом анализе
- § 29. Квантовомеханические представления о строении комплексов
- § 30. Равновесия в растворах комплексных соединений
- § 31. Константы нестойкости комплексов
- § 32. Внутрикомплексные соединения
- § 33. Методы разложения и образования комплексов, применяемых в аналитической химии
- § 34. Применение метода комплексообразования в химическом анализе
- ГЛАВА II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Окисление—восстановление как один из основных методов химического анализа
- § 2. Направление реакций окисления—восстановления
- § 3. Окислительно-восстановительные потенциалы
- § 4. Зависимость между величинами окислительно-восстановительных потенциалов и условиями, в которых протекают реакции окисления—восстановления
- § 5. Вычисление окислительно-восстановительных потенциалов
- § 6. Вычисление окислительно-восстановительных потенциалов с учетом коэффициентов активности
- ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
- § 1. Обнаружение отдельных элементов
- § 2. Анализ мокрым и сухим путем
- § 3. Химические и физические методы качественного анализа
- § 4. Макро-, полумикро- и микрометоды
- § 5. Капельный анализ
- § 6. Микрокристаллоскопический анализ
- § 7. Метод растирания порошков
- § 8. Методы анализа, основанные на нагревании и сплавлении веществ
- § 9. Спектральный качественный анализ
- § 10. Хроматографический метод анализа
- § 11. Кинетические методы анализа
- Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
- § 12. Специфичность и чувствительность реакций
- § 13. Максимальная чувствительность аналитических реактивов
- § 14. Способы повышения чувствительности реакций
- § 15. Маскировка мешающих ионов
- § 16. Определение pH среды
- § 17. Регулирование pH среды в процессе аналитических определений
- В. РЕАКТИВЫ
- § 18. Понятие о химических реактивах
- § 19. Концентрация применяемых реактивов
- § 20. Техника пользования реактивами
- Г. ПОСУДА И ПРИБОРЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕННОМ АНАЛИЗЕ
- § 21. Химическая посуда
- § 22. Приборы
- Д. АНАЛИТИЧЕСКИЕ ГРУППЫ
- § 23. Дробный и систематический анализ
- § 24. Аналитическая классификация катионов
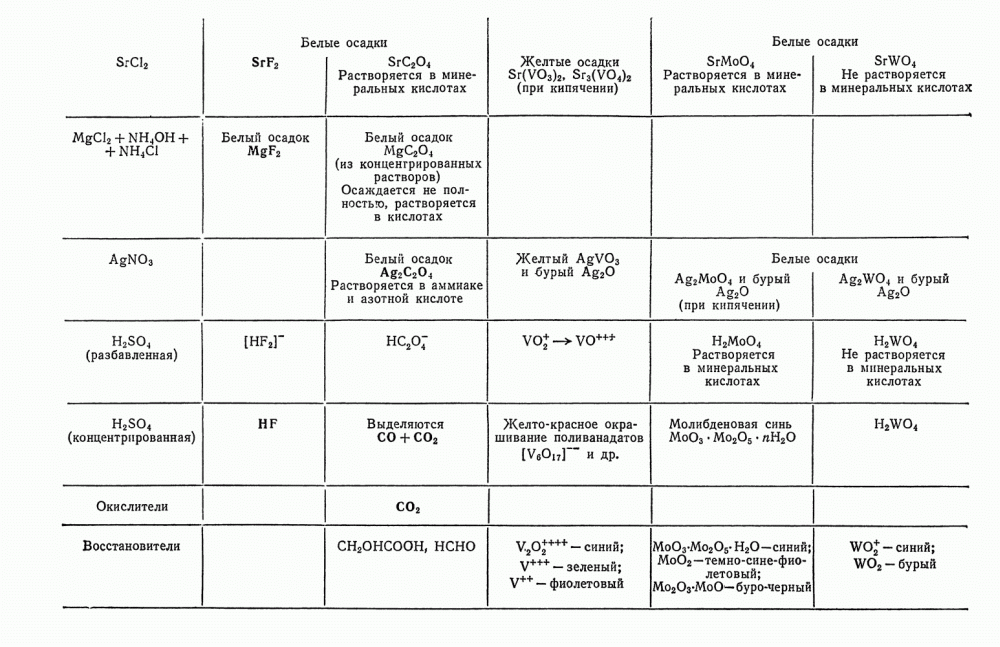
- § 25. Сводные таблицы действия реактивов на катионы и анионы
- Е. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ ИОНОВ
- § 26. Значение периодического закона в аналитической химии
- § 27. Периодическая система элементов Д. И. Менделеева как классификация атомов по их строению
- § 28. Зависимость некоторых химических свойств элементов от положения их в периодической системе Д. И. Менделеева
- § 29. Растворимость химических соединений в связи с положением элементов в периодической системе Д. И. Менделеева
- § 30. Открытие новых аналитических реакций
- § 31. Аналитические группы и периодическая система элементов Д. И. Менделеева
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ КАТИОНОВ И АНАЛИЗ СМЕСЕЙ КАТИОНОВ
- § 1. Характеристика первой аналитической группы катионов
- § 2. Общие реакции катионов первой аналитической группы
- РЕАКЦИИ КАТИОНОВ 1-й ПОДГРУППЫ
- § 3. Обнаружение NН-ионов
- § 4. Методы разложения и удаления солей аммония
- § 5. Обнаружение K-ионов
- § 6. Обнаружение Rb-ионов
- § 7. Обнаружение Cs-ионов
- § 8. Анализ смеси катионов первой подгруппы
- РЕАКЦИИ КАТИОНОВ 2-й ПОДГРУППЫ
- § 9. Обнаружение Li-ионов
- § 10. Обнаружение Na-ионов
- § 11. Обнаружение Mg-ионов
- § 12. Обзор действия реактивов на катионы первой аналитической группы
- § 13. Анализ смеси катионов второй подгруппы
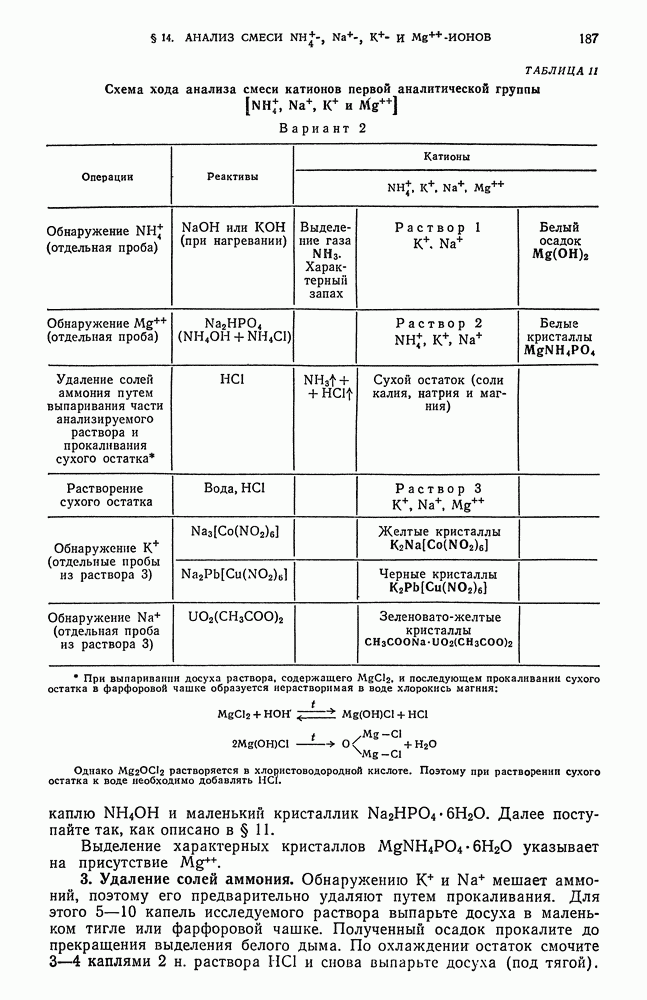
- § 14. Анализ смеси ионов
- § 15. Анализ смеси ионов
- ГЛАВА V. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика второй аналитической группы катионов
- § 2. Общие реакции катионов второй аналитической группы
- § 3. Обнаружение Ca-ионов
- § 4. Обнаружение Sr-ионов
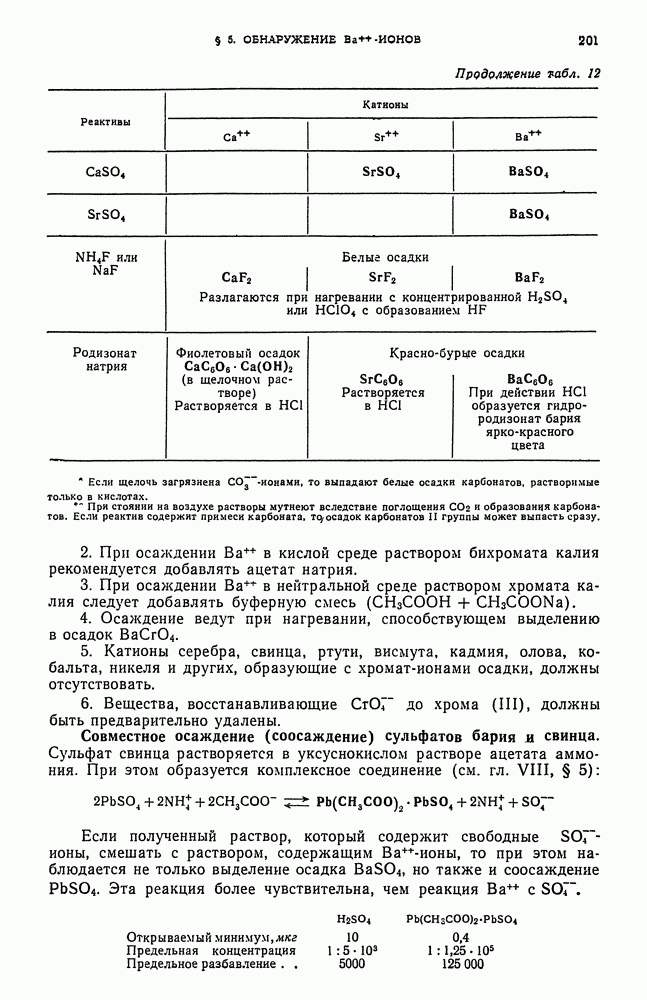
- § 5. Обнаружение Ba-ионов
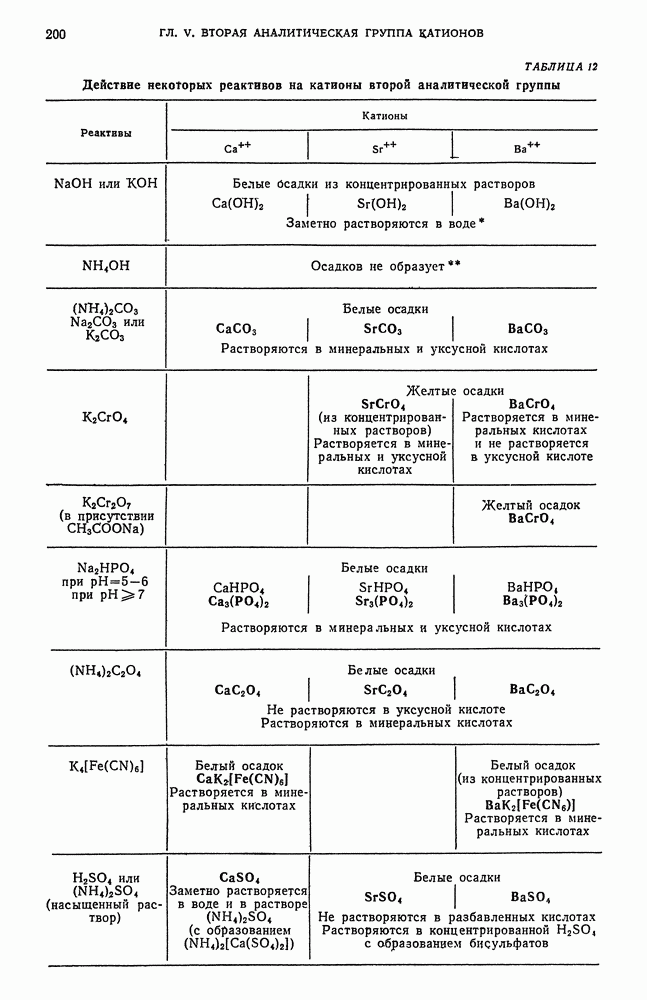
- § 6. Обзор действия реактивов на катионы второй аналитической группы
- § 7. Основы теории осаждения катионов второй аналитической группы групповым реактивом—карбонатом аммония
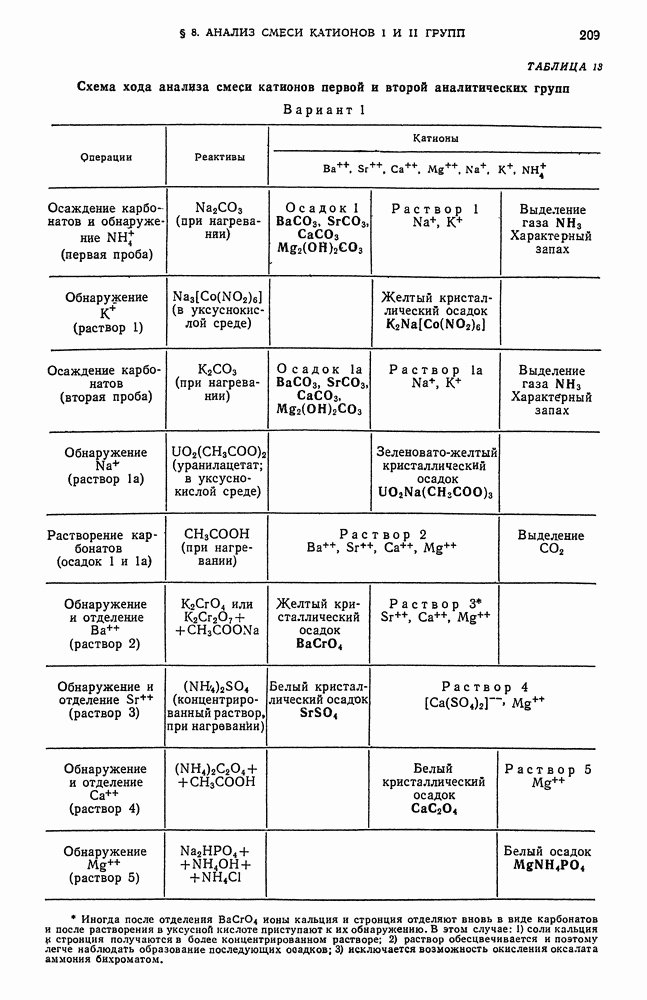
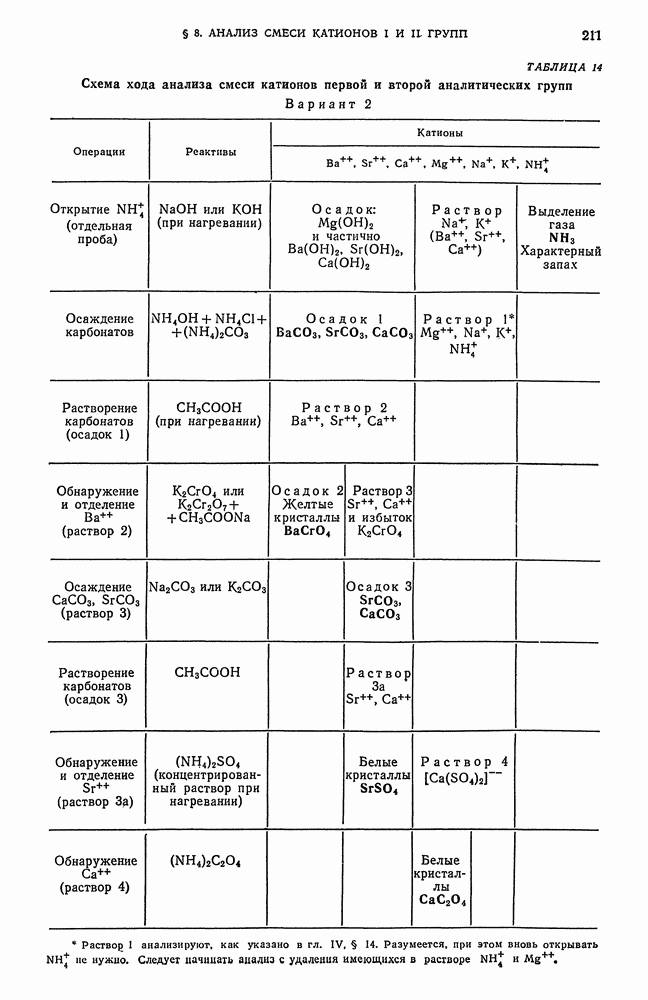
- § 8. Систематический ход анализа смеси катионов первой и второй аналитических групп
- § 9. Систематический ход анализа смеси катионов первой и второй аналитических групп в присутствии ионов
- § 10. Теоретические основы перевода сульфатов катионов второй аналитической группы в карбонаты
- ГЛАВА VI. ТРЕТЬЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика третьей аналитической группы катионов
- § 2. Общие реакции катионов третьей аналитической группы
- § 3. Обнаружение Be-ионов
- § 4. Обнаружение Al-ионов
- § 5. Обнаружение ионов титана (IV)
- § 6. Обнаружение Cr-ионов
- § 7. Обнаружение Mn-ионов
- § 8. Обнаружение Fe-ионов
- § 9. Обнаружение Fe-ионов
- § 10. Обнаружение Co-ионов
- § 13. Обнаружение ионов циркония (IV)
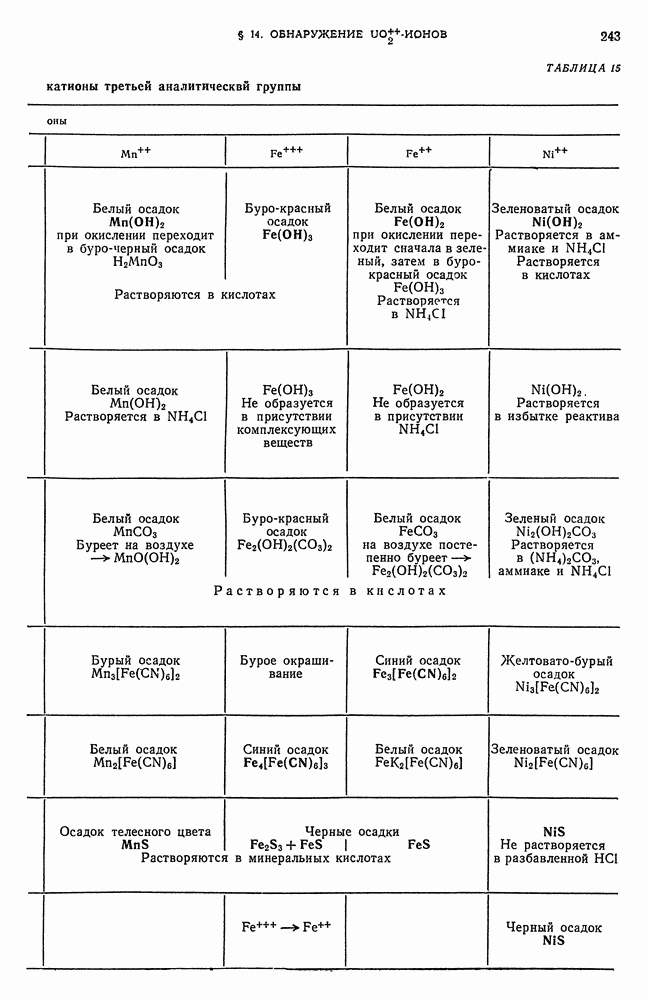
- § 14. Обнаружение UO-ионов
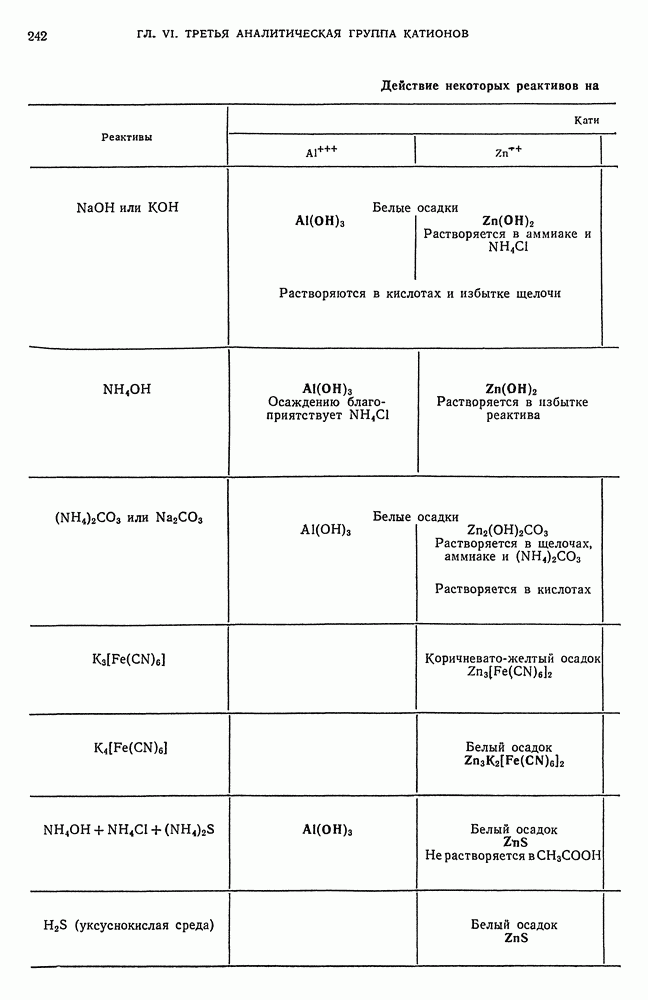
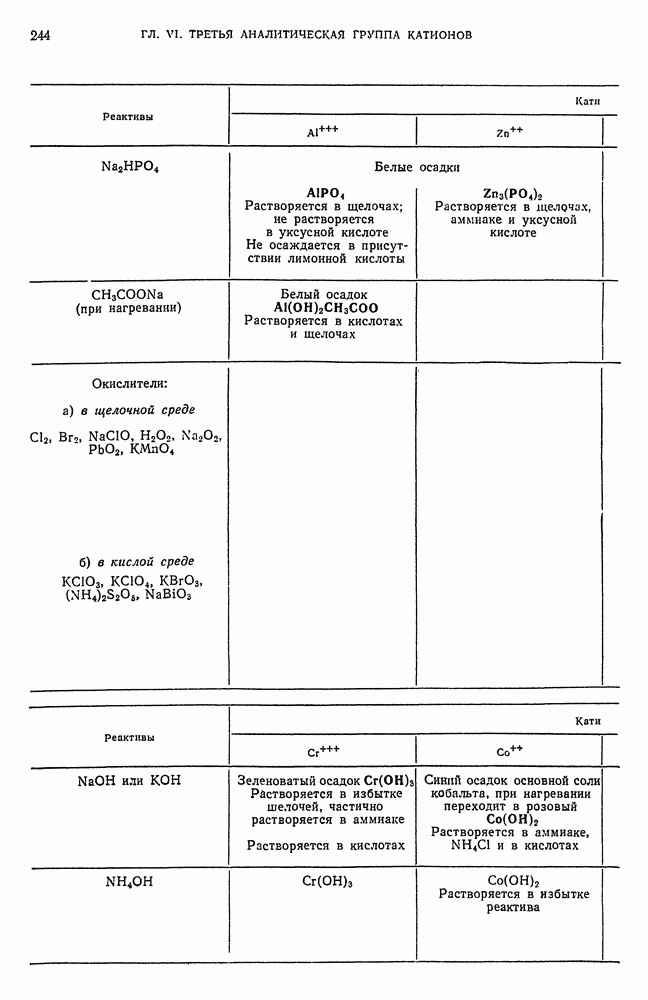
- § 15. Обзор действия реактивов на катионы третьей аналитической группы
- § 16. Использование коллоидных систем в химическом анализе
- § 17. Основы теории осаждения катионов третьей аналитической группы групповым реактивом — сульфидом аммония
- § 18. Теоретические основы применения органических реактивов в качественном анализе неорганических веществ
- § 19. Методы разделения некоторых катионов третьей аналитической группы
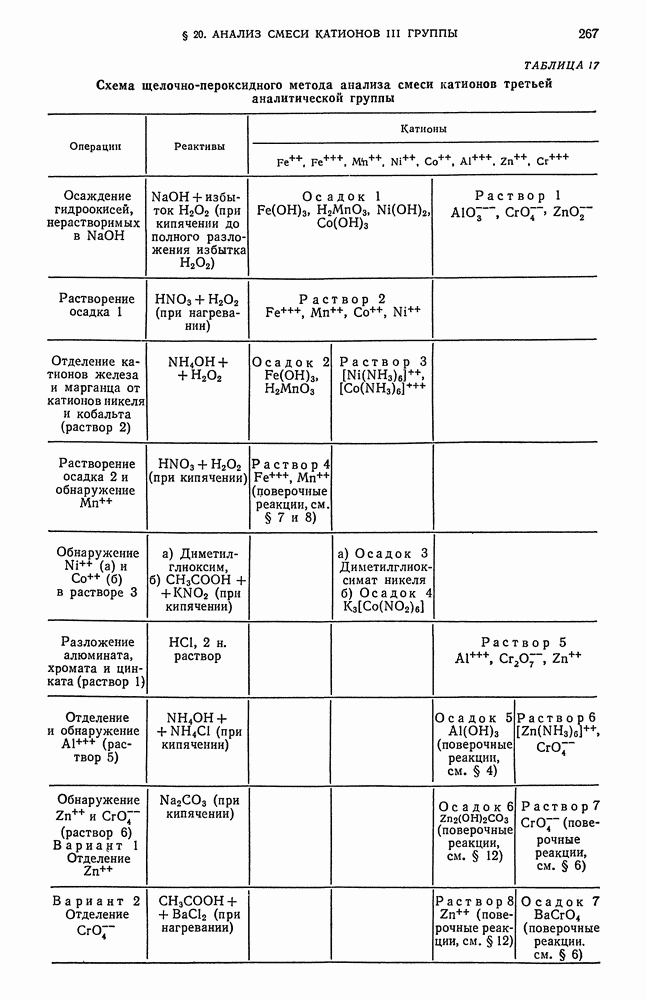
- § 20. Систематический ход анализа смеси катионов третьей аналитической группы
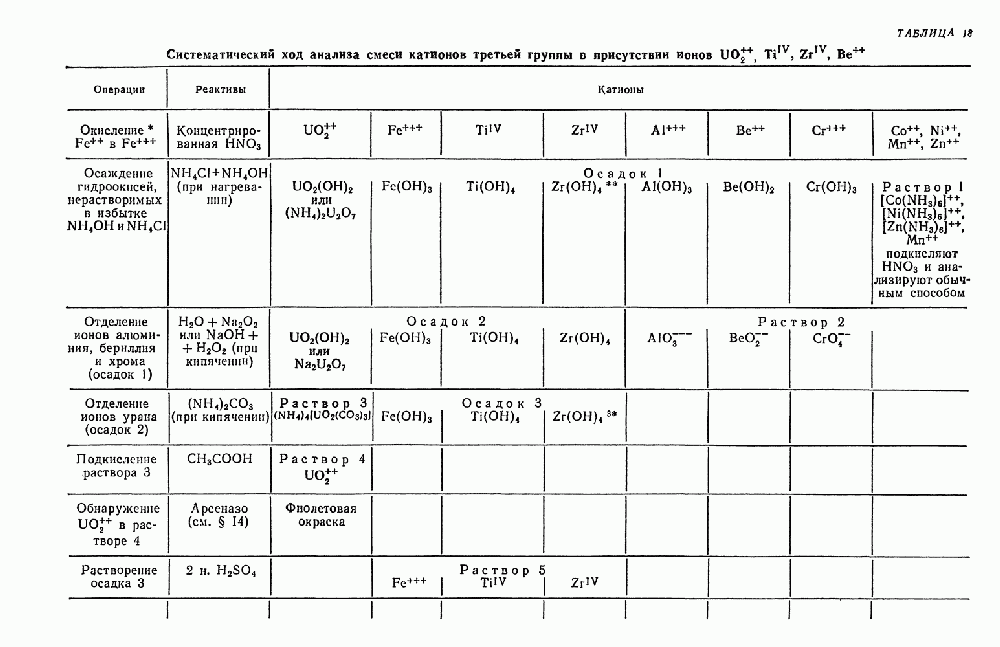
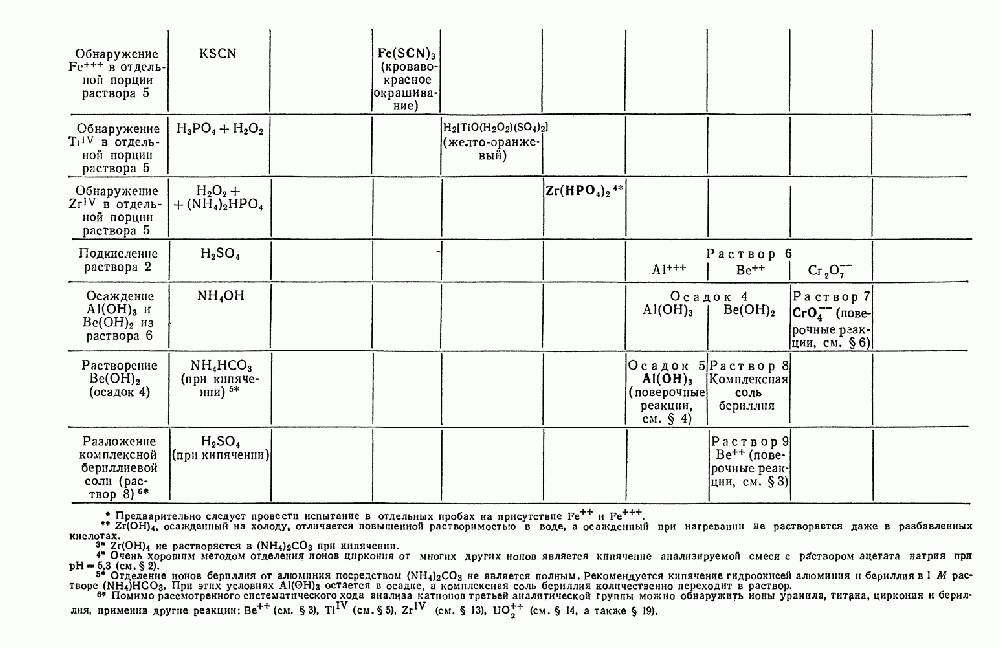
- § 21. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп
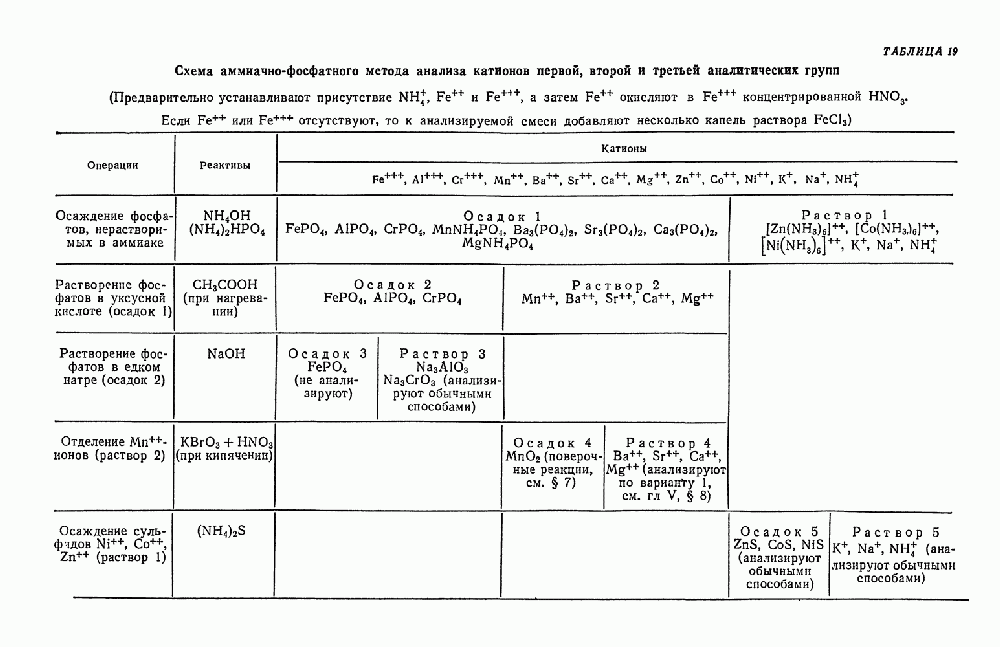
- § 22. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп в присутствии PO-ионов
- ГЛАВА VII. ЧЕТВЕРТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика четвертой аналитической группы катионов
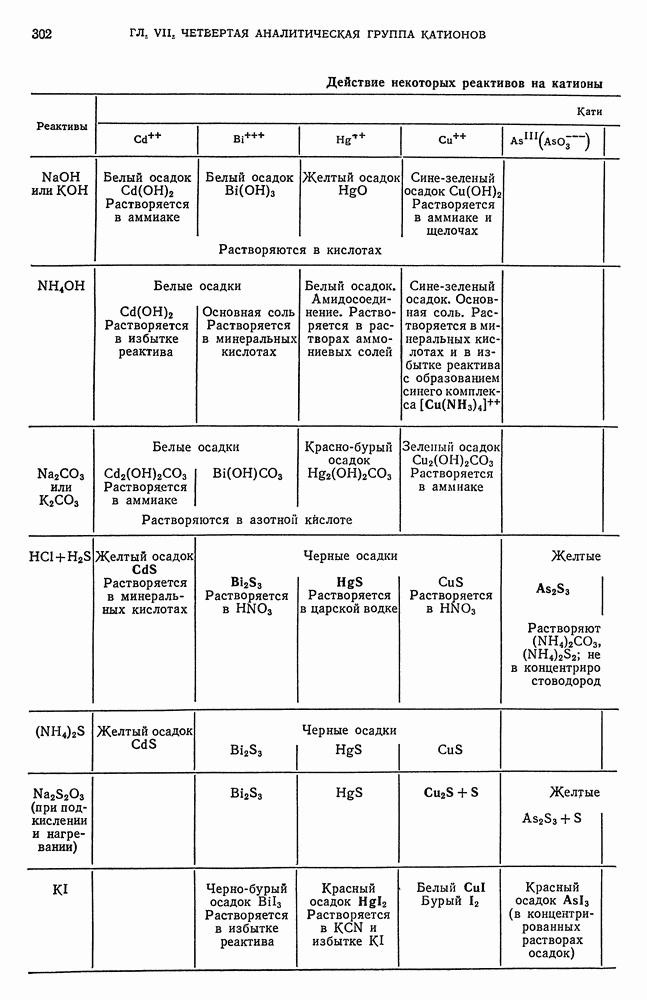
- § 2. Общие реакции катионов четвертой аналитической группы
- РЕАКЦИИ КАТИОНОВ ПЕРВОЙ ПОДГРУППЫ (ПОДГРУППЫ МЕДИ)
- § 3. Обнаружение Hg-ионов
- § 4. Обнаружение Cu-ионов
- § 5. Обнаружение Cd-ионов
- § 6. Обнаружение Bi-ионов
- РЕАКЦИИ КАТИОНОВ ВТОРОЙ ПОДГРУППЫ (ПОДГРУППЫ МЫШЬЯКА)
- § 7. Обнаружение ионов мышьяка (III)
- § 8. Обнаружение ионов мышьяка (V)
- § 9. Общие реакции обнаружения
- § 10. Обнаружение ионов сурьмы (III)
- § 11. Обнаружение ионов сурьмы (V)
- § 12. Общие реакции обнаружения Sb
- § 13. Обнаружение ионов олова (II)
- § 14. Обнаружение ионов олова (IV)
- § 15. Общие реакции обнаружения ионов олова (II) и олова (IV)
- § 16. Отделение ионов олова от других ирнов четвертой аналитической группы
- § 17. Обнаружение ионов германия (IV)
- § 18. Отделение ионов германия от других ионов четвертой аналитической группы
- § 19. Обзор действия реактивов на катионы четвертой аналитической группы
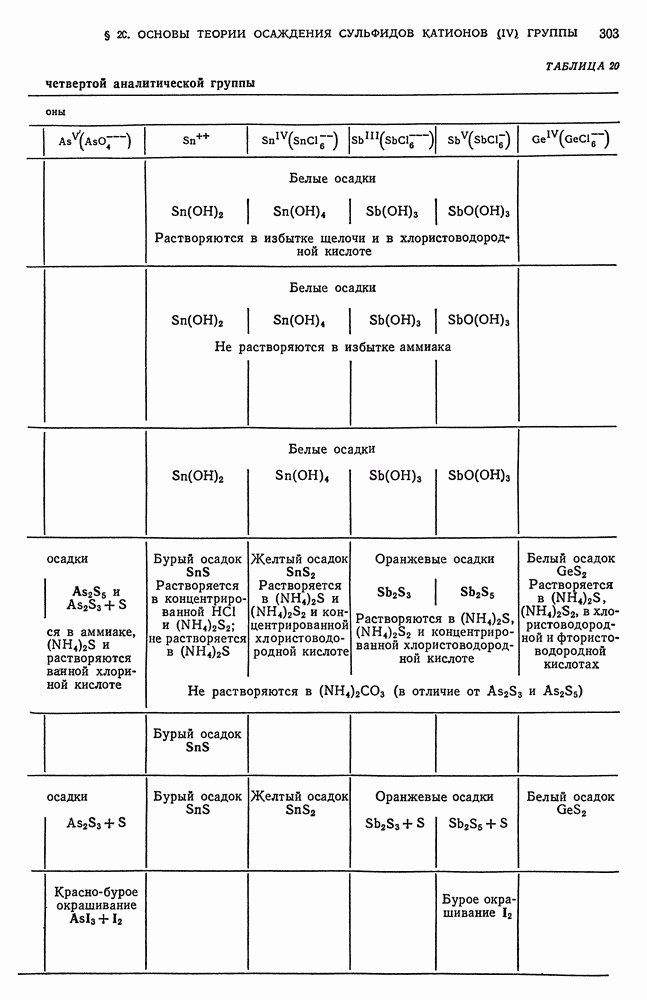
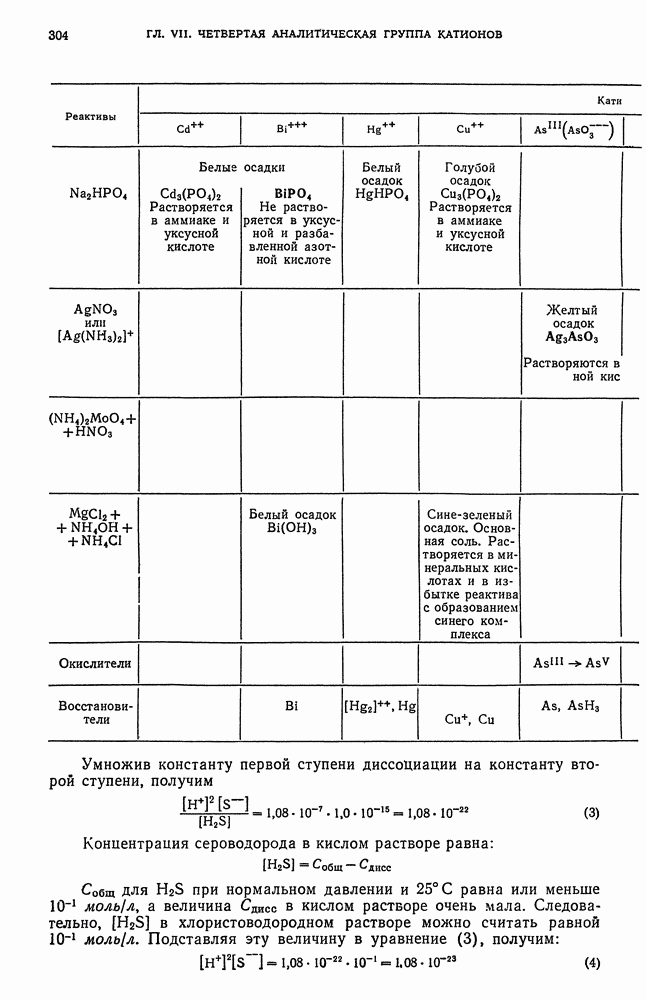
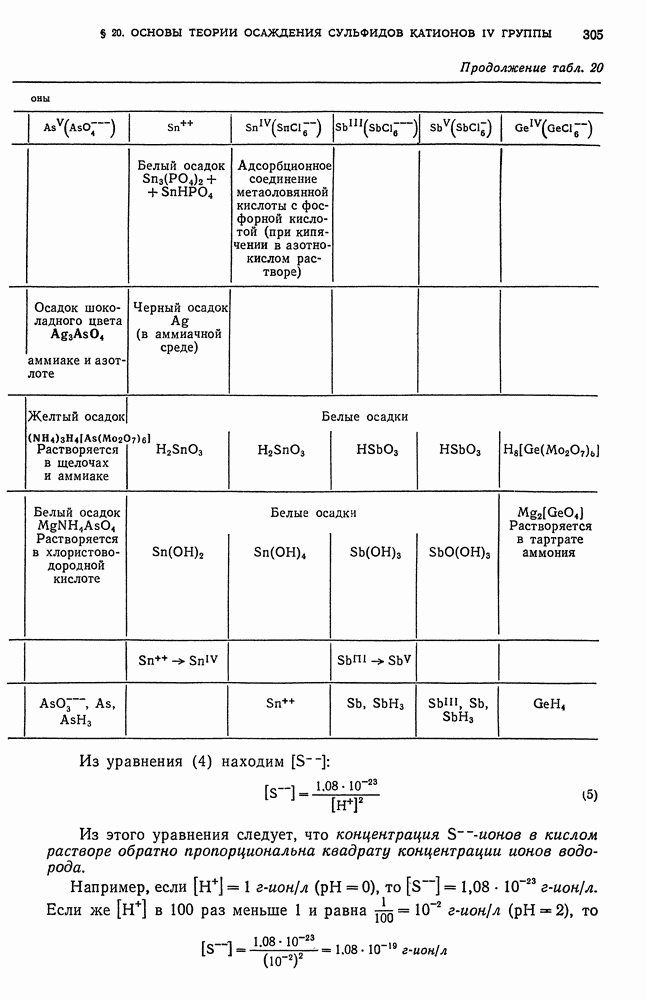
- § 20. Основы теории осаждения сульфидов катионов четвертой аналитической группы групповым реактивом — сероводородом
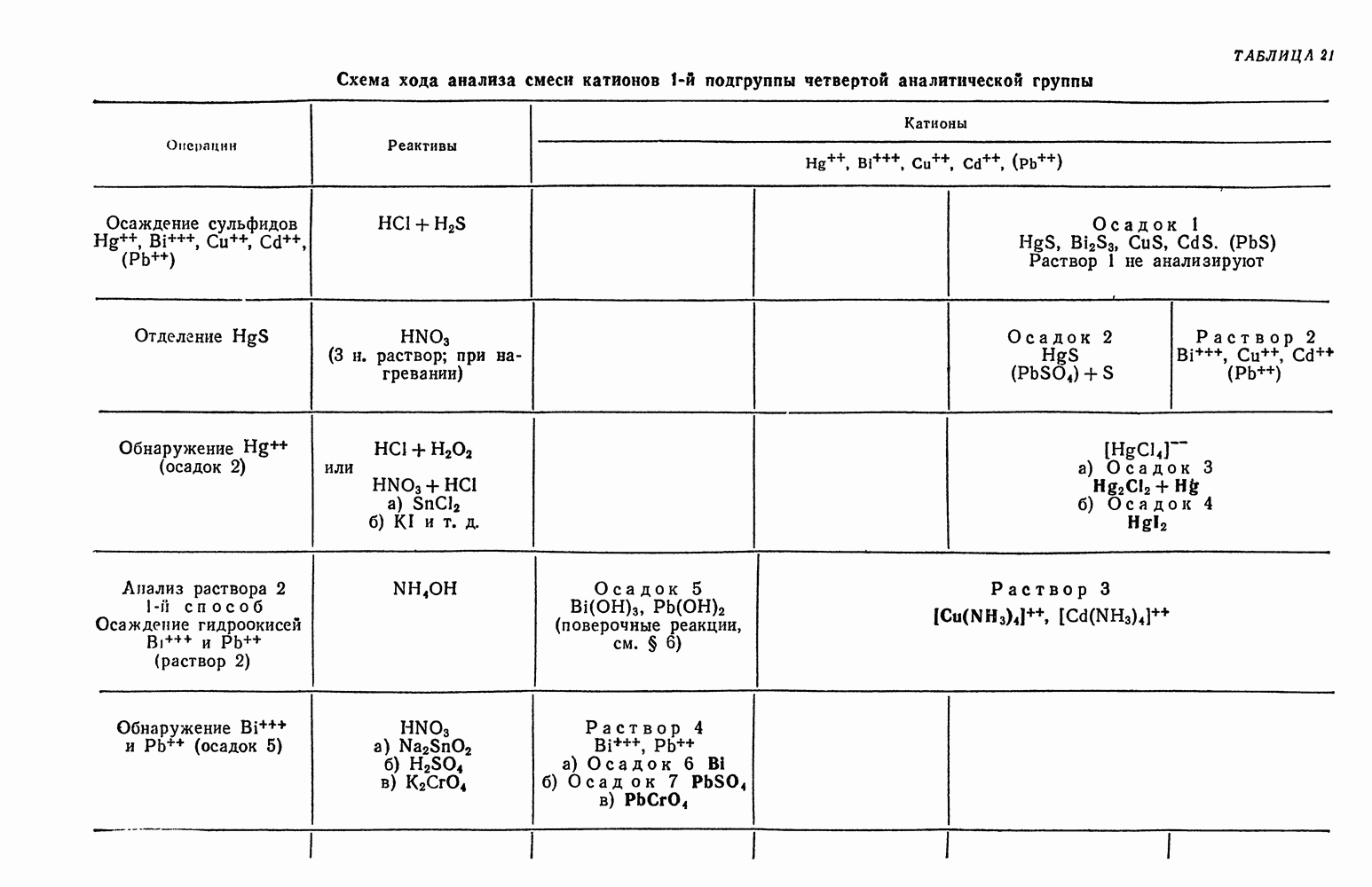
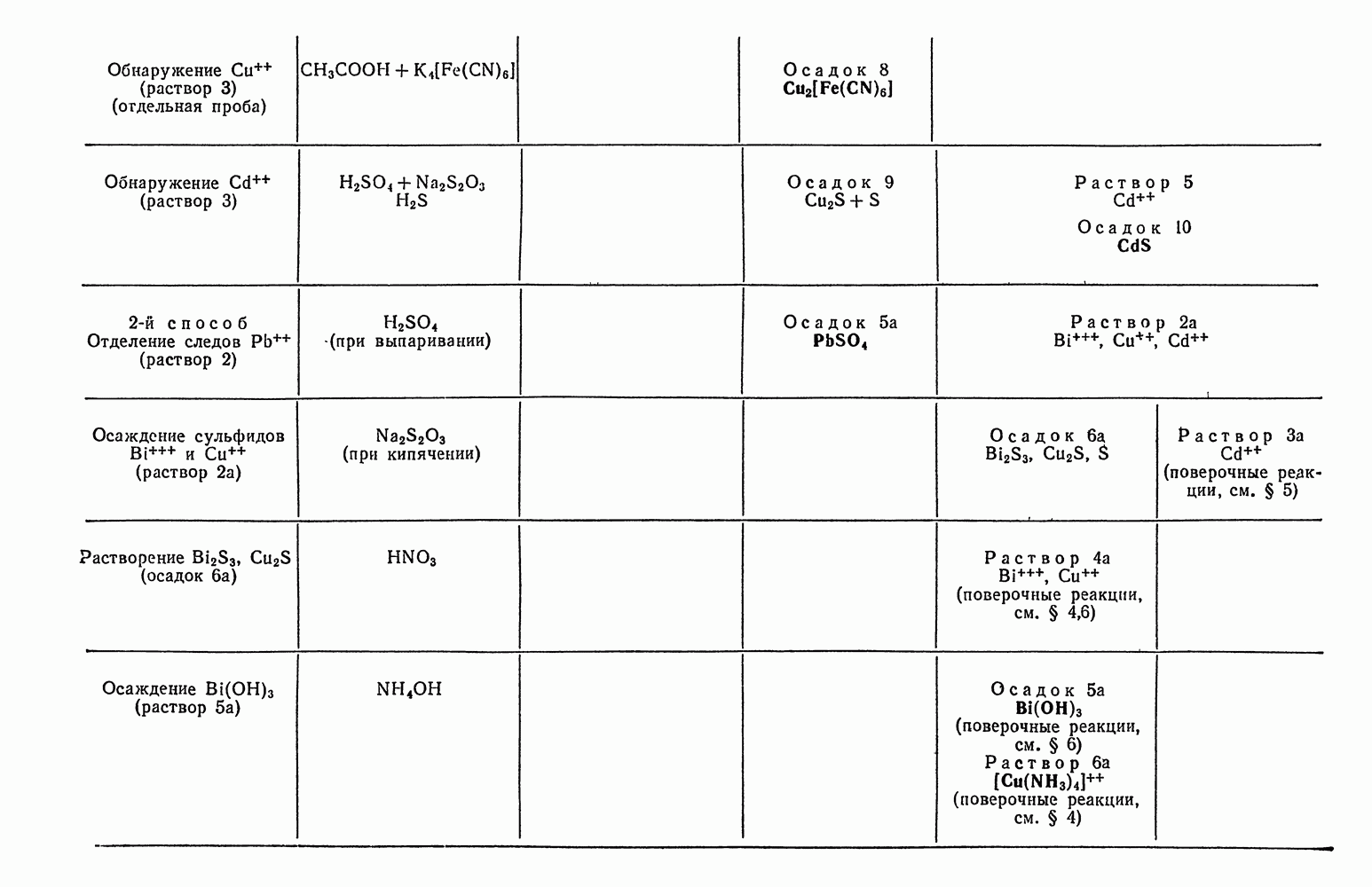
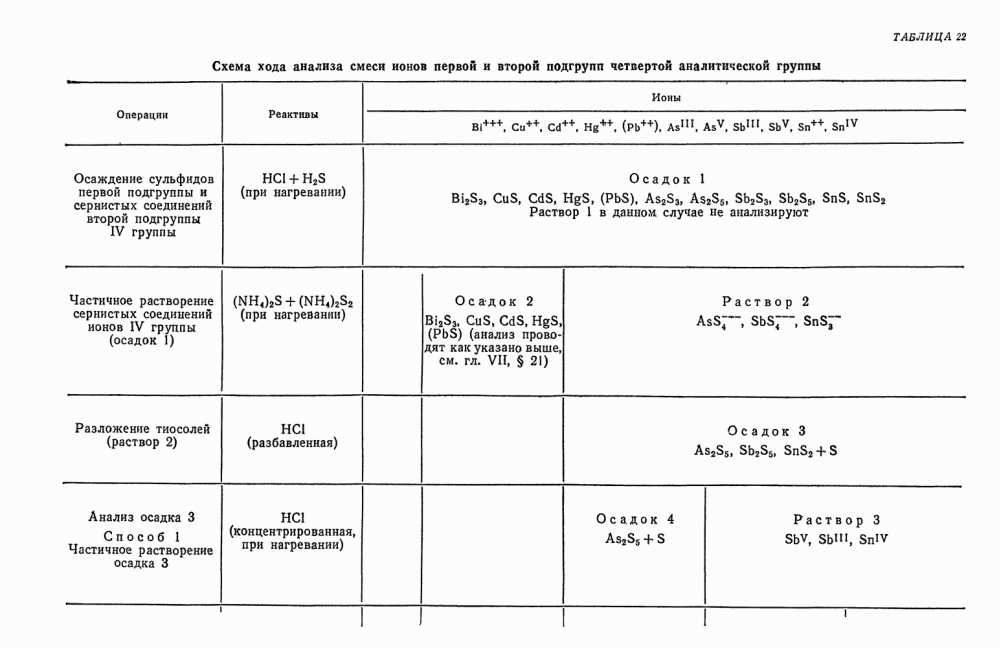
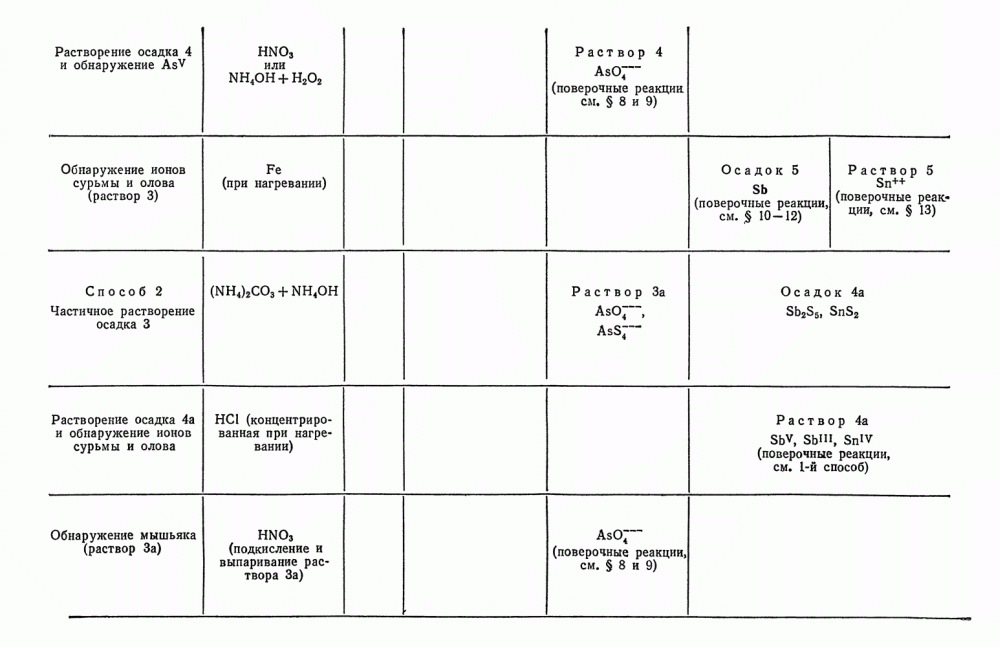
- § 21. Систематический ход анализа смеси катионов четвертой аналитической группы
- ГЛАВА VIII. ПЯТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ (ГРУППА СЕРЕБРА)
- § 1. Характеристика пятой аналитической группы катионов
- § 2. Общие реакции катионов пятой аналитической группы
- § 3. Обнаружение Ag-ионов
- § 4. Обнаружение [Hg]-ионов
- § 5. Обнаружение Pb-ионов
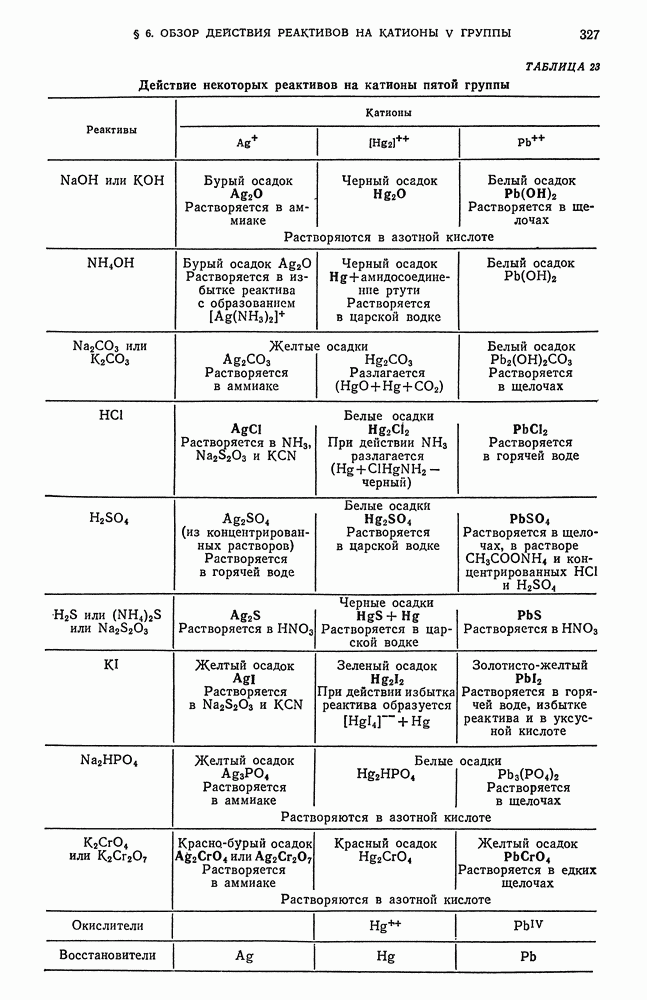
- § 6. Обзор действия реактивов на катионы пятой аналитической группы
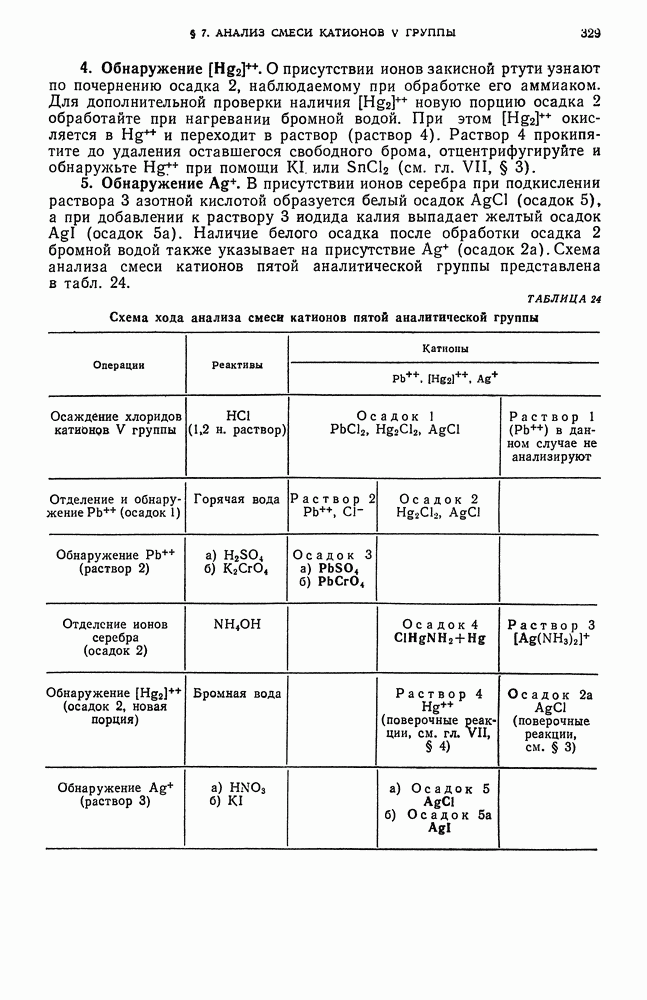
- § 7. Систематический ход анализа смеси катионов пятой аналитической группы
- ГЛАВА IX. АНАЛИЗ СМЕСИ ИОНОВ ВСЕХ ПЯТИ АНАЛИТИЧЕСКИХ ГРУПП
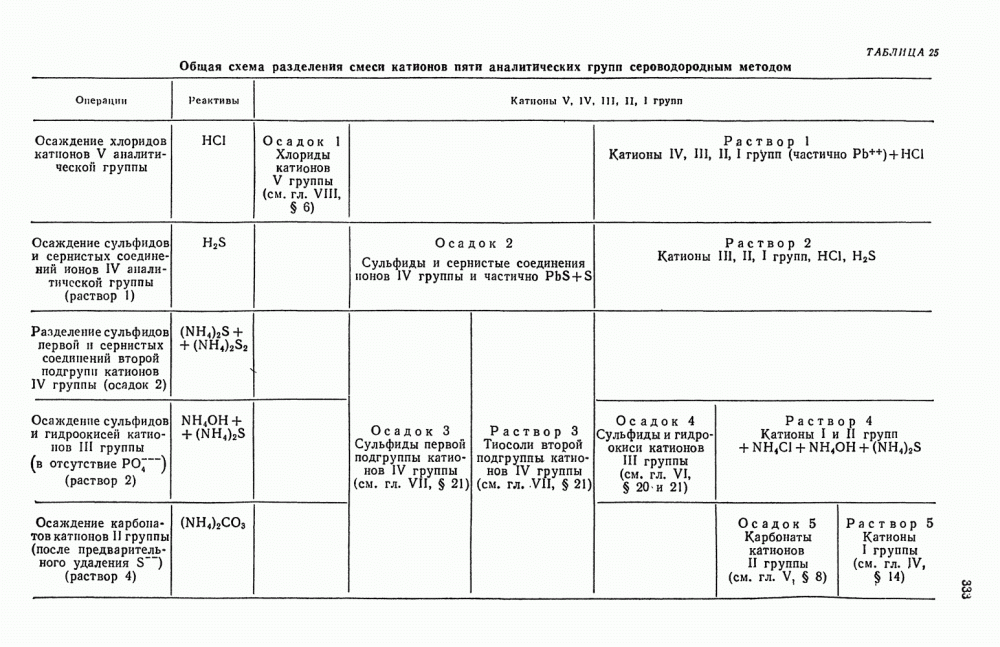
- § 1. Сероводородный метод анализа
- § 2. Недостатки сероводородного метода анализа
- § 3. Ошибки, возникающие при анализе смеси ионов пяти аналитических групп
- § 4. Бессероводородные методы анализа
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ АНИОНОВ И АНАЛИЗ СМЕСЕЙ АНИОНОВ
- § 1. Аналитическая классификация анионов
- § 2. Групповые реактивы на анионы
- § 3. Классификация методов анализа анионов
- ГЛАВА XI. ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика первой группы анионов
- § 2. Реакции анионов первой группы
- § 3. Обнаружение CI-ионов
- § 4. Обнаружение Br-ионов
- § 5. Обнаружение I-ионов
- § 6. Обнаружение CN-ионов
- § 7. Обнаружение SCN-ионов
- § 8. Обнаружение [Fe(CN)]-ионов
- § 9. Обнаружение Fe(CN)-ионов
- § 10. Обнаружение NO-ионов
- § 11. Обнаружение NO2-ионов
- § 12. Обнаружение S-ионов
- § 13. Обнаружение CH3COOO-ионов
- § 14. Обнаружение BrO3-ионов
- § 15. Обнаружение ClO3-ионов
- § 16. Обнаружение ClO4-ионов
- § 17. Обзор действия реактивов на анионы первой группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 18. Анализ смеси Cl, Br и I-ионов
- § 19. Анализ смеси Cl, Br, I и SCN-ионов
- § 20. Анализ смеси Cl, ClO3 и ClO4-ионов
- § 21. Анализ смеси NO2 и NO3-ионов
- § 22. Анализ смеси анионов первой группы
- ГЛАВА XII. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика второй группы анионов
- § 2. Общие реакции анионов второй группы
- § 3. Обнаружение SO3-ионов
- § 4. Обнаружение S2O3-ионов
- § 5. Обнаружение S2O3 в присутствии SO3-ионов
- § 6. Обнаружение SO4-ионов
- § 7. Обнаружение CO3-ионов
- § 8. Обнаружение CO3-ионов в присутствии SO3 и S2O3-ионов
- § 9. Обнаружение PO4-ионов
- § 10. Обнаружение CrO4-ионов
- § 11. Обнаружение AsO3-ионов
- § 12. Обнаружение AsO4-ионов
- § 13. Обнаружение BO2 и BO3-ионов
- § 14. Обнаружение SiO3-ионов
- § 15. Обнаружение F-ионов
- § 16. Обнаружение C2O4-ионов
- § 17. Обнаружение VO3-ионов
- § 18. Обнаружение MoO4-ионов
- § 19. Обнаружение WO4-ионов
- § 20. Обзор действия реактивов на анионы второй группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 21. Анализ смеси ионов
- § 22. Анализ смеси SO3, SO4, S2O3 и CO3-ионов
- § 23. Анализ смеси VO2, MoO4 и WO4-ионов
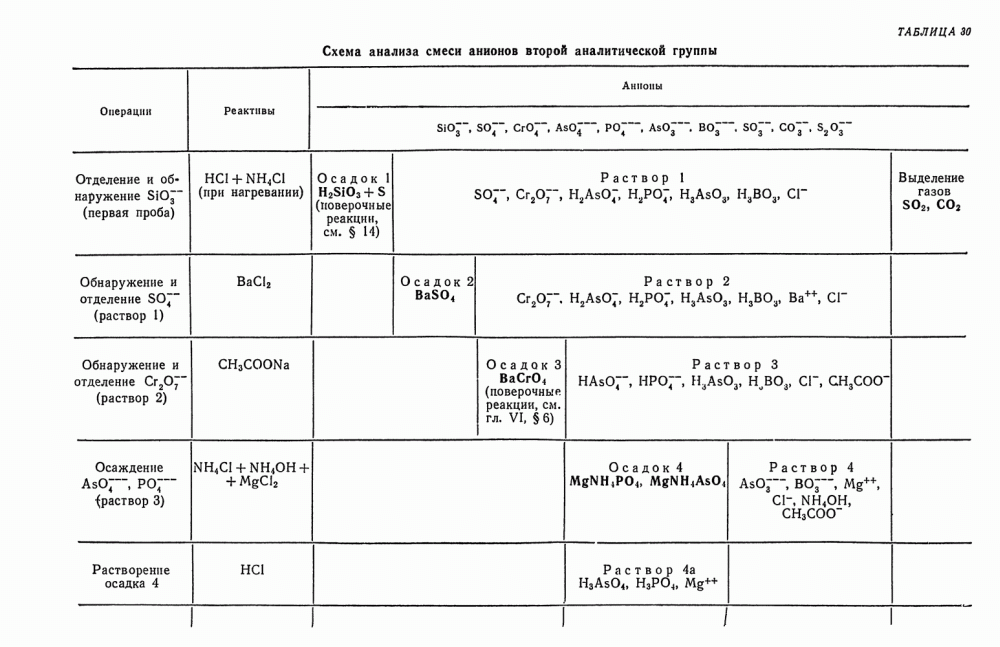
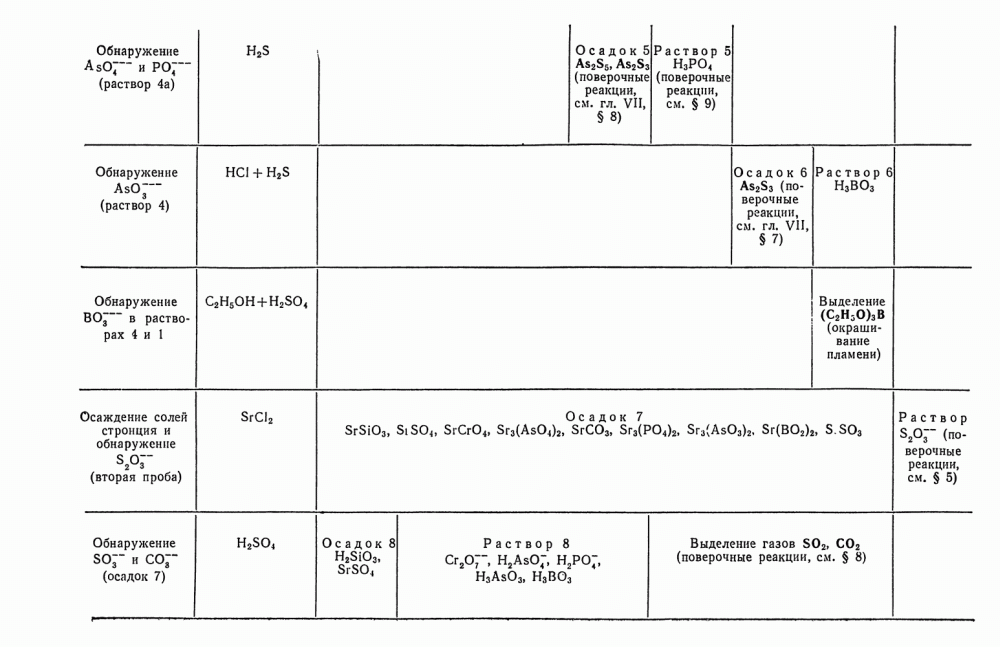
- § 24. Анализ смеси анионов второй группы
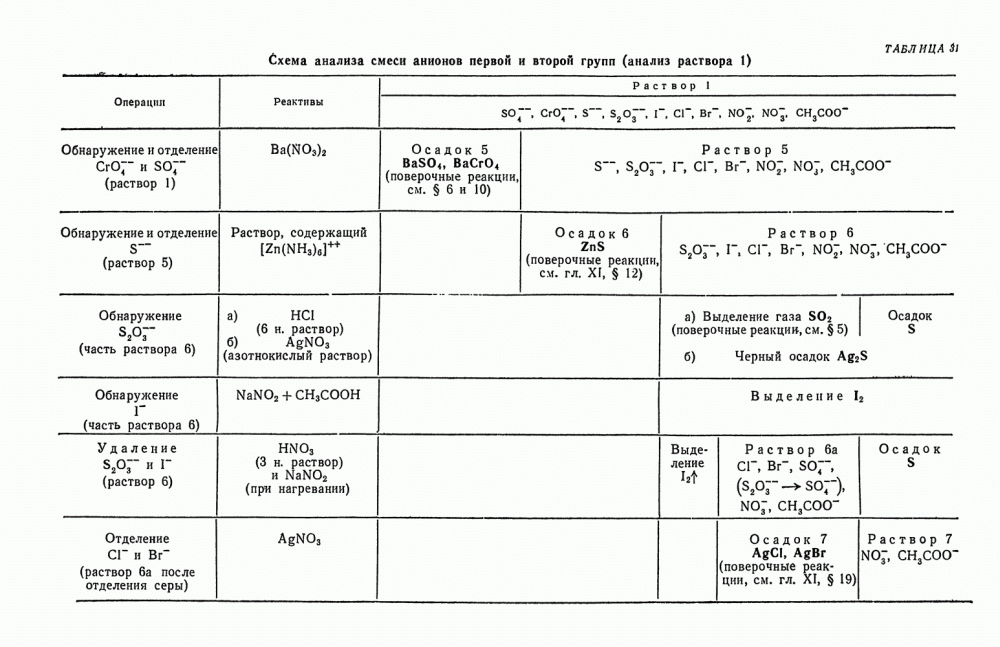
- § 25. Анализ смеси анионов первой и второй групп
- ГЛАВА XIII. ОБНАРУЖЕНИЕ СВОБОДНЫХ МЕТАЛЛОВ И НЕМЕТАЛЛОВ, ИДЕНТИФИЦИРОВАНИЕ СОЛЕЙ И ДРУГИХ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И АНАЛИЗ ИХ СМЕСЕЙ
- § 1. Подготовка вещества к анализу
- § 2. Предварительные испытания
- § 3. Растворение анализируемого вещества в воде, кислотах и щелочах
- § 4. Переведение в растворимое состояние веществ, нерастворимых в воде, кислотах и щелочах
- § 5. Анализ неизвестного вещества
- § 6. Обнаружение свободных элементов
- § 7. Идентифицирование солей и других индивидуальных соединений
- § 8. Обнаружение микропримесей
- § 9. Анализ сплавов
- § 10. Анализ силикатов и алюмосиликатов
- § 11. Анализ смеси неорганических веществ
- § 12. Экспрессный метод анализа смесей катионов и анионов
- § 13. Идентифицирование нерастворимых веществ
- ЛИТЕРАТУРА