| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
А. МЕТОДЫ КАЧЕСТВЕННОГО АНАЛИЗА
§ 1. Обнаружение отдельных элементов
В качественном анализе для установления состава исследуемого вещества используют характерные химические или физические свойства этого вещества. Например, аммиак легко узнают по специфическому запаху, а соли аммония — по выделению аммиака, образующегося при нагревании этих солей с едкой щелочью:

Совершенно нет необходимости выделять открываемые элементы в чистом виде, чтобы обнаружить их присутствие в анализируемом веществе. Однако выделение в чистом виде металлов, неметаллов и ил соединений иногда используется в качественном анализе для их идентификации, хотя такой путь анализа весьма труден. Для обнаружения отдельных элементов пользуются более простыми и удобными методами анализа, основанными на химических реакциях, характерных для ионов данных элементов и протекающих при строго определенных условиях. Так, для открытия серы в сульфиде железа (II) к пробе исследуемого вещества добавляют хлористоводородную кислоту. При этом сульфид железа (II) растворяется и появляется запах сероводорода, образующегося в результате реакции:

О присутствии  в полученном растворе судят по выделению синего осадка
в полученном растворе судят по выделению синего осадка  , который образуется при добавлении к полученному раствору гексацианоферрата (III) калия
, который образуется при добавлении к полученному раствору гексацианоферрата (III) калия  :
:

Итак, в одном случае аналитическим признаком присутствия в анализируемом соединении искомого элемента является выделение газа, отличающегося специфическим запахом; в другом — выпадение осадка, характеризующегося определенным цветом.
Аналитические признаки. Помимо образования характерных осадков и газов аналитическими признаками ряда соединений являются также их определенная растворимость в воде, кислотах, щелочах, органических растворителях; отношение к нагреванию (частичная или полная возгонка, термическое разложение, обугливание), к действию окислителей и восстановителей, к концентрированной  поведение при нагревании с плавнями (с
поведение при нагревании с плавнями (с  ), образование кристаллов определенной формы, изменение цвета раствора, окрашивание бесцветного пламени горелки и т. п.
), образование кристаллов определенной формы, изменение цвета раствора, окрашивание бесцветного пламени горелки и т. п.
Например, аналитическими признаками являются: для  — белый цвет, нерастворимость в воде, кислотах и щелочах и
— белый цвет, нерастворимость в воде, кислотах и щелочах и  для
для  белый цвет, нерастворимость в воде и уксусной кислоте, термическое разложение на
белый цвет, нерастворимость в воде и уксусной кислоте, термическое разложение на  при нагревании и
при нагревании и  при прокаливании, обесцвечивание кислого раствора
при прокаливании, обесцвечивание кислого раствора  и др., для кристаллогидратов — выделение воды при нагревании; для органических соединений — обугливание при прокаливании; для восстановителей — обесцвечивание подкисленного серной кислотой раствора перманганата калия
и др., для кристаллогидратов — выделение воды при нагревании; для органических соединений — обугливание при прокаливании; для восстановителей — обесцвечивание подкисленного серной кислотой раствора перманганата калия  для окислителей — выделение иода из нейтральных или кислых растворов при действии на них KI; для карбонатов — выделение двуокиси углерода при действии на них кислот и т. д. и т. п.
для окислителей — выделение иода из нейтральных или кислых растворов при действии на них KI; для карбонатов — выделение двуокиси углерода при действии на них кислот и т. д. и т. п.
Одной из характерных качественных реакций на кислоты или щелочи, известных еще в древние времена, является изменение окраски лакмуса (индикатора).
Реакции, протекающие между твердыми веществами и газами. Аналитические реакции могут протекать не только в растворах, но и между твердыми, а также и газообразными веществами.
Примером реакции между твердыми веществами является описываемая ниже реакция выделения металлической ртути при нагревании сухих солей ее с карбонатом натрия (см. § 2).
Образование белого дыма при взаимодействии газообразного аммиака с хлористым водородом

может служить примером аналитической реакции с участием газообразных веществ.
Реакции, применяемые в качественном анализе. Реакции, используемые в качественном анализе, можно подразделить на следующие группы.
1. Реакции осаждения, сопровождающиеся образованием осадков различного цвета. Например,  — белого цвета,
— белого цвета,  -синий,
-синий,  — черный,
— черный,  — канареечножелтого цвета,
— канареечножелтого цвета,  — красный,
— красный,  — телесно-розовый,
— телесно-розовый,  — золотистый и т. д.
— золотистый и т. д.
Образующиеся осадки могут отличаться определенной кристаллической структурой, растворимостью в кислотах, щелочах, аммиаке и т. п.
2. Реакции, сопровождающиеся образованием газов, обладающих известным запахом, растворимостью и т. д.:

3. Реакции, сопровождающиеся образованием слабых электролитов. К числу таких реакций относят реакции, в результате которых образуются:  и т. п.
и т. п.

Р. Бойль (1627—1691).
Реакциями этого же типа можно считать реакции кислотно-основного взаимодействия, сопровождающиеся образованием нейтральных молекул воды, реакции образования газов и малорастворимых в воде осадков и реакции комплексообразования.
4. Реакции кислотно-основного взаимодействия, сопровождающиеся переходом протонов (см. гл. И, § 2).
5. Реакции комплексообразования, сопровождающиеся присоединением к атомам комплексообразователя различных лигандов — ионов и молекул (см. гл. I, § 28).
6. Реакции комплексообразования, связанные с кислотно-основным взаимодействием (см. гл. I, § 33—34).
7. Реакции окисления — восстановления, сопровождающиеся переходом электронов (см. гл. II, § 1).
8. Реакции окисления — восстановления, связанные с кислотно-основным взаимодействием (см. гл. II, § 1).
9. Реакции окисления — восстановления, связанные с комплексооб-разованием. Например:

10. Реакции окисления — восстановления, сопровождающиеся образованием осадков:

11. Реакции ионного обмена, протекающие на катионитах или анионитах (см. гл. III, § 10).
12. Каталитические реакции (см. гл. VI, § 7), используемые в кинетических методах анализа (см. гл. III, § 11).
Общие и частные аналитические реакции. Различают общие и частные аналитические реакции. Общими реакциями называют реакции, при которых реактив реагирует с несколькими ионами. Например, общей реакцией для  является их взаимодействие с
является их взаимодействие с  , с которыми они образуют белые кристаллические осадки
, с которыми они образуют белые кристаллические осадки  . Другими словами, общие реакции характеризуют целую группу ионов. Использование этих реакций дает возможность аналитику судить о наличии или отсутствии в исследуемом веществе определенной группы ионов.
. Другими словами, общие реакции характеризуют целую группу ионов. Использование этих реакций дает возможность аналитику судить о наличии или отсутствии в исследуемом веществе определенной группы ионов.
Частными реакциями называют реакции, при которых различные реактивы образуют характерные соединения с определенными ионами; частные реакции свойственны данному иону. Известно небольшое число реакций, характерных только для определенных ионов.
Реакций обнаружения и разделения ионов. В качественном анализе различают реакции обнаружения, или распознавания, или открытия, ионов и реакции разделения ионов.
Приведенная ранее реакция  является примером реакции обнаружения.
является примером реакции обнаружения.

И. Я. Берцелиус (1799—1848).
Реакции, при помощи которых отделяют одни виды ионов от других, называют реакциями отделения (разделения). Очень часто реакции обнаружения являются также реакциями разделения.
Отделить ионы друг от друга можно, например, прибавлением реактива, образующего малорастворимые соединения с одними ионами и не оказывающего такого действия на другие. Так,  можно отделить от
можно отделить от  добавлением
добавлением  , полностью осаждающего катионы щелочноземельных металлов в виде малорастворимых карбонатов.
, полностью осаждающего катионы щелочноземельных металлов в виде малорастворимых карбонатов.
Реакции разделения должны удовлетворять главному условию: они должны практически полностью отделять одни ионы от других.
Историческая справка. Основателем качественного анализа считают знаменитого английского химика и физика Роберта Бойля (1627—1691), разработавшего общие понятия о химическом анализе. Он систематизировал известные в то время качественные реакции и предложил реакций на хлор, аммиак, сульфаты и др., впервые применил лакмус (используемый и до настоящего времени) в качестве индикатора на кислоты и основания.
Шведский ученый Т. О. Бергман (1735—1784) разработал систематический ход качественного анализа, основные положения которого сохранились до наших дней. Он усовершенствовал сухой способ анализа (с примененем калильной трубки).
Французский ученый Л. Ж. Тенар (1777—1857) одним из первых химиков применил общий систематический ход анализа. Он опубликовал книгу по аналитической химии, в которой рассмотрен систематический ход анализа, основанный на делении катионов по свойствам их сернистых соединений.
Систематический ход анализа был усовершенствован немецким химиком К. Р. Фрезениусом (1818—1897). К. Р. Фрезениус написал фундаментальные руководства по качественному и количественному анализу. В 1862 г. он основал первый журнал по аналитической химии (Zeitschrift  analytische Chemie).
analytische Chemie).
В дальнейшем методы химического анализа непрерывно развивались и совершенствовались, появлялись новые методы, позволяющие не только устанавливать состав сложных веществ, но также открывать новые элементы и определять их атомные веса. Большая работа в этом направлении была проведена выдающимся шведским химиком И. Я. Берцелиусом (1779—1848). Ему принадлежит честь открытия церия, селена, торий и тантала; он определил атомные веса 50 элементов и разработал оригинальный метод элементного анализа органических соединений, усовершенствованный впоследствии немецким химиком Ю. Либихом (1803—1873).
В 1844 г. профессором Казанского университета К. К. Клаусом (1796—1864) был открыт новый элемент, названный в честь России рутением (от Ruthenia — Россия). В 1862 г. К. К. Клаус опубликовал «Методйческие таблицы реакций, применяемых при химико-аналитических исследованиях», в которых были представлены разнообразные способы анализа неорганических веществ, приведена аналитическая классификация химических элементов и описан систематический сероводородный метод качественного анализа.
Большую роль в развитии аналитической химии вообще и качественного анализа в частности сыграли работы русских ученых: М. В. Ломоносова, Т. Е. Ловица, В. М. Севергина, Д. И. Менделеева, Н. А. Меншуткина и др.
Н. А. Меншуткин (1842-1907) из основателей Русского химического общества — первым определил аналитическую химию как самостоятельную научную дисциплину и ввел в практику ее преподавания оригинальный научный метод. Его руководство по аналитической химии, опубликованное в 1871 г., выдержало много изданий и было переведено на ряд иностранных языков. По этой книге обучалось несколько поколений химиков-аналитиков.
В развитии аналитической химии большую роль сыграла теория электролитической диссоциации, предложенная шведским ученым С. А. Арениусом.
Среди других Иностранных ученых, внесших свой вклад в развитие аналитической химии, следует отметить несколько имен. Швейцарский химик Ф. П. Тредвелл, создавший оригинальный курс аналитической химии, который многократно издавался на разных языках, в том числе и на русском языке.

К. К. Клаус (1796—1864).
Американский ученый И. М. Кольтгоф, опубликовавший большое число теоретических и экспериментальных работ, учебников и монографий по аналитической химии, некоторые из которых переведены на русский язык. Ф. Файгль, разработавший одновременно с советским ученым Н. А. Тананаевым капельный метод анализа. Французский ученый Г. Шарло опубликовавший ряд известных книг по аналитической химии. В. Ф. Гиллебранд, знакомый советским читателям по его фундаментальной монографии «Практическое руководство по неорганическому анализу» и др.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Анализ и синтез
- § 2. Предмет аналитической химии
- § 3. Развитие аналитической химии
- § 4. Качественный и количественный анализ
- ГЛАВА I. ПРИМЕНЕНИЕ ЗАКОНА ДЕЙСТВИЯ МАСС В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Влияние среды на состояние ионов в растворах
- § 2. Обратимые и необратимые аналитические реакции
- § 3. Направление аналитических реакций; правила обменного разложения
- § 4. Закон действия масс и следствие из него
- § 5. Границы применимости закона действия масс
- § 6. Сильные и слабые электролиты
- § 7. Активность
- § 8. Коэффициент активности и ионная сила
- Б. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ (В ГОМОГЕННЫХ СИСТЕМАХ)
- § 9. Гомогенные и гетерогенные системы
- § 10. Ионное произведение воды
- § 11. Ионы гидроксония
- § 12. Равновесие ионов в водных растворах; понятие о pH
- § 13. Равновесие в водных растворах слабых электролитов
- § 14. Влияние сильных кислот или сильных оснований на степень электролитической диссоциации слабых электролитов
- § 15. Приближенные формулы для расчета [H+] и [OH-] в водных растворах кислот и оснований
- В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
- § 16. Буферные растворы
- § 17. Применение буферных растворов в химическом анализе
- Г. РАВНОВЕСИЯ В РАСТВОРАХ ГИДРОЛИЗУЮЩИХСЯ СОЛЕЙ
- § 18. Теоретические основы гидролиза
- § 19. Механизм гидролитического расщепления
- § 20. Подавление и усиление гидролиза солей
- Д. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ТИПИЧНО АМФОТЕРНЫХ ЭЛЕКТРОЛИТОВ
- § 21. Поведение амфотерных гидроокисей в водных растворах
- § 22. Константы электролитической диссоциации амфотерных гидроокисей
- Е. РАВНОВЕСИЯ В СИСТЕМАХ: ОСАДОК-НАСЫЩЕННЫЙ РАСТВОР
- § 23. Осаждение как один из основных методов химического анализа
- § 24. Произведение растворимости
- § 25. Произведение активностей
- § 26. Вычисление растворимости электролитов в воде по величине произведения растворимости
- § 27. Влияние различных факторов на растворимость малорастворимых электролитов
- Ж. ОСНОВЫ ТЕОРИИ ОБРАЗОВАНИЯ И РАЗЛОЖЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИИ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 28. Характеристика комплексных соединений, имеющих значение в химическом анализе
- § 29. Квантовомеханические представления о строении комплексов
- § 30. Равновесия в растворах комплексных соединений
- § 31. Константы нестойкости комплексов
- § 32. Внутрикомплексные соединения
- § 33. Методы разложения и образования комплексов, применяемых в аналитической химии
- § 34. Применение метода комплексообразования в химическом анализе
- ГЛАВА II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Окисление—восстановление как один из основных методов химического анализа
- § 2. Направление реакций окисления—восстановления
- § 3. Окислительно-восстановительные потенциалы
- § 4. Зависимость между величинами окислительно-восстановительных потенциалов и условиями, в которых протекают реакции окисления—восстановления
- § 5. Вычисление окислительно-восстановительных потенциалов
- § 6. Вычисление окислительно-восстановительных потенциалов с учетом коэффициентов активности
- ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
- § 1. Обнаружение отдельных элементов
- § 2. Анализ мокрым и сухим путем
- § 3. Химические и физические методы качественного анализа
- § 4. Макро-, полумикро- и микрометоды
- § 5. Капельный анализ
- § 6. Микрокристаллоскопический анализ
- § 7. Метод растирания порошков
- § 8. Методы анализа, основанные на нагревании и сплавлении веществ
- § 9. Спектральный качественный анализ
- § 10. Хроматографический метод анализа
- § 11. Кинетические методы анализа
- Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
- § 12. Специфичность и чувствительность реакций
- § 13. Максимальная чувствительность аналитических реактивов
- § 14. Способы повышения чувствительности реакций
- § 15. Маскировка мешающих ионов
- § 16. Определение pH среды
- § 17. Регулирование pH среды в процессе аналитических определений
- В. РЕАКТИВЫ
- § 18. Понятие о химических реактивах
- § 19. Концентрация применяемых реактивов
- § 20. Техника пользования реактивами
- Г. ПОСУДА И ПРИБОРЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕННОМ АНАЛИЗЕ
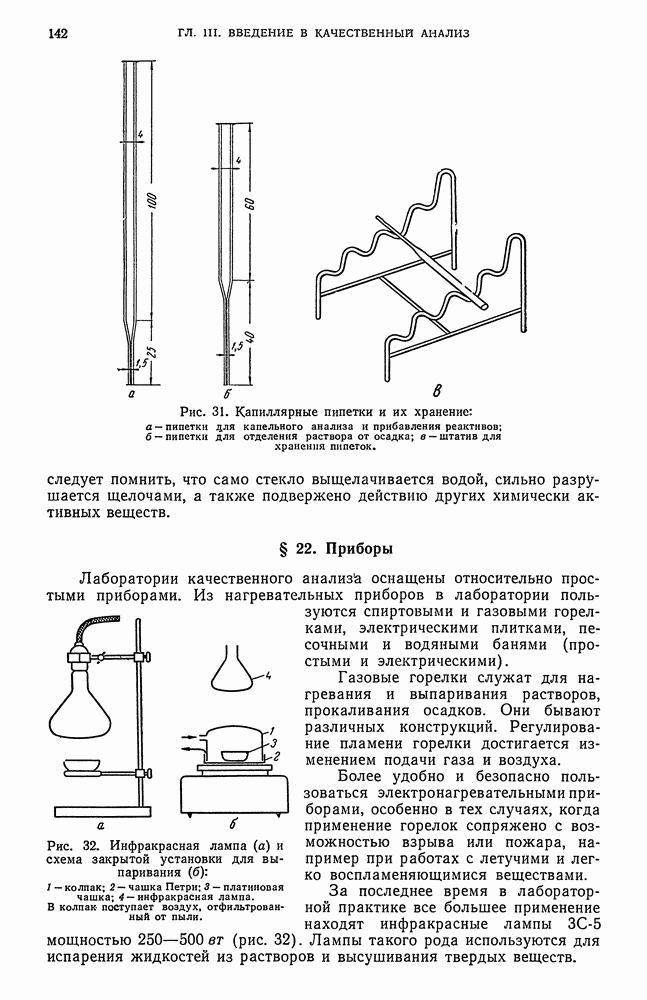
- § 21. Химическая посуда
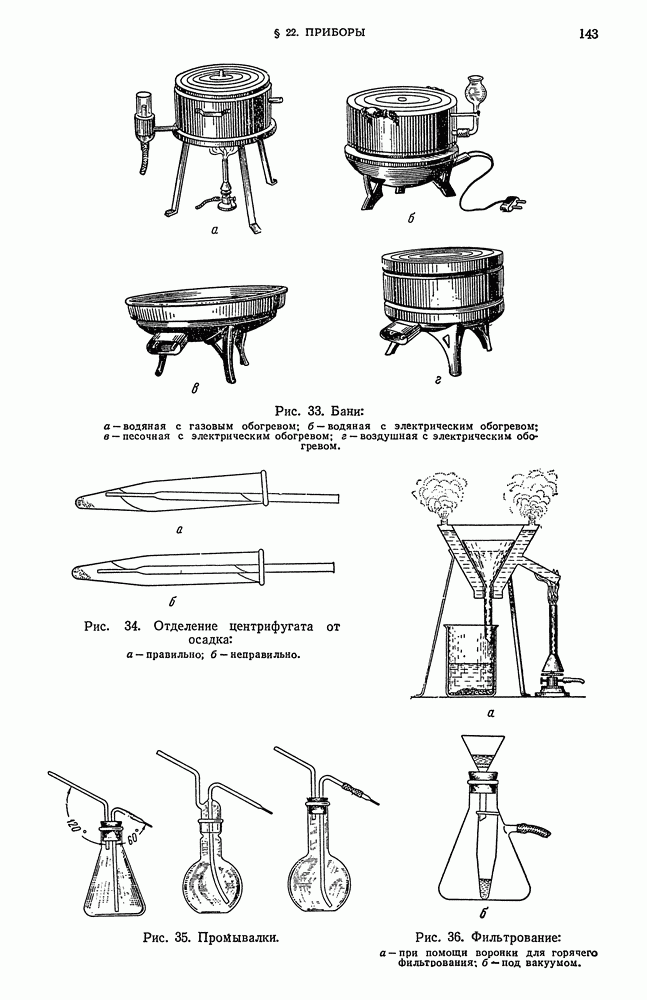
- § 22. Приборы
- Д. АНАЛИТИЧЕСКИЕ ГРУППЫ
- § 23. Дробный и систематический анализ
- § 24. Аналитическая классификация катионов
- § 25. Сводные таблицы действия реактивов на катионы и анионы
- Е. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ ИОНОВ
- § 26. Значение периодического закона в аналитической химии
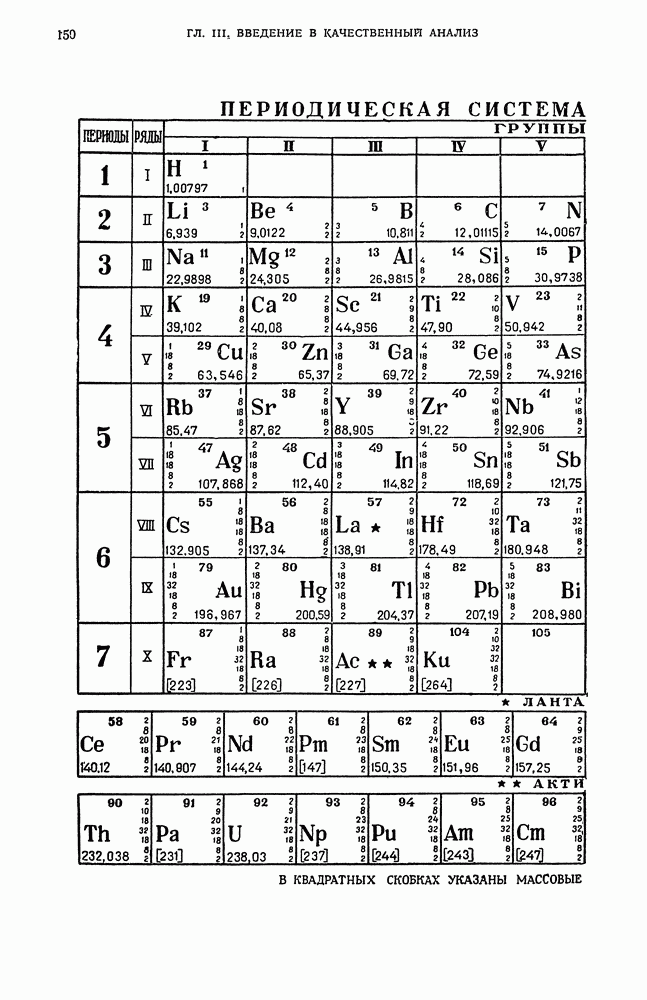
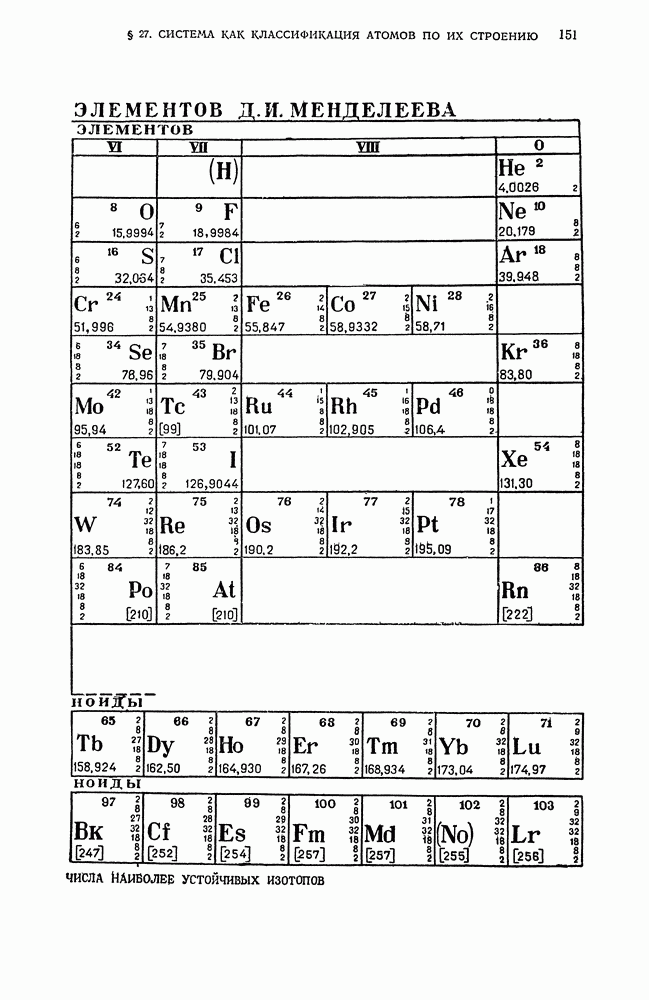
- § 27. Периодическая система элементов Д. И. Менделеева как классификация атомов по их строению
- § 28. Зависимость некоторых химических свойств элементов от положения их в периодической системе Д. И. Менделеева
- § 29. Растворимость химических соединений в связи с положением элементов в периодической системе Д. И. Менделеева
- § 30. Открытие новых аналитических реакций
- § 31. Аналитические группы и периодическая система элементов Д. И. Менделеева
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ КАТИОНОВ И АНАЛИЗ СМЕСЕЙ КАТИОНОВ
- § 1. Характеристика первой аналитической группы катионов
- § 2. Общие реакции катионов первой аналитической группы
- РЕАКЦИИ КАТИОНОВ 1-й ПОДГРУППЫ
- § 3. Обнаружение NН-ионов
- § 4. Методы разложения и удаления солей аммония
- § 5. Обнаружение K-ионов
- § 6. Обнаружение Rb-ионов
- § 7. Обнаружение Cs-ионов
- § 8. Анализ смеси катионов первой подгруппы
- РЕАКЦИИ КАТИОНОВ 2-й ПОДГРУППЫ
- § 9. Обнаружение Li-ионов
- § 10. Обнаружение Na-ионов
- § 11. Обнаружение Mg-ионов
- § 12. Обзор действия реактивов на катионы первой аналитической группы
- § 13. Анализ смеси катионов второй подгруппы
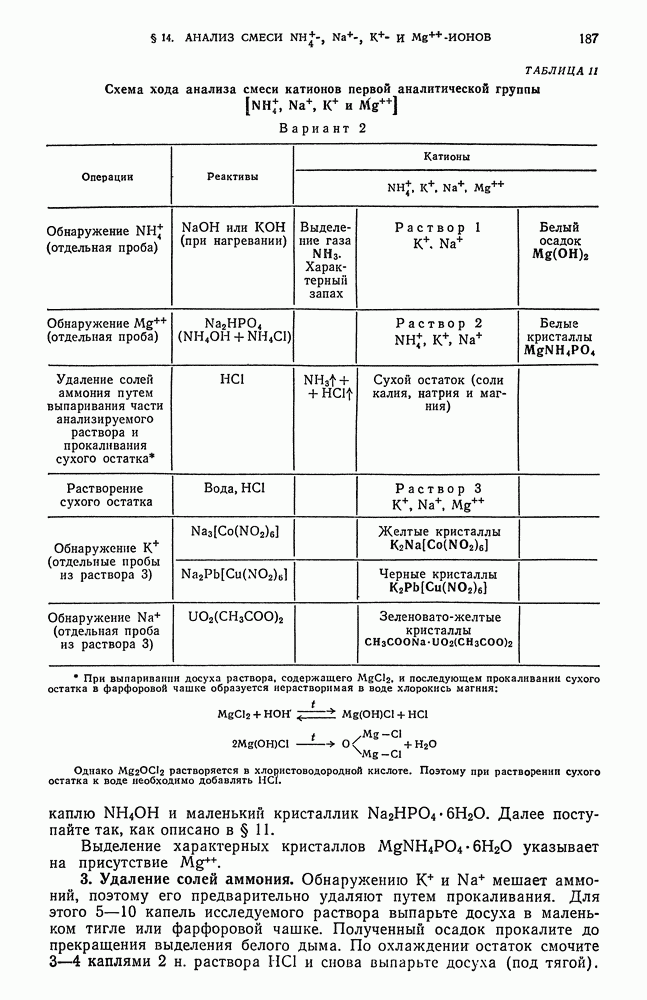
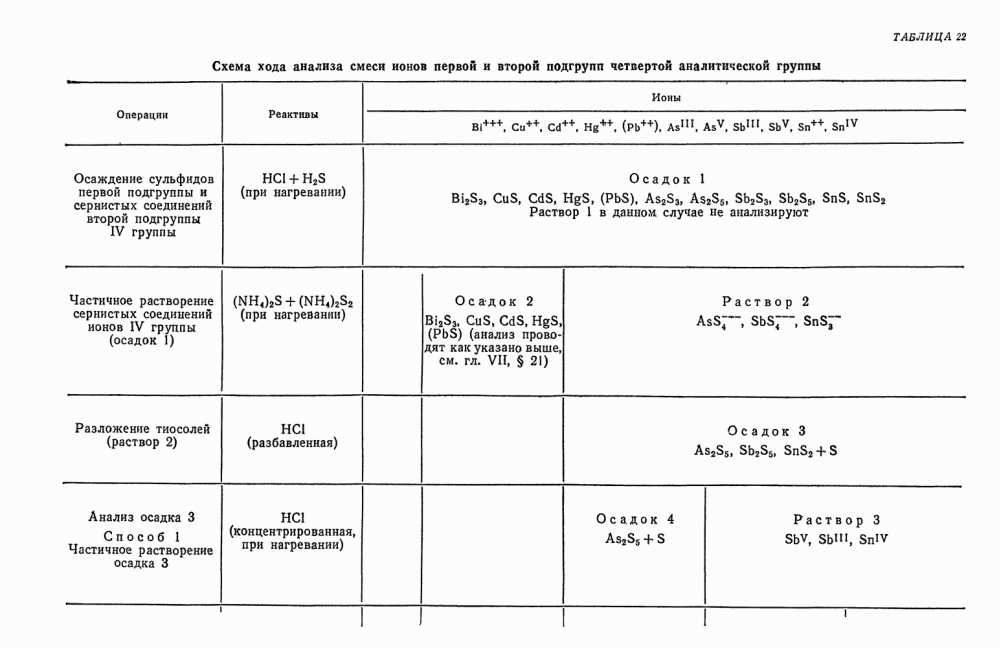
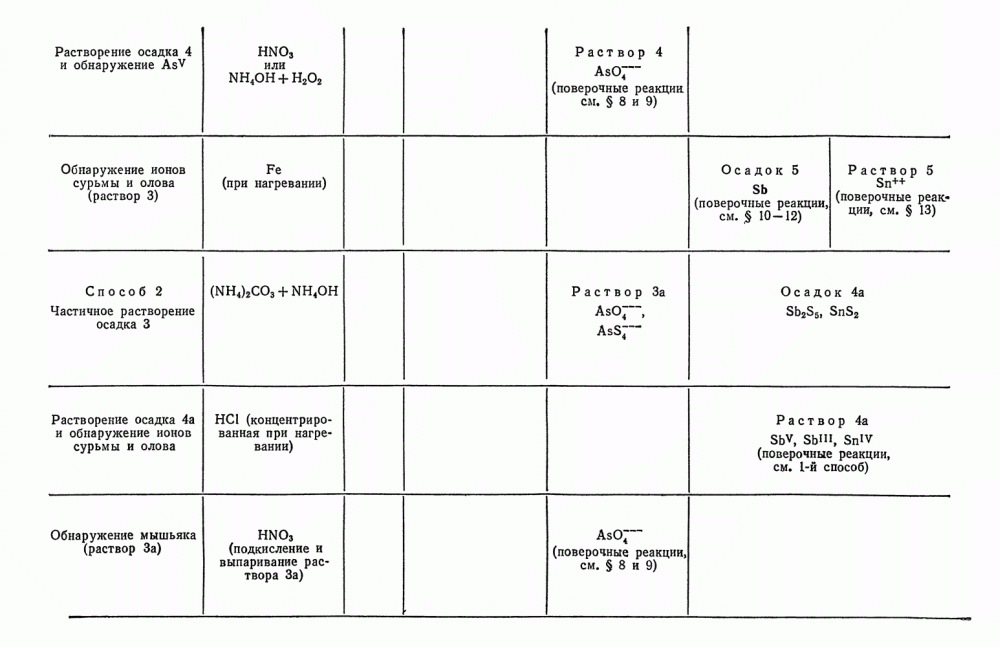
- § 14. Анализ смеси ионов
- § 15. Анализ смеси ионов
- ГЛАВА V. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика второй аналитической группы катионов
- § 2. Общие реакции катионов второй аналитической группы
- § 3. Обнаружение Ca-ионов
- § 4. Обнаружение Sr-ионов
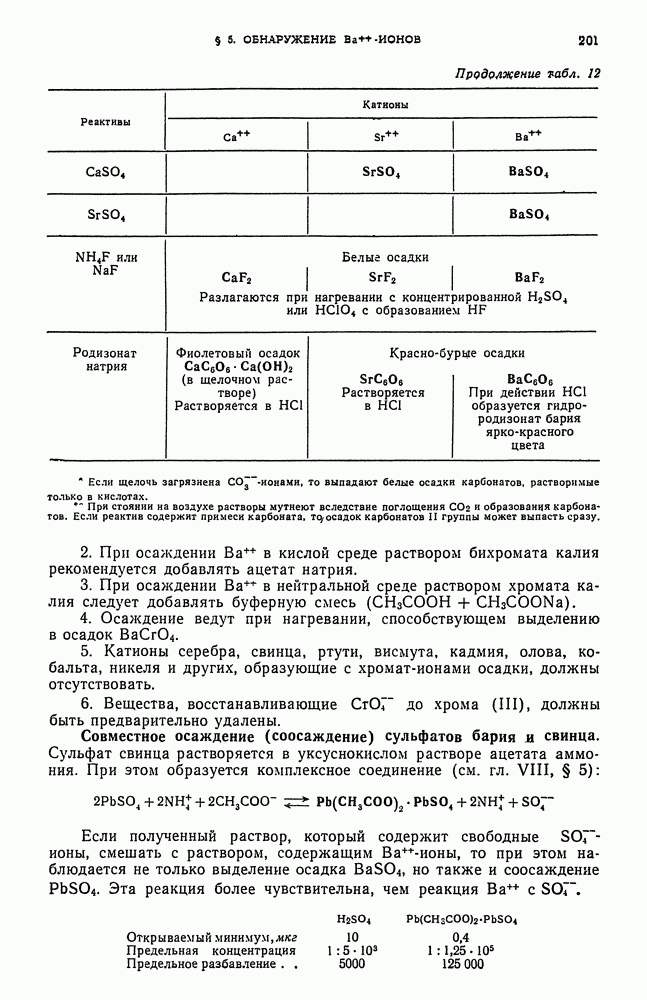
- § 5. Обнаружение Ba-ионов
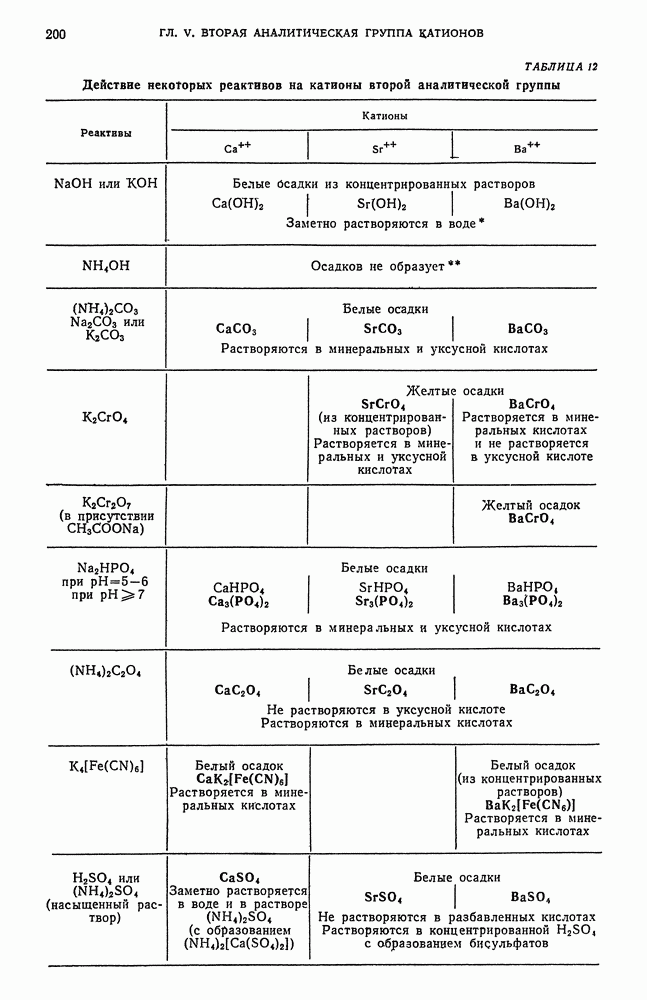
- § 6. Обзор действия реактивов на катионы второй аналитической группы
- § 7. Основы теории осаждения катионов второй аналитической группы групповым реактивом—карбонатом аммония
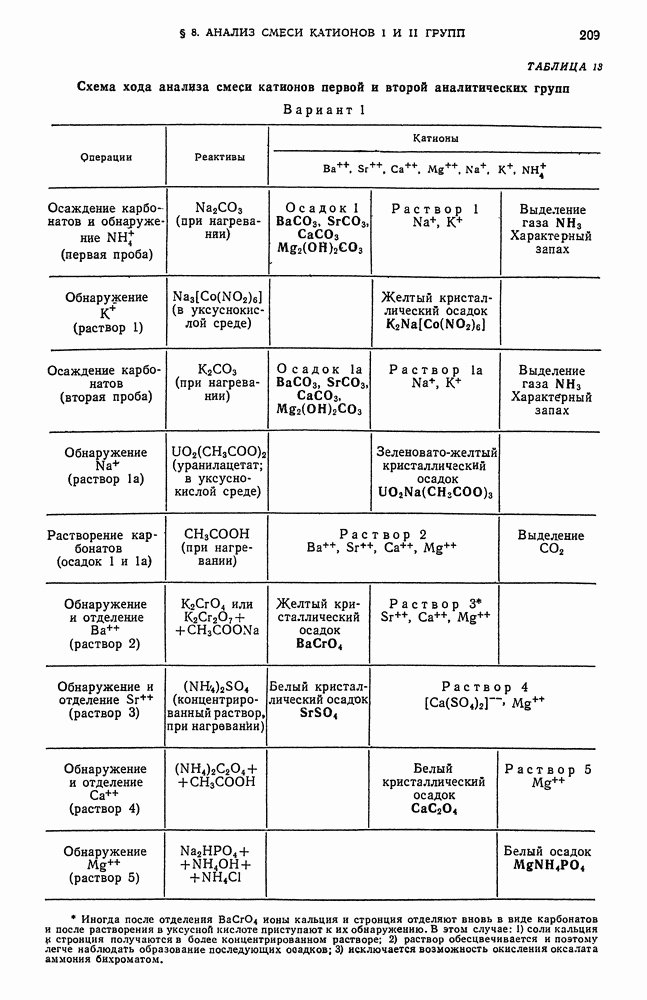
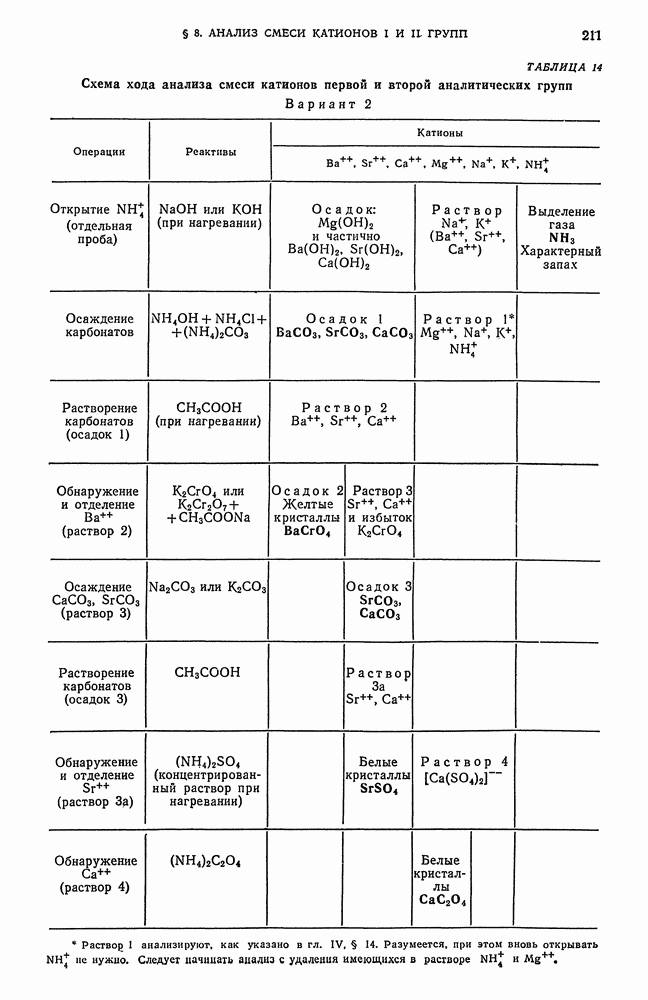
- § 8. Систематический ход анализа смеси катионов первой и второй аналитических групп
- § 9. Систематический ход анализа смеси катионов первой и второй аналитических групп в присутствии ионов
- § 10. Теоретические основы перевода сульфатов катионов второй аналитической группы в карбонаты
- ГЛАВА VI. ТРЕТЬЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика третьей аналитической группы катионов
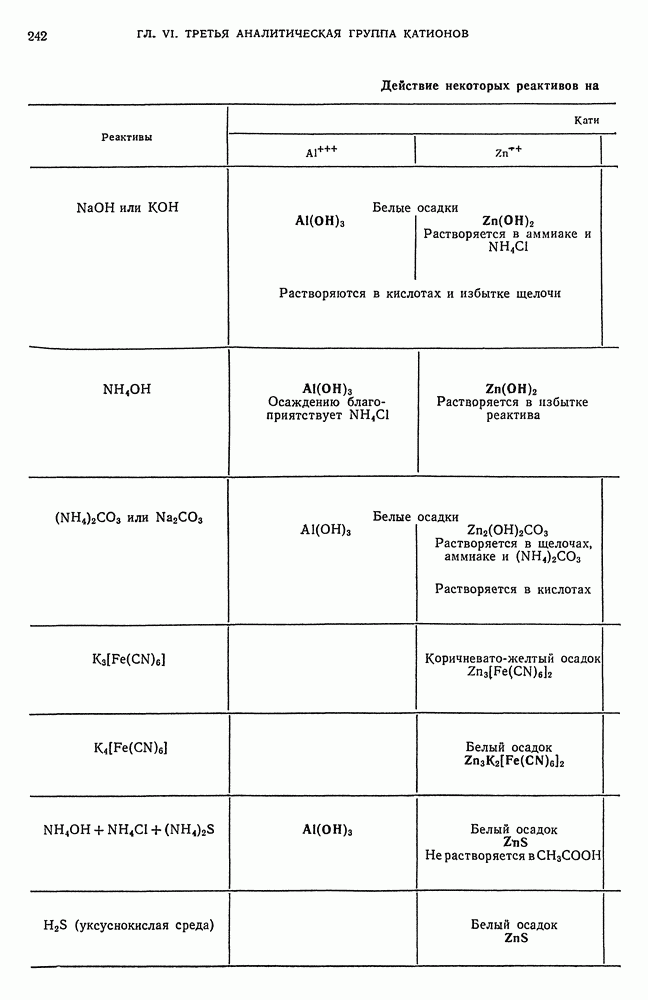
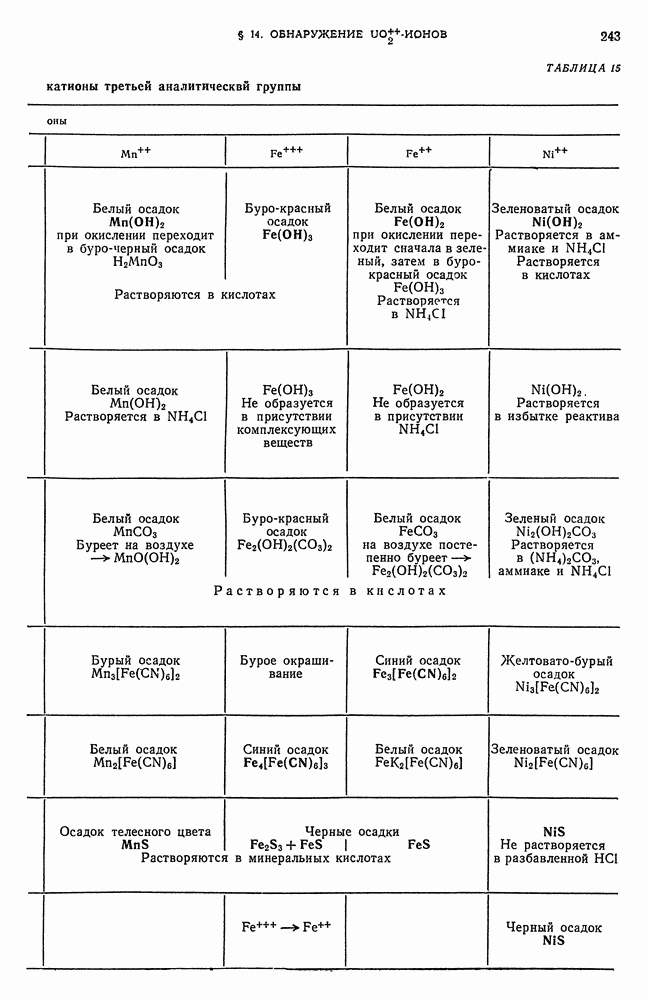
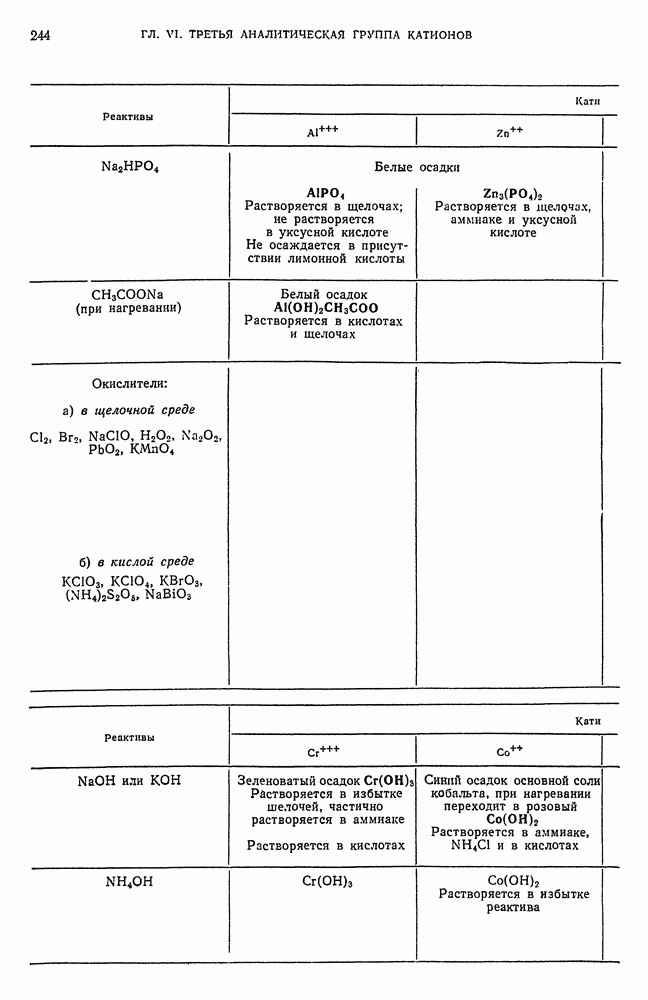
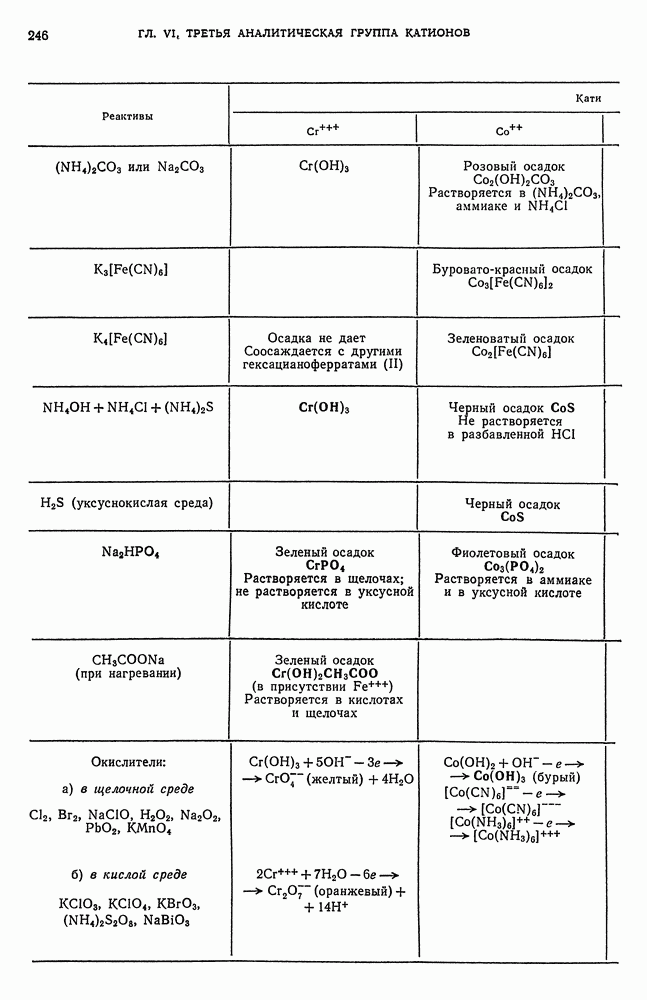
- § 2. Общие реакции катионов третьей аналитической группы
- § 3. Обнаружение Be-ионов
- § 4. Обнаружение Al-ионов
- § 5. Обнаружение ионов титана (IV)
- § 6. Обнаружение Cr-ионов
- § 7. Обнаружение Mn-ионов
- § 8. Обнаружение Fe-ионов
- § 9. Обнаружение Fe-ионов
- § 10. Обнаружение Co-ионов
- § 13. Обнаружение ионов циркония (IV)
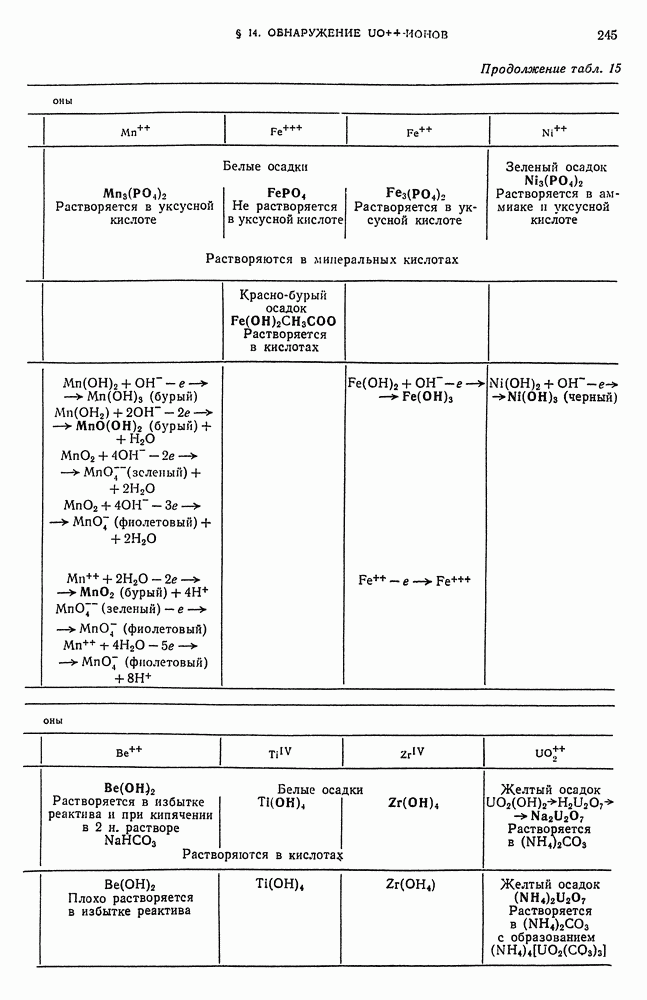
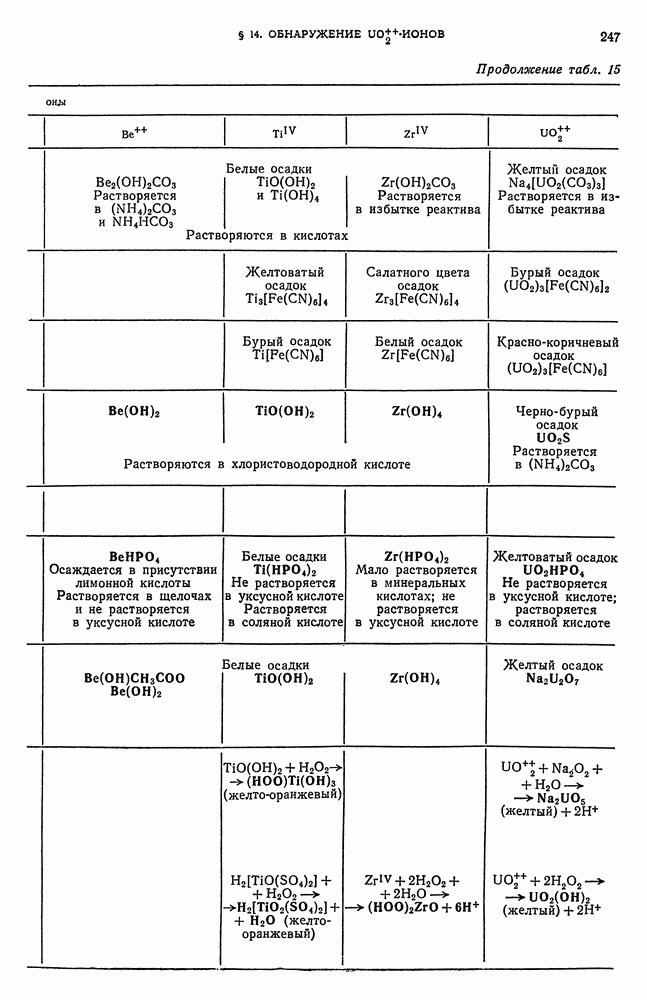
- § 14. Обнаружение UO-ионов
- § 15. Обзор действия реактивов на катионы третьей аналитической группы
- § 16. Использование коллоидных систем в химическом анализе
- § 17. Основы теории осаждения катионов третьей аналитической группы групповым реактивом — сульфидом аммония
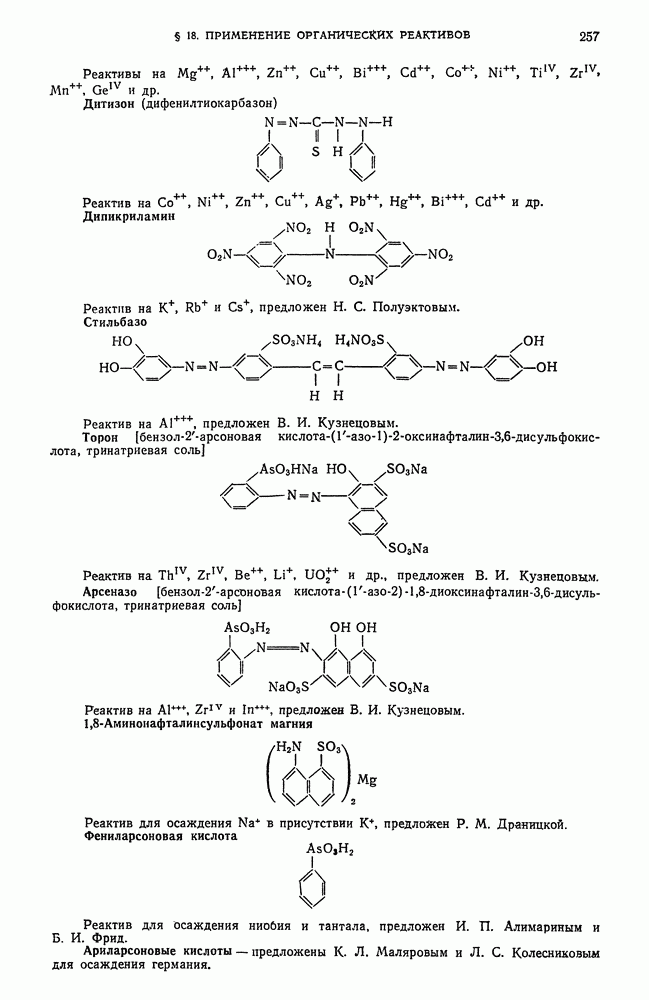
- § 18. Теоретические основы применения органических реактивов в качественном анализе неорганических веществ
- § 19. Методы разделения некоторых катионов третьей аналитической группы
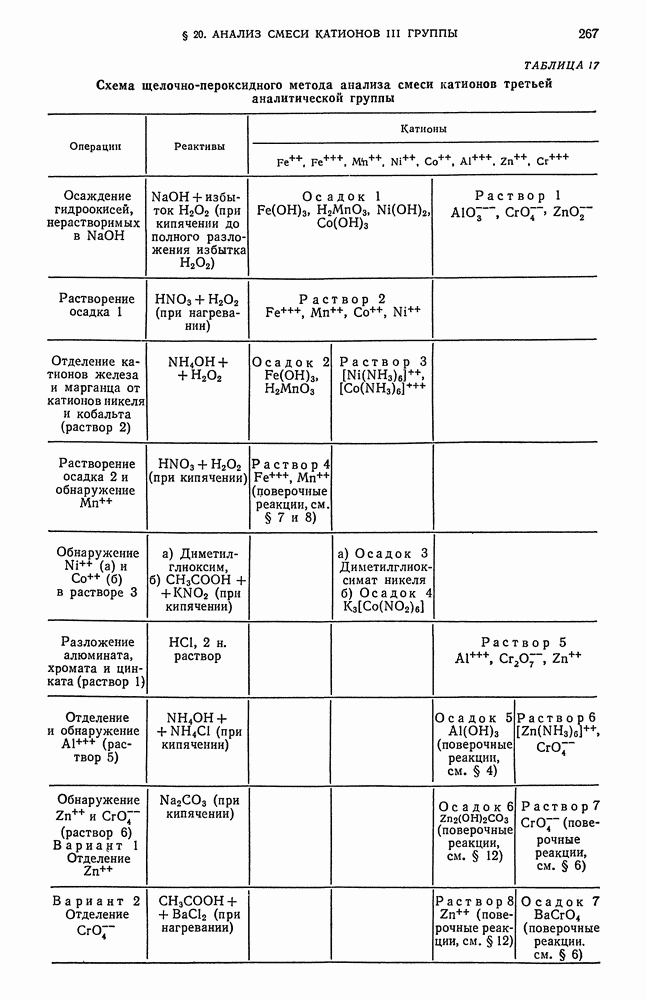
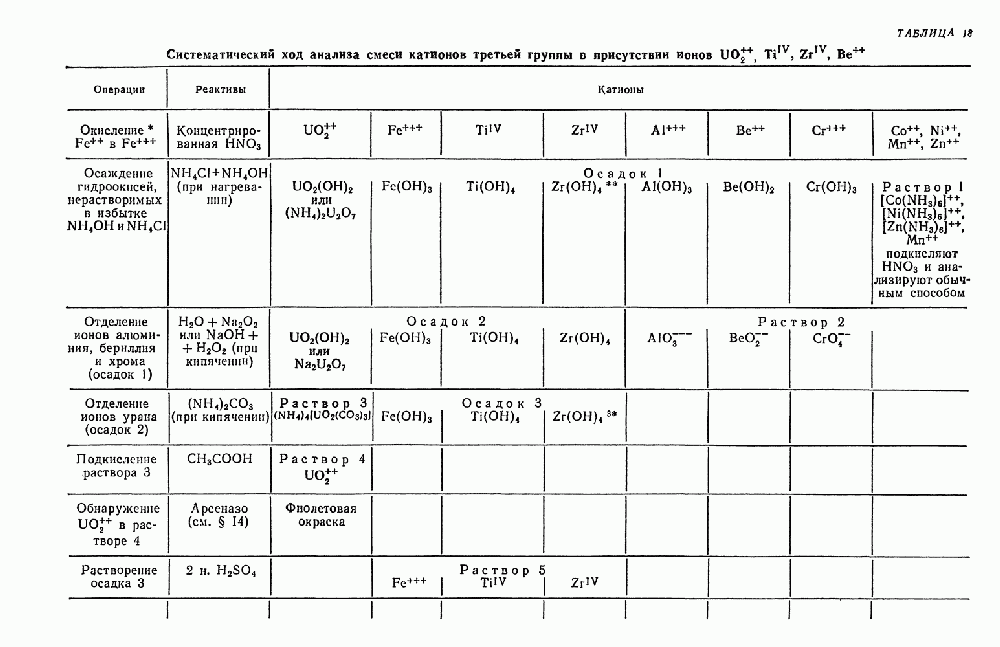
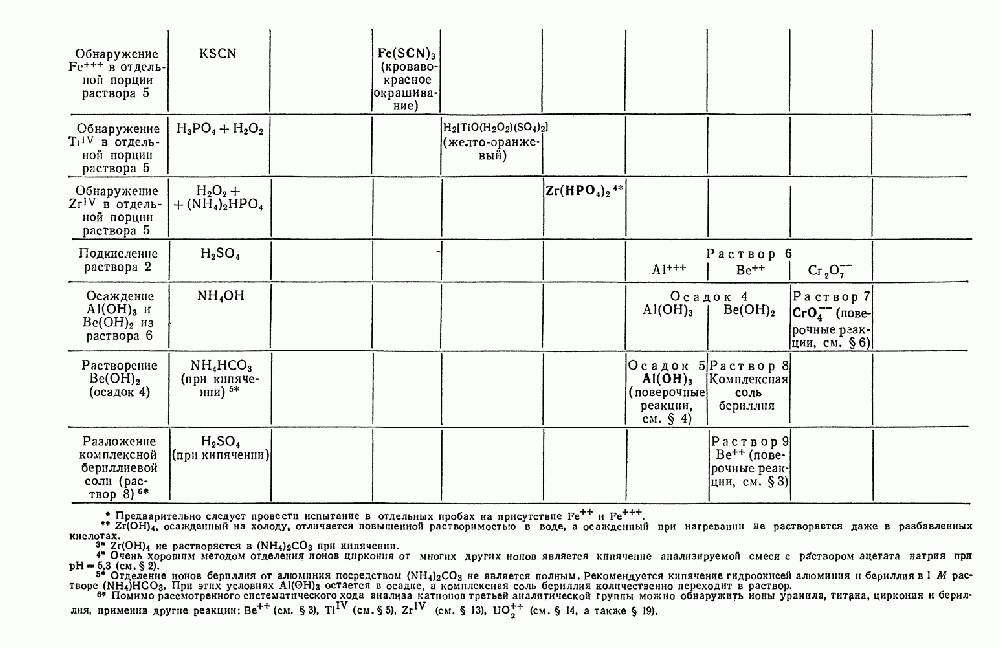
- § 20. Систематический ход анализа смеси катионов третьей аналитической группы
- § 21. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп
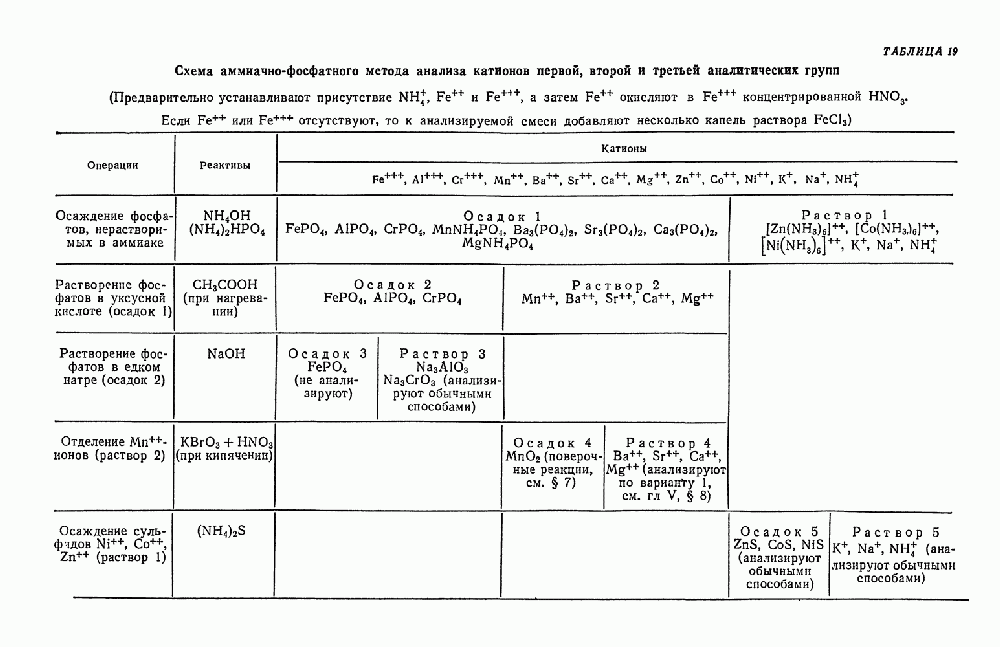
- § 22. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп в присутствии PO-ионов
- ГЛАВА VII. ЧЕТВЕРТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика четвертой аналитической группы катионов
- § 2. Общие реакции катионов четвертой аналитической группы
- РЕАКЦИИ КАТИОНОВ ПЕРВОЙ ПОДГРУППЫ (ПОДГРУППЫ МЕДИ)
- § 3. Обнаружение Hg-ионов
- § 4. Обнаружение Cu-ионов
- § 5. Обнаружение Cd-ионов
- § 6. Обнаружение Bi-ионов
- РЕАКЦИИ КАТИОНОВ ВТОРОЙ ПОДГРУППЫ (ПОДГРУППЫ МЫШЬЯКА)
- § 7. Обнаружение ионов мышьяка (III)
- § 8. Обнаружение ионов мышьяка (V)
- § 9. Общие реакции обнаружения
- § 10. Обнаружение ионов сурьмы (III)
- § 11. Обнаружение ионов сурьмы (V)
- § 12. Общие реакции обнаружения Sb
- § 13. Обнаружение ионов олова (II)
- § 14. Обнаружение ионов олова (IV)
- § 15. Общие реакции обнаружения ионов олова (II) и олова (IV)
- § 16. Отделение ионов олова от других ирнов четвертой аналитической группы
- § 17. Обнаружение ионов германия (IV)
- § 18. Отделение ионов германия от других ионов четвертой аналитической группы
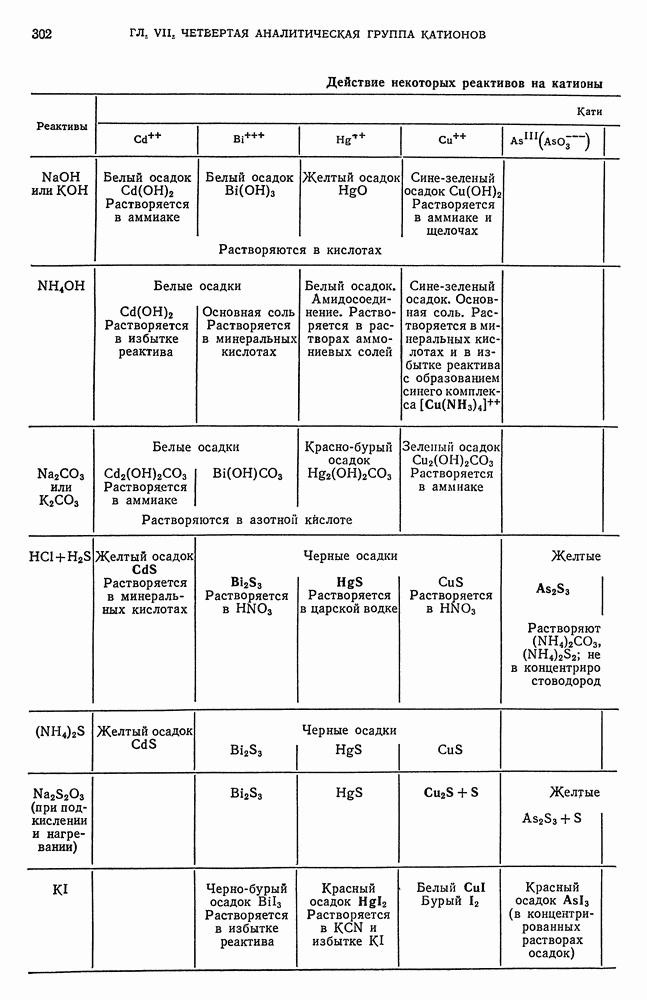
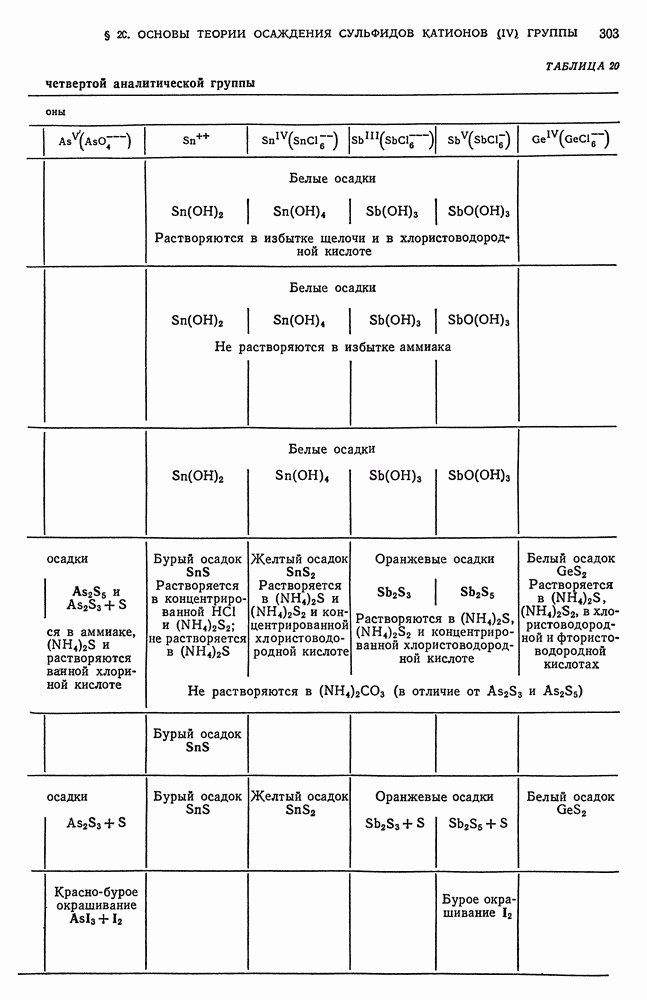
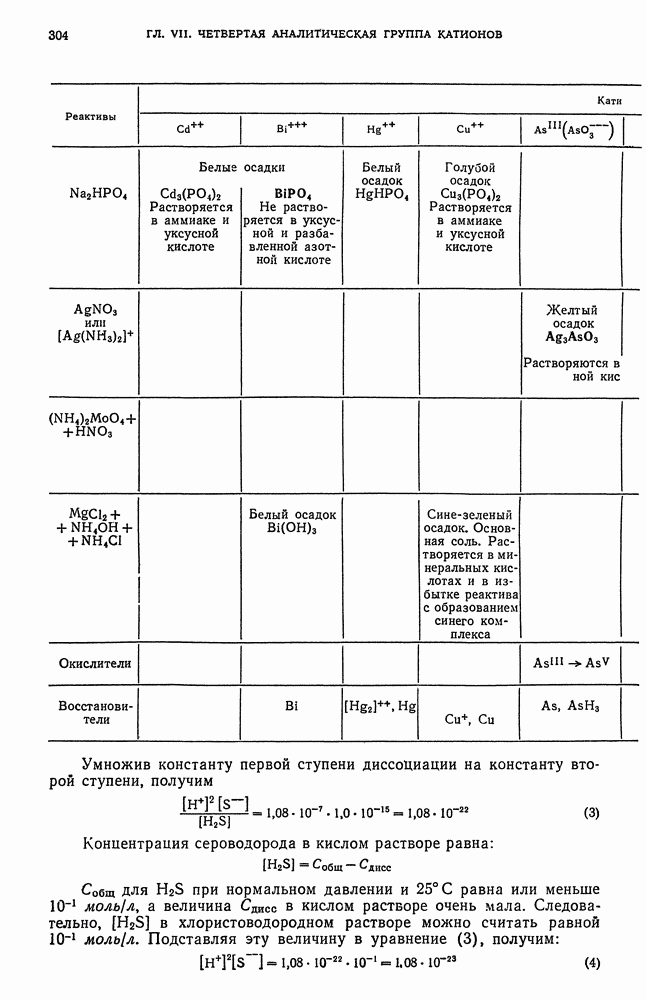
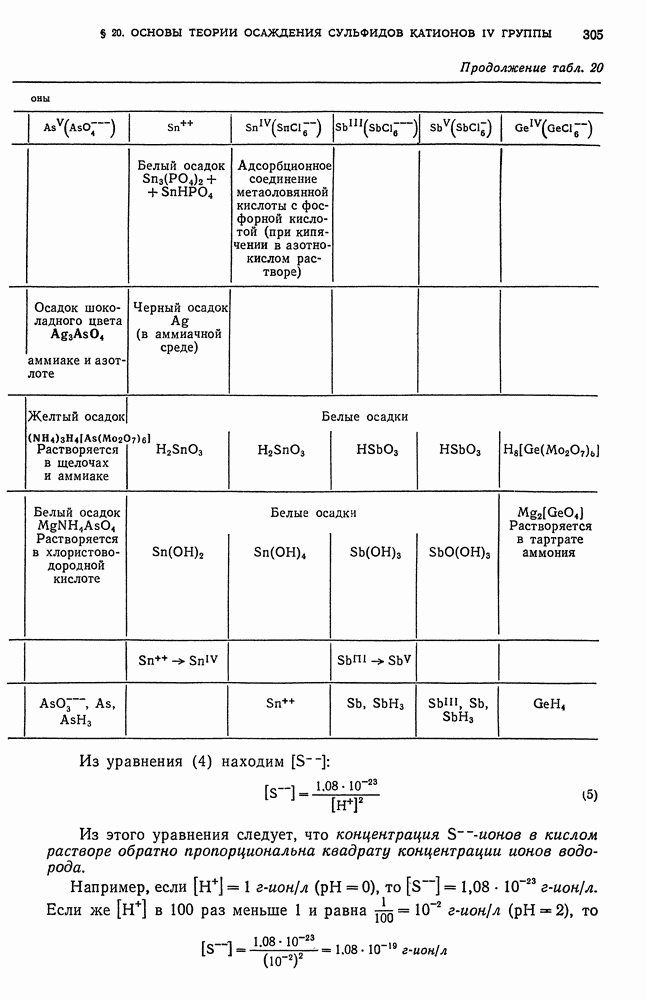
- § 19. Обзор действия реактивов на катионы четвертой аналитической группы
- § 20. Основы теории осаждения сульфидов катионов четвертой аналитической группы групповым реактивом — сероводородом
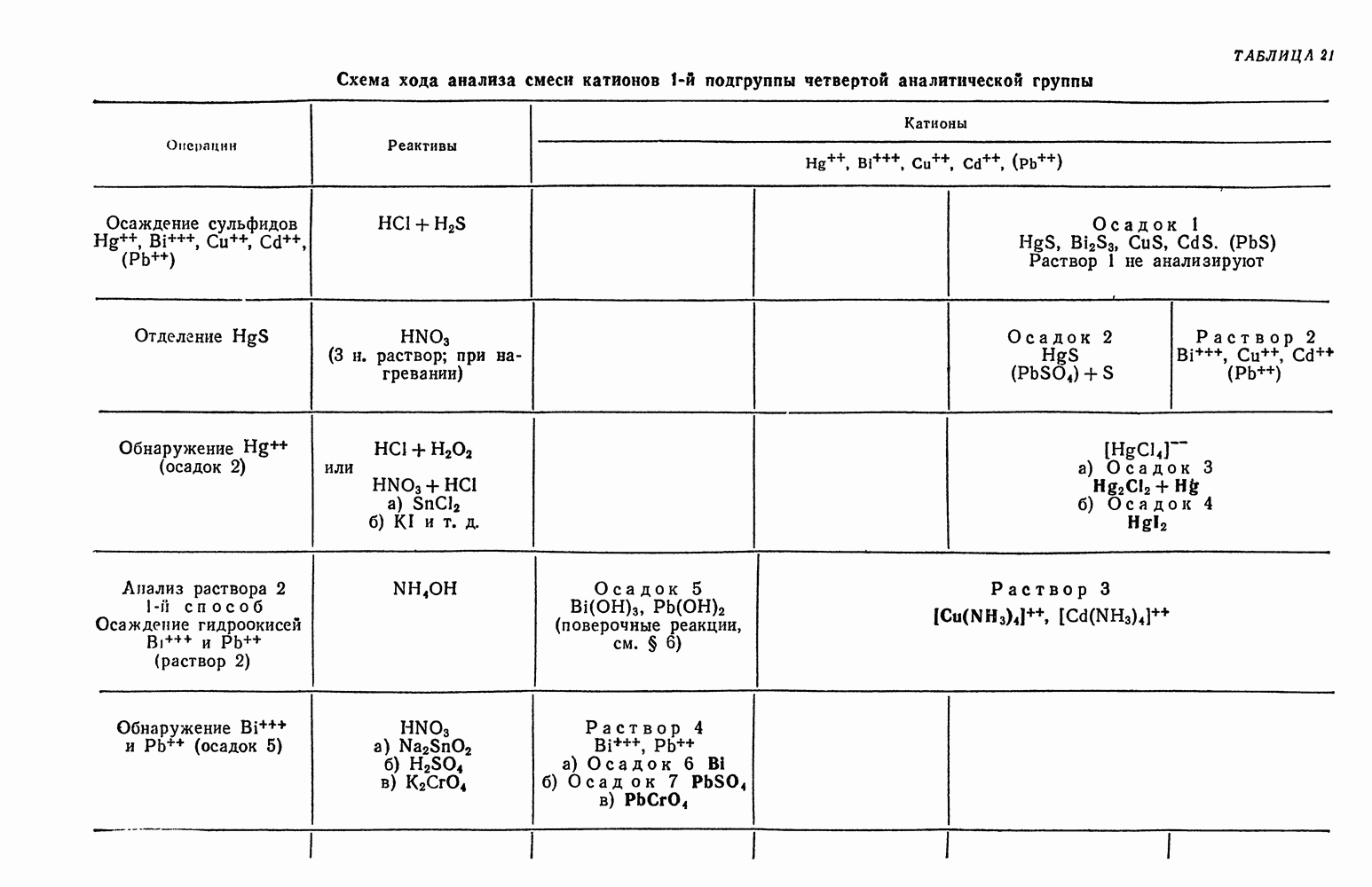
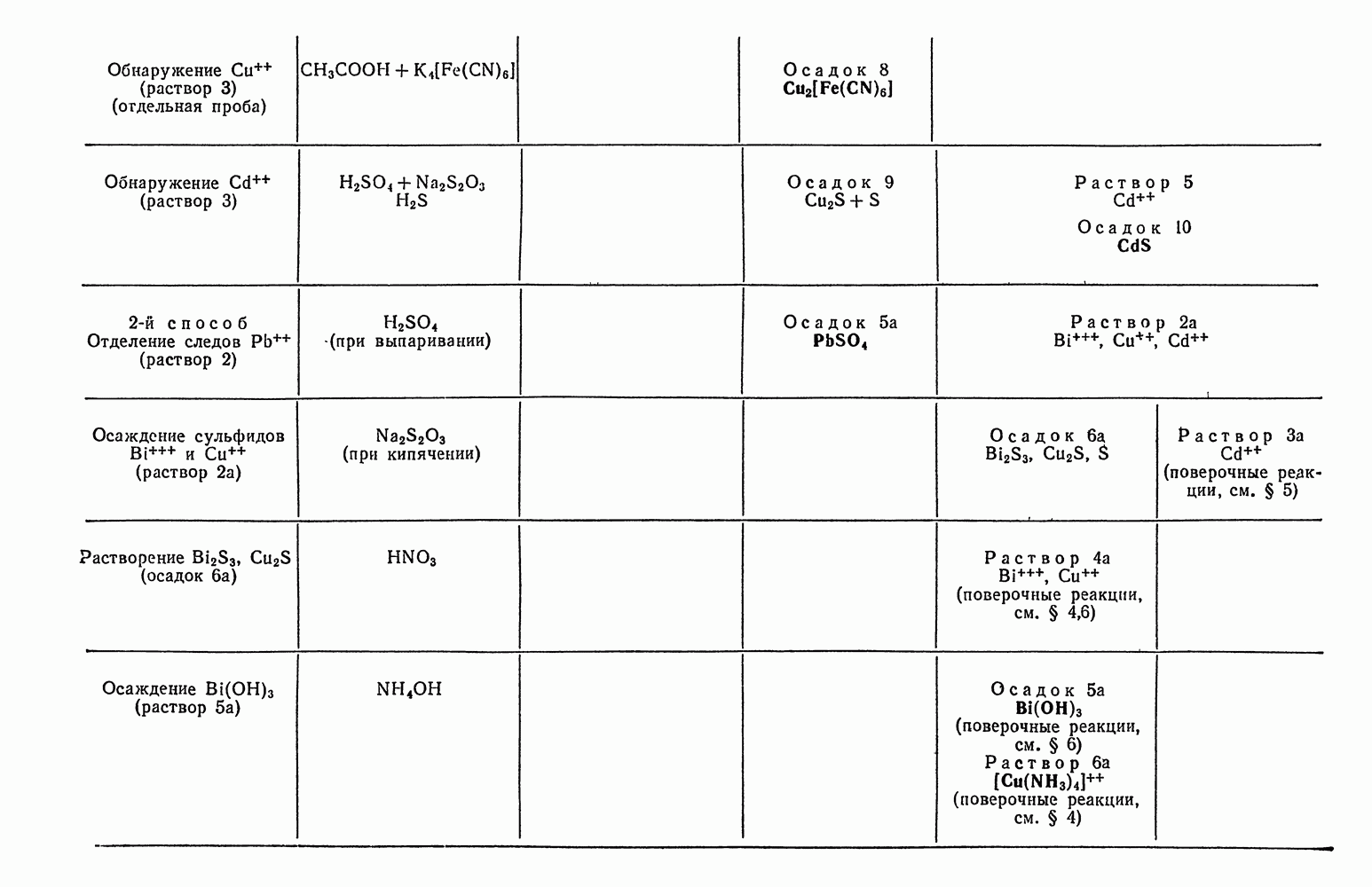
- § 21. Систематический ход анализа смеси катионов четвертой аналитической группы
- ГЛАВА VIII. ПЯТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ (ГРУППА СЕРЕБРА)
- § 1. Характеристика пятой аналитической группы катионов
- § 2. Общие реакции катионов пятой аналитической группы
- § 3. Обнаружение Ag-ионов
- § 4. Обнаружение [Hg]-ионов
- § 5. Обнаружение Pb-ионов
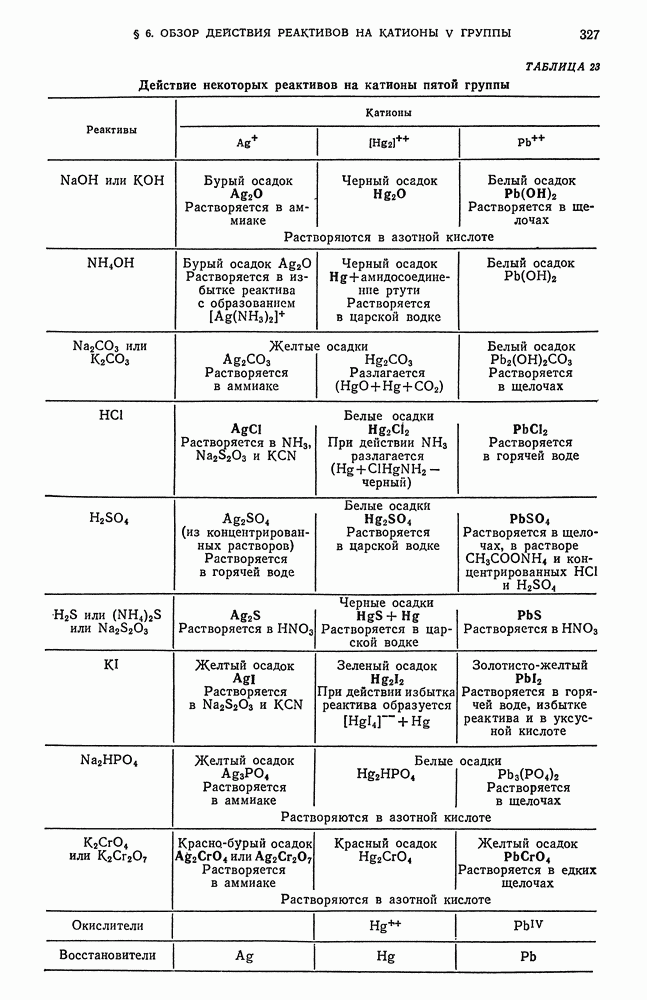
- § 6. Обзор действия реактивов на катионы пятой аналитической группы
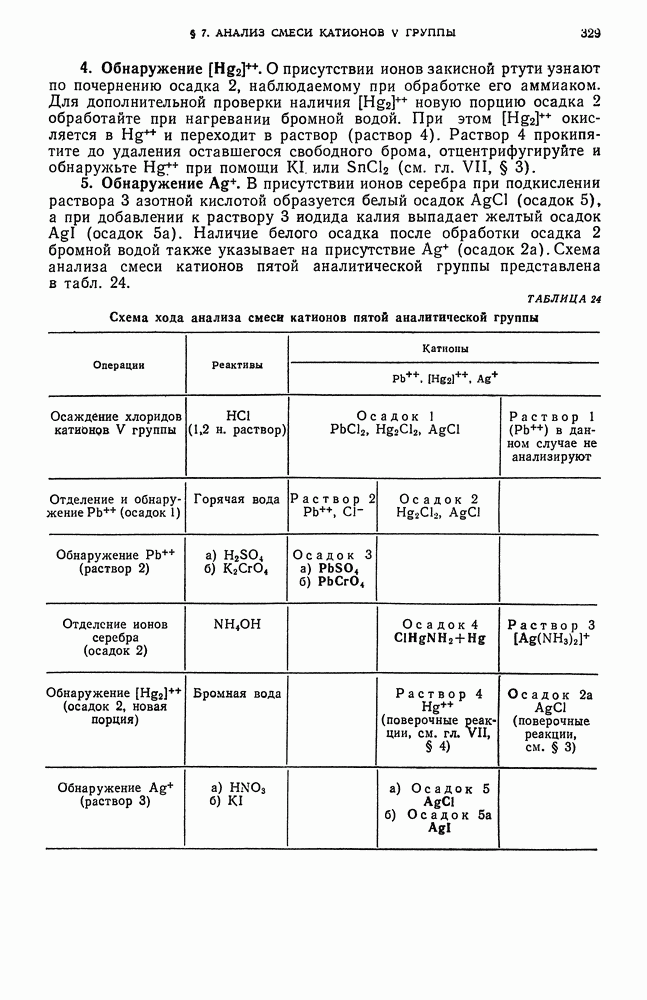
- § 7. Систематический ход анализа смеси катионов пятой аналитической группы
- ГЛАВА IX. АНАЛИЗ СМЕСИ ИОНОВ ВСЕХ ПЯТИ АНАЛИТИЧЕСКИХ ГРУПП
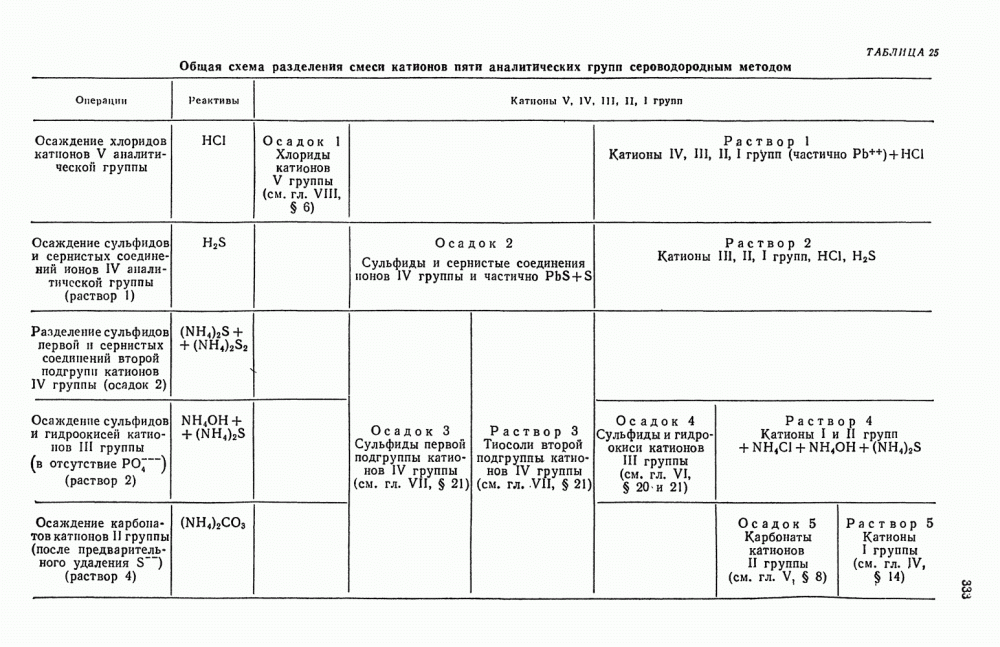
- § 1. Сероводородный метод анализа
- § 2. Недостатки сероводородного метода анализа
- § 3. Ошибки, возникающие при анализе смеси ионов пяти аналитических групп
- § 4. Бессероводородные методы анализа
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ АНИОНОВ И АНАЛИЗ СМЕСЕЙ АНИОНОВ
- § 1. Аналитическая классификация анионов
- § 2. Групповые реактивы на анионы
- § 3. Классификация методов анализа анионов
- ГЛАВА XI. ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика первой группы анионов
- § 2. Реакции анионов первой группы
- § 3. Обнаружение CI-ионов
- § 4. Обнаружение Br-ионов
- § 5. Обнаружение I-ионов
- § 6. Обнаружение CN-ионов
- § 7. Обнаружение SCN-ионов
- § 8. Обнаружение [Fe(CN)]-ионов
- § 9. Обнаружение Fe(CN)-ионов
- § 10. Обнаружение NO-ионов
- § 11. Обнаружение NO2-ионов
- § 12. Обнаружение S-ионов
- § 13. Обнаружение CH3COOO-ионов
- § 14. Обнаружение BrO3-ионов
- § 15. Обнаружение ClO3-ионов
- § 16. Обнаружение ClO4-ионов
- § 17. Обзор действия реактивов на анионы первой группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 18. Анализ смеси Cl, Br и I-ионов
- § 19. Анализ смеси Cl, Br, I и SCN-ионов
- § 20. Анализ смеси Cl, ClO3 и ClO4-ионов
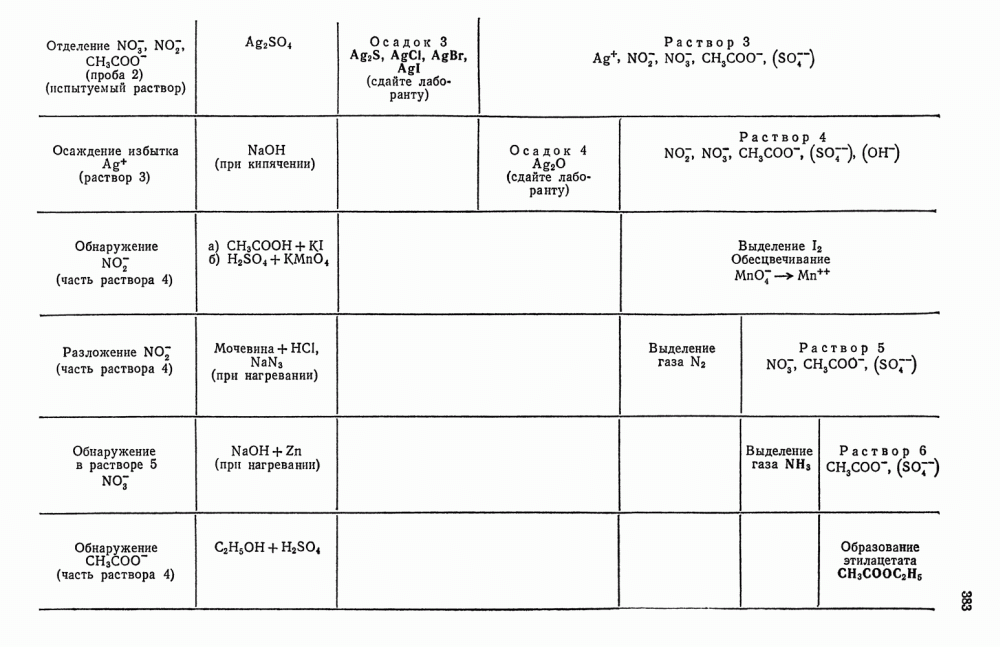
- § 21. Анализ смеси NO2 и NO3-ионов
- § 22. Анализ смеси анионов первой группы
- ГЛАВА XII. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика второй группы анионов
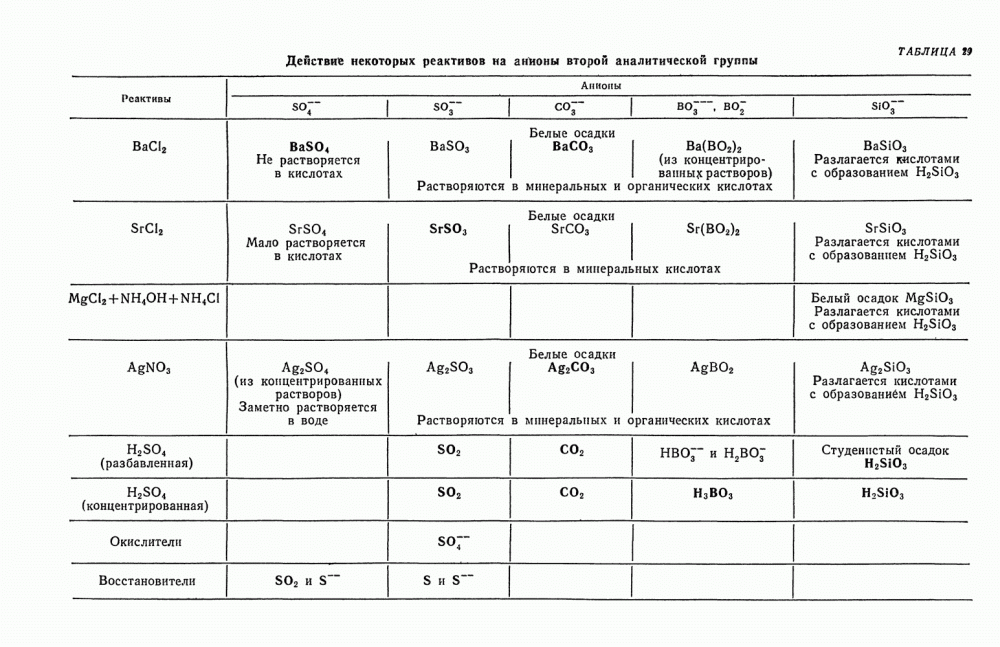
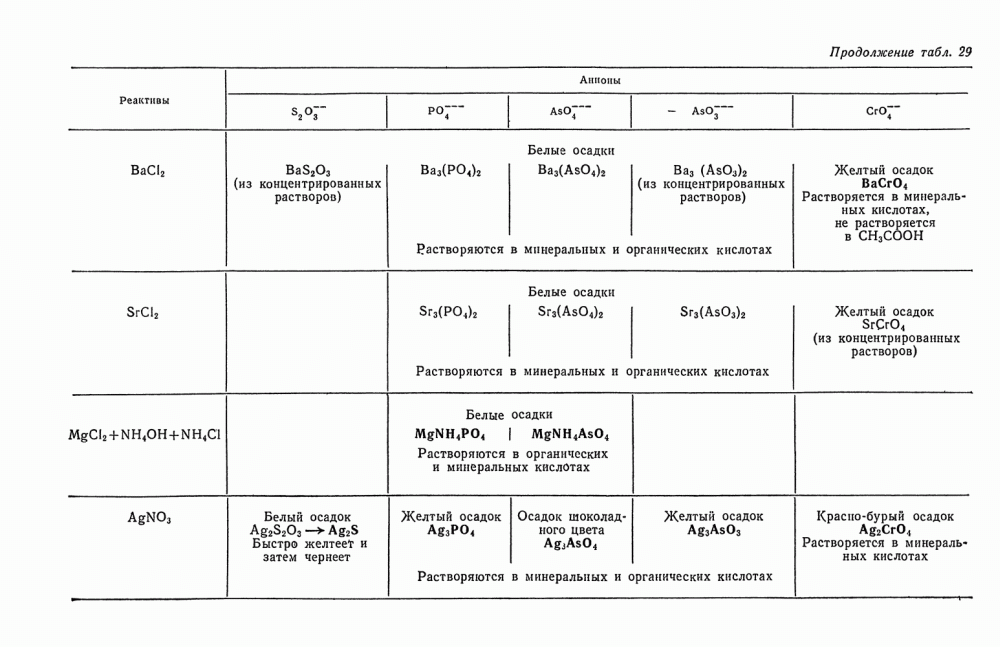
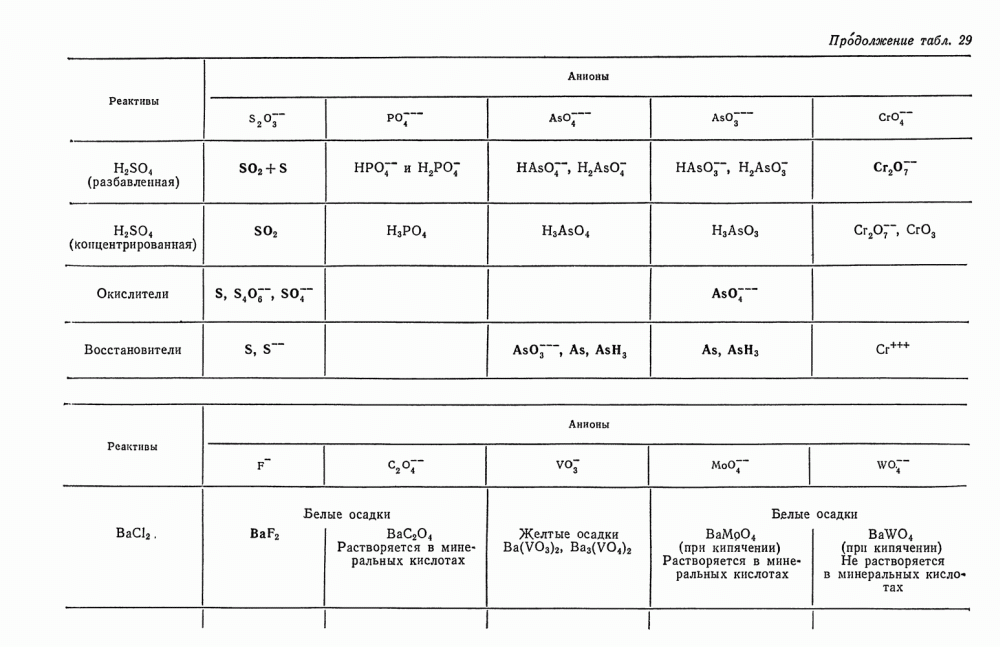
- § 2. Общие реакции анионов второй группы
- § 3. Обнаружение SO3-ионов
- § 4. Обнаружение S2O3-ионов
- § 5. Обнаружение S2O3 в присутствии SO3-ионов
- § 6. Обнаружение SO4-ионов
- § 7. Обнаружение CO3-ионов
- § 8. Обнаружение CO3-ионов в присутствии SO3 и S2O3-ионов
- § 9. Обнаружение PO4-ионов
- § 10. Обнаружение CrO4-ионов
- § 11. Обнаружение AsO3-ионов
- § 12. Обнаружение AsO4-ионов
- § 13. Обнаружение BO2 и BO3-ионов
- § 14. Обнаружение SiO3-ионов
- § 15. Обнаружение F-ионов
- § 16. Обнаружение C2O4-ионов
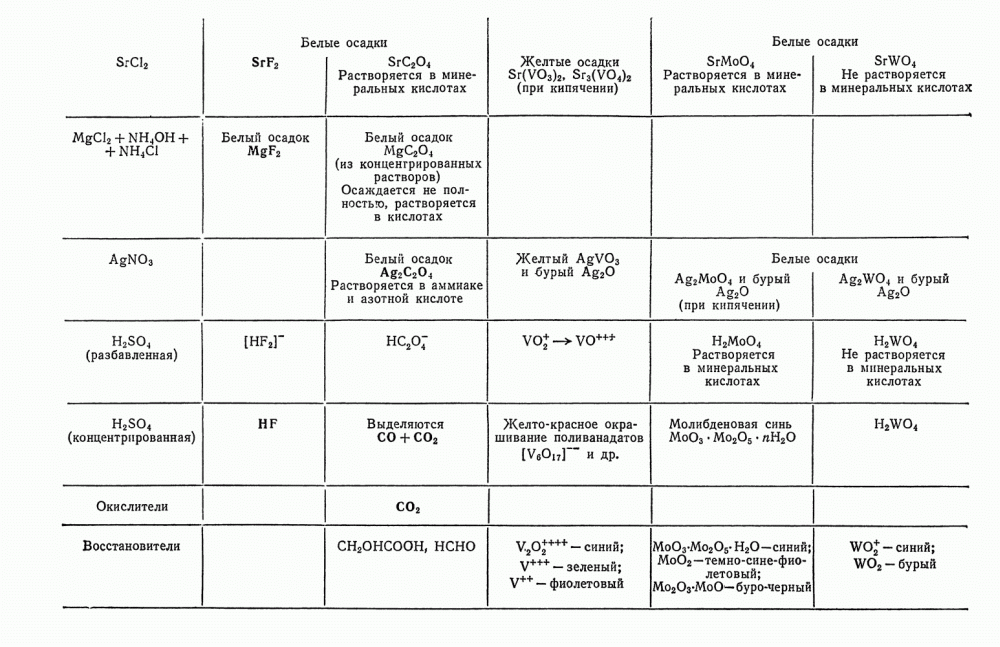
- § 17. Обнаружение VO3-ионов
- § 18. Обнаружение MoO4-ионов
- § 19. Обнаружение WO4-ионов
- § 20. Обзор действия реактивов на анионы второй группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 21. Анализ смеси ионов
- § 22. Анализ смеси SO3, SO4, S2O3 и CO3-ионов
- § 23. Анализ смеси VO2, MoO4 и WO4-ионов
- § 24. Анализ смеси анионов второй группы
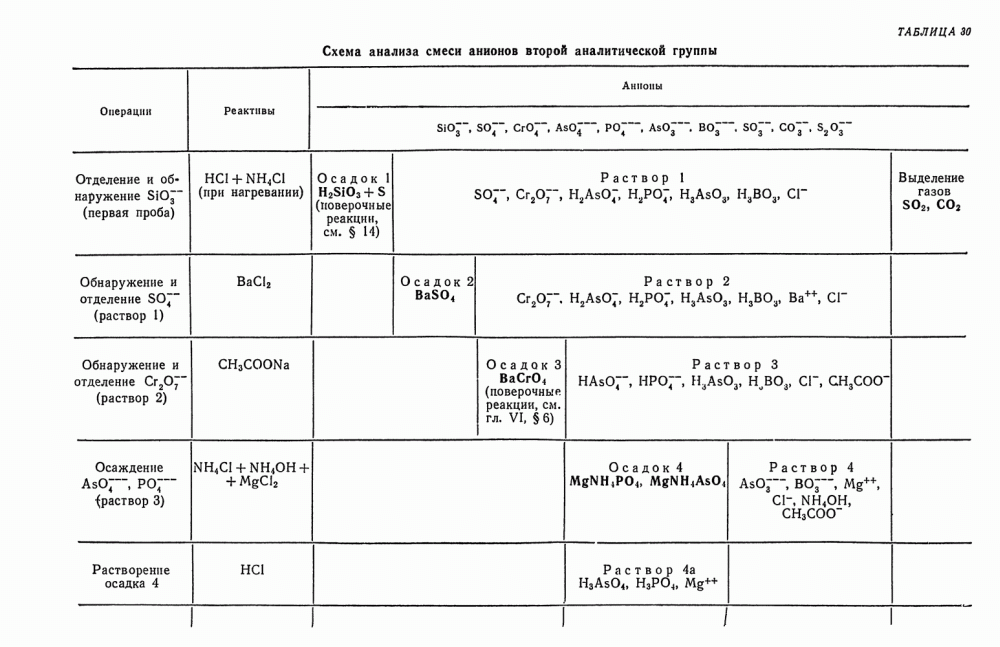
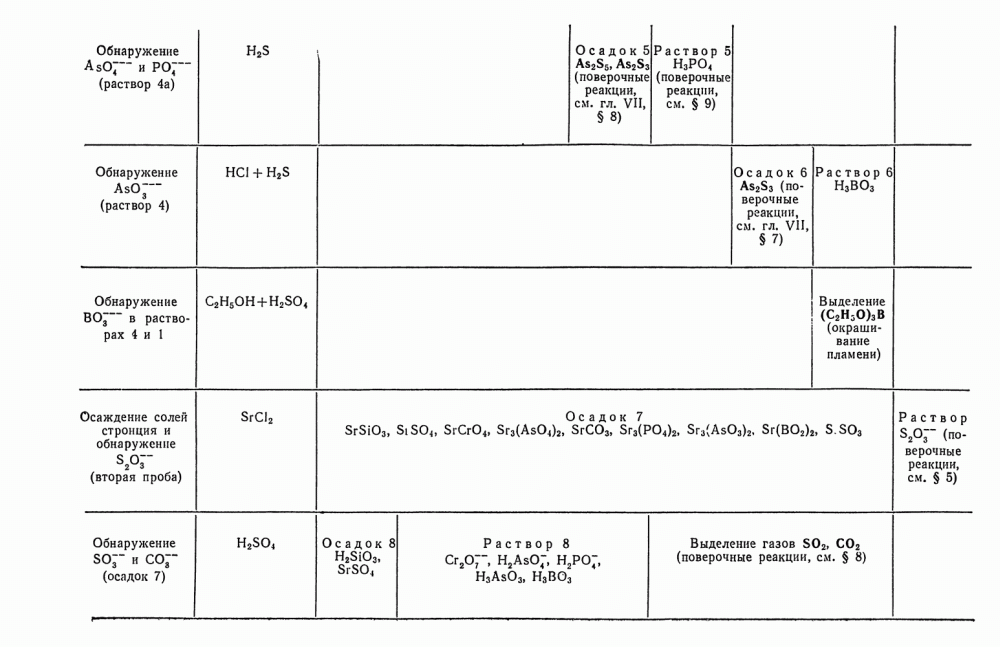
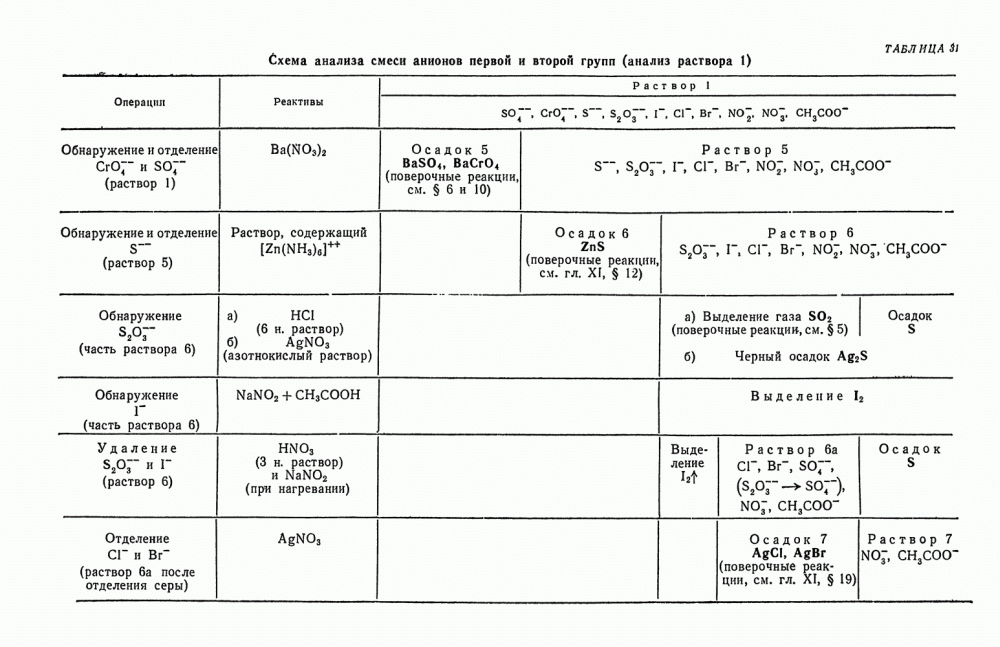
- § 25. Анализ смеси анионов первой и второй групп
- ГЛАВА XIII. ОБНАРУЖЕНИЕ СВОБОДНЫХ МЕТАЛЛОВ И НЕМЕТАЛЛОВ, ИДЕНТИФИЦИРОВАНИЕ СОЛЕЙ И ДРУГИХ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И АНАЛИЗ ИХ СМЕСЕЙ
- § 1. Подготовка вещества к анализу
- § 2. Предварительные испытания
- § 3. Растворение анализируемого вещества в воде, кислотах и щелочах
- § 4. Переведение в растворимое состояние веществ, нерастворимых в воде, кислотах и щелочах
- § 5. Анализ неизвестного вещества
- § 6. Обнаружение свободных элементов
- § 7. Идентифицирование солей и других индивидуальных соединений
- § 8. Обнаружение микропримесей
- § 9. Анализ сплавов
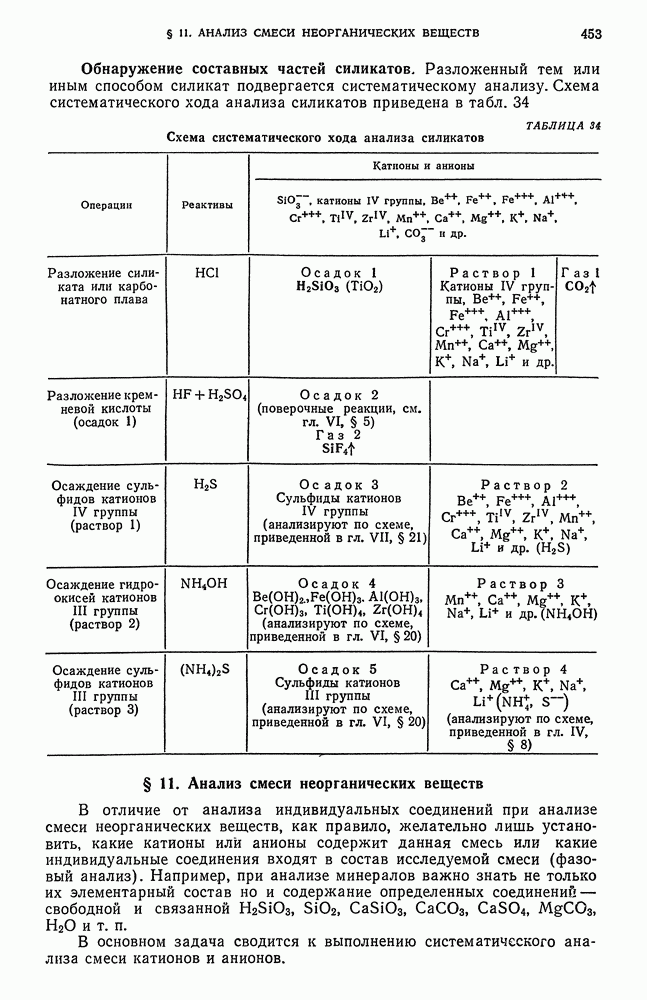
- § 10. Анализ силикатов и алюмосиликатов
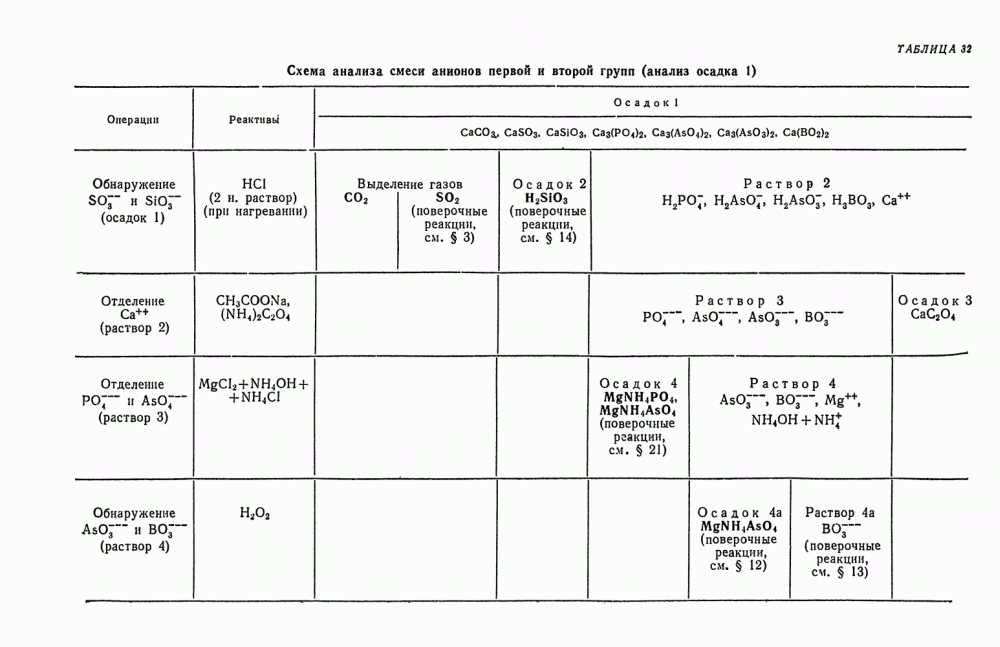
- § 11. Анализ смеси неорганических веществ
- § 12. Экспрессный метод анализа смесей катионов и анионов
- § 13. Идентифицирование нерастворимых веществ
- ЛИТЕРАТУРА