| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
§ 12. Специфичность и чувствительность реакций
Специфичные реакции. В качественном анализе практическое значение имеют не все химические реакции. Особенное значение в качественном анализе имеют специфичные реакции.
Специфичными реакциями (или реактивами) называют реакции (или реактивы), при помощи которых можно в определенных условиях обнаруживать одни ионы в присутствии других ионов по специфическому изменению цвета, образованию характерного осадка, выделению газа и т. п. Например, при действии роданида аммония на соли кобальта образуются соединения, окрашенные в ярко-синий цвет, а при действии того же реактива на соли железа (III) образуются соединения, окрашенные в красный цвет. Ионы никеля можно обнаружить по образованию розово-красного осадка при добавлении диметилглиоксима и др.
Чувствительность реакции. Чувствительность реакции определяется наименьшим количеством искомого вещества, которое может быть обнаружено данным реактивом в капле раствора  .
.
Чувствительность реакции выражают рядом взаимно связанных величин: открываемым минимумом, минимальной (предельной) концентрацией, предельным разбавлением.
Открываемым минимумом называют наименьшее количество вещества, содержащееся в исследуемом растворе и открываемое данным реактивом при определенных условиях выполнения реакции. Величина открываемого минимума обычно очень мала, она составляет миллионные доли грамма (0,000001 г или  ). Например, открываемый минимум
). Например, открываемый минимум  ионов, осаждаемых платинохлористоводородной кислотой в виде
ионов, осаждаемых платинохлористоводородной кислотой в виде  в одной капле (объемом
в одной капле (объемом  ) анализируемого предельно разбавленного раствора равен
) анализируемого предельно разбавленного раствора равен  .
.
Минимальная (предельная) концентрация показывает, при какой наименьшей концентрации раствора данная реакция позволяет еще однозначно открывать обнаруживаемое вещество в небольшой порции (обычно в одной капле) анализируемого раствора.
Например, предельная концентрация  , осаждаемого в виде желтого кристаллического осадка
, осаждаемого в виде желтого кристаллического осадка  из одной капли анализируемого раствора (объемом
из одной капли анализируемого раствора (объемом  ), равна
), равна  000. Это означает, что
000. Это означает, что  еще можно обнаружить в виде
еще можно обнаружить в виде  в водном растворе, содержащем 1 г
в водном растворе, содержащем 1 г  . Но если предельная концентрация
. Но если предельная концентрация  меньше, чем
меньше, чем  то обнаружить его в виде
то обнаружить его в виде  в одной капле исследуемого раствора уже невозможно.
в одной капле исследуемого раствора уже невозможно.
Предельное разбавление выражается предельным числом миллилитров водного раствора, содержащего 1 г обнаруживаемого вещества, еще открываемого при помощи данной реакции (реактива). Это означает, что в предельно разбавленном растворе, содержащем 1 г открываемых ионов в определенном объеме, данные ионы могут быть обнаружены с помощью избранного реактива в одной капле исследуемого раствора.
Например, предельное разбавление, допускаемое при обнаружении  в виде
в виде  из одной капли раствора, равно 10000, т. е. объем раствора, содержащего 1 г ионов калия, не может быть разбавлен в этом случае свыше, чем до
из одной капли раствора, равно 10000, т. е. объем раствора, содержащего 1 г ионов калия, не может быть разбавлен в этом случае свыше, чем до  .
.
Предельное разбавление есть величина, обратная предельной концентрации.
Другими словами, возможность обнаружения того или иного вещества ограничена концентрацией его раствора. Лучшей аналитической реакцией следует считать такую, которая дает возможность обнаруживать не абсолютно малые, а относительно малые количества вещества.
Величина предельного разбавления увеличивается по мере увеличения чувствительности реакции. Очень удобно выражать чувствительность реакции с помощью логарифмов величин предельного разбавления. Для двух сравниваемых реакций, отличающихся друг от друга различными величинами предельного разбавления (10000 и 100000), логарифмы их величин предельного разбавления соответственно равны 4 и 5. Это указывает, что вторая реакция более чувствительна, чем первая.
Следовательно, аналитическая реакция тем чувствительней, чем меньше открываемый минимум, чем меньше минимальная (предельная) концентрация анализируемого раствора, чем больше предельное разбавление.
Требуемые величины вычисляют по формулам:


где  — открываемый минимум,
— открываемый минимум,  ;
;  — минимальная (предельная) концентрация;
— минимальная (предельная) концентрация;  предельное разбавление;
предельное разбавление;  минимальный объем раствора в миллилитрах, требуемый для обнаружения открываемых ионов.
минимальный объем раствора в миллилитрах, требуемый для обнаружения открываемых ионов.
Пример 1. Вычислить минимальный объем раствора, требуемый для обнаружения  -ионоа в виде желтого кристаллического осадка
-ионоа в виде желтого кристаллического осадка  Открываемый минимум
Открываемый минимум  этим путем равен
этим путем равен  предельная концентрация
предельная концентрация  ; предельное разбавление 50000.
; предельное разбавление 50000.
Решение. Минимальный объем вычисляют по формуле (1):

Таким образом, для обнаружения  в виде указанного осадка необходимо
в виде указанного осадка необходимо  не менее
не менее  предельно разбавленного раствора, содержащего 1 г
предельно разбавленного раствора, содержащего 1 г  .
.
Пример 2. Вычислить величины минимальной концентрации и предельного разбавления соли натрия, если известно, что открываемый минимум ионов натрия в  предельно разбавленного раствора при помощи реакции с цинк-уранилацетатом, сопровождающейся образованием зеленовато-желтого осадка
предельно разбавленного раствора при помощи реакции с цинк-уранилацетатом, сопровождающейся образованием зеленовато-желтого осадка  , равен
, равен  .
.
Решение. Предельное разбавление вычисляют по формуле (2):

Минимальную (предельную) концентрацию вычисляют по формуле (3):

Пример 3. Вычислить открываемый минимум  , осаждаемого в виде
, осаждаемого в виде  из
из  (Кмин), если известна предельная концентрация, равная
(Кмин), если известна предельная концентрация, равная  (предельное разбавление 10 000).
(предельное разбавление 10 000).
Решение. Открываемый минимум рассчитывают по формуле

Чувствительность реакйии определяется также временем, в течение которого протекает реакция. Более чувствительными считаются реакции, в которых реактив реагирует с обнаруживаемым ионом за более короткий промежуток времени.
Например  можно открыть при помощи моногидрофосфата натрия
можно открыть при помощи моногидрофосфата натрия  или карбоната натрия
или карбоната натрия  , причем с первым реактивом в аммиачной среде быстрее образуется осадок
, причем с первым реактивом в аммиачной среде быстрее образуется осадок  , чем со вторым — осадок
, чем со вторым — осадок  . Следовательно, более чувствительной из сравниваемых реакций нужно признать реакцию с
. Следовательно, более чувствительной из сравниваемых реакций нужно признать реакцию с  .
.
Ионы калия можно открыть действием платинохлористоводородной кислоты, винной кислоты или гексанитрокобальтата (III) натрия. Платинохлористоводородная кислота не осаждает хлорплатинат калия из  н. раствора
н. раствора  даже через 3 мин; при действии винной кислоты в этих же условиях осадок
даже через 3 мин; при действии винной кислоты в этих же условиях осадок  выпадает через 2 мин; гексанитрокобальтат (III) натрия реагирует тотчас же.
выпадает через 2 мин; гексанитрокобальтат (III) натрия реагирует тотчас же.
Следовательно, наиболее чувствительной является последняя реакция. Еще более чувствительна на  реакция с тетрафенилборатом натрия (см. IV, § 5).
реакция с тетрафенилборатом натрия (см. IV, § 5).
Чувствительность реакции зависит от условий ее проведения и остается постоянной только при точном соблюдении всех условий. Чувствительность реакции изменяется в присутствии посторонних веществ.
Отношение количества исследуемого вещества, которое еще может быть обнаружено в присутствии постороннего вещества, к количеству постороннего вещества, изменяющего чувствительность данной реакции, называют предельным отношением.
Интервал концентраций данного иона, в пределах которого пробы с данным реактивом дают то положительную, то отрицательную реакцию, называют областью ненадежной реакции.
Следует иметь в виду, что область ненадежной реакции сильно расширяется, если реакция проводится не при строго определенных условиях. Например, бесполезно пытаться осаждать растворимые в кислотах осадки в сильнокислой среде (при  ); растворимые в щелочах осадки — в сильнощелочной среде (при
); растворимые в щелочах осадки — в сильнощелочной среде (при  ) и т. п.
) и т. п.
Интересно отметить, что согласно исследованиям профессора Флорентийского университета Джоржио Пиккарда, самый опытный эспериментатор в самых строгих лабораторных опытах способен контролировать лишь только некоторые условия проведения реакций (температуру, давление, концентрацию реагирующих веществ,  раствора и т. п.). Все условия опыта контролировать невозможно.
раствора и т. п.). Все условия опыта контролировать невозможно.
Например, течение реакций зависит также от напряжения окружающего магнитного поля, меняющегося в зависимости от времени в соответствии с характером движения Земли в космическом пространстве.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Анализ и синтез
- § 2. Предмет аналитической химии
- § 3. Развитие аналитической химии
- § 4. Качественный и количественный анализ
- ГЛАВА I. ПРИМЕНЕНИЕ ЗАКОНА ДЕЙСТВИЯ МАСС В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Влияние среды на состояние ионов в растворах
- § 2. Обратимые и необратимые аналитические реакции
- § 3. Направление аналитических реакций; правила обменного разложения
- § 4. Закон действия масс и следствие из него
- § 5. Границы применимости закона действия масс
- § 6. Сильные и слабые электролиты
- § 7. Активность
- § 8. Коэффициент активности и ионная сила
- Б. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ (В ГОМОГЕННЫХ СИСТЕМАХ)
- § 9. Гомогенные и гетерогенные системы
- § 10. Ионное произведение воды
- § 11. Ионы гидроксония
- § 12. Равновесие ионов в водных растворах; понятие о pH
- § 13. Равновесие в водных растворах слабых электролитов
- § 14. Влияние сильных кислот или сильных оснований на степень электролитической диссоциации слабых электролитов
- § 15. Приближенные формулы для расчета [H+] и [OH-] в водных растворах кислот и оснований
- В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
- § 16. Буферные растворы
- § 17. Применение буферных растворов в химическом анализе
- Г. РАВНОВЕСИЯ В РАСТВОРАХ ГИДРОЛИЗУЮЩИХСЯ СОЛЕЙ
- § 18. Теоретические основы гидролиза
- § 19. Механизм гидролитического расщепления
- § 20. Подавление и усиление гидролиза солей
- Д. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ТИПИЧНО АМФОТЕРНЫХ ЭЛЕКТРОЛИТОВ
- § 21. Поведение амфотерных гидроокисей в водных растворах
- § 22. Константы электролитической диссоциации амфотерных гидроокисей
- Е. РАВНОВЕСИЯ В СИСТЕМАХ: ОСАДОК-НАСЫЩЕННЫЙ РАСТВОР
- § 23. Осаждение как один из основных методов химического анализа
- § 24. Произведение растворимости
- § 25. Произведение активностей
- § 26. Вычисление растворимости электролитов в воде по величине произведения растворимости
- § 27. Влияние различных факторов на растворимость малорастворимых электролитов
- Ж. ОСНОВЫ ТЕОРИИ ОБРАЗОВАНИЯ И РАЗЛОЖЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИИ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 28. Характеристика комплексных соединений, имеющих значение в химическом анализе
- § 29. Квантовомеханические представления о строении комплексов
- § 30. Равновесия в растворах комплексных соединений
- § 31. Константы нестойкости комплексов
- § 32. Внутрикомплексные соединения
- § 33. Методы разложения и образования комплексов, применяемых в аналитической химии
- § 34. Применение метода комплексообразования в химическом анализе
- ГЛАВА II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Окисление—восстановление как один из основных методов химического анализа
- § 2. Направление реакций окисления—восстановления
- § 3. Окислительно-восстановительные потенциалы
- § 4. Зависимость между величинами окислительно-восстановительных потенциалов и условиями, в которых протекают реакции окисления—восстановления
- § 5. Вычисление окислительно-восстановительных потенциалов
- § 6. Вычисление окислительно-восстановительных потенциалов с учетом коэффициентов активности
- ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
- § 1. Обнаружение отдельных элементов
- § 2. Анализ мокрым и сухим путем
- § 3. Химические и физические методы качественного анализа
- § 4. Макро-, полумикро- и микрометоды
- § 5. Капельный анализ
- § 6. Микрокристаллоскопический анализ
- § 7. Метод растирания порошков
- § 8. Методы анализа, основанные на нагревании и сплавлении веществ
- § 9. Спектральный качественный анализ
- § 10. Хроматографический метод анализа
- § 11. Кинетические методы анализа
- Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
- § 12. Специфичность и чувствительность реакций
- § 13. Максимальная чувствительность аналитических реактивов
- § 14. Способы повышения чувствительности реакций
- § 15. Маскировка мешающих ионов
- § 16. Определение pH среды
- § 17. Регулирование pH среды в процессе аналитических определений
- В. РЕАКТИВЫ
- § 18. Понятие о химических реактивах
- § 19. Концентрация применяемых реактивов
- § 20. Техника пользования реактивами
- Г. ПОСУДА И ПРИБОРЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕННОМ АНАЛИЗЕ
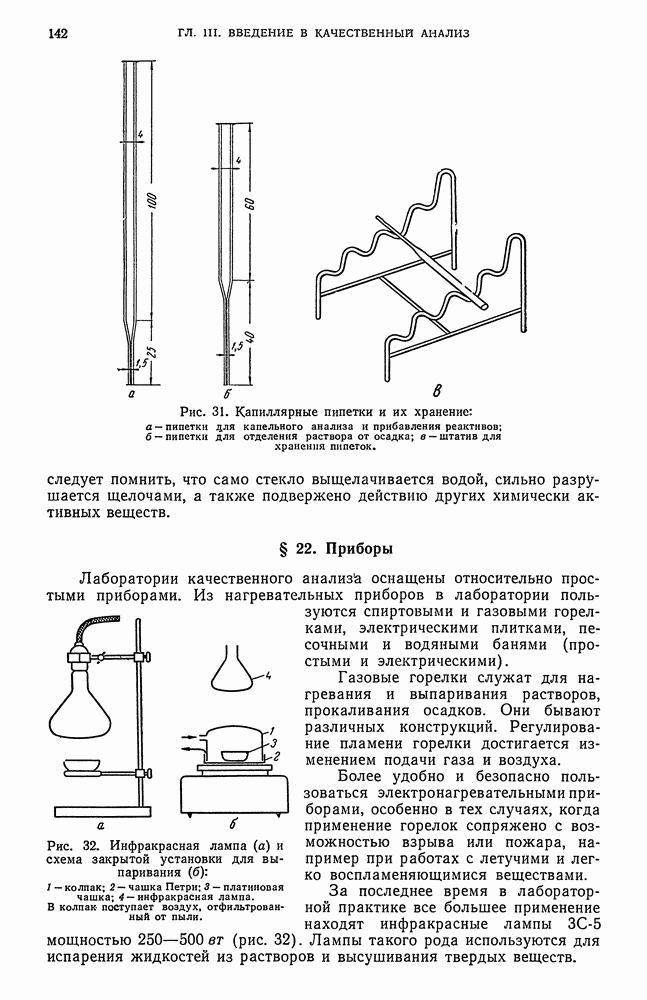
- § 21. Химическая посуда
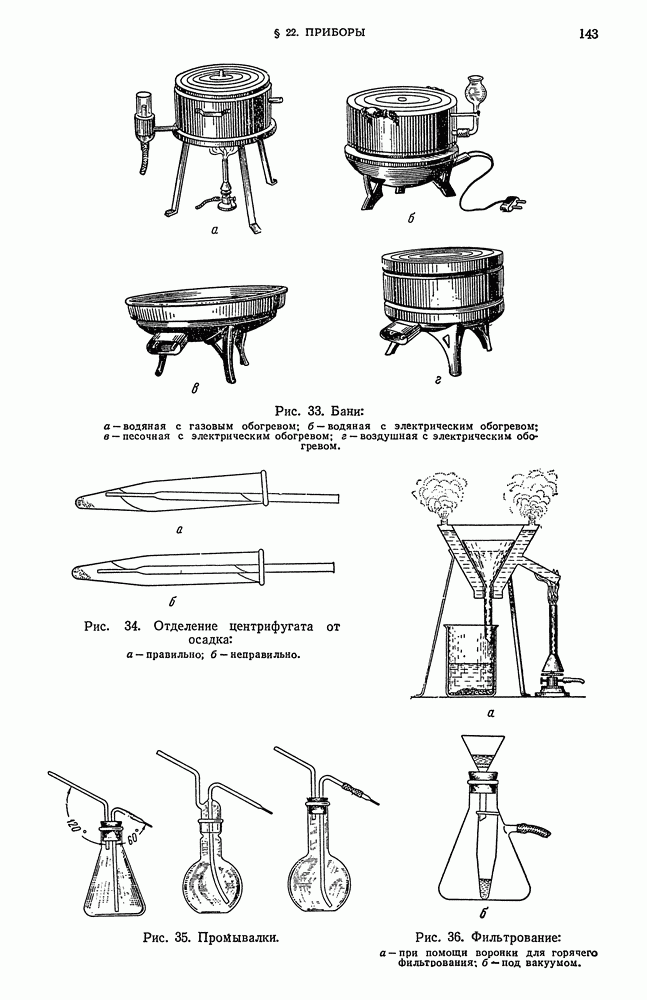
- § 22. Приборы
- Д. АНАЛИТИЧЕСКИЕ ГРУППЫ
- § 23. Дробный и систематический анализ
- § 24. Аналитическая классификация катионов
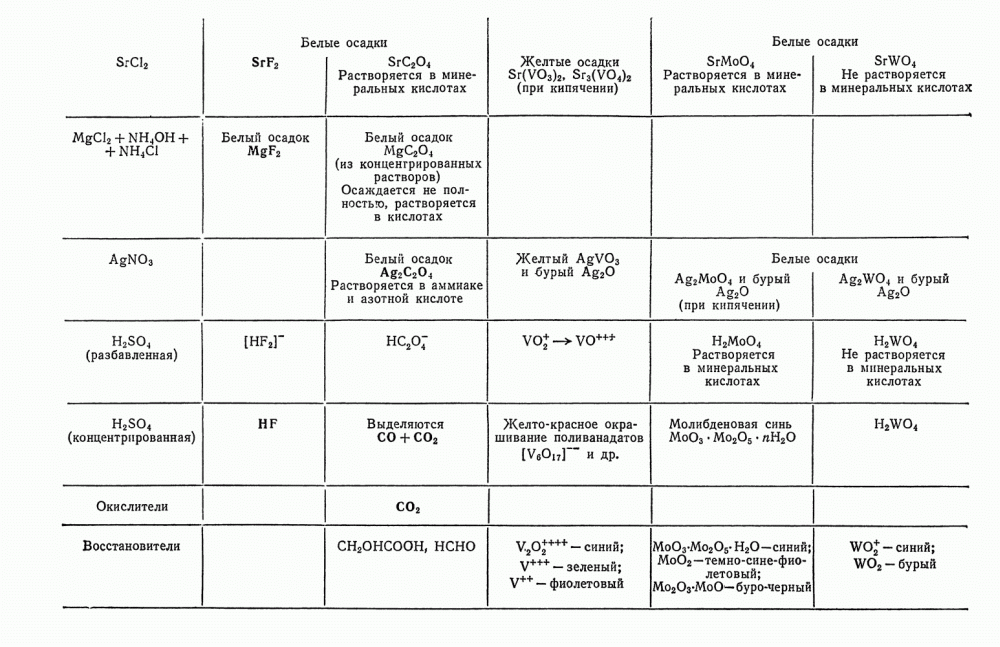
- § 25. Сводные таблицы действия реактивов на катионы и анионы
- Е. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ ИОНОВ
- § 26. Значение периодического закона в аналитической химии
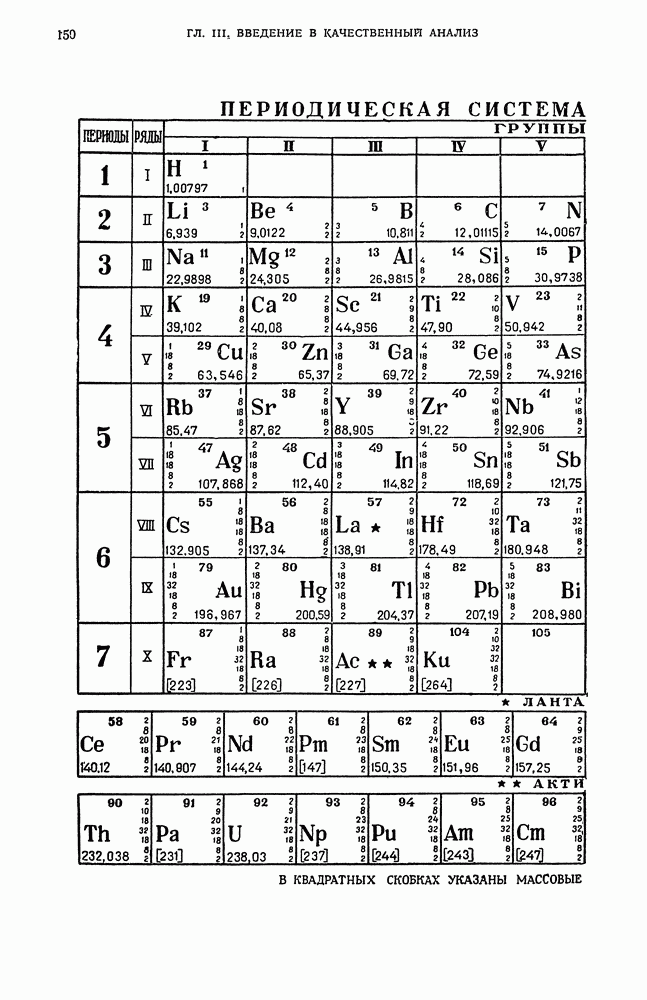
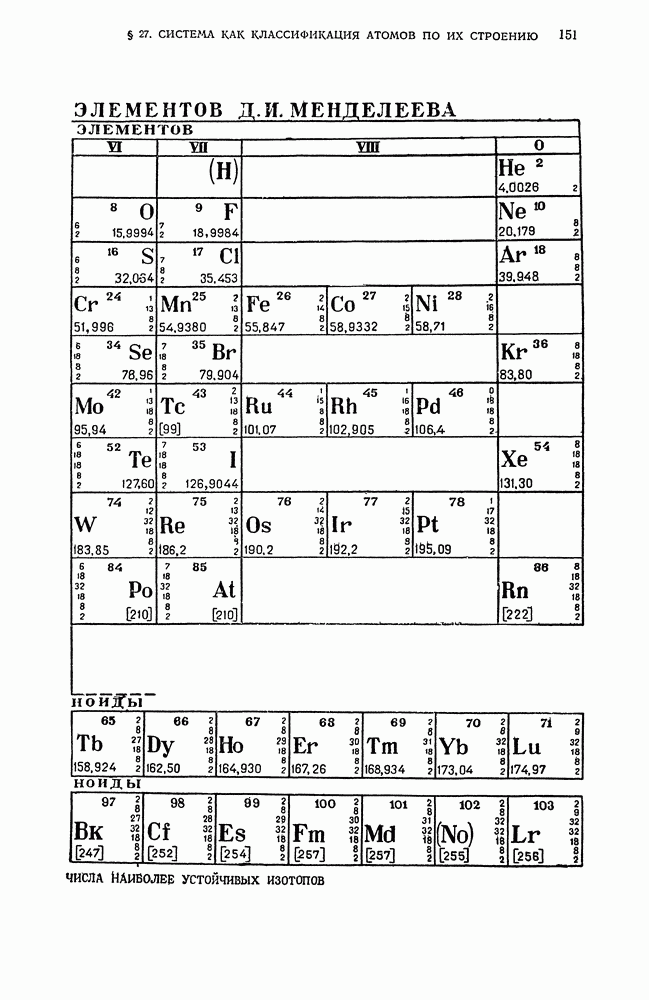
- § 27. Периодическая система элементов Д. И. Менделеева как классификация атомов по их строению
- § 28. Зависимость некоторых химических свойств элементов от положения их в периодической системе Д. И. Менделеева
- § 29. Растворимость химических соединений в связи с положением элементов в периодической системе Д. И. Менделеева
- § 30. Открытие новых аналитических реакций
- § 31. Аналитические группы и периодическая система элементов Д. И. Менделеева
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ КАТИОНОВ И АНАЛИЗ СМЕСЕЙ КАТИОНОВ
- § 1. Характеристика первой аналитической группы катионов
- § 2. Общие реакции катионов первой аналитической группы
- РЕАКЦИИ КАТИОНОВ 1-й ПОДГРУППЫ
- § 3. Обнаружение NН-ионов
- § 4. Методы разложения и удаления солей аммония
- § 5. Обнаружение K-ионов
- § 6. Обнаружение Rb-ионов
- § 7. Обнаружение Cs-ионов
- § 8. Анализ смеси катионов первой подгруппы
- РЕАКЦИИ КАТИОНОВ 2-й ПОДГРУППЫ
- § 9. Обнаружение Li-ионов
- § 10. Обнаружение Na-ионов
- § 11. Обнаружение Mg-ионов
- § 12. Обзор действия реактивов на катионы первой аналитической группы
- § 13. Анализ смеси катионов второй подгруппы
- § 14. Анализ смеси ионов
- § 15. Анализ смеси ионов
- ГЛАВА V. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика второй аналитической группы катионов
- § 2. Общие реакции катионов второй аналитической группы
- § 3. Обнаружение Ca-ионов
- § 4. Обнаружение Sr-ионов
- § 5. Обнаружение Ba-ионов
- § 6. Обзор действия реактивов на катионы второй аналитической группы
- § 7. Основы теории осаждения катионов второй аналитической группы групповым реактивом—карбонатом аммония
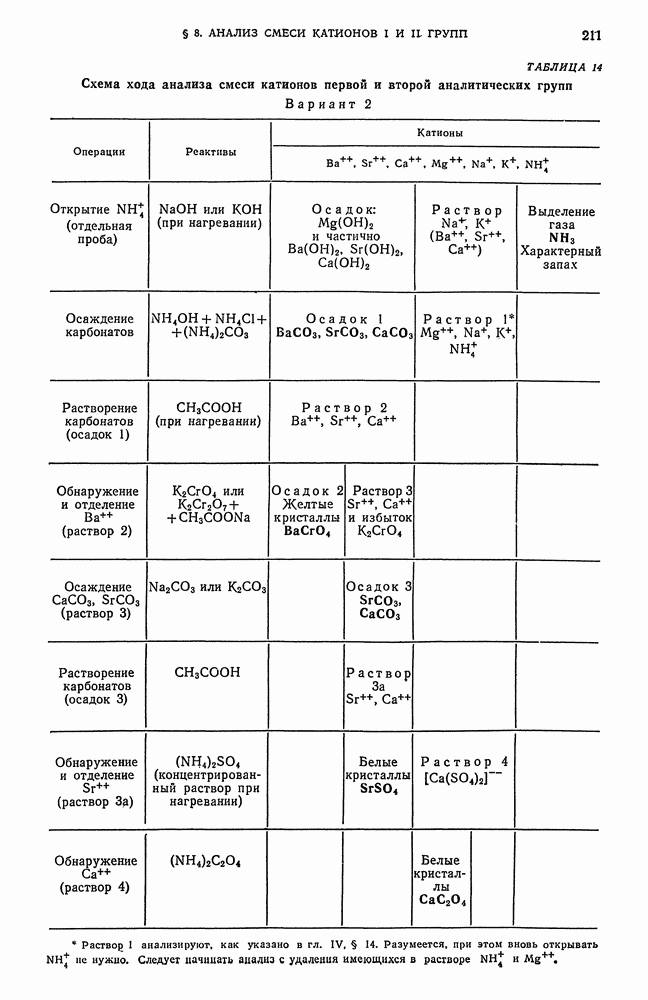
- § 8. Систематический ход анализа смеси катионов первой и второй аналитических групп
- § 9. Систематический ход анализа смеси катионов первой и второй аналитических групп в присутствии ионов
- § 10. Теоретические основы перевода сульфатов катионов второй аналитической группы в карбонаты
- ГЛАВА VI. ТРЕТЬЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика третьей аналитической группы катионов
- § 2. Общие реакции катионов третьей аналитической группы
- § 3. Обнаружение Be-ионов
- § 4. Обнаружение Al-ионов
- § 5. Обнаружение ионов титана (IV)
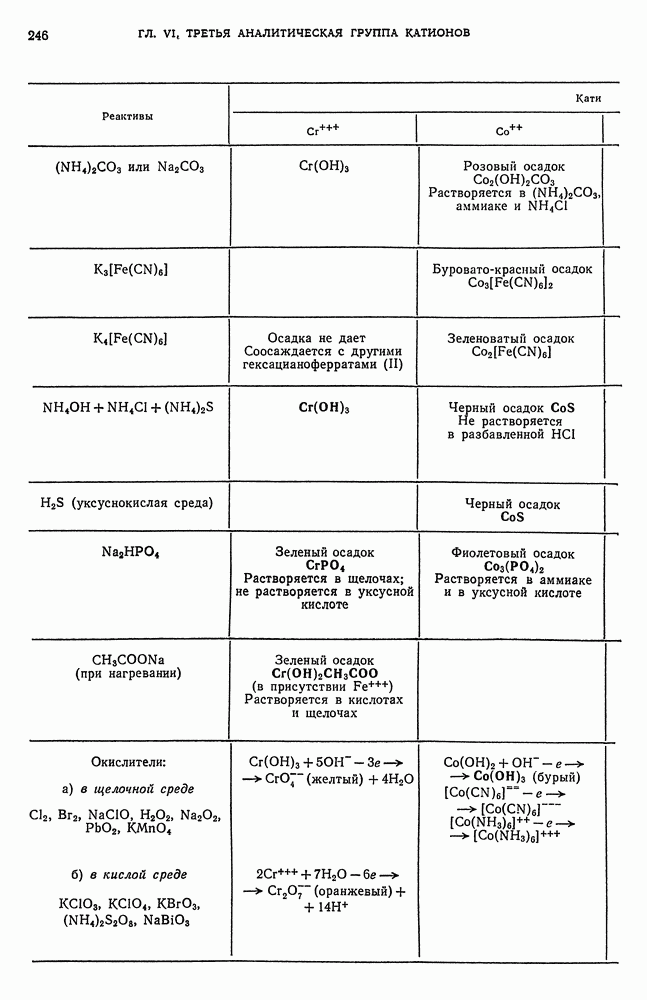
- § 6. Обнаружение Cr-ионов
- § 7. Обнаружение Mn-ионов
- § 8. Обнаружение Fe-ионов
- § 9. Обнаружение Fe-ионов
- § 10. Обнаружение Co-ионов
- § 13. Обнаружение ионов циркония (IV)
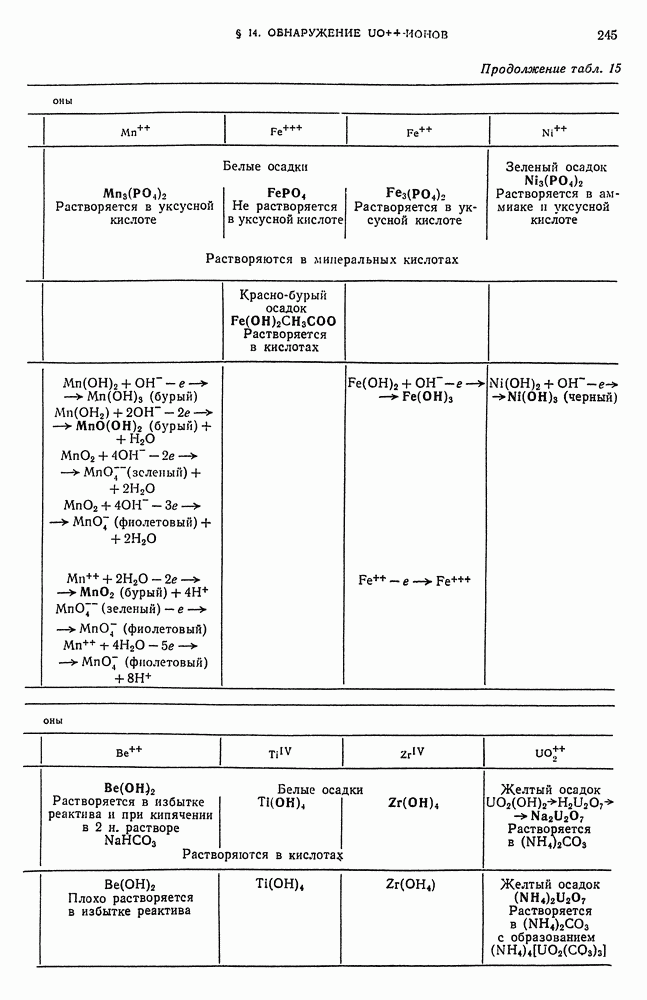
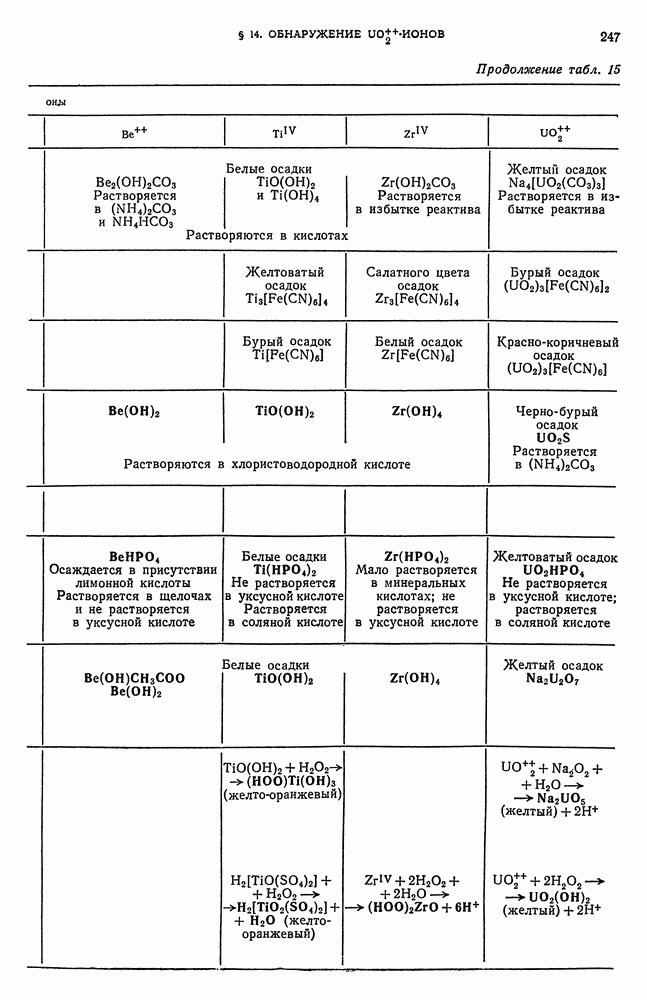
- § 14. Обнаружение UO-ионов
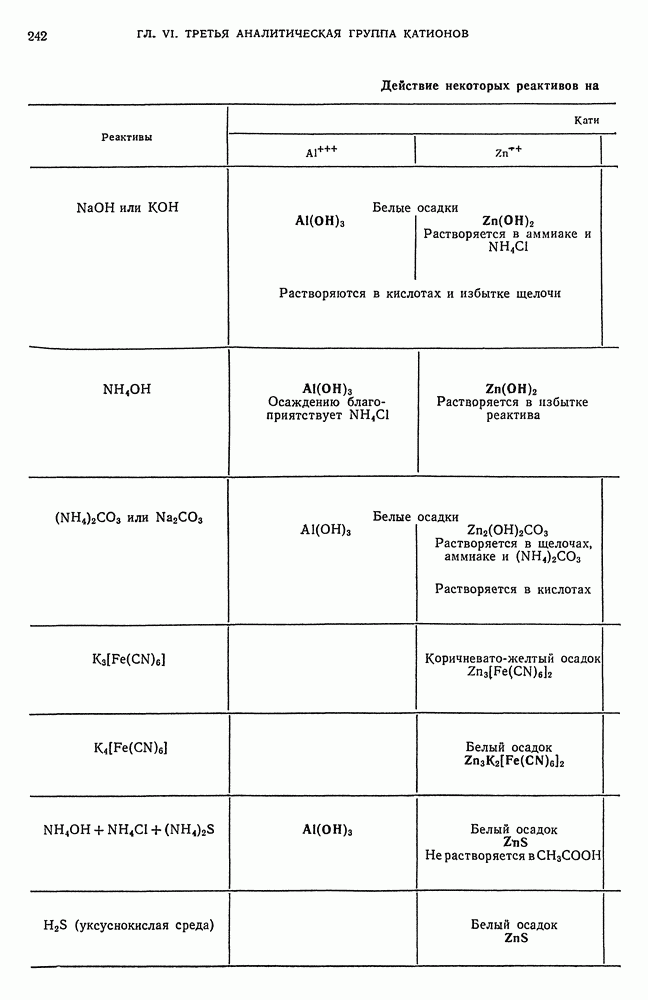
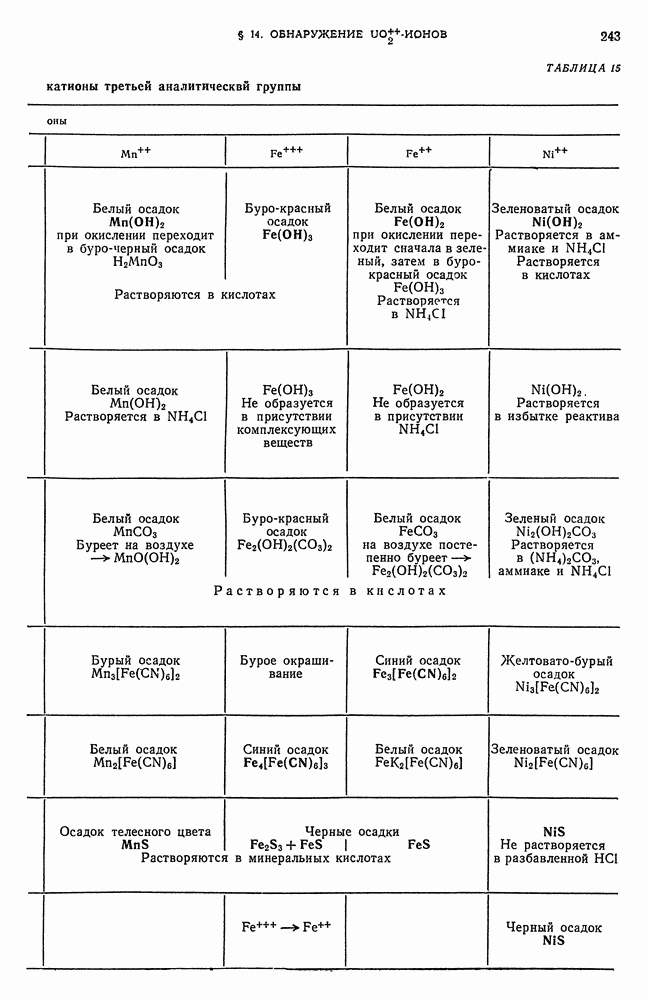
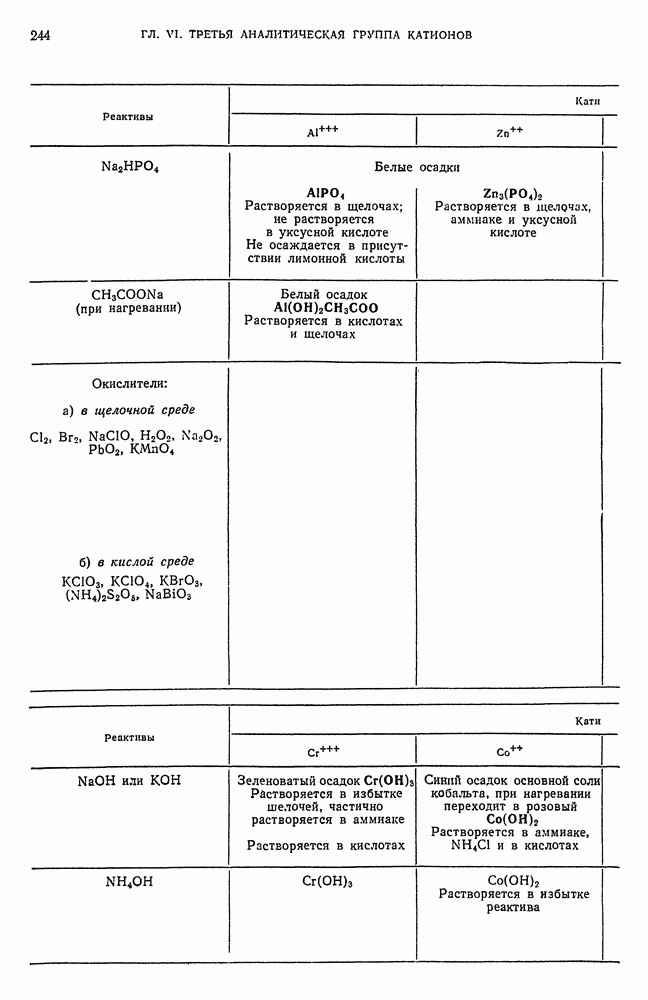
- § 15. Обзор действия реактивов на катионы третьей аналитической группы
- § 16. Использование коллоидных систем в химическом анализе
- § 17. Основы теории осаждения катионов третьей аналитической группы групповым реактивом — сульфидом аммония
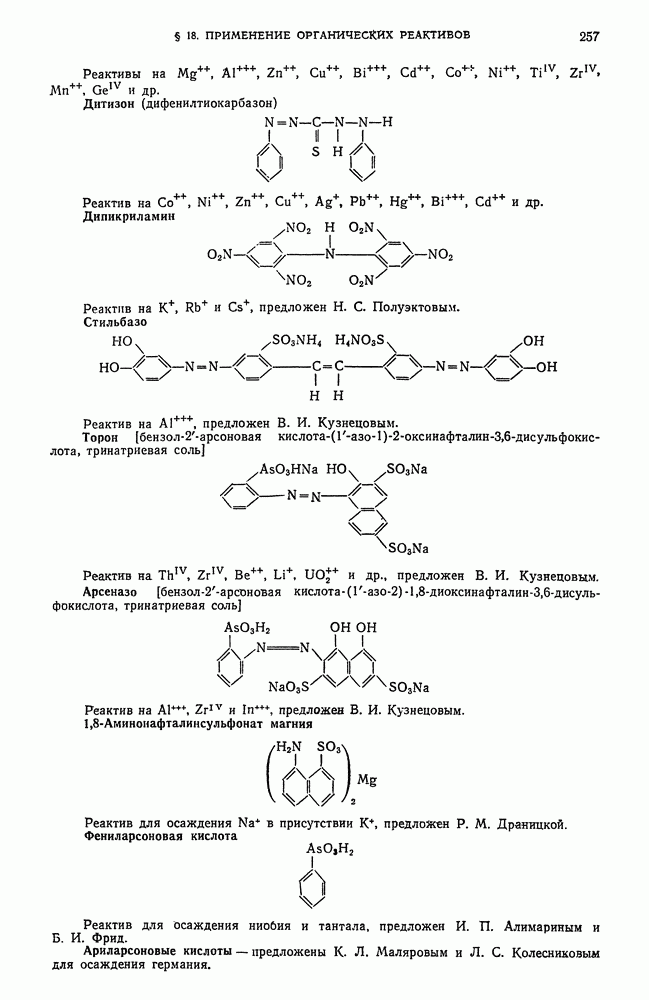
- § 18. Теоретические основы применения органических реактивов в качественном анализе неорганических веществ
- § 19. Методы разделения некоторых катионов третьей аналитической группы
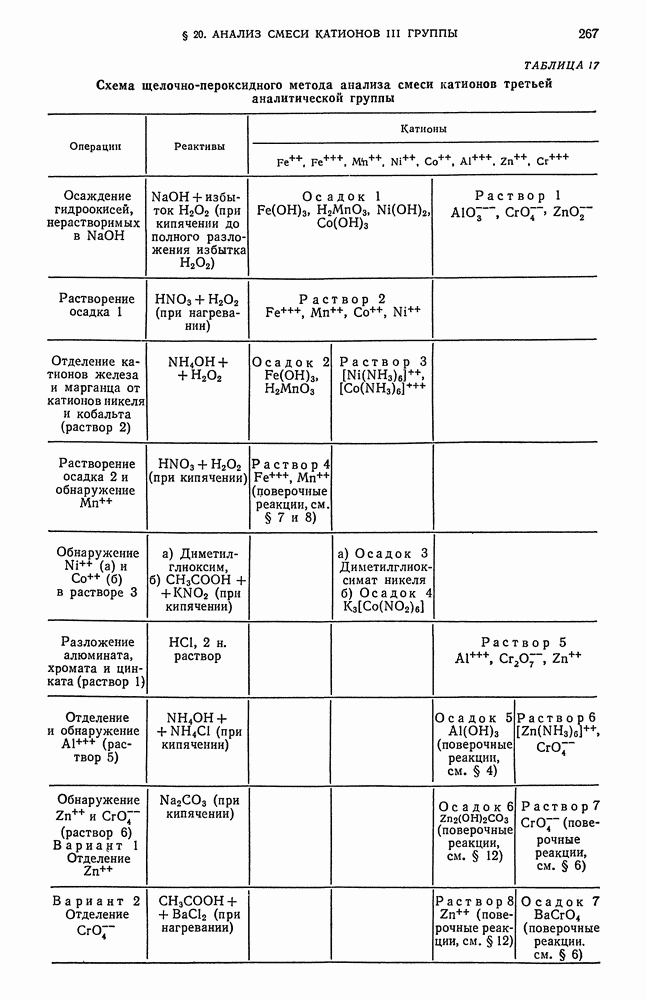
- § 20. Систематический ход анализа смеси катионов третьей аналитической группы
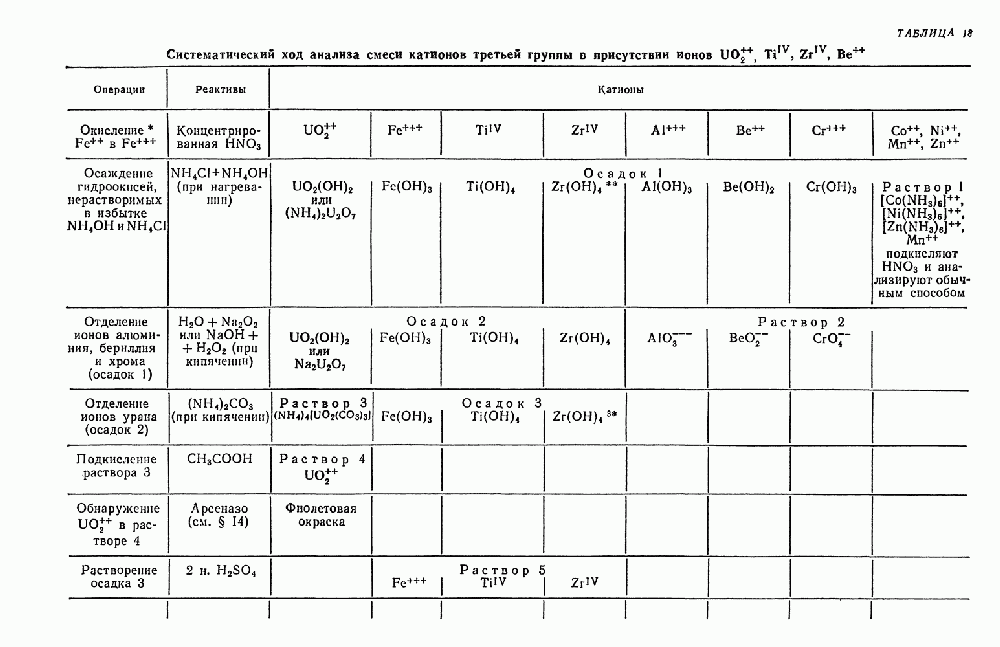
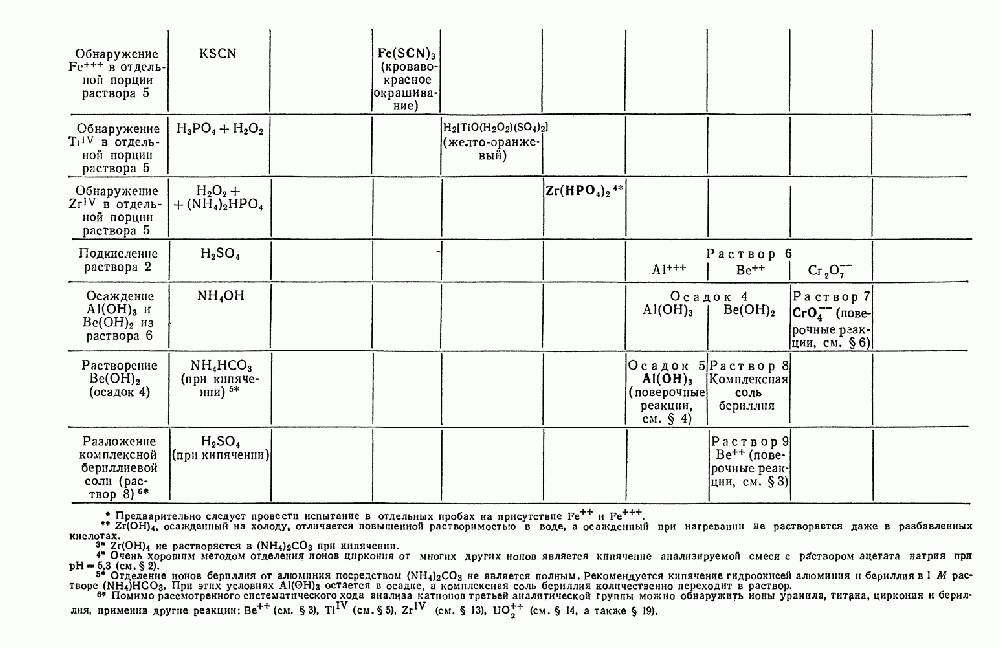
- § 21. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп
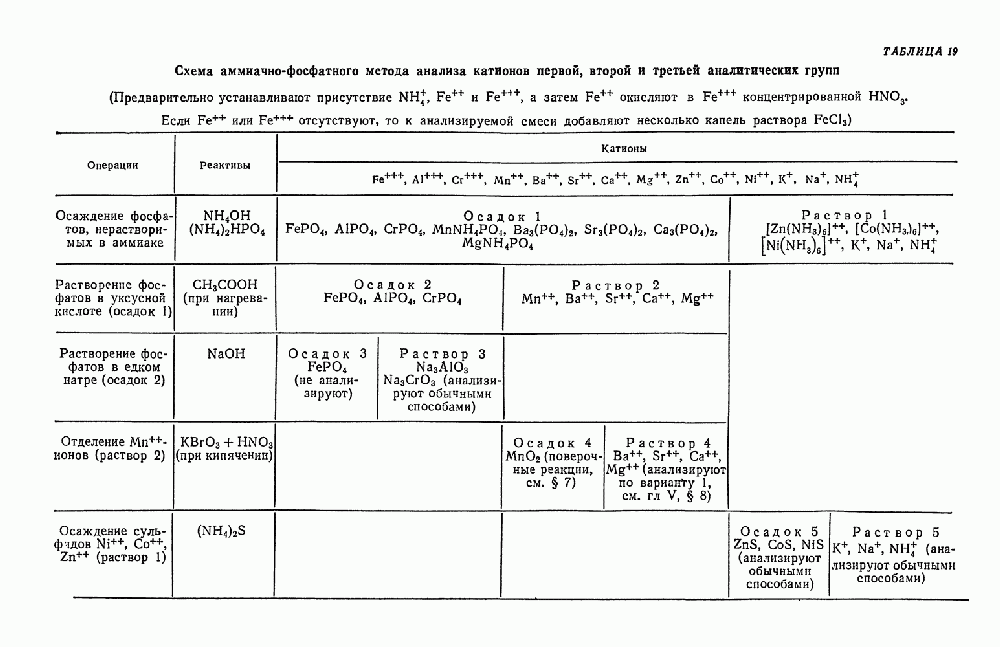
- § 22. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп в присутствии PO-ионов
- ГЛАВА VII. ЧЕТВЕРТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика четвертой аналитической группы катионов
- § 2. Общие реакции катионов четвертой аналитической группы
- РЕАКЦИИ КАТИОНОВ ПЕРВОЙ ПОДГРУППЫ (ПОДГРУППЫ МЕДИ)
- § 3. Обнаружение Hg-ионов
- § 4. Обнаружение Cu-ионов
- § 5. Обнаружение Cd-ионов
- § 6. Обнаружение Bi-ионов
- РЕАКЦИИ КАТИОНОВ ВТОРОЙ ПОДГРУППЫ (ПОДГРУППЫ МЫШЬЯКА)
- § 7. Обнаружение ионов мышьяка (III)
- § 8. Обнаружение ионов мышьяка (V)
- § 9. Общие реакции обнаружения
- § 10. Обнаружение ионов сурьмы (III)
- § 11. Обнаружение ионов сурьмы (V)
- § 12. Общие реакции обнаружения Sb
- § 13. Обнаружение ионов олова (II)
- § 14. Обнаружение ионов олова (IV)
- § 15. Общие реакции обнаружения ионов олова (II) и олова (IV)
- § 16. Отделение ионов олова от других ирнов четвертой аналитической группы
- § 17. Обнаружение ионов германия (IV)
- § 18. Отделение ионов германия от других ионов четвертой аналитической группы
- § 19. Обзор действия реактивов на катионы четвертой аналитической группы
- § 20. Основы теории осаждения сульфидов катионов четвертой аналитической группы групповым реактивом — сероводородом
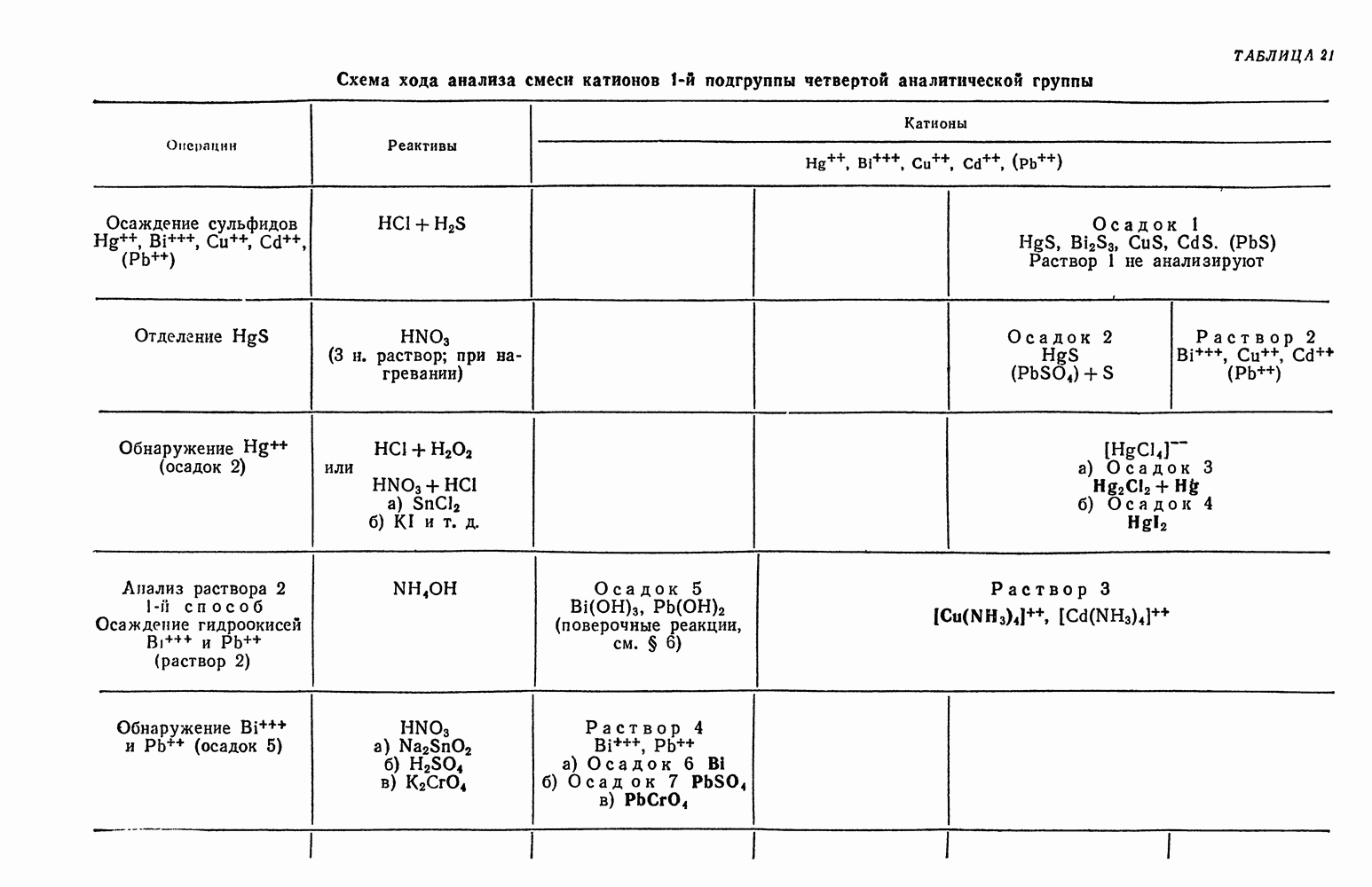
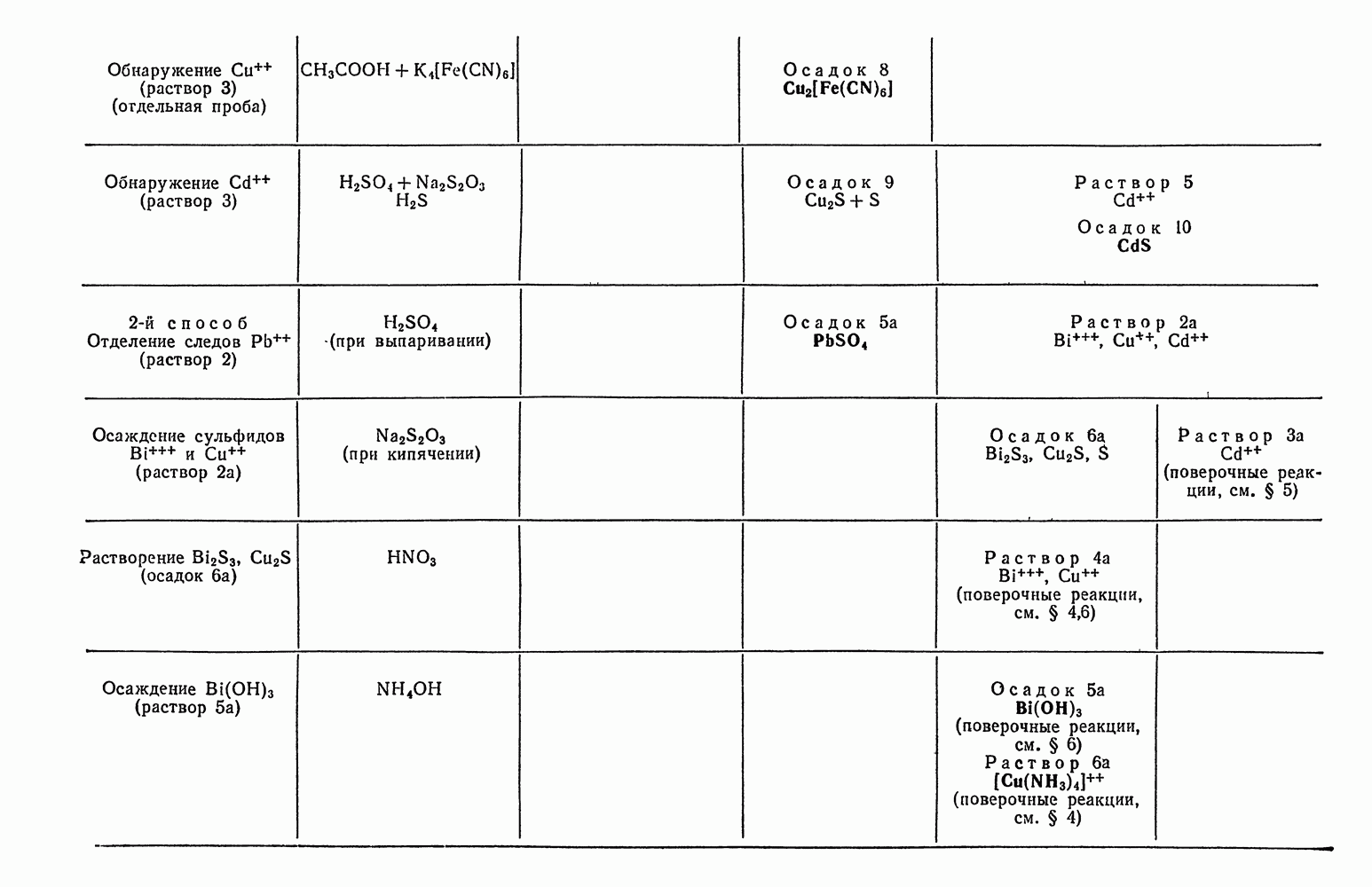
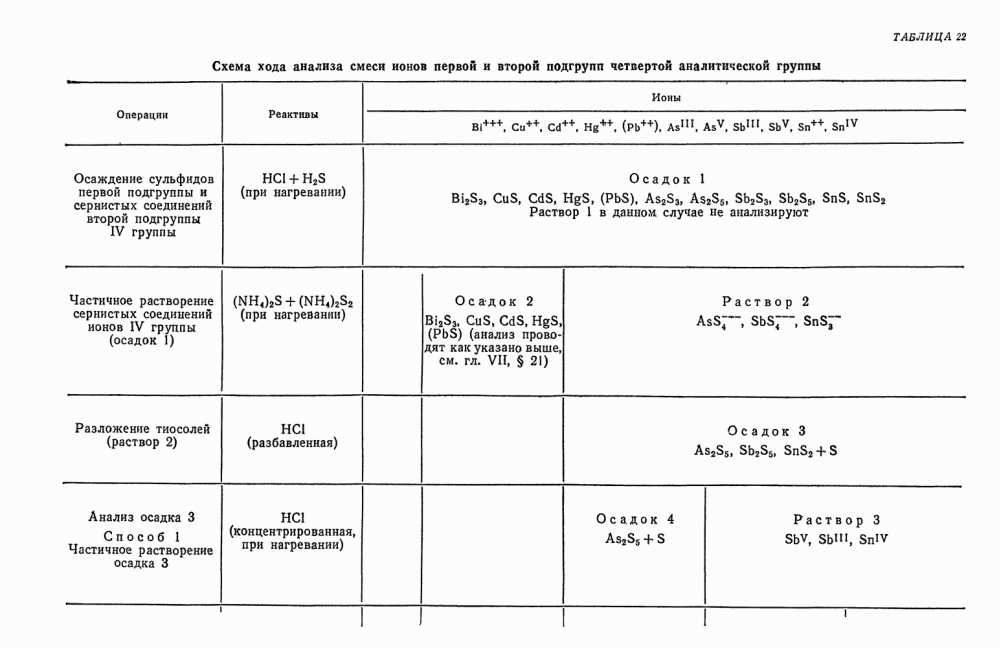
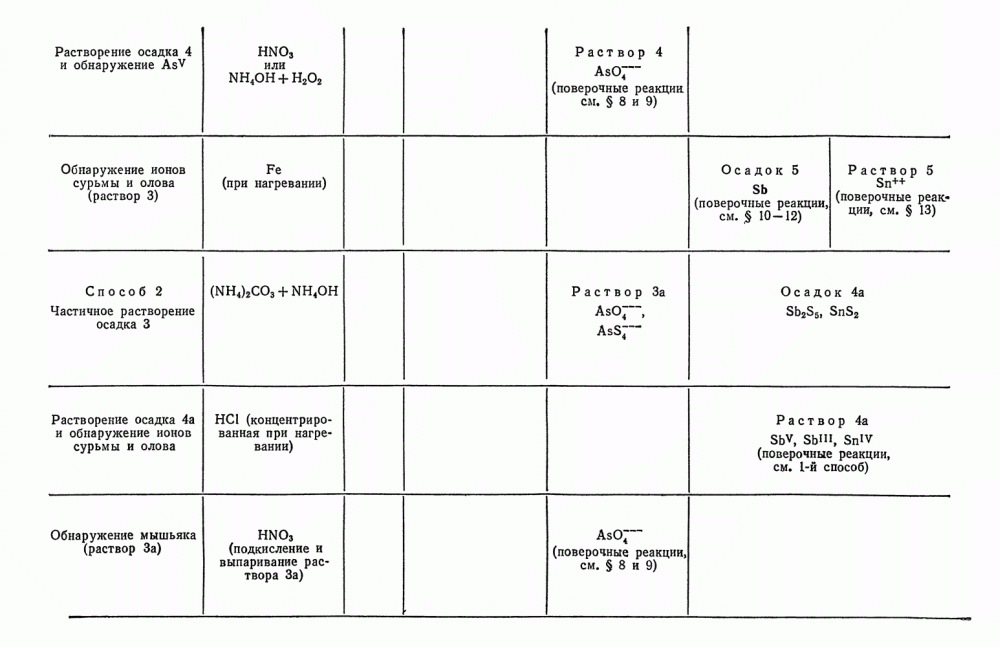
- § 21. Систематический ход анализа смеси катионов четвертой аналитической группы
- ГЛАВА VIII. ПЯТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ (ГРУППА СЕРЕБРА)
- § 1. Характеристика пятой аналитической группы катионов
- § 2. Общие реакции катионов пятой аналитической группы
- § 3. Обнаружение Ag-ионов
- § 4. Обнаружение [Hg]-ионов
- § 5. Обнаружение Pb-ионов
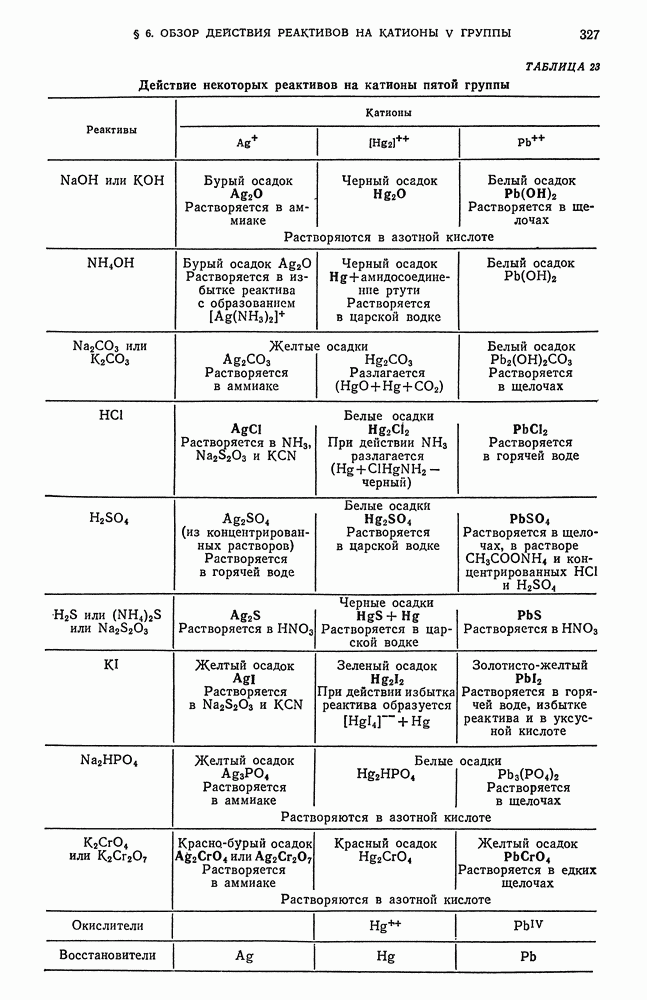
- § 6. Обзор действия реактивов на катионы пятой аналитической группы
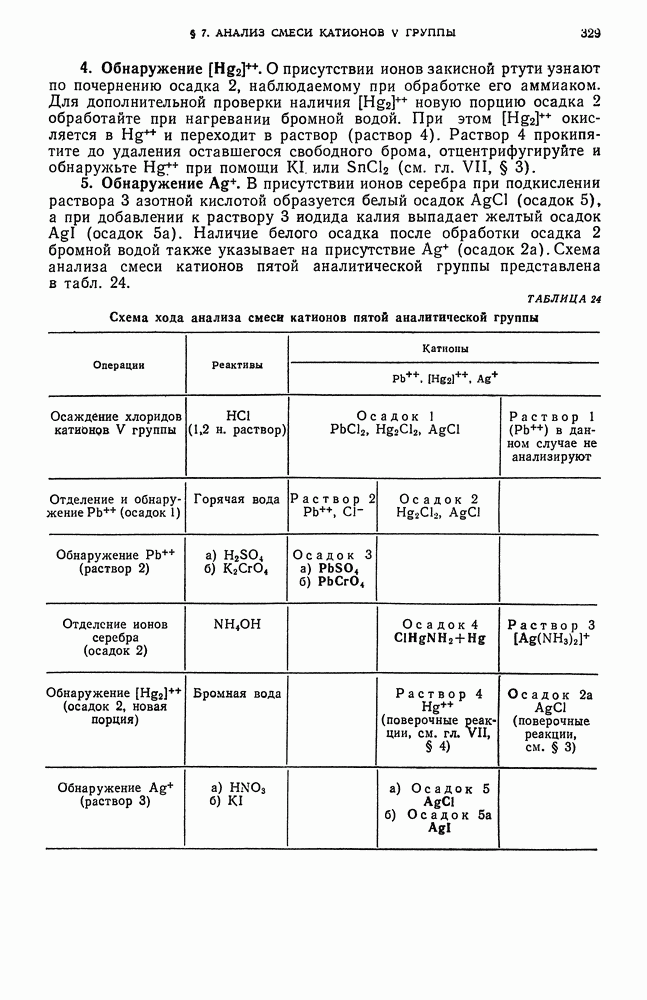
- § 7. Систематический ход анализа смеси катионов пятой аналитической группы
- ГЛАВА IX. АНАЛИЗ СМЕСИ ИОНОВ ВСЕХ ПЯТИ АНАЛИТИЧЕСКИХ ГРУПП
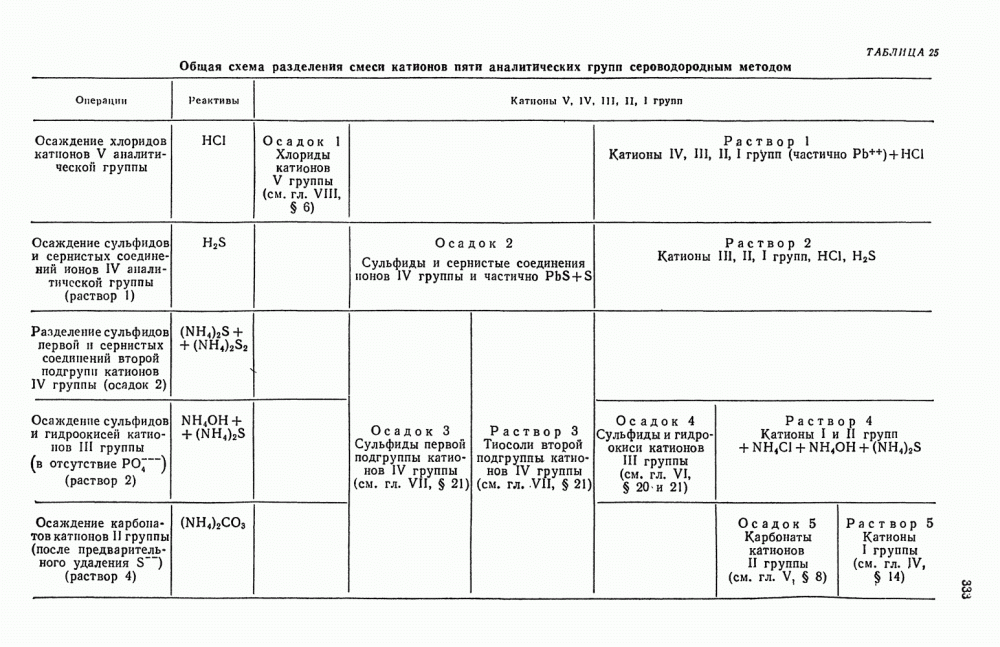
- § 1. Сероводородный метод анализа
- § 2. Недостатки сероводородного метода анализа
- § 3. Ошибки, возникающие при анализе смеси ионов пяти аналитических групп
- § 4. Бессероводородные методы анализа
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ АНИОНОВ И АНАЛИЗ СМЕСЕЙ АНИОНОВ
- § 1. Аналитическая классификация анионов
- § 2. Групповые реактивы на анионы
- § 3. Классификация методов анализа анионов
- ГЛАВА XI. ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика первой группы анионов
- § 2. Реакции анионов первой группы
- § 3. Обнаружение CI-ионов
- § 4. Обнаружение Br-ионов
- § 5. Обнаружение I-ионов
- § 6. Обнаружение CN-ионов
- § 7. Обнаружение SCN-ионов
- § 8. Обнаружение [Fe(CN)]-ионов
- § 9. Обнаружение Fe(CN)-ионов
- § 10. Обнаружение NO-ионов
- § 11. Обнаружение NO2-ионов
- § 12. Обнаружение S-ионов
- § 13. Обнаружение CH3COOO-ионов
- § 14. Обнаружение BrO3-ионов
- § 15. Обнаружение ClO3-ионов
- § 16. Обнаружение ClO4-ионов
- § 17. Обзор действия реактивов на анионы первой группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 18. Анализ смеси Cl, Br и I-ионов
- § 19. Анализ смеси Cl, Br, I и SCN-ионов
- § 20. Анализ смеси Cl, ClO3 и ClO4-ионов
- § 21. Анализ смеси NO2 и NO3-ионов
- § 22. Анализ смеси анионов первой группы
- ГЛАВА XII. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика второй группы анионов
- § 2. Общие реакции анионов второй группы
- § 3. Обнаружение SO3-ионов
- § 4. Обнаружение S2O3-ионов
- § 5. Обнаружение S2O3 в присутствии SO3-ионов
- § 6. Обнаружение SO4-ионов
- § 7. Обнаружение CO3-ионов
- § 8. Обнаружение CO3-ионов в присутствии SO3 и S2O3-ионов
- § 9. Обнаружение PO4-ионов
- § 10. Обнаружение CrO4-ионов
- § 11. Обнаружение AsO3-ионов
- § 12. Обнаружение AsO4-ионов
- § 13. Обнаружение BO2 и BO3-ионов
- § 14. Обнаружение SiO3-ионов
- § 15. Обнаружение F-ионов
- § 16. Обнаружение C2O4-ионов
- § 17. Обнаружение VO3-ионов
- § 18. Обнаружение MoO4-ионов
- § 19. Обнаружение WO4-ионов
- § 20. Обзор действия реактивов на анионы второй группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 21. Анализ смеси ионов
- § 22. Анализ смеси SO3, SO4, S2O3 и CO3-ионов
- § 23. Анализ смеси VO2, MoO4 и WO4-ионов
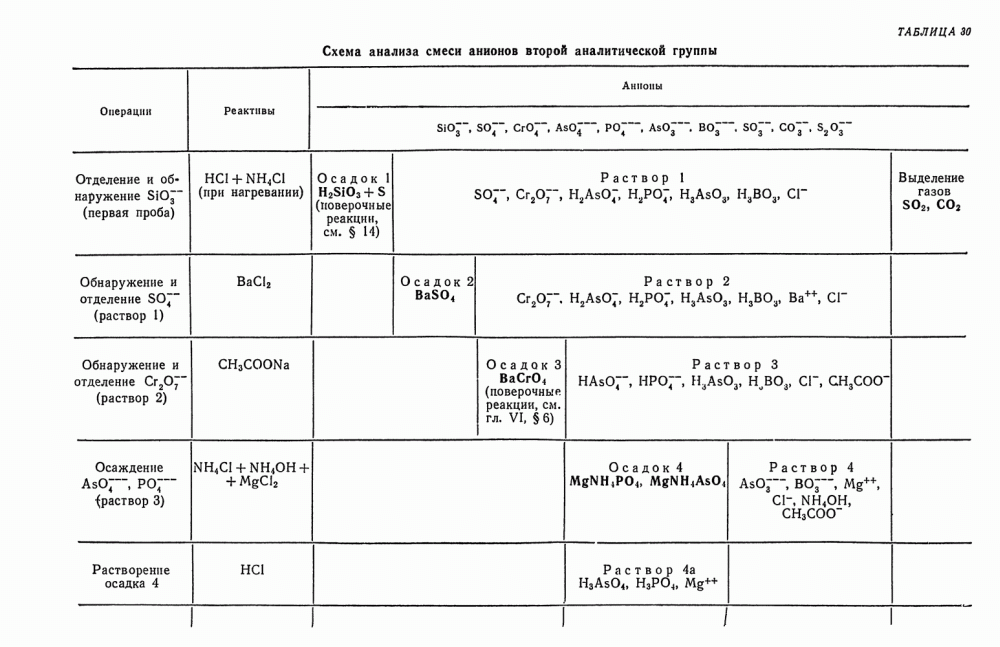
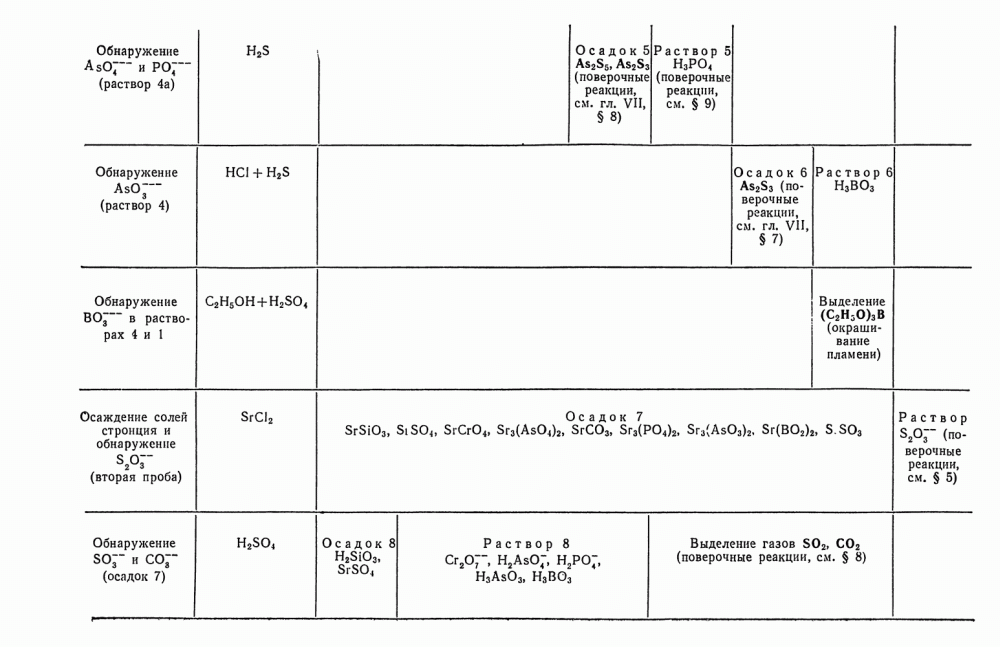
- § 24. Анализ смеси анионов второй группы
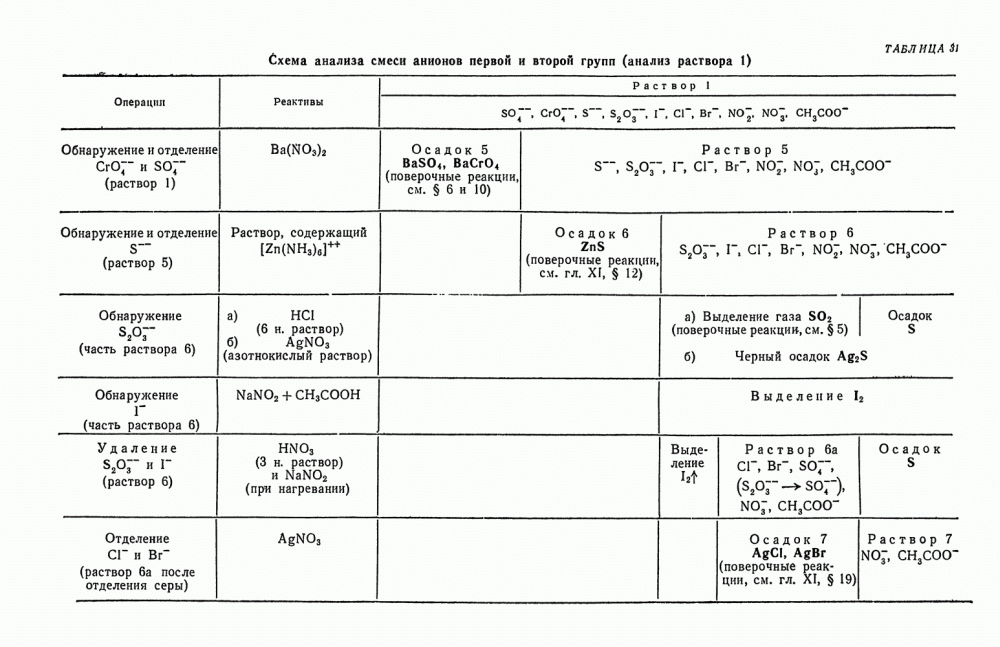
- § 25. Анализ смеси анионов первой и второй групп
- ГЛАВА XIII. ОБНАРУЖЕНИЕ СВОБОДНЫХ МЕТАЛЛОВ И НЕМЕТАЛЛОВ, ИДЕНТИФИЦИРОВАНИЕ СОЛЕЙ И ДРУГИХ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И АНАЛИЗ ИХ СМЕСЕЙ
- § 1. Подготовка вещества к анализу
- § 2. Предварительные испытания
- § 3. Растворение анализируемого вещества в воде, кислотах и щелочах
- § 4. Переведение в растворимое состояние веществ, нерастворимых в воде, кислотах и щелочах
- § 5. Анализ неизвестного вещества
- § 6. Обнаружение свободных элементов
- § 7. Идентифицирование солей и других индивидуальных соединений
- § 8. Обнаружение микропримесей
- § 9. Анализ сплавов
- § 10. Анализ силикатов и алюмосиликатов
- § 11. Анализ смеси неорганических веществ
- § 12. Экспрессный метод анализа смесей катионов и анионов
- § 13. Идентифицирование нерастворимых веществ
- ЛИТЕРАТУРА