| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 14. Способы повышения чувствительности реакций
На чувствительность реакции влияют разнообразные факторы, поэтому для химика-аналитика большое значение приобретают способы повышения чувствительности реакции.
Поскольку чувствительность реакции обусловлена открываемым минимумом, минимальной концентрацией и предельным разбавлением, т. е. связана с концентрацией открываемого вещества, то естественно, что повышение чувствительности реакции в первую очередь может быть достигнуто в результате повышения концентрации дайного вещества в растворе.
Повысить чувствительность реакции можно, применяя химически чистые реактивы, свободные от каких-либо посторонних примесей, мешающих данной реакции, а также предварительным отделением или маскировкой посторонних ионов, мешающих реакции.
Для этого применяют выпаривание растворов; предварительное осаждение в виде малорастворимого соединения с последующим растворением его в подходящем растворителе; экстракцию соединений органическими растворителями; дистилляцию; избирательную адсорбцию ионов на твердом веществе—адсорбенте и другие специальные методы.
Метод соосаждения. Во многих случаях требуется определять в различных природных и технических объектах химические элементы при их содержании  . Определение таких малых количеств элементов, минуя стадию концентрирования, не всегда может быть осуществлено с помощью даже высокочувствительных методов. Поэтому для таких анализов определяемые элементы предварительно концентрируют различными способами. Одним из наиболее простых и эффективных способов концентрирования является соосаждение.
. Определение таких малых количеств элементов, минуя стадию концентрирования, не всегда может быть осуществлено с помощью даже высокочувствительных методов. Поэтому для таких анализов определяемые элементы предварительно концентрируют различными способами. Одним из наиболее простых и эффективных способов концентрирования является соосаждение.
В анализируемый раствор специально вносят небольшое количество постороннего вещества (катиона или аниона) и осаждают его соответствующим реактивом в виде малорастворимого соединения. На осадке, называемом коллектором (собирателем), в процессе его образования соосаждаются (концентрируются) следы определяемых ионов.
Коллектор, как показывает опыт, тем полнее адсорбирует ионы, чем меньше их концентрация.
Метод соосаждения на коллекторе широко применяется в аналитической практике.
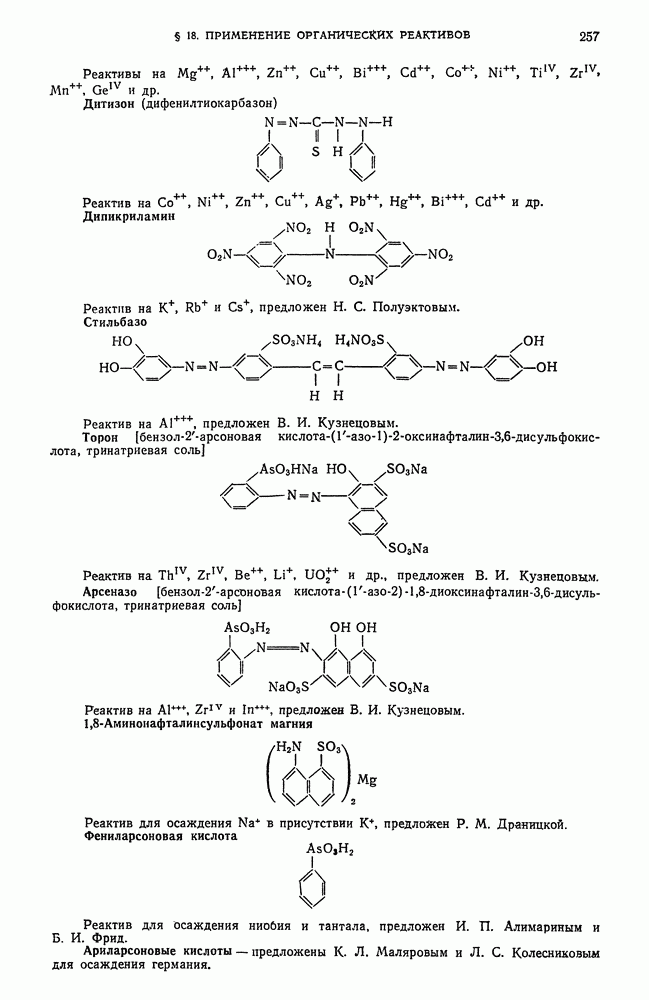
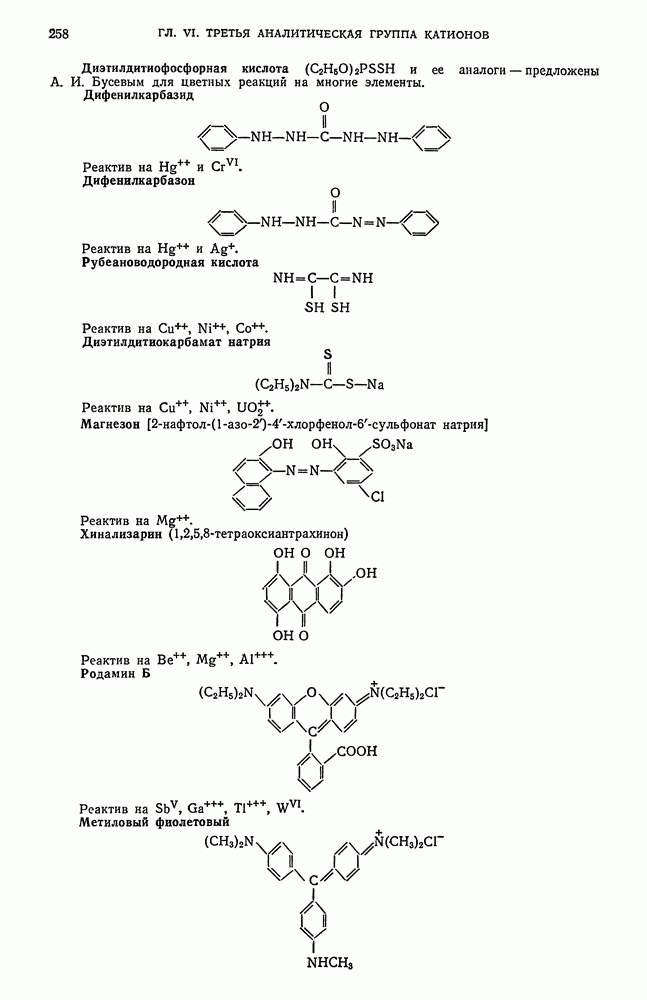
Соосадителями могут быть неорганические, органические и смешанные соединения. В качестве неорганических соосадителей применяют гидроокись или фосфат железа, гидроокись алюминия и другие неорганические соединения, нерастворимые в данной среде. В качестве органических соосадителей применяют малорастворимые органические соединения, образующиеся при добавлении к анализируемым растворам, содержащим органические катионы или анионы, солей тяжелых органических ионов противоположного заряда. Реагентами, поставляющими органические катионы, являются метиловый фиолетовый,  -диметиламиноазобензол, родамины и другие соединения.
-диметиламиноазобензол, родамины и другие соединения.
В качестве реагентов, поставляющих анионы, применяют нафталин- -сульфокислоту, метиловый оранжевый и другие соединения, содержащие сульфогруппы.
-сульфокислоту, метиловый оранжевый и другие соединения, содержащие сульфогруппы.
Органические соосадители отличаются рядом преимуществ по сравнению с неорганическими и смешанными коллекторами, образованными ионами металлов при действии органических осадителей и комплексообразующих веществ. Например, они легко озоляются, что позволяет получать соосажденные элементы практически в чистом виде; они отличаются достаточно большой селективностью, что дает возможность соосаждать следы ионов определяемых элементов в присутствии других посторонних ионов; наконец, при их помощи достигается количественное выделение ионов из предельно разбавленных растворов с концентрацией определяемого элемента до  .
.
Существует несколько точек зрения, объясняющих механизм соосаждения ионов определяемых элементов с неорганическими и органическими коллекторами: 1) образование твердых растворов; 2) адсорбция ионов или соединений соосаждаемого элемента на поверхности сооса-дителя; 3) образование соосаждаемым соединением элемента центров кристаллизации, на которых происходит отложение выпадающего со-осадителя; 4) ионный обмен и др.
Большую роль в развитии методов соосаждения сыграли работы советских ученых В. И. Кузнецова (по органическим соосадителям) и В. Т. Чуйко (по неорганическим соосадителям).
Пример соосаждения. Метод соосаждения был использован В. И. Кузнецовым для определения содержания урана в морской воде.
Содержание урана в морской воде так мало, что непосредственно определить его ни в воде, ни в сухом остатке после выпаривания воды не удается. Для концентрирования урана используют различные приемы. Малые количества урана можно выделить соосаждением его с гидроокисью или с фосфатом железа или алюминия. Кузнецовым было применено соосаждение урана с органическими соединениями. При действии избытка роданида в кислой среде уран образует слабодиссоцннрующий роданидный анион  , который может быть количественно соосажден малорастворимыми родадидами тяжелых органических катионов, например роданидами основных красителей (метилового фиолетового и др.).
, который может быть количественно соосажден малорастворимыми родадидами тяжелых органических катионов, например роданидами основных красителей (метилового фиолетового и др.).
Вместе с ураном выделяются все ионы, образующие комплексные роданидные анионы или нерастворимые роданиды, т. е.  и др. В присутствии комплексона III (двунатриевая соль этилендиаминтетрауксусной кислоты, трилои Б) число соосаждаемых ионов уменьшается. Осадок отфильтровывают и озоляют. Уран, отделенный от солей, содержавшихся в морской воде, остается в золе. Дальнейшее определение урана не вызывает особых затруднений. Количественное соосаждение урана этим методом достигается из растворов с концентрацией
и др. В присутствии комплексона III (двунатриевая соль этилендиаминтетрауксусной кислоты, трилои Б) число соосаждаемых ионов уменьшается. Осадок отфильтровывают и озоляют. Уран, отделенный от солей, содержавшихся в морской воде, остается в золе. Дальнейшее определение урана не вызывает особых затруднений. Количественное соосаждение урана этим методом достигается из растворов с концентрацией  .
.
Метод экстракции. Для разделения смесей, содержащих растворимые в органических растворителях компонецты, применяют извлечение того или иного вещества из водного раствора с помощью органического растворителя (экстрагента), не смешивающегося с водой. Такой процесс называют экстрагированием (или экстракцией). Вещество, растворимое в воде и органическом растворителе, распределяется между двумя несмешивающимися слоями жидкости. При этом отношение активностей (а) или концентраций (С) в обеих жидкостях при данной температуре есть величина постоянная:

Органический растворитель подбирают так, чтобы в нем количественно растворялось определяемое вещество и плохо или совсем не растворялись другие компоненты анализируемого продукта.
Для выделения вещества в чистом виде экстракт подвергают выпариванию, высушиванию, перегонке или кристаллизации.
Метод экстракции органическими растворителями отличается рядом преимуществ по сравнению с другими методами повышения концентрации:
1) можно извлечь определяемое вещество из очень разбавленного раствора, т. е. повышается чувствительность метода;
2) не происходит соосаждения и экстрагируемое вещество количественно выделяют в чистом виде;
3) оказывается возможным выделять и разделять вещества, которые трудно или невозможно разделить другими способами.
Экстракцию в сочетании с другими методами применяют как для качественного, так и для количественного анализа.
Ионы железа (III) экстрагируют из солянокислого водного раствора эфиром в виде  . Ионы лития отделяют в виде
. Ионы лития отделяют в виде  от других щелочных металлов экстрагированием ацетоном, в котором нерастворимы хлориды натрия, калия и др. Роданидные комплексы железа, кобальта, молибдена экстрагируются смесью изоами-лового спирта и эфира. Соединения некоторых металлов с органическими реагентами — купфероном, оксихинолином, дитизоном и др. — экстрагируются эфиром, хлороформом, четыреххлористым углеродом и т. д.
от других щелочных металлов экстрагированием ацетоном, в котором нерастворимы хлориды натрия, калия и др. Роданидные комплексы железа, кобальта, молибдена экстрагируются смесью изоами-лового спирта и эфира. Соединения некоторых металлов с органическими реагентами — купфероном, оксихинолином, дитизоном и др. — экстрагируются эфиром, хлороформом, четыреххлористым углеродом и т. д.
В качественном анализе экстракцию используют для разделения веществ и извлечения окрашенных в характерный цвет соединений.
Факторы, понижающие чувствительность реакций. Следует учитывать, что при изменении факторов, оказывающих существенное влияние на реакции, чувствительность реакции может быть не только повышена, но и понижена.
Например, нагревание, способствующее увеличению скорости реакции, приводит к повышению растворимости осаждаемого соединения, в результате чего чувствительность реакции понижается.
Так, осаждение  с помощью антимоната калия
с помощью антимоната калия  в виде
в виде  лучше идет на холоду, так как растворимость
лучше идет на холоду, так как растворимость  при нагревании сильно увеличивается и осадок не выпадает.
при нагревании сильно увеличивается и осадок не выпадает.
Прибавление избытка реактива благоприятствует повышению чувствительности реакции, но иногда приводит к растворению осадка (вследствие образования комплексного иона) и чувствительность реакции уменьшается. Например, осаждение  в виде красного кристаллического осадка
в виде красного кристаллического осадка  при избытке добавляемого иодида приводит к растворению
при избытке добавляемого иодида приводит к растворению  с образованием комплексного аниона:
с образованием комплексного аниона:

Сильно влияет на чувствительность реакции  среды. Многие реакции протекают в строго определенной среде, т. е. при определенных значениях
среды. Многие реакции протекают в строго определенной среде, т. е. при определенных значениях  . При несоблюдении этого условия реакции не происходят или протекают в нежелательном направлении.
. При несоблюдении этого условия реакции не происходят или протекают в нежелательном направлении.
Например, при окислении смеси, содержащей  , перманганатом калия чувствительность реакции повышается по мере увеличения концентрации ионов водорода. При
, перманганатом калия чувствительность реакции повышается по мере увеличения концентрации ионов водорода. При  раствор
раствор  окисляет только
окисляет только  до
до  , не оказывая действия на
, не оказывая действия на  , при
, при  окисляется также
окисляется также  до
до  , а при
, а при  окисляется и
окисляется и  до
до  .
.
Поэтому, если нужно последовательно окислить указанные ионы, то следует придерживаться строго определенных значений  среды. При несоблюдении этого условия реакция не пойдет совсем или сразу все ионы окислятся перманганатом.
среды. При несоблюдении этого условия реакция не пойдет совсем или сразу все ионы окислятся перманганатом.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Анализ и синтез
- § 2. Предмет аналитической химии
- § 3. Развитие аналитической химии
- § 4. Качественный и количественный анализ
- ГЛАВА I. ПРИМЕНЕНИЕ ЗАКОНА ДЕЙСТВИЯ МАСС В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Влияние среды на состояние ионов в растворах
- § 2. Обратимые и необратимые аналитические реакции
- § 3. Направление аналитических реакций; правила обменного разложения
- § 4. Закон действия масс и следствие из него
- § 5. Границы применимости закона действия масс
- § 6. Сильные и слабые электролиты
- § 7. Активность
- § 8. Коэффициент активности и ионная сила
- Б. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ (В ГОМОГЕННЫХ СИСТЕМАХ)
- § 9. Гомогенные и гетерогенные системы
- § 10. Ионное произведение воды
- § 11. Ионы гидроксония
- § 12. Равновесие ионов в водных растворах; понятие о pH
- § 13. Равновесие в водных растворах слабых электролитов
- § 14. Влияние сильных кислот или сильных оснований на степень электролитической диссоциации слабых электролитов
- § 15. Приближенные формулы для расчета [H+] и [OH-] в водных растворах кислот и оснований
- В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
- § 16. Буферные растворы
- § 17. Применение буферных растворов в химическом анализе
- Г. РАВНОВЕСИЯ В РАСТВОРАХ ГИДРОЛИЗУЮЩИХСЯ СОЛЕЙ
- § 18. Теоретические основы гидролиза
- § 19. Механизм гидролитического расщепления
- § 20. Подавление и усиление гидролиза солей
- Д. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ТИПИЧНО АМФОТЕРНЫХ ЭЛЕКТРОЛИТОВ
- § 21. Поведение амфотерных гидроокисей в водных растворах
- § 22. Константы электролитической диссоциации амфотерных гидроокисей
- Е. РАВНОВЕСИЯ В СИСТЕМАХ: ОСАДОК-НАСЫЩЕННЫЙ РАСТВОР
- § 23. Осаждение как один из основных методов химического анализа
- § 24. Произведение растворимости
- § 25. Произведение активностей
- § 26. Вычисление растворимости электролитов в воде по величине произведения растворимости
- § 27. Влияние различных факторов на растворимость малорастворимых электролитов
- Ж. ОСНОВЫ ТЕОРИИ ОБРАЗОВАНИЯ И РАЗЛОЖЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИИ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 28. Характеристика комплексных соединений, имеющих значение в химическом анализе
- § 29. Квантовомеханические представления о строении комплексов
- § 30. Равновесия в растворах комплексных соединений
- § 31. Константы нестойкости комплексов
- § 32. Внутрикомплексные соединения
- § 33. Методы разложения и образования комплексов, применяемых в аналитической химии
- § 34. Применение метода комплексообразования в химическом анализе
- ГЛАВА II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Окисление—восстановление как один из основных методов химического анализа
- § 2. Направление реакций окисления—восстановления
- § 3. Окислительно-восстановительные потенциалы
- § 4. Зависимость между величинами окислительно-восстановительных потенциалов и условиями, в которых протекают реакции окисления—восстановления
- § 5. Вычисление окислительно-восстановительных потенциалов
- § 6. Вычисление окислительно-восстановительных потенциалов с учетом коэффициентов активности
- ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
- § 1. Обнаружение отдельных элементов
- § 2. Анализ мокрым и сухим путем
- § 3. Химические и физические методы качественного анализа
- § 4. Макро-, полумикро- и микрометоды
- § 5. Капельный анализ
- § 6. Микрокристаллоскопический анализ
- § 7. Метод растирания порошков
- § 8. Методы анализа, основанные на нагревании и сплавлении веществ
- § 9. Спектральный качественный анализ
- § 10. Хроматографический метод анализа
- § 11. Кинетические методы анализа
- Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
- § 12. Специфичность и чувствительность реакций
- § 13. Максимальная чувствительность аналитических реактивов
- § 14. Способы повышения чувствительности реакций
- § 15. Маскировка мешающих ионов
- § 16. Определение pH среды
- § 17. Регулирование pH среды в процессе аналитических определений
- В. РЕАКТИВЫ
- § 18. Понятие о химических реактивах
- § 19. Концентрация применяемых реактивов
- § 20. Техника пользования реактивами
- Г. ПОСУДА И ПРИБОРЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕННОМ АНАЛИЗЕ
- § 21. Химическая посуда
- § 22. Приборы
- Д. АНАЛИТИЧЕСКИЕ ГРУППЫ
- § 23. Дробный и систематический анализ
- § 24. Аналитическая классификация катионов
- § 25. Сводные таблицы действия реактивов на катионы и анионы
- Е. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ ИОНОВ
- § 26. Значение периодического закона в аналитической химии
- § 27. Периодическая система элементов Д. И. Менделеева как классификация атомов по их строению
- § 28. Зависимость некоторых химических свойств элементов от положения их в периодической системе Д. И. Менделеева
- § 29. Растворимость химических соединений в связи с положением элементов в периодической системе Д. И. Менделеева
- § 30. Открытие новых аналитических реакций
- § 31. Аналитические группы и периодическая система элементов Д. И. Менделеева
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ КАТИОНОВ И АНАЛИЗ СМЕСЕЙ КАТИОНОВ
- § 1. Характеристика первой аналитической группы катионов
- § 2. Общие реакции катионов первой аналитической группы
- РЕАКЦИИ КАТИОНОВ 1-й ПОДГРУППЫ
- § 3. Обнаружение NН-ионов
- § 4. Методы разложения и удаления солей аммония
- § 5. Обнаружение K-ионов
- § 6. Обнаружение Rb-ионов
- § 7. Обнаружение Cs-ионов
- § 8. Анализ смеси катионов первой подгруппы
- РЕАКЦИИ КАТИОНОВ 2-й ПОДГРУППЫ
- § 9. Обнаружение Li-ионов
- § 10. Обнаружение Na-ионов
- § 11. Обнаружение Mg-ионов
- § 12. Обзор действия реактивов на катионы первой аналитической группы
- § 13. Анализ смеси катионов второй подгруппы
- § 14. Анализ смеси ионов
- § 15. Анализ смеси ионов
- ГЛАВА V. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика второй аналитической группы катионов
- § 2. Общие реакции катионов второй аналитической группы
- § 3. Обнаружение Ca-ионов
- § 4. Обнаружение Sr-ионов
- § 5. Обнаружение Ba-ионов
- § 6. Обзор действия реактивов на катионы второй аналитической группы
- § 7. Основы теории осаждения катионов второй аналитической группы групповым реактивом—карбонатом аммония
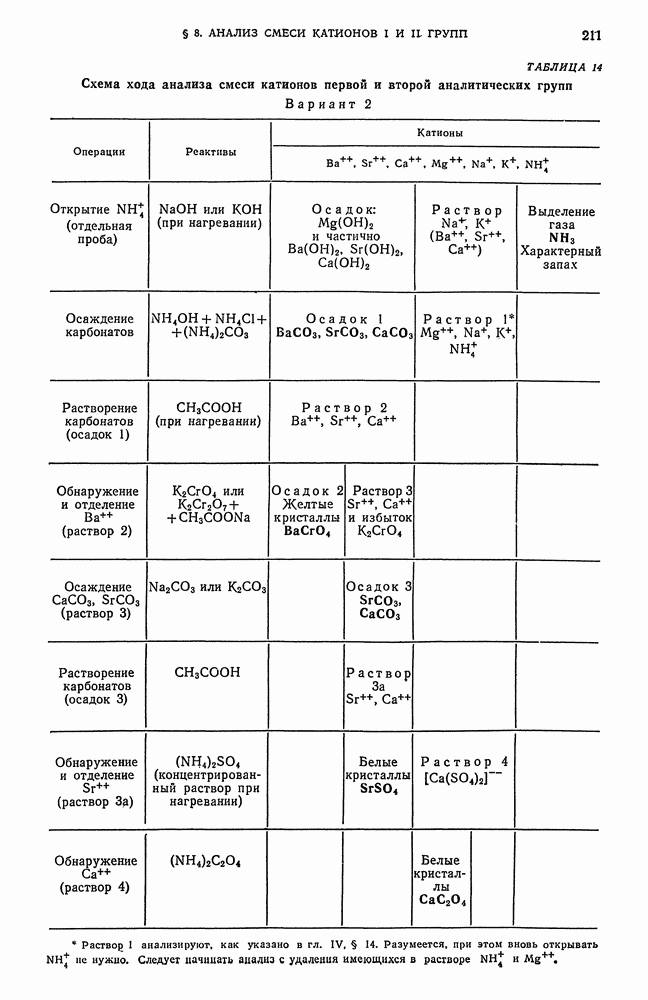
- § 8. Систематический ход анализа смеси катионов первой и второй аналитических групп
- § 9. Систематический ход анализа смеси катионов первой и второй аналитических групп в присутствии ионов
- § 10. Теоретические основы перевода сульфатов катионов второй аналитической группы в карбонаты
- ГЛАВА VI. ТРЕТЬЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика третьей аналитической группы катионов
- § 2. Общие реакции катионов третьей аналитической группы
- § 3. Обнаружение Be-ионов
- § 4. Обнаружение Al-ионов
- § 5. Обнаружение ионов титана (IV)
- § 6. Обнаружение Cr-ионов
- § 7. Обнаружение Mn-ионов
- § 8. Обнаружение Fe-ионов
- § 9. Обнаружение Fe-ионов
- § 10. Обнаружение Co-ионов
- § 13. Обнаружение ионов циркония (IV)
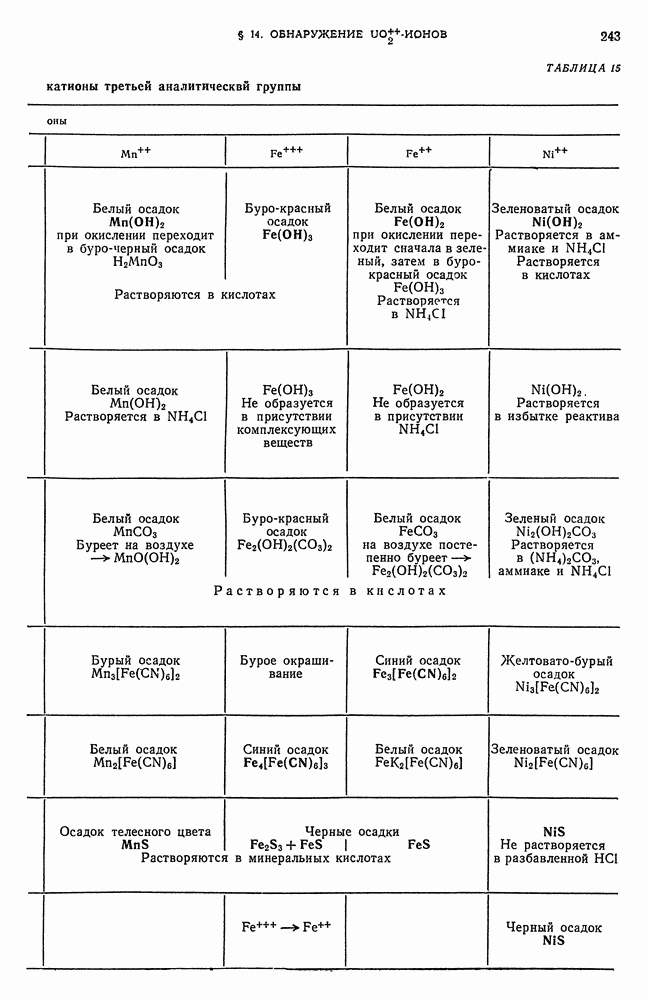
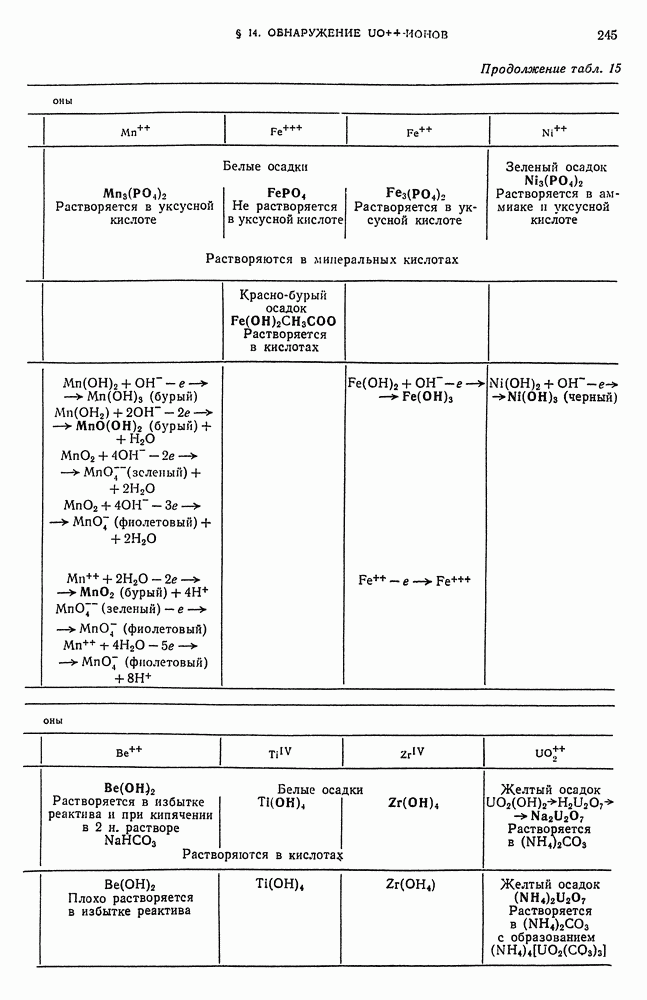
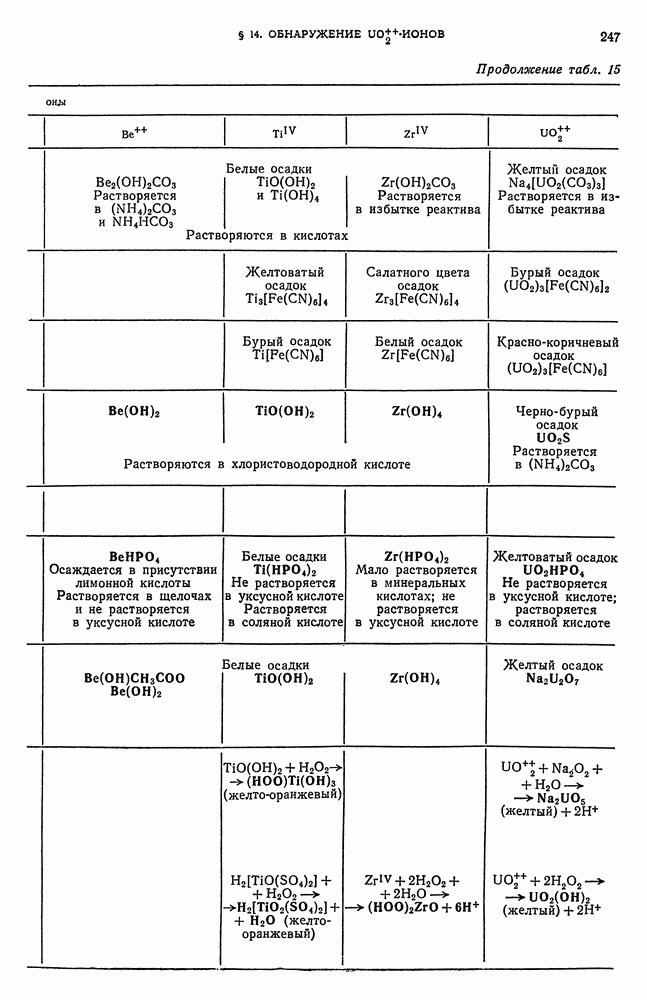
- § 14. Обнаружение UO-ионов
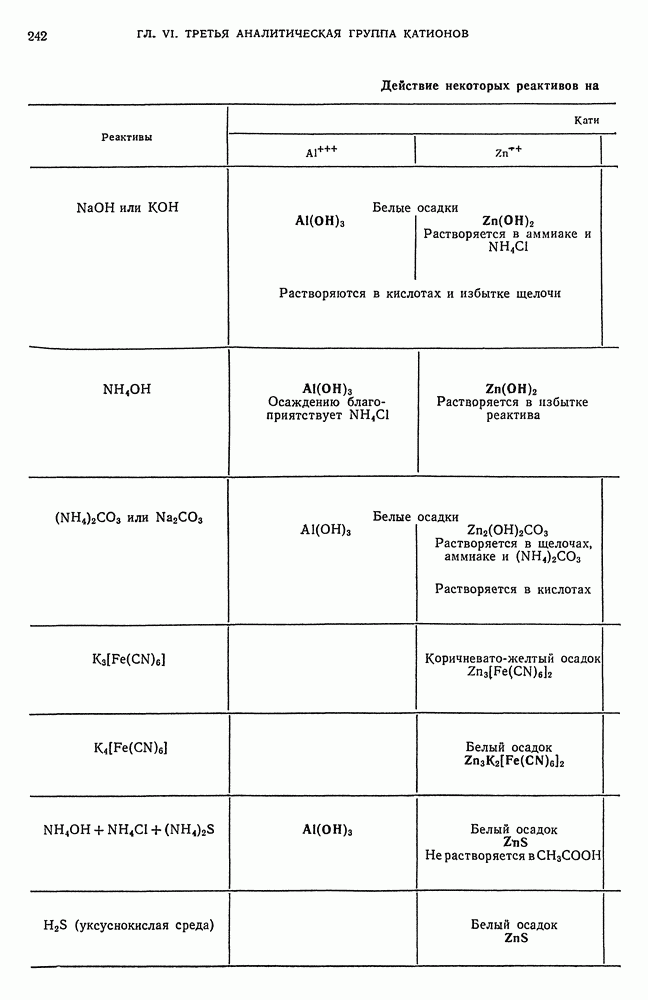
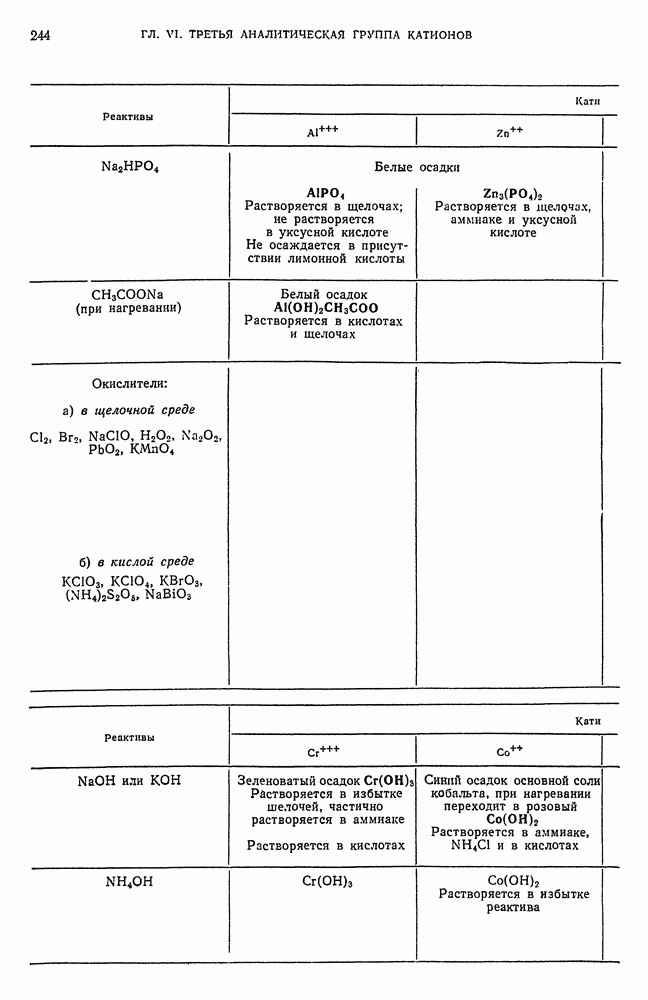
- § 15. Обзор действия реактивов на катионы третьей аналитической группы
- § 16. Использование коллоидных систем в химическом анализе
- § 17. Основы теории осаждения катионов третьей аналитической группы групповым реактивом — сульфидом аммония
- § 18. Теоретические основы применения органических реактивов в качественном анализе неорганических веществ
- § 19. Методы разделения некоторых катионов третьей аналитической группы
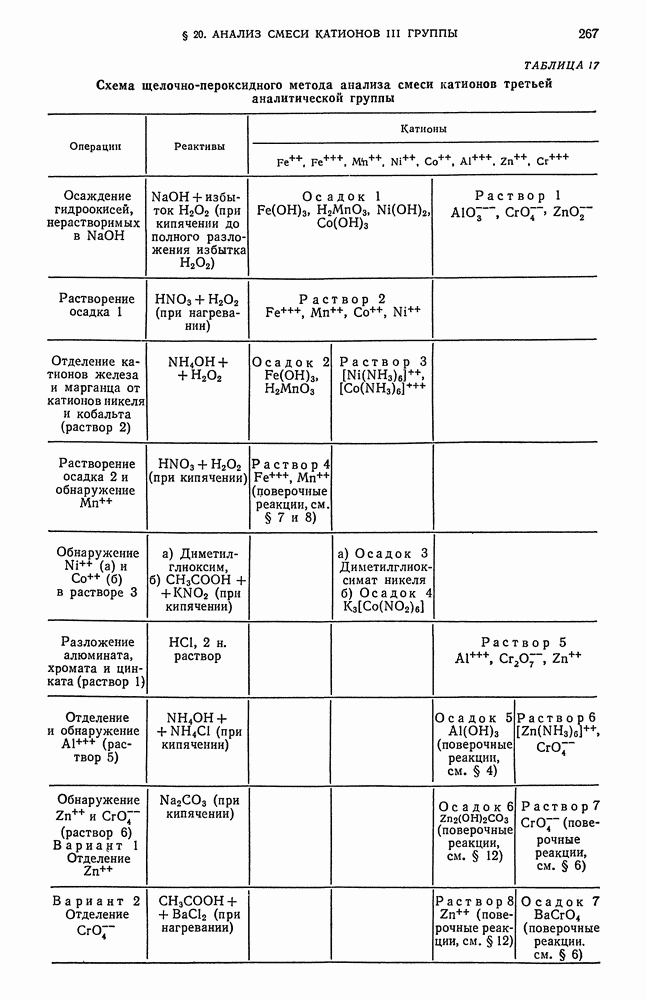
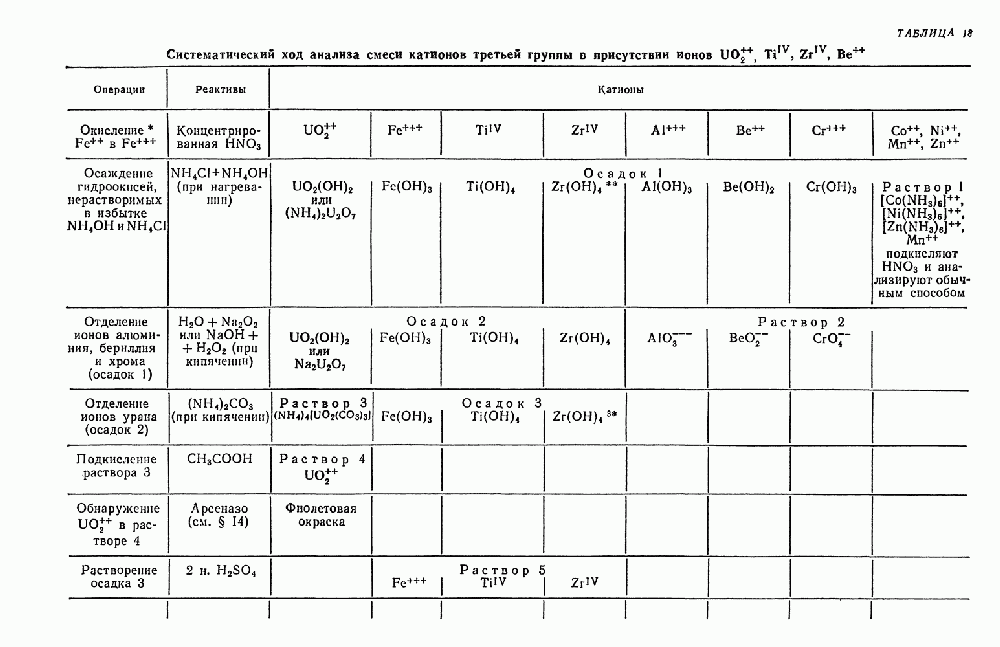
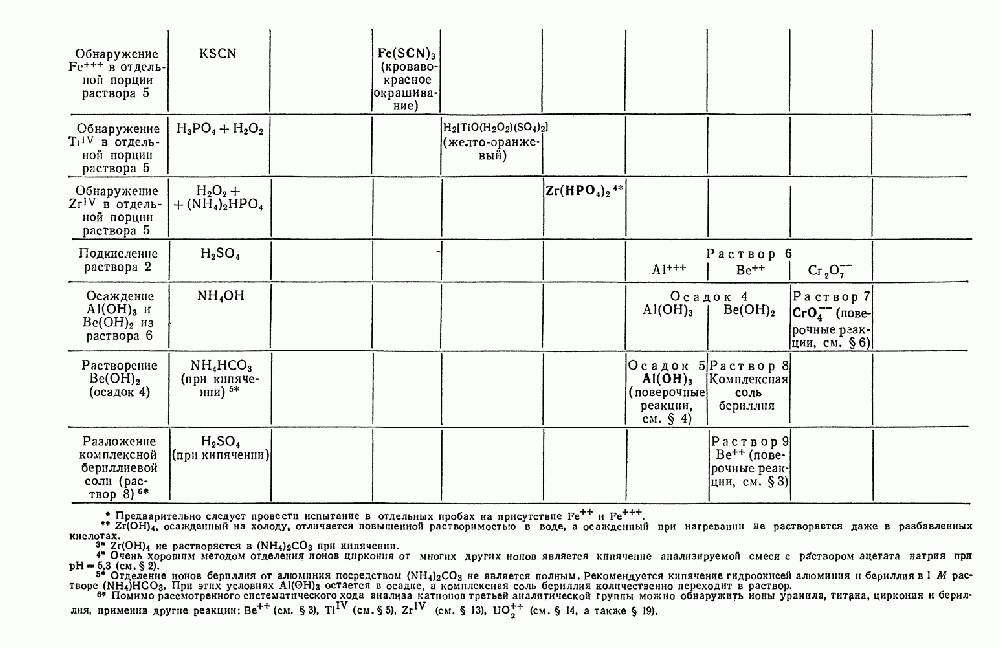
- § 20. Систематический ход анализа смеси катионов третьей аналитической группы
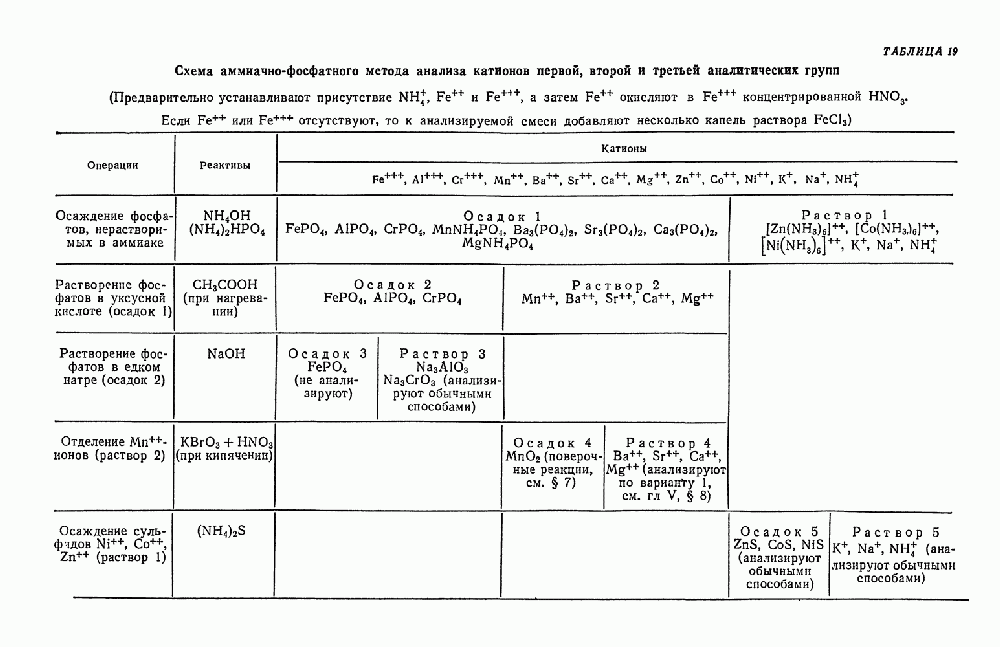
- § 21. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп
- § 22. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп в присутствии PO-ионов
- ГЛАВА VII. ЧЕТВЕРТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика четвертой аналитической группы катионов
- § 2. Общие реакции катионов четвертой аналитической группы
- РЕАКЦИИ КАТИОНОВ ПЕРВОЙ ПОДГРУППЫ (ПОДГРУППЫ МЕДИ)
- § 3. Обнаружение Hg-ионов
- § 4. Обнаружение Cu-ионов
- § 5. Обнаружение Cd-ионов
- § 6. Обнаружение Bi-ионов
- РЕАКЦИИ КАТИОНОВ ВТОРОЙ ПОДГРУППЫ (ПОДГРУППЫ МЫШЬЯКА)
- § 7. Обнаружение ионов мышьяка (III)
- § 8. Обнаружение ионов мышьяка (V)
- § 9. Общие реакции обнаружения
- § 10. Обнаружение ионов сурьмы (III)
- § 11. Обнаружение ионов сурьмы (V)
- § 12. Общие реакции обнаружения Sb
- § 13. Обнаружение ионов олова (II)
- § 14. Обнаружение ионов олова (IV)
- § 15. Общие реакции обнаружения ионов олова (II) и олова (IV)
- § 16. Отделение ионов олова от других ирнов четвертой аналитической группы
- § 17. Обнаружение ионов германия (IV)
- § 18. Отделение ионов германия от других ионов четвертой аналитической группы
- § 19. Обзор действия реактивов на катионы четвертой аналитической группы
- § 20. Основы теории осаждения сульфидов катионов четвертой аналитической группы групповым реактивом — сероводородом
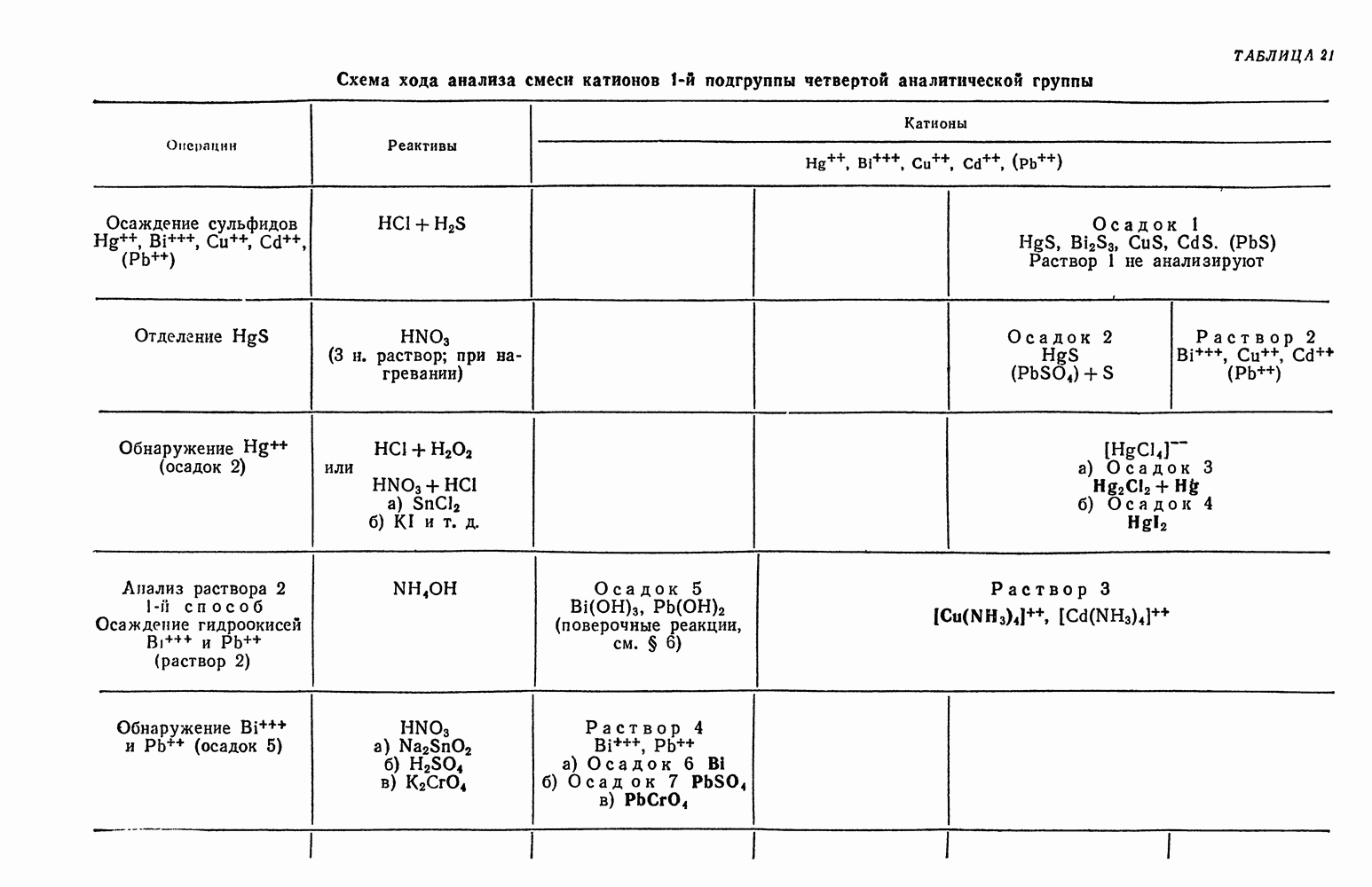
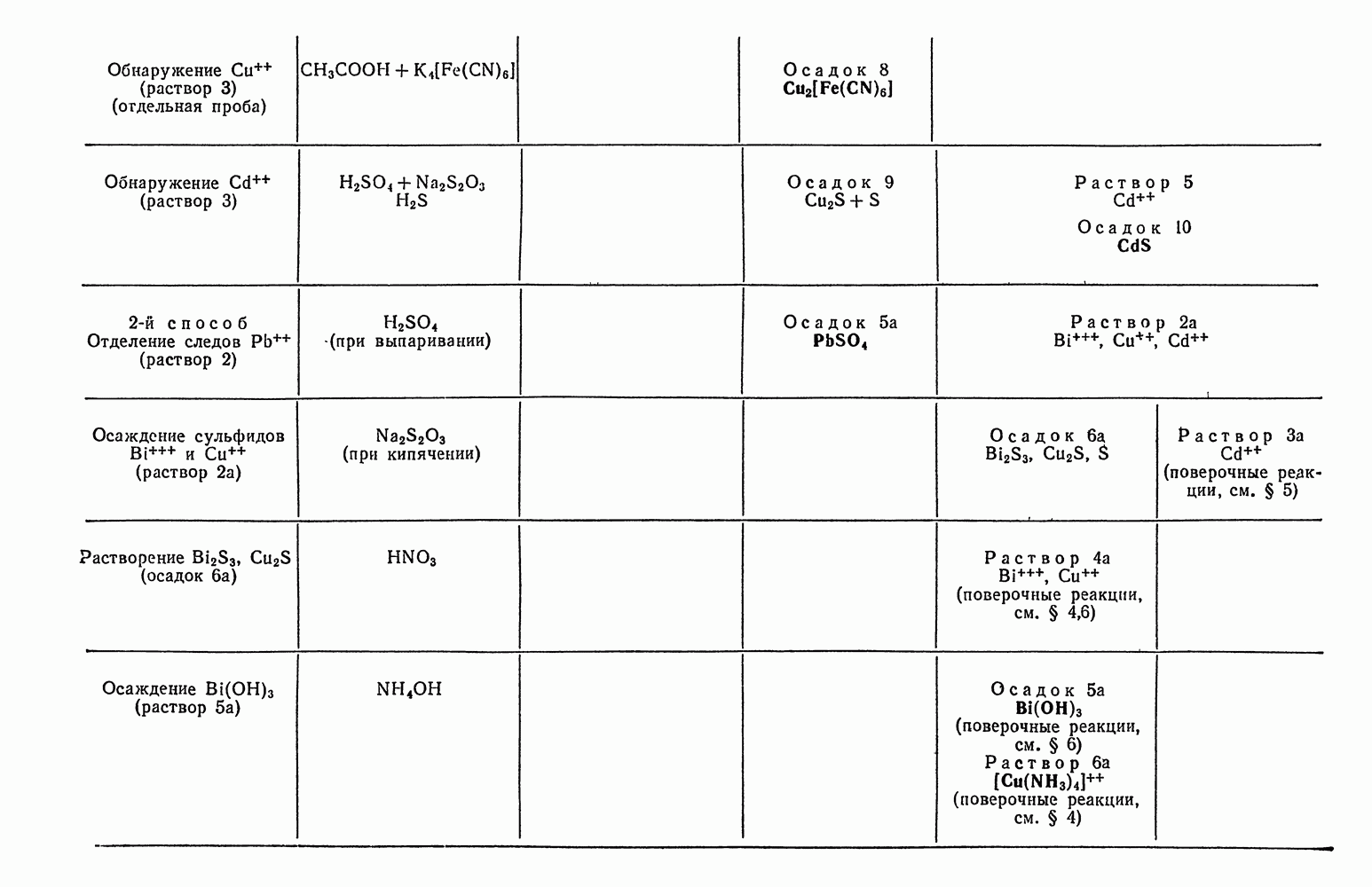
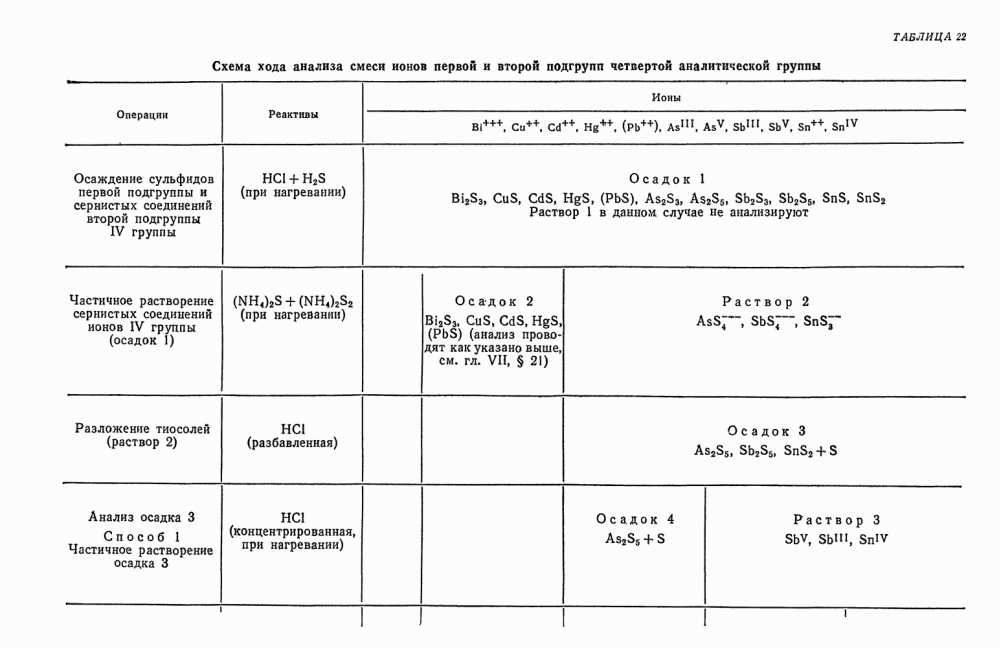
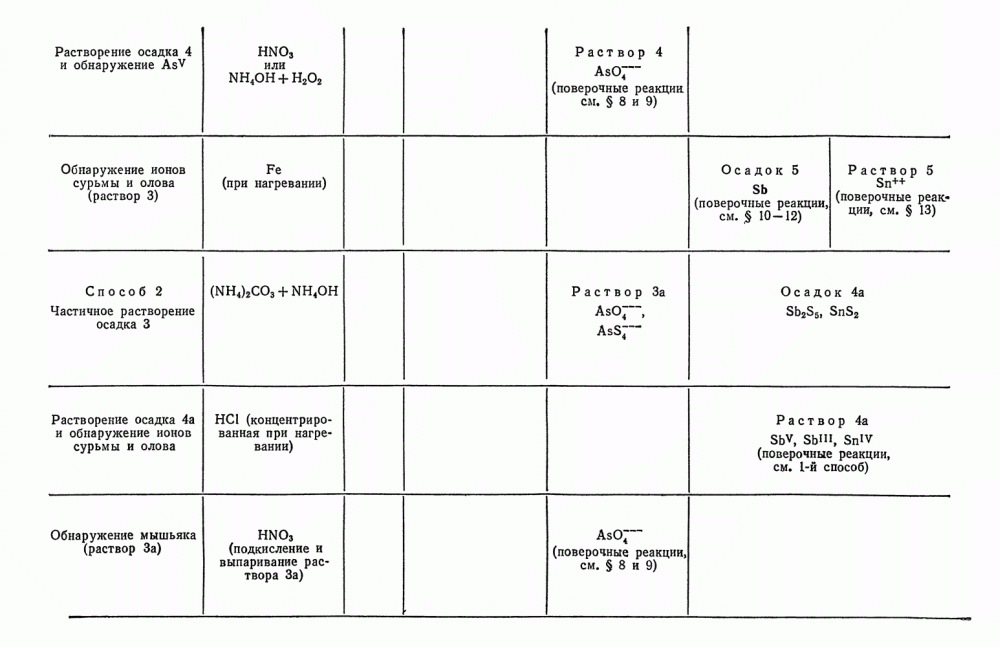
- § 21. Систематический ход анализа смеси катионов четвертой аналитической группы
- ГЛАВА VIII. ПЯТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ (ГРУППА СЕРЕБРА)
- § 1. Характеристика пятой аналитической группы катионов
- § 2. Общие реакции катионов пятой аналитической группы
- § 3. Обнаружение Ag-ионов
- § 4. Обнаружение [Hg]-ионов
- § 5. Обнаружение Pb-ионов
- § 6. Обзор действия реактивов на катионы пятой аналитической группы
- § 7. Систематический ход анализа смеси катионов пятой аналитической группы
- ГЛАВА IX. АНАЛИЗ СМЕСИ ИОНОВ ВСЕХ ПЯТИ АНАЛИТИЧЕСКИХ ГРУПП
- § 1. Сероводородный метод анализа
- § 2. Недостатки сероводородного метода анализа
- § 3. Ошибки, возникающие при анализе смеси ионов пяти аналитических групп
- § 4. Бессероводородные методы анализа
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ АНИОНОВ И АНАЛИЗ СМЕСЕЙ АНИОНОВ
- § 1. Аналитическая классификация анионов
- § 2. Групповые реактивы на анионы
- § 3. Классификация методов анализа анионов
- ГЛАВА XI. ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика первой группы анионов
- § 2. Реакции анионов первой группы
- § 3. Обнаружение CI-ионов
- § 4. Обнаружение Br-ионов
- § 5. Обнаружение I-ионов
- § 6. Обнаружение CN-ионов
- § 7. Обнаружение SCN-ионов
- § 8. Обнаружение [Fe(CN)]-ионов
- § 9. Обнаружение Fe(CN)-ионов
- § 10. Обнаружение NO-ионов
- § 11. Обнаружение NO2-ионов
- § 12. Обнаружение S-ионов
- § 13. Обнаружение CH3COOO-ионов
- § 14. Обнаружение BrO3-ионов
- § 15. Обнаружение ClO3-ионов
- § 16. Обнаружение ClO4-ионов
- § 17. Обзор действия реактивов на анионы первой группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 18. Анализ смеси Cl, Br и I-ионов
- § 19. Анализ смеси Cl, Br, I и SCN-ионов
- § 20. Анализ смеси Cl, ClO3 и ClO4-ионов
- § 21. Анализ смеси NO2 и NO3-ионов
- § 22. Анализ смеси анионов первой группы
- ГЛАВА XII. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика второй группы анионов
- § 2. Общие реакции анионов второй группы
- § 3. Обнаружение SO3-ионов
- § 4. Обнаружение S2O3-ионов
- § 5. Обнаружение S2O3 в присутствии SO3-ионов
- § 6. Обнаружение SO4-ионов
- § 7. Обнаружение CO3-ионов
- § 8. Обнаружение CO3-ионов в присутствии SO3 и S2O3-ионов
- § 9. Обнаружение PO4-ионов
- § 10. Обнаружение CrO4-ионов
- § 11. Обнаружение AsO3-ионов
- § 12. Обнаружение AsO4-ионов
- § 13. Обнаружение BO2 и BO3-ионов
- § 14. Обнаружение SiO3-ионов
- § 15. Обнаружение F-ионов
- § 16. Обнаружение C2O4-ионов
- § 17. Обнаружение VO3-ионов
- § 18. Обнаружение MoO4-ионов
- § 19. Обнаружение WO4-ионов
- § 20. Обзор действия реактивов на анионы второй группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 21. Анализ смеси ионов
- § 22. Анализ смеси SO3, SO4, S2O3 и CO3-ионов
- § 23. Анализ смеси VO2, MoO4 и WO4-ионов
- § 24. Анализ смеси анионов второй группы
- § 25. Анализ смеси анионов первой и второй групп
- ГЛАВА XIII. ОБНАРУЖЕНИЕ СВОБОДНЫХ МЕТАЛЛОВ И НЕМЕТАЛЛОВ, ИДЕНТИФИЦИРОВАНИЕ СОЛЕЙ И ДРУГИХ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И АНАЛИЗ ИХ СМЕСЕЙ
- § 1. Подготовка вещества к анализу
- § 2. Предварительные испытания
- § 3. Растворение анализируемого вещества в воде, кислотах и щелочах
- § 4. Переведение в растворимое состояние веществ, нерастворимых в воде, кислотах и щелочах
- § 5. Анализ неизвестного вещества
- § 6. Обнаружение свободных элементов
- § 7. Идентифицирование солей и других индивидуальных соединений
- § 8. Обнаружение микропримесей
- § 9. Анализ сплавов
- § 10. Анализ силикатов и алюмосиликатов
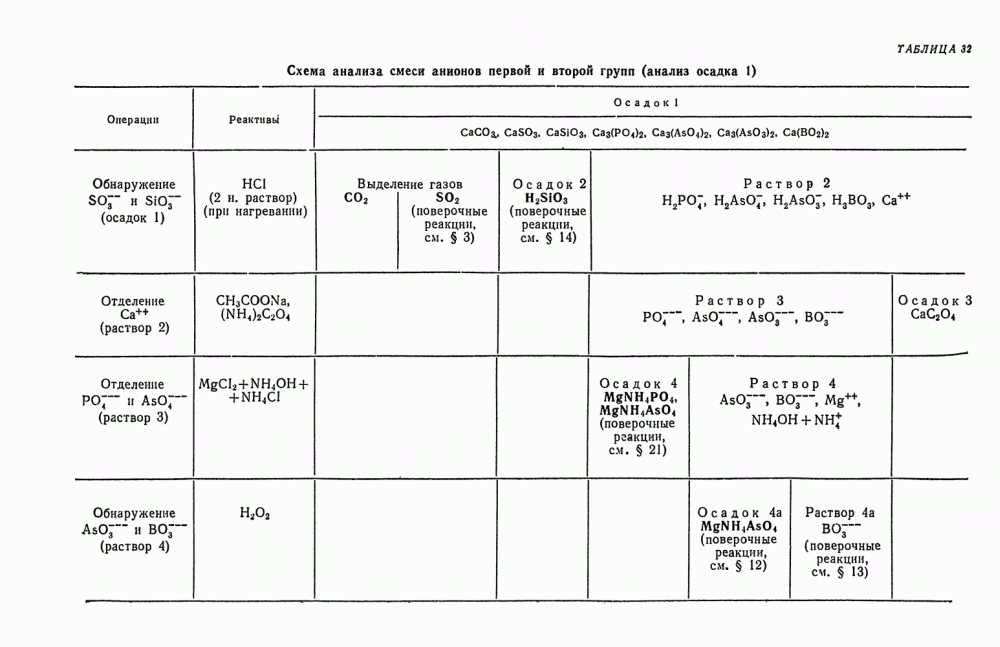
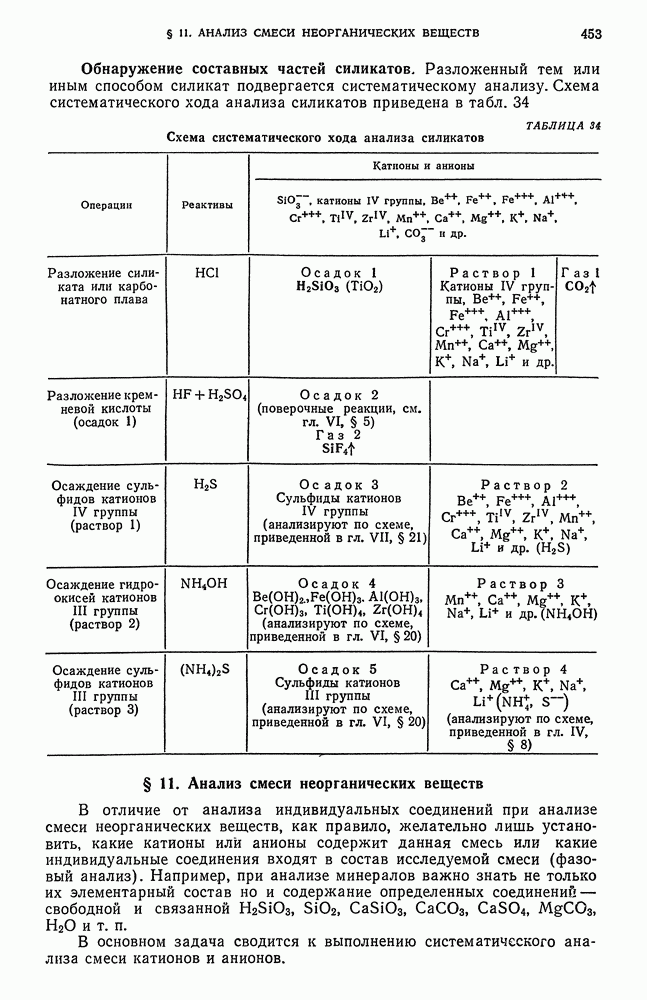
- § 11. Анализ смеси неорганических веществ
- § 12. Экспрессный метод анализа смесей катионов и анионов
- § 13. Идентифицирование нерастворимых веществ
- ЛИТЕРАТУРА