| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
§ 16. Буферные растворы
В 0,001 н. растворе хлористоводородной кислоты  . При разбавлении данного раствора в 10 раз концентрация ионов водорода во вновь полученном растворе тоже уменьшится в 10 раз и станет равной
. При разбавлении данного раствора в 10 раз концентрация ионов водорода во вновь полученном растворе тоже уменьшится в 10 раз и станет равной  . При добавлении к исходному раствору
. При добавлении к исходному раствору  более концентрированного раствора
более концентрированного раствора  , например равного объема 0,2 н. раствора
, например равного объема 0,2 н. раствора  , концентрация ионов водорода во вновь полученном растворе увеличивается:
, концентрация ионов водорода во вновь полученном растворе увеличивается:

При добавлении к 0,01 н. раствору  эквивалентного количества
эквивалентного количества  раствор станет нейтральным, а величина
раствор станет нейтральным, а величина  уменьшится и будет равна
уменьшится и будет равна  .
.
Следовательно, если к разбавленным растворам сильных кислот или оснований добавлять воду, кислоты или щелочи, то происходят резкие изменения  .
.
В смесях водных растворов слабых кислот и их солей, а также в смесях слабых оснований и их солей концентрации ионов водорода и гидроксила зависят не от абсолютных количеств, а от соотношений кислоты или основания и их солей. Это значит, что величина  в таких смесях не зависит от разбавления смеси. В самом деле, если подобную смесь разбавить в 10 раз, то в 10 раз уменьшится концентрация компонентов смеси, а соотношение кислоты или основания и их солей не изменится и величина
в таких смесях не зависит от разбавления смеси. В самом деле, если подобную смесь разбавить в 10 раз, то в 10 раз уменьшится концентрация компонентов смеси, а соотношение кислоты или основания и их солей не изменится и величина  останется постоянной. Свойство некоторых растворов сохранять неизменной концентрацию ионов водорода при разбавлении, а также, что будет показано ниже, при добавлении к ним небольших количеств сильных кислот или щелочей, известно под названием буферного действия (см. книга 2, гл. II, § 5 и
останется постоянной. Свойство некоторых растворов сохранять неизменной концентрацию ионов водорода при разбавлении, а также, что будет показано ниже, при добавлении к ним небольших количеств сильных кислот или щелочей, известно под названием буферного действия (см. книга 2, гл. II, § 5 и  ).
).
Растворы, содержащие одновременно какую-либо слабую кислоту и ее соль или какое-либо слабое основание и его соль и оказывающие буферное действие, называют буферными растворами. Буферные растворы можно рассматривать как смеси электролитов, имеющих одноименные ионы. Присутствие в растворе слабой кислоты или слабого основания и их солей уменьшает влияние разбавления или действия других кислот и оснований на  раствора.
раствора.
Такими буферными растворами являются следующие смеси:  и др.
и др.
Буферные растворы, представляющие собой смеси слабых кислот и их солей, как правйло, имеют кислую реакцию  . Например, буферная смесь 0,1 М раствора
. Например, буферная смесь 0,1 М раствора  М раствора
М раствора  имеет
имеет 
Буферные растворы, представляющие собой смеси слабых оснований и их солей, как правило, имеют щелочную реакцию  . Например, буферная смесь 0,1 М раствора
. Например, буферная смесь 0,1 М раствора  М раствора
М раствора  имеет
имеет  .
.
Интересно отметить, что растворы некоторых индивидуальных солей, образованных катионами сильных оснований и анионами слабых кислот или катионами слабых оснований и анионами сильных кислот и характеризующиеся шелочной или кислой реакцией, также обладают буферным действием. Например, буферное действие прояв-» ляет раствор тетрабората натрия (буры)  , характеризующийся щелочной реакцией
, характеризующийся щелочной реакцией  и раствор битартрата калия
и раствор битартрата калия  , характеризующийся кислой реакцией
, характеризующийся кислой реакцией  .
.
Буферное действие растворов индивидуальных солей объясняется возникновением в процессе гидролиза кислот и оснований. Например, в растворе тетрабората натрия:

в растворе битартрата калия:

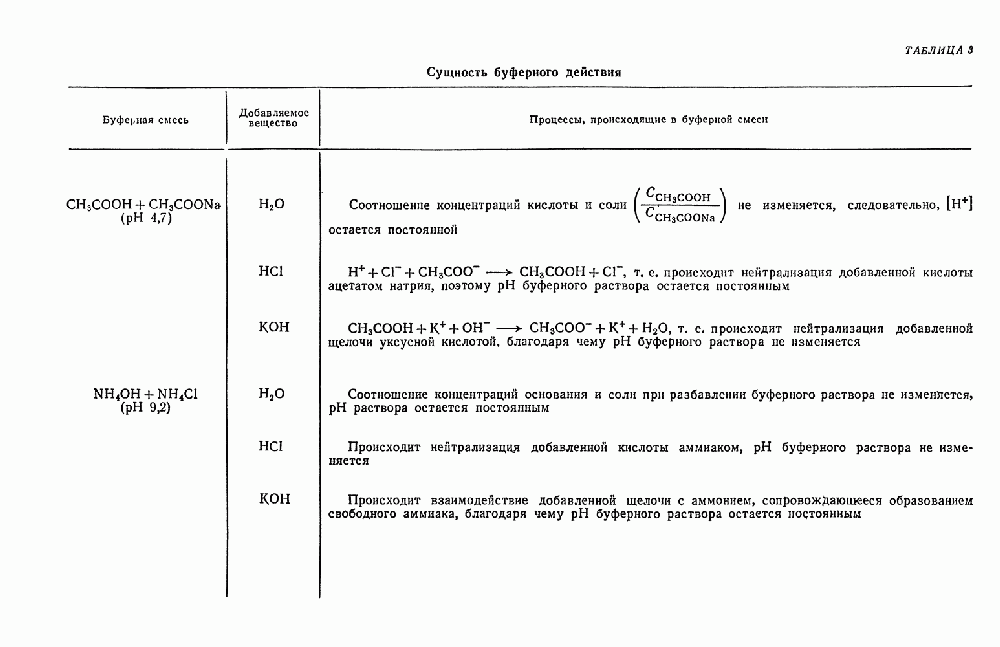
Сущность буферного действия. Действие буферных растворов основано на том, что отдельные компоненты буферных смесей связывают ионы водорода или гидроксила вводимых в них кислот или оснований с образованием слабых электролитов. Например, если к буферному раствору, содержащему слабую кислоту  и соль этой кислоты
и соль этой кислоты  , прибавить сильное основание, то произойдет реакция образования слабого электролита — воды:
, прибавить сильное основание, то произойдет реакция образования слабого электролита — воды:

Вместо израсходованных ионов водорода, вследствие последующей диссоциации кислоты  , появляются новые ионы водорода. В результате прежняя концентрация
, появляются новые ионы водорода. В результате прежняя концентрация  -ионов в буферном растворе восстановится до ее первоначального значения.
-ионов в буферном растворе восстановится до ее первоначального значения.
Если к указанной буферной смеси прибавить сильную  то произойдет реакция
то произойдет реакция

т. е.  -ионы, образующиеся при электролитической диссоциации соли
-ионы, образующиеся при электролитической диссоциации соли  , соединяясь с ионами водорода прибавленной кислоты, образуют молекулы слабой кислоты. Поэтому концентрация ионов водорода от прибавления сильной кислоты к буферной смеси тоже практически не изменится. Подобным же образом можно объяснить действие других буферных смесей (табл. 3).
, соединяясь с ионами водорода прибавленной кислоты, образуют молекулы слабой кислоты. Поэтому концентрация ионов водорода от прибавления сильной кислоты к буферной смеси тоже практически не изменится. Подобным же образом можно объяснить действие других буферных смесей (табл. 3).
Буферная емкость. Способность буферных растворов поддерживать постоянство значения  небезгранична и зависит от качественного состава буферного раствора и концентрации его компонентов. При добавлении к буферному раствору значительных количеств сильной кислоты или сильного основания наблюдается заметное изменение
небезгранична и зависит от качественного состава буферного раствора и концентрации его компонентов. При добавлении к буферному раствору значительных количеств сильной кислоты или сильного основания наблюдается заметное изменение  . Причем для различных буферных смесей, отличающихся друг от друга по составу, буферное действие неодинаково. Следовательно, буферные смеси можно различать по силе оказываемого ими сопротивления по отношению к действию кислот и оснований, вводимых в буферный раствор в одинаковых количествах и определенной концентрации. Предельное количество кислоты или основания определенной концентрации
. Причем для различных буферных смесей, отличающихся друг от друга по составу, буферное действие неодинаково. Следовательно, буферные смеси можно различать по силе оказываемого ими сопротивления по отношению к действию кислот и оснований, вводимых в буферный раствор в одинаковых количествах и определенной концентрации. Предельное количество кислоты или основания определенной концентрации  или
или  , которое можно добавить к
, которое можно добавить к  буферного раствора, чтобы значение
буферного раствора, чтобы значение  его изменилось только на единицу, называют буферной емкостью.
его изменилось только на единицу, называют буферной емкостью.
Если величина  одного буферного раствора изменяется при добавлении сильной кислоты меньше, чем величина
одного буферного раствора изменяется при добавлении сильной кислоты меньше, чем величина  другого буферного раствора при добавлении того же количества кислоты, то первая смесь обладает большей буферной емкостью. Для одного и того же буферного раствора буферная емкость тем больше, чем выше концентрация его компонентов.
другого буферного раствора при добавлении того же количества кислоты, то первая смесь обладает большей буферной емкостью. Для одного и того же буферного раствора буферная емкость тем больше, чем выше концентрация его компонентов.
Пример 1. Определите, какая будет среда раствора, если к  прибавить хлористоводородную кислоту.
прибавить хлористоводородную кислоту.
Решение. При смешении  могут быть три случая:
могут быть три случая:
1) смешаны эквивалентные количества  :
:

2) кислоты взято больше требуемого эквивалентного количества:

Таблица 3. Сущность буферного действия

3) кислоты взято меньше эквивалентного количества:

избыток
В первом случае  обусловливается концентрацией образовавшейся уксусной кислоты, т. е. среда полученного раствора будет слабокислой.
обусловливается концентрацией образовавшейся уксусной кислоты, т. е. среда полученного раствора будет слабокислой.
Во втором случае  обусловливается концентрацией избыточной
обусловливается концентрацией избыточной  , т. е. среда будет кислой.
, т. е. среда будет кислой.
В третьем случае  обусловливается соотношением концентрации полученной уксусной кислоты и избытка
обусловливается соотношением концентрации полученной уксусной кислоты и избытка  , т. е. среда может оказаться слабокислой, нейтральной и слабощелочной. Если
, т. е. среда может оказаться слабокислой, нейтральной и слабощелочной. Если

тогда  слабокислая.
слабокислая.
Если указанное отношение больше 1 — среда кислая; равно  — нейтральная; меньше
— нейтральная; меньше  — щелочная. (См. книга 2, гл. II, § 5 и сл.).
— щелочная. (См. книга 2, гл. II, § 5 и сл.).
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Анализ и синтез
- § 2. Предмет аналитической химии
- § 3. Развитие аналитической химии
- § 4. Качественный и количественный анализ
- ГЛАВА I. ПРИМЕНЕНИЕ ЗАКОНА ДЕЙСТВИЯ МАСС В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Влияние среды на состояние ионов в растворах
- § 2. Обратимые и необратимые аналитические реакции
- § 3. Направление аналитических реакций; правила обменного разложения
- § 4. Закон действия масс и следствие из него
- § 5. Границы применимости закона действия масс
- § 6. Сильные и слабые электролиты
- § 7. Активность
- § 8. Коэффициент активности и ионная сила
- Б. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ (В ГОМОГЕННЫХ СИСТЕМАХ)
- § 9. Гомогенные и гетерогенные системы
- § 10. Ионное произведение воды
- § 11. Ионы гидроксония
- § 12. Равновесие ионов в водных растворах; понятие о pH
- § 13. Равновесие в водных растворах слабых электролитов
- § 14. Влияние сильных кислот или сильных оснований на степень электролитической диссоциации слабых электролитов
- § 15. Приближенные формулы для расчета [H+] и [OH-] в водных растворах кислот и оснований
- В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
- § 16. Буферные растворы
- § 17. Применение буферных растворов в химическом анализе
- Г. РАВНОВЕСИЯ В РАСТВОРАХ ГИДРОЛИЗУЮЩИХСЯ СОЛЕЙ
- § 18. Теоретические основы гидролиза
- § 19. Механизм гидролитического расщепления
- § 20. Подавление и усиление гидролиза солей
- Д. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ТИПИЧНО АМФОТЕРНЫХ ЭЛЕКТРОЛИТОВ
- § 21. Поведение амфотерных гидроокисей в водных растворах
- § 22. Константы электролитической диссоциации амфотерных гидроокисей
- Е. РАВНОВЕСИЯ В СИСТЕМАХ: ОСАДОК-НАСЫЩЕННЫЙ РАСТВОР
- § 23. Осаждение как один из основных методов химического анализа
- § 24. Произведение растворимости
- § 25. Произведение активностей
- § 26. Вычисление растворимости электролитов в воде по величине произведения растворимости
- § 27. Влияние различных факторов на растворимость малорастворимых электролитов
- Ж. ОСНОВЫ ТЕОРИИ ОБРАЗОВАНИЯ И РАЗЛОЖЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИИ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 28. Характеристика комплексных соединений, имеющих значение в химическом анализе
- § 29. Квантовомеханические представления о строении комплексов
- § 30. Равновесия в растворах комплексных соединений
- § 31. Константы нестойкости комплексов
- § 32. Внутрикомплексные соединения
- § 33. Методы разложения и образования комплексов, применяемых в аналитической химии
- § 34. Применение метода комплексообразования в химическом анализе
- ГЛАВА II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Окисление—восстановление как один из основных методов химического анализа
- § 2. Направление реакций окисления—восстановления
- § 3. Окислительно-восстановительные потенциалы
- § 4. Зависимость между величинами окислительно-восстановительных потенциалов и условиями, в которых протекают реакции окисления—восстановления
- § 5. Вычисление окислительно-восстановительных потенциалов
- § 6. Вычисление окислительно-восстановительных потенциалов с учетом коэффициентов активности
- ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
- § 1. Обнаружение отдельных элементов
- § 2. Анализ мокрым и сухим путем
- § 3. Химические и физические методы качественного анализа
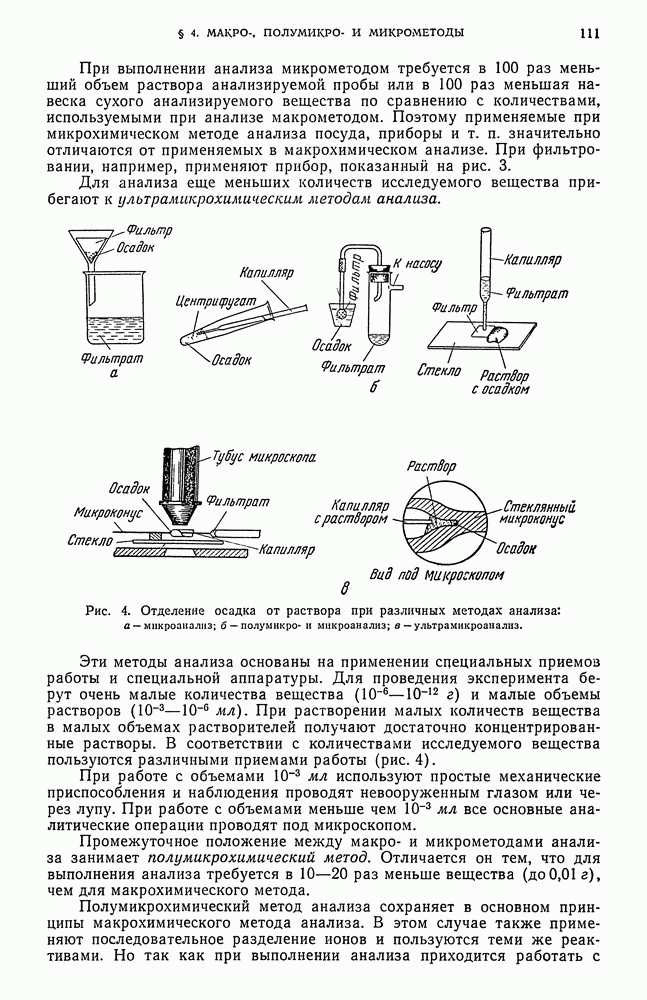
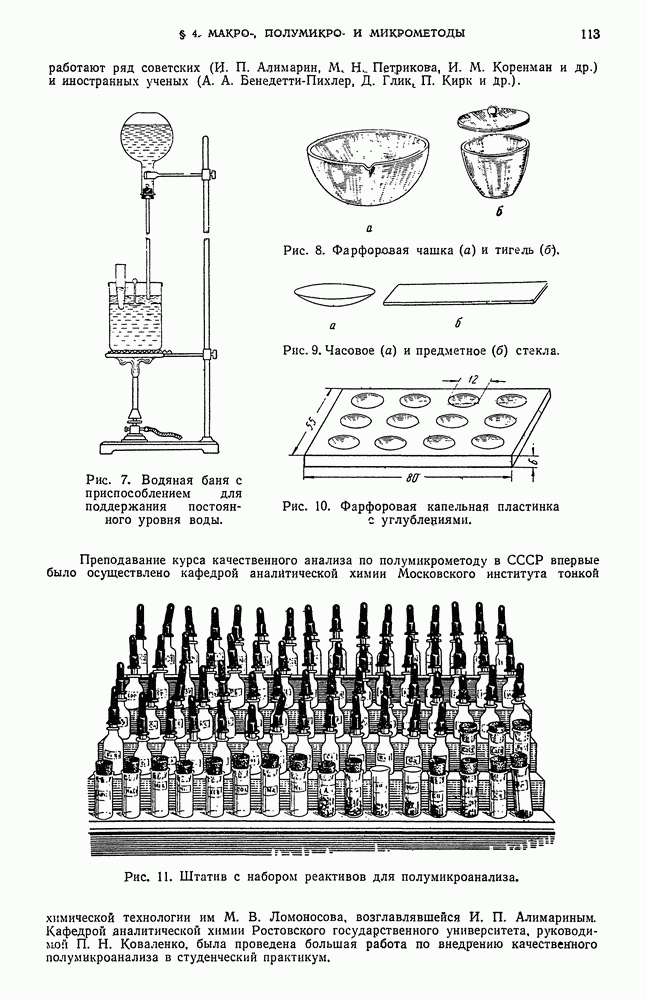
- § 4. Макро-, полумикро- и микрометоды
- § 5. Капельный анализ
- § 6. Микрокристаллоскопический анализ
- § 7. Метод растирания порошков
- § 8. Методы анализа, основанные на нагревании и сплавлении веществ
- § 9. Спектральный качественный анализ
- § 10. Хроматографический метод анализа
- § 11. Кинетические методы анализа
- Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
- § 12. Специфичность и чувствительность реакций
- § 13. Максимальная чувствительность аналитических реактивов
- § 14. Способы повышения чувствительности реакций
- § 15. Маскировка мешающих ионов
- § 16. Определение pH среды
- § 17. Регулирование pH среды в процессе аналитических определений
- В. РЕАКТИВЫ
- § 18. Понятие о химических реактивах
- § 19. Концентрация применяемых реактивов
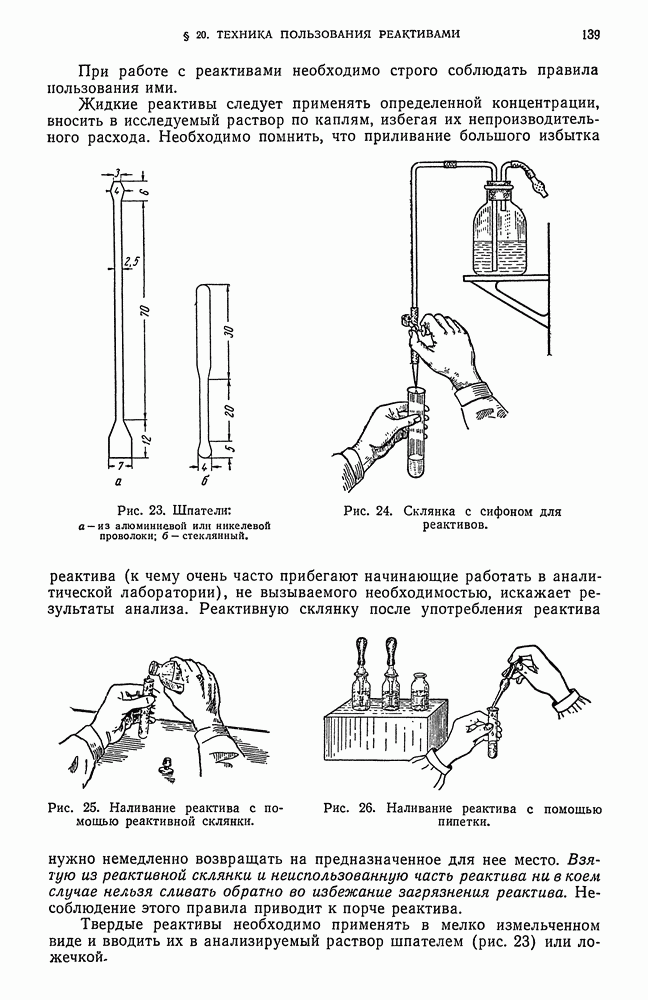
- § 20. Техника пользования реактивами
- Г. ПОСУДА И ПРИБОРЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕННОМ АНАЛИЗЕ
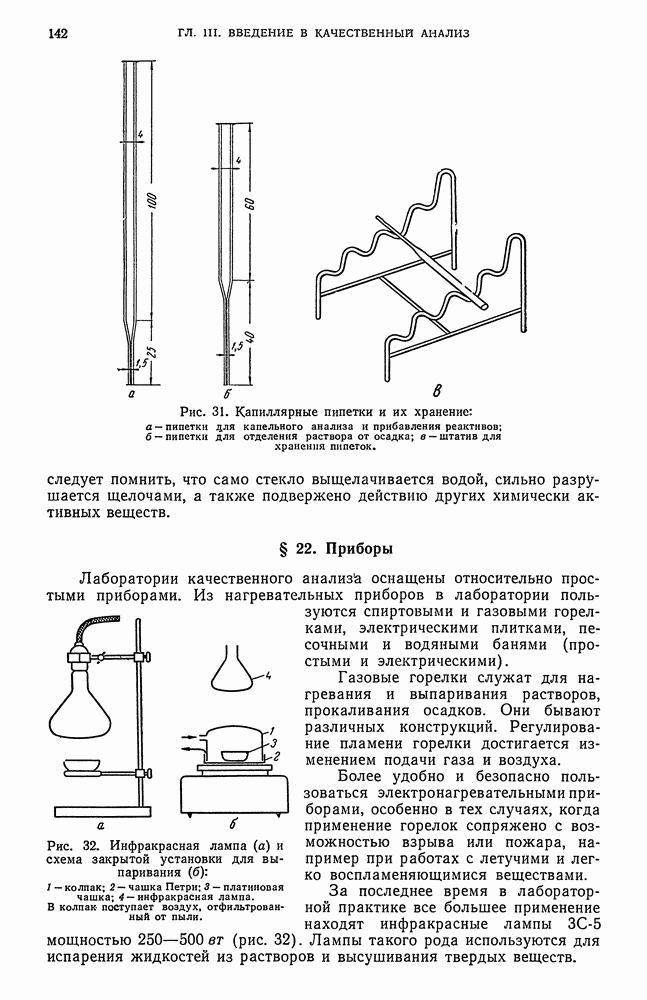
- § 21. Химическая посуда
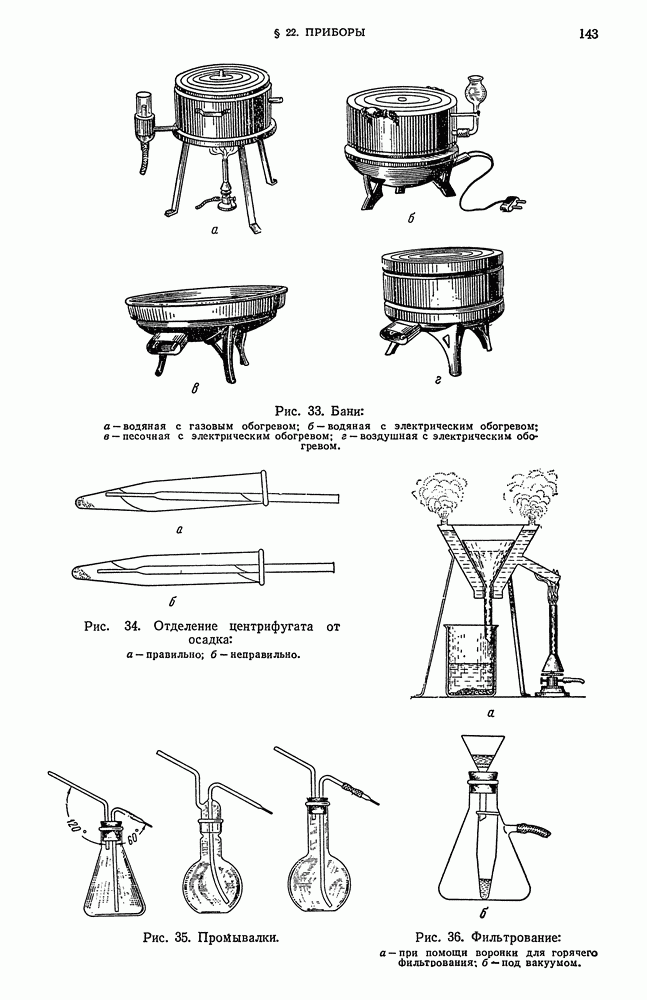
- § 22. Приборы
- Д. АНАЛИТИЧЕСКИЕ ГРУППЫ
- § 23. Дробный и систематический анализ
- § 24. Аналитическая классификация катионов
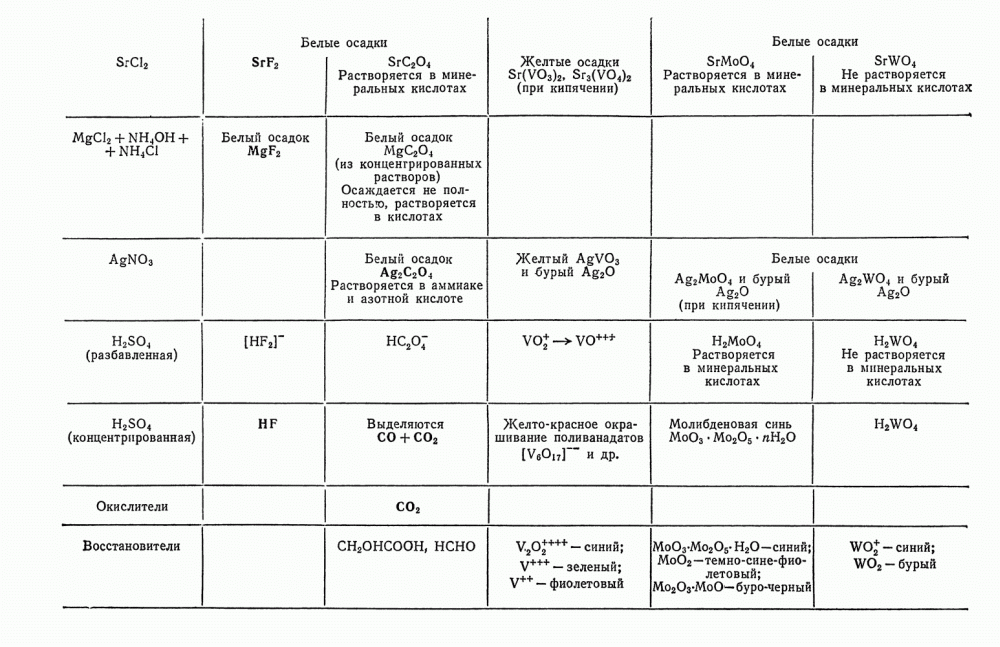
- § 25. Сводные таблицы действия реактивов на катионы и анионы
- Е. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ ИОНОВ
- § 26. Значение периодического закона в аналитической химии
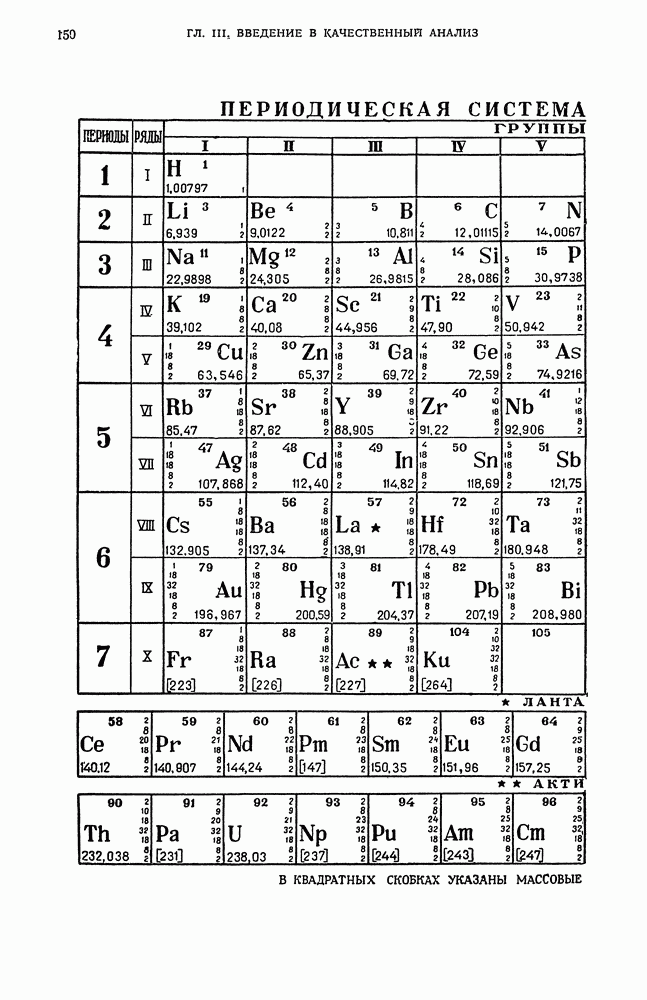
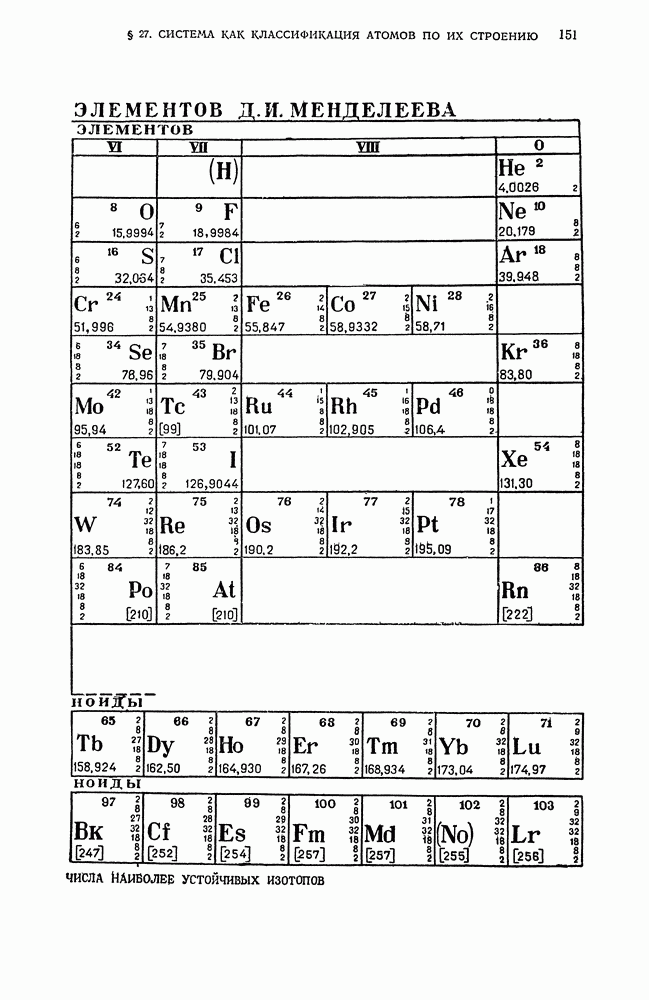
- § 27. Периодическая система элементов Д. И. Менделеева как классификация атомов по их строению
- § 28. Зависимость некоторых химических свойств элементов от положения их в периодической системе Д. И. Менделеева
- § 29. Растворимость химических соединений в связи с положением элементов в периодической системе Д. И. Менделеева
- § 30. Открытие новых аналитических реакций
- § 31. Аналитические группы и периодическая система элементов Д. И. Менделеева
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ КАТИОНОВ И АНАЛИЗ СМЕСЕЙ КАТИОНОВ
- § 1. Характеристика первой аналитической группы катионов
- § 2. Общие реакции катионов первой аналитической группы
- РЕАКЦИИ КАТИОНОВ 1-й ПОДГРУППЫ
- § 3. Обнаружение NН-ионов
- § 4. Методы разложения и удаления солей аммония
- § 5. Обнаружение K-ионов
- § 6. Обнаружение Rb-ионов
- § 7. Обнаружение Cs-ионов
- § 8. Анализ смеси катионов первой подгруппы
- РЕАКЦИИ КАТИОНОВ 2-й ПОДГРУППЫ
- § 9. Обнаружение Li-ионов
- § 10. Обнаружение Na-ионов
- § 11. Обнаружение Mg-ионов
- § 12. Обзор действия реактивов на катионы первой аналитической группы
- § 13. Анализ смеси катионов второй подгруппы
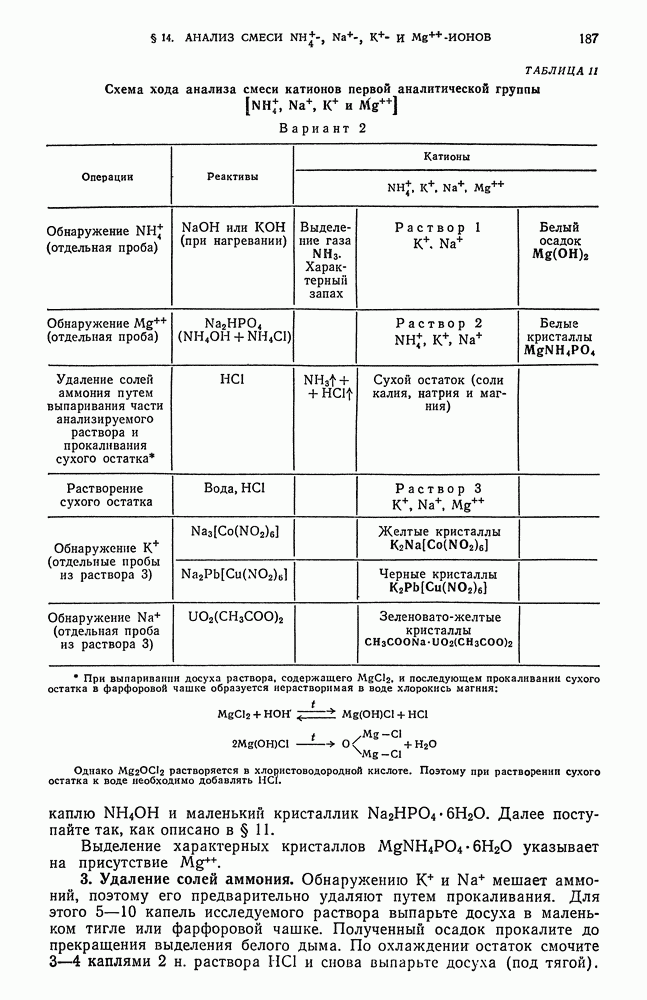
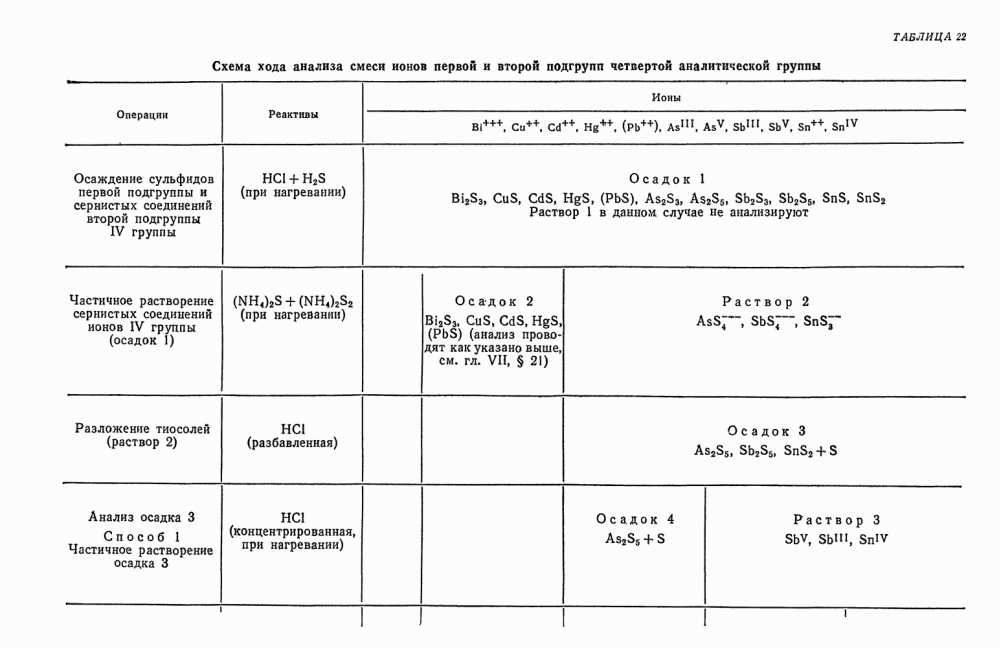
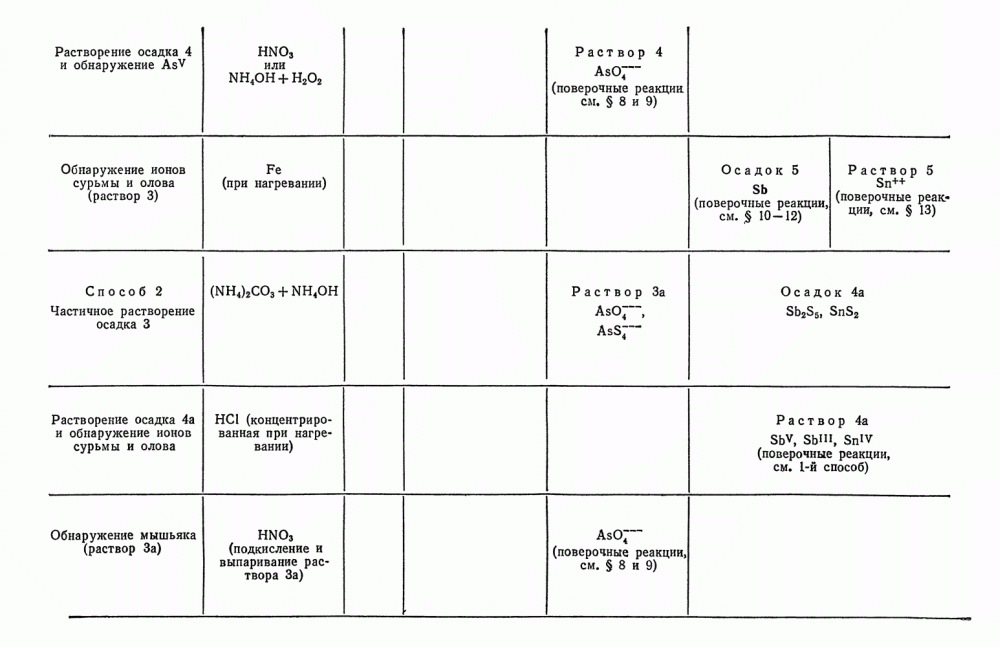
- § 14. Анализ смеси ионов
- § 15. Анализ смеси ионов
- ГЛАВА V. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика второй аналитической группы катионов
- § 2. Общие реакции катионов второй аналитической группы
- § 3. Обнаружение Ca-ионов
- § 4. Обнаружение Sr-ионов
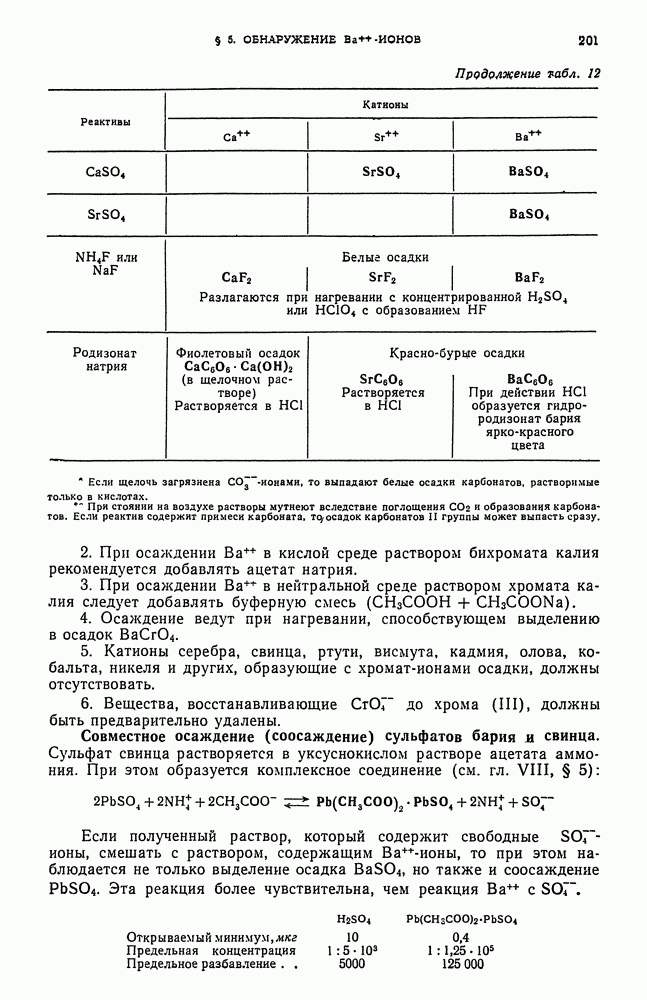
- § 5. Обнаружение Ba-ионов
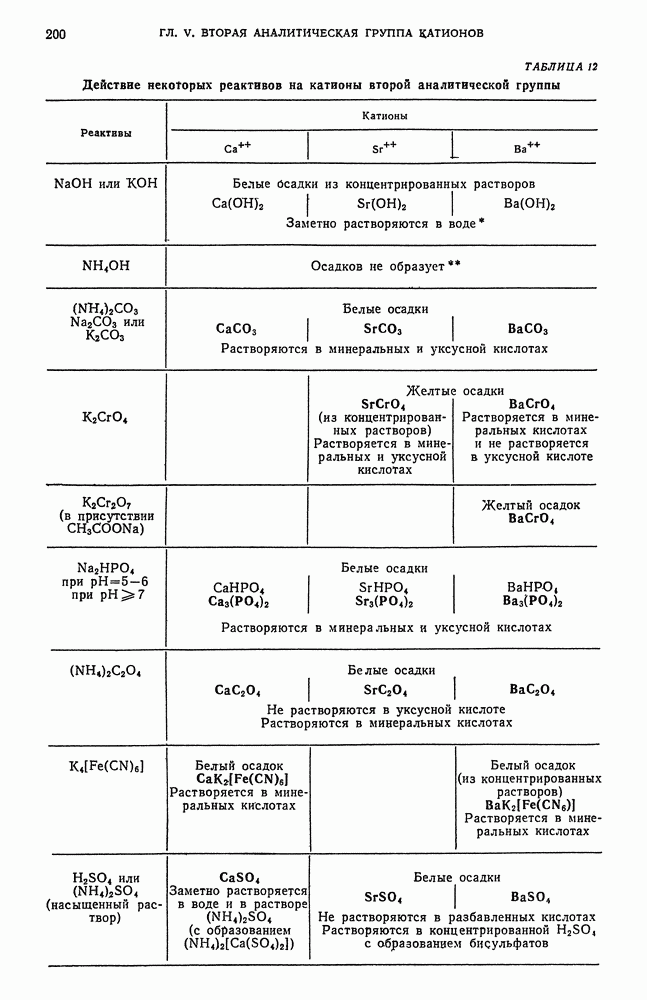
- § 6. Обзор действия реактивов на катионы второй аналитической группы
- § 7. Основы теории осаждения катионов второй аналитической группы групповым реактивом—карбонатом аммония
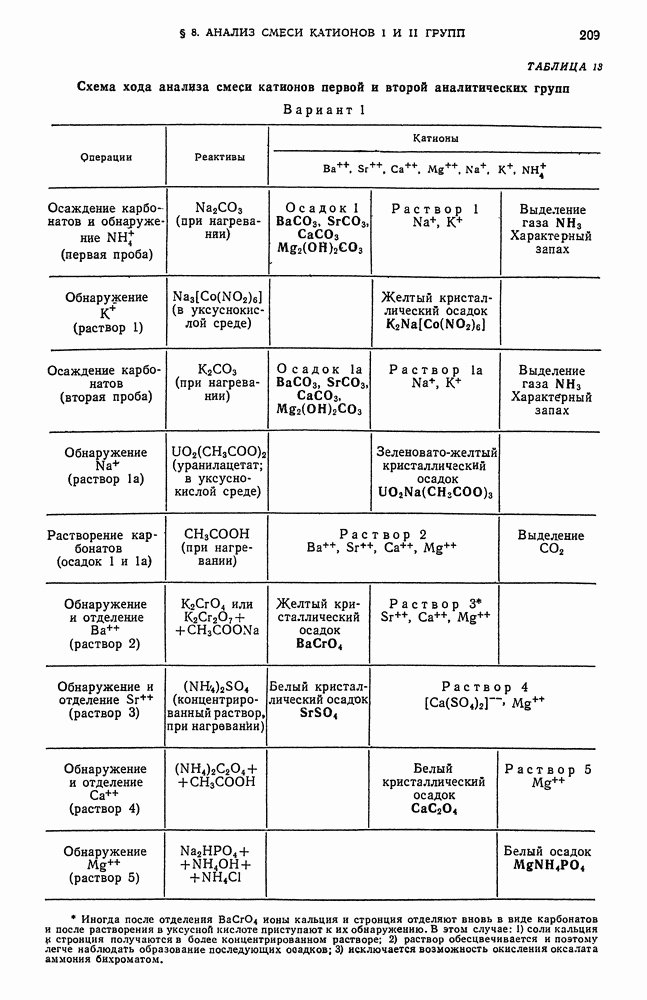
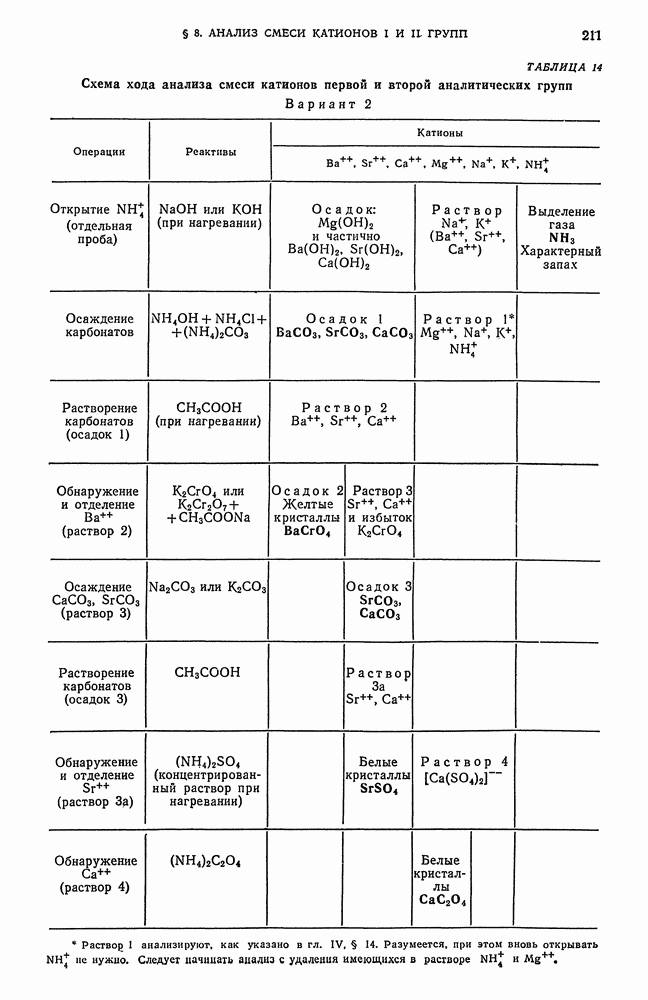
- § 8. Систематический ход анализа смеси катионов первой и второй аналитических групп
- § 9. Систематический ход анализа смеси катионов первой и второй аналитических групп в присутствии ионов
- § 10. Теоретические основы перевода сульфатов катионов второй аналитической группы в карбонаты
- ГЛАВА VI. ТРЕТЬЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика третьей аналитической группы катионов
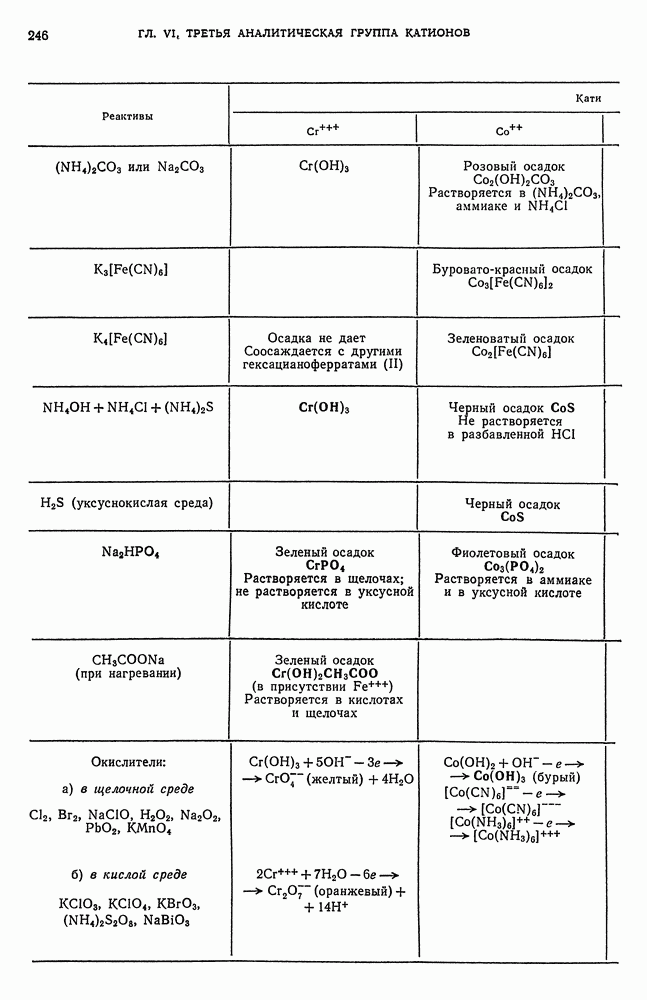
- § 2. Общие реакции катионов третьей аналитической группы
- § 3. Обнаружение Be-ионов
- § 4. Обнаружение Al-ионов
- § 5. Обнаружение ионов титана (IV)
- § 6. Обнаружение Cr-ионов
- § 7. Обнаружение Mn-ионов
- § 8. Обнаружение Fe-ионов
- § 9. Обнаружение Fe-ионов
- § 10. Обнаружение Co-ионов
- § 13. Обнаружение ионов циркония (IV)
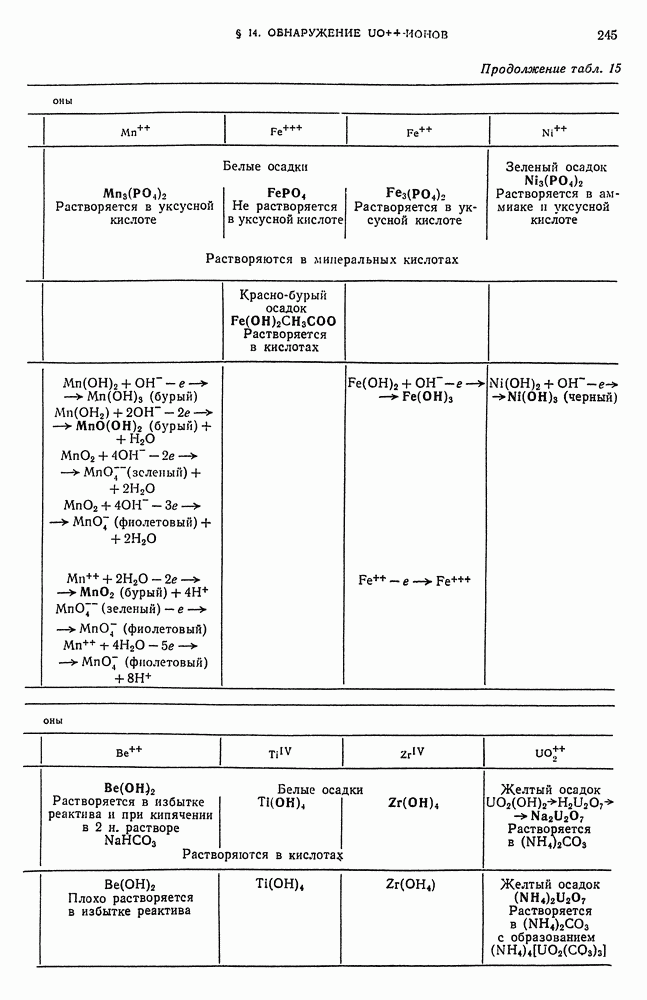
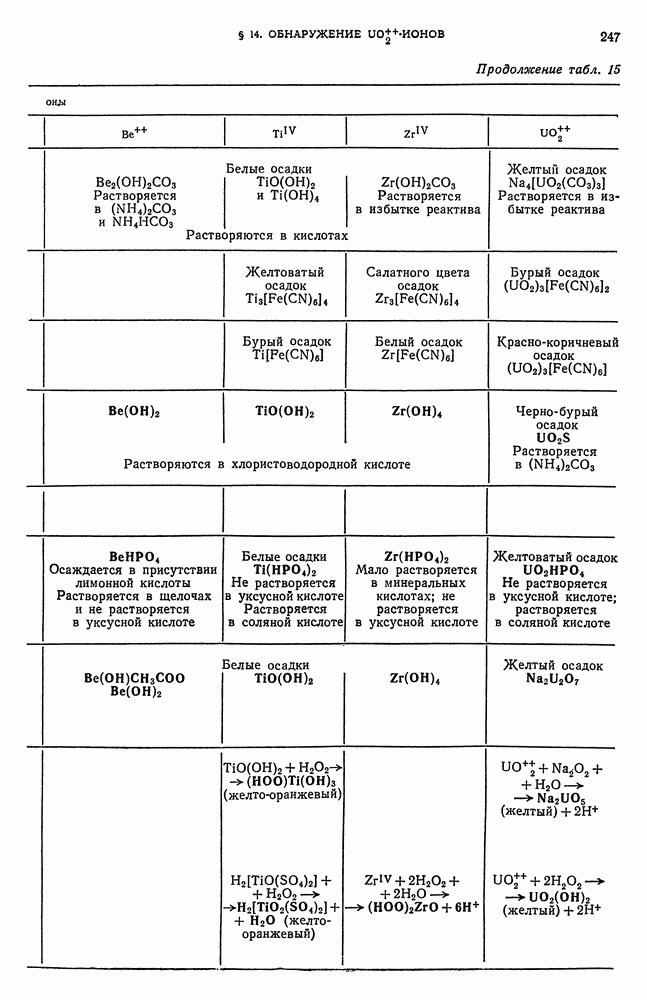
- § 14. Обнаружение UO-ионов
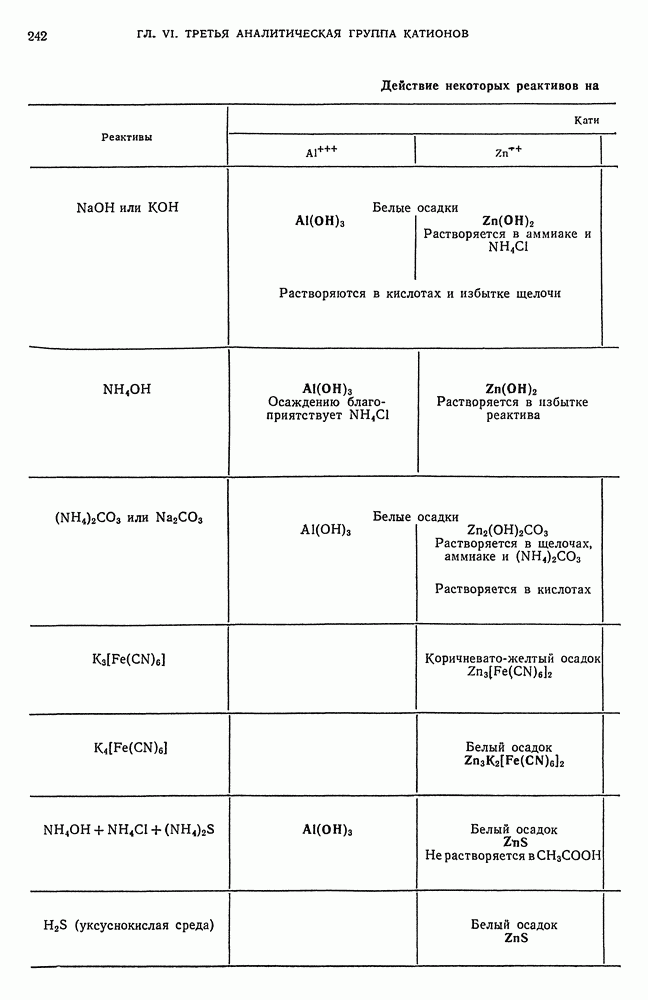
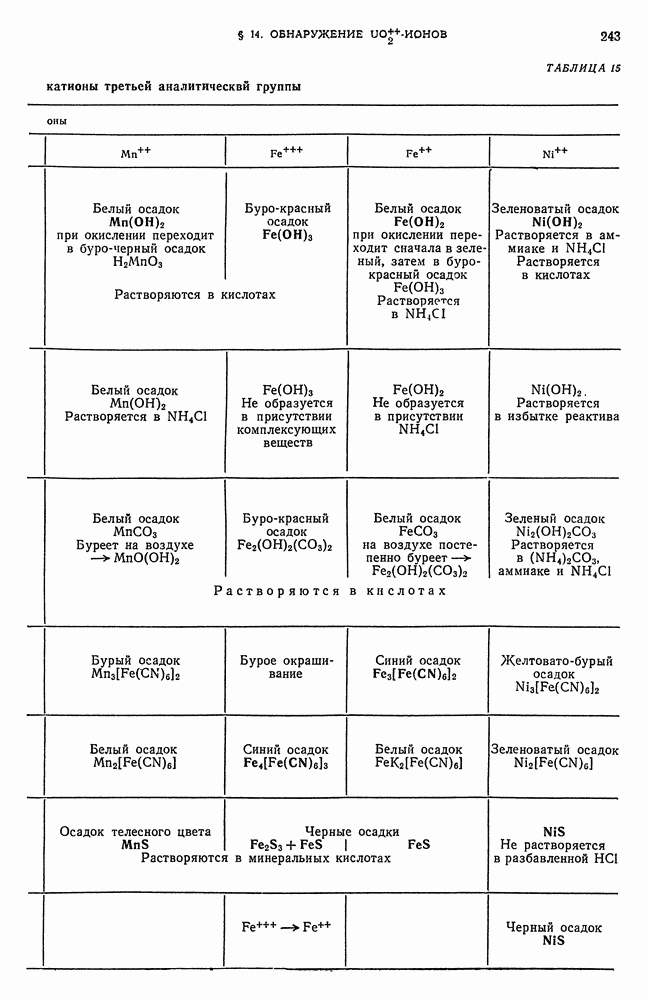
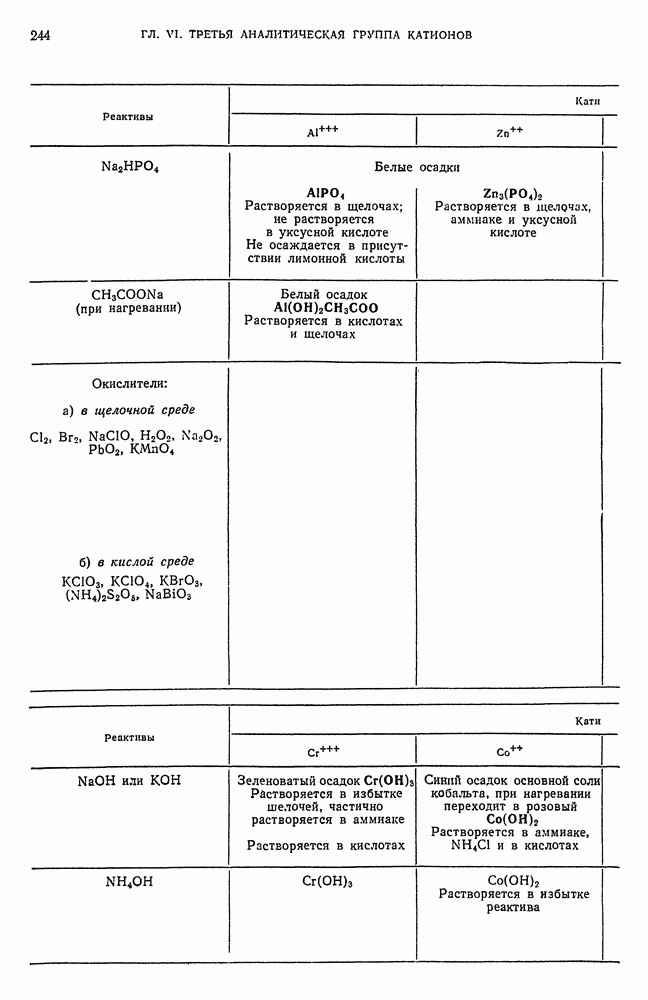
- § 15. Обзор действия реактивов на катионы третьей аналитической группы
- § 16. Использование коллоидных систем в химическом анализе
- § 17. Основы теории осаждения катионов третьей аналитической группы групповым реактивом — сульфидом аммония
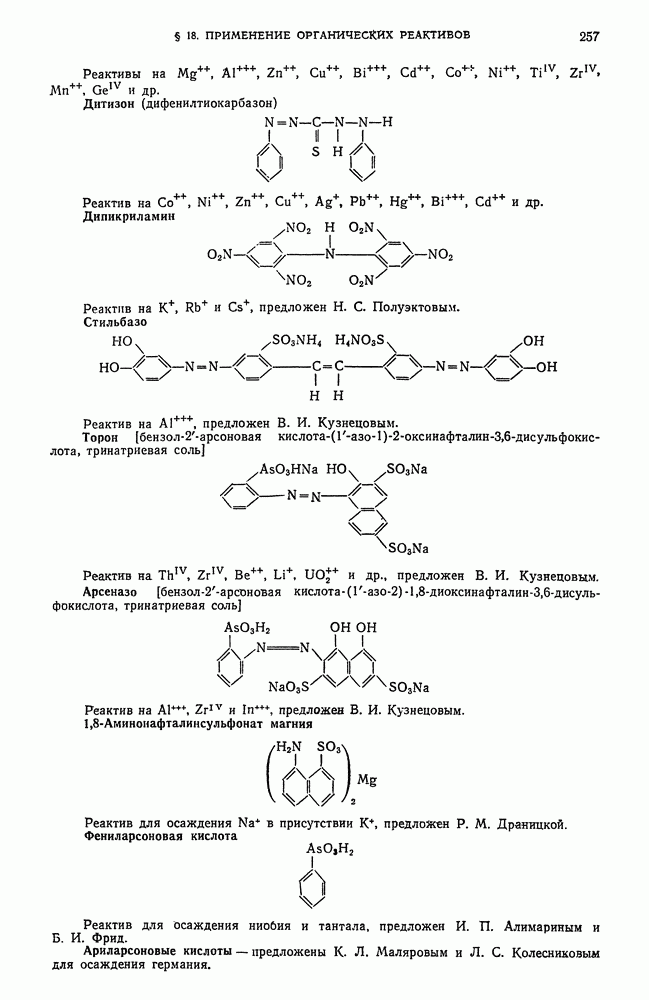
- § 18. Теоретические основы применения органических реактивов в качественном анализе неорганических веществ
- § 19. Методы разделения некоторых катионов третьей аналитической группы
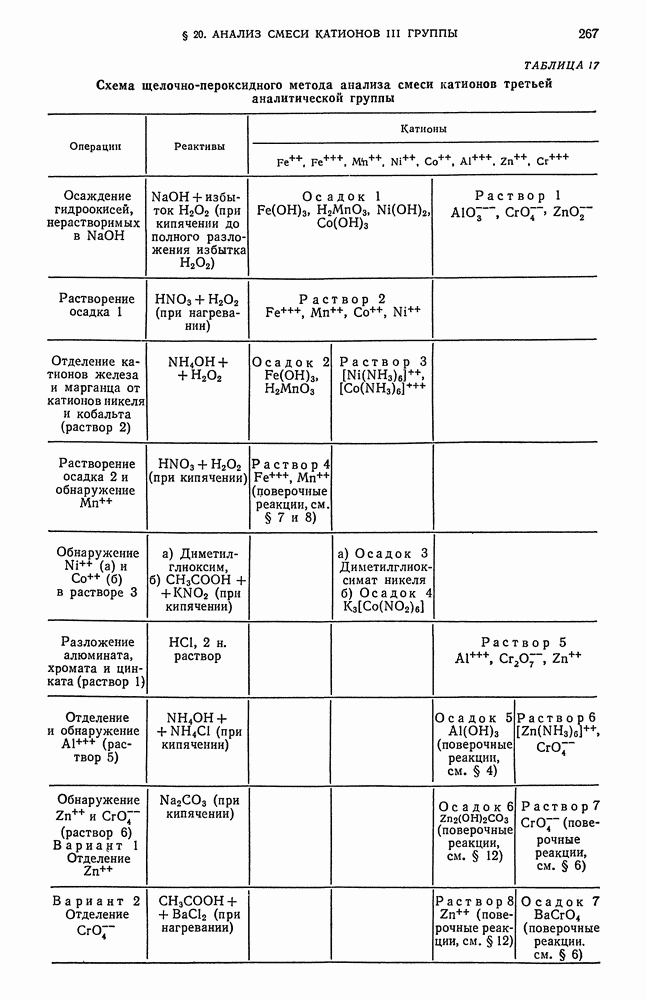
- § 20. Систематический ход анализа смеси катионов третьей аналитической группы
- § 21. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп
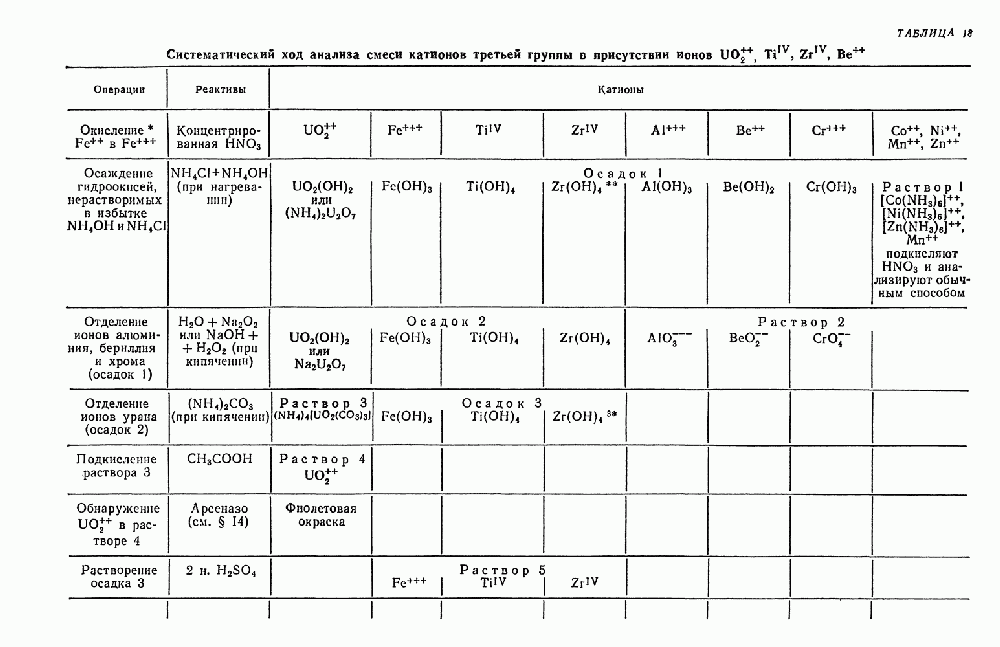
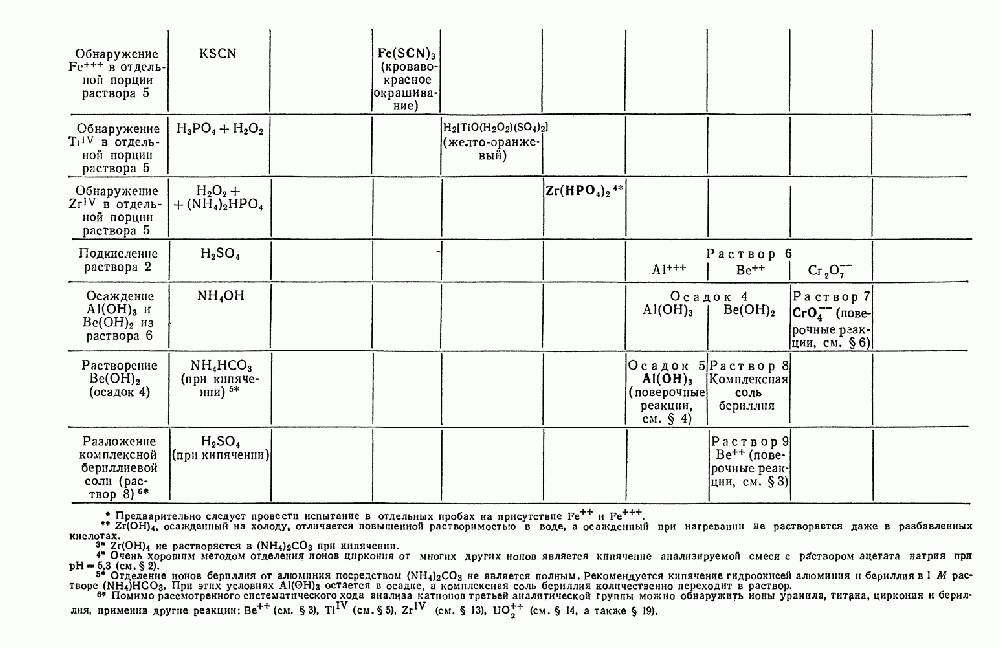
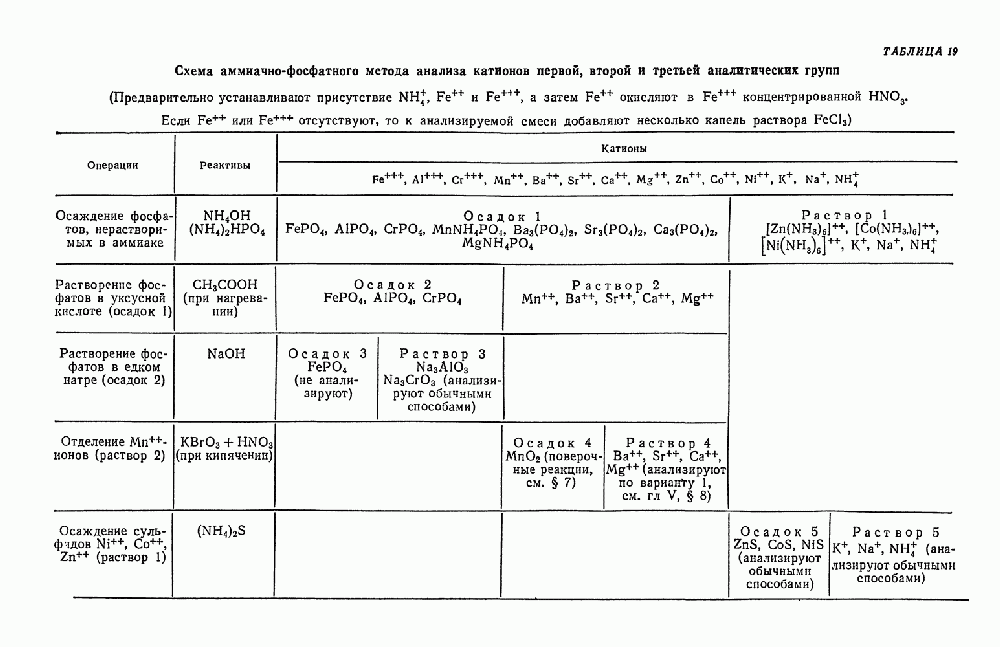
- § 22. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп в присутствии PO-ионов
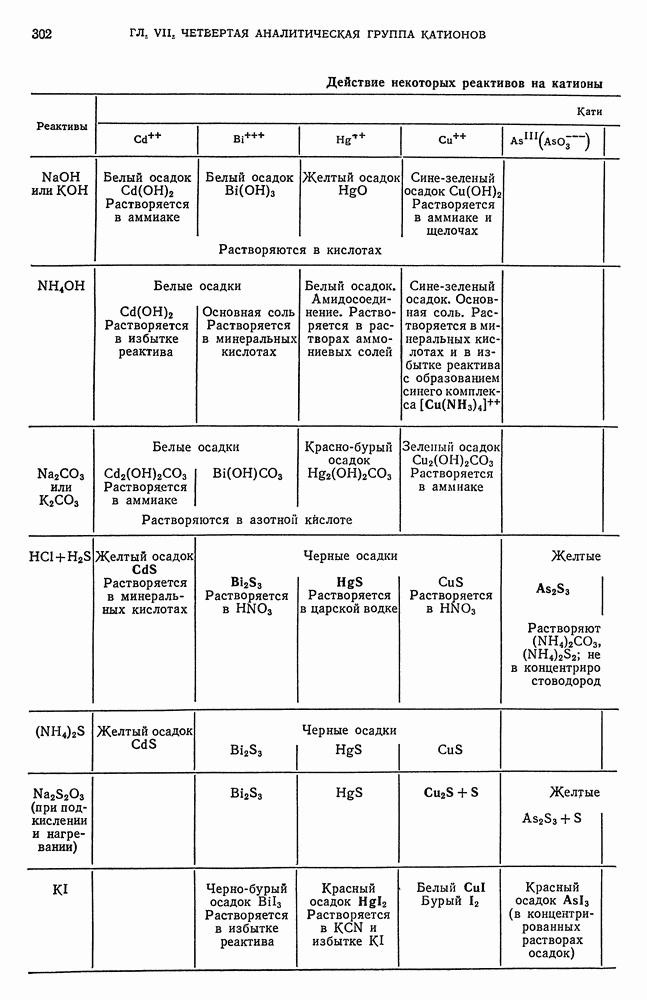
- ГЛАВА VII. ЧЕТВЕРТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика четвертой аналитической группы катионов
- § 2. Общие реакции катионов четвертой аналитической группы
- РЕАКЦИИ КАТИОНОВ ПЕРВОЙ ПОДГРУППЫ (ПОДГРУППЫ МЕДИ)
- § 3. Обнаружение Hg-ионов
- § 4. Обнаружение Cu-ионов
- § 5. Обнаружение Cd-ионов
- § 6. Обнаружение Bi-ионов
- РЕАКЦИИ КАТИОНОВ ВТОРОЙ ПОДГРУППЫ (ПОДГРУППЫ МЫШЬЯКА)
- § 7. Обнаружение ионов мышьяка (III)
- § 8. Обнаружение ионов мышьяка (V)
- § 9. Общие реакции обнаружения
- § 10. Обнаружение ионов сурьмы (III)
- § 11. Обнаружение ионов сурьмы (V)
- § 12. Общие реакции обнаружения Sb
- § 13. Обнаружение ионов олова (II)
- § 14. Обнаружение ионов олова (IV)
- § 15. Общие реакции обнаружения ионов олова (II) и олова (IV)
- § 16. Отделение ионов олова от других ирнов четвертой аналитической группы
- § 17. Обнаружение ионов германия (IV)
- § 18. Отделение ионов германия от других ионов четвертой аналитической группы
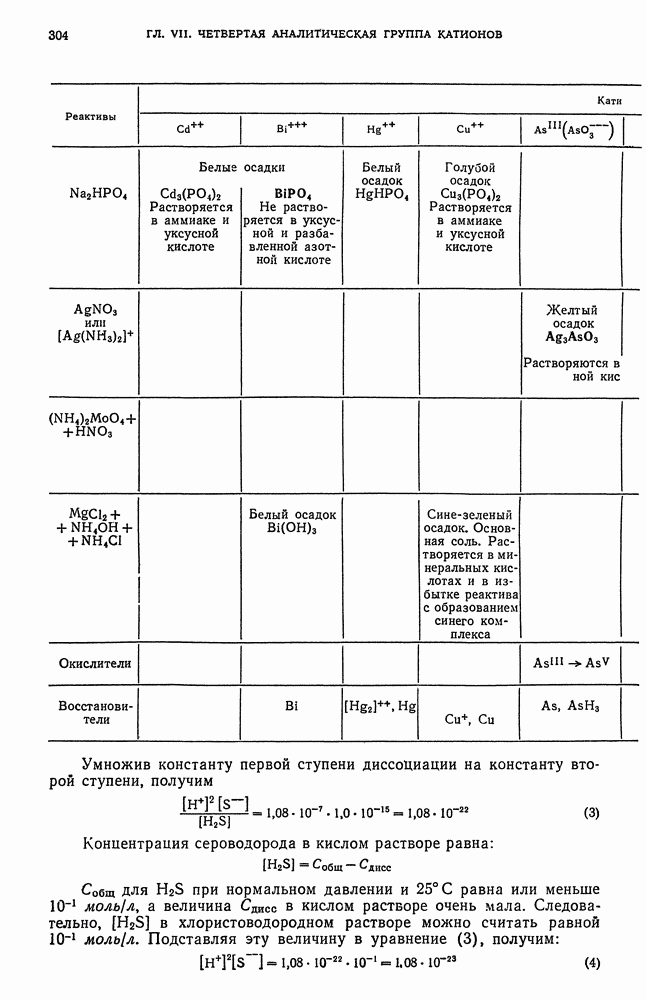
- § 19. Обзор действия реактивов на катионы четвертой аналитической группы
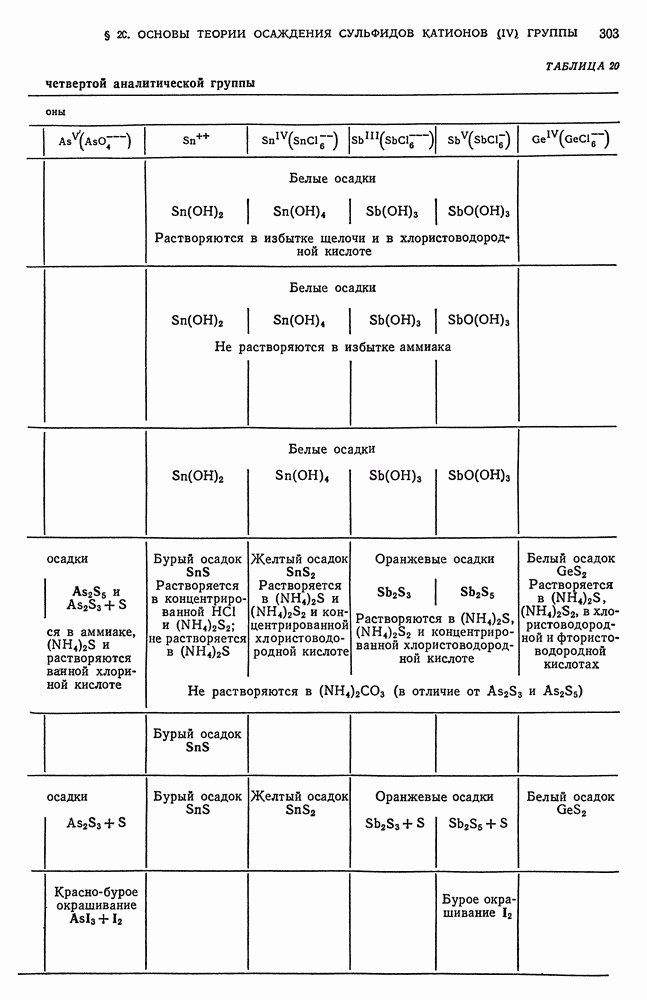
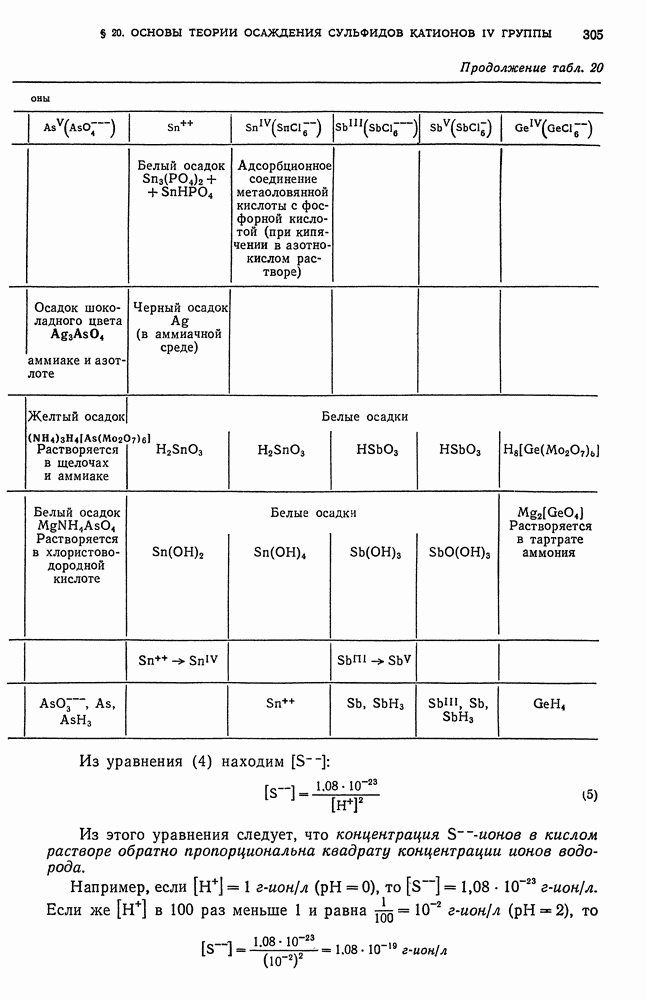
- § 20. Основы теории осаждения сульфидов катионов четвертой аналитической группы групповым реактивом — сероводородом
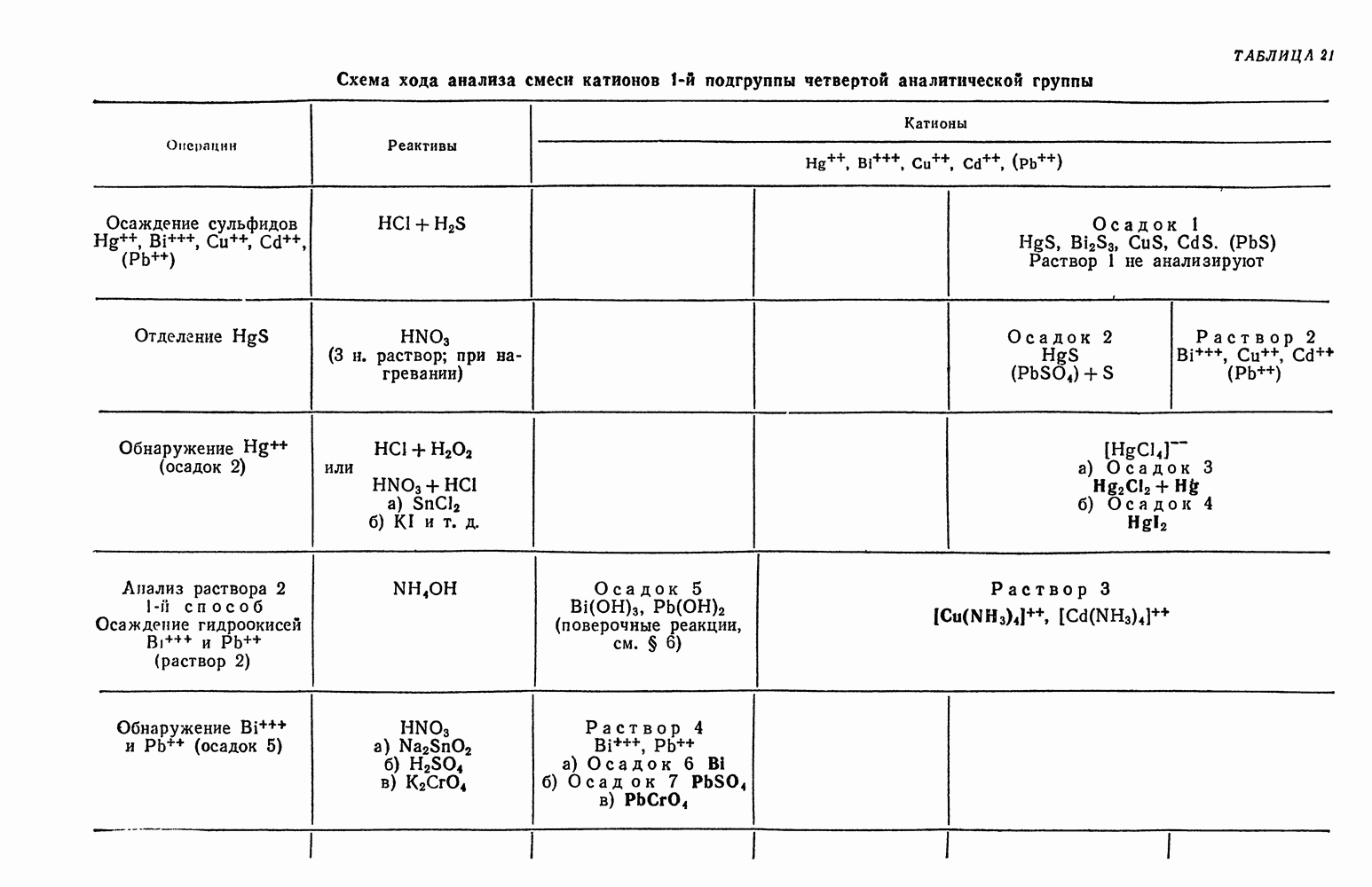
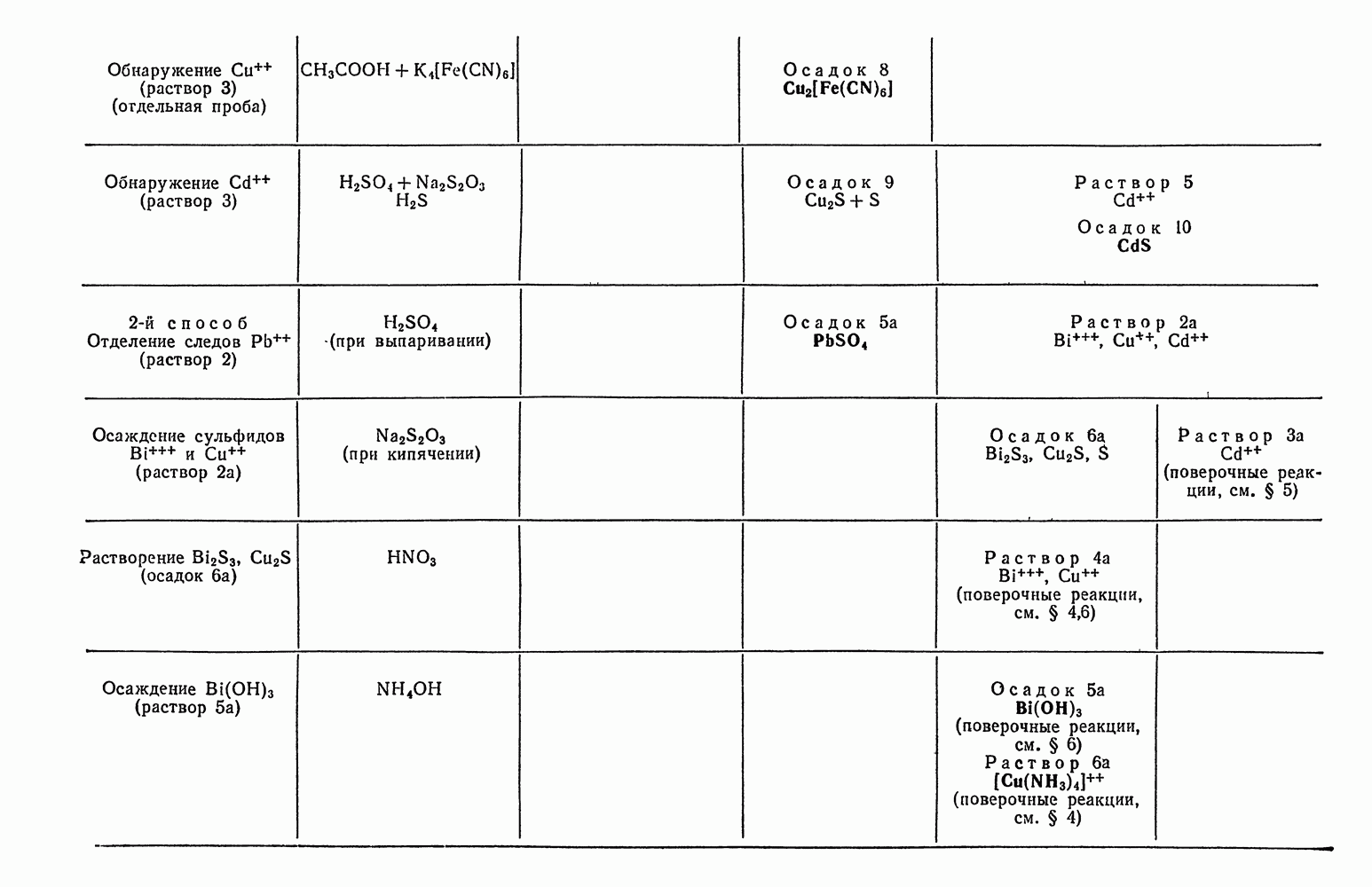
- § 21. Систематический ход анализа смеси катионов четвертой аналитической группы
- ГЛАВА VIII. ПЯТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ (ГРУППА СЕРЕБРА)
- § 1. Характеристика пятой аналитической группы катионов
- § 2. Общие реакции катионов пятой аналитической группы
- § 3. Обнаружение Ag-ионов
- § 4. Обнаружение [Hg]-ионов
- § 5. Обнаружение Pb-ионов
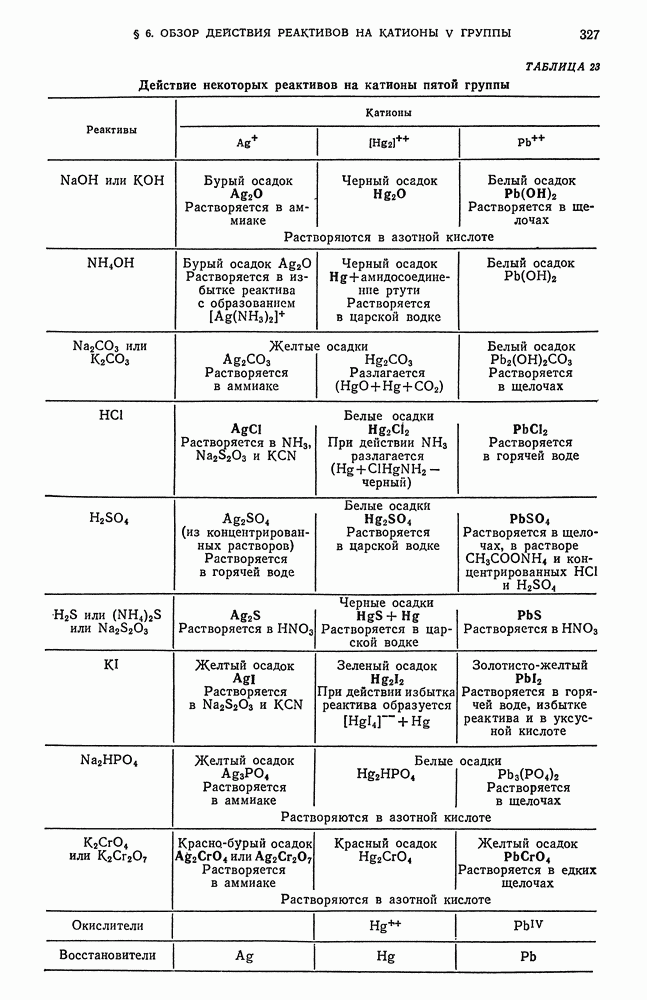
- § 6. Обзор действия реактивов на катионы пятой аналитической группы
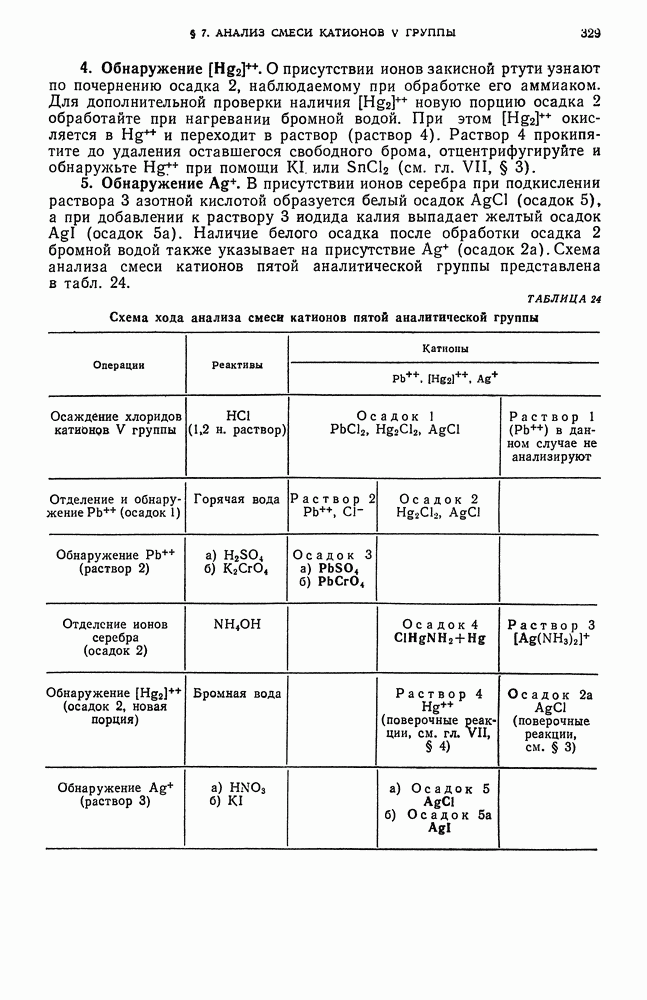
- § 7. Систематический ход анализа смеси катионов пятой аналитической группы
- ГЛАВА IX. АНАЛИЗ СМЕСИ ИОНОВ ВСЕХ ПЯТИ АНАЛИТИЧЕСКИХ ГРУПП
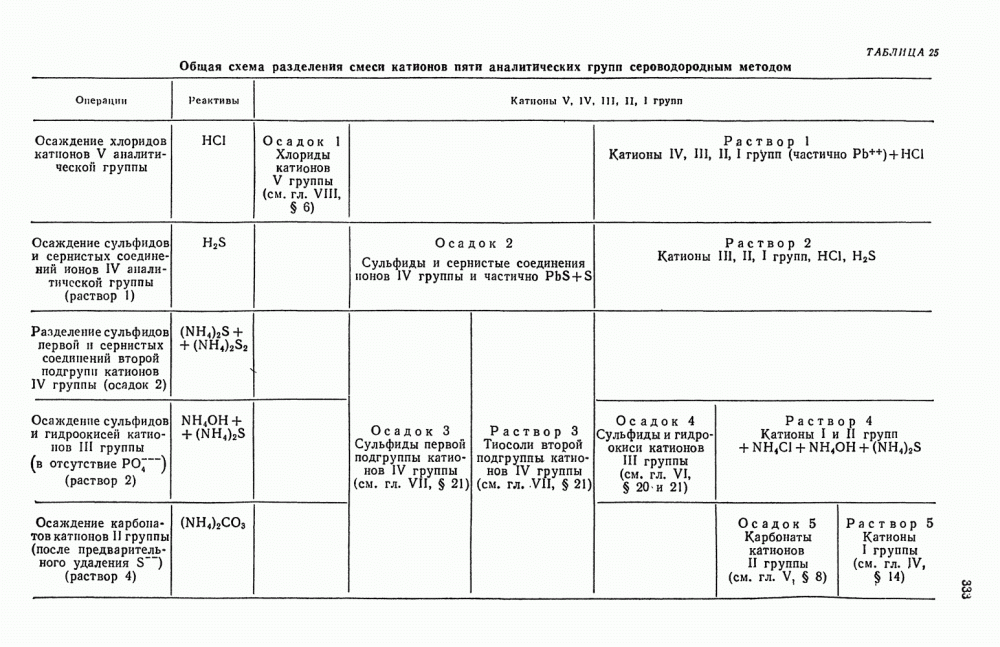
- § 1. Сероводородный метод анализа
- § 2. Недостатки сероводородного метода анализа
- § 3. Ошибки, возникающие при анализе смеси ионов пяти аналитических групп
- § 4. Бессероводородные методы анализа
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ АНИОНОВ И АНАЛИЗ СМЕСЕЙ АНИОНОВ
- § 1. Аналитическая классификация анионов
- § 2. Групповые реактивы на анионы
- § 3. Классификация методов анализа анионов
- ГЛАВА XI. ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика первой группы анионов
- § 2. Реакции анионов первой группы
- § 3. Обнаружение CI-ионов
- § 4. Обнаружение Br-ионов
- § 5. Обнаружение I-ионов
- § 6. Обнаружение CN-ионов
- § 7. Обнаружение SCN-ионов
- § 8. Обнаружение [Fe(CN)]-ионов
- § 9. Обнаружение Fe(CN)-ионов
- § 10. Обнаружение NO-ионов
- § 11. Обнаружение NO2-ионов
- § 12. Обнаружение S-ионов
- § 13. Обнаружение CH3COOO-ионов
- § 14. Обнаружение BrO3-ионов
- § 15. Обнаружение ClO3-ионов
- § 16. Обнаружение ClO4-ионов
- § 17. Обзор действия реактивов на анионы первой группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 18. Анализ смеси Cl, Br и I-ионов
- § 19. Анализ смеси Cl, Br, I и SCN-ионов
- § 20. Анализ смеси Cl, ClO3 и ClO4-ионов
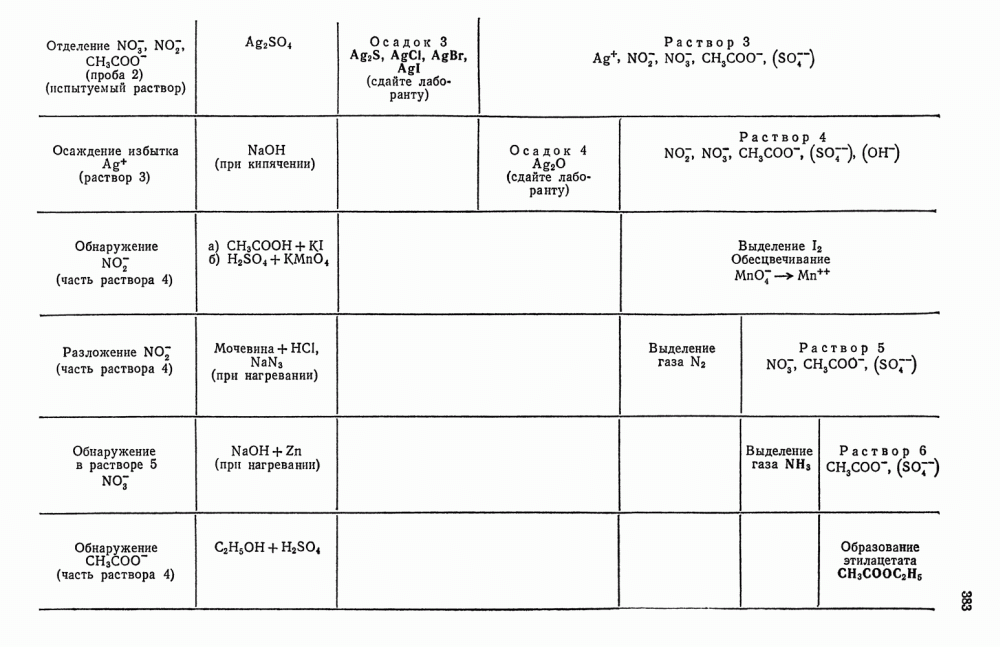
- § 21. Анализ смеси NO2 и NO3-ионов
- § 22. Анализ смеси анионов первой группы
- ГЛАВА XII. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика второй группы анионов
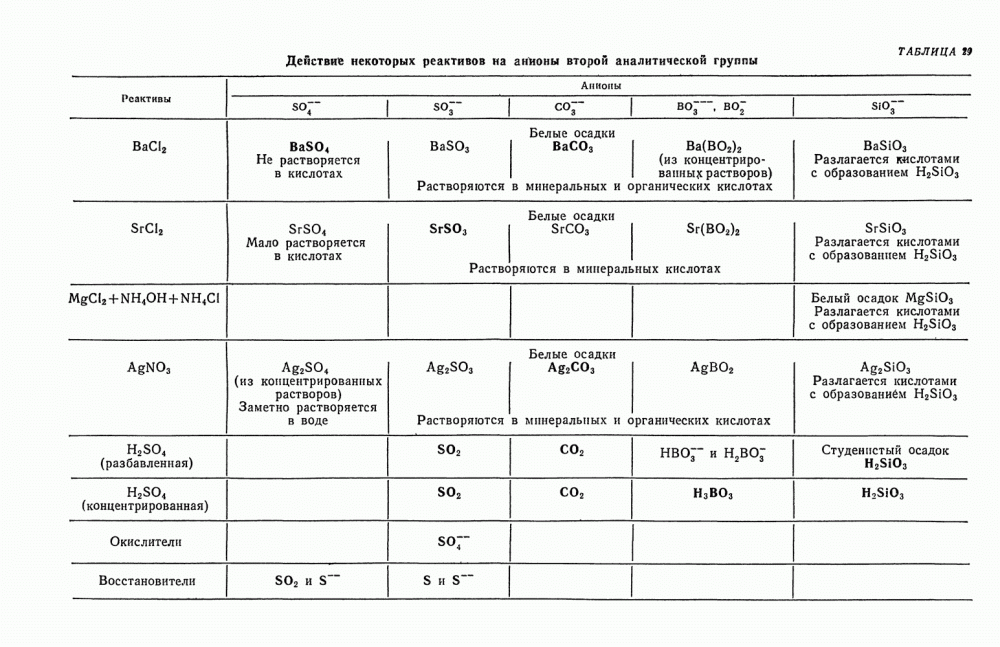
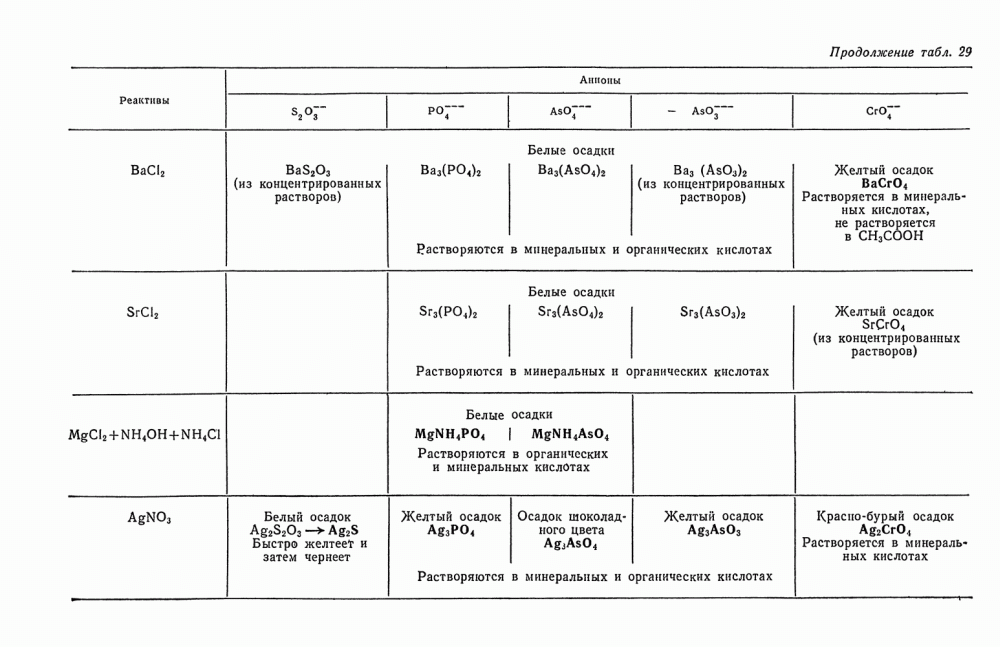
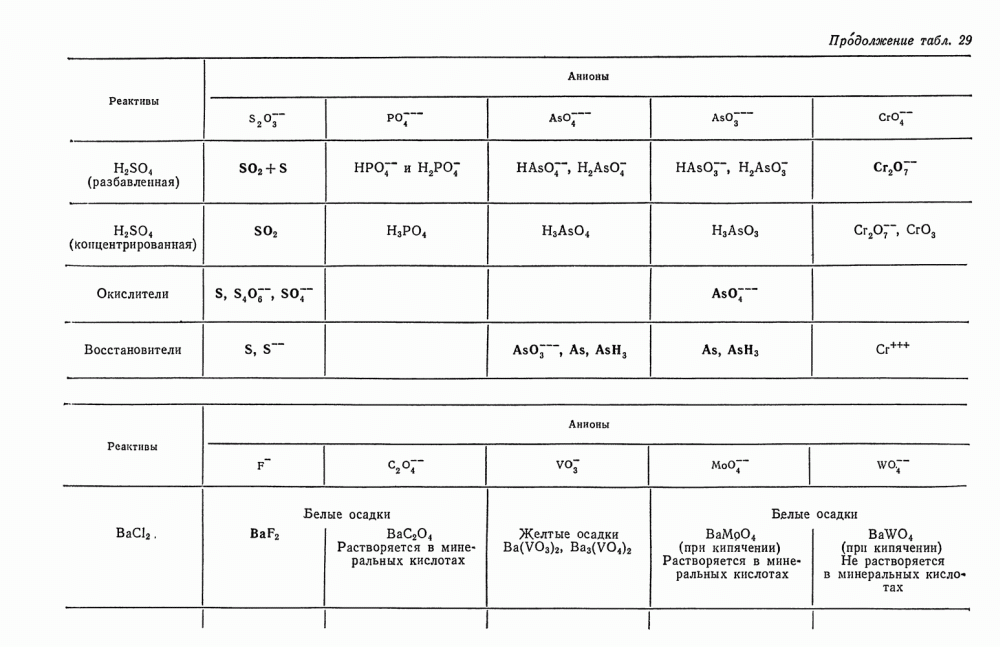
- § 2. Общие реакции анионов второй группы
- § 3. Обнаружение SO3-ионов
- § 4. Обнаружение S2O3-ионов
- § 5. Обнаружение S2O3 в присутствии SO3-ионов
- § 6. Обнаружение SO4-ионов
- § 7. Обнаружение CO3-ионов
- § 8. Обнаружение CO3-ионов в присутствии SO3 и S2O3-ионов
- § 9. Обнаружение PO4-ионов
- § 10. Обнаружение CrO4-ионов
- § 11. Обнаружение AsO3-ионов
- § 12. Обнаружение AsO4-ионов
- § 13. Обнаружение BO2 и BO3-ионов
- § 14. Обнаружение SiO3-ионов
- § 15. Обнаружение F-ионов
- § 16. Обнаружение C2O4-ионов
- § 17. Обнаружение VO3-ионов
- § 18. Обнаружение MoO4-ионов
- § 19. Обнаружение WO4-ионов
- § 20. Обзор действия реактивов на анионы второй группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 21. Анализ смеси ионов
- § 22. Анализ смеси SO3, SO4, S2O3 и CO3-ионов
- § 23. Анализ смеси VO2, MoO4 и WO4-ионов
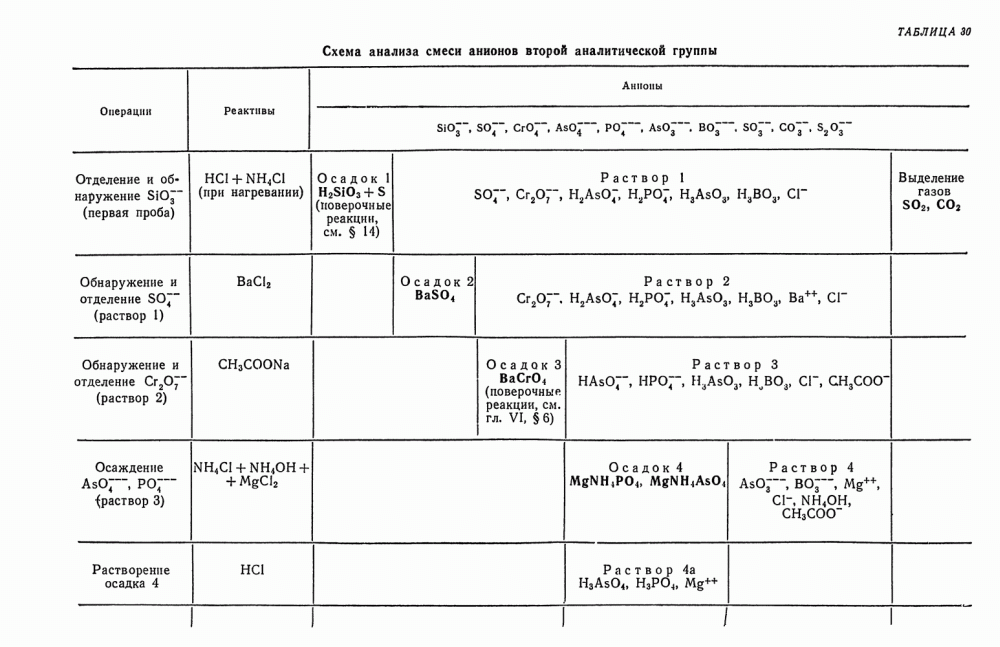
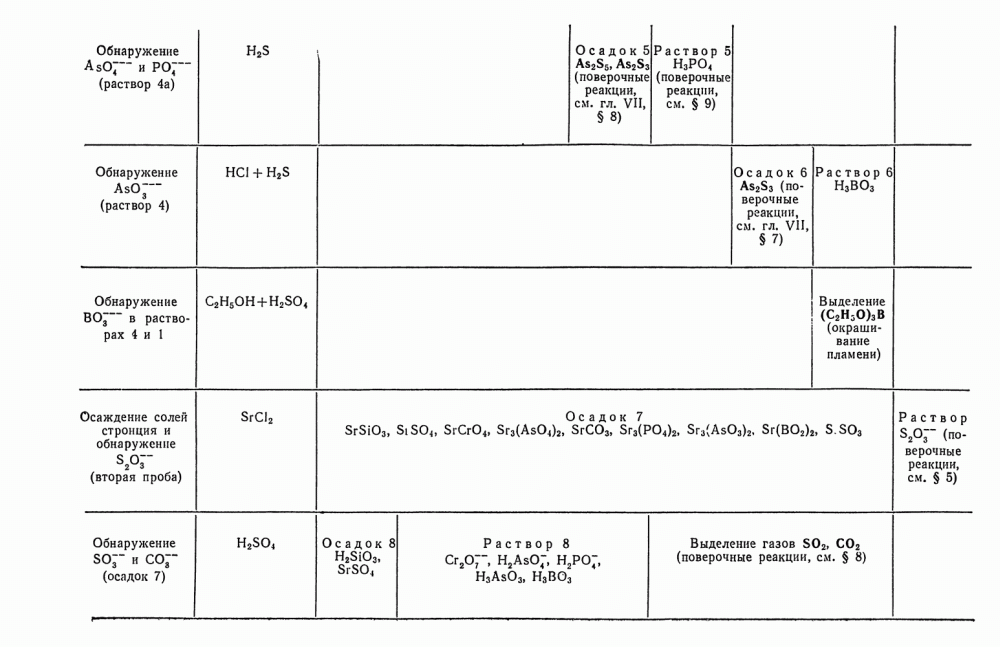
- § 24. Анализ смеси анионов второй группы
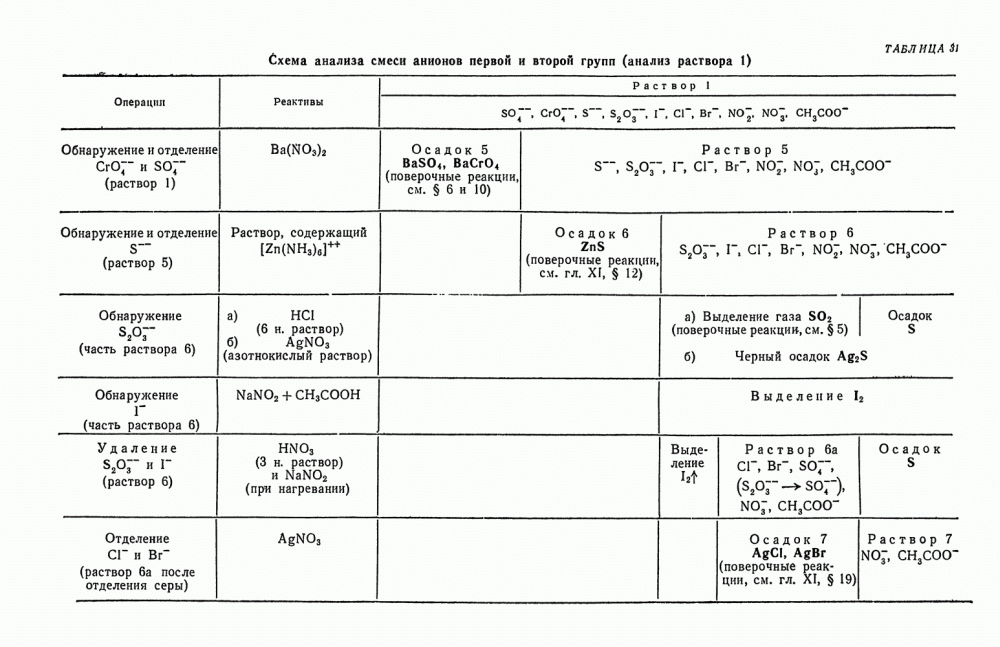
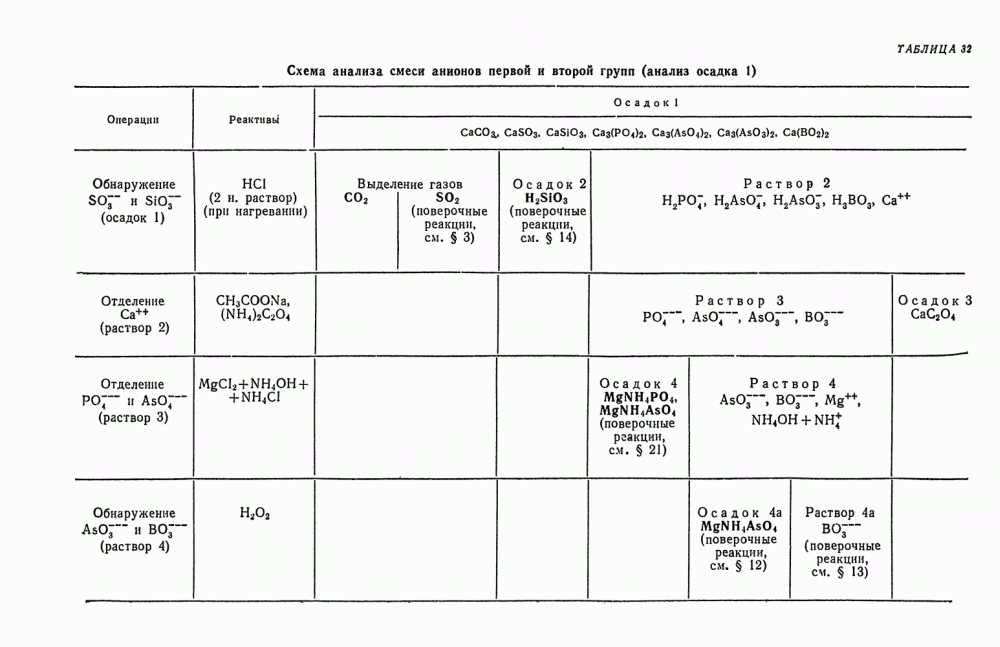
- § 25. Анализ смеси анионов первой и второй групп
- ГЛАВА XIII. ОБНАРУЖЕНИЕ СВОБОДНЫХ МЕТАЛЛОВ И НЕМЕТАЛЛОВ, ИДЕНТИФИЦИРОВАНИЕ СОЛЕЙ И ДРУГИХ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И АНАЛИЗ ИХ СМЕСЕЙ
- § 1. Подготовка вещества к анализу
- § 2. Предварительные испытания
- § 3. Растворение анализируемого вещества в воде, кислотах и щелочах
- § 4. Переведение в растворимое состояние веществ, нерастворимых в воде, кислотах и щелочах
- § 5. Анализ неизвестного вещества
- § 6. Обнаружение свободных элементов
- § 7. Идентифицирование солей и других индивидуальных соединений
- § 8. Обнаружение микропримесей
- § 9. Анализ сплавов
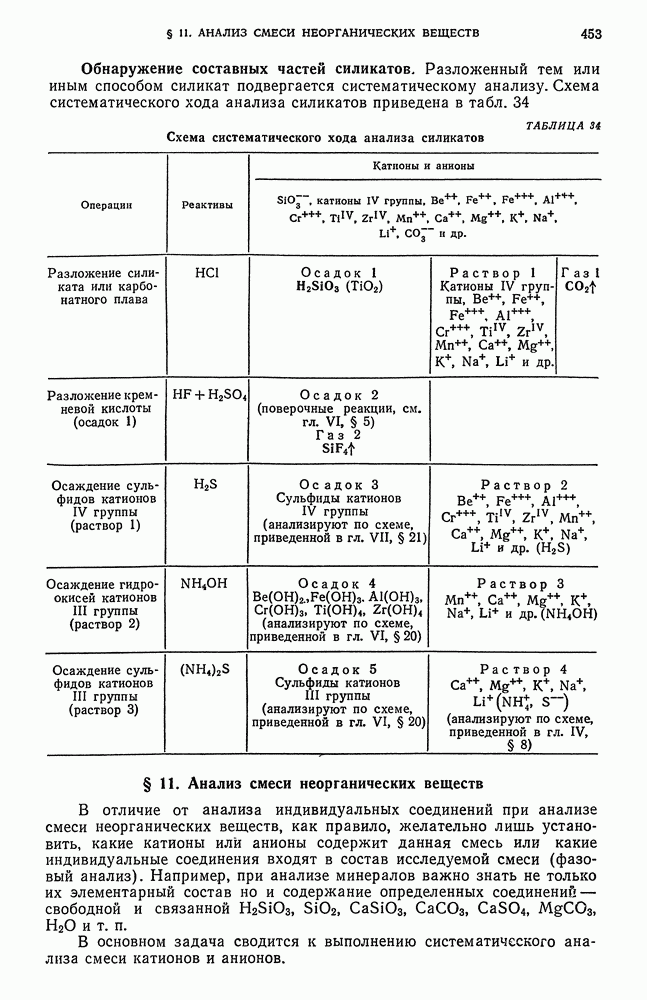
- § 10. Анализ силикатов и алюмосиликатов
- § 11. Анализ смеси неорганических веществ
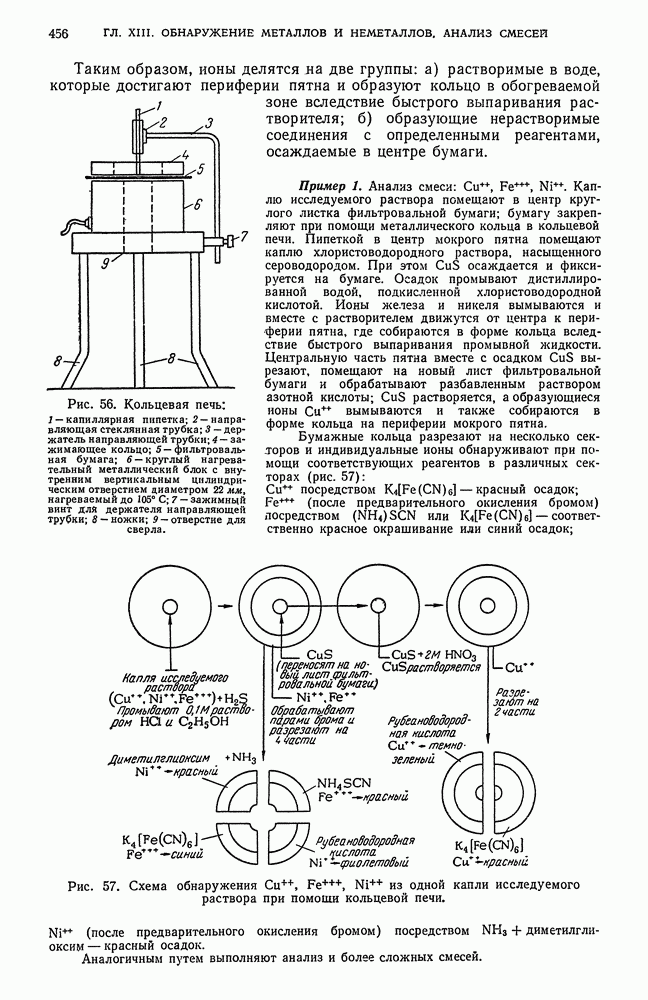
- § 12. Экспрессный метод анализа смесей катионов и анионов
- § 13. Идентифицирование нерастворимых веществ
- ЛИТЕРАТУРА