| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 3. Обнаружение CI-ионов
Свойства хлоридов. Соли хлористоводородной кислоты (хлориды), образованные катионами сильных оснований, в водных растворах имеют нейтральную реакцию; соли слабых оснований — кислую.
Хлориды тяжелых металлов при гидролизе образуют осадки гидроокисей, оксихлоридов и хлорокисей. Для подавления гидролиза к растворам указанных солей приливают хлористоводородную кислоту.
Анион хлористоводородной кислоты бесцветен. Окрашенные соли образуются только с окрашенными катионами. Некоторые хлориды образуют окрашенные в различные цвета гидраты, например:  — сине-фиолетовый,
— сине-фиолетовый,  — розово-фиолетовый,
— розово-фиолетовый,  — розовый и др.
— розовый и др.
При полном гидролизе хлоридов таких элементов, как  , Р (например,
, Р (например,  , которые в отличие от солей называют хлорангидридами), образуются две кислоты: галогеноводородная и кислородсодержащая:
, которые в отличие от солей называют хлорангидридами), образуются две кислоты: галогеноводородная и кислородсодержащая:

Хлориды высоковалентных элементов, обладающих свойствами окислителей, неустойчивы. Они разлагаются с выделением свободного хлора, например:

Нагревание способствует такому разложению.
Хлориды благородных металлов разлагаются при прокаливании с образованием металла и свободного хлора:

Хлористоводородная кислота и ее соли в кислой среде являются восстановителями и способны окисляться сильными окислителями с выделением элементарного хлора:

Хлориды способны связывать некоторые ионы в комплексы, например:

Этим объясняется растворимость некоторых обычно нерастворимых в воде и азотной кислоте хлоридов в избытке осаждающего их реактива (соляной кислоты или хлоридов) и в царской водке.
Большинство хлоридов растворимо в воде. Малорастворимыми являются хлориды серебра, закисной ртути, свинца и меди (I).
Реакция окисления хлористоводородной кислоты и хлоридов до элементарного хлора. Поместите в пробирку 5 капель раствора, содержащего  , добавьте 5 капель концентрированного раствора
, добавьте 5 капель концентрированного раствора  капель концентрированной
капель концентрированной  и нагрейте (под
и нагрейте (под  ). При этом наблюдается частичное или полное обесцвечивание раствора
). При этом наблюдается частичное или полное обесцвечивание раствора  и выделение газообразного хлора, который обнаруживают с помощью иодокрахмальной бумаги (синее окрашивание), анилина (красно-фиолетовое окрашивание), смеси фенола с анилином (синее окрашивание), смеси флюоресцеина с
и выделение газообразного хлора, который обнаруживают с помощью иодокрахмальной бумаги (синее окрашивание), анилина (красно-фиолетовое окрашивание), смеси фенола с анилином (синее окрашивание), смеси флюоресцеина с  (розовое окрашивание) и т. д. Хлор обладает характерным запахом.
(розовое окрашивание) и т. д. Хлор обладает характерным запахом.
Реакция протекает согласно уравнению:

Для обнаружения выделяющегося  поднесите к отверстию пробирки влажную иодокрахмальную бумагу. В присутствии хлора появляется синее окрашивание вследствие выделения элементарного иода:
поднесите к отверстию пробирки влажную иодокрахмальную бумагу. В присутствии хлора появляется синее окрашивание вследствие выделения элементарного иода:

Окисляющее действие на  оказывают манганиты, манганаты, перманганаты, двуокиси марганца и свинца, хромовый ангидрид, хлорноватистая, хлорноватая, азотная кислоты и т. п.
оказывают манганиты, манганаты, перманганаты, двуокиси марганца и свинца, хромовый ангидрид, хлорноватистая, хлорноватая, азотная кислоты и т. п.
Условия проведения реакций. 1. Все реакции окисления  протекают в сильнокислой среде. Если окисляется сама хлористоводородная кислота, то берут ее избыток. Если окислению подвергаются хлориды, то для подкисления раствора можно использовать серную кислоту. В нейтральной среде окисление хлоридов не происходит; в щелочной среде свободный хлор не
протекают в сильнокислой среде. Если окисляется сама хлористоводородная кислота, то берут ее избыток. Если окислению подвергаются хлориды, то для подкисления раствора можно использовать серную кислоту. В нейтральной среде окисление хлоридов не происходит; в щелочной среде свободный хлор не  , так как при
, так как при  он легко вступает в реакцию диспропорционирования с образованием смеси хлоридов и гипохлоритов:
он легко вступает в реакцию диспропорционирования с образованием смеси хлоридов и гипохлоритов:

2. В качестве окислителя удобно пользоваться перманганатом калия, который обесцвечивается в присутствии  , вследствие чего реакция становится более наглядной.
, вследствие чего реакция становится более наглядной.
3. Нагревание способствует реакции окисления — восстановления.
4. В концентрированных растворах окисление — восстановление протекает энергичней.
5. Сильные восстановители, легче окисляющиеся, чем  , препятствуют окислению хлоридов.
, препятствуют окислению хлоридов.
6. Реакцию следует проводить под тягой, так как хлор является отравляющим веществом.
Реакция с бихроматом калия. Поместите в пробирку, предварительно растерев в фарфоровой ступке,  твердого
твердого  и равное количество
и равное количество  . Прибавьте не более 5—10 капель концентрированной
. Прибавьте не более 5—10 капель концентрированной  и осторожно нагрейте.
и осторожно нагрейте.
В присутствии хлоридов образуется летучее соединение хрома — хлористый хромил  :
:

Для улавливания выделяющихся красно-бурых паров хлористого хромила в реакционную пробирку опустите стеклянную палочку с шариком, смоченным раствором едкого натра. Стеклянную палочку в пробирке нужно держать высоко над жидкостью, а не опускать ее в раствор.
Выделяющиеся пары хлористого хромила поглощаются раствором едкого натра. После окончания реакции выньте палочку из пробирки, поместите ее в чистую пробирку и ополосните дистиллированной водой, полученный раствор подкислите серной или уксусной кислотой и откройте в нем  (см. гл. VI, § 6). Обнаружение
(см. гл. VI, § 6). Обнаружение  является косвенным доказательством наличия
является косвенным доказательством наличия  .
.
Хлористый хромил легко подвергается гидролизу. При поглощении его раствором щелочи гидролиз хлористого хромила протекает согласно уравнению:

Условия проведения реакции. 1. Разбавленные растворы анализируемого вещества следует предварительно сконцентрировать осторожным выпариванием на водяной бане. При сильном нагревании легко возгоняющиеся хлориды могут улетучиться.
2. Кислые растворы предварительно нейтрализуют, чтобы избежать потерь  при выпаривании. Сама хлористоводородная: кислота при нагревании с
при выпаривании. Сама хлористоводородная: кислота при нагревании с  окисляется до
окисляется до  .
.
3. При увеличении соотношения бихромата по сравнению с хлоридом наступает реакция образования свободного хлора:

Выделение хлора приводит к уменьшению чувствительности реакции.
4. Бромиды и иодиды не мешают проведению реакции, выделяя при аналогичных условиях свободный бром и иод, которые улетучиваются вместе с  , но тотчас обесцвечиваются в щелочном растворе.
, но тотчас обесцвечиваются в щелочном растворе.
5. Малорастворимые хлориды серебра, ртути и свинца, а также хлориды олова и сурьмы не дают отчетливую реакцию образования хлористого хромила при взаимодействии с  .
.
6. Проведению реакции мешают фториды, образующие  , а также большие количества восстановителей и окислителей.
, а также большие количества восстановителей и окислителей.
Реакция с нитратом серебра. К нескольким каплям испытуемого раствора добавьте по нескольку капель азотной кислоты и раствора  . Выпадает белый осадок
. Выпадает белый осадок  , который растворяется в растворах аммиака,
, который растворяется в растворах аммиака,  с образованием комплексных ионов.
с образованием комплексных ионов.
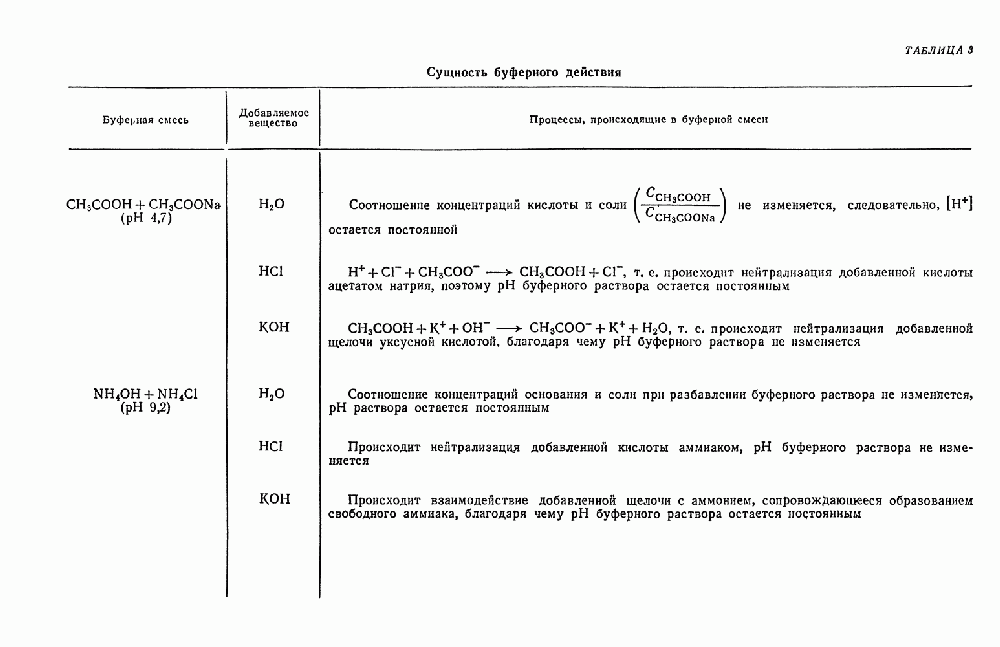
Чтобы отличить хлорид серебра от бромида серебра (частично также растворимого в растворе аммиака  ), для растворения осадка применяют различные буферные смеси, содержащие аммиак. В этих смесях
), для растворения осадка применяют различные буферные смеси, содержащие аммиак. В этих смесях  не растворяются, но растворяется
не растворяются, но растворяется  . Одной из таких смесей является раствор, содержащий 0,25 М
. Одной из таких смесей является раствор, содержащий 0,25 М  .
.
Если полученный раствор подкислить разбавленной  , то аммиачные комплексные ионы разрушаются вследствие образования более прочных
, то аммиачные комплексные ионы разрушаются вследствие образования более прочных  -ионов и вновь выпадает осадок
-ионов и вновь выпадает осадок  .
.
Хлорид серебра реатирует с гексацианоферратом (II) калия:

а) При обработке тщательно отмытого от избытка гексацианоферрата (II) калия полученного белого осадка  каплей концентрированной
каплей концентрированной  он превращается в оранжевый осадок
он превращается в оранжевый осадок  :
:

б) При обработке тщательно отмытого от избьтка гексацианоферрата (II) калия полученного белого осадка  каплей раствора
каплей раствора  образуется берлинская лазурь и осадок окрашивается в синий цвет:
образуется берлинская лазурь и осадок окрашивается в синий цвет:

Другие галогекиды серебра реагируют аналогичным образом.
Условия проведения реакции. 1. Осаждение ведут в азотнокислой среде.
2. Осадок  тщательно промывают от посторонних примесей.
тщательно промывают от посторонних примесей.
3. Буферную смесь прибавляют по каплям, не стремясь полностью растворить осадок, а добиваясь лишь получения нескольких капель раствора, достаточных для обнаружения в них  мешают этой реакции, так как образуют с
мешают этой реакции, так как образуют с  аналогичные осадки.
аналогичные осадки.
Осаждение хлорида серебра в присутствии некоторых других ионов, осаждаемых нитратом серебра. Другой реакцией, позволяющей обнаруживать  -ионы, в присутствии
-ионы, в присутствии  , также осаждаемых
, также осаждаемых  , является описываемая ниже реакция с нитратом серебра, протекающая в уксуснокислом растворе
, является описываемая ниже реакция с нитратом серебра, протекающая в уксуснокислом растворе  -оксихино-лина и перекиси водорода, к которой предварительно добавляют разбавленную уксусную кислоту (2: 1).
-оксихино-лина и перекиси водорода, к которой предварительно добавляют разбавленную уксусную кислоту (2: 1).
В отличие от бромидов и иодидов, окисляемых перекисью водорода в уксуснокислом растворе до элементарного брома и иода, хлориды не окисляются в тех же условиях. Если окисление проводить в присутствии  -оксихинолина, то бром и иод образуют с ним бром- и иодпроизводные. Поэтому
-оксихинолина, то бром и иод образуют с ним бром- и иодпроизводные. Поэтому  уже не реагируют с
уже не реагируют с  дает с
дает с  осадок
осадок  . Если при этом в растворе имеется
. Если при этом в растворе имеется  , то он окисляется при нагревании перекисью водорода и не дает осадка
, то он окисляется при нагревании перекисью водорода и не дает осадка  . Цианиды разлагаются уксусной кислотой с образованием летучей HCN, поэтому они также не мешают обнаружению
. Цианиды разлагаются уксусной кислотой с образованием летучей HCN, поэтому они также не мешают обнаружению  .
.
Реакцию проводят следующим образом. 1 каплю испытуемого раствора смешивают с 1 каплей уксуснокислого раствора  каплей уксуснокислого раствора
каплей уксуснокислого раствора  с 1 каплей
с 1 каплей  и нагревают около 4 мин. Затем добавляют к смеси
и нагревают около 4 мин. Затем добавляют к смеси  каплю раствора
каплю раствора  . В присутствии хлоридов в зависимости от их концентрации появляется либо белый осадок, либо муть (холостой опыт!).
. В присутствии хлоридов в зависимости от их концентрации появляется либо белый осадок, либо муть (холостой опыт!).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Анализ и синтез
- § 2. Предмет аналитической химии
- § 3. Развитие аналитической химии
- § 4. Качественный и количественный анализ
- ГЛАВА I. ПРИМЕНЕНИЕ ЗАКОНА ДЕЙСТВИЯ МАСС В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Влияние среды на состояние ионов в растворах
- § 2. Обратимые и необратимые аналитические реакции
- § 3. Направление аналитических реакций; правила обменного разложения
- § 4. Закон действия масс и следствие из него
- § 5. Границы применимости закона действия масс
- § 6. Сильные и слабые электролиты
- § 7. Активность
- § 8. Коэффициент активности и ионная сила
- Б. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ (В ГОМОГЕННЫХ СИСТЕМАХ)
- § 9. Гомогенные и гетерогенные системы
- § 10. Ионное произведение воды
- § 11. Ионы гидроксония
- § 12. Равновесие ионов в водных растворах; понятие о pH
- § 13. Равновесие в водных растворах слабых электролитов
- § 14. Влияние сильных кислот или сильных оснований на степень электролитической диссоциации слабых электролитов
- § 15. Приближенные формулы для расчета [H+] и [OH-] в водных растворах кислот и оснований
- В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
- § 16. Буферные растворы
- § 17. Применение буферных растворов в химическом анализе
- Г. РАВНОВЕСИЯ В РАСТВОРАХ ГИДРОЛИЗУЮЩИХСЯ СОЛЕЙ
- § 18. Теоретические основы гидролиза
- § 19. Механизм гидролитического расщепления
- § 20. Подавление и усиление гидролиза солей
- Д. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ТИПИЧНО АМФОТЕРНЫХ ЭЛЕКТРОЛИТОВ
- § 21. Поведение амфотерных гидроокисей в водных растворах
- § 22. Константы электролитической диссоциации амфотерных гидроокисей
- Е. РАВНОВЕСИЯ В СИСТЕМАХ: ОСАДОК-НАСЫЩЕННЫЙ РАСТВОР
- § 23. Осаждение как один из основных методов химического анализа
- § 24. Произведение растворимости
- § 25. Произведение активностей
- § 26. Вычисление растворимости электролитов в воде по величине произведения растворимости
- § 27. Влияние различных факторов на растворимость малорастворимых электролитов
- Ж. ОСНОВЫ ТЕОРИИ ОБРАЗОВАНИЯ И РАЗЛОЖЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИИ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 28. Характеристика комплексных соединений, имеющих значение в химическом анализе
- § 29. Квантовомеханические представления о строении комплексов
- § 30. Равновесия в растворах комплексных соединений
- § 31. Константы нестойкости комплексов
- § 32. Внутрикомплексные соединения
- § 33. Методы разложения и образования комплексов, применяемых в аналитической химии
- § 34. Применение метода комплексообразования в химическом анализе
- ГЛАВА II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Окисление—восстановление как один из основных методов химического анализа
- § 2. Направление реакций окисления—восстановления
- § 3. Окислительно-восстановительные потенциалы
- § 4. Зависимость между величинами окислительно-восстановительных потенциалов и условиями, в которых протекают реакции окисления—восстановления
- § 5. Вычисление окислительно-восстановительных потенциалов
- § 6. Вычисление окислительно-восстановительных потенциалов с учетом коэффициентов активности
- ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
- § 1. Обнаружение отдельных элементов
- § 2. Анализ мокрым и сухим путем
- § 3. Химические и физические методы качественного анализа
- § 4. Макро-, полумикро- и микрометоды
- § 5. Капельный анализ
- § 6. Микрокристаллоскопический анализ
- § 7. Метод растирания порошков
- § 8. Методы анализа, основанные на нагревании и сплавлении веществ
- § 9. Спектральный качественный анализ
- § 10. Хроматографический метод анализа
- § 11. Кинетические методы анализа
- Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
- § 12. Специфичность и чувствительность реакций
- § 13. Максимальная чувствительность аналитических реактивов
- § 14. Способы повышения чувствительности реакций
- § 15. Маскировка мешающих ионов
- § 16. Определение pH среды
- § 17. Регулирование pH среды в процессе аналитических определений
- В. РЕАКТИВЫ
- § 18. Понятие о химических реактивах
- § 19. Концентрация применяемых реактивов
- § 20. Техника пользования реактивами
- Г. ПОСУДА И ПРИБОРЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕННОМ АНАЛИЗЕ
- § 21. Химическая посуда
- § 22. Приборы
- Д. АНАЛИТИЧЕСКИЕ ГРУППЫ
- § 23. Дробный и систематический анализ
- § 24. Аналитическая классификация катионов
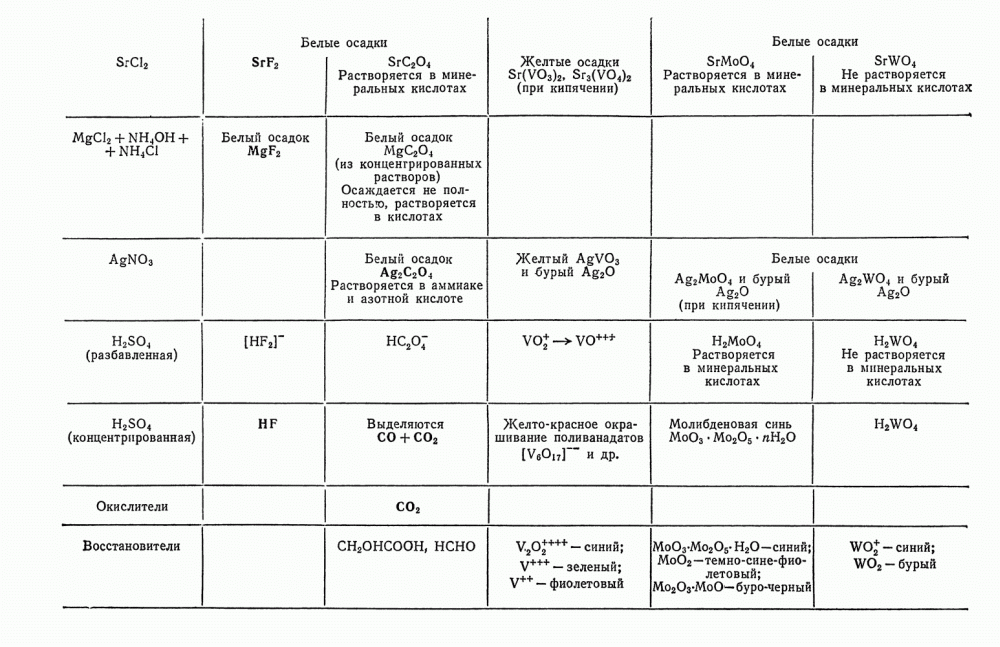
- § 25. Сводные таблицы действия реактивов на катионы и анионы
- Е. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ ИОНОВ
- § 26. Значение периодического закона в аналитической химии
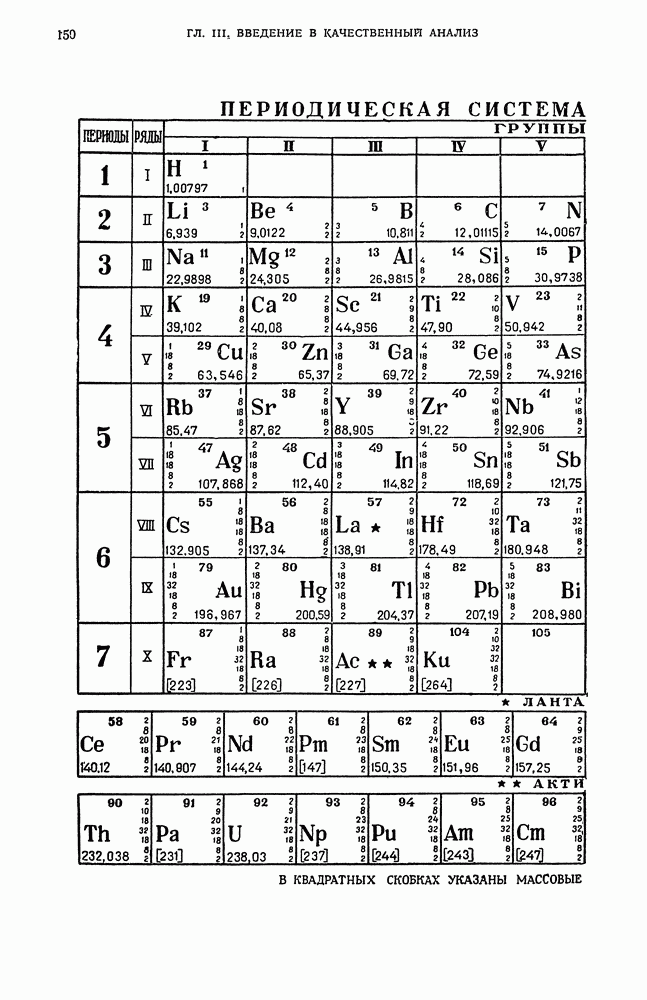
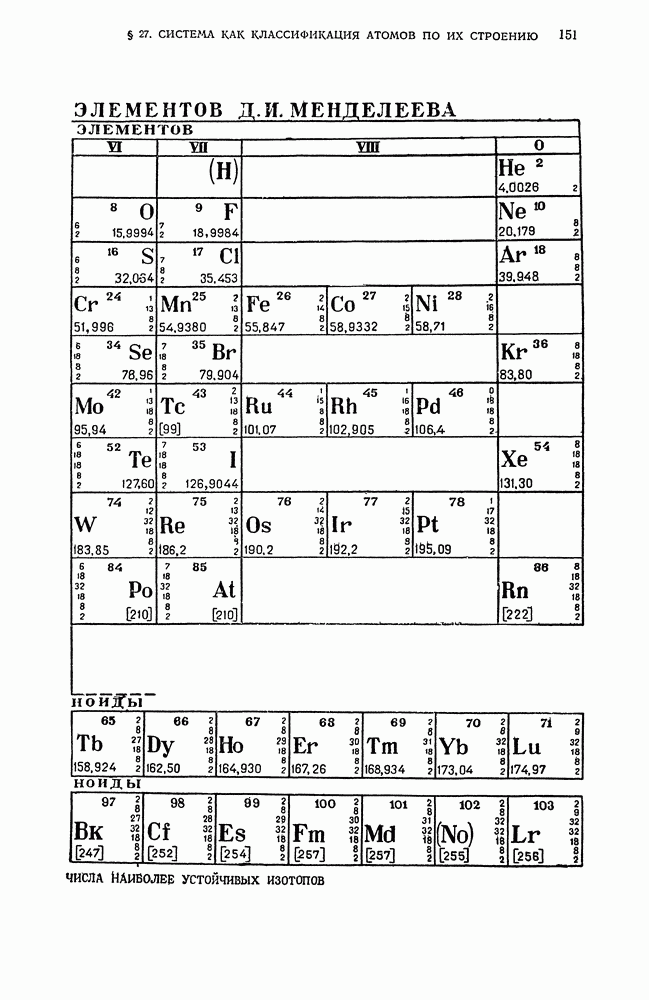
- § 27. Периодическая система элементов Д. И. Менделеева как классификация атомов по их строению
- § 28. Зависимость некоторых химических свойств элементов от положения их в периодической системе Д. И. Менделеева
- § 29. Растворимость химических соединений в связи с положением элементов в периодической системе Д. И. Менделеева
- § 30. Открытие новых аналитических реакций
- § 31. Аналитические группы и периодическая система элементов Д. И. Менделеева
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ КАТИОНОВ И АНАЛИЗ СМЕСЕЙ КАТИОНОВ
- § 1. Характеристика первой аналитической группы катионов
- § 2. Общие реакции катионов первой аналитической группы
- РЕАКЦИИ КАТИОНОВ 1-й ПОДГРУППЫ
- § 3. Обнаружение NН-ионов
- § 4. Методы разложения и удаления солей аммония
- § 5. Обнаружение K-ионов
- § 6. Обнаружение Rb-ионов
- § 7. Обнаружение Cs-ионов
- § 8. Анализ смеси катионов первой подгруппы
- РЕАКЦИИ КАТИОНОВ 2-й ПОДГРУППЫ
- § 9. Обнаружение Li-ионов
- § 10. Обнаружение Na-ионов
- § 11. Обнаружение Mg-ионов
- § 12. Обзор действия реактивов на катионы первой аналитической группы
- § 13. Анализ смеси катионов второй подгруппы
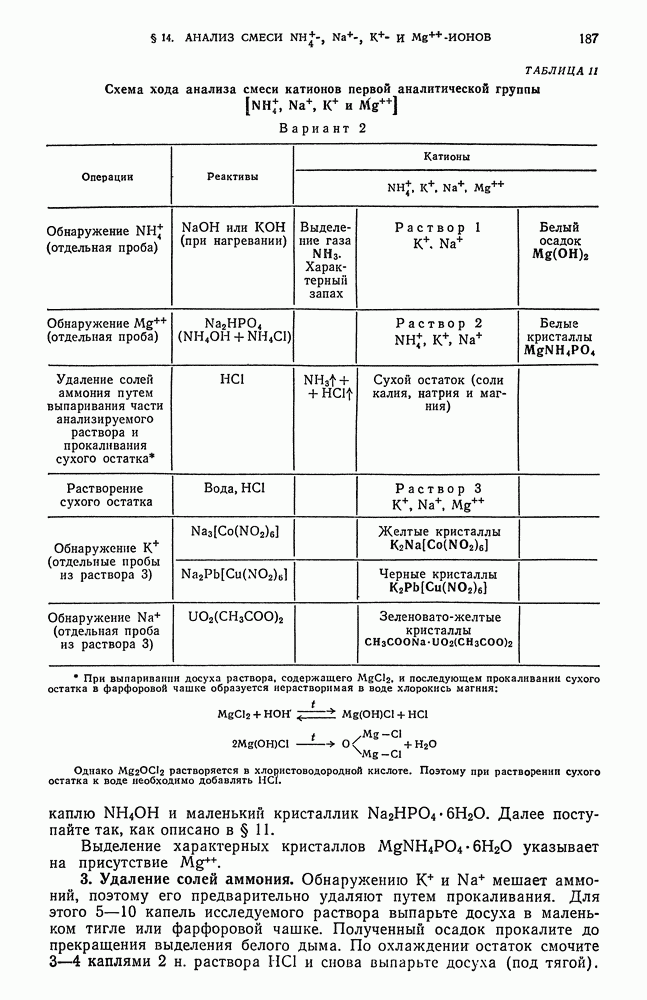
- § 14. Анализ смеси ионов
- § 15. Анализ смеси ионов
- ГЛАВА V. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика второй аналитической группы катионов
- § 2. Общие реакции катионов второй аналитической группы
- § 3. Обнаружение Ca-ионов
- § 4. Обнаружение Sr-ионов
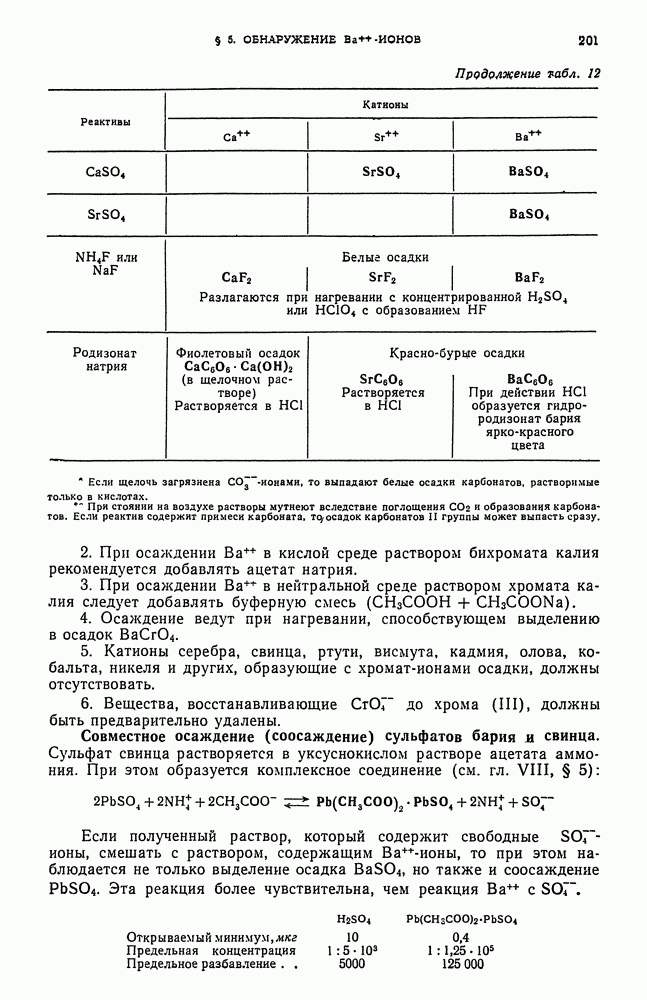
- § 5. Обнаружение Ba-ионов
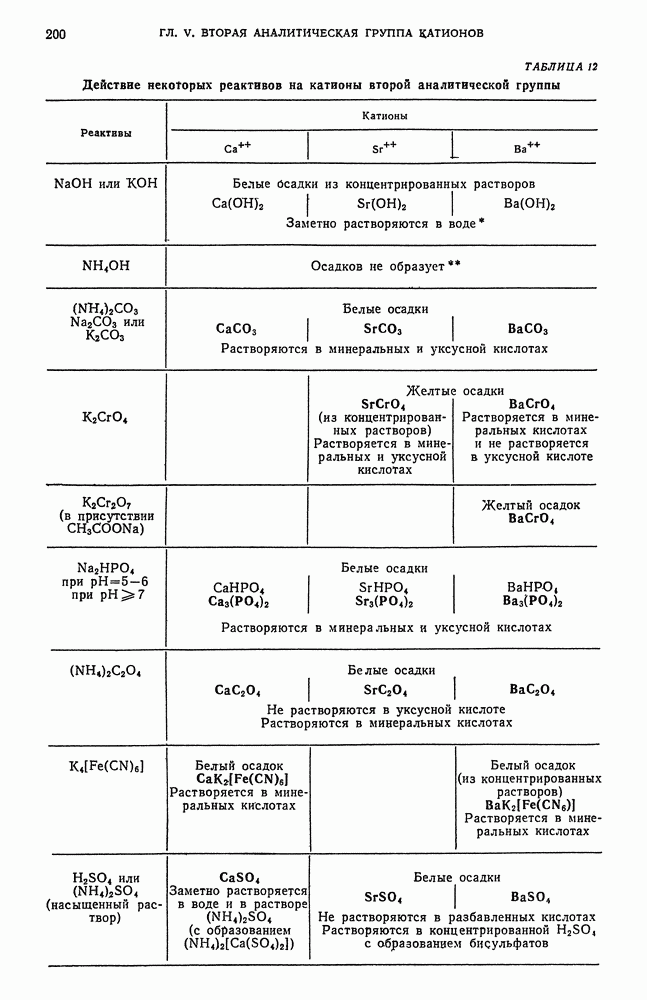
- § 6. Обзор действия реактивов на катионы второй аналитической группы
- § 7. Основы теории осаждения катионов второй аналитической группы групповым реактивом—карбонатом аммония
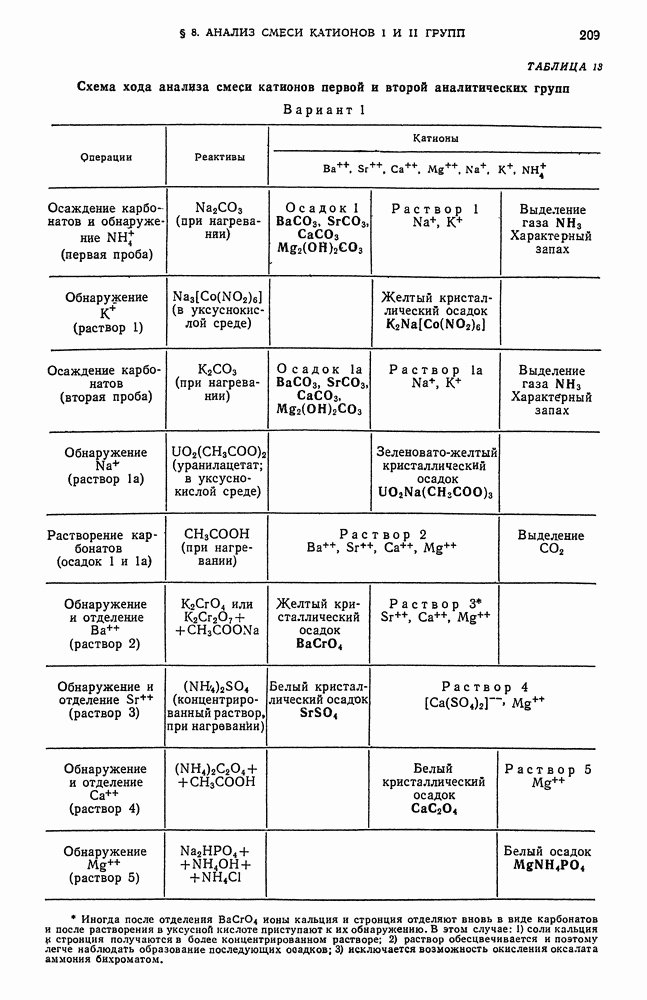
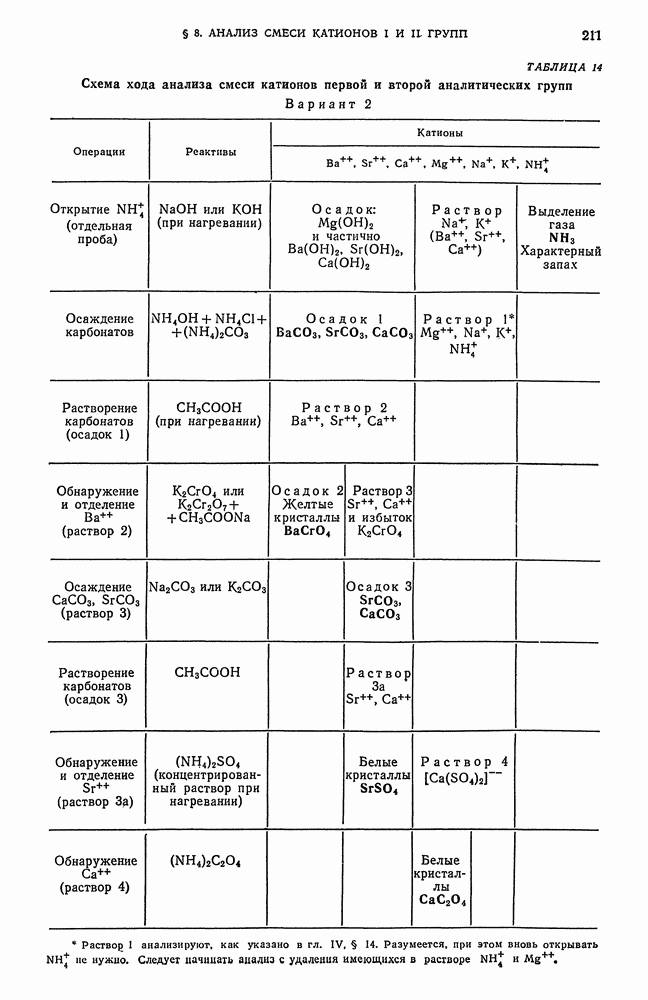
- § 8. Систематический ход анализа смеси катионов первой и второй аналитических групп
- § 9. Систематический ход анализа смеси катионов первой и второй аналитических групп в присутствии ионов
- § 10. Теоретические основы перевода сульфатов катионов второй аналитической группы в карбонаты
- ГЛАВА VI. ТРЕТЬЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика третьей аналитической группы катионов
- § 2. Общие реакции катионов третьей аналитической группы
- § 3. Обнаружение Be-ионов
- § 4. Обнаружение Al-ионов
- § 5. Обнаружение ионов титана (IV)
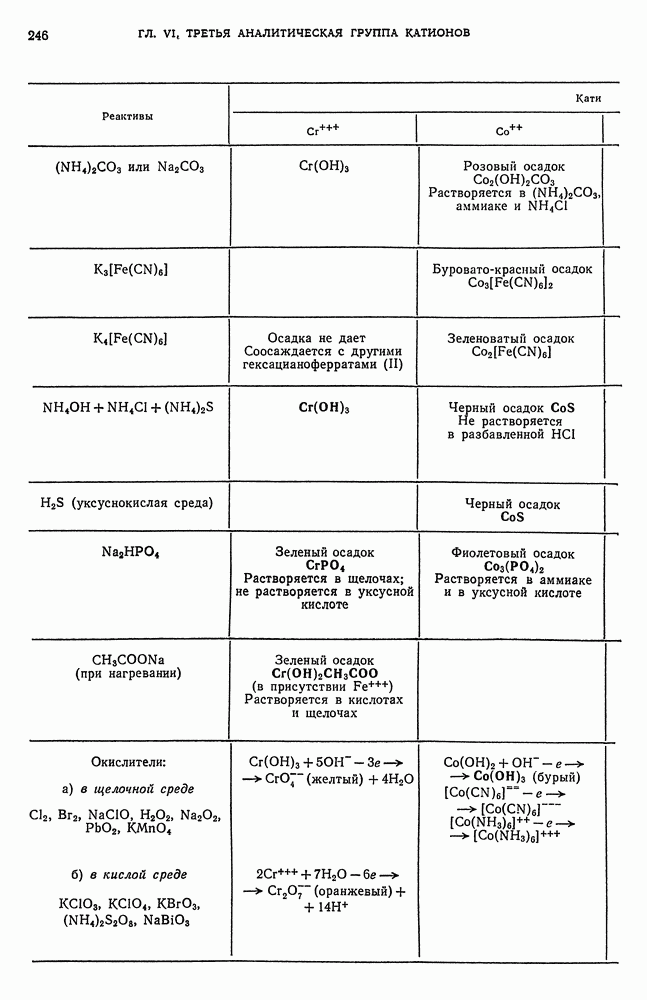
- § 6. Обнаружение Cr-ионов
- § 7. Обнаружение Mn-ионов
- § 8. Обнаружение Fe-ионов
- § 9. Обнаружение Fe-ионов
- § 10. Обнаружение Co-ионов
- § 13. Обнаружение ионов циркония (IV)
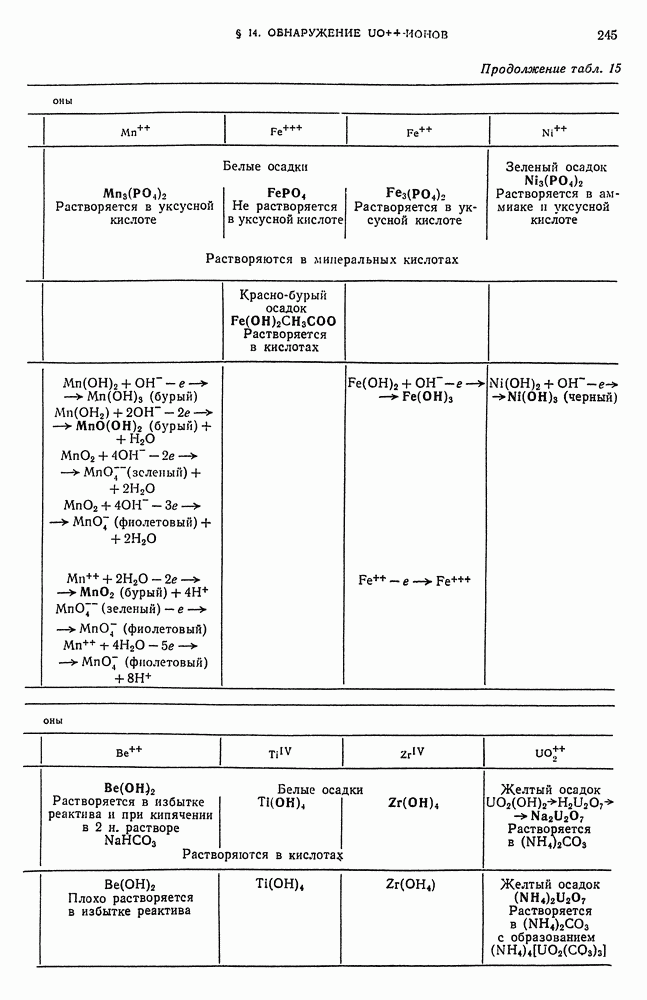
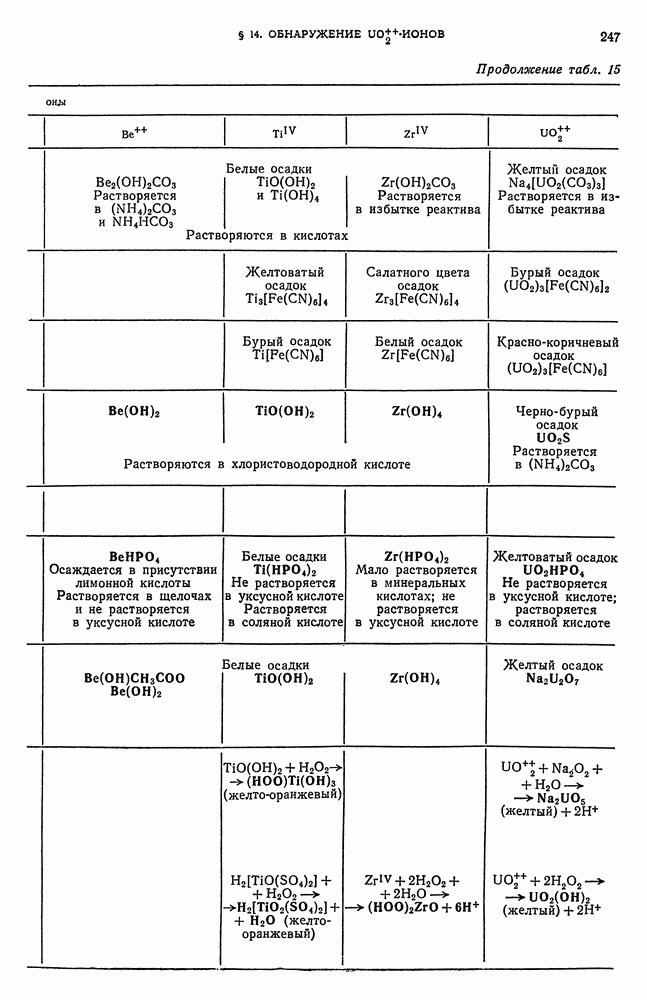
- § 14. Обнаружение UO-ионов
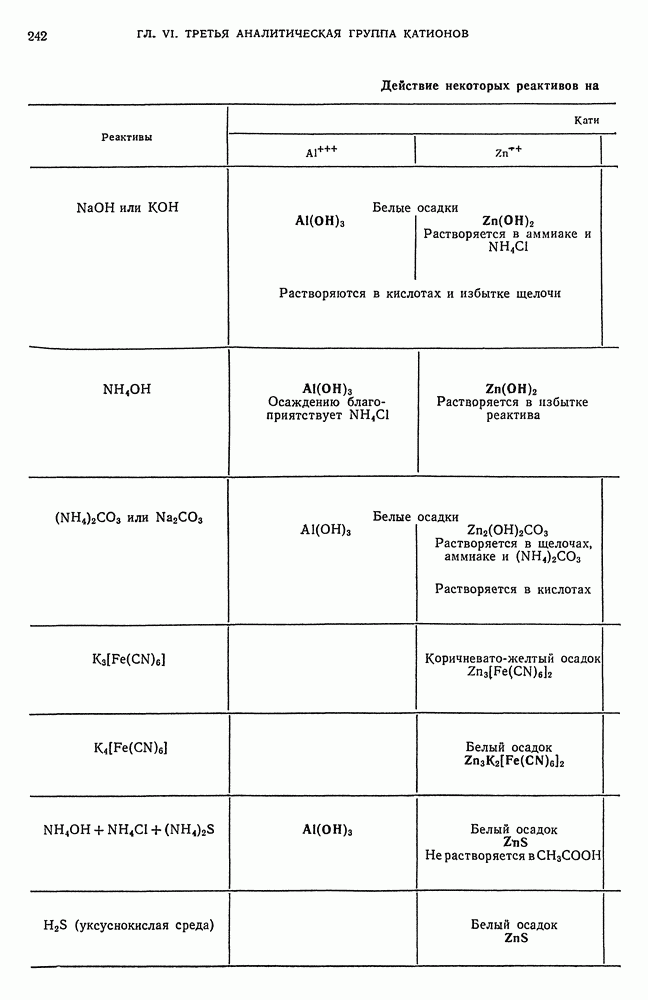
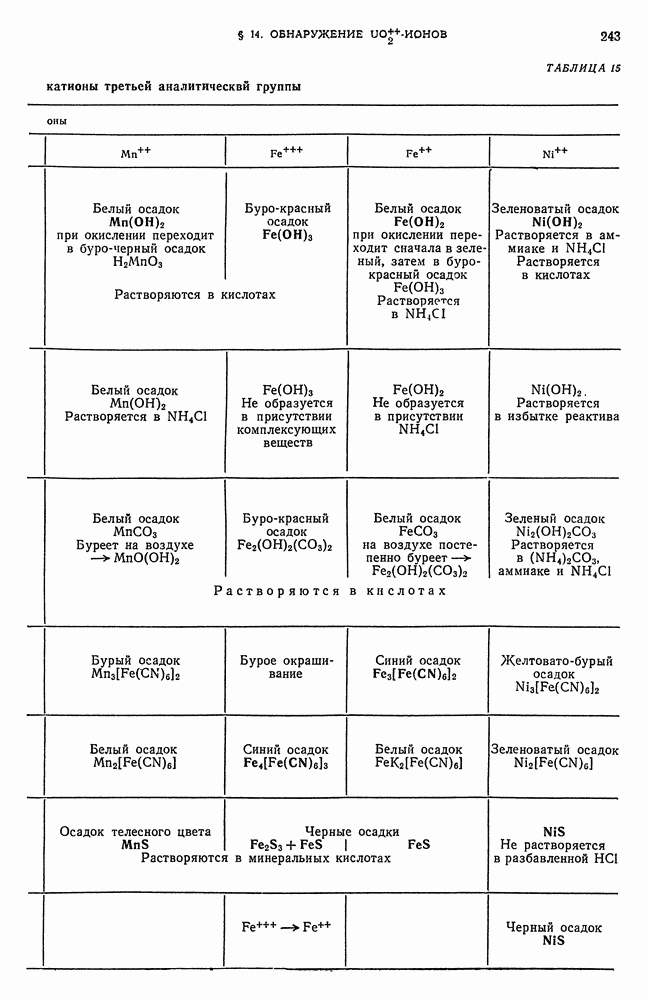
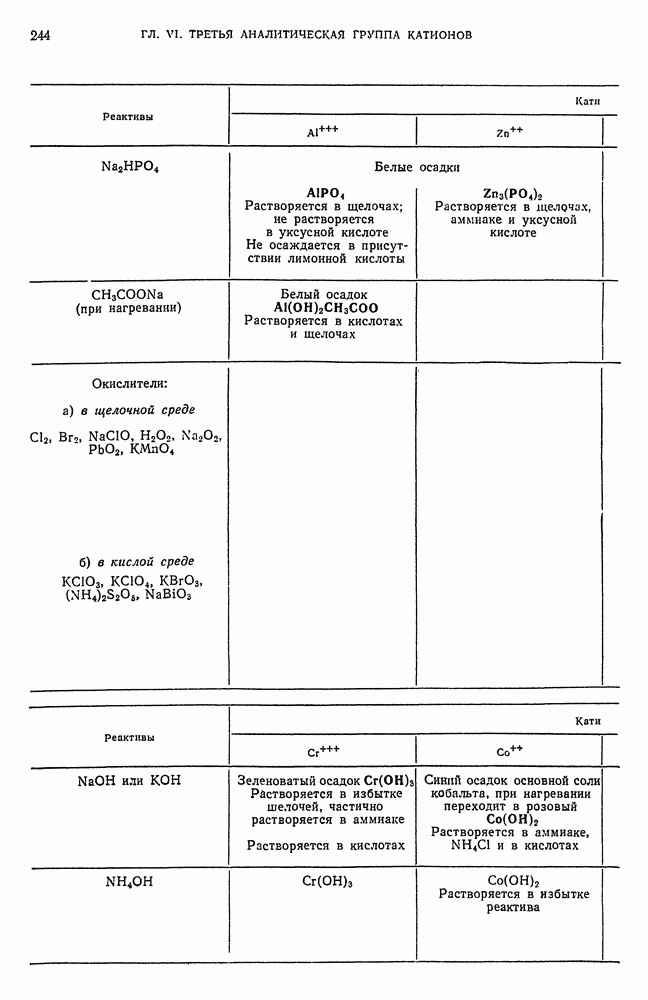
- § 15. Обзор действия реактивов на катионы третьей аналитической группы
- § 16. Использование коллоидных систем в химическом анализе
- § 17. Основы теории осаждения катионов третьей аналитической группы групповым реактивом — сульфидом аммония
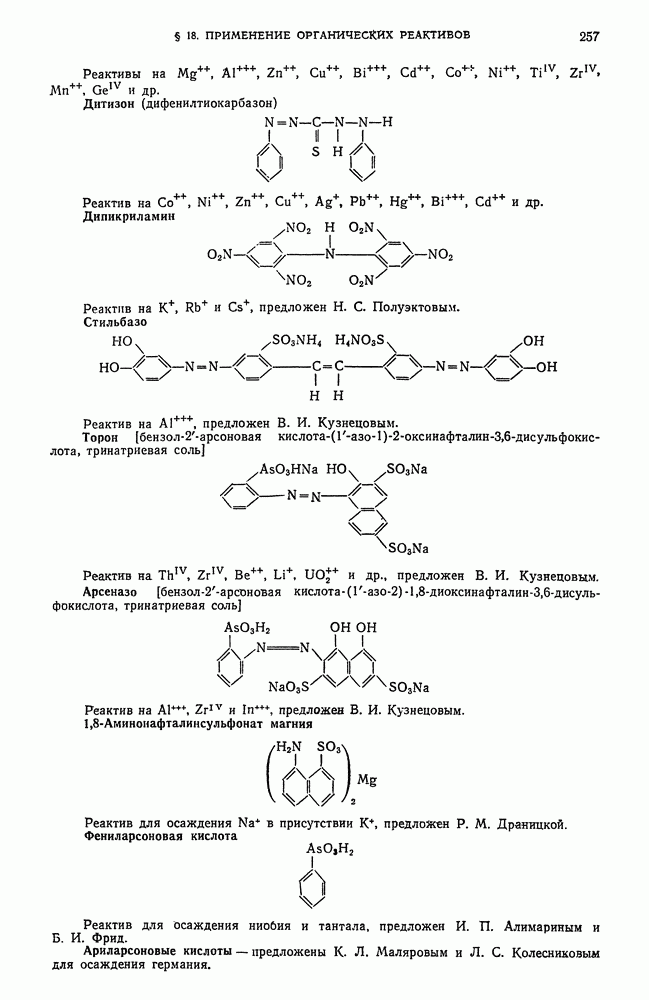
- § 18. Теоретические основы применения органических реактивов в качественном анализе неорганических веществ
- § 19. Методы разделения некоторых катионов третьей аналитической группы
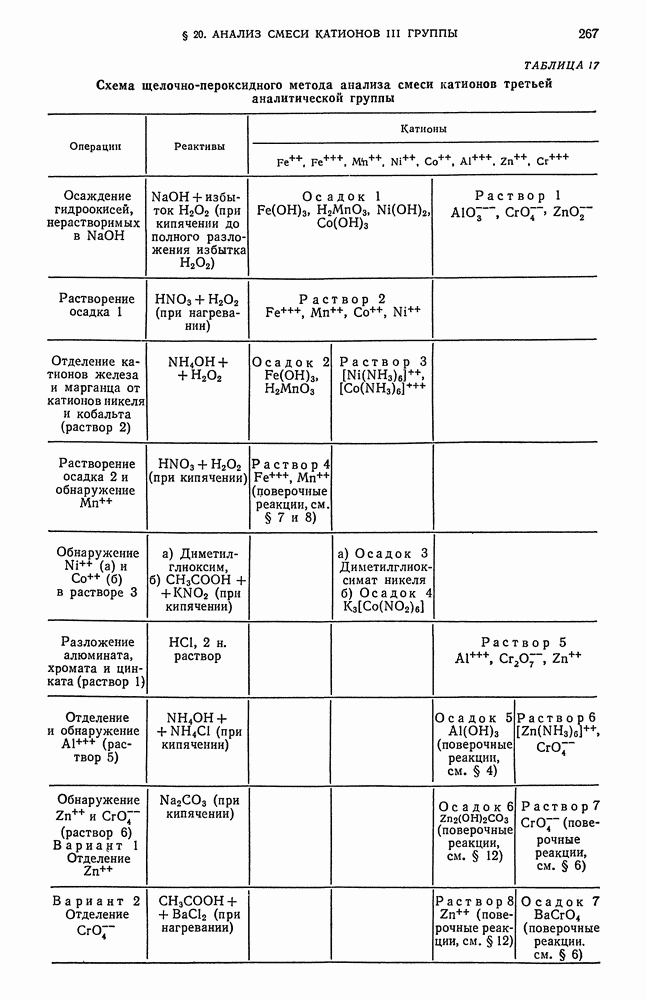
- § 20. Систематический ход анализа смеси катионов третьей аналитической группы
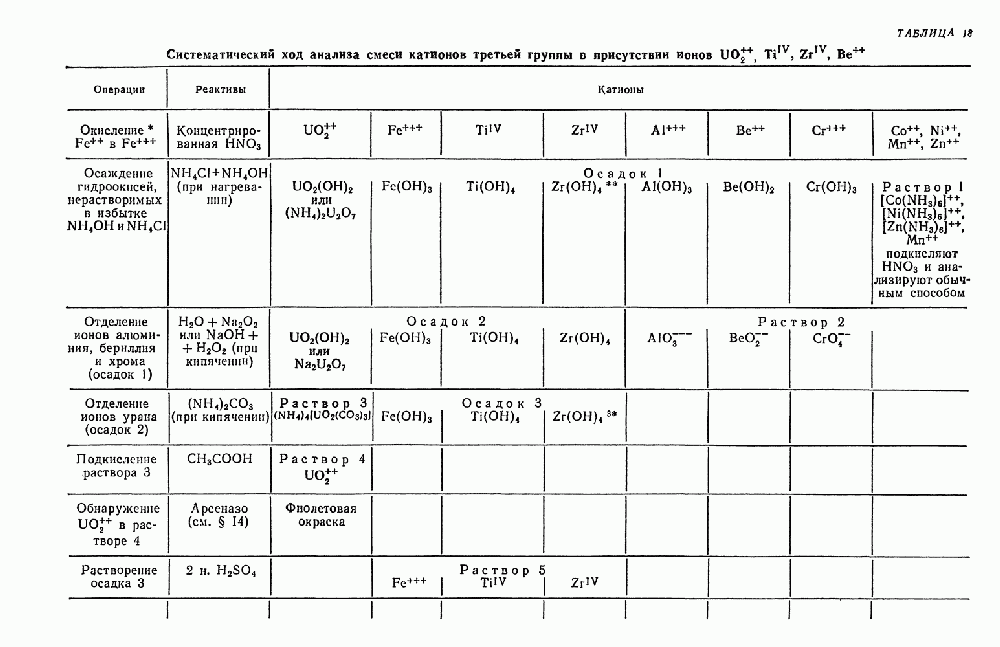
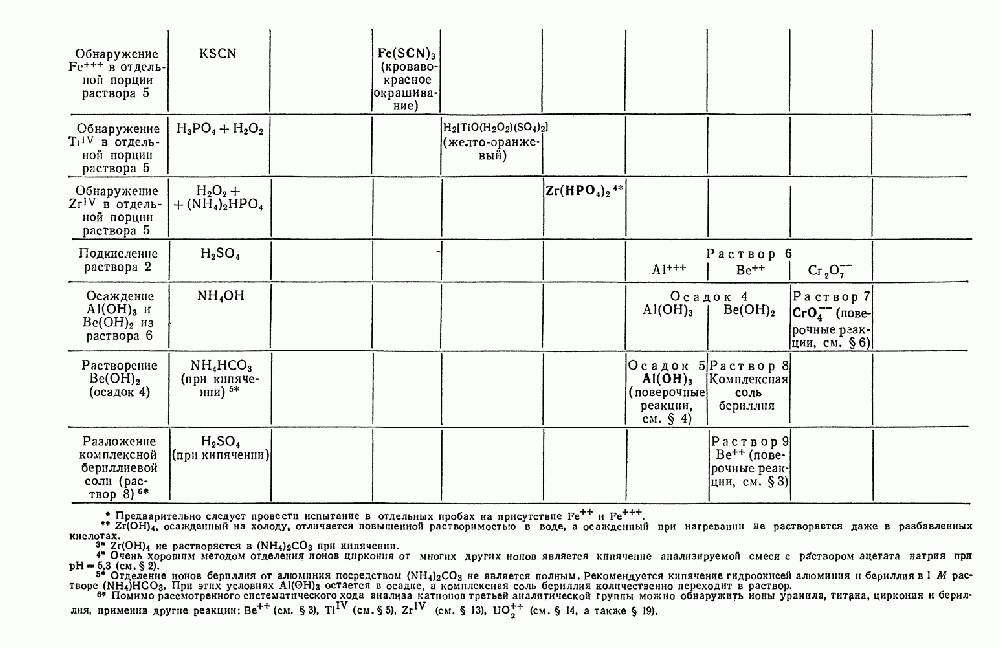
- § 21. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп
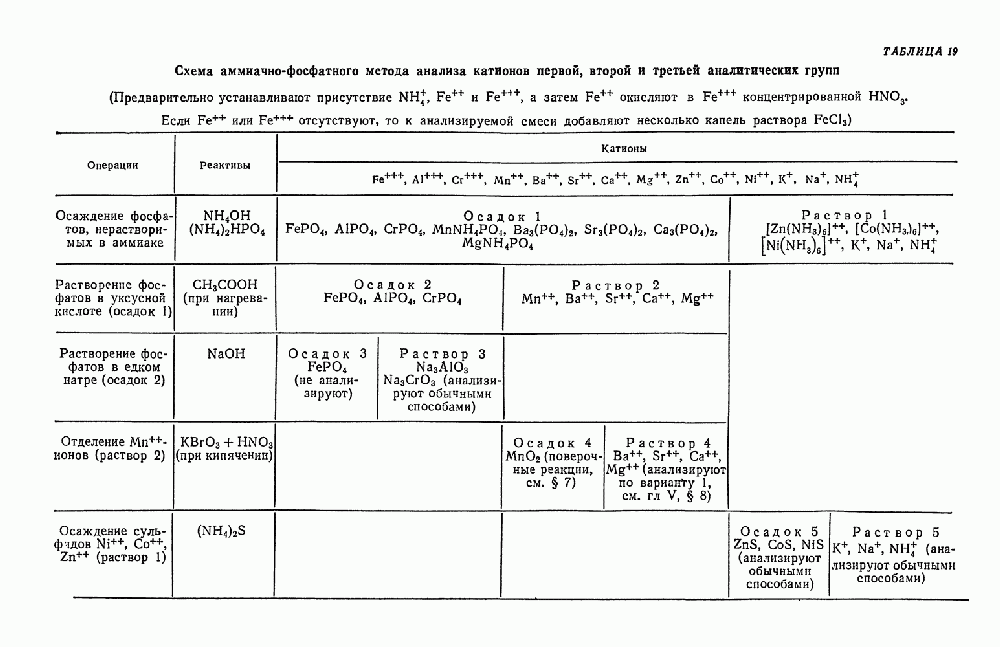
- § 22. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп в присутствии PO-ионов
- ГЛАВА VII. ЧЕТВЕРТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика четвертой аналитической группы катионов
- § 2. Общие реакции катионов четвертой аналитической группы
- РЕАКЦИИ КАТИОНОВ ПЕРВОЙ ПОДГРУППЫ (ПОДГРУППЫ МЕДИ)
- § 3. Обнаружение Hg-ионов
- § 4. Обнаружение Cu-ионов
- § 5. Обнаружение Cd-ионов
- § 6. Обнаружение Bi-ионов
- РЕАКЦИИ КАТИОНОВ ВТОРОЙ ПОДГРУППЫ (ПОДГРУППЫ МЫШЬЯКА)
- § 7. Обнаружение ионов мышьяка (III)
- § 8. Обнаружение ионов мышьяка (V)
- § 9. Общие реакции обнаружения
- § 10. Обнаружение ионов сурьмы (III)
- § 11. Обнаружение ионов сурьмы (V)
- § 12. Общие реакции обнаружения Sb
- § 13. Обнаружение ионов олова (II)
- § 14. Обнаружение ионов олова (IV)
- § 15. Общие реакции обнаружения ионов олова (II) и олова (IV)
- § 16. Отделение ионов олова от других ирнов четвертой аналитической группы
- § 17. Обнаружение ионов германия (IV)
- § 18. Отделение ионов германия от других ионов четвертой аналитической группы
- § 19. Обзор действия реактивов на катионы четвертой аналитической группы
- § 20. Основы теории осаждения сульфидов катионов четвертой аналитической группы групповым реактивом — сероводородом
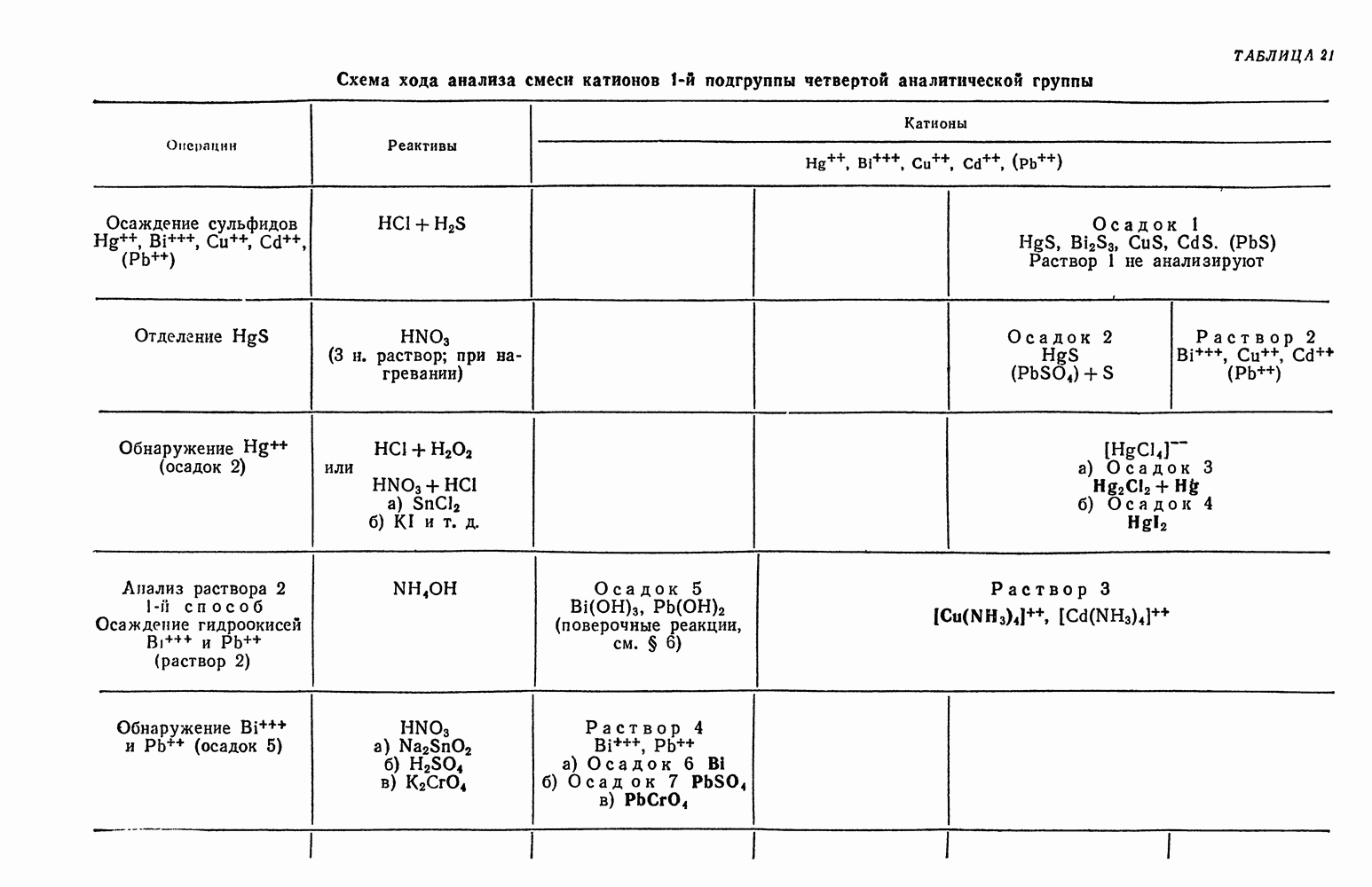
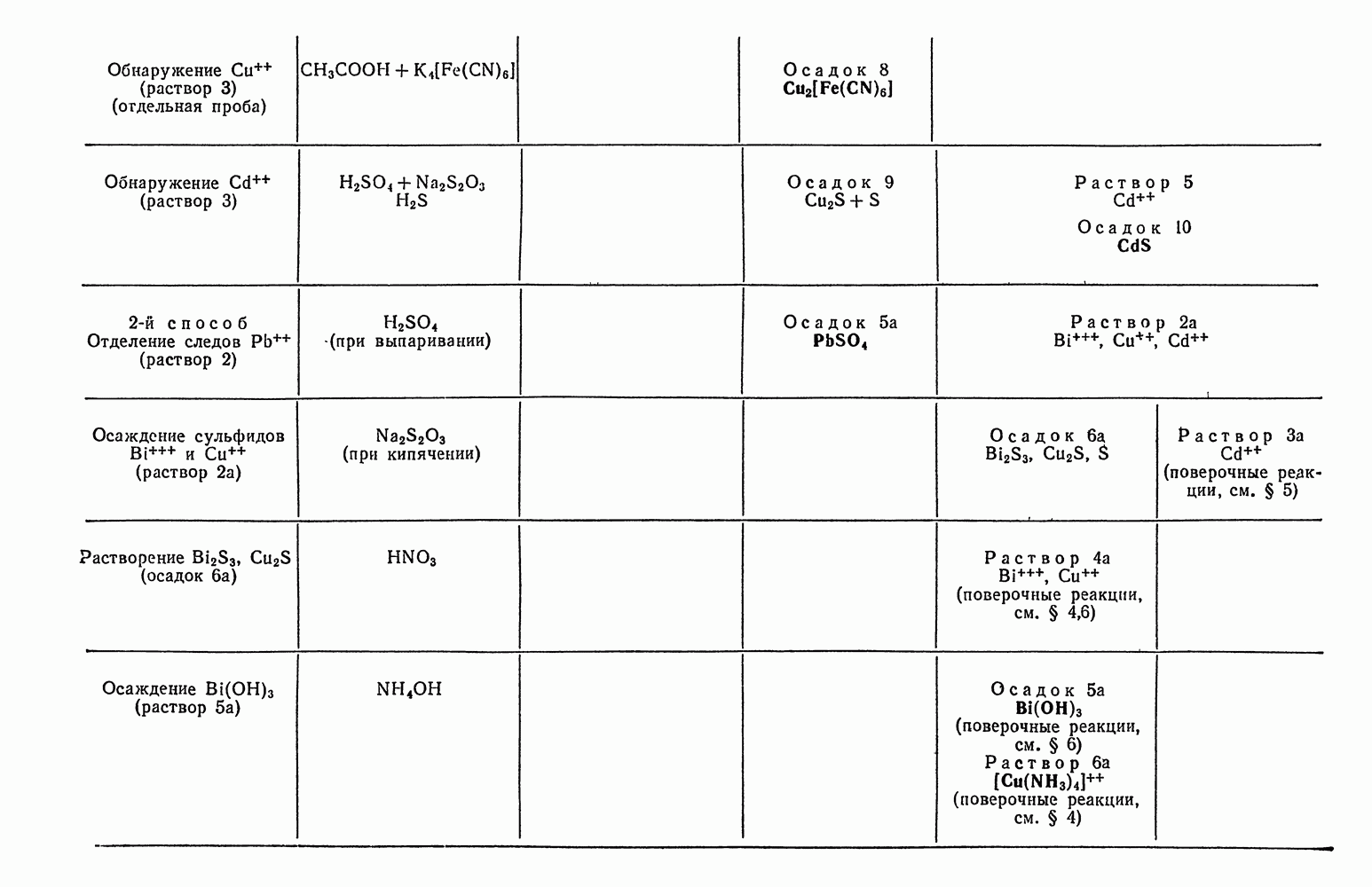
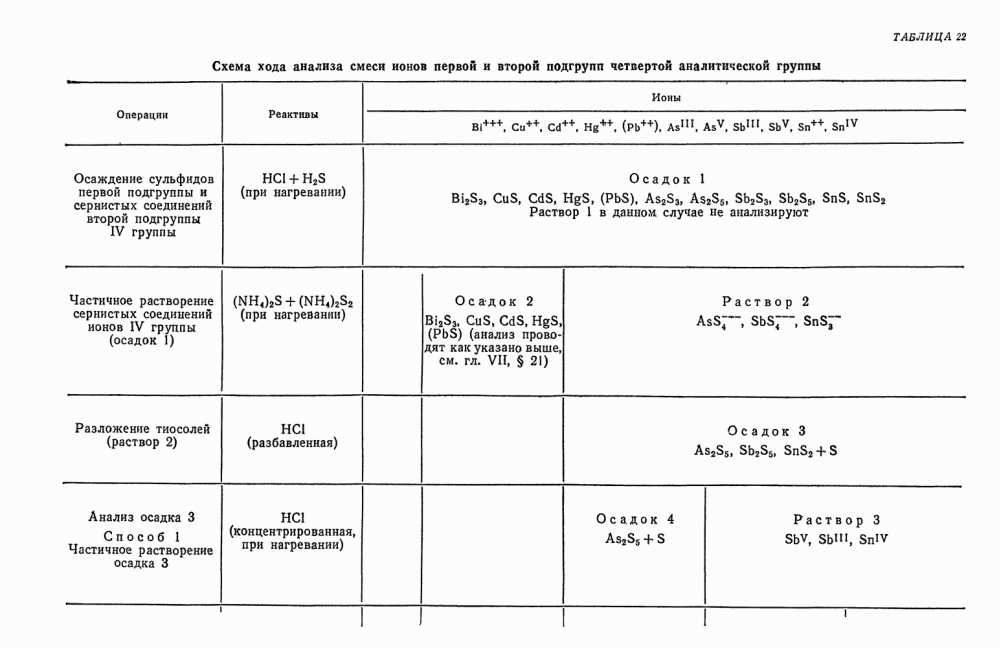
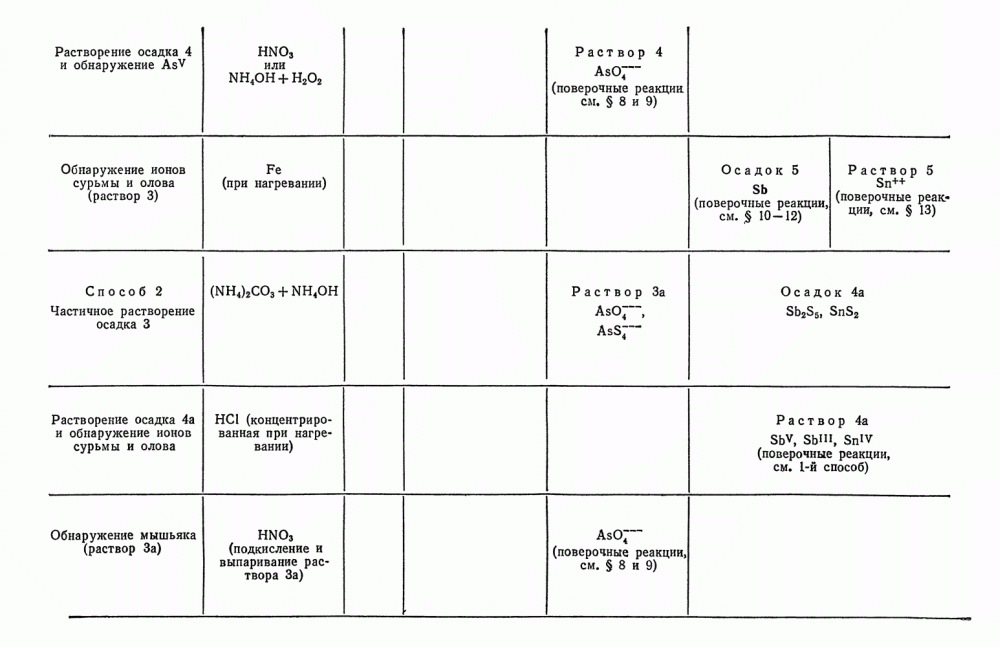
- § 21. Систематический ход анализа смеси катионов четвертой аналитической группы
- ГЛАВА VIII. ПЯТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ (ГРУППА СЕРЕБРА)
- § 1. Характеристика пятой аналитической группы катионов
- § 2. Общие реакции катионов пятой аналитической группы
- § 3. Обнаружение Ag-ионов
- § 4. Обнаружение [Hg]-ионов
- § 5. Обнаружение Pb-ионов
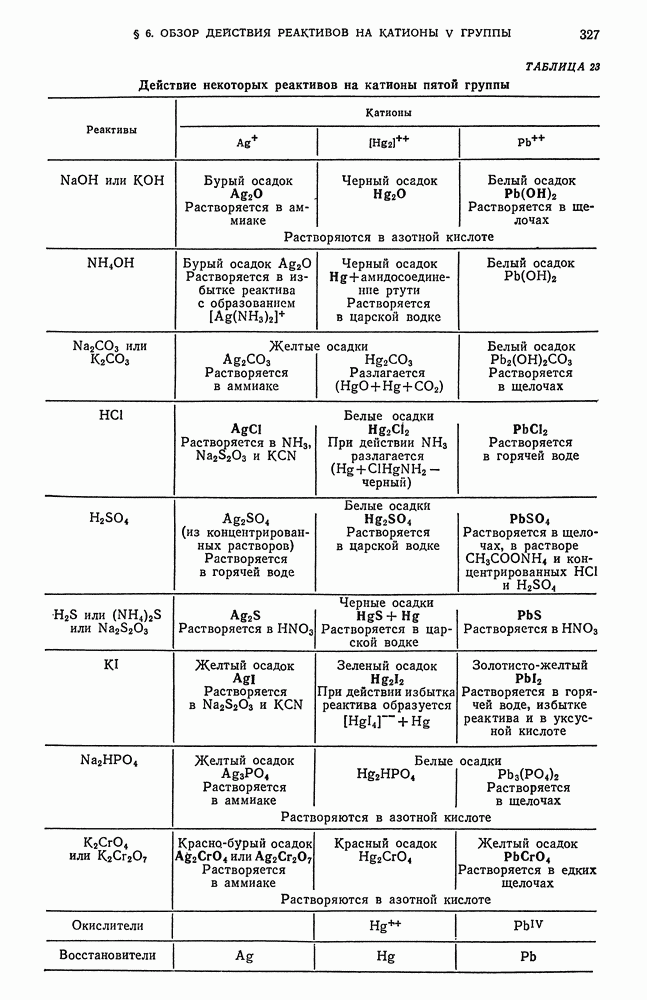
- § 6. Обзор действия реактивов на катионы пятой аналитической группы
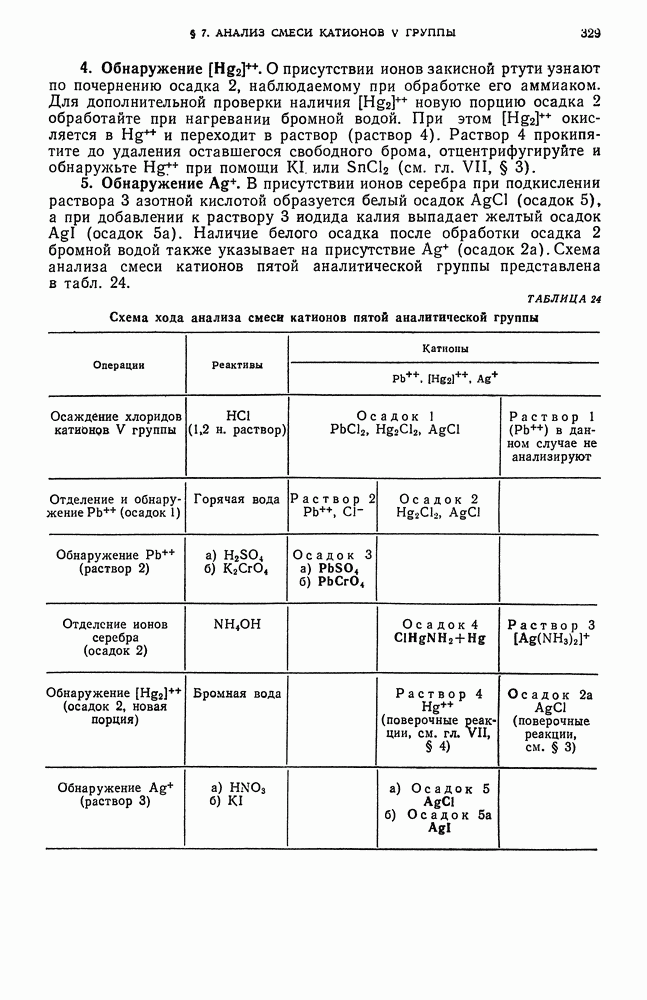
- § 7. Систематический ход анализа смеси катионов пятой аналитической группы
- ГЛАВА IX. АНАЛИЗ СМЕСИ ИОНОВ ВСЕХ ПЯТИ АНАЛИТИЧЕСКИХ ГРУПП
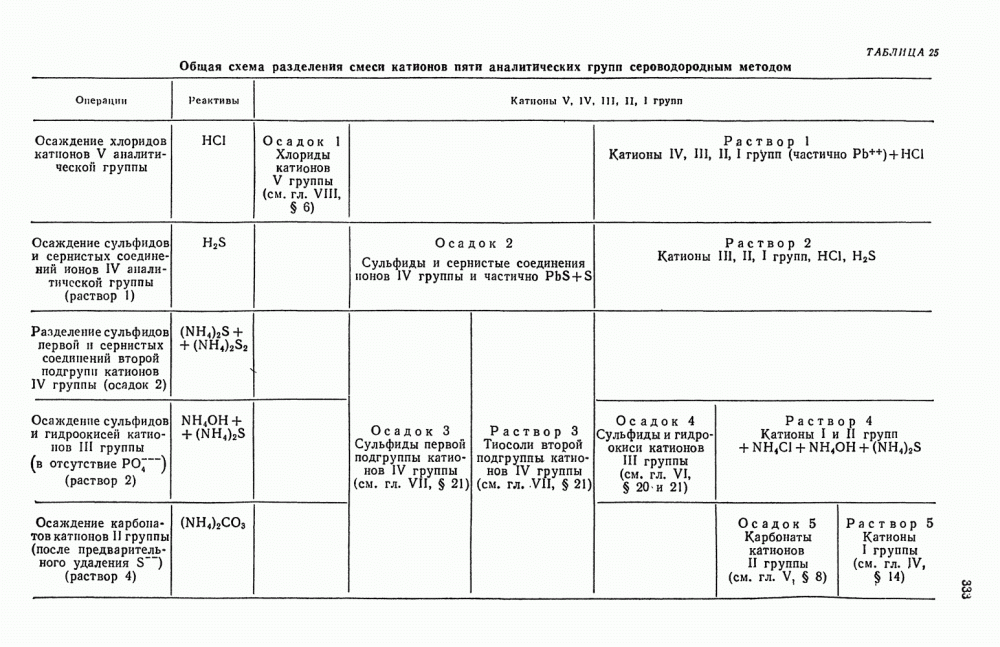
- § 1. Сероводородный метод анализа
- § 2. Недостатки сероводородного метода анализа
- § 3. Ошибки, возникающие при анализе смеси ионов пяти аналитических групп
- § 4. Бессероводородные методы анализа
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ АНИОНОВ И АНАЛИЗ СМЕСЕЙ АНИОНОВ
- § 1. Аналитическая классификация анионов
- § 2. Групповые реактивы на анионы
- § 3. Классификация методов анализа анионов
- ГЛАВА XI. ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика первой группы анионов
- § 2. Реакции анионов первой группы
- § 3. Обнаружение CI-ионов
- § 4. Обнаружение Br-ионов
- § 5. Обнаружение I-ионов
- § 6. Обнаружение CN-ионов
- § 7. Обнаружение SCN-ионов
- § 8. Обнаружение [Fe(CN)]-ионов
- § 9. Обнаружение Fe(CN)-ионов
- § 10. Обнаружение NO-ионов
- § 11. Обнаружение NO2-ионов
- § 12. Обнаружение S-ионов
- § 13. Обнаружение CH3COOO-ионов
- § 14. Обнаружение BrO3-ионов
- § 15. Обнаружение ClO3-ионов
- § 16. Обнаружение ClO4-ионов
- § 17. Обзор действия реактивов на анионы первой группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 18. Анализ смеси Cl, Br и I-ионов
- § 19. Анализ смеси Cl, Br, I и SCN-ионов
- § 20. Анализ смеси Cl, ClO3 и ClO4-ионов
- § 21. Анализ смеси NO2 и NO3-ионов
- § 22. Анализ смеси анионов первой группы
- ГЛАВА XII. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика второй группы анионов
- § 2. Общие реакции анионов второй группы
- § 3. Обнаружение SO3-ионов
- § 4. Обнаружение S2O3-ионов
- § 5. Обнаружение S2O3 в присутствии SO3-ионов
- § 6. Обнаружение SO4-ионов
- § 7. Обнаружение CO3-ионов
- § 8. Обнаружение CO3-ионов в присутствии SO3 и S2O3-ионов
- § 9. Обнаружение PO4-ионов
- § 10. Обнаружение CrO4-ионов
- § 11. Обнаружение AsO3-ионов
- § 12. Обнаружение AsO4-ионов
- § 13. Обнаружение BO2 и BO3-ионов
- § 14. Обнаружение SiO3-ионов
- § 15. Обнаружение F-ионов
- § 16. Обнаружение C2O4-ионов
- § 17. Обнаружение VO3-ионов
- § 18. Обнаружение MoO4-ионов
- § 19. Обнаружение WO4-ионов
- § 20. Обзор действия реактивов на анионы второй группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 21. Анализ смеси ионов
- § 22. Анализ смеси SO3, SO4, S2O3 и CO3-ионов
- § 23. Анализ смеси VO2, MoO4 и WO4-ионов
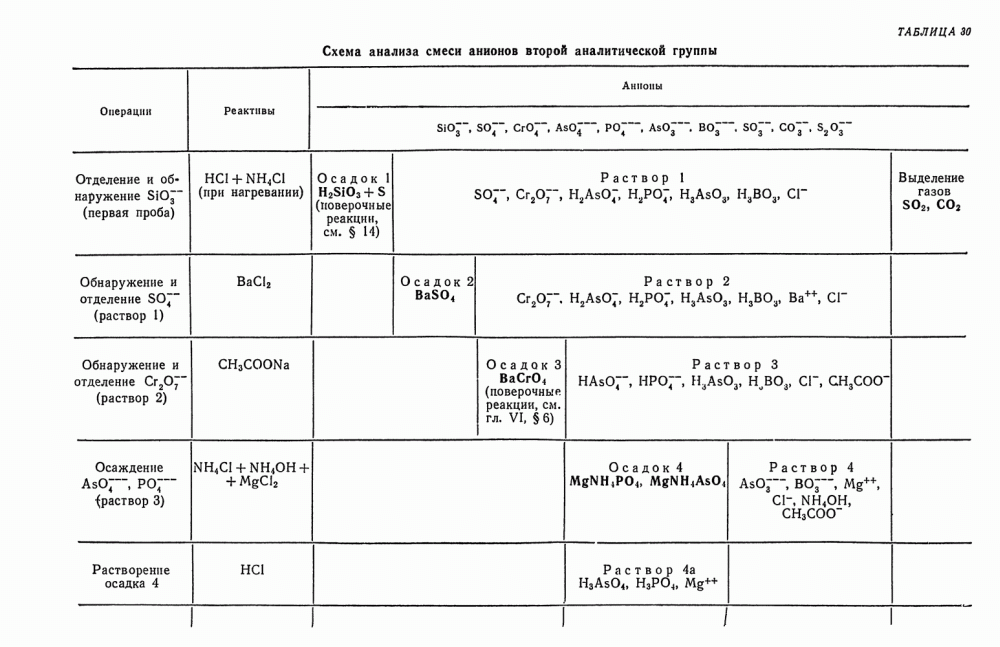
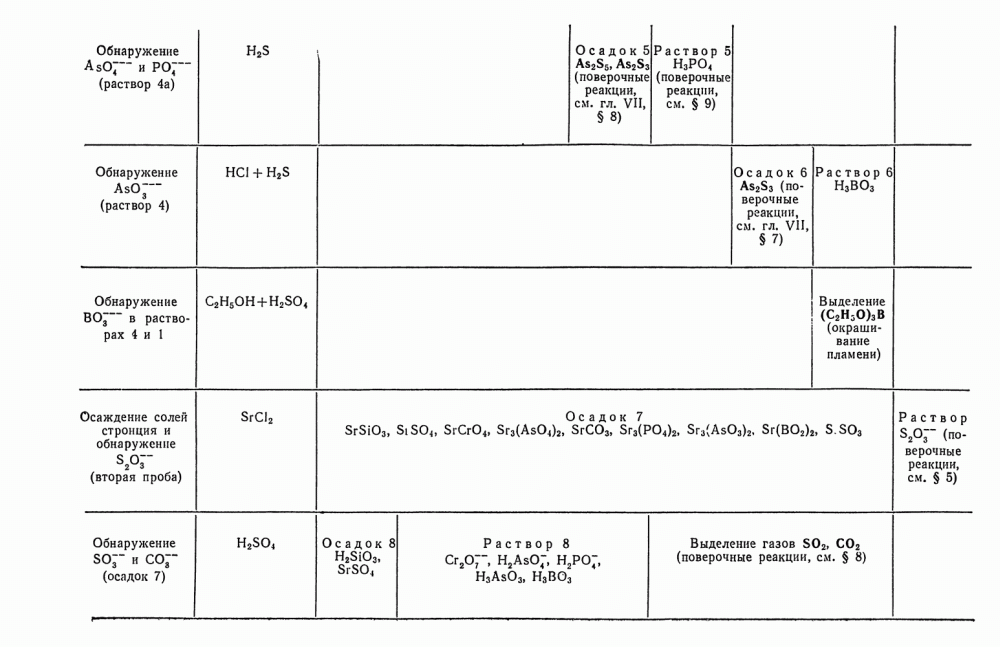
- § 24. Анализ смеси анионов второй группы
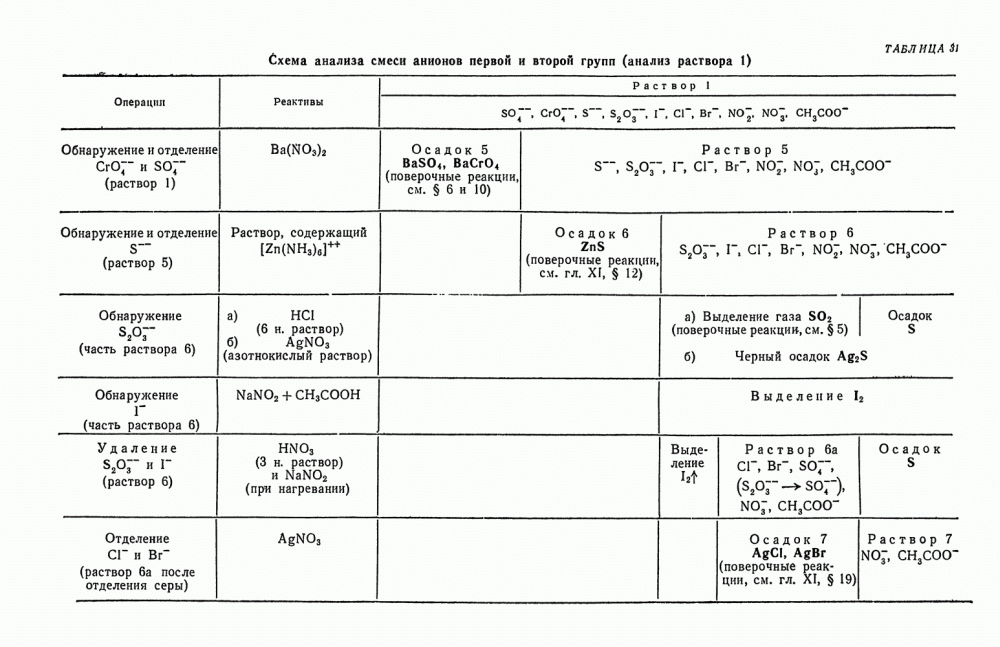
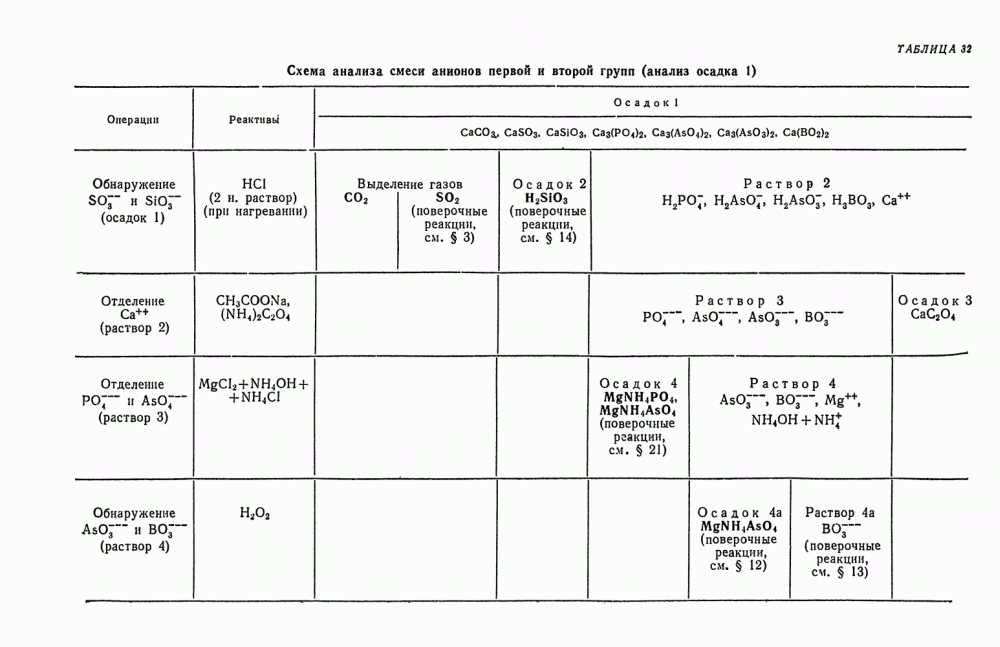
- § 25. Анализ смеси анионов первой и второй групп
- ГЛАВА XIII. ОБНАРУЖЕНИЕ СВОБОДНЫХ МЕТАЛЛОВ И НЕМЕТАЛЛОВ, ИДЕНТИФИЦИРОВАНИЕ СОЛЕЙ И ДРУГИХ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И АНАЛИЗ ИХ СМЕСЕЙ
- § 1. Подготовка вещества к анализу
- § 2. Предварительные испытания
- § 3. Растворение анализируемого вещества в воде, кислотах и щелочах
- § 4. Переведение в растворимое состояние веществ, нерастворимых в воде, кислотах и щелочах
- § 5. Анализ неизвестного вещества
- § 6. Обнаружение свободных элементов
- § 7. Идентифицирование солей и других индивидуальных соединений
- § 8. Обнаружение микропримесей
- § 9. Анализ сплавов
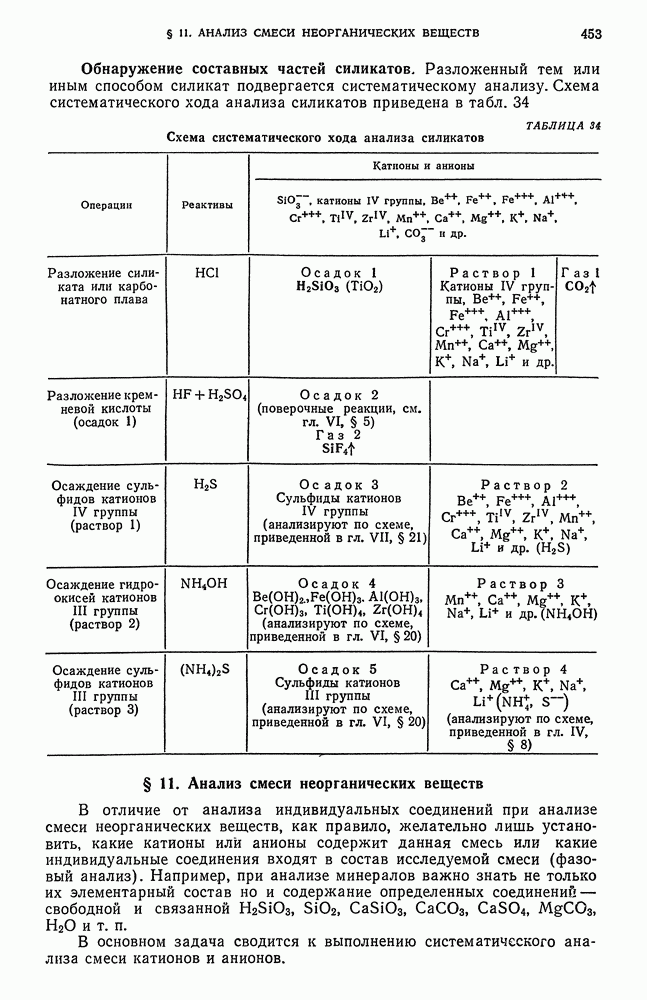
- § 10. Анализ силикатов и алюмосиликатов
- § 11. Анализ смеси неорганических веществ
- § 12. Экспрессный метод анализа смесей катионов и анионов
- § 13. Идентифицирование нерастворимых веществ
- ЛИТЕРАТУРА