| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 14. Анализ смеси ионов
Анализ смеси  может быть проведен разными способами.
может быть проведен разными способами.
Обычно анализ начинают с испытания реакции среды и определения  раствора, Для этого каплю анализируемого раствора наносят стеклянной палочкой на индикаторную бумагу или помещают каплю индикатора в исследуемый раствор (см. гл. III, § 16).
раствора, Для этого каплю анализируемого раствора наносят стеклянной палочкой на индикаторную бумагу или помещают каплю индикатора в исследуемый раствор (см. гл. III, § 16).
Эта проверка ицеет большое значение, позволяя сделать некоторые заключения, например сильнощелочная реакция раствора, не содержащего осадка и не пахнущего аммиаком, указывает на присутствие гидролизующихся солай типа  или свободных щелочей, и на отсутствие
или свободных щелочей, и на отсутствие  и NHJ; кислая реакция — на присутствие аммонийных солей сильных кислот или свободных кислот.
и NHJ; кислая реакция — на присутствие аммонийных солей сильных кислот или свободных кислот.
В дальнейшем мы не будем повторять о необходимости проверки реакции среды, но это испытание нужно проводить систематически в процессе анализа разнообразных смесей и индивидуальных соединений.
Предварительно из отдельной пробы открывают аммоний, который мешает дальнейшему обнаружению  . Если NHX отсутствует, то приступают к открытию других ионов. Если же предварительным опытом установлено, что анализируемый раствор содержит
. Если NHX отсутствует, то приступают к открытию других ионов. Если же предварительным опытом установлено, что анализируемый раствор содержит  -ионы, то их следует удалить перед проведением реакций на
-ионы, то их следует удалить перед проведением реакций на  (см. § 4).
(см. § 4).
Ход анализа Вариант 1
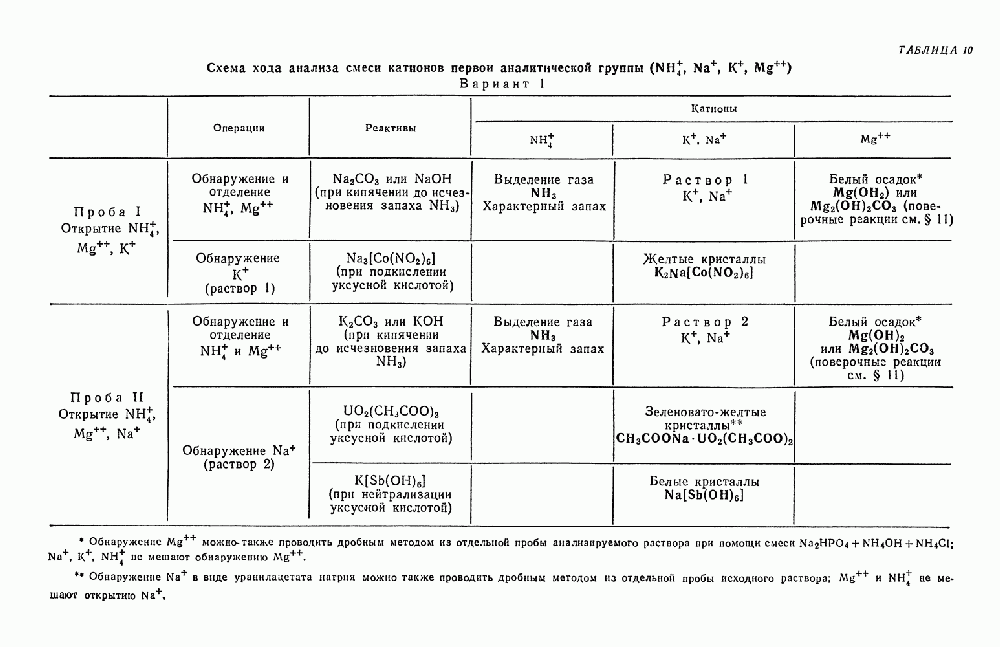
Рекомендуемый вариант систематического хода анализа смеси катионов I аналитической группы представлен в табл. 10.
1. Обнаружение и отделение  -ионов. Поместите в две пробирки по 5 капель анализируемой смеси. В одну пробирку (проба I), в которой предполагается открыть
-ионов. Поместите в две пробирки по 5 капель анализируемой смеси. В одну пробирку (проба I), в которой предполагается открыть  , добавьте 5 капель 2 н. раствора
, добавьте 5 капель 2 н. раствора  или
или  . В другую пробирку (проба II), в которой будете обнаруживать
. В другую пробирку (проба II), в которой будете обнаруживать  , прилейте 5 капель 2 н. раствора
, прилейте 5 капель 2 н. раствора  или КОН. Затем содержимое пробирок нагрейте на слабом пламени горелки до кипения. При этом в случае присутствия в анализируемом растворе солей аммония из обеих пробирок выделяется
или КОН. Затем содержимое пробирок нагрейте на слабом пламени горелки до кипения. При этом в случае присутствия в анализируемом растворе солей аммония из обеих пробирок выделяется  , который обнаруживают указанными в § 3 методами. Обнаружению
, который обнаруживают указанными в § 3 методами. Обнаружению  другие катионы не мешают.
другие катионы не мешают.
При наличии солей аммония необходимо кипятить раствор до полного исчезновения запаха аммиака.
2. Обнаружение и отделение  . При кипячении исследуемого раствора с
. При кипячении исследуемого раствора с  или
или  ионы калия и натрия остаются в растворе,
ионы калия и натрия остаются в растворе,  выпадает в осадок в виде оксикарбоната или гидроокиси (см. § 2).
выпадает в осадок в виде оксикарбоната или гидроокиси (см. § 2).
Если анализу подвергается смесь, содержащая только  , то в случае выделения осадка оксикарбоната, образующегося при кипячении отдельной порции исследуемого раствора с
, то в случае выделения осадка оксикарбоната, образующегося при кипячении отдельной порции исследуемого раствора с  или
или  , можно сделать вывод о присутствии
, можно сделать вывод о присутствии  .
.
Выпавшие при кипячении анализируемого раствора с  или
или  осадки
осадки  или
или  отделите от раствора фильтрованием или центрифугированием, растворите их в
отделите от раствора фильтрованием или центрифугированием, растворите их в  или
или  и проделайте поверочные реакции на
и проделайте поверочные реакции на  (§ 11). Так как
(§ 11). Так как  обнаружению
обнаружению  с реактивом
с реактивом  не мешают, то ионы магния могут быть обнаружены также из отдельной пробы раствора дробным методом.
не мешают, то ионы магния могут быть обнаружены также из отдельной пробы раствора дробным методом.
Для проведения реакции на  дробным методом поместите в пробирку 2 капли исходного анализируемого раствора и прибавьте по 2 капли 2 н. раствора
дробным методом поместите в пробирку 2 капли исходного анализируемого раствора и прибавьте по 2 капли 2 н. раствора  н. раствора
н. раствора  и 2 н. раствора
и 2 н. раствора  . Реакция раствора должна быть щелочной.
. Реакция раствора должна быть щелочной.
Таблица 10. Схема хода анализа смеси катионов первой аналитической группы ( ).
).

Содержимое пробирки нагрейте. В присутствии  выпадает белый кристаллический осадок магний-аммоний фосфата
выпадает белый кристаллический осадок магний-аммоний фосфата  (см. § 11).
(см. § 11).
С фильтратом, полученным из первой пробирки, в которую был прибавлен  или
или  , проведите реакции на
, проведите реакции на  (см. § 5); с фильтратом из второй пробирки, в которую был прибавлен
(см. § 5); с фильтратом из второй пробирки, в которую был прибавлен  или КОН, — выполните реакции для обнаружения
или КОН, — выполните реакции для обнаружения  (см. § 10).
(см. § 10).
3. Обнаружение  -ионов. Если ионы аммония в анализируемом растворе отсутствуют, то обнаружение
-ионов. Если ионы аммония в анализируемом растворе отсутствуют, то обнаружение  можно провести и из общей пробы при помощи
можно провести и из общей пробы при помощи  (см. § 5). В присутствии
(см. § 5). В присутствии  выпадает желтый кристаллический осадок
выпадает желтый кристаллический осадок  .
.
В этом случае открытие  можно провести также при помощи
можно провести также при помощи  . В присутствии ионов калия выпадает белый кристаллический осадок
. В присутствии ионов калия выпадает белый кристаллический осадок  , нерастворимый в минеральных кислотах (см. § 5).
, нерастворимый в минеральных кислотах (см. § 5).
Если же аммоний присутствует, то предварительно удалите его из раствора кипячением с  или
или  , как указано выше. Затем фильтрат подкислите уксусной кислотой и проведите реакцию на
, как указано выше. Затем фильтрат подкислите уксусной кислотой и проведите реакцию на  при помощи
при помощи  (см. § 5).
(см. § 5).
В этом случае открытие  можно провести также при помощи
можно провести также при помощи  в среде 3 н. раствора
в среде 3 н. раствора  (см. § 5).
(см. § 5).
4. Обнаружение  . Если в анализируемом растворе отсутствуют
. Если в анализируемом растворе отсутствуют  , то можно в отдельной пробе анализируемого раствора обнаружить
, то можно в отдельной пробе анализируемого раствора обнаружить  при помощи
при помощи  или
или  (см. § 10).
(см. § 10).
Если присутствуют соли аммония и магния, то для открытия  с помощью
с помощью  предварительно удалите их из раствора кипячением с
предварительно удалите их из раствора кипячением с  или КОН, как указано выше. Затем фильтрат нейтрализуйте уксусной кислотой и при помощи раствора
или КОН, как указано выше. Затем фильтрат нейтрализуйте уксусной кислотой и при помощи раствора  проведите реакции обнаружения
проведите реакции обнаружения  .
.
 можно также открыть по образованию характерных кристаллов уранилацетата натрия
можно также открыть по образованию характерных кристаллов уранилацетата натрия  .
.
5. Дополнительные поверочные реакции. Для проверки полученных результатов анализа рекомендуется проделать дополнительные поверочные реакции:
1) для обнаружения  — реакцию окрашивания пламени (см. § 10);
— реакцию окрашивания пламени (см. § 10);
2) для обнаружения  — микрокристаллоскопическую реакцию с
— микрокристаллоскопическую реакцию с  и реакцию окрашивания пламени (см. § 5);
и реакцию окрашивания пламени (см. § 5);
3) для обнаружения  — капельную реакцию Н. А. Тананаева и реакцию с гипоиодитйм (см. § 11).
— капельную реакцию Н. А. Тананаева и реакцию с гипоиодитйм (см. § 11).
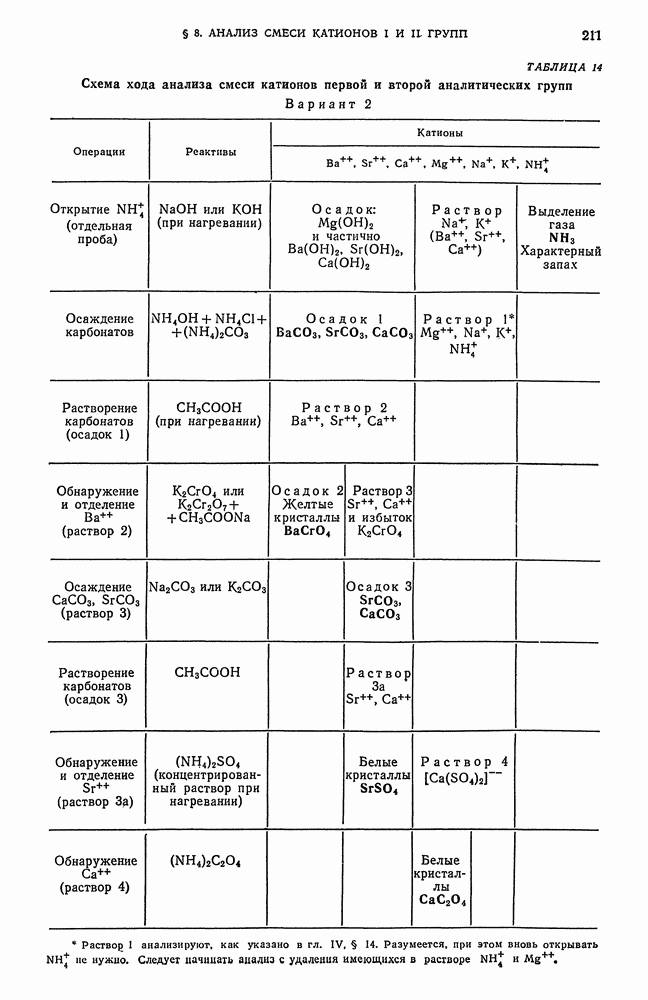
Вариант 2
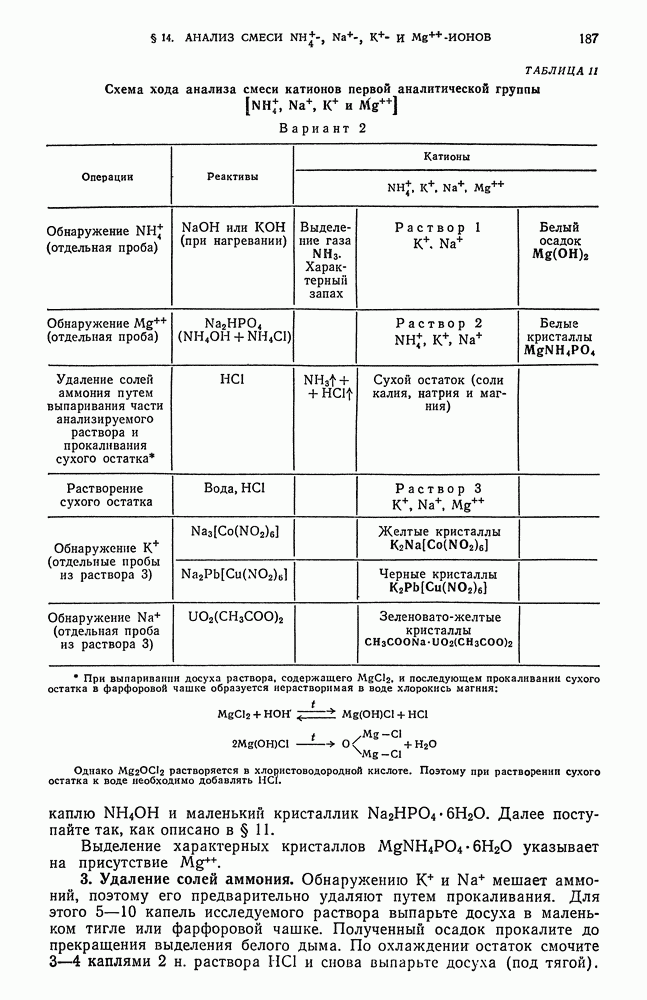
Схема этого варианта хода анализа смеси катионов I аналитической группы приведена в табл. 11.
1. Обнаружение  . Прилейте к 1—2 каплям анализируемого раствора, помещенного на часовое стекло или в пробирку, снабженную насадкой, 2—3 капли 2 н. раствора
. Прилейте к 1—2 каплям анализируемого раствора, помещенного на часовое стекло или в пробирку, снабженную насадкой, 2—3 капли 2 н. раствора  , чтобы раствор был щелочным. Далее поступайте так, как описано в § 3.
, чтобы раствор был щелочным. Далее поступайте так, как описано в § 3.
Выделение аммиака указывает на присутствие NHJ, а образование осадка  — на присутствие
— на присутствие  . Если
. Если  не выпадает, то это еще не означает, что
не выпадает, то это еще не означает, что  отсутствует.
отсутствует.
2. Обнаружение  . Поместите каплю анализируемого раствора на предметное стекло.
. Поместите каплю анализируемого раствора на предметное стекло.
ТАБЛИЦА 11. Схема хода анализа смеси катионов первой аналитической группы 
Вариант 2

Прибавьте к ней каплю раствора  ,
,

Однако  растворяется в хлористоводородной кислоте. Поэтому при растворении сухого остатка к воде необходимо добавлять
растворяется в хлористоводородной кислоте. Поэтому при растворении сухого остатка к воде необходимо добавлять  .
.
Прибавьте к ней каплю раствора  каплю
каплю  и маленький кристаллик
и маленький кристаллик  . Далее поступайте так, как описано в § 11.
. Далее поступайте так, как описано в § 11.
Выделение характерных кристаллов  указывает на присутствие
указывает на присутствие  .
.
3. Удаление солей аммония. Обнаружению  мешает аммоний, поэтому его предварительно удаляют путем прокаливания. Для этого 5—10 капель исследуемого раствора выпарьте досуха в маленьком тигле или фарфоровой чашке. Полученный осадок прокалите до прекращения выделения белого дыма. По охлаждении остаток смочите 3—4 каплями 2 н. раствора
мешает аммоний, поэтому его предварительно удаляют путем прокаливания. Для этого 5—10 капель исследуемого раствора выпарьте досуха в маленьком тигле или фарфоровой чашке. Полученный осадок прокалите до прекращения выделения белого дыма. По охлаждении остаток смочите 3—4 каплями 2 н. раствора  и снова выпарьте досуха (под тягой).
и снова выпарьте досуха (под тягой).
К остатку прибавьте каплю хлористоводородной кислоты, несколько капель воды и слегка нагрейте. Осадок отцентрифугируйте, а раствор проверьте на присутствие  . Удаление и разложение солей аммония может быть также проведено другими способами (см. § 4).
. Удаление и разложение солей аммония может быть также проведено другими способами (см. § 4).
4. Обнаружение  -ионов. Для обнаружения
-ионов. Для обнаружения  к одной капле свободного от солей аммония раствора на фарфоровой пластинке прибавьте 1—2 капли раствора
к одной капле свободного от солей аммония раствора на фарфоровой пластинке прибавьте 1—2 капли раствора  . Образующийся при этом желтый осадок указывает на присутствие
. Образующийся при этом желтый осадок указывает на присутствие  .
.
Для обнаружения  можно также применить микрокристаллоско-пическую реакцию с
можно также применить микрокристаллоско-пическую реакцию с  (см. § 5). Образование характерных черных кристаллов
(см. § 5). Образование характерных черных кристаллов  указывает на присутствие
указывает на присутствие  .
.
5. Обнаружение  -ионов. Выпарьте почти досуха на предметном стекле одну каплю свободного от солей аммония раствора, полученного, как указано при обнаружении ионов калия. Рядом с сухим остатком поместите каплю раствора уранилацетата. Далее поступайте так, как описано в § 10. Выделение характерных зеленовато-желтых кристаллоз указывает на присутствие
-ионов. Выпарьте почти досуха на предметном стекле одну каплю свободного от солей аммония раствора, полученного, как указано при обнаружении ионов калия. Рядом с сухим остатком поместите каплю раствора уранилацетата. Далее поступайте так, как описано в § 10. Выделение характерных зеленовато-желтых кристаллоз указывает на присутствие  .
.
6. Дополнительные поверочные реакции. Для проверки полученных результатов анализа рекомендуется проделать опыты на окрашивание бесцветного пламени горелки.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Анализ и синтез
- § 2. Предмет аналитической химии
- § 3. Развитие аналитической химии
- § 4. Качественный и количественный анализ
- ГЛАВА I. ПРИМЕНЕНИЕ ЗАКОНА ДЕЙСТВИЯ МАСС В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Влияние среды на состояние ионов в растворах
- § 2. Обратимые и необратимые аналитические реакции
- § 3. Направление аналитических реакций; правила обменного разложения
- § 4. Закон действия масс и следствие из него
- § 5. Границы применимости закона действия масс
- § 6. Сильные и слабые электролиты
- § 7. Активность
- § 8. Коэффициент активности и ионная сила
- Б. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ (В ГОМОГЕННЫХ СИСТЕМАХ)
- § 9. Гомогенные и гетерогенные системы
- § 10. Ионное произведение воды
- § 11. Ионы гидроксония
- § 12. Равновесие ионов в водных растворах; понятие о pH
- § 13. Равновесие в водных растворах слабых электролитов
- § 14. Влияние сильных кислот или сильных оснований на степень электролитической диссоциации слабых электролитов
- § 15. Приближенные формулы для расчета [H+] и [OH-] в водных растворах кислот и оснований
- В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
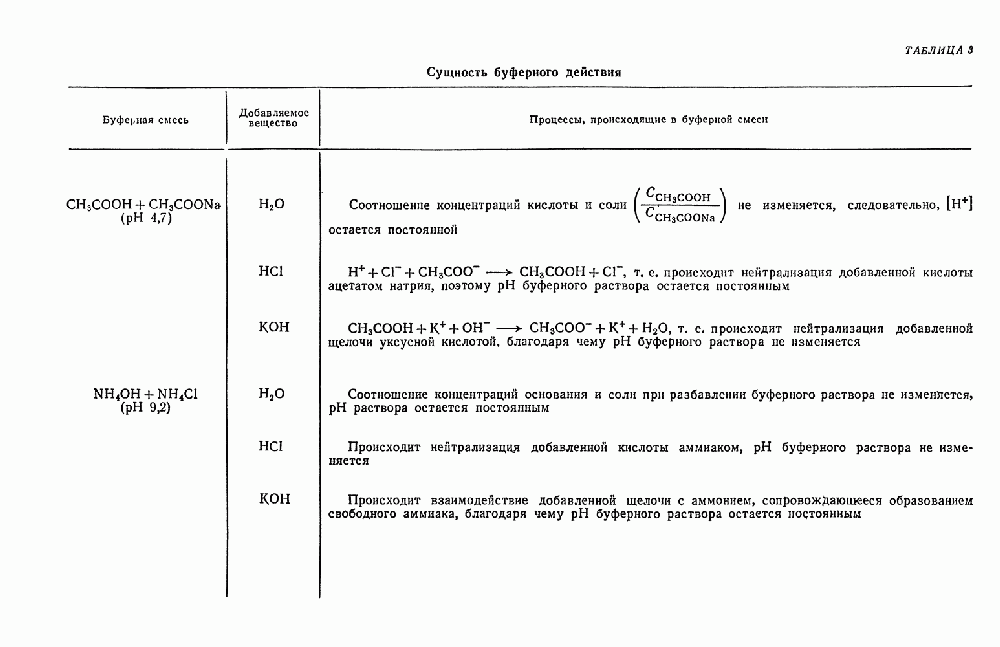
- § 16. Буферные растворы
- § 17. Применение буферных растворов в химическом анализе
- Г. РАВНОВЕСИЯ В РАСТВОРАХ ГИДРОЛИЗУЮЩИХСЯ СОЛЕЙ
- § 18. Теоретические основы гидролиза
- § 19. Механизм гидролитического расщепления
- § 20. Подавление и усиление гидролиза солей
- Д. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ТИПИЧНО АМФОТЕРНЫХ ЭЛЕКТРОЛИТОВ
- § 21. Поведение амфотерных гидроокисей в водных растворах
- § 22. Константы электролитической диссоциации амфотерных гидроокисей
- Е. РАВНОВЕСИЯ В СИСТЕМАХ: ОСАДОК-НАСЫЩЕННЫЙ РАСТВОР
- § 23. Осаждение как один из основных методов химического анализа
- § 24. Произведение растворимости
- § 25. Произведение активностей
- § 26. Вычисление растворимости электролитов в воде по величине произведения растворимости
- § 27. Влияние различных факторов на растворимость малорастворимых электролитов
- Ж. ОСНОВЫ ТЕОРИИ ОБРАЗОВАНИЯ И РАЗЛОЖЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИИ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 28. Характеристика комплексных соединений, имеющих значение в химическом анализе
- § 29. Квантовомеханические представления о строении комплексов
- § 30. Равновесия в растворах комплексных соединений
- § 31. Константы нестойкости комплексов
- § 32. Внутрикомплексные соединения
- § 33. Методы разложения и образования комплексов, применяемых в аналитической химии
- § 34. Применение метода комплексообразования в химическом анализе
- ГЛАВА II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Окисление—восстановление как один из основных методов химического анализа
- § 2. Направление реакций окисления—восстановления
- § 3. Окислительно-восстановительные потенциалы
- § 4. Зависимость между величинами окислительно-восстановительных потенциалов и условиями, в которых протекают реакции окисления—восстановления
- § 5. Вычисление окислительно-восстановительных потенциалов
- § 6. Вычисление окислительно-восстановительных потенциалов с учетом коэффициентов активности
- ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
- § 1. Обнаружение отдельных элементов
- § 2. Анализ мокрым и сухим путем
- § 3. Химические и физические методы качественного анализа
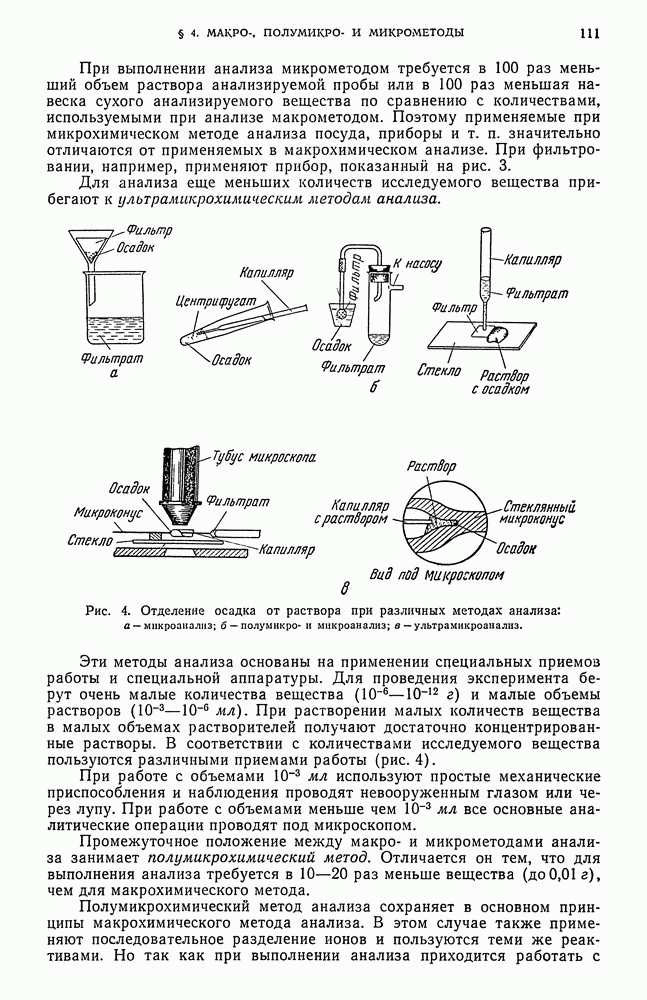
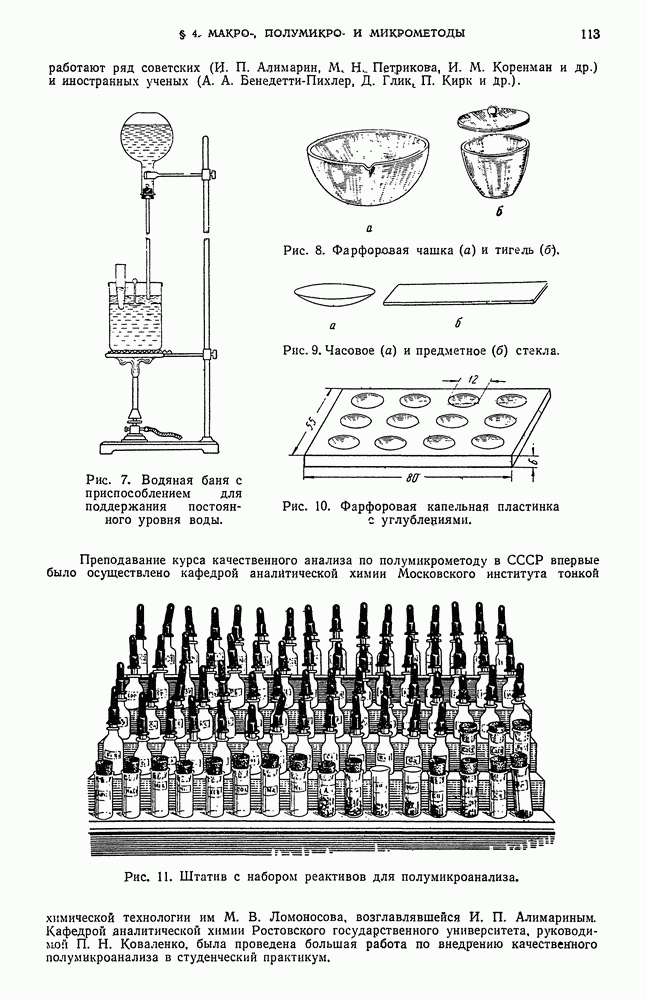
- § 4. Макро-, полумикро- и микрометоды
- § 5. Капельный анализ
- § 6. Микрокристаллоскопический анализ
- § 7. Метод растирания порошков
- § 8. Методы анализа, основанные на нагревании и сплавлении веществ
- § 9. Спектральный качественный анализ
- § 10. Хроматографический метод анализа
- § 11. Кинетические методы анализа
- Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
- § 12. Специфичность и чувствительность реакций
- § 13. Максимальная чувствительность аналитических реактивов
- § 14. Способы повышения чувствительности реакций
- § 15. Маскировка мешающих ионов
- § 16. Определение pH среды
- § 17. Регулирование pH среды в процессе аналитических определений
- В. РЕАКТИВЫ
- § 18. Понятие о химических реактивах
- § 19. Концентрация применяемых реактивов
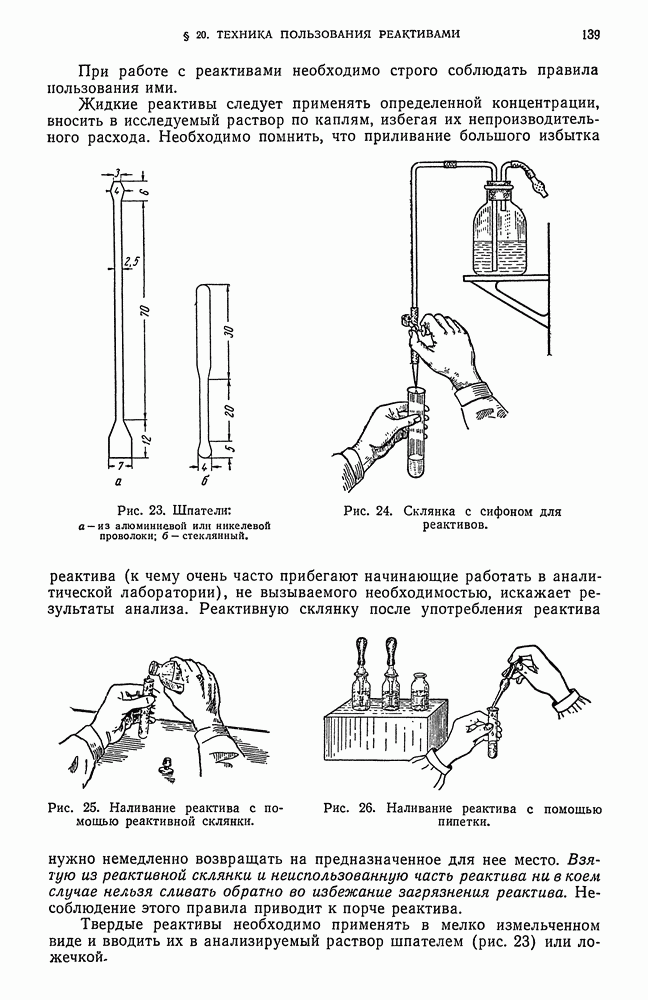
- § 20. Техника пользования реактивами
- Г. ПОСУДА И ПРИБОРЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕННОМ АНАЛИЗЕ
- § 21. Химическая посуда
- § 22. Приборы
- Д. АНАЛИТИЧЕСКИЕ ГРУППЫ
- § 23. Дробный и систематический анализ
- § 24. Аналитическая классификация катионов
- § 25. Сводные таблицы действия реактивов на катионы и анионы
- Е. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ ИОНОВ
- § 26. Значение периодического закона в аналитической химии
- § 27. Периодическая система элементов Д. И. Менделеева как классификация атомов по их строению
- § 28. Зависимость некоторых химических свойств элементов от положения их в периодической системе Д. И. Менделеева
- § 29. Растворимость химических соединений в связи с положением элементов в периодической системе Д. И. Менделеева
- § 30. Открытие новых аналитических реакций
- § 31. Аналитические группы и периодическая система элементов Д. И. Менделеева
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ КАТИОНОВ И АНАЛИЗ СМЕСЕЙ КАТИОНОВ
- § 1. Характеристика первой аналитической группы катионов
- § 2. Общие реакции катионов первой аналитической группы
- РЕАКЦИИ КАТИОНОВ 1-й ПОДГРУППЫ
- § 3. Обнаружение NН-ионов
- § 4. Методы разложения и удаления солей аммония
- § 5. Обнаружение K-ионов
- § 6. Обнаружение Rb-ионов
- § 7. Обнаружение Cs-ионов
- § 8. Анализ смеси катионов первой подгруппы
- РЕАКЦИИ КАТИОНОВ 2-й ПОДГРУППЫ
- § 9. Обнаружение Li-ионов
- § 10. Обнаружение Na-ионов
- § 11. Обнаружение Mg-ионов
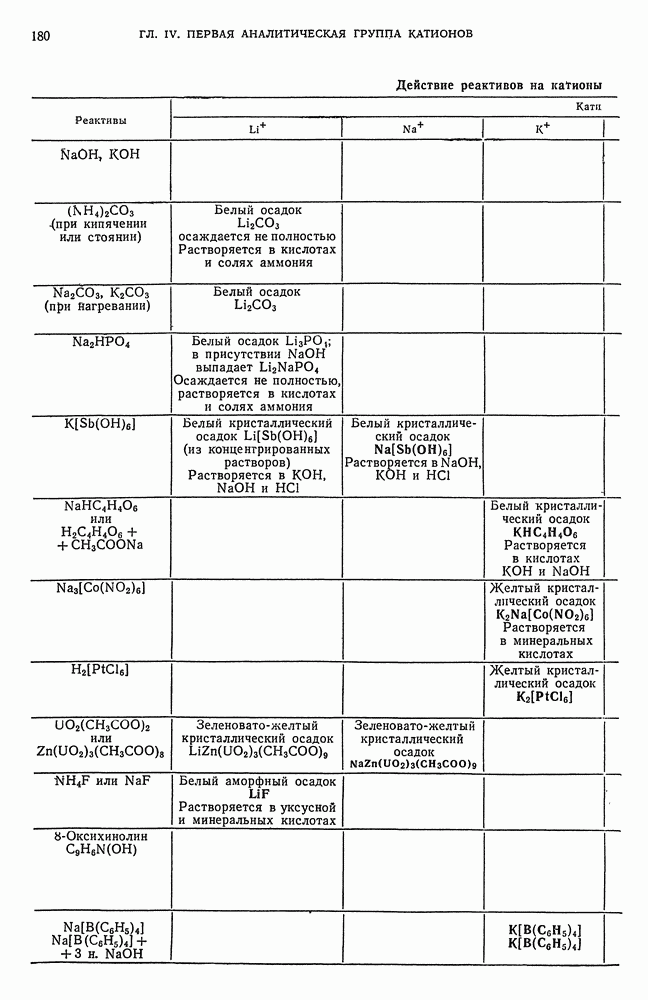
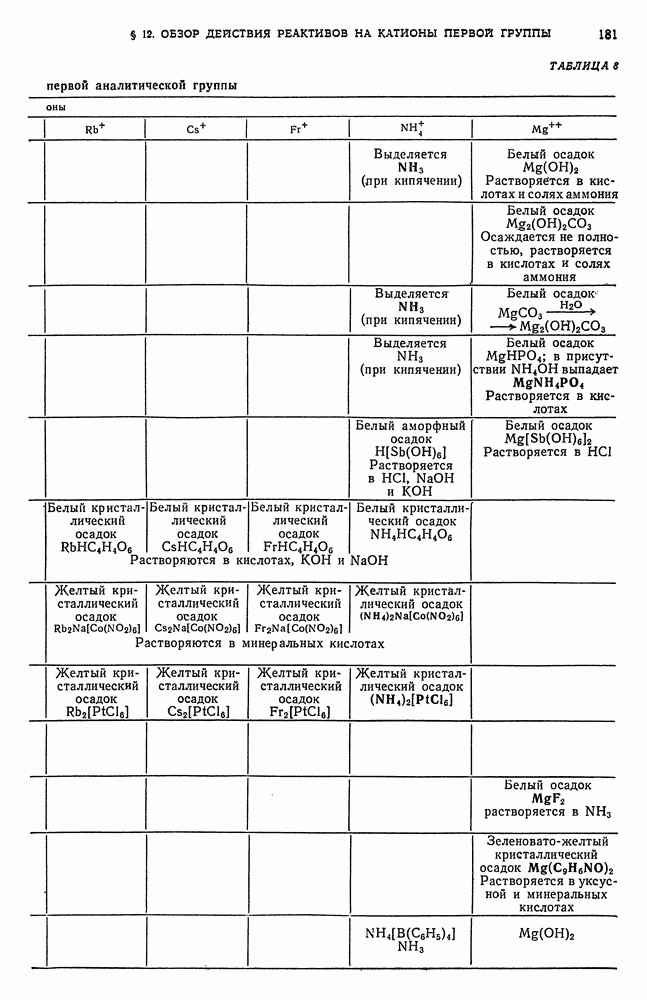
- § 12. Обзор действия реактивов на катионы первой аналитической группы
- § 13. Анализ смеси катионов второй подгруппы
- § 14. Анализ смеси ионов
- § 15. Анализ смеси ионов
- ГЛАВА V. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика второй аналитической группы катионов
- § 2. Общие реакции катионов второй аналитической группы
- § 3. Обнаружение Ca-ионов
- § 4. Обнаружение Sr-ионов
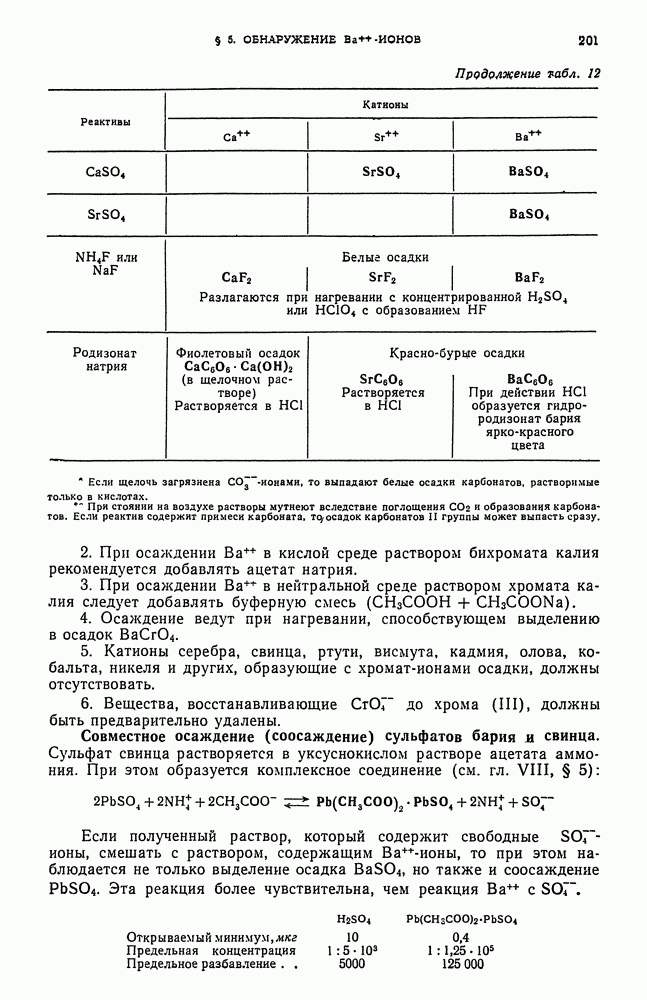
- § 5. Обнаружение Ba-ионов
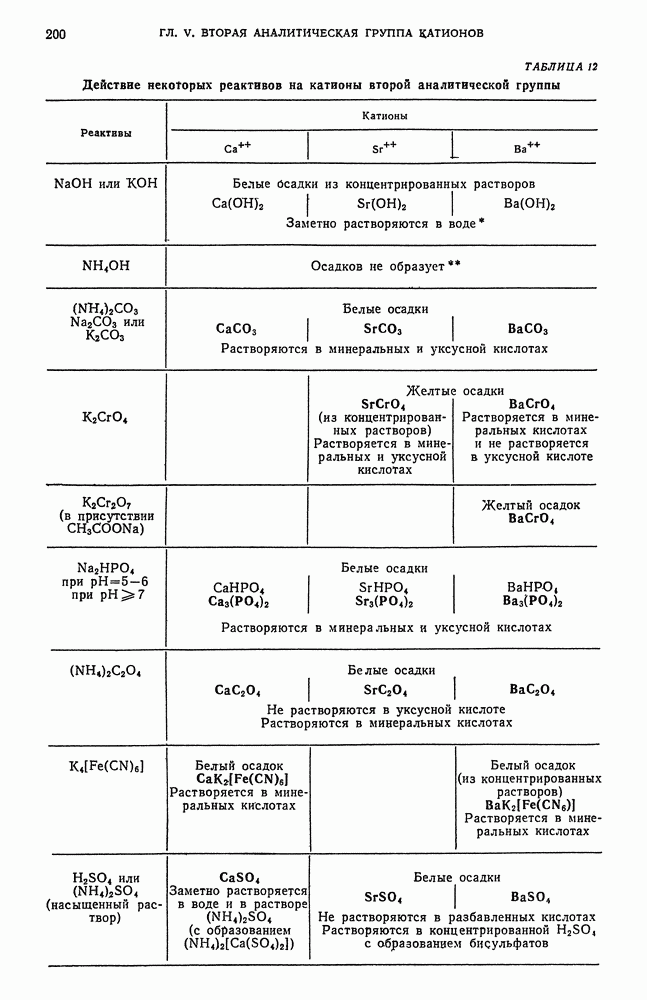
- § 6. Обзор действия реактивов на катионы второй аналитической группы
- § 7. Основы теории осаждения катионов второй аналитической группы групповым реактивом—карбонатом аммония
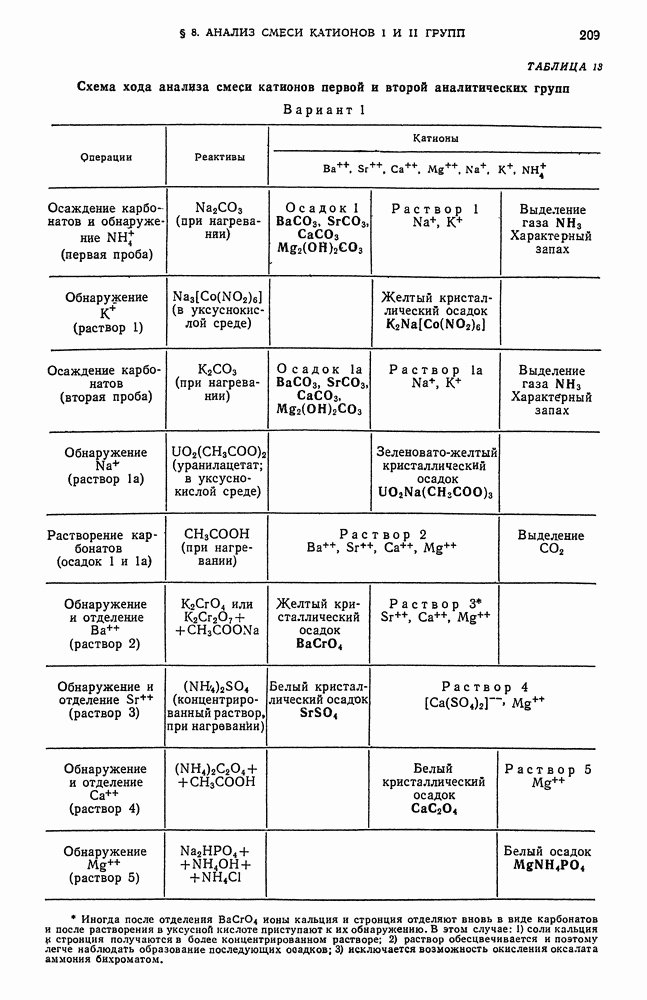
- § 8. Систематический ход анализа смеси катионов первой и второй аналитических групп
- § 9. Систематический ход анализа смеси катионов первой и второй аналитических групп в присутствии ионов
- § 10. Теоретические основы перевода сульфатов катионов второй аналитической группы в карбонаты
- ГЛАВА VI. ТРЕТЬЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика третьей аналитической группы катионов
- § 2. Общие реакции катионов третьей аналитической группы
- § 3. Обнаружение Be-ионов
- § 4. Обнаружение Al-ионов
- § 5. Обнаружение ионов титана (IV)
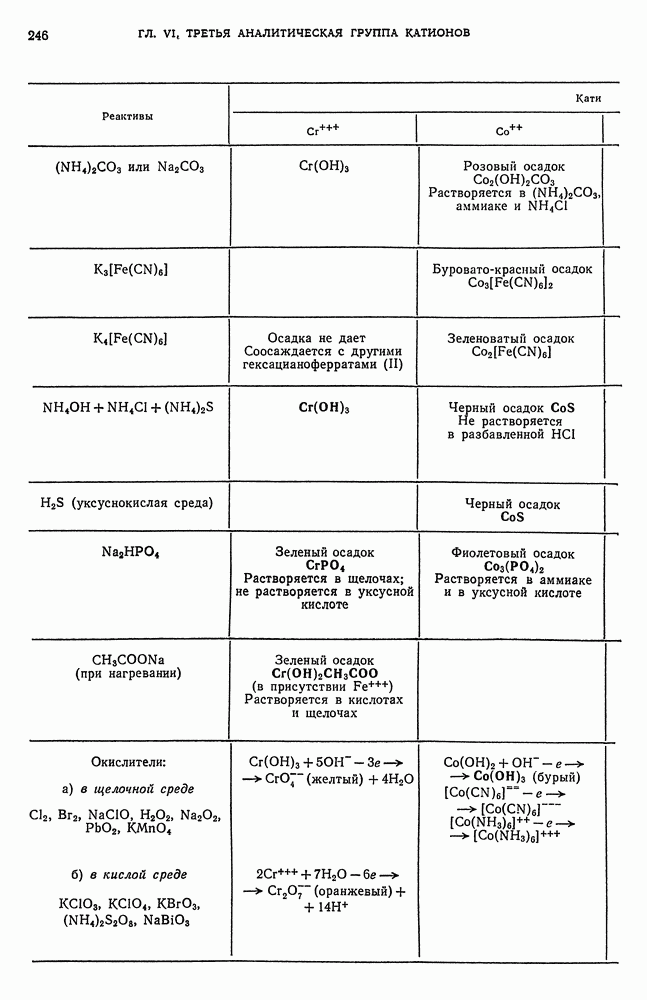
- § 6. Обнаружение Cr-ионов
- § 7. Обнаружение Mn-ионов
- § 8. Обнаружение Fe-ионов
- § 9. Обнаружение Fe-ионов
- § 10. Обнаружение Co-ионов
- § 13. Обнаружение ионов циркония (IV)
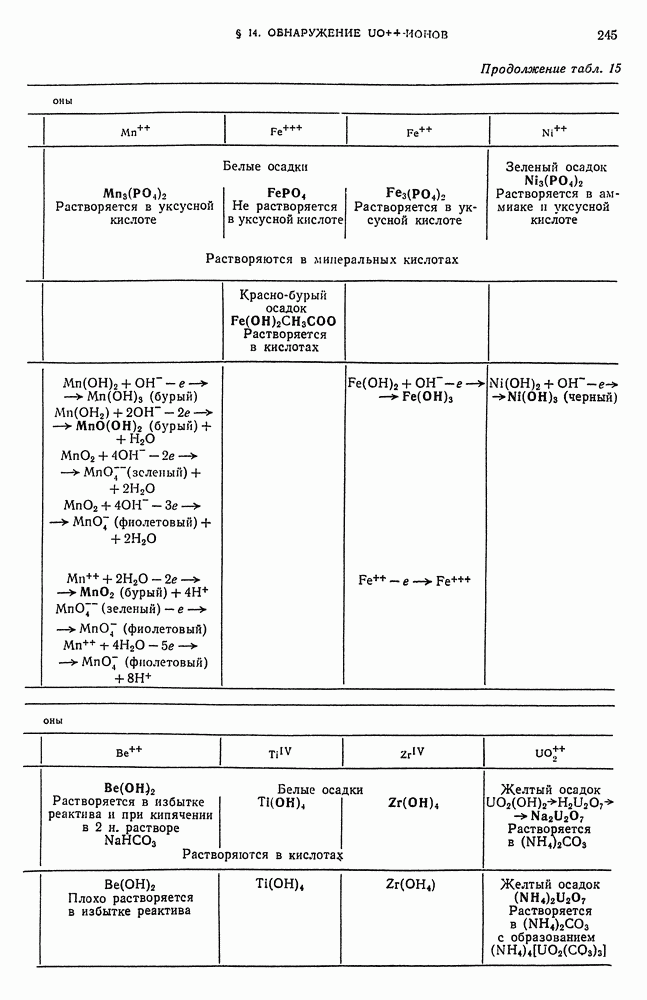
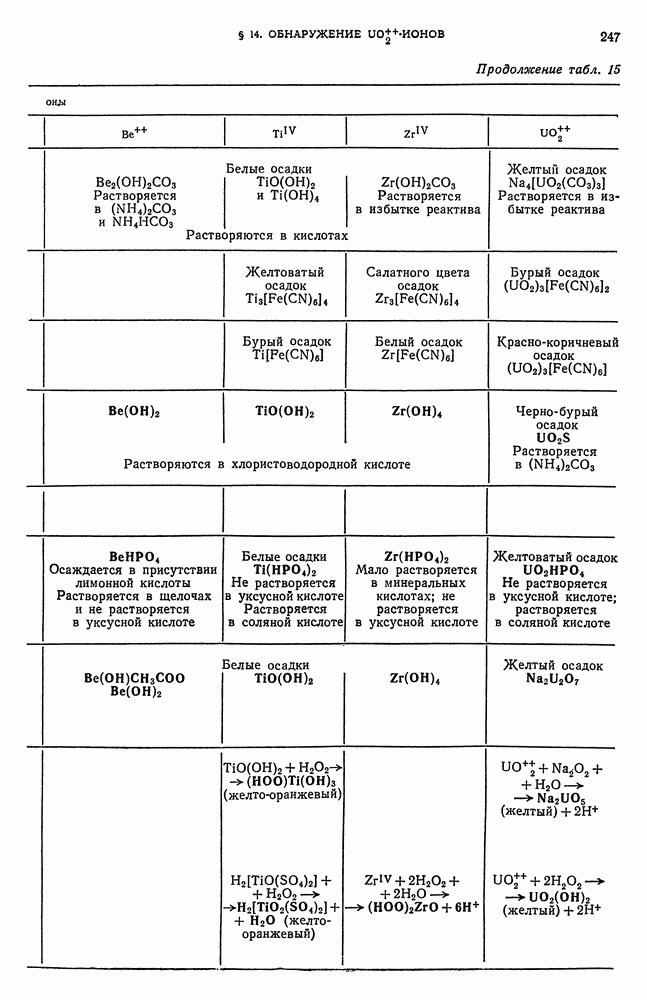
- § 14. Обнаружение UO-ионов
- § 15. Обзор действия реактивов на катионы третьей аналитической группы
- § 16. Использование коллоидных систем в химическом анализе
- § 17. Основы теории осаждения катионов третьей аналитической группы групповым реактивом — сульфидом аммония
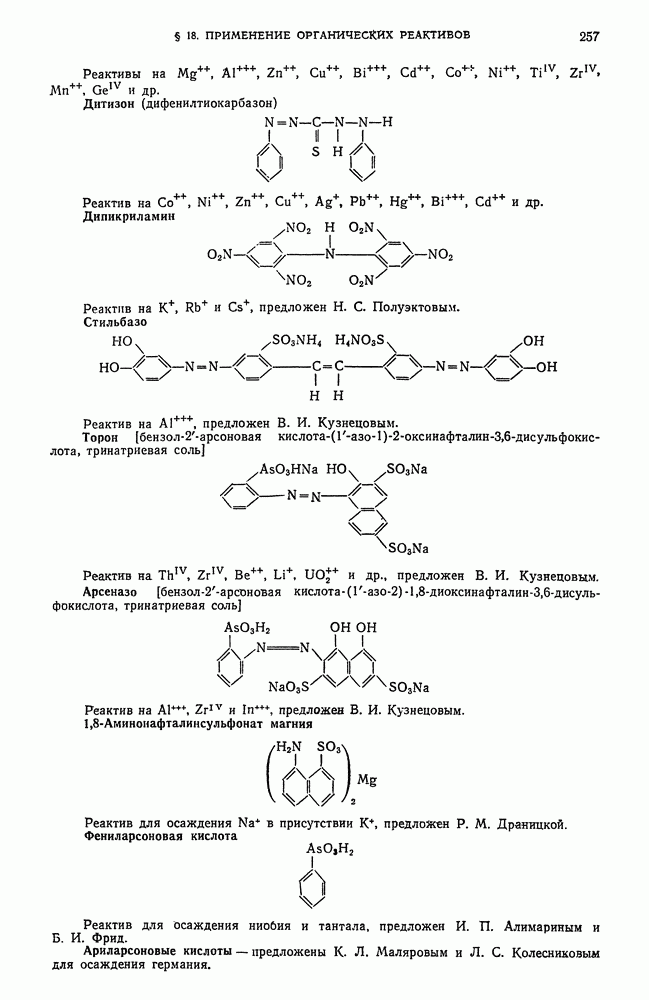
- § 18. Теоретические основы применения органических реактивов в качественном анализе неорганических веществ
- § 19. Методы разделения некоторых катионов третьей аналитической группы
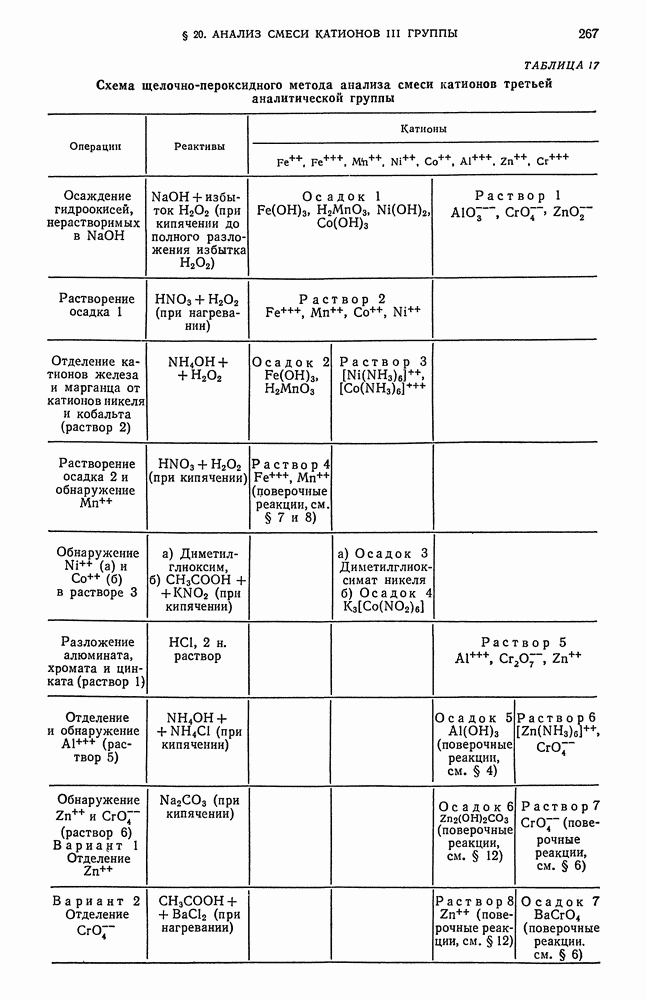
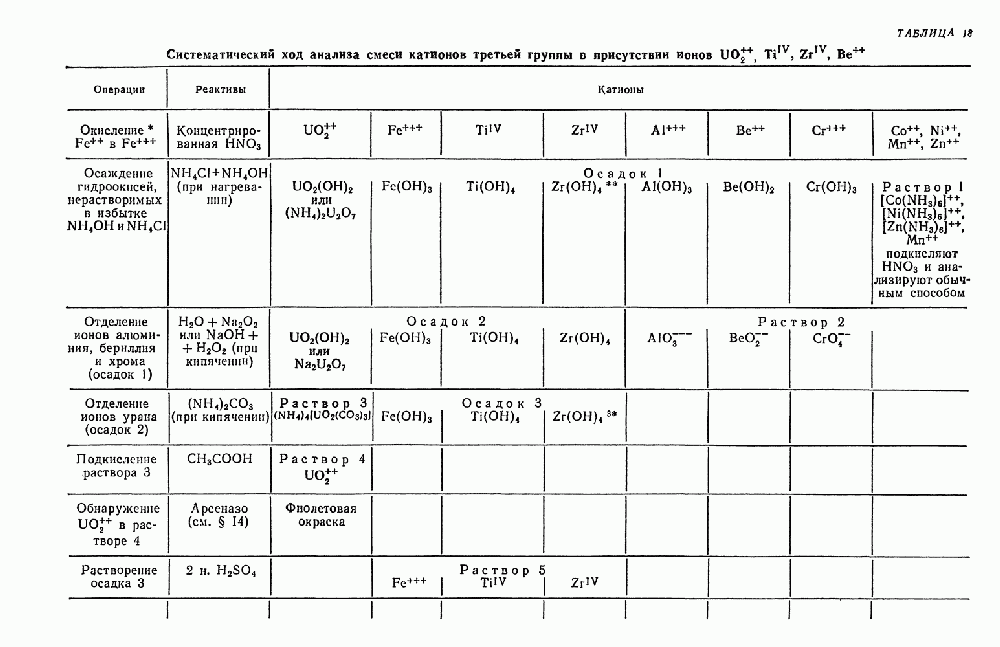
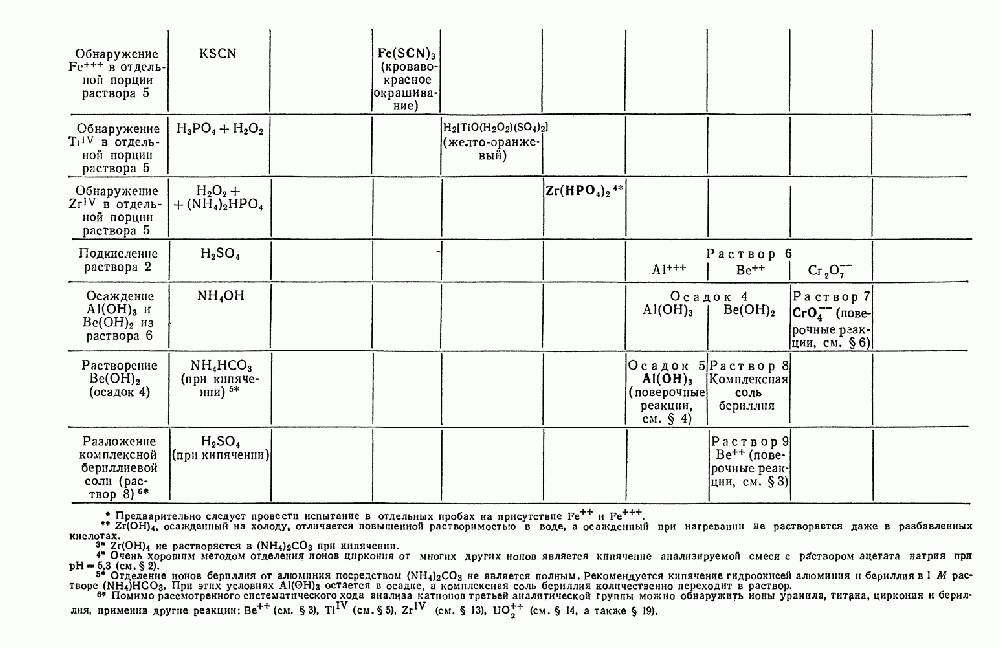
- § 20. Систематический ход анализа смеси катионов третьей аналитической группы
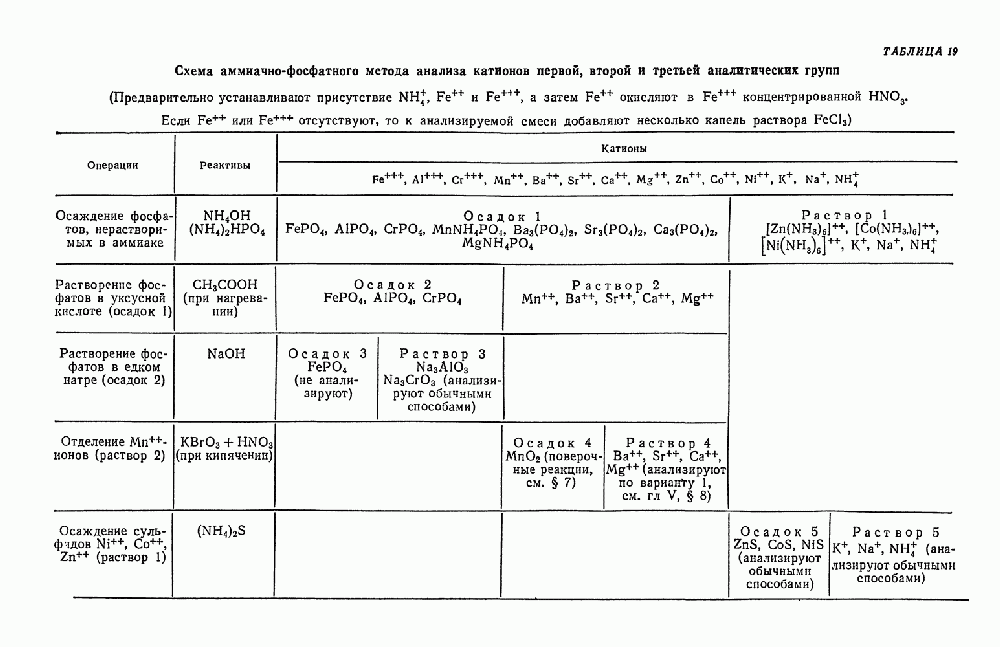
- § 21. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп
- § 22. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп в присутствии PO-ионов
- ГЛАВА VII. ЧЕТВЕРТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика четвертой аналитической группы катионов
- § 2. Общие реакции катионов четвертой аналитической группы
- РЕАКЦИИ КАТИОНОВ ПЕРВОЙ ПОДГРУППЫ (ПОДГРУППЫ МЕДИ)
- § 3. Обнаружение Hg-ионов
- § 4. Обнаружение Cu-ионов
- § 5. Обнаружение Cd-ионов
- § 6. Обнаружение Bi-ионов
- РЕАКЦИИ КАТИОНОВ ВТОРОЙ ПОДГРУППЫ (ПОДГРУППЫ МЫШЬЯКА)
- § 7. Обнаружение ионов мышьяка (III)
- § 8. Обнаружение ионов мышьяка (V)
- § 9. Общие реакции обнаружения
- § 10. Обнаружение ионов сурьмы (III)
- § 11. Обнаружение ионов сурьмы (V)
- § 12. Общие реакции обнаружения Sb
- § 13. Обнаружение ионов олова (II)
- § 14. Обнаружение ионов олова (IV)
- § 15. Общие реакции обнаружения ионов олова (II) и олова (IV)
- § 16. Отделение ионов олова от других ирнов четвертой аналитической группы
- § 17. Обнаружение ионов германия (IV)
- § 18. Отделение ионов германия от других ионов четвертой аналитической группы
- § 19. Обзор действия реактивов на катионы четвертой аналитической группы
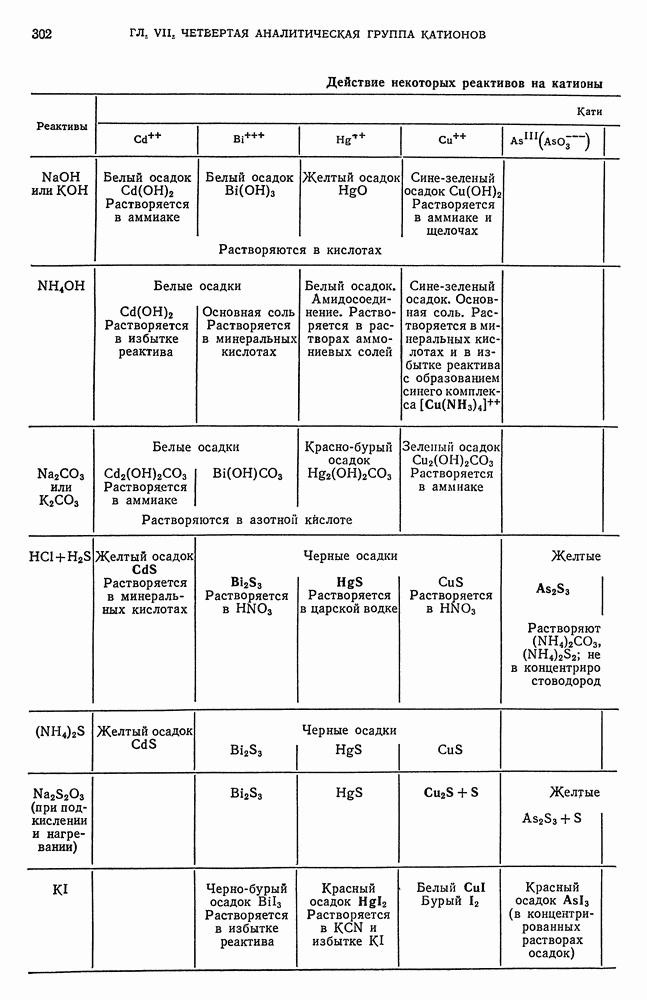
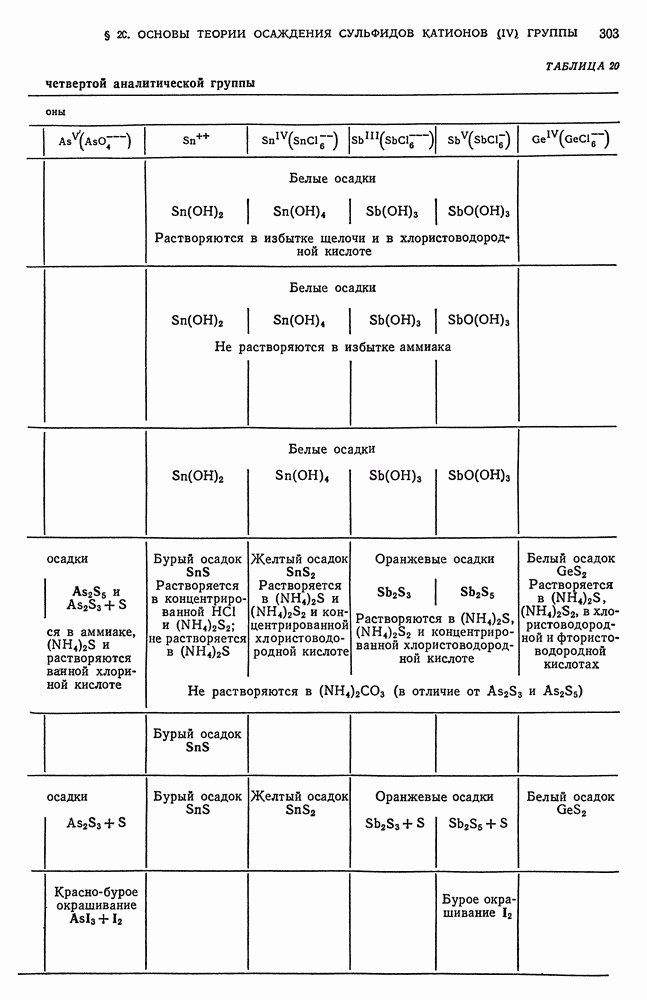
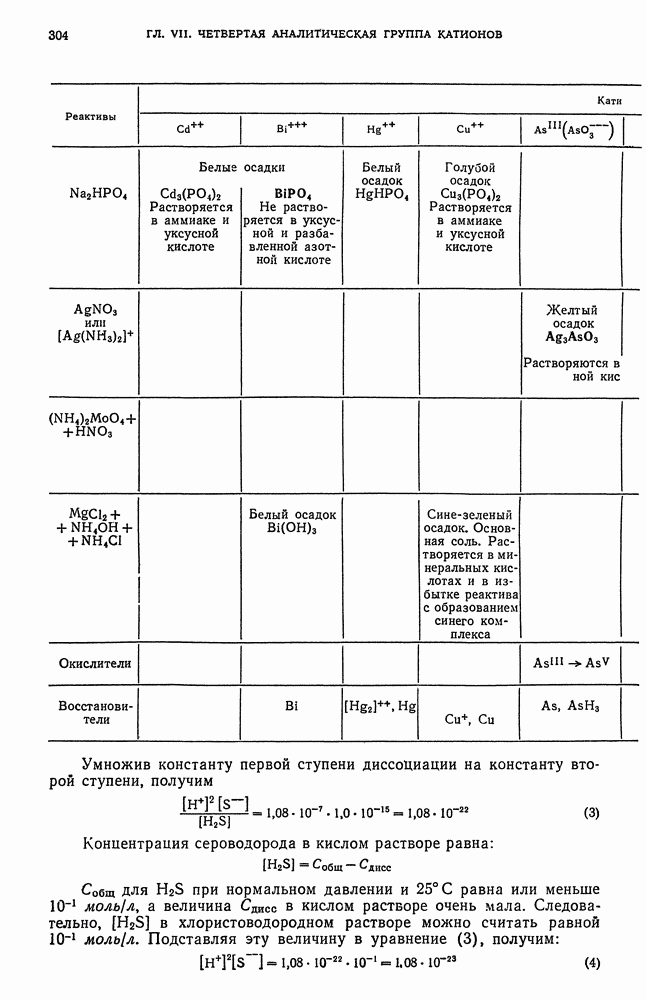
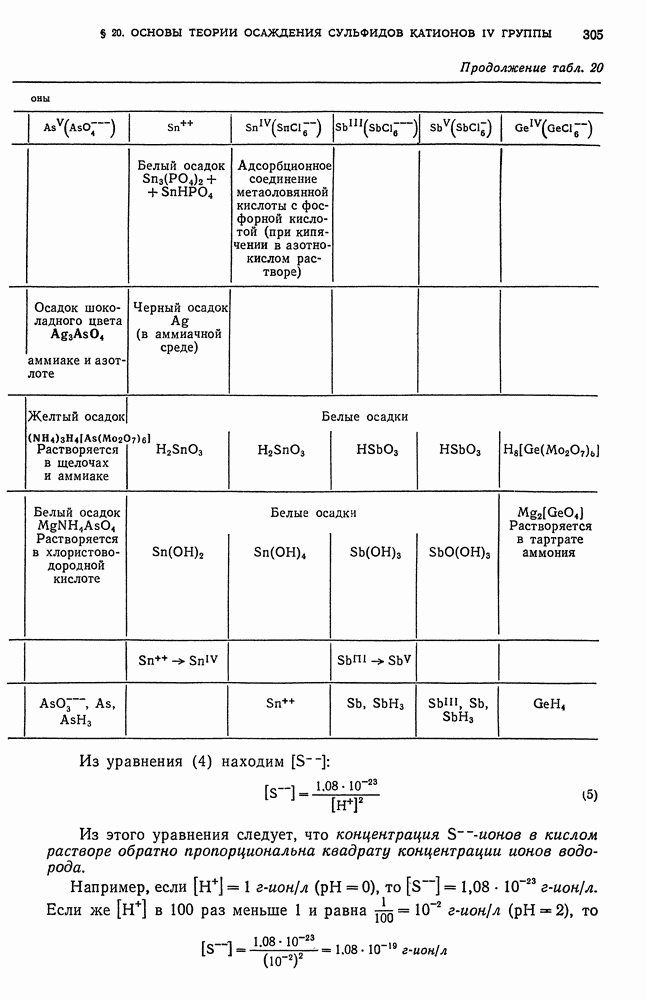
- § 20. Основы теории осаждения сульфидов катионов четвертой аналитической группы групповым реактивом — сероводородом
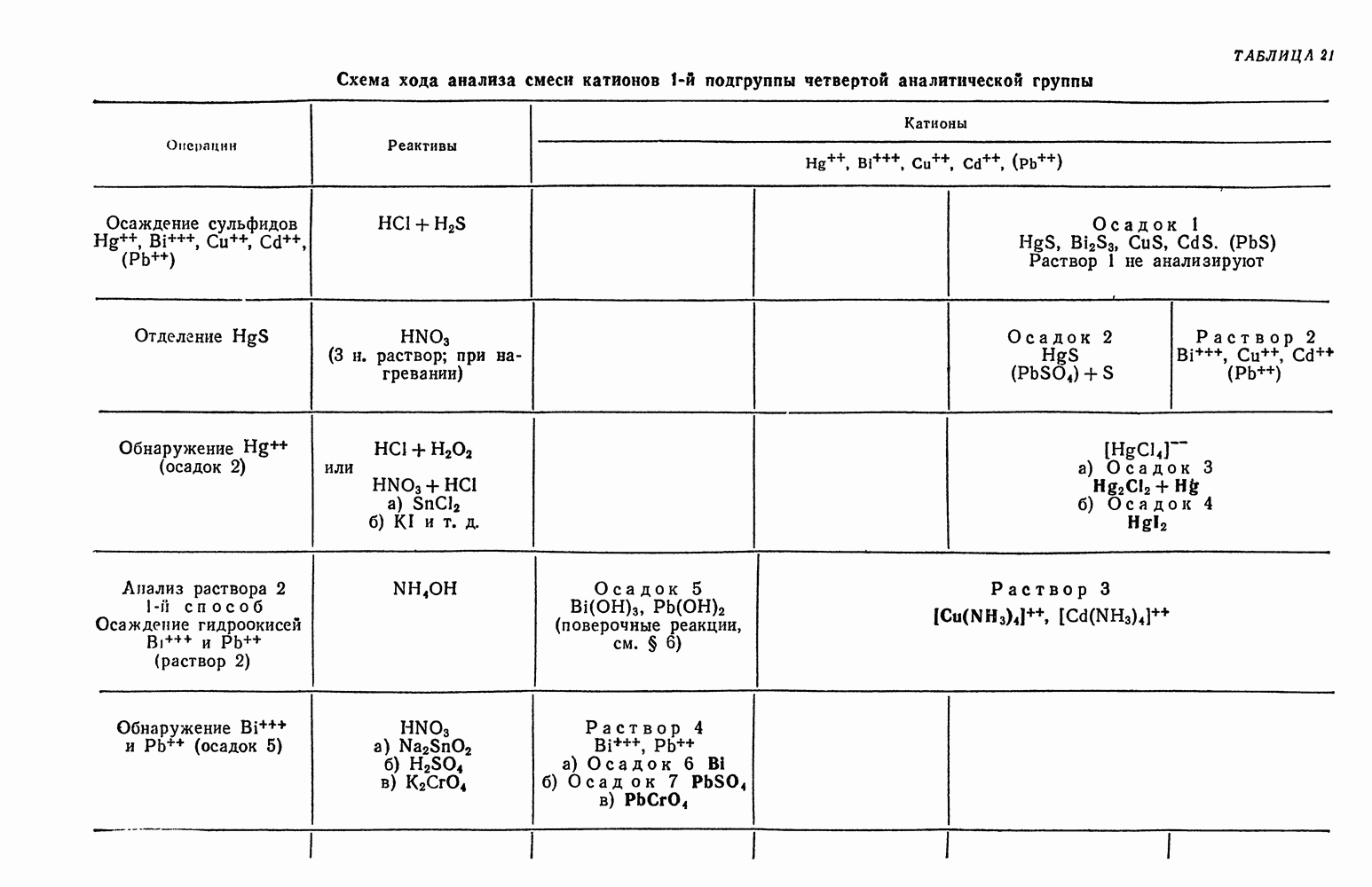
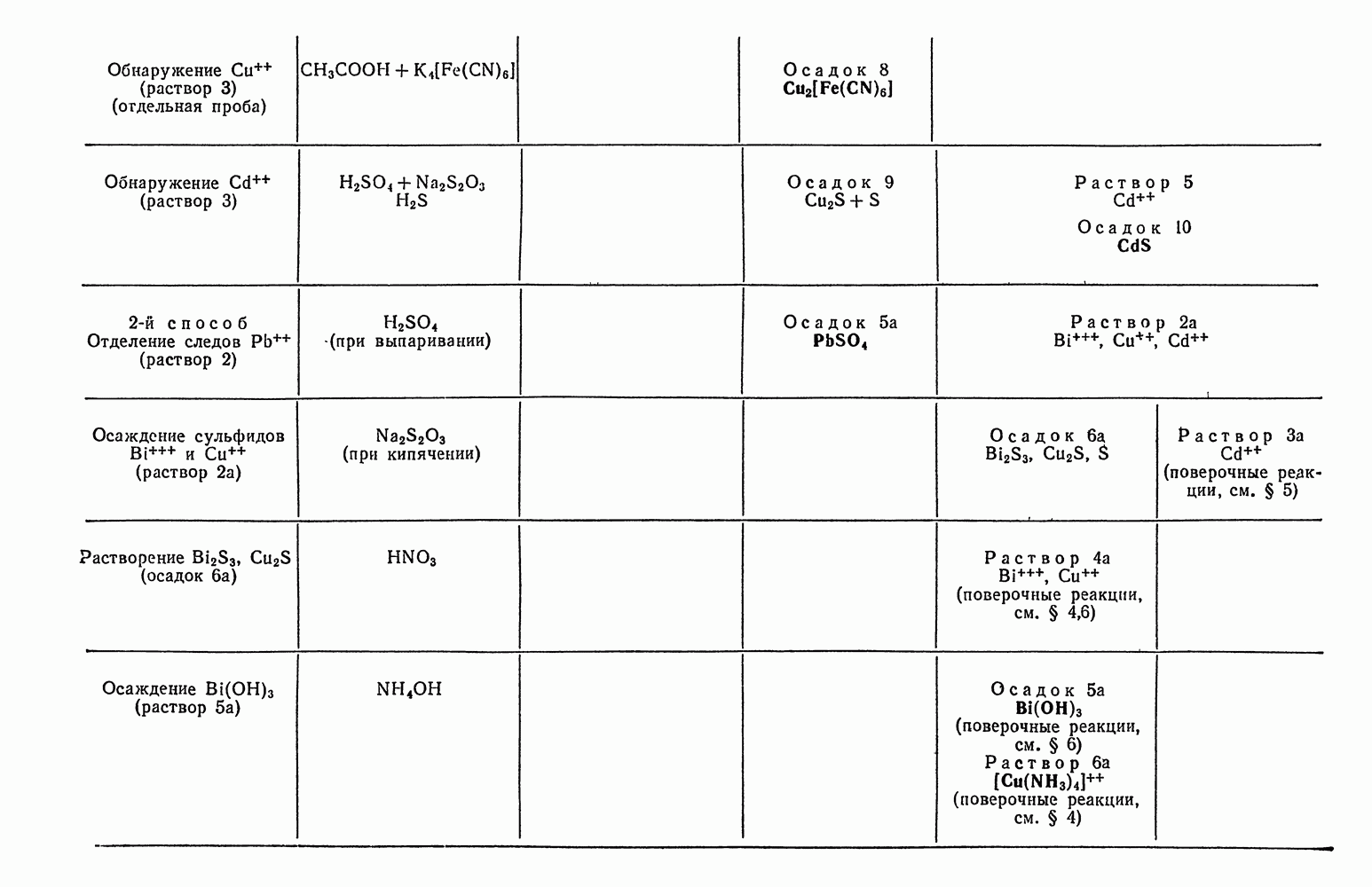
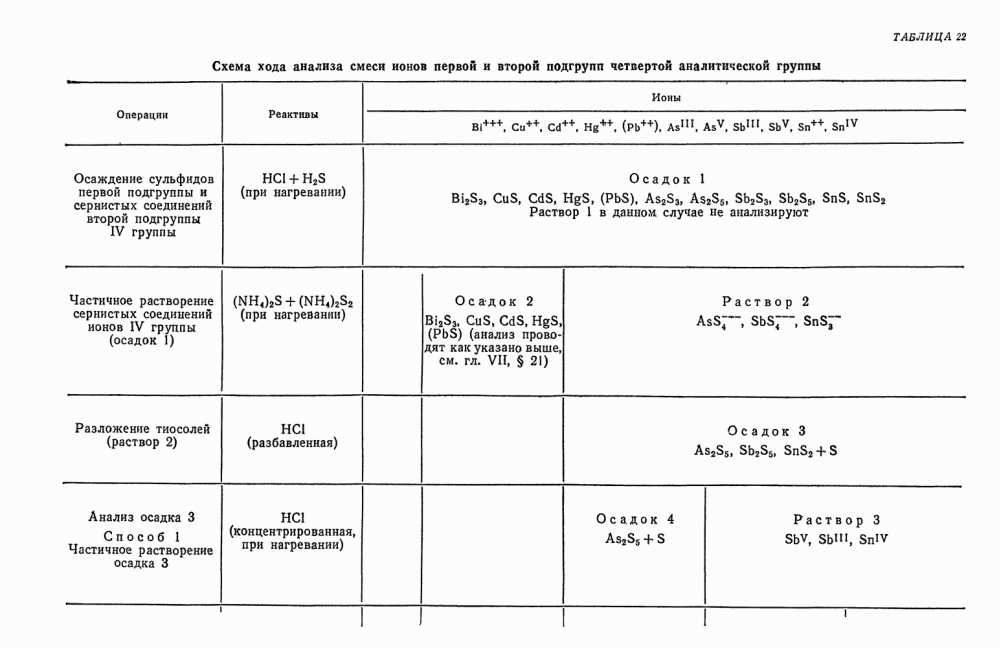
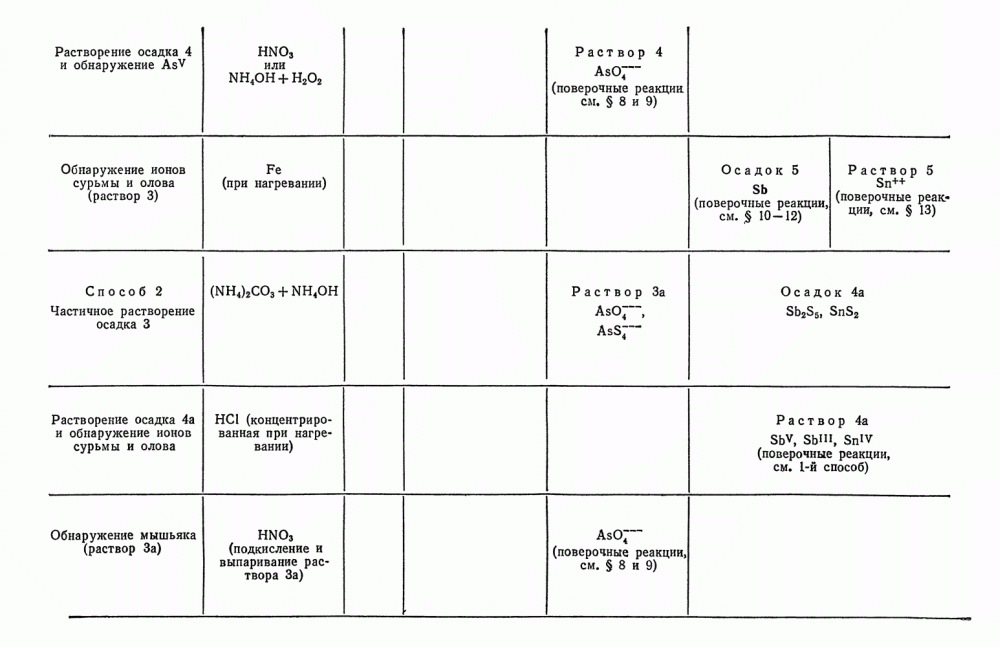
- § 21. Систематический ход анализа смеси катионов четвертой аналитической группы
- ГЛАВА VIII. ПЯТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ (ГРУППА СЕРЕБРА)
- § 1. Характеристика пятой аналитической группы катионов
- § 2. Общие реакции катионов пятой аналитической группы
- § 3. Обнаружение Ag-ионов
- § 4. Обнаружение [Hg]-ионов
- § 5. Обнаружение Pb-ионов
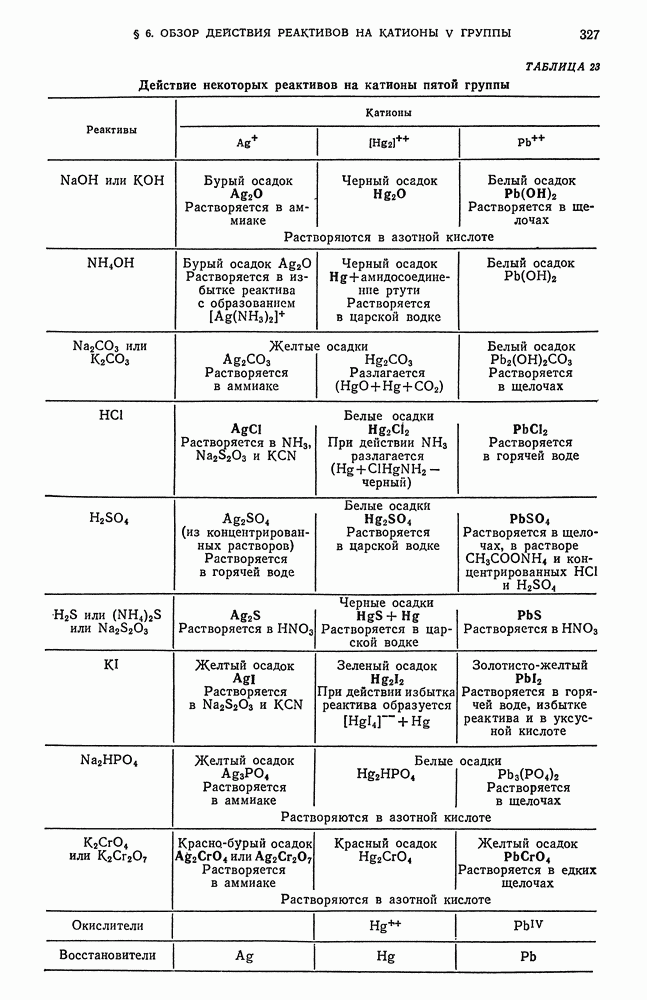
- § 6. Обзор действия реактивов на катионы пятой аналитической группы
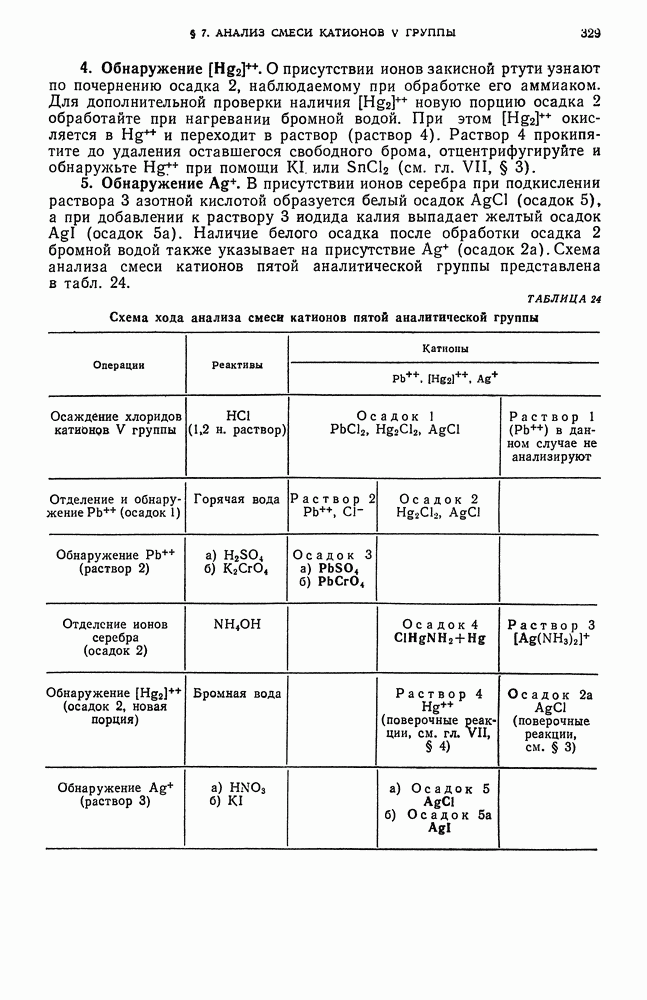
- § 7. Систематический ход анализа смеси катионов пятой аналитической группы
- ГЛАВА IX. АНАЛИЗ СМЕСИ ИОНОВ ВСЕХ ПЯТИ АНАЛИТИЧЕСКИХ ГРУПП
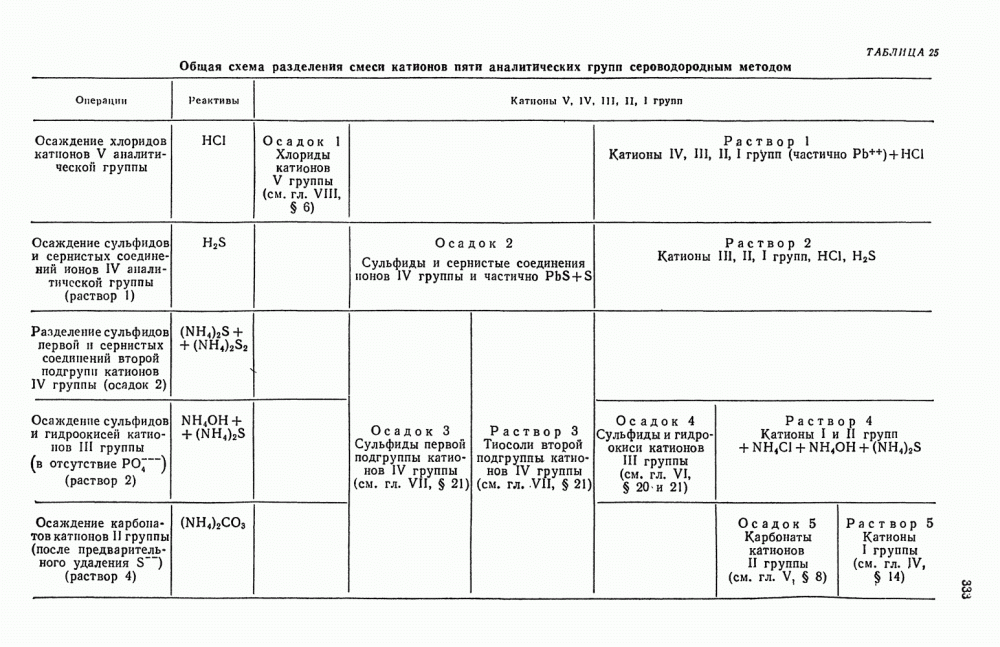
- § 1. Сероводородный метод анализа
- § 2. Недостатки сероводородного метода анализа
- § 3. Ошибки, возникающие при анализе смеси ионов пяти аналитических групп
- § 4. Бессероводородные методы анализа
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ АНИОНОВ И АНАЛИЗ СМЕСЕЙ АНИОНОВ
- § 1. Аналитическая классификация анионов
- § 2. Групповые реактивы на анионы
- § 3. Классификация методов анализа анионов
- ГЛАВА XI. ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика первой группы анионов
- § 2. Реакции анионов первой группы
- § 3. Обнаружение CI-ионов
- § 4. Обнаружение Br-ионов
- § 5. Обнаружение I-ионов
- § 6. Обнаружение CN-ионов
- § 7. Обнаружение SCN-ионов
- § 8. Обнаружение [Fe(CN)]-ионов
- § 9. Обнаружение Fe(CN)-ионов
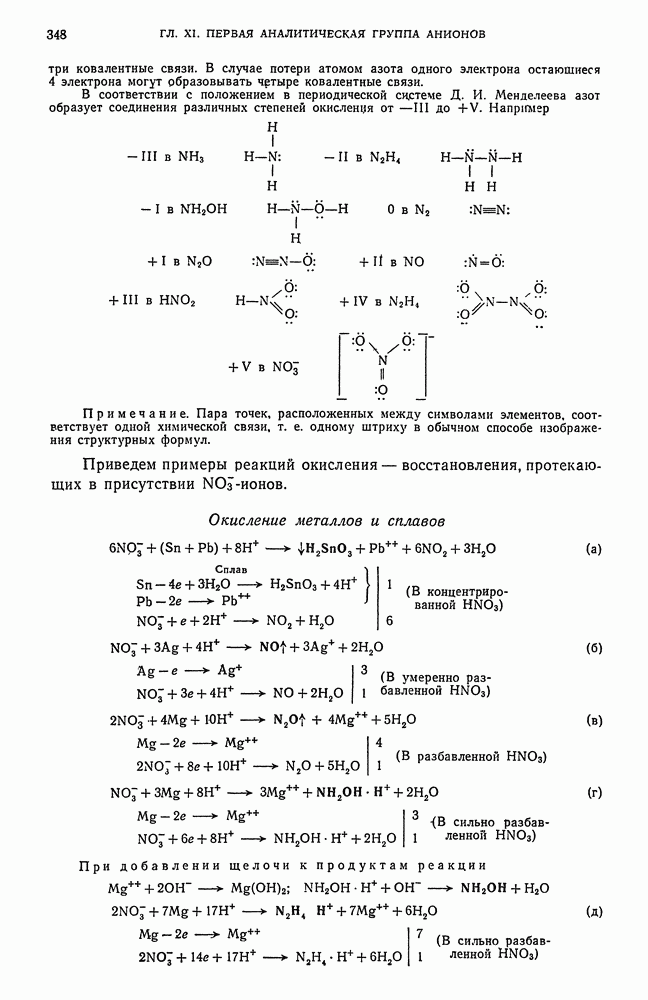
- § 10. Обнаружение NO-ионов
- § 11. Обнаружение NO2-ионов
- § 12. Обнаружение S-ионов
- § 13. Обнаружение CH3COOO-ионов
- § 14. Обнаружение BrO3-ионов
- § 15. Обнаружение ClO3-ионов
- § 16. Обнаружение ClO4-ионов
- § 17. Обзор действия реактивов на анионы первой группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 18. Анализ смеси Cl, Br и I-ионов
- § 19. Анализ смеси Cl, Br, I и SCN-ионов
- § 20. Анализ смеси Cl, ClO3 и ClO4-ионов
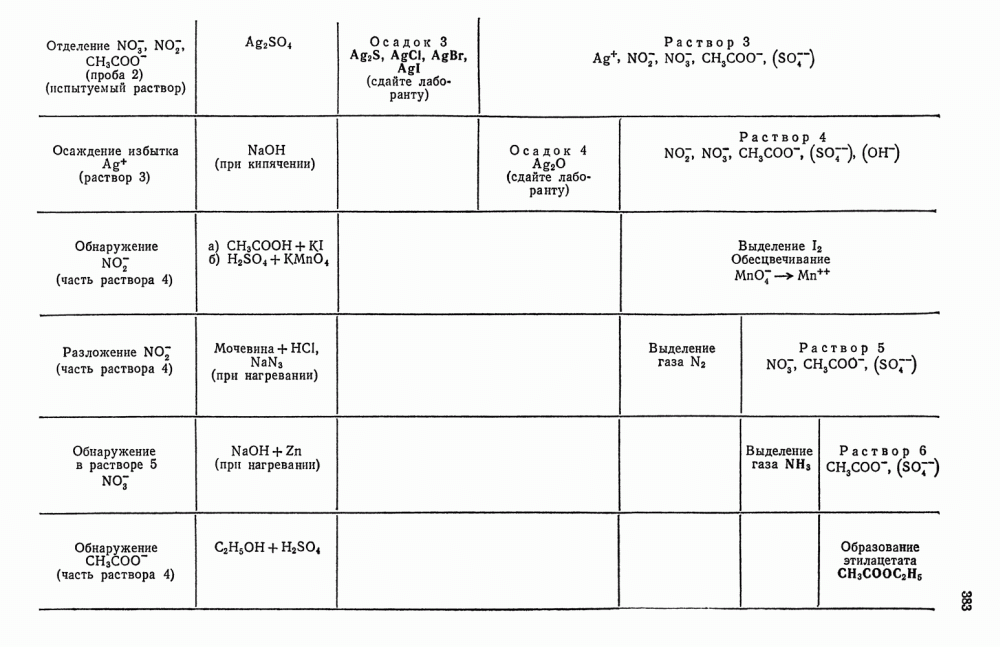
- § 21. Анализ смеси NO2 и NO3-ионов
- § 22. Анализ смеси анионов первой группы
- ГЛАВА XII. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика второй группы анионов
- § 2. Общие реакции анионов второй группы
- § 3. Обнаружение SO3-ионов
- § 4. Обнаружение S2O3-ионов
- § 5. Обнаружение S2O3 в присутствии SO3-ионов
- § 6. Обнаружение SO4-ионов
- § 7. Обнаружение CO3-ионов
- § 8. Обнаружение CO3-ионов в присутствии SO3 и S2O3-ионов
- § 9. Обнаружение PO4-ионов
- § 10. Обнаружение CrO4-ионов
- § 11. Обнаружение AsO3-ионов
- § 12. Обнаружение AsO4-ионов
- § 13. Обнаружение BO2 и BO3-ионов
- § 14. Обнаружение SiO3-ионов
- § 15. Обнаружение F-ионов
- § 16. Обнаружение C2O4-ионов
- § 17. Обнаружение VO3-ионов
- § 18. Обнаружение MoO4-ионов
- § 19. Обнаружение WO4-ионов
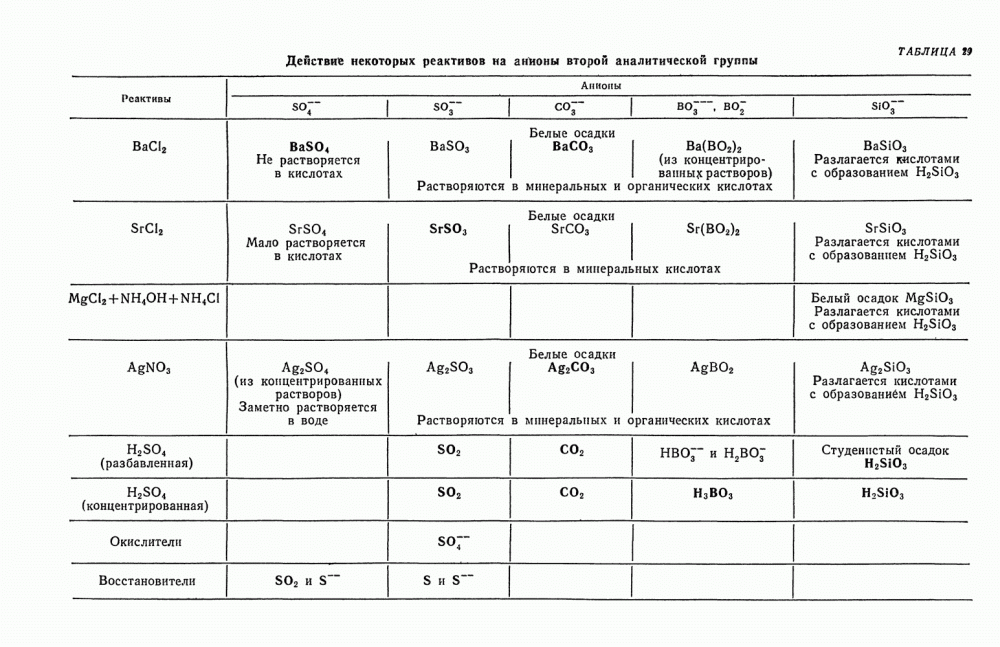
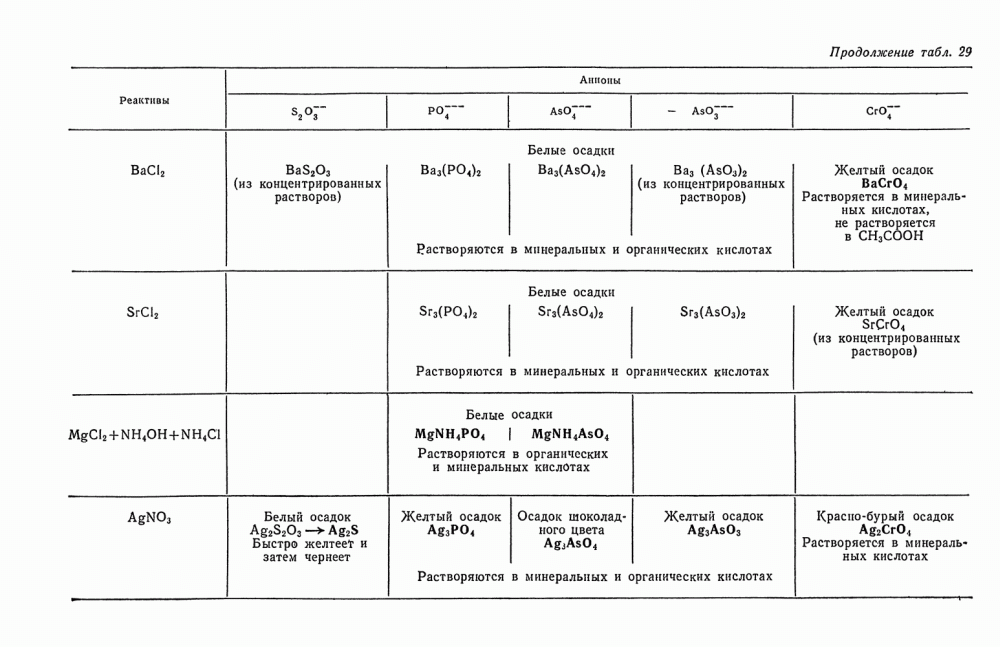
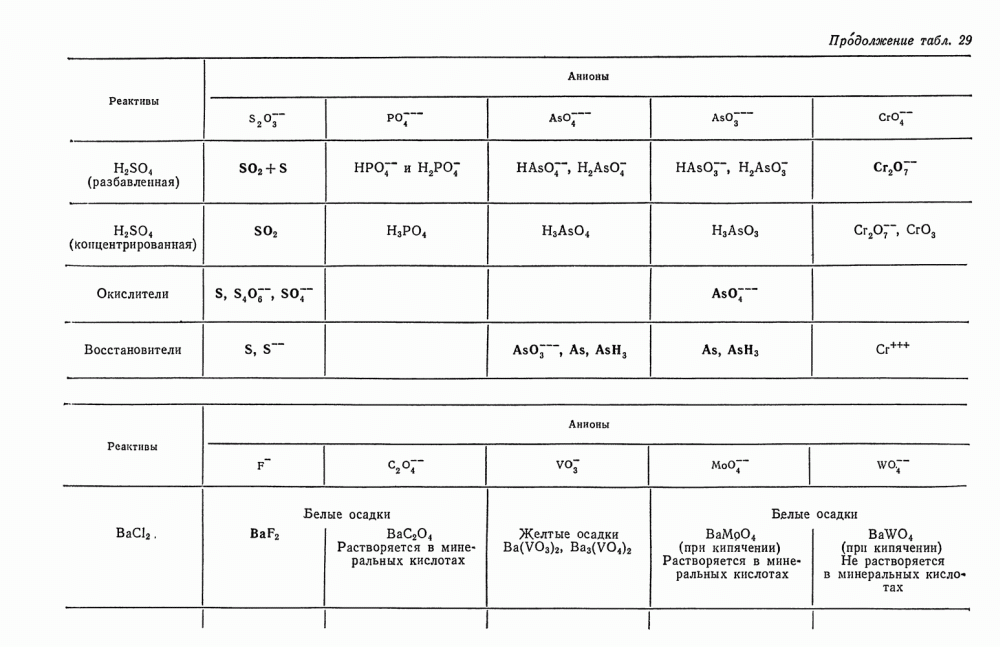
- § 20. Обзор действия реактивов на анионы второй группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
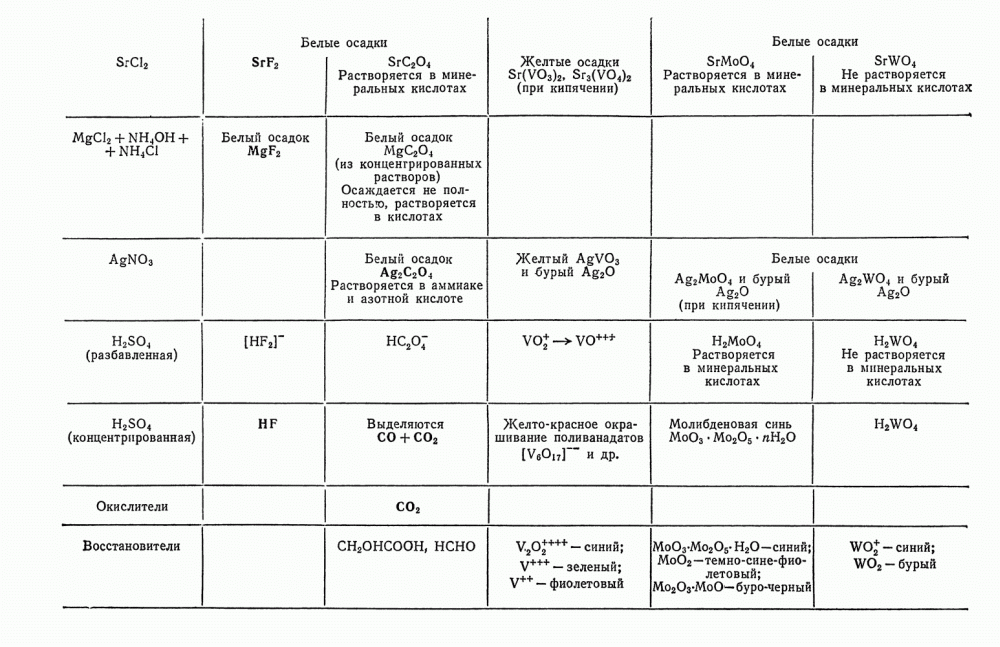
- § 21. Анализ смеси ионов
- § 22. Анализ смеси SO3, SO4, S2O3 и CO3-ионов
- § 23. Анализ смеси VO2, MoO4 и WO4-ионов
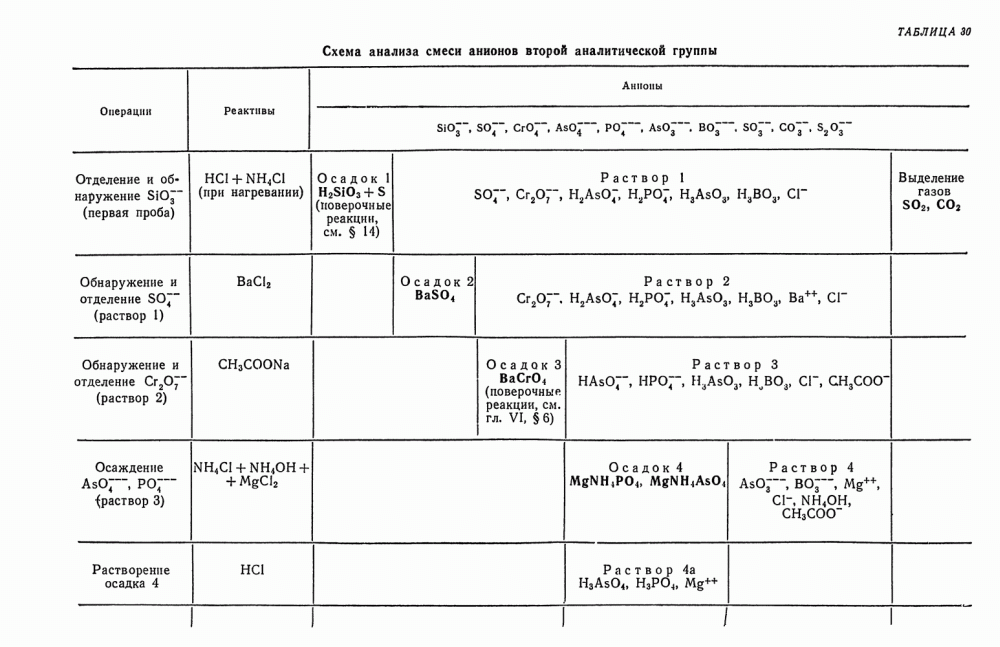
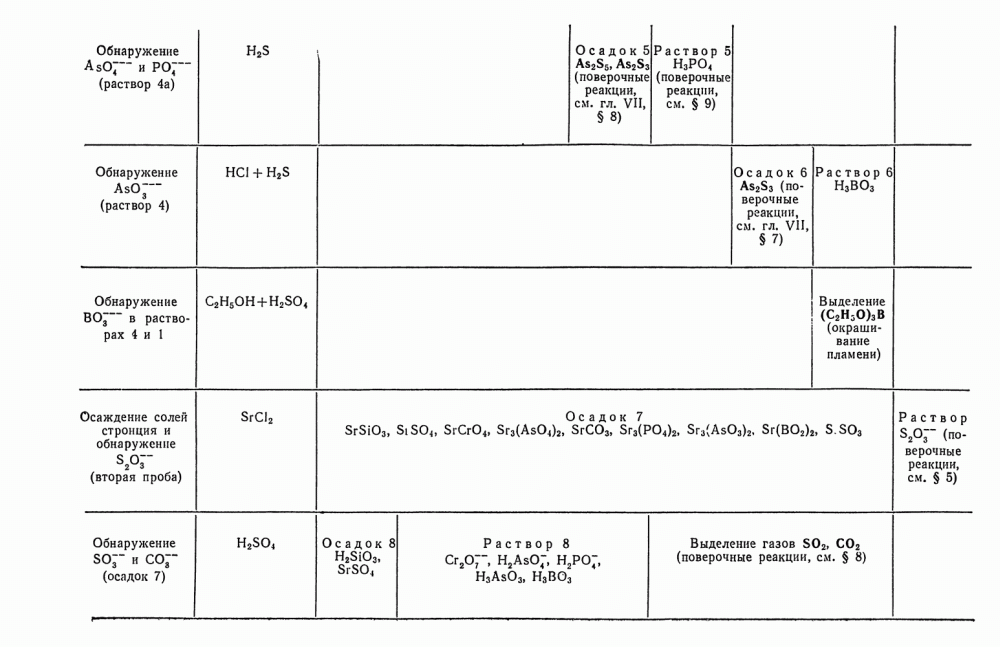
- § 24. Анализ смеси анионов второй группы
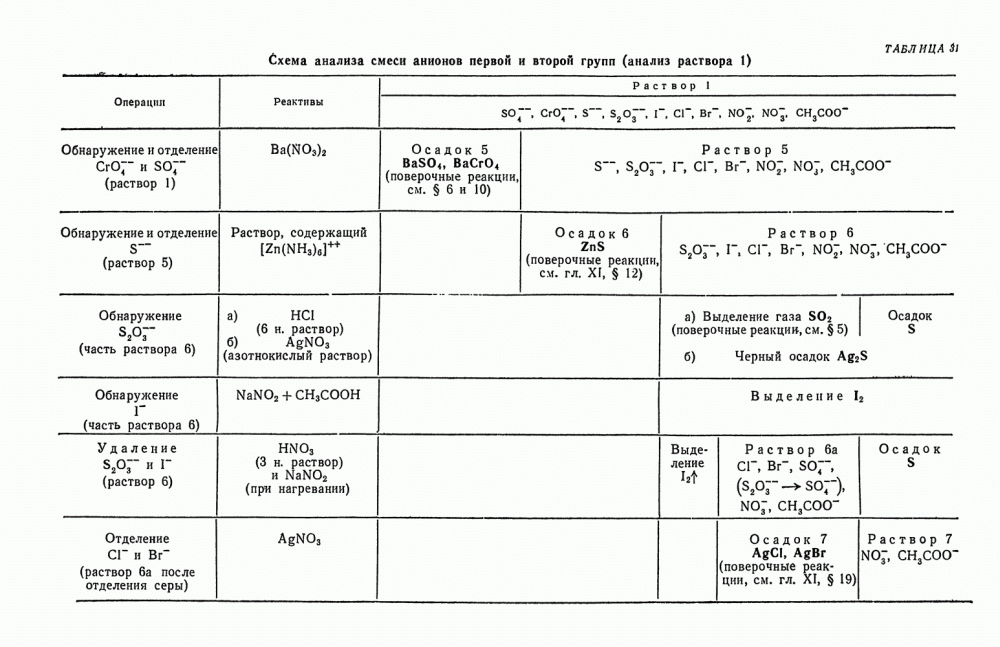
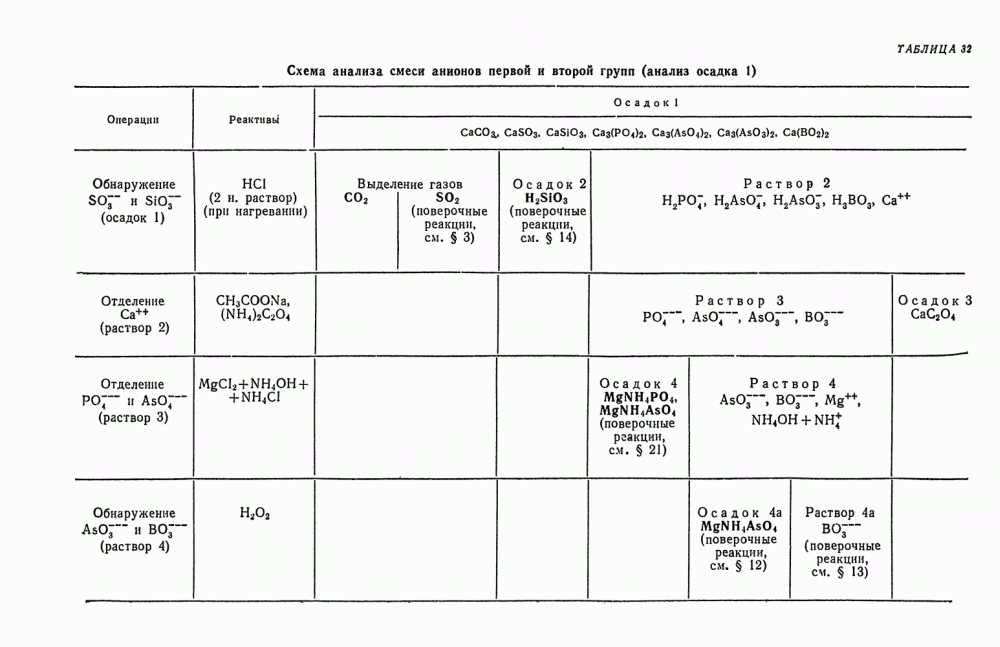
- § 25. Анализ смеси анионов первой и второй групп
- ГЛАВА XIII. ОБНАРУЖЕНИЕ СВОБОДНЫХ МЕТАЛЛОВ И НЕМЕТАЛЛОВ, ИДЕНТИФИЦИРОВАНИЕ СОЛЕЙ И ДРУГИХ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И АНАЛИЗ ИХ СМЕСЕЙ
- § 1. Подготовка вещества к анализу
- § 2. Предварительные испытания
- § 3. Растворение анализируемого вещества в воде, кислотах и щелочах
- § 4. Переведение в растворимое состояние веществ, нерастворимых в воде, кислотах и щелочах
- § 5. Анализ неизвестного вещества
- § 6. Обнаружение свободных элементов
- § 7. Идентифицирование солей и других индивидуальных соединений
- § 8. Обнаружение микропримесей
- § 9. Анализ сплавов
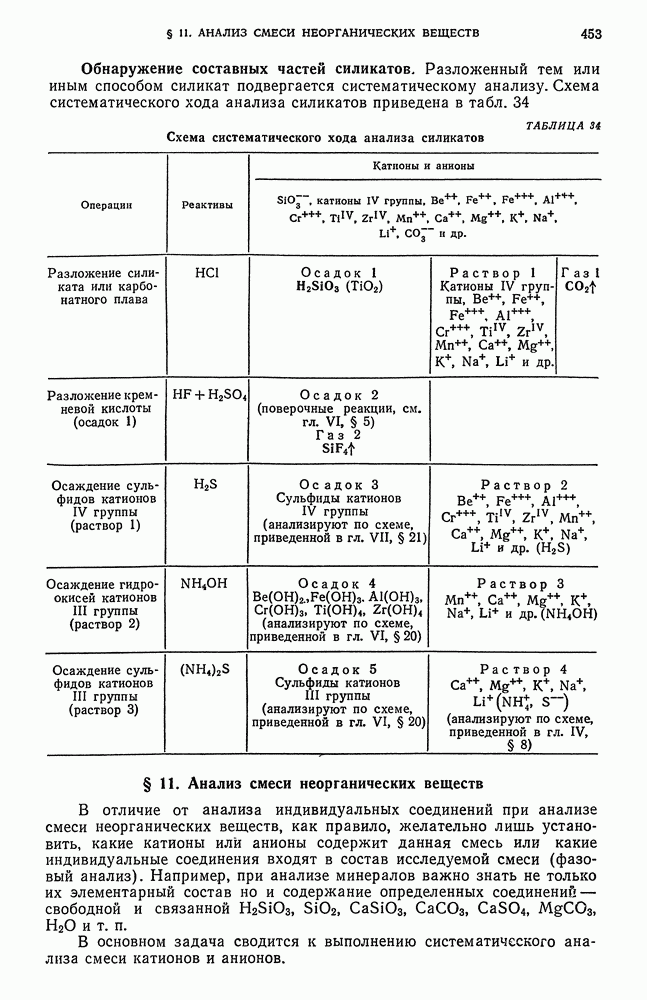
- § 10. Анализ силикатов и алюмосиликатов
- § 11. Анализ смеси неорганических веществ
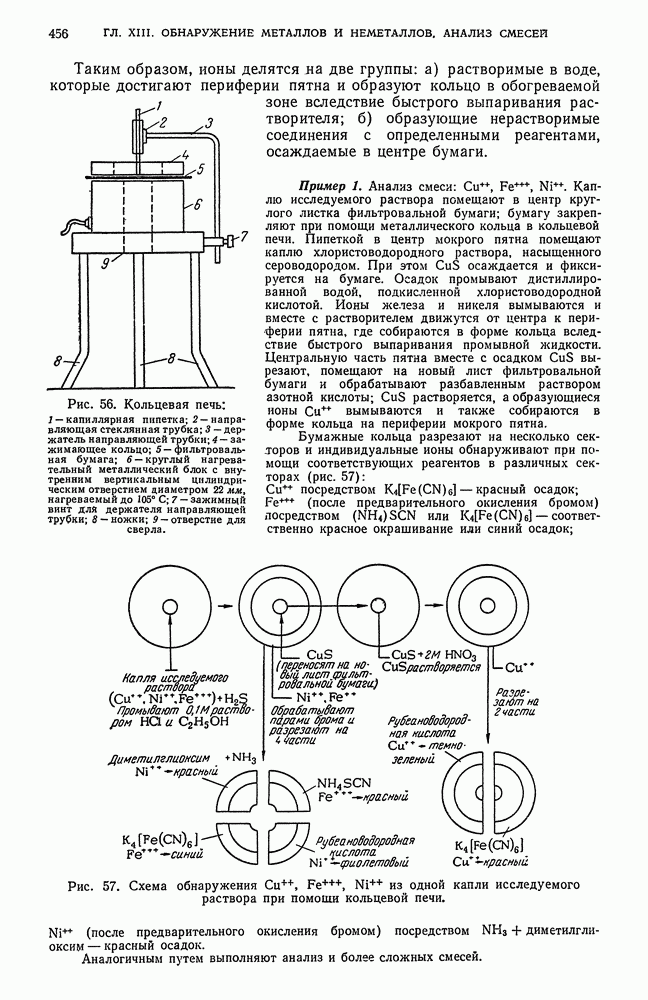
- § 12. Экспрессный метод анализа смесей катионов и анионов
- § 13. Идентифицирование нерастворимых веществ
- ЛИТЕРАТУРА