| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 24. Анализ смеси анионов второй группы
Предварительные испытания. 1. Определите характер среды испытуемого вещества. Кислая среда указывает на присутствие свободных кислот, щелочная среда — на присутствие свободных оснований, (которые даны для анализа или образовались в результате гидролиза), нейтральная среда — на отсутствие свободных кислот и оснований.
2. Установите в отдельных пробах, как действует раствор  на нейтральный и на подкисленный хлористоводородной кислотой испытуемый раствор.
на нейтральный и на подкисленный хлористоводородной кислотой испытуемый раствор.
Если от прибавления раствора  к нейтральному раствору осадок не образуется, можно сделать вывод, что в анализируемом растворе отсутствуют анионы, образующие малорастворимые соединения с ионами бария. Однако
к нейтральному раствору осадок не образуется, можно сделать вывод, что в анализируемом растворе отсутствуют анионы, образующие малорастворимые соединения с ионами бария. Однако  могут присутствовать, так как они образуют осадки с
могут присутствовать, так как они образуют осадки с  только из концентрированных растворов. Если осадок образуется и в кислой среде, то вероятно присутствие
только из концентрированных растворов. Если осадок образуется и в кислой среде, то вероятно присутствие  .
.
По образованию в кислой среде осадка  еще нельзя с полной уверенностью сказать, что в нейтральном анализируемом растворе имелся
еще нельзя с полной уверенностью сказать, что в нейтральном анализируемом растворе имелся  , так как он может образоваться за счет окисления в кислой среде соединений, содержащих серу, присутствующими в анализируемом растворе окислителями.
, так как он может образоваться за счет окисления в кислой среде соединений, содержащих серу, присутствующими в анализируемом растворе окислителями.
3. Установите, как действует раствор  на испытуемый раствор. Если от прибавления раствора
на испытуемый раствор. Если от прибавления раствора  осадок не образуется, то можно сделать вывод, что в анализируемом растворе отсутствуют анионы, образующие осадок с ионами серебра, т. е. все анионы II группы, кроме
осадок не образуется, то можно сделать вывод, что в анализируемом растворе отсутствуют анионы, образующие осадок с ионами серебра, т. е. все анионы II группы, кроме  .
.
Образование осадка при добавлении раствора  свидетельствует о присутствии в растворе всех или некоторых анионов II группы. Образование белого осадка указывает на возможное отсутствие анионов, образующих с ионами серебра цветные осадки, а именно:
свидетельствует о присутствии в растворе всех или некоторых анионов II группы. Образование белого осадка указывает на возможное отсутствие анионов, образующих с ионами серебра цветные осадки, а именно:  образование желтого осадка указывает на присутствие
образование желтого осадка указывает на присутствие  или
или  образование черного осадка— на присутствие
образование черного осадка— на присутствие  красного —
красного —  шоколадного
шоколадного  .
.
4. Проверьте, как действуют растворы KI и  на подкисленный испытуемый раствор. Эти реакции дают возможность установить, имеются ли в смеси окислители и восстановители.
на подкисленный испытуемый раствор. Эти реакции дают возможность установить, имеются ли в смеси окислители и восстановители.
Если подкисленный уксусной кислотой испытуемый раствор не изменяется от прибавления раствора KI, значит окислители  отсутствуют. Выделение свободного иода (посинение крахмальной бумаги) свидетельствует о присутствии
отсутствуют. Выделение свободного иода (посинение крахмальной бумаги) свидетельствует о присутствии  .
.
Обесцвечивание раствора  при сливании его на холоду с подкисленным испытуемым раствором свидетельствует о наличии в последнем
при сливании его на холоду с подкисленным испытуемым раствором свидетельствует о наличии в последнем  , а обесцвечивание при нагревании о наличии
, а обесцвечивание при нагревании о наличии  .
.
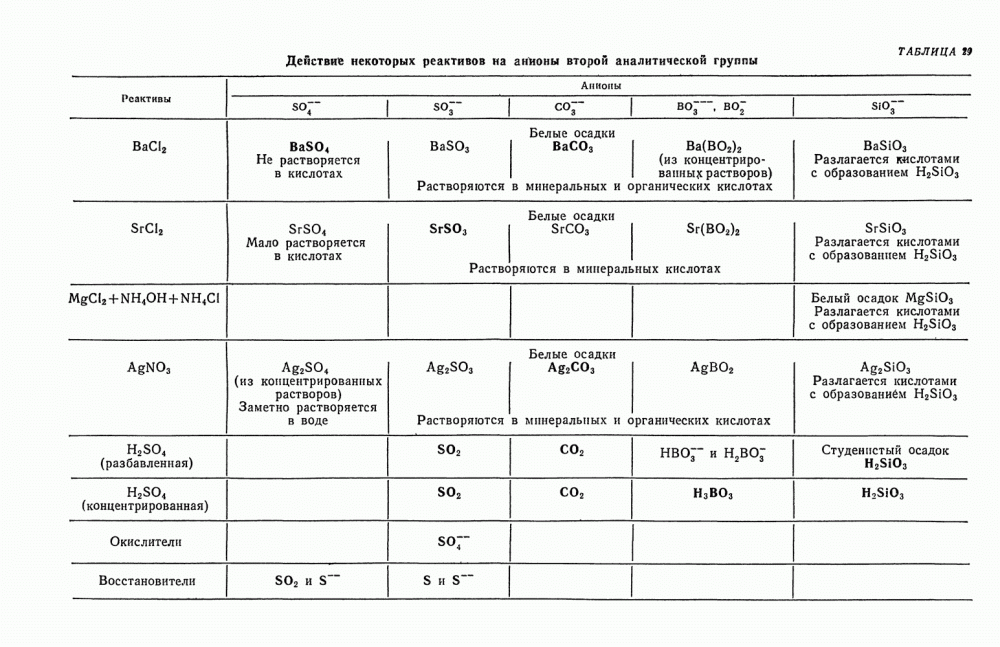
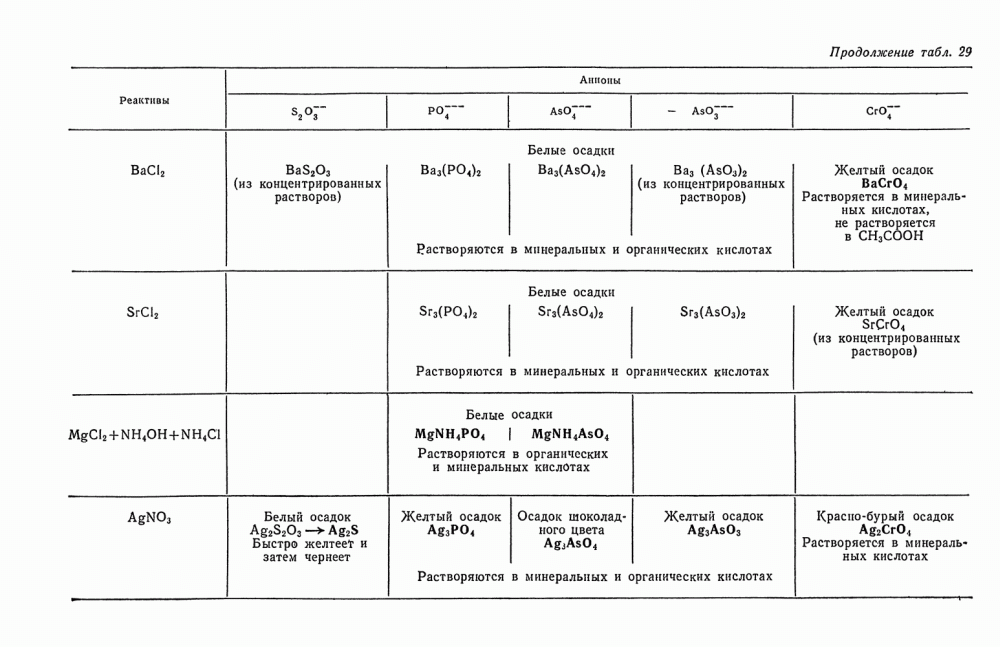
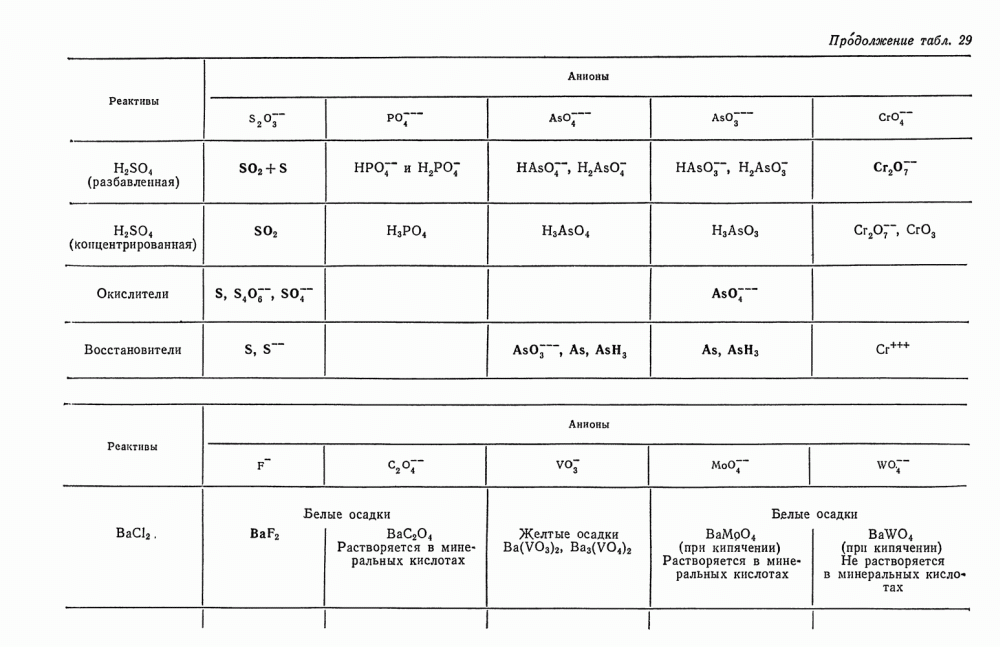
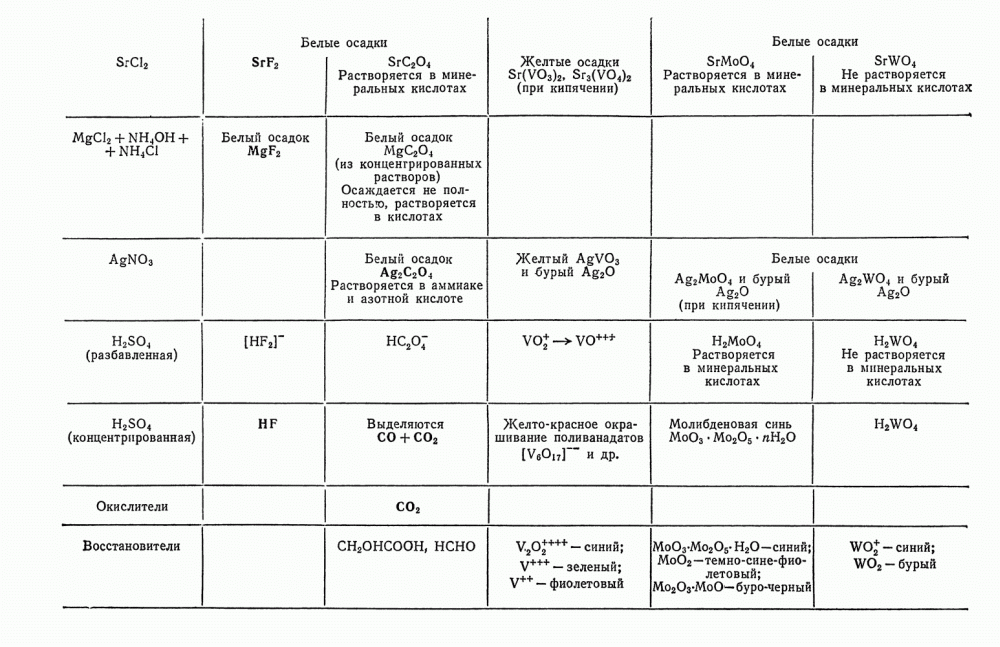
5. Проверьте действие разбавленной и концентрированной  . Эти реакции также позволяют сделать ряд выводов о присутствии некоторых анионов II группы (см. табл. 29).
. Эти реакции также позволяют сделать ряд выводов о присутствии некоторых анионов II группы (см. табл. 29).
6. Проверьте наличие  (см, § 7) и
(см, § 7) и  (см. § 9).
(см. § 9).
Подготовка вещества к анализу. Если для исследования были даны соли щелочных металлов, то дальнейший анализ проводят непосредственно с раствором этих солей, как указано ниже. Если для исследования были даны соли других металлов, то перед систематическим ходом анализа (после окончания предварительных испытаний) приходится отделять катионы тяжелых металлов методом «содовой вытяжки» (см. гл. V, § 8, 9). Делается это для того, чтобы избежать многих затруднений и предотвратить побочные реакции при дальнейшем ходе анализа.
Необходимо также помнить, что несовместимые друг с другом анионы — окислители и восстановители, как, например,  и т. п., при определенных значениях
и т. п., при определенных значениях  могут переходить в окисленные или восстановленные формы; вследствие этого возможны ошибки при последующем анализе. Поэтому всегда нужно всесторонне исследовать данный для анализа раствор и делать окончательное
могут переходить в окисленные или восстановленные формы; вследствие этого возможны ошибки при последующем анализе. Поэтому всегда нужно всесторонне исследовать данный для анализа раствор и делать окончательное  все результаты предварительных испытаний и систематического анализа.
все результаты предварительных испытаний и систематического анализа.
Систематический ход анализа. Перед выполнением систематического анализа необходимо проделать частные реакции на некоторые из анионов в отдельных пробах подготовленного раствора. Полученные при этом результаты не очень надежны, тем не менее они могут служить удобным ориентиром в выборе возможного варианта анализа смеси анионов, так как по ним можно приблизительно установить состав анализируемой смеси.
Далее приступают к систематическому анализу, который заключается в разделении испытуемой смеси на подгруппы, более удобные для анализа, и в выделении отдельных анионов из смеси.
Отделение и обнаружение  -ионов. К части анализируемого раствора в фарфоровой чашке прибавьте хлористоводородную кислоту,
-ионов. К части анализируемого раствора в фарфоровой чашке прибавьте хлористоводородную кислоту,  и выпарьте смесь досуха. При этом сернистая, тиосерная и угольная кислоты разлагаются. Сухой остаток обработайте 2 н. раствором
и выпарьте смесь досуха. При этом сернистая, тиосерная и угольная кислоты разлагаются. Сухой остаток обработайте 2 н. раствором  :
:

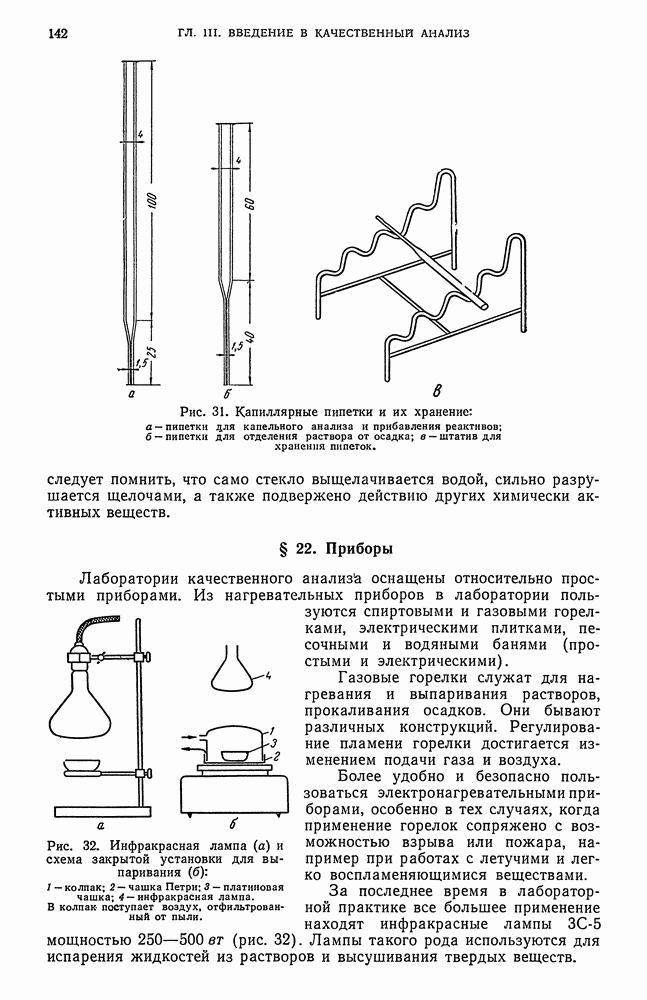
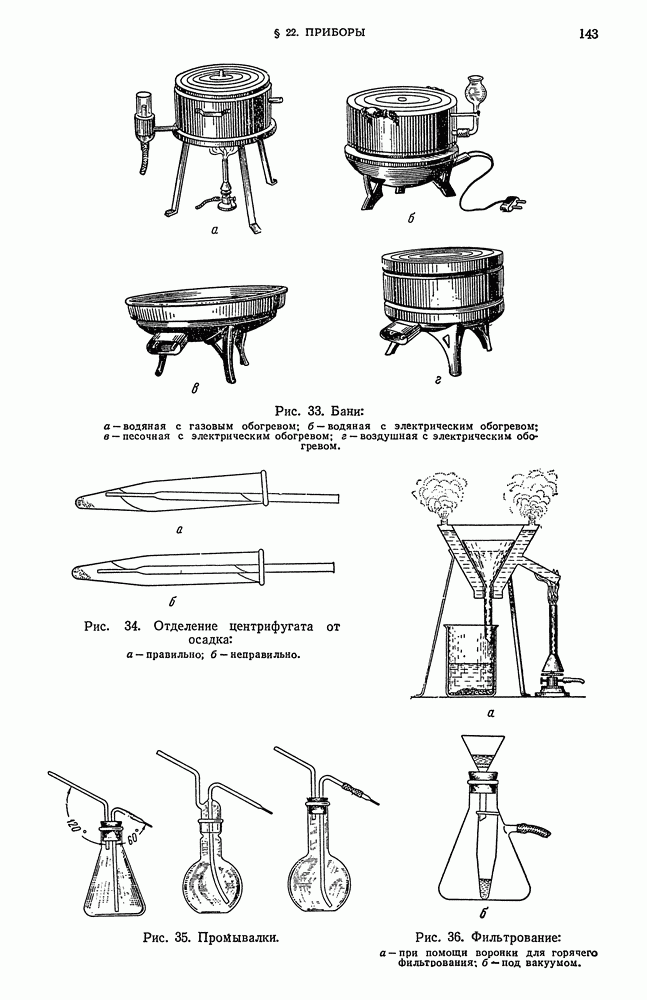
К сухому остатку, помещенному в фарфоровую чашку, снова прибавьте хлористоводородную кислоту и воду. Желатинообразный осадок представляет собой кремневую кислоту. Осадок перенесите на воронку, раствор отфильтруйте под вакуумом и осадок промойте водой, подкисленной  . Промывные воды объедините с фильтратом. Вместо отсасывания под вакуумом можно удалить жидкость с помощью пипетки.
. Промывные воды объедините с фильтратом. Вместо отсасывания под вакуумом можно удалить жидкость с помощью пипетки.
Чтобы окончательно убедиться в том, что осадок представляет собой кремневую кислоту, с ним проделывают поверочные реакции: окрашивание метиленовым голубым; образование фторида кремния; открытие кремневой кислоты реакциями с  и бензидином (см. § 14).
и бензидином (см. § 14).
Обнаружение и отделение  -ионов. Для обнаружения
-ионов. Для обнаружения  прибавляют раствор
прибавляют раствор  в кислой среде. В этих условиях
в кислой среде. В этих условиях  не образует осадка с другими анионами. Так как избыток
не образует осадка с другими анионами. Так как избыток  в дальнейшем мешает открытию других анионов, то раствор его прилейте сначала только к 1—2 каплям раствора 1, полученного после осаждения кремневой кислоты. Если осадка не образуется, то приливать раствор
в дальнейшем мешает открытию других анионов, то раствор его прилейте сначала только к 1—2 каплям раствора 1, полученного после осаждения кремневой кислоты. Если осадка не образуется, то приливать раствор  ко всему испытуемому раствору не следует. Если осадок образуется, то для отделения
ко всему испытуемому раствору не следует. Если осадок образуется, то для отделения  к части раствора 1 прилейте раствор
к части раствора 1 прилейте раствор  и проверьте полноту осаждения. Небольшой избыток
и проверьте полноту осаждения. Небольшой избыток  не вредит. Затем к полученной смеси добавьте
не вредит. Затем к полученной смеси добавьте  оставшегося исходного раствора. Таким образом можно достигнуть почти полного осаждения
оставшегося исходного раствора. Таким образом можно достигнуть почти полного осаждения  и избежать большого избытка
и избежать большого избытка  .
.
Смесь нагрейте и отцентрифугируйте осадок:

Обнаружение и отделение  -ионов. Для обнаружения
-ионов. Для обнаружения  раствор 2 слегка упарьте и добавьте к нему несколько капель ацетата натрия для понижения кислотности раствора. В присутствии
раствор 2 слегка упарьте и добавьте к нему несколько капель ацетата натрия для понижения кислотности раствора. В присутствии  оранжево-красная окраска раствора изменяется в желтую и выделяется желтый осадок
оранжево-красная окраска раствора изменяется в желтую и выделяется желтый осадок 

Если осадок  сразу не выпал, то прилейте еще 1—2 капли раствора
сразу не выпал, то прилейте еще 1—2 капли раствора  . Если при повторном добавлении
. Если при повторном добавлении  осадка не образуется, то это свидетельствует об отсутствии в растворе
осадка не образуется, то это свидетельствует об отсутствии в растворе  . Если осадок 3 образовался, то его следует отделить фильтрованием, растворить в минеральной кислоте и проделать поверочные реакции на
. Если осадок 3 образовался, то его следует отделить фильтрованием, растворить в минеральной кислоте и проделать поверочные реакции на  (см. § 10).
(см. § 10).
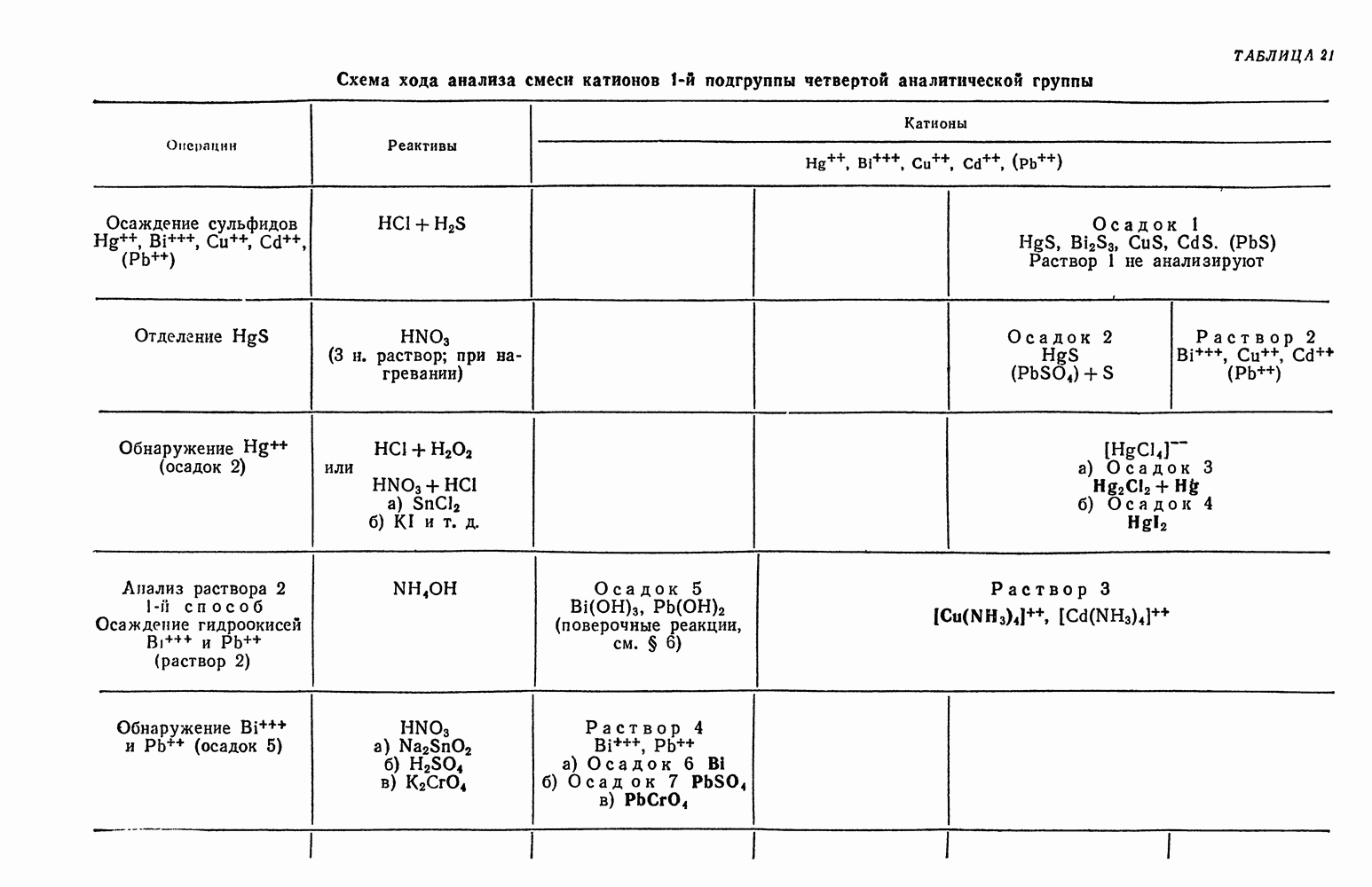
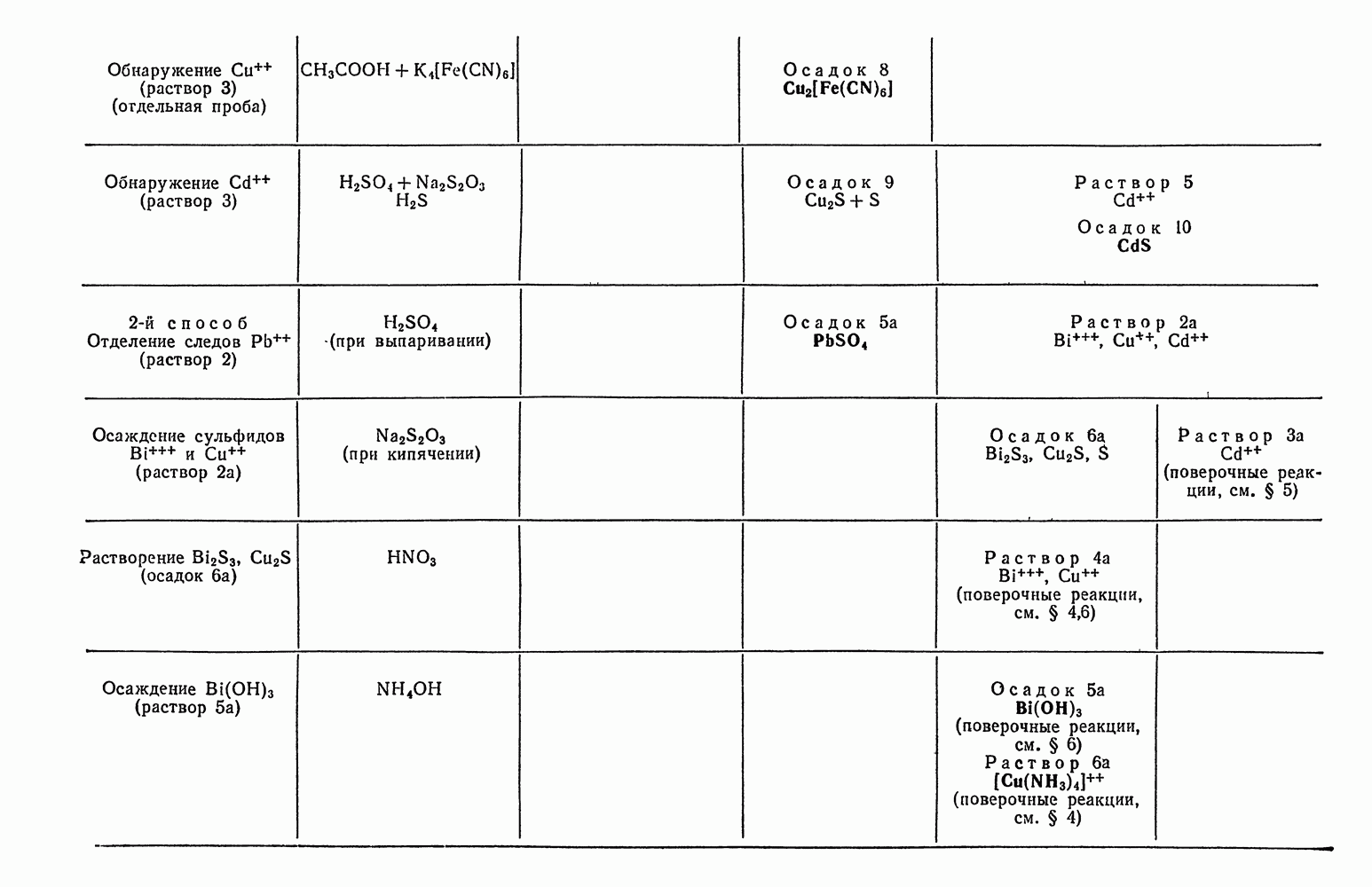
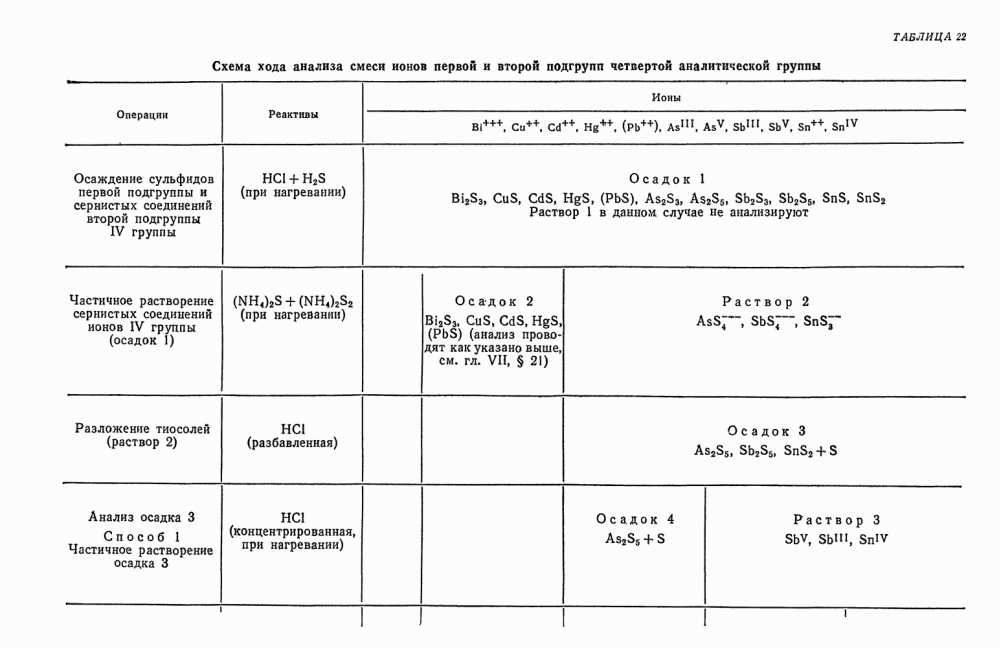
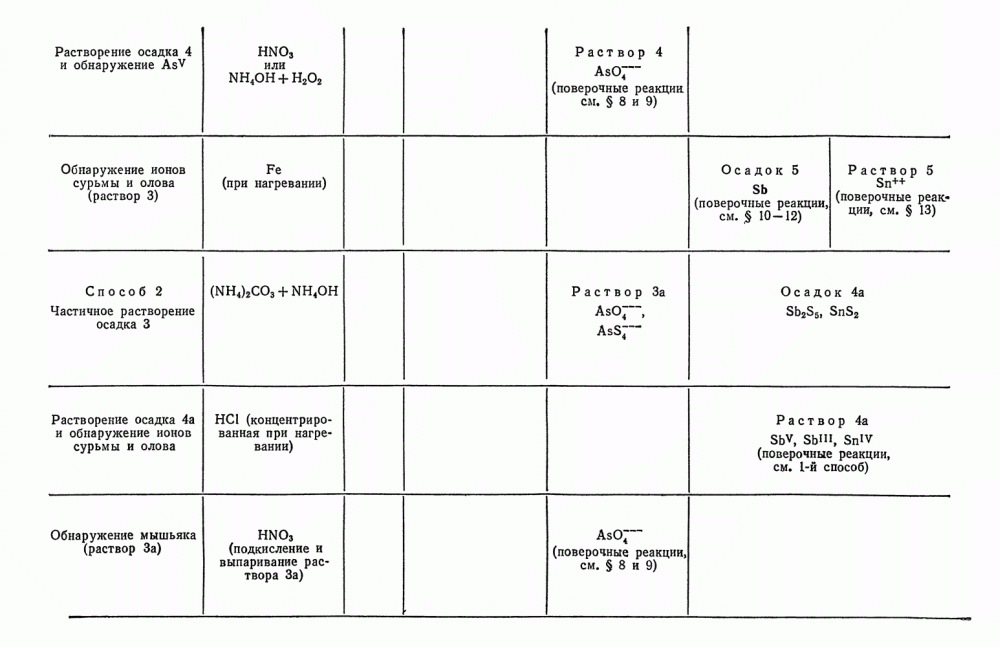
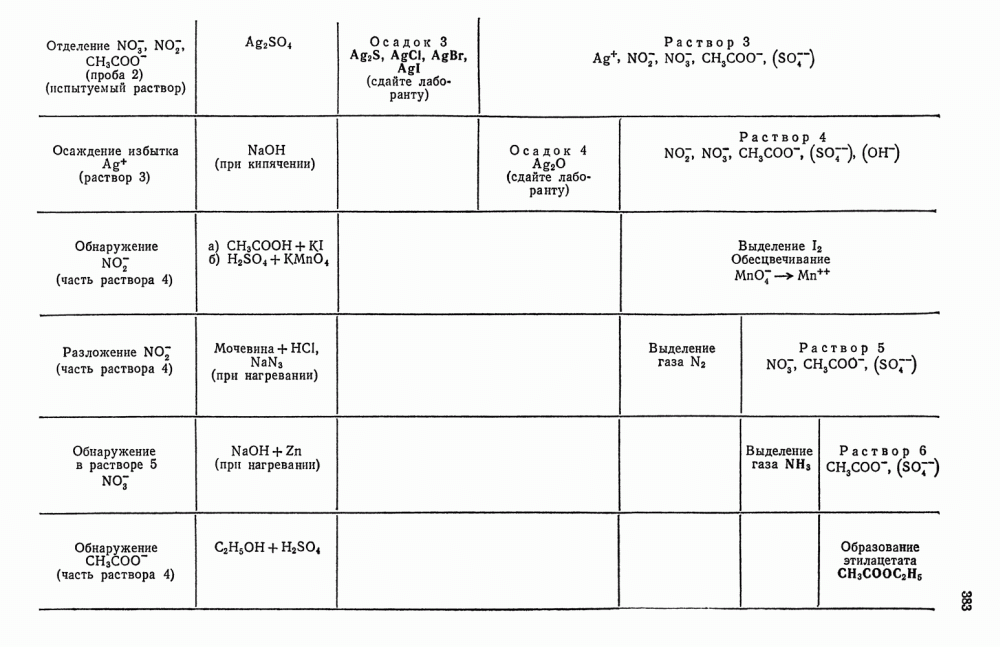
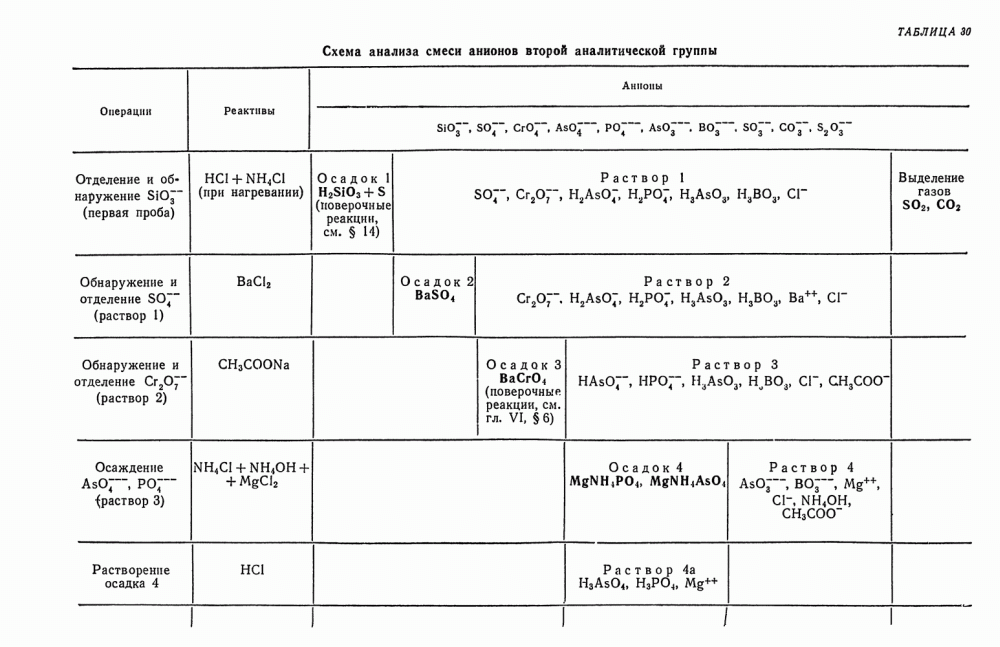
Таблица 30. Схема анализов смеси анионов второй аналитической группы

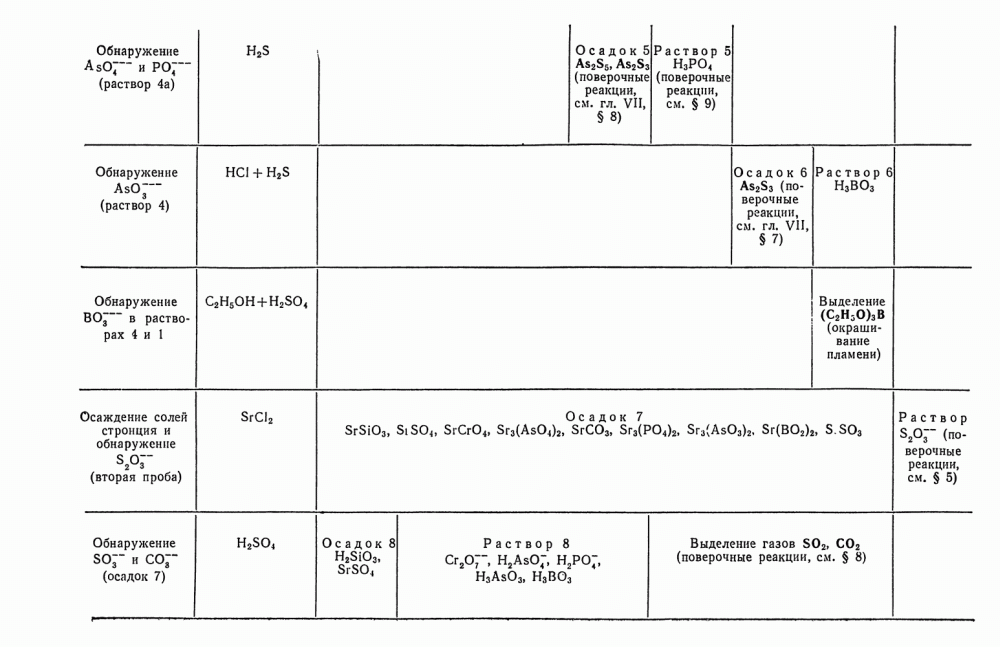
Продолжение табл. 30.

Осаждение  -ионов. Арсенаты и фосфаты осаждаются магнезиальной смесью.
-ионов. Арсенаты и фосфаты осаждаются магнезиальной смесью.
Обнаружение  и
и  -ионов выполняют, как описано в § 21. Для анализа смеси
-ионов выполняют, как описано в § 21. Для анализа смеси  и
и  поступают, как описано в § 22.
поступают, как описано в § 22.
Схема анализа смеси анионов второй группы представлена в табл. 30.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Анализ и синтез
- § 2. Предмет аналитической химии
- § 3. Развитие аналитической химии
- § 4. Качественный и количественный анализ
- ГЛАВА I. ПРИМЕНЕНИЕ ЗАКОНА ДЕЙСТВИЯ МАСС В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Влияние среды на состояние ионов в растворах
- § 2. Обратимые и необратимые аналитические реакции
- § 3. Направление аналитических реакций; правила обменного разложения
- § 4. Закон действия масс и следствие из него
- § 5. Границы применимости закона действия масс
- § 6. Сильные и слабые электролиты
- § 7. Активность
- § 8. Коэффициент активности и ионная сила
- Б. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ (В ГОМОГЕННЫХ СИСТЕМАХ)
- § 9. Гомогенные и гетерогенные системы
- § 10. Ионное произведение воды
- § 11. Ионы гидроксония
- § 12. Равновесие ионов в водных растворах; понятие о pH
- § 13. Равновесие в водных растворах слабых электролитов
- § 14. Влияние сильных кислот или сильных оснований на степень электролитической диссоциации слабых электролитов
- § 15. Приближенные формулы для расчета [H+] и [OH-] в водных растворах кислот и оснований
- В. РАВНОВЕСИЯ В БУФЕРНЫХ РАСТВОРАХ
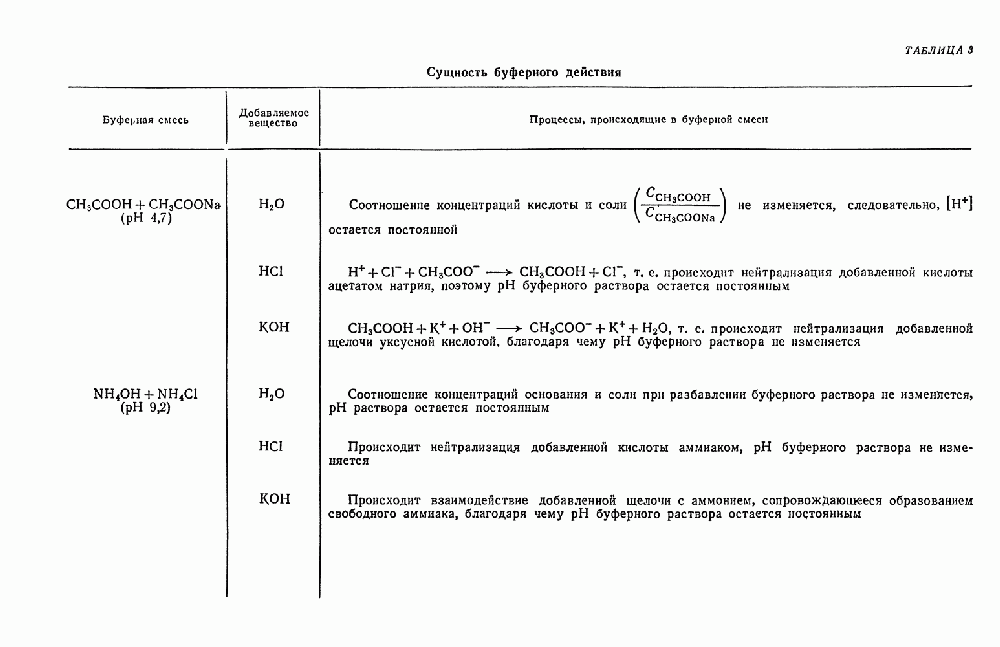
- § 16. Буферные растворы
- § 17. Применение буферных растворов в химическом анализе
- Г. РАВНОВЕСИЯ В РАСТВОРАХ ГИДРОЛИЗУЮЩИХСЯ СОЛЕЙ
- § 18. Теоретические основы гидролиза
- § 19. Механизм гидролитического расщепления
- § 20. Подавление и усиление гидролиза солей
- Д. РАВНОВЕСИЯ В ВОДНЫХ РАСТВОРАХ ТИПИЧНО АМФОТЕРНЫХ ЭЛЕКТРОЛИТОВ
- § 21. Поведение амфотерных гидроокисей в водных растворах
- § 22. Константы электролитической диссоциации амфотерных гидроокисей
- Е. РАВНОВЕСИЯ В СИСТЕМАХ: ОСАДОК-НАСЫЩЕННЫЙ РАСТВОР
- § 23. Осаждение как один из основных методов химического анализа
- § 24. Произведение растворимости
- § 25. Произведение активностей
- § 26. Вычисление растворимости электролитов в воде по величине произведения растворимости
- § 27. Влияние различных факторов на растворимость малорастворимых электролитов
- Ж. ОСНОВЫ ТЕОРИИ ОБРАЗОВАНИЯ И РАЗЛОЖЕНИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИИ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 28. Характеристика комплексных соединений, имеющих значение в химическом анализе
- § 29. Квантовомеханические представления о строении комплексов
- § 30. Равновесия в растворах комплексных соединений
- § 31. Константы нестойкости комплексов
- § 32. Внутрикомплексные соединения
- § 33. Методы разложения и образования комплексов, применяемых в аналитической химии
- § 34. Применение метода комплексообразования в химическом анализе
- ГЛАВА II. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРИМЕНЯЕМЫХ В АНАЛИТИЧЕСКОЙ ХИМИИ
- § 1. Окисление—восстановление как один из основных методов химического анализа
- § 2. Направление реакций окисления—восстановления
- § 3. Окислительно-восстановительные потенциалы
- § 4. Зависимость между величинами окислительно-восстановительных потенциалов и условиями, в которых протекают реакции окисления—восстановления
- § 5. Вычисление окислительно-восстановительных потенциалов
- § 6. Вычисление окислительно-восстановительных потенциалов с учетом коэффициентов активности
- ГЛАВА III. ВВЕДЕНИЕ В КАЧЕСТВЕННЫЙ АНАЛИЗ
- § 1. Обнаружение отдельных элементов
- § 2. Анализ мокрым и сухим путем
- § 3. Химические и физические методы качественного анализа
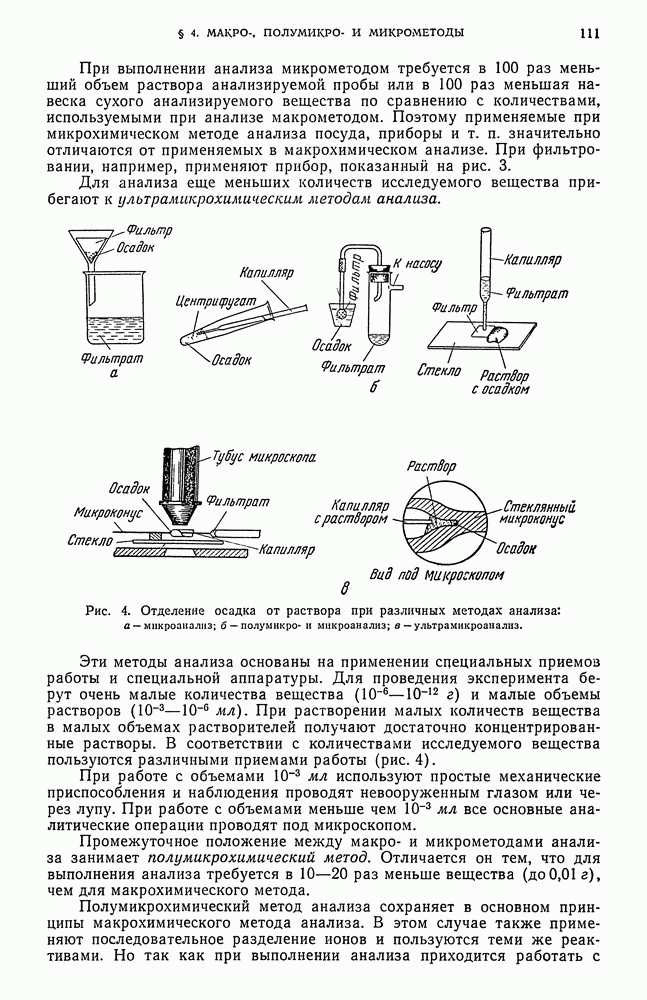
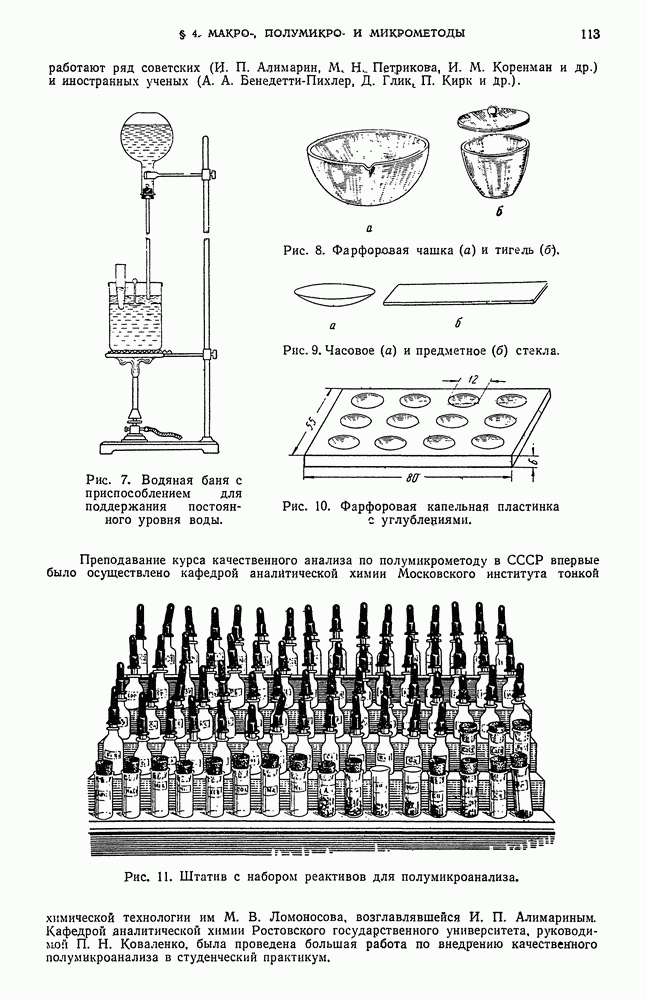
- § 4. Макро-, полумикро- и микрометоды
- § 5. Капельный анализ
- § 6. Микрокристаллоскопический анализ
- § 7. Метод растирания порошков
- § 8. Методы анализа, основанные на нагревании и сплавлении веществ
- § 9. Спектральный качественный анализ
- § 10. Хроматографический метод анализа
- § 11. Кинетические методы анализа
- Б. УСЛОВИЯ ВЫПОЛНЕНИЯ КАЧЕСТВЕННЫХ РЕАКЦИЙ
- § 12. Специфичность и чувствительность реакций
- § 13. Максимальная чувствительность аналитических реактивов
- § 14. Способы повышения чувствительности реакций
- § 15. Маскировка мешающих ионов
- § 16. Определение pH среды
- § 17. Регулирование pH среды в процессе аналитических определений
- В. РЕАКТИВЫ
- § 18. Понятие о химических реактивах
- § 19. Концентрация применяемых реактивов
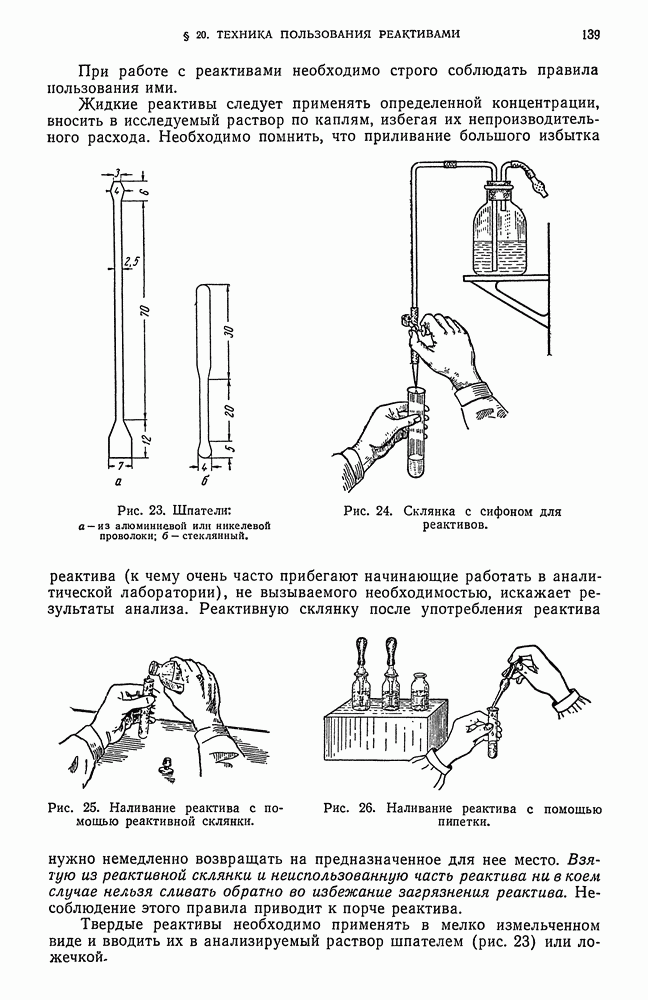
- § 20. Техника пользования реактивами
- Г. ПОСУДА И ПРИБОРЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕННОМ АНАЛИЗЕ
- § 21. Химическая посуда
- § 22. Приборы
- Д. АНАЛИТИЧЕСКИЕ ГРУППЫ
- § 23. Дробный и систематический анализ
- § 24. Аналитическая классификация катионов
- § 25. Сводные таблицы действия реактивов на катионы и анионы
- Е. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И АНАЛИТИЧЕСКАЯ КЛАССИФИКАЦИЯ ИОНОВ
- § 26. Значение периодического закона в аналитической химии
- § 27. Периодическая система элементов Д. И. Менделеева как классификация атомов по их строению
- § 28. Зависимость некоторых химических свойств элементов от положения их в периодической системе Д. И. Менделеева
- § 29. Растворимость химических соединений в связи с положением элементов в периодической системе Д. И. Менделеева
- § 30. Открытие новых аналитических реакций
- § 31. Аналитические группы и периодическая система элементов Д. И. Менделеева
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ КАТИОНОВ И АНАЛИЗ СМЕСЕЙ КАТИОНОВ
- § 1. Характеристика первой аналитической группы катионов
- § 2. Общие реакции катионов первой аналитической группы
- РЕАКЦИИ КАТИОНОВ 1-й ПОДГРУППЫ
- § 3. Обнаружение NН-ионов
- § 4. Методы разложения и удаления солей аммония
- § 5. Обнаружение K-ионов
- § 6. Обнаружение Rb-ионов
- § 7. Обнаружение Cs-ионов
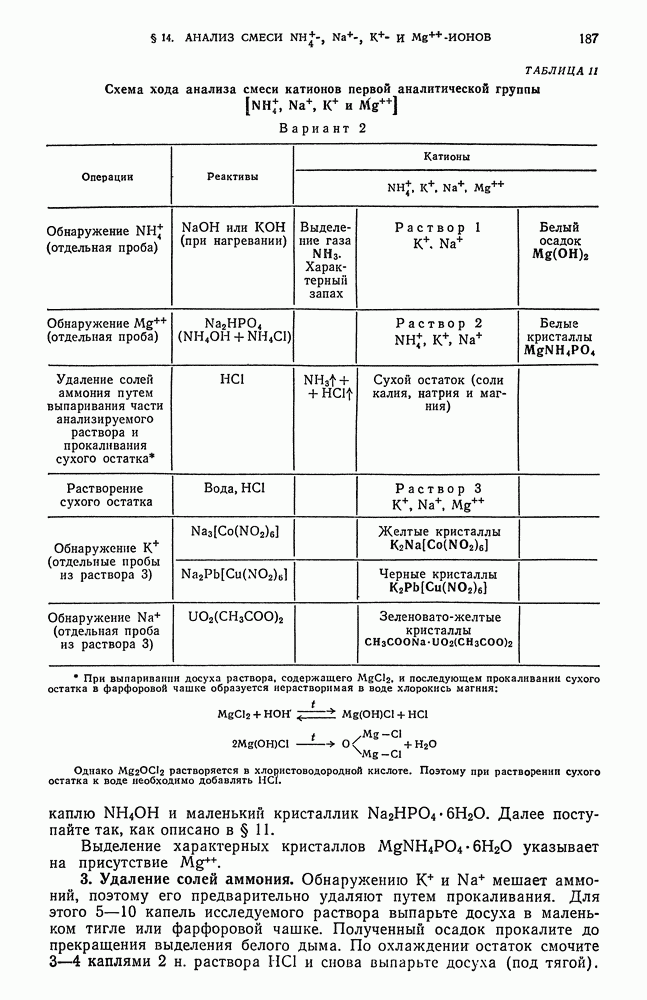
- § 8. Анализ смеси катионов первой подгруппы
- РЕАКЦИИ КАТИОНОВ 2-й ПОДГРУППЫ
- § 9. Обнаружение Li-ионов
- § 10. Обнаружение Na-ионов
- § 11. Обнаружение Mg-ионов
- § 12. Обзор действия реактивов на катионы первой аналитической группы
- § 13. Анализ смеси катионов второй подгруппы
- § 14. Анализ смеси ионов
- § 15. Анализ смеси ионов
- ГЛАВА V. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика второй аналитической группы катионов
- § 2. Общие реакции катионов второй аналитической группы
- § 3. Обнаружение Ca-ионов
- § 4. Обнаружение Sr-ионов
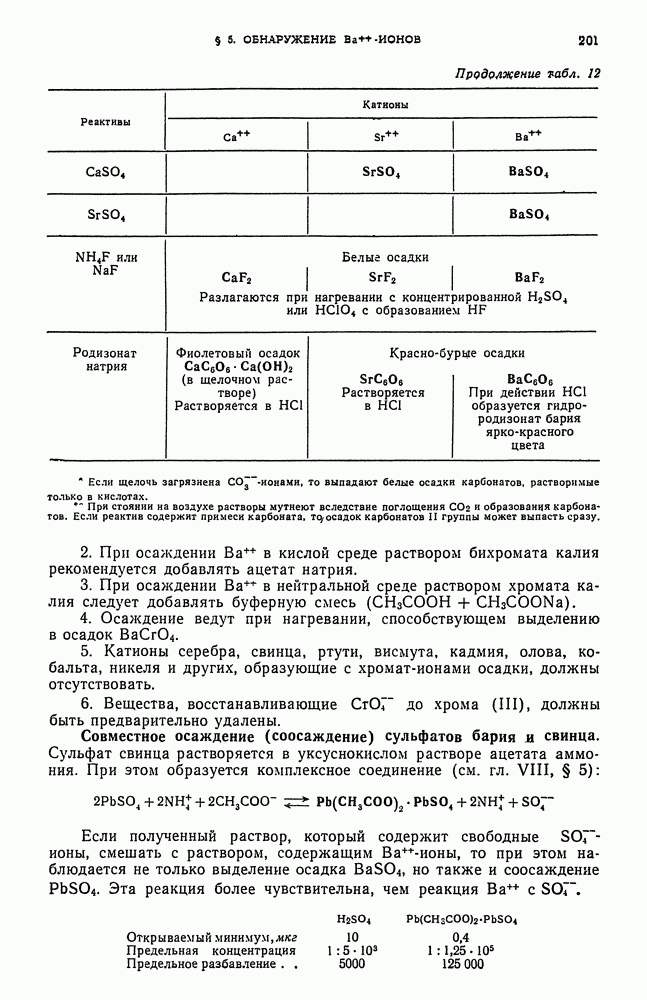
- § 5. Обнаружение Ba-ионов
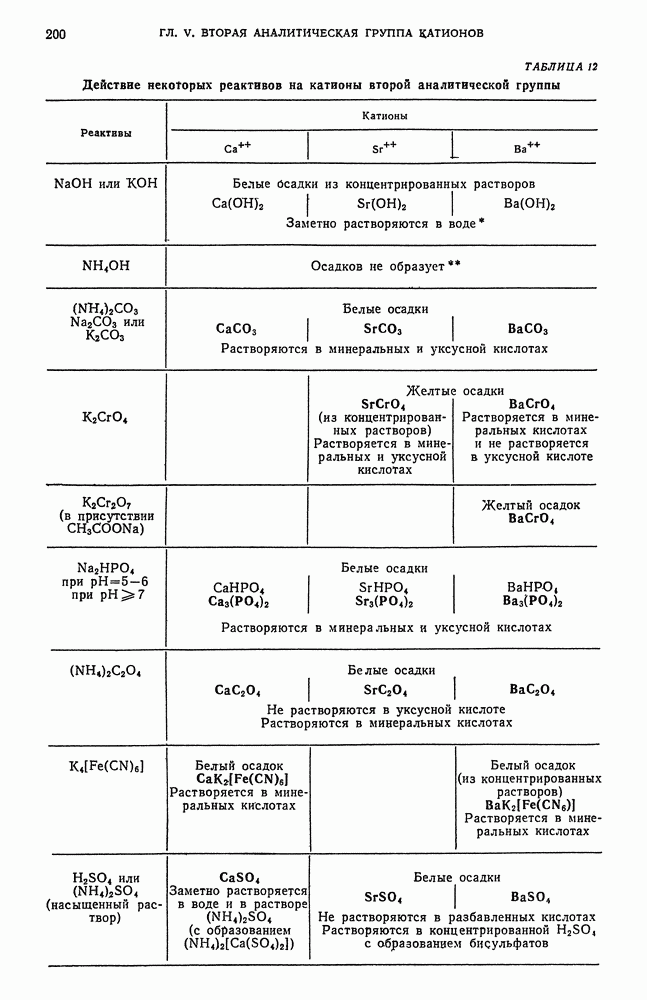
- § 6. Обзор действия реактивов на катионы второй аналитической группы
- § 7. Основы теории осаждения катионов второй аналитической группы групповым реактивом—карбонатом аммония
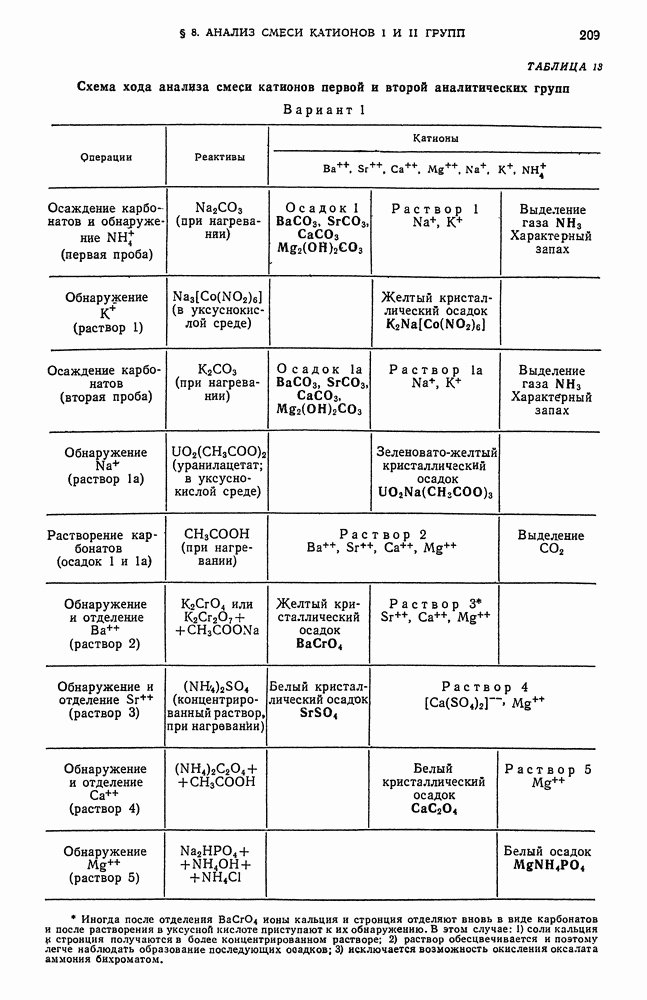
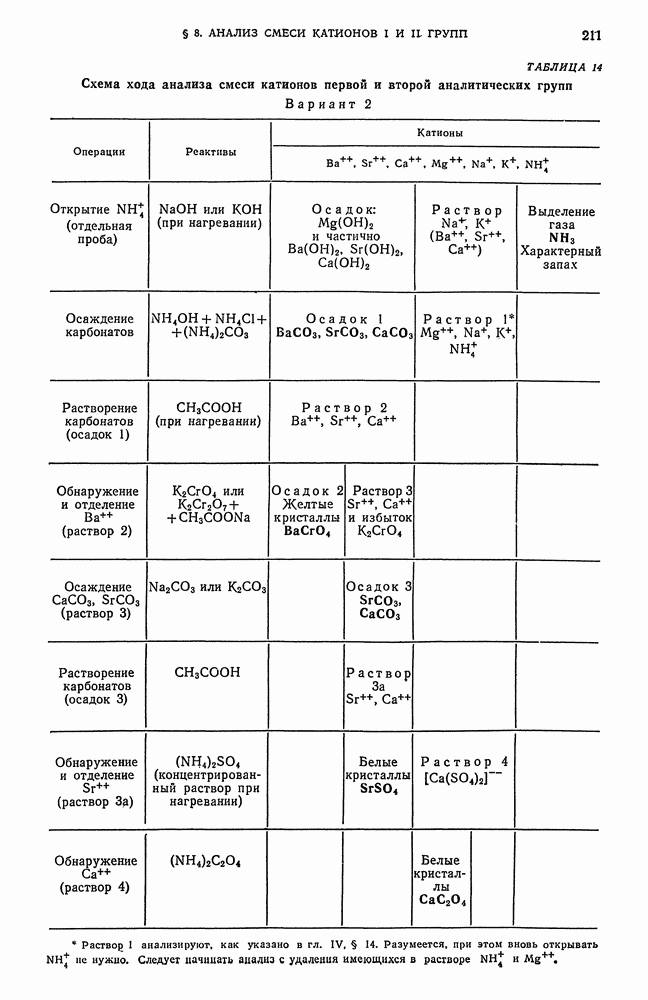
- § 8. Систематический ход анализа смеси катионов первой и второй аналитических групп
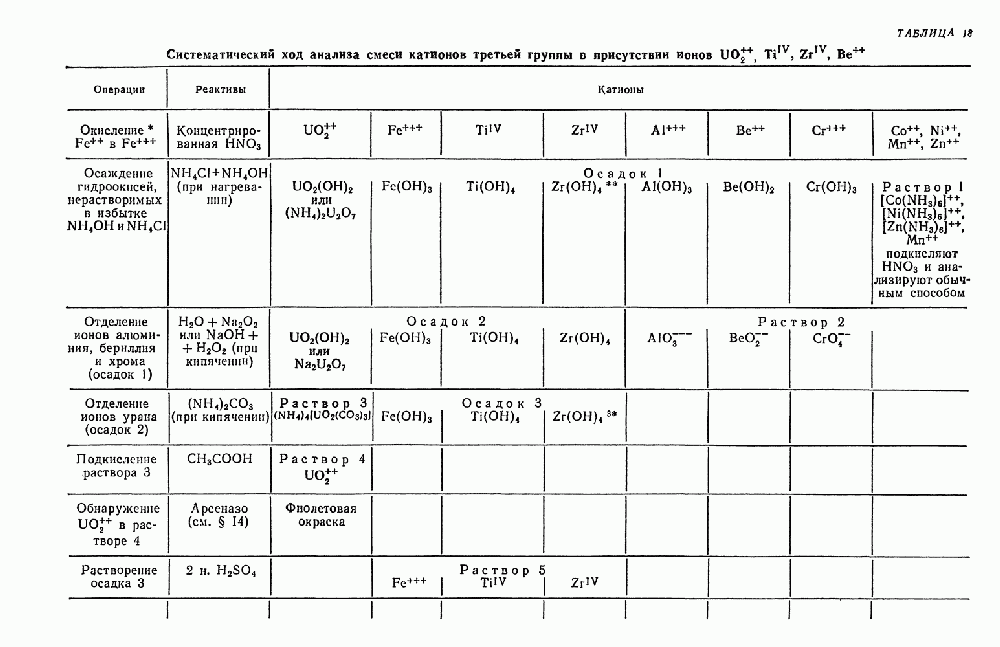
- § 9. Систематический ход анализа смеси катионов первой и второй аналитических групп в присутствии ионов
- § 10. Теоретические основы перевода сульфатов катионов второй аналитической группы в карбонаты
- ГЛАВА VI. ТРЕТЬЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика третьей аналитической группы катионов
- § 2. Общие реакции катионов третьей аналитической группы
- § 3. Обнаружение Be-ионов
- § 4. Обнаружение Al-ионов
- § 5. Обнаружение ионов титана (IV)
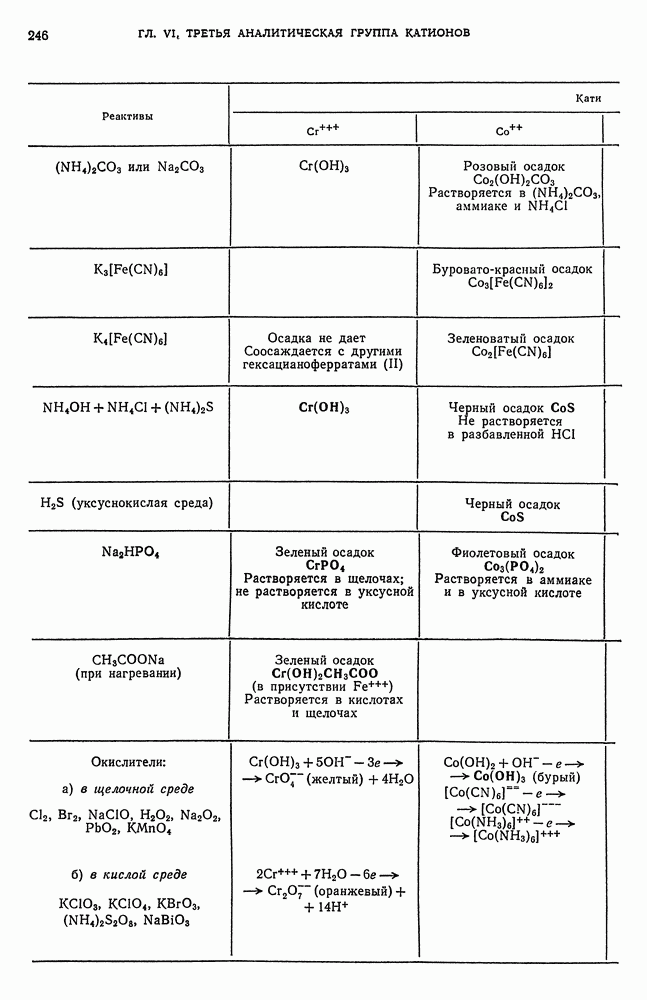
- § 6. Обнаружение Cr-ионов
- § 7. Обнаружение Mn-ионов
- § 8. Обнаружение Fe-ионов
- § 9. Обнаружение Fe-ионов
- § 10. Обнаружение Co-ионов
- § 13. Обнаружение ионов циркония (IV)
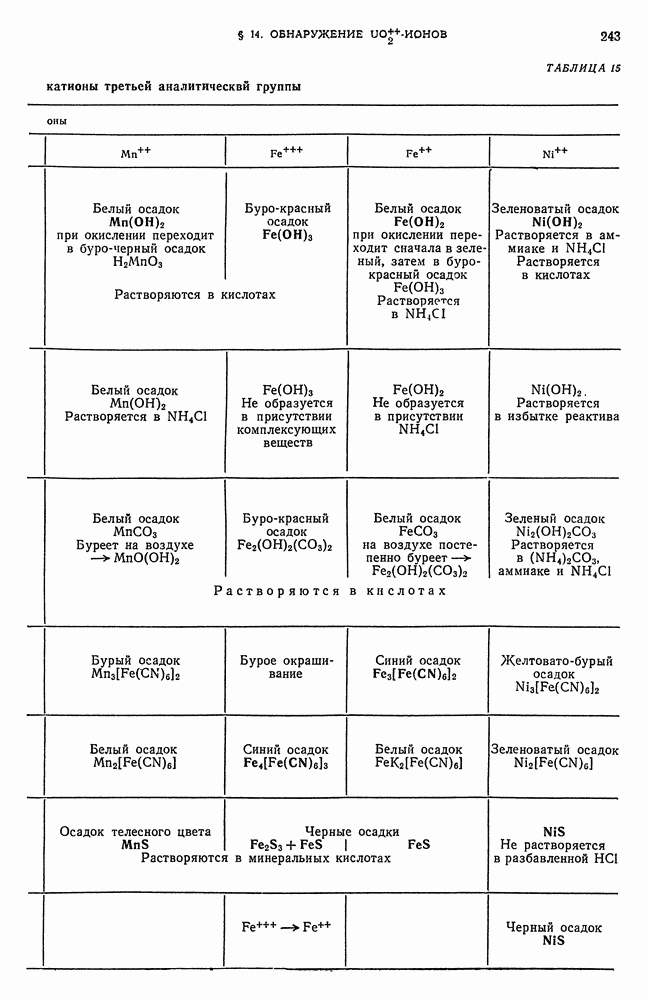
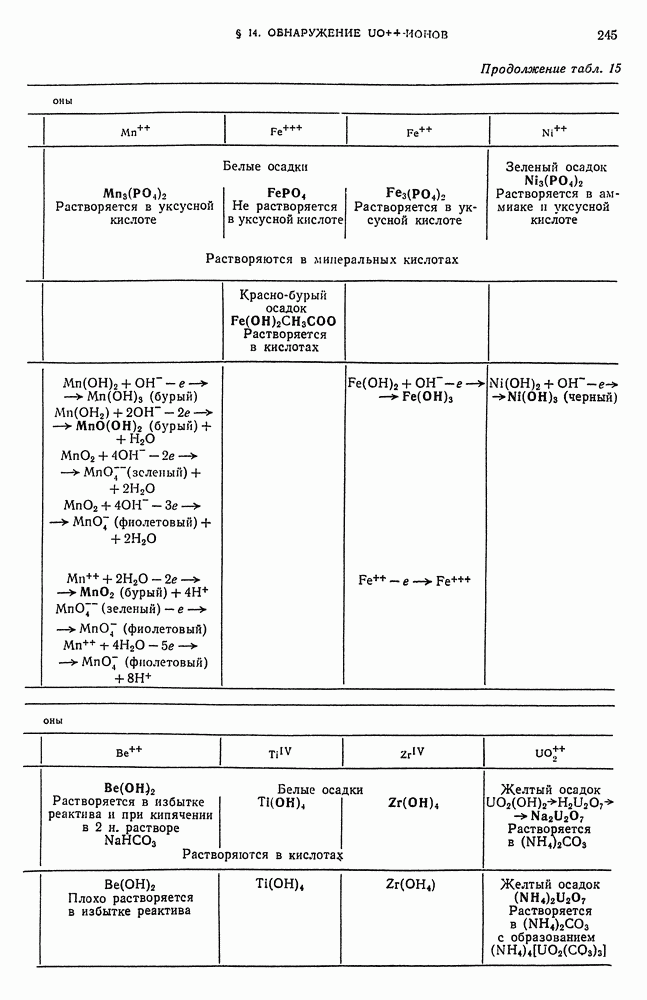
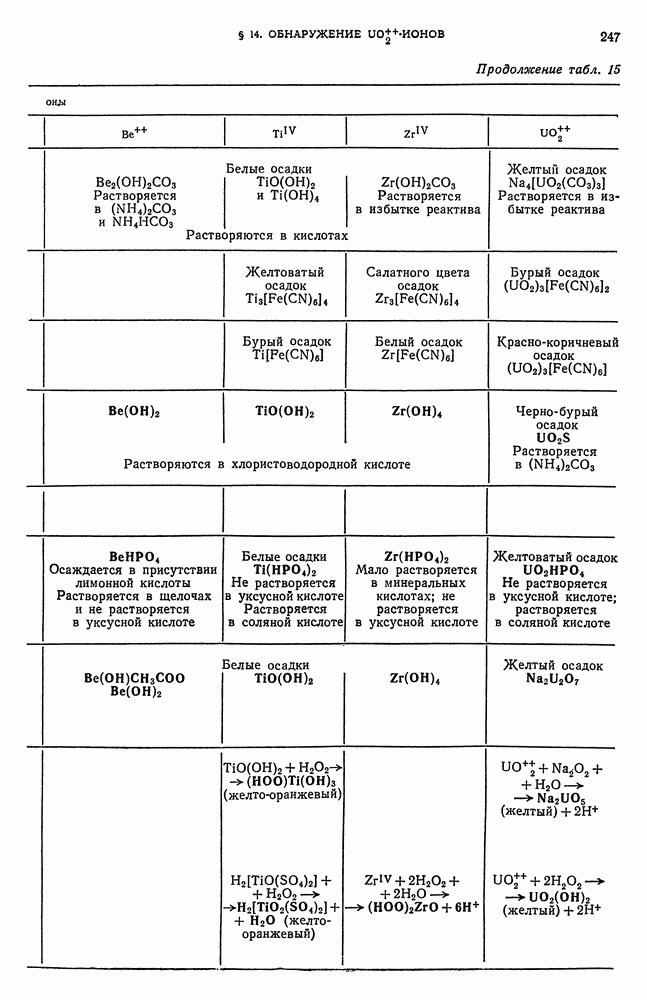
- § 14. Обнаружение UO-ионов
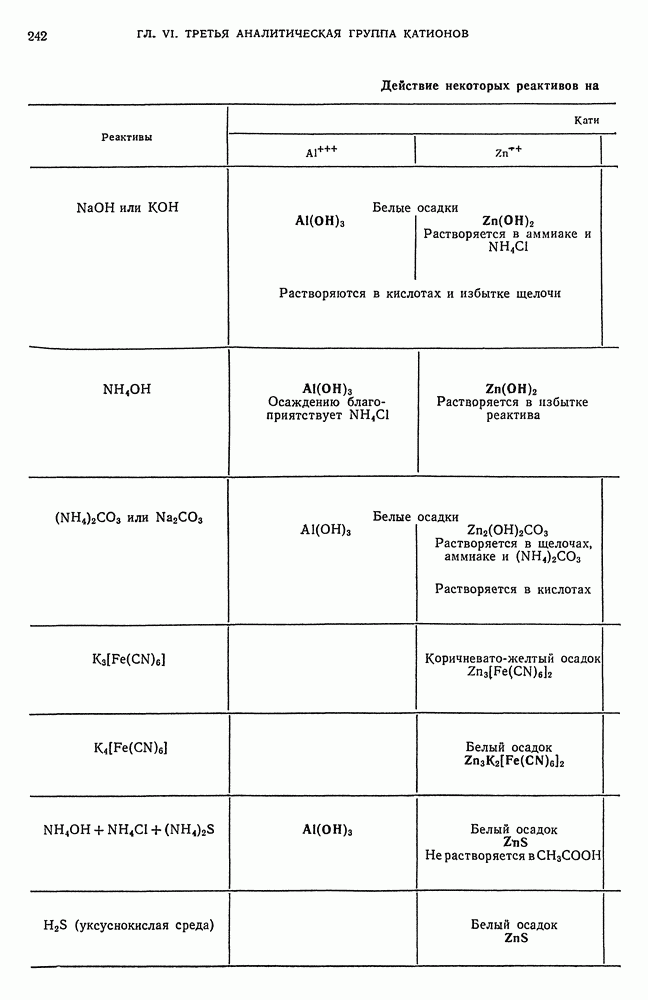
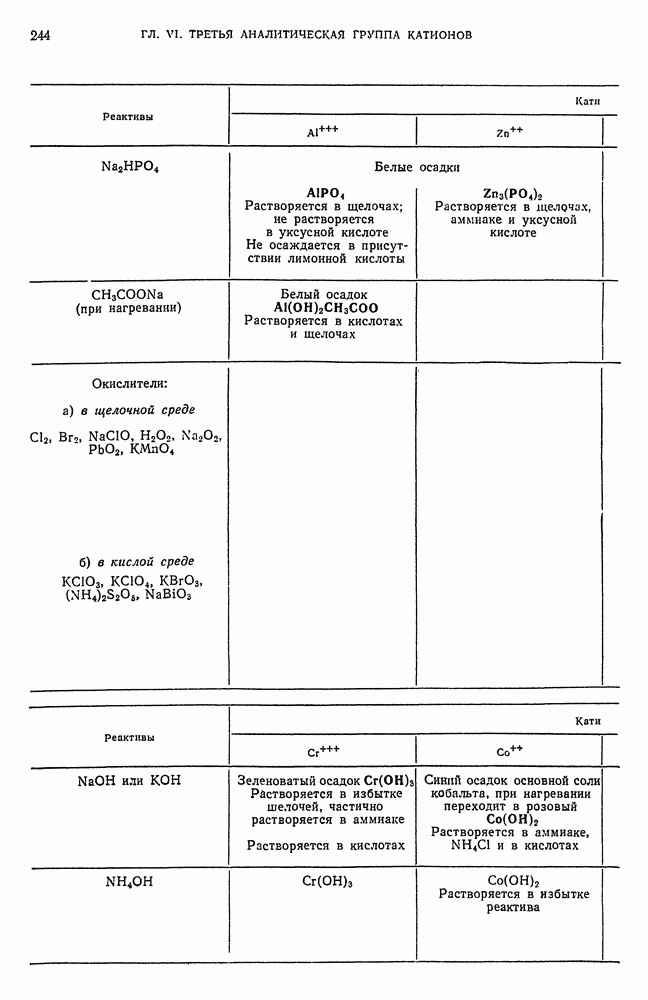
- § 15. Обзор действия реактивов на катионы третьей аналитической группы
- § 16. Использование коллоидных систем в химическом анализе
- § 17. Основы теории осаждения катионов третьей аналитической группы групповым реактивом — сульфидом аммония
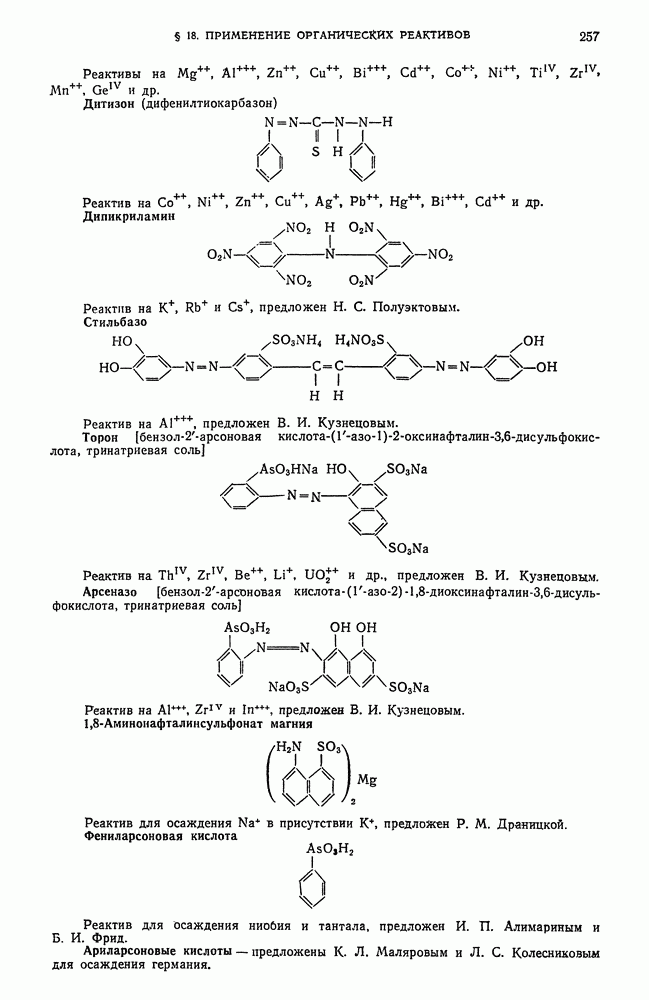
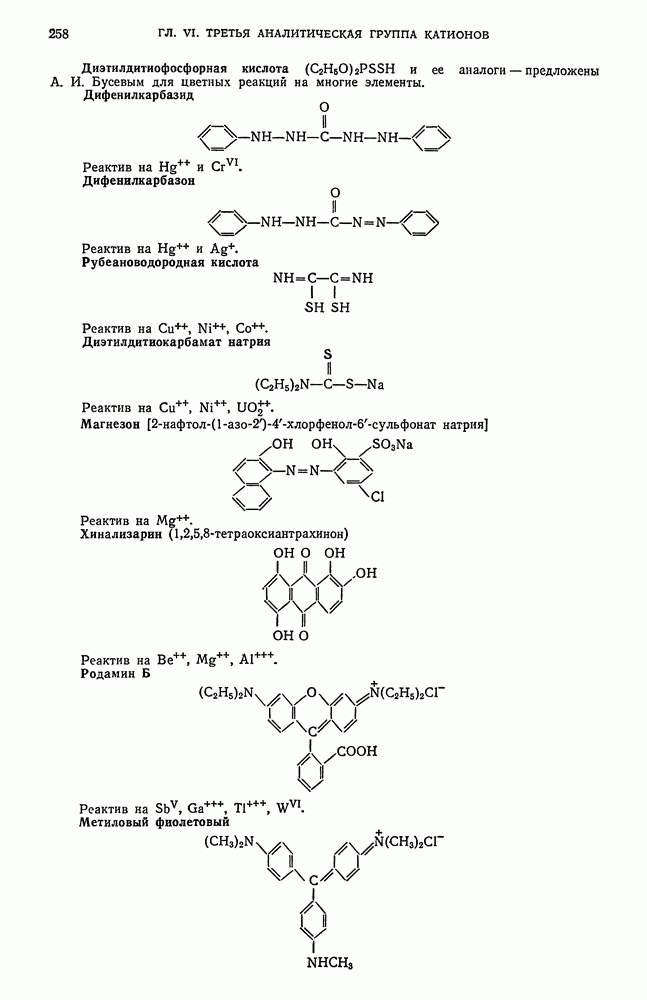
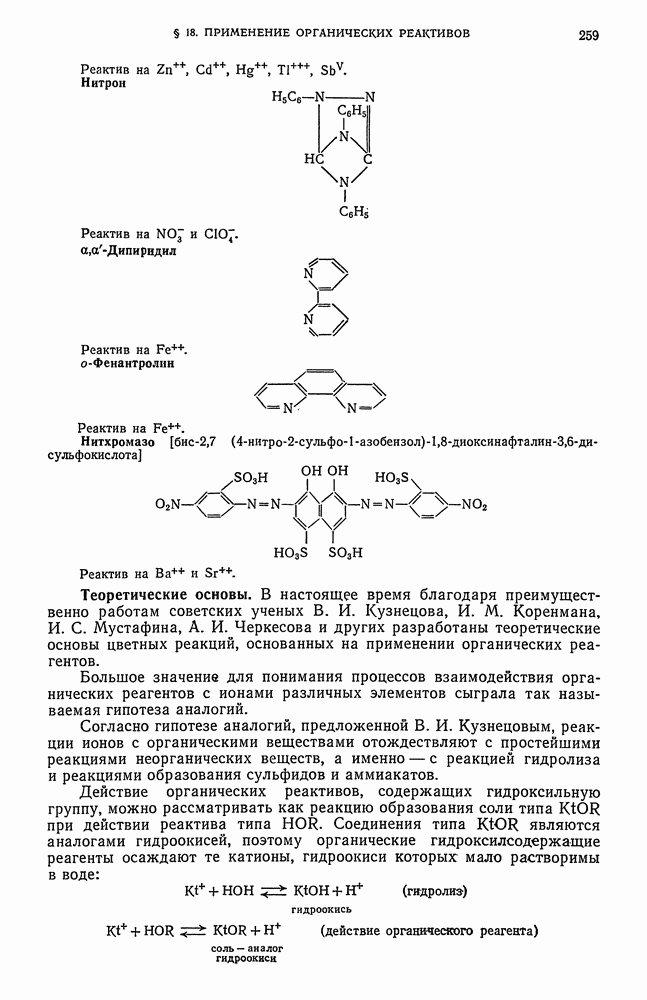
- § 18. Теоретические основы применения органических реактивов в качественном анализе неорганических веществ
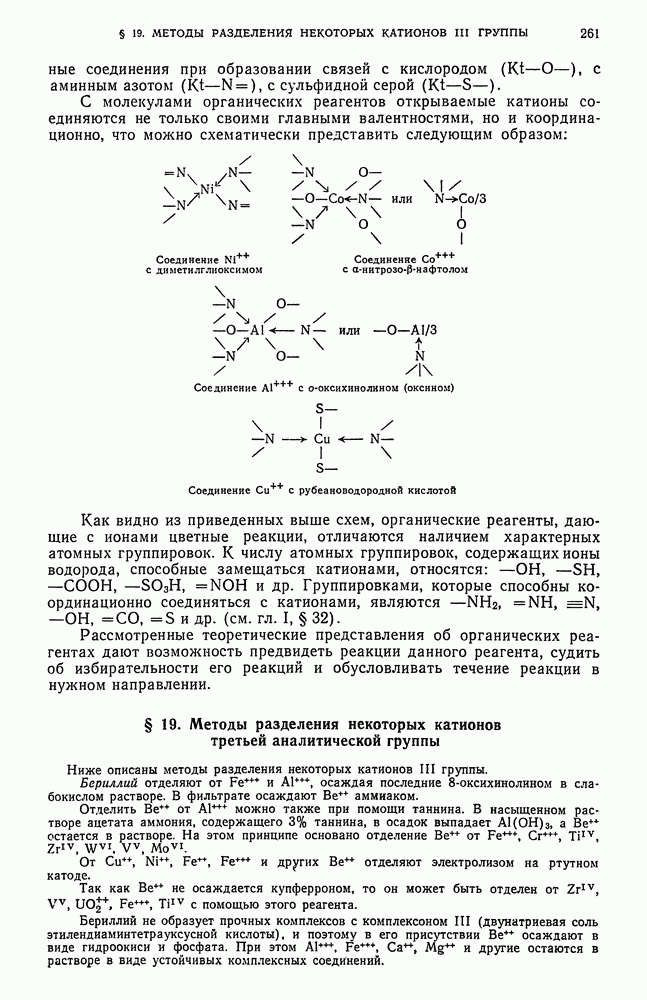
- § 19. Методы разделения некоторых катионов третьей аналитической группы
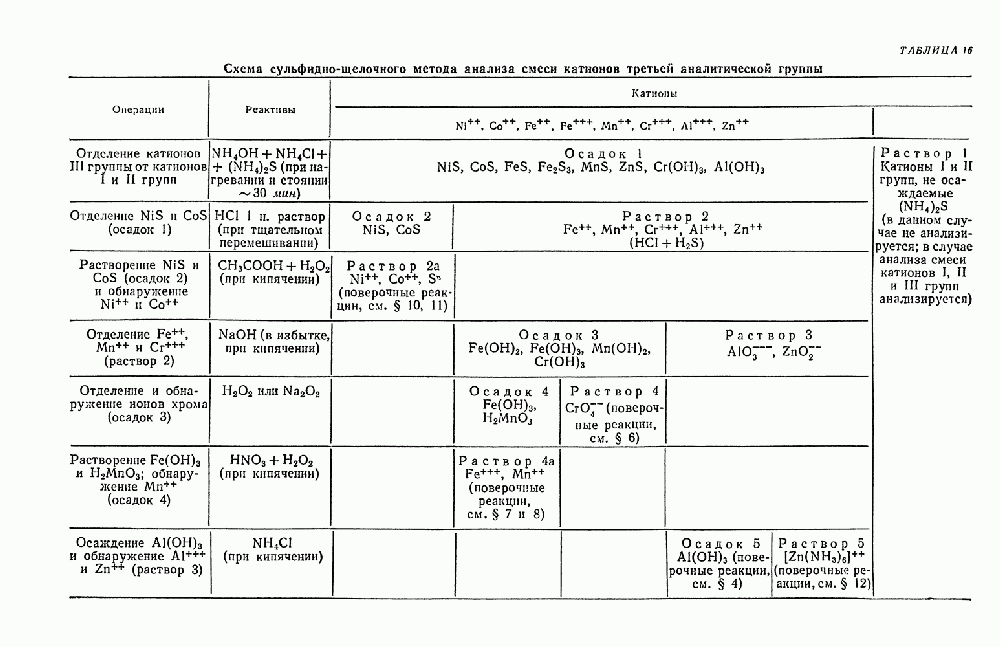
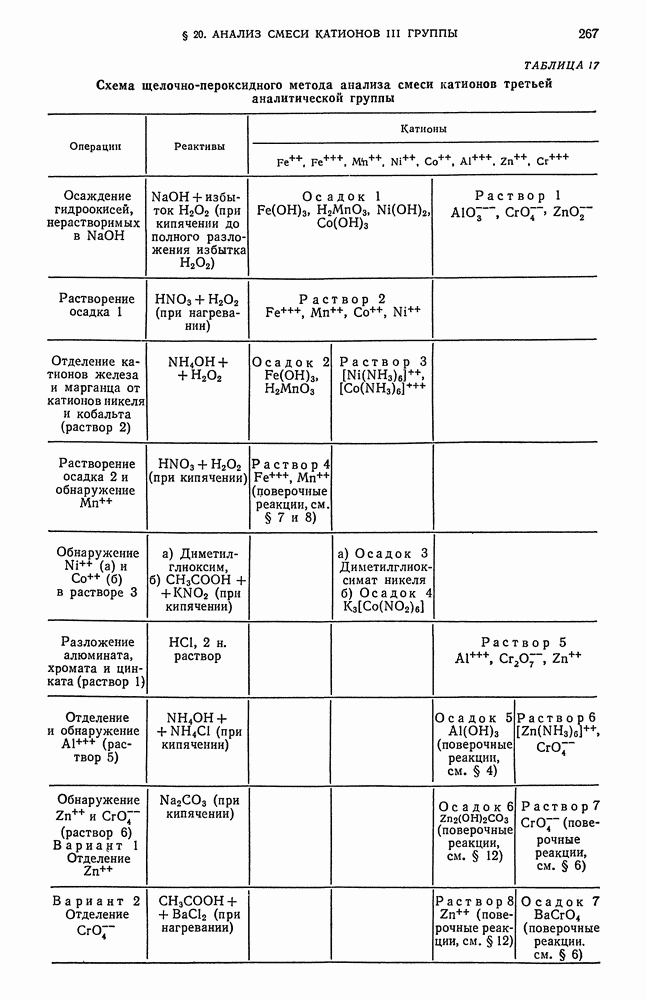
- § 20. Систематический ход анализа смеси катионов третьей аналитической группы
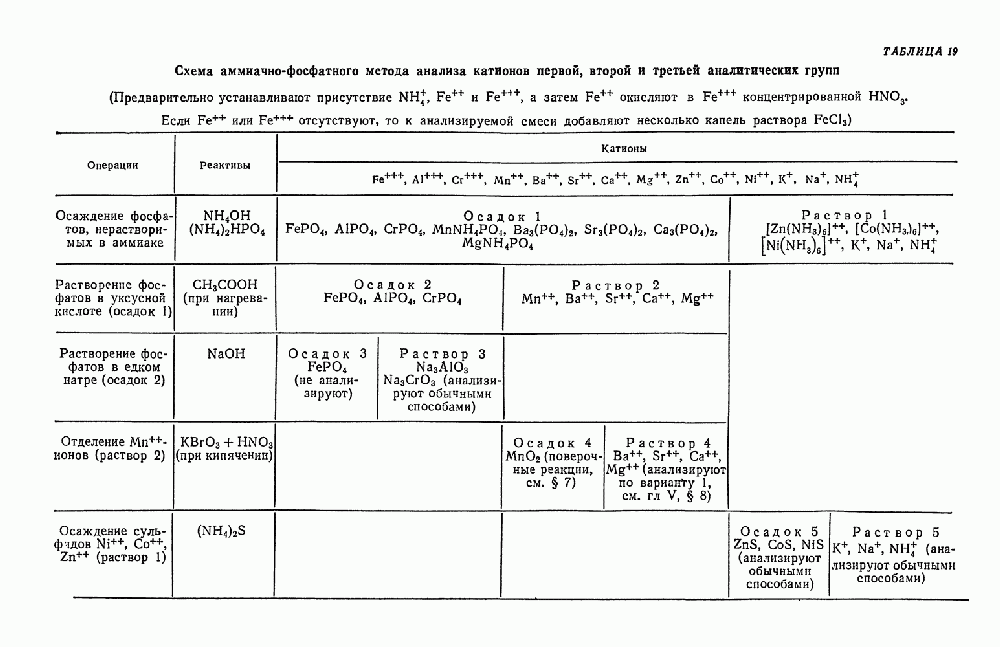
- § 21. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп
- § 22. Систематический ход анализа смеси катионов первой, второй и третьей аналитических групп в присутствии PO-ионов
- ГЛАВА VII. ЧЕТВЕРТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ
- § 1. Характеристика четвертой аналитической группы катионов
- § 2. Общие реакции катионов четвертой аналитической группы
- РЕАКЦИИ КАТИОНОВ ПЕРВОЙ ПОДГРУППЫ (ПОДГРУППЫ МЕДИ)
- § 3. Обнаружение Hg-ионов
- § 4. Обнаружение Cu-ионов
- § 5. Обнаружение Cd-ионов
- § 6. Обнаружение Bi-ионов
- РЕАКЦИИ КАТИОНОВ ВТОРОЙ ПОДГРУППЫ (ПОДГРУППЫ МЫШЬЯКА)
- § 7. Обнаружение ионов мышьяка (III)
- § 8. Обнаружение ионов мышьяка (V)
- § 9. Общие реакции обнаружения
- § 10. Обнаружение ионов сурьмы (III)
- § 11. Обнаружение ионов сурьмы (V)
- § 12. Общие реакции обнаружения Sb
- § 13. Обнаружение ионов олова (II)
- § 14. Обнаружение ионов олова (IV)
- § 15. Общие реакции обнаружения ионов олова (II) и олова (IV)
- § 16. Отделение ионов олова от других ирнов четвертой аналитической группы
- § 17. Обнаружение ионов германия (IV)
- § 18. Отделение ионов германия от других ионов четвертой аналитической группы
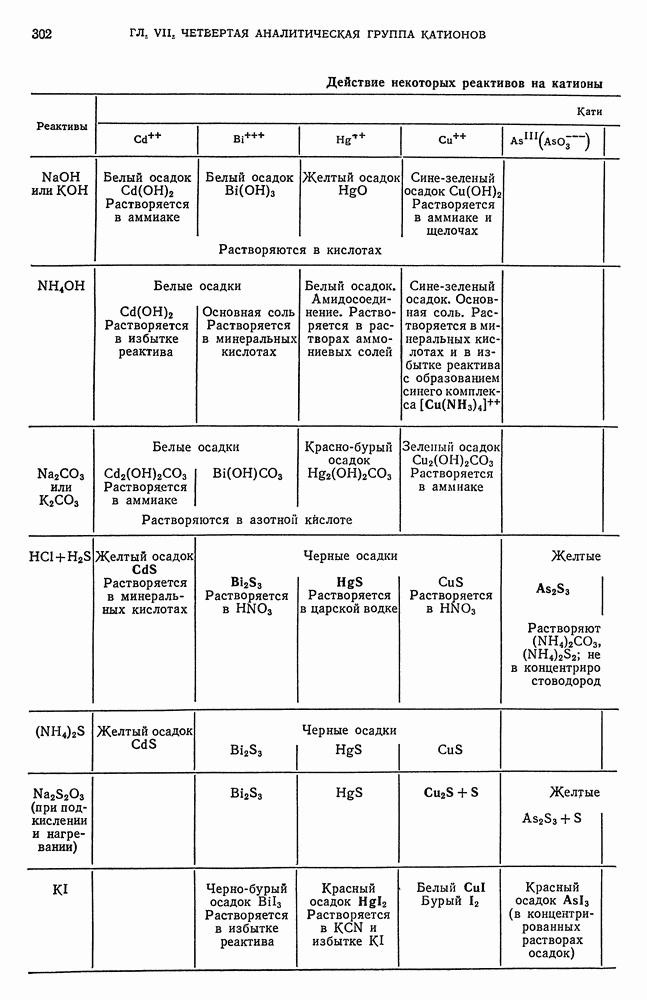
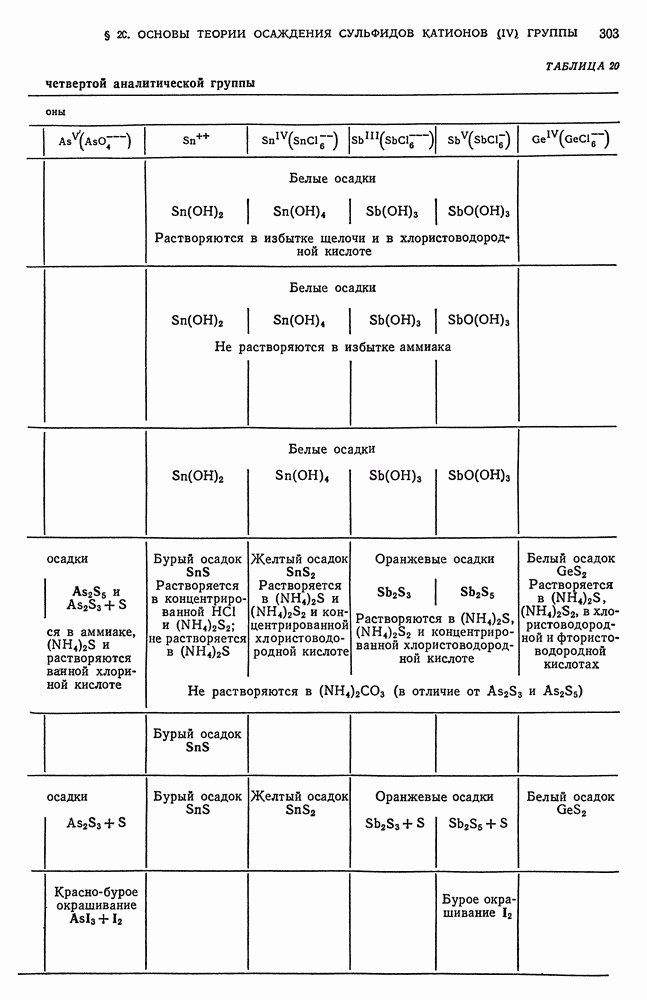
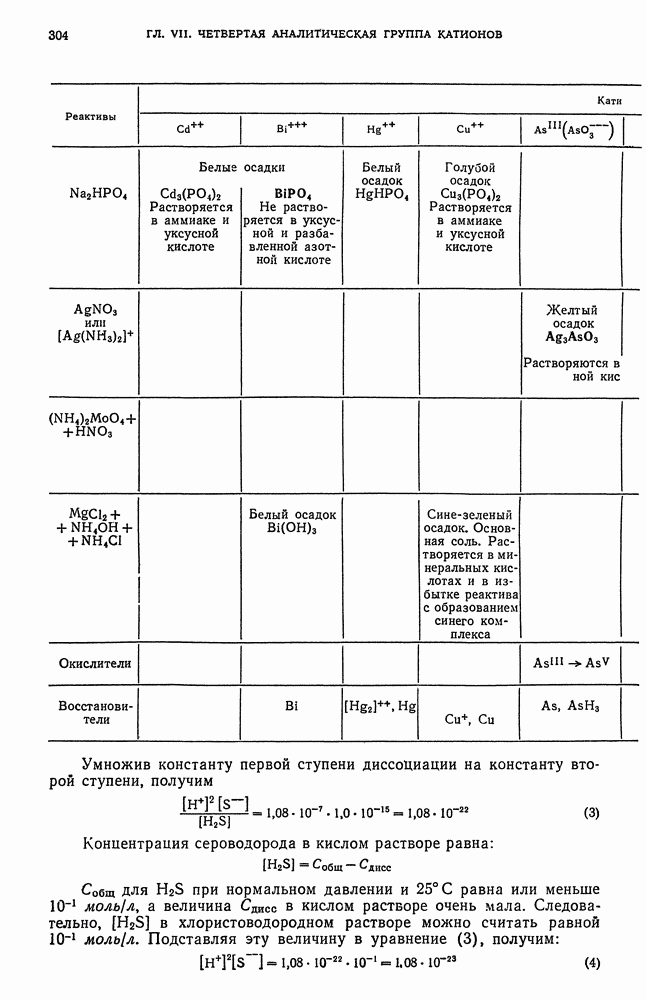
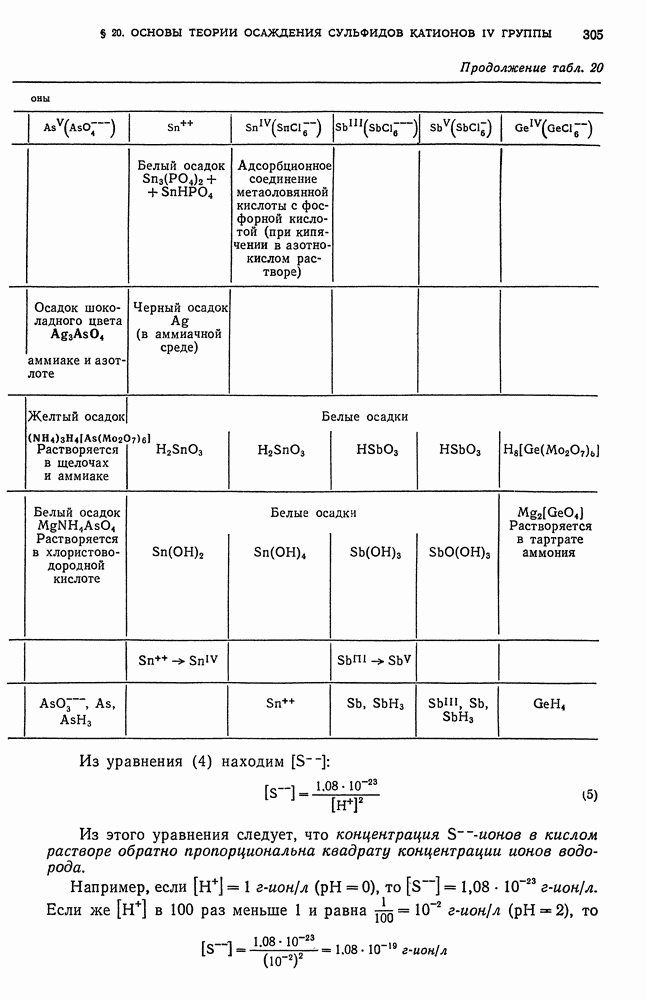
- § 19. Обзор действия реактивов на катионы четвертой аналитической группы
- § 20. Основы теории осаждения сульфидов катионов четвертой аналитической группы групповым реактивом — сероводородом
- § 21. Систематический ход анализа смеси катионов четвертой аналитической группы
- ГЛАВА VIII. ПЯТАЯ АНАЛИТИЧЕСКАЯ ГРУППА КАТИОНОВ (ГРУППА СЕРЕБРА)
- § 1. Характеристика пятой аналитической группы катионов
- § 2. Общие реакции катионов пятой аналитической группы
- § 3. Обнаружение Ag-ионов
- § 4. Обнаружение [Hg]-ионов
- § 5. Обнаружение Pb-ионов
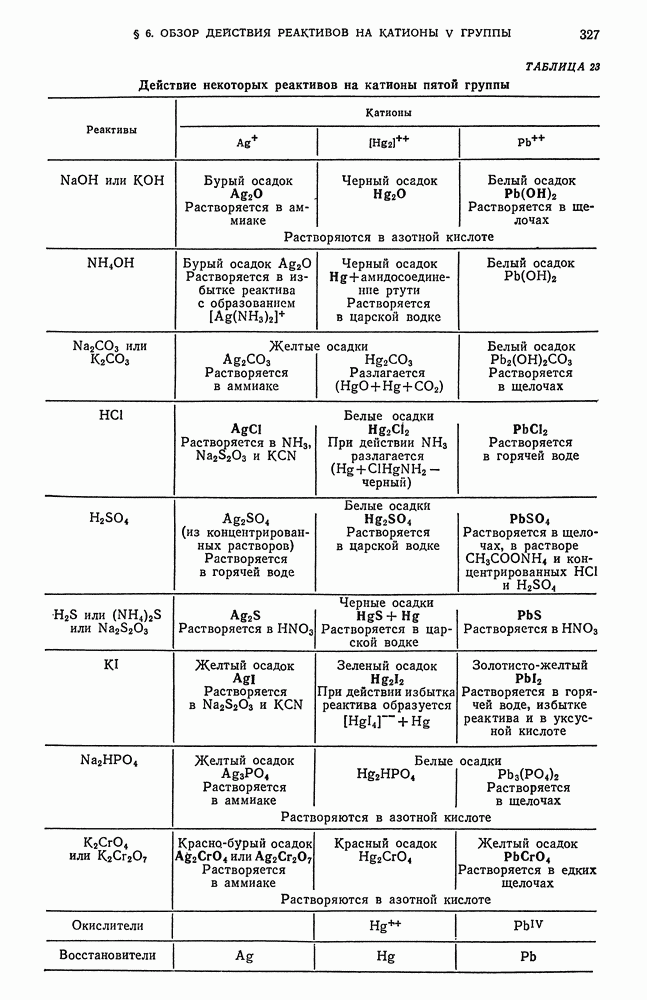
- § 6. Обзор действия реактивов на катионы пятой аналитической группы
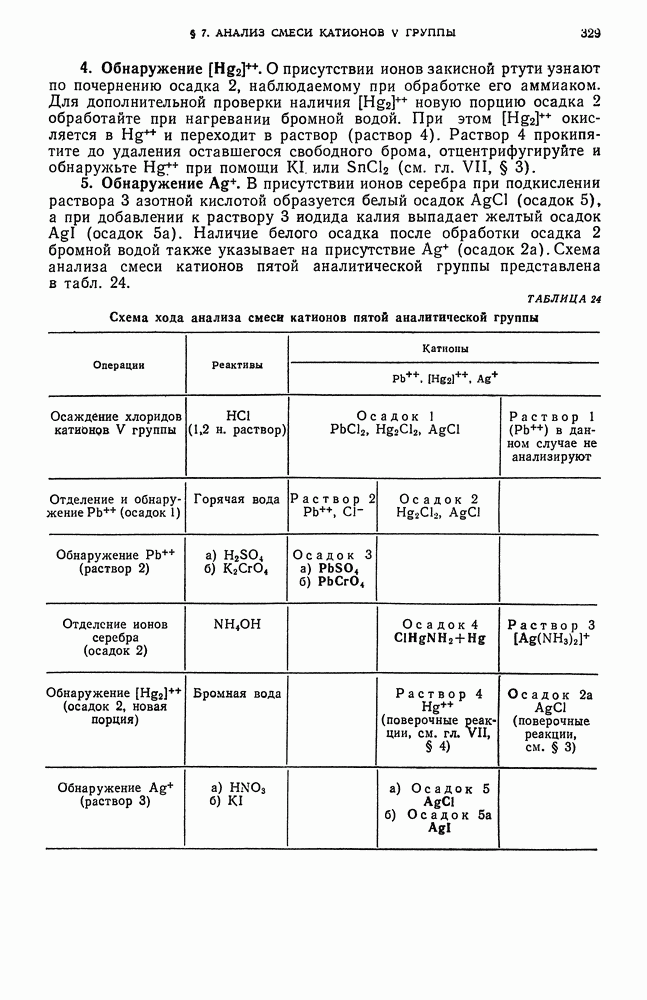
- § 7. Систематический ход анализа смеси катионов пятой аналитической группы
- ГЛАВА IX. АНАЛИЗ СМЕСИ ИОНОВ ВСЕХ ПЯТИ АНАЛИТИЧЕСКИХ ГРУПП
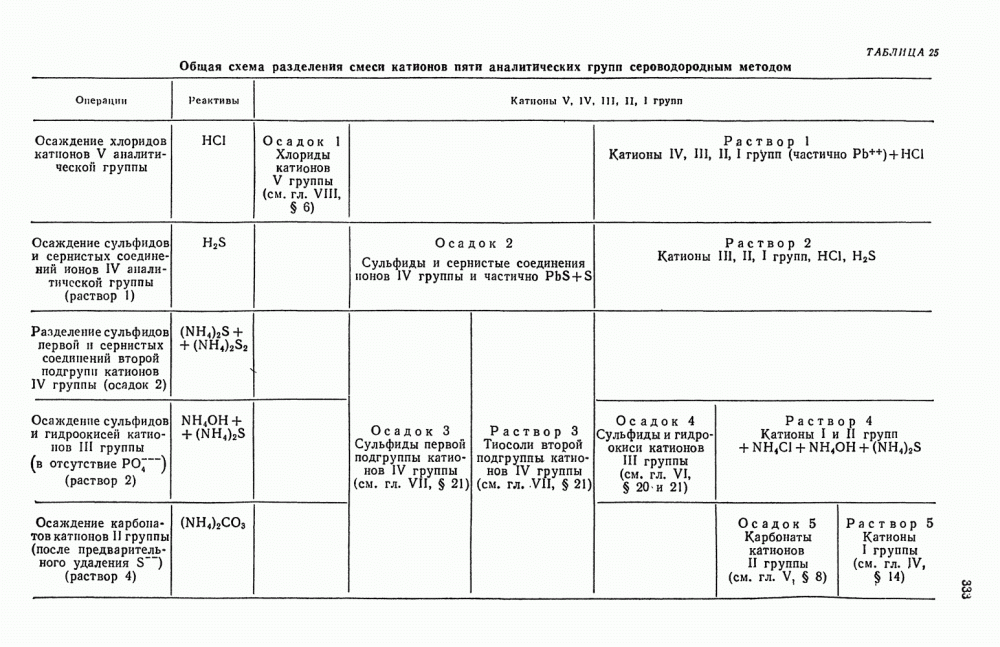
- § 1. Сероводородный метод анализа
- § 2. Недостатки сероводородного метода анализа
- § 3. Ошибки, возникающие при анализе смеси ионов пяти аналитических групп
- § 4. Бессероводородные методы анализа
- ОБНАРУЖЕНИЕ ИНДИВИДУАЛЬНЫХ АНИОНОВ И АНАЛИЗ СМЕСЕЙ АНИОНОВ
- § 1. Аналитическая классификация анионов
- § 2. Групповые реактивы на анионы
- § 3. Классификация методов анализа анионов
- ГЛАВА XI. ПЕРВАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика первой группы анионов
- § 2. Реакции анионов первой группы
- § 3. Обнаружение CI-ионов
- § 4. Обнаружение Br-ионов
- § 5. Обнаружение I-ионов
- § 6. Обнаружение CN-ионов
- § 7. Обнаружение SCN-ионов
- § 8. Обнаружение [Fe(CN)]-ионов
- § 9. Обнаружение Fe(CN)-ионов
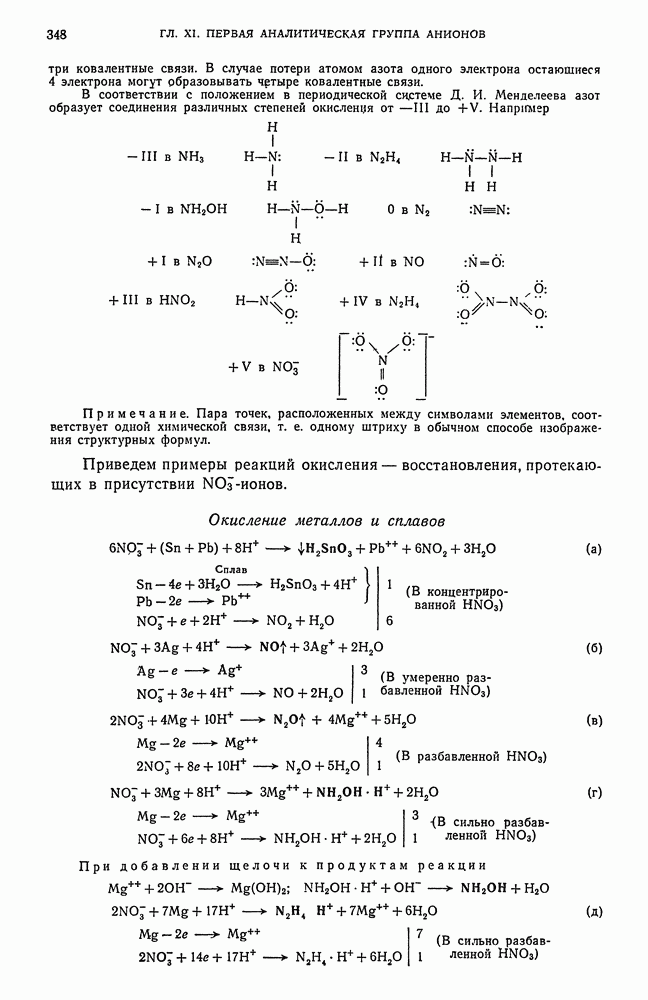
- § 10. Обнаружение NO-ионов
- § 11. Обнаружение NO2-ионов
- § 12. Обнаружение S-ионов
- § 13. Обнаружение CH3COOO-ионов
- § 14. Обнаружение BrO3-ионов
- § 15. Обнаружение ClO3-ионов
- § 16. Обнаружение ClO4-ионов
- § 17. Обзор действия реактивов на анионы первой группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 18. Анализ смеси Cl, Br и I-ионов
- § 19. Анализ смеси Cl, Br, I и SCN-ионов
- § 20. Анализ смеси Cl, ClO3 и ClO4-ионов
- § 21. Анализ смеси NO2 и NO3-ионов
- § 22. Анализ смеси анионов первой группы
- ГЛАВА XII. ВТОРАЯ АНАЛИТИЧЕСКАЯ ГРУППА АНИОНОВ
- § 1. Характеристика второй группы анионов
- § 2. Общие реакции анионов второй группы
- § 3. Обнаружение SO3-ионов
- § 4. Обнаружение S2O3-ионов
- § 5. Обнаружение S2O3 в присутствии SO3-ионов
- § 6. Обнаружение SO4-ионов
- § 7. Обнаружение CO3-ионов
- § 8. Обнаружение CO3-ионов в присутствии SO3 и S2O3-ионов
- § 9. Обнаружение PO4-ионов
- § 10. Обнаружение CrO4-ионов
- § 11. Обнаружение AsO3-ионов
- § 12. Обнаружение AsO4-ионов
- § 13. Обнаружение BO2 и BO3-ионов
- § 14. Обнаружение SiO3-ионов
- § 15. Обнаружение F-ионов
- § 16. Обнаружение C2O4-ионов
- § 17. Обнаружение VO3-ионов
- § 18. Обнаружение MoO4-ионов
- § 19. Обнаружение WO4-ионов
- § 20. Обзор действия реактивов на анионы второй группы
- МЕТОДЫ АНАЛИЗА НЕКОТОРЫХ СМЕСЕЙ АНИОНОВ
- § 21. Анализ смеси ионов
- § 22. Анализ смеси SO3, SO4, S2O3 и CO3-ионов
- § 23. Анализ смеси VO2, MoO4 и WO4-ионов
- § 24. Анализ смеси анионов второй группы
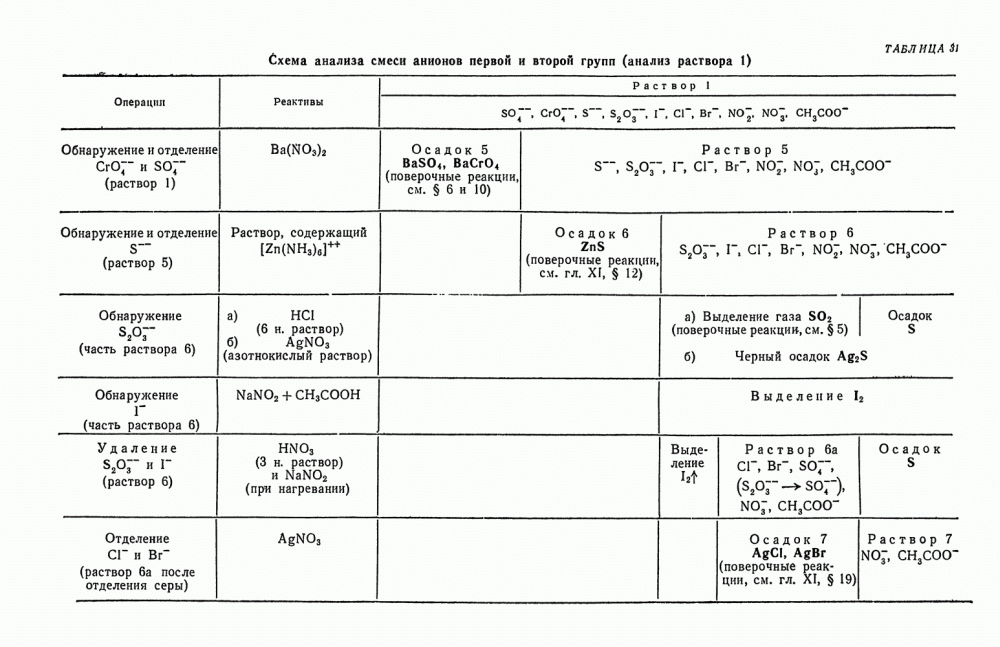
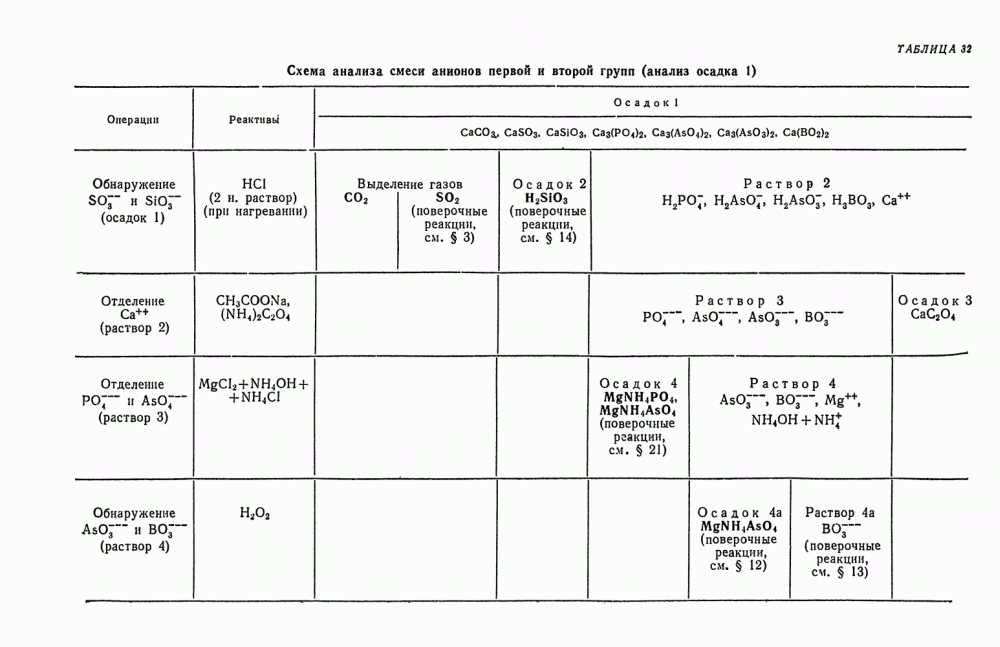
- § 25. Анализ смеси анионов первой и второй групп
- ГЛАВА XIII. ОБНАРУЖЕНИЕ СВОБОДНЫХ МЕТАЛЛОВ И НЕМЕТАЛЛОВ, ИДЕНТИФИЦИРОВАНИЕ СОЛЕЙ И ДРУГИХ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И АНАЛИЗ ИХ СМЕСЕЙ
- § 1. Подготовка вещества к анализу
- § 2. Предварительные испытания
- § 3. Растворение анализируемого вещества в воде, кислотах и щелочах
- § 4. Переведение в растворимое состояние веществ, нерастворимых в воде, кислотах и щелочах
- § 5. Анализ неизвестного вещества
- § 6. Обнаружение свободных элементов
- § 7. Идентифицирование солей и других индивидуальных соединений
- § 8. Обнаружение микропримесей
- § 9. Анализ сплавов
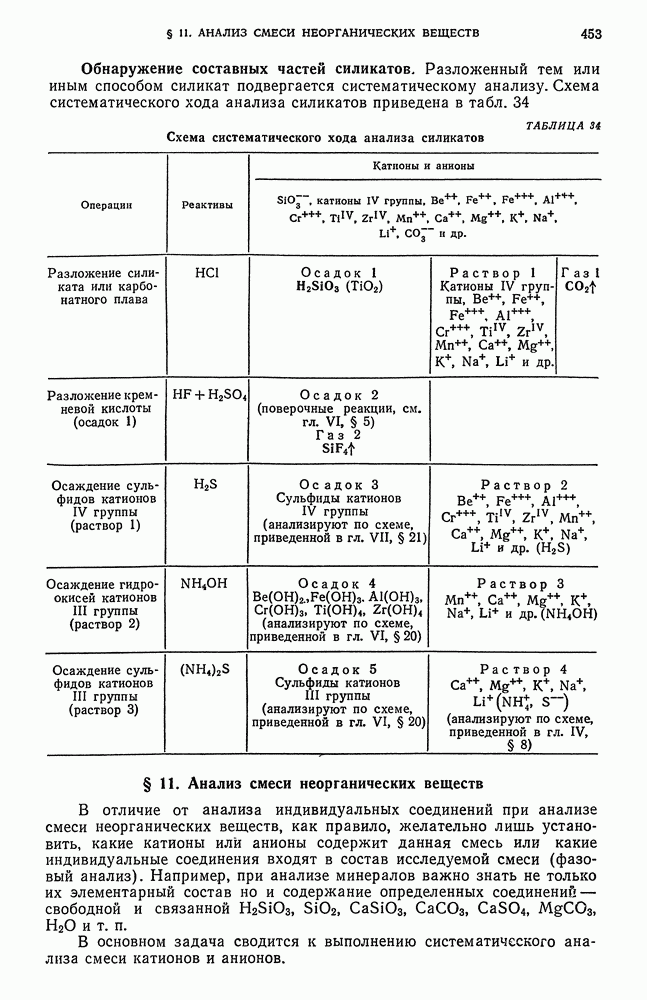
- § 10. Анализ силикатов и алюмосиликатов
- § 11. Анализ смеси неорганических веществ
- § 12. Экспрессный метод анализа смесей катионов и анионов
- § 13. Идентифицирование нерастворимых веществ
- ЛИТЕРАТУРА