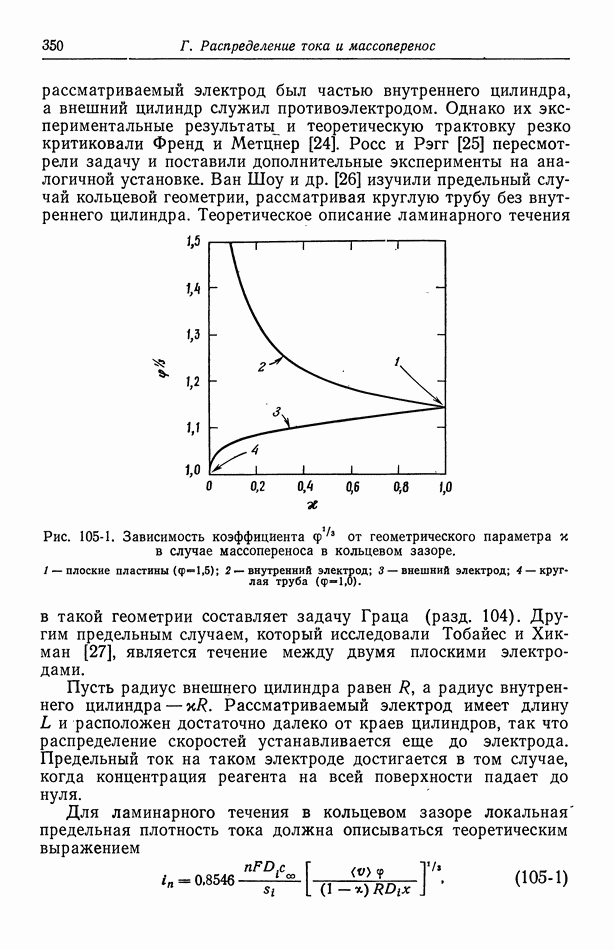
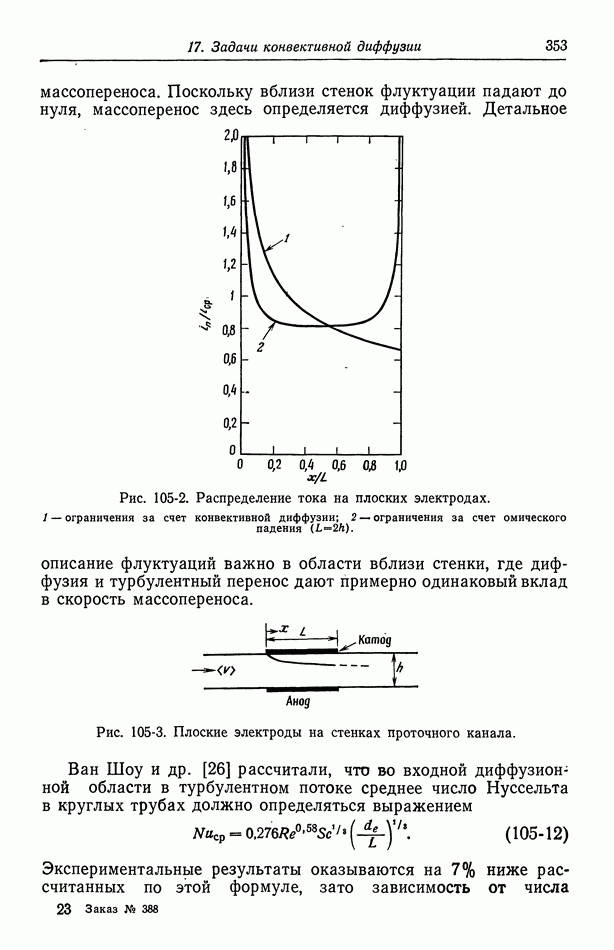
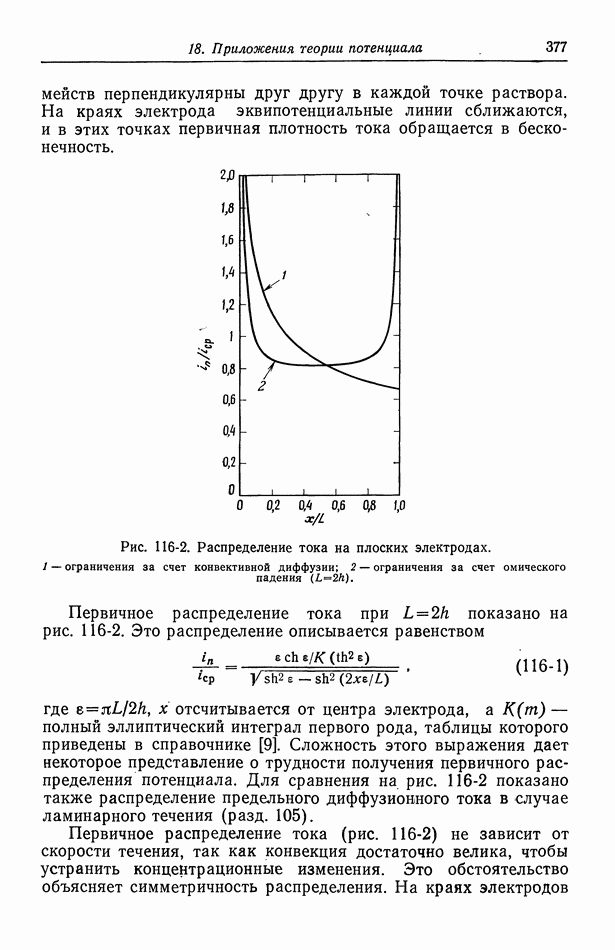
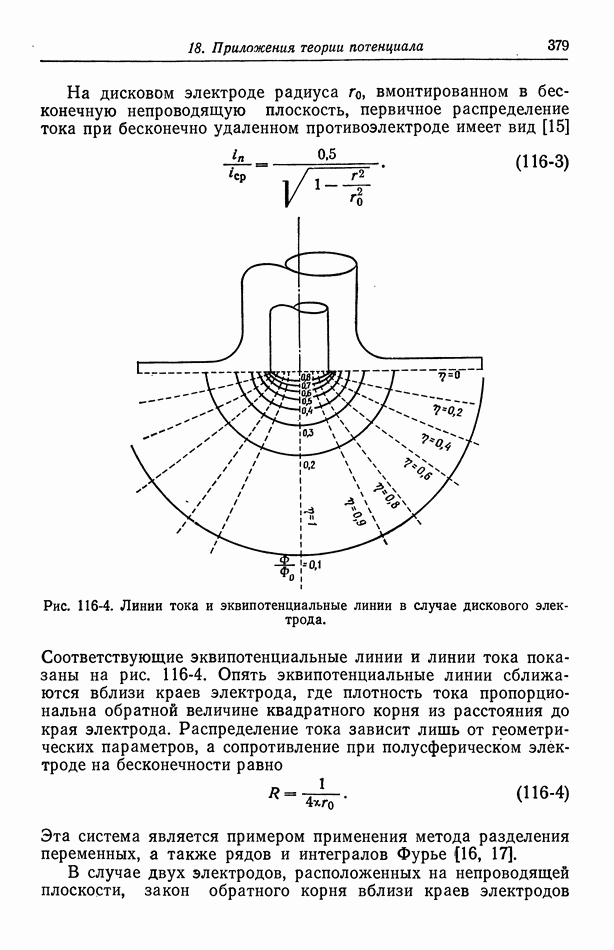
| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
10. Фоновый электролит
Мы провели довольно подробное обсуждение явлений, связанных с прохождением тока через раствор, содержащий сульфат меди. На практике принято добавлять инертный электролит, не участвующий в электродных реакциях, главным образом
для того, чтобы увеличить проводимость и тем самым уменьщить омическое падение потенциала. Например, раствор  будет иметь проводимость около
будет иметь проводимость около  Тогда равенство (3-11) дает сопротивление, равное лишь 0,0118 Ом, в противоположность величине 0,74 Ом для 0,1 М раствора
Тогда равенство (3-11) дает сопротивление, равное лишь 0,0118 Ом, в противоположность величине 0,74 Ом для 0,1 М раствора  не содержащего серной кислоты.
не содержащего серной кислоты.
Вторым следствием добавления серной кислоты будет уменьшение вклада миграции в поток ионов меди. Поскольку электрическое поле значительно уменьшается, миграция становится несущественной по сравнению с диффузией и конвекцией. Следовательно, предельный ток осаждения меди на катоде также будет меньшим. Учитывая должным образом изменения коэффициентов вязкости и диффузии при добавлении серной кислоты, находим теперь, что предельный ток равен  при скорости вращения 900 об/мин в противоположность току
при скорости вращения 900 об/мин в противоположность току  полученному в разд. 5.
полученному в разд. 5.
В присутствии избытка серной кислоты мы должны были бы выразить концентрационное перенапряжение в приближенной форме

вместо того, чтобы пользоваться равенством  Здесь можно пренебречь изменением проводимости в диффузионном слое; кроме того, пренебрежение поправками на коэффициенты активности в данном случае более оправдано, чем в случае раствора одного лишь сульфата меди. Наконец, можно ожидать, что добавление серной кислоты изменит параметры, используемые для описания кинетики электродных процессов.
Здесь можно пренебречь изменением проводимости в диффузионном слое; кроме того, пренебрежение поправками на коэффициенты активности в данном случае более оправдано, чем в случае раствора одного лишь сульфата меди. Наконец, можно ожидать, что добавление серной кислоты изменит параметры, используемые для описания кинетики электродных процессов.
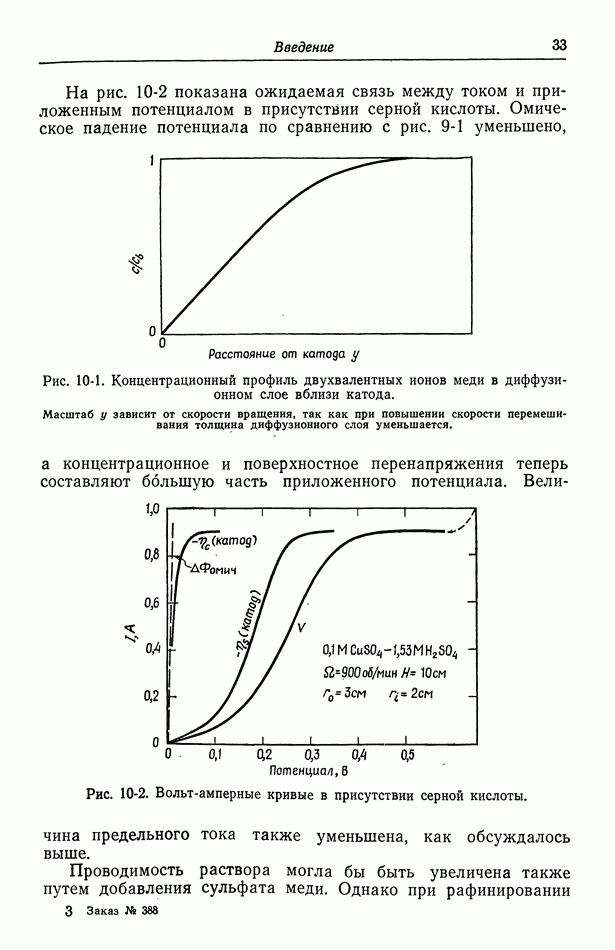
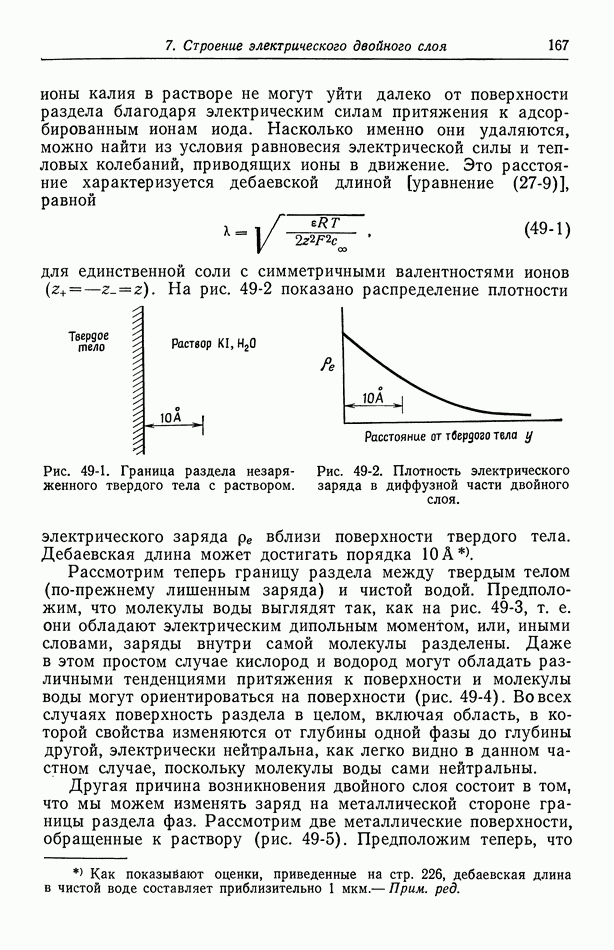
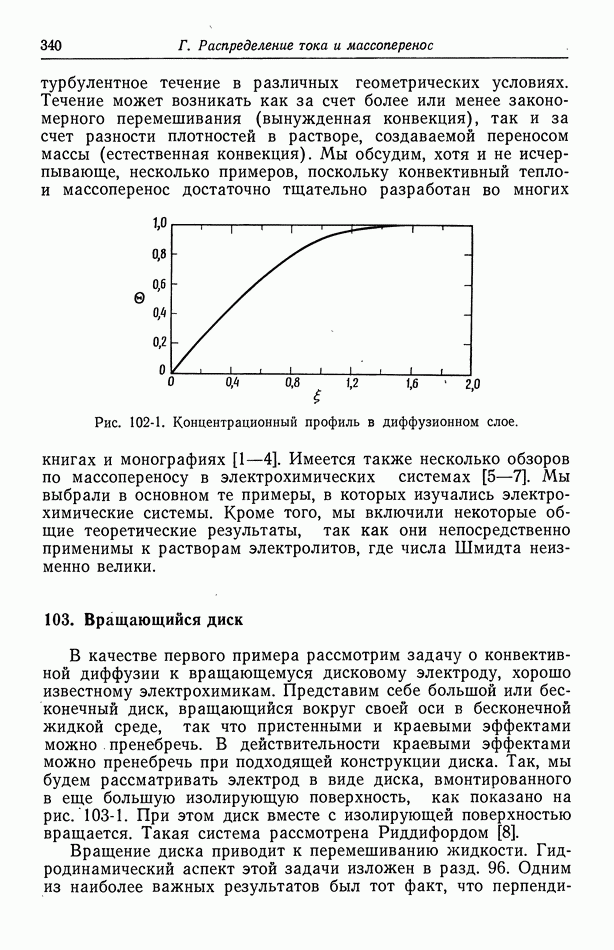
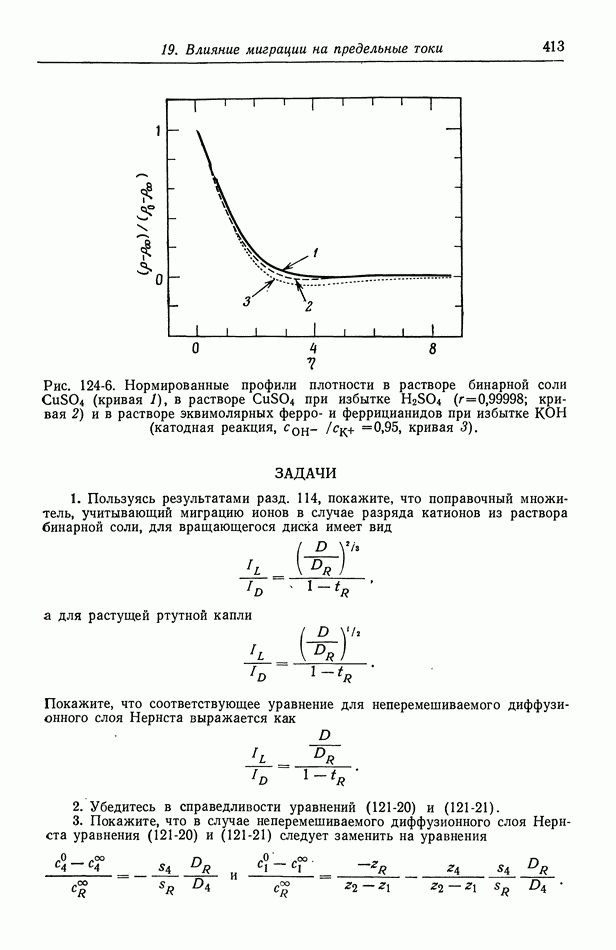
На рис. 10-1 показан концентрационный профиль двухвалентных ионов меди в диффузионном слое вблизи катода. Если серная кислота не добавлялась, то и миграция, и диффузия будут стремиться двигать катионы к электроду, так как в эту сторону направлено электрическое поле и концентрация уменьшается по направлению к электроду. Вдали от электрода преобладает конвективный транспорт, а концентрация становится однородной. Вследствие истощения раствора электрическое поле вблизи электрода повышено, и роль миграции возрастает, хотя концентрация понижается [миграционный поток пропорционален электрическому полю, умноженному на концентрацию; см. равенство (5-2)]. Равенство  содержит вклад миграции в случае раствора лишь одного электролита. Добавление серной кислоты уменьшает электрическое поле и эффективно устраняет миграционный вклад. Это уменьшает предельный ток или скорость транспорта ионов меди при заданном режиме конвекции.
содержит вклад миграции в случае раствора лишь одного электролита. Добавление серной кислоты уменьшает электрическое поле и эффективно устраняет миграционный вклад. Это уменьшает предельный ток или скорость транспорта ионов меди при заданном режиме конвекции.
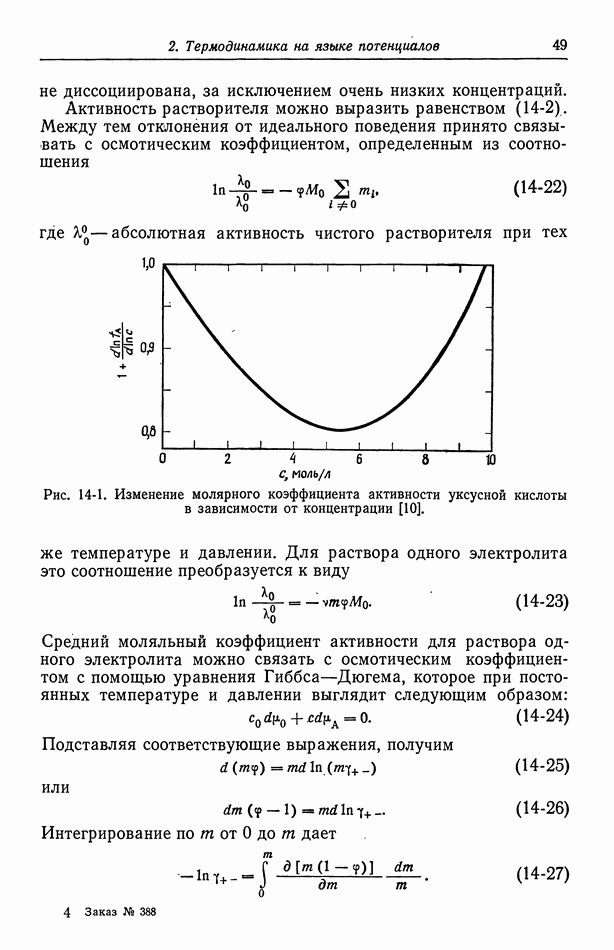
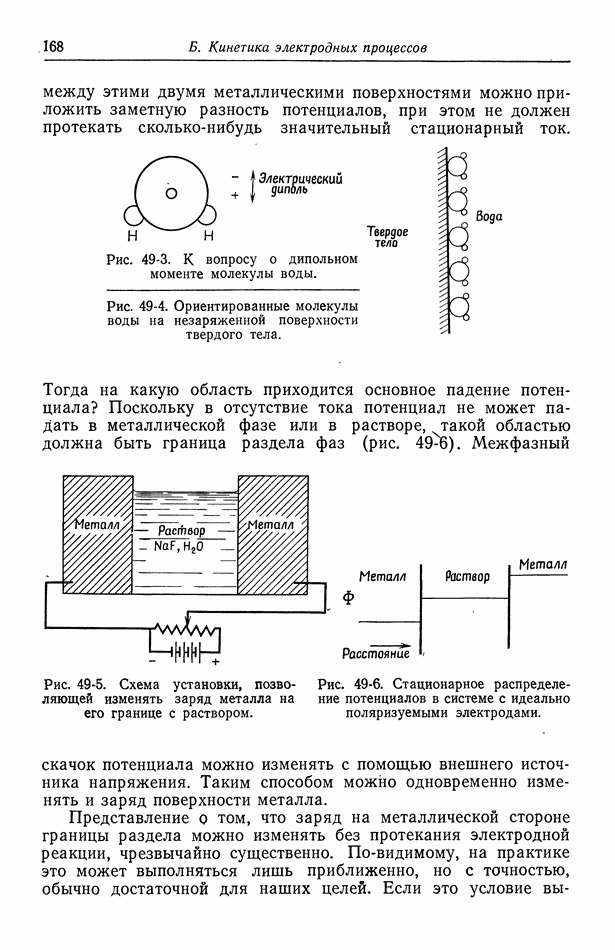
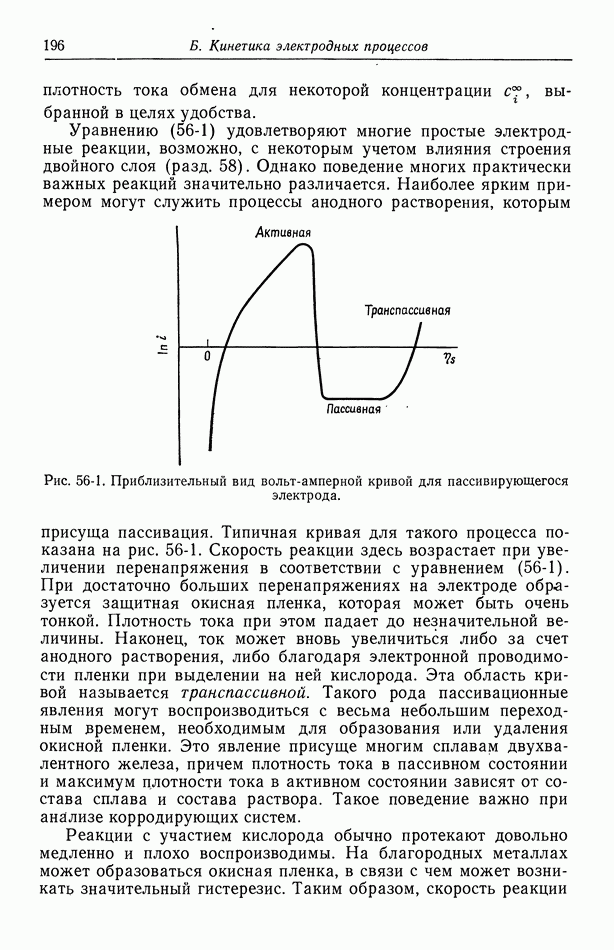
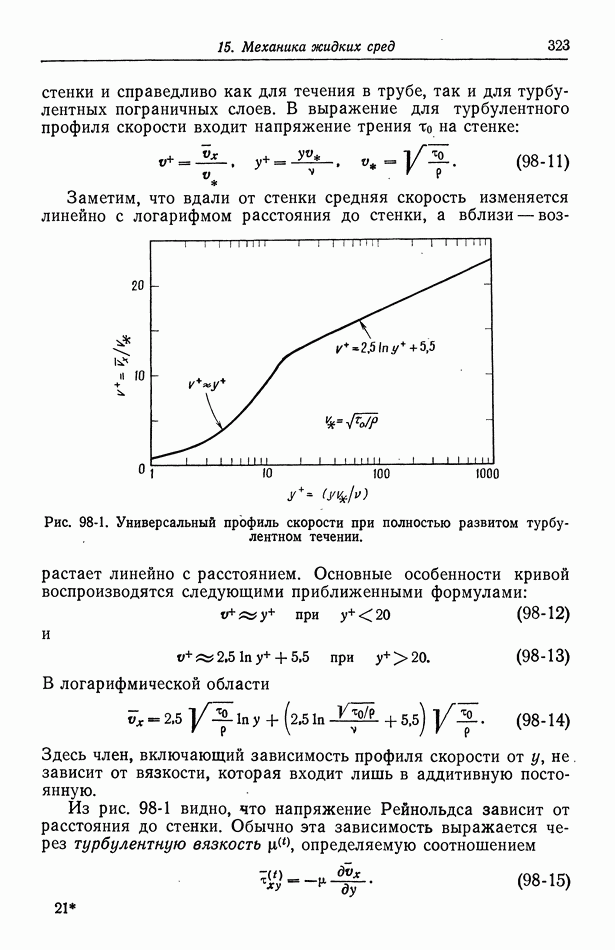
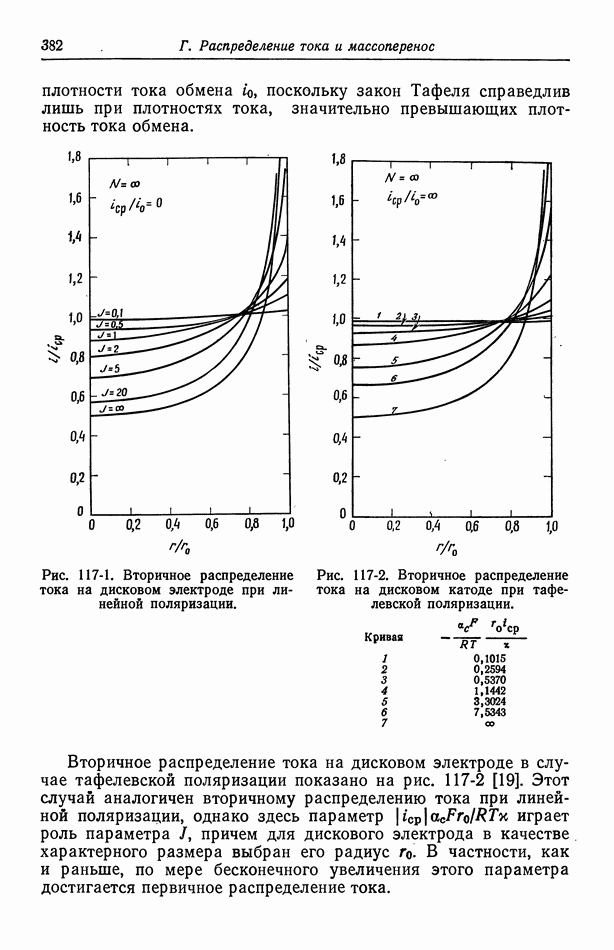
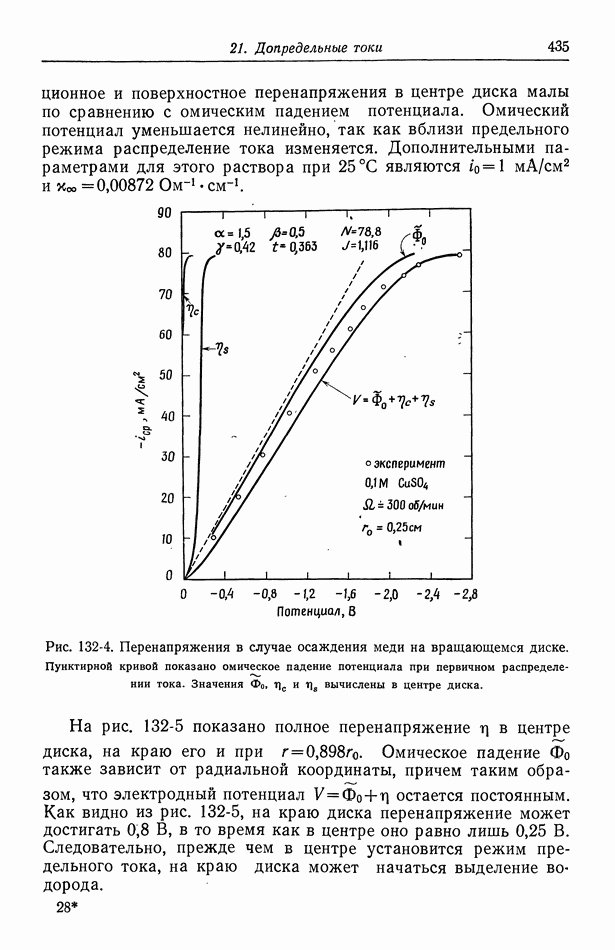
На рис. 10-2 показана ожидаемая связь между током и приложенным потенциалом в присутствии серной кислоты. Омическое падение потенциала по сравнению с рис. 9-1 уменьшено, а концентрационное и поверхностное перенапряжения теперь составляют большую часть приложенного потенциала.

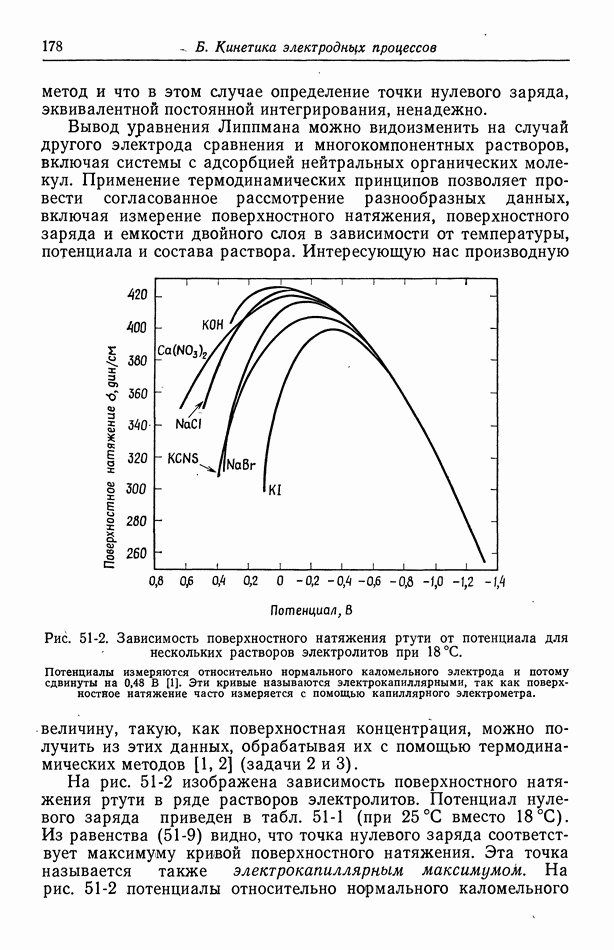
Рис. 10-1. Концентрационный профиль двухвалентных ионов меди в диффузионном слое вблизи катода.
Масштаб у зависит от скорости вращения, так как при повышении скорости перемешивания толщина диффузионного слоя уменьшается.
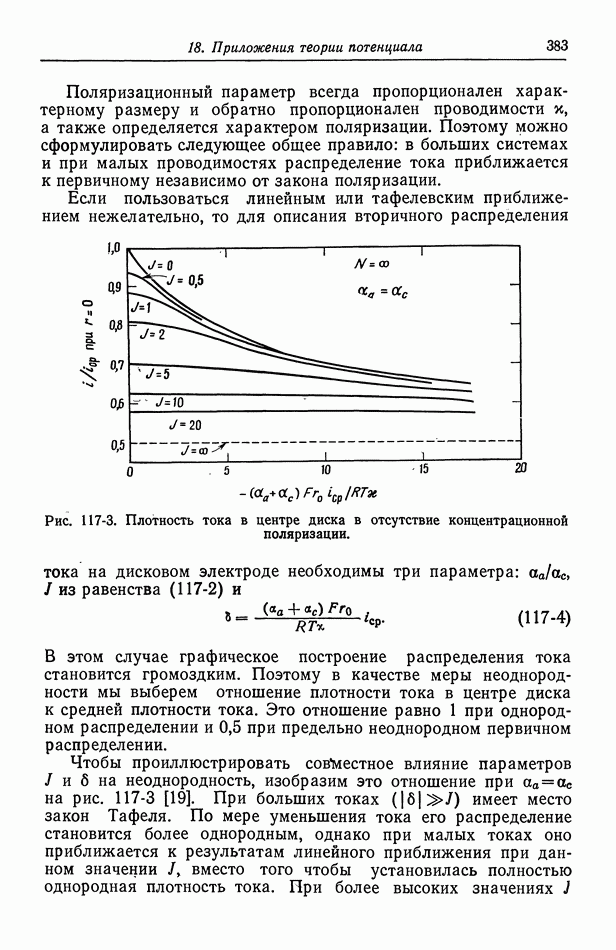
Величина предельного тока также уменьшена, как обсуждалось выше.

Рис. 10-2. Вольт-амперные кривые в присутствии серной кислоты.
Проводимость раствора могла бы быть увеличена также путем добавления сульфата меди. Однако при рафинировании
благородных металлов желательно поддерживать концентрацию в системе на низком уровне. Кроме того, растворимость сульфата меди составляет лишь  Чтобы избежать пересыщения на аноде, можно было бы установить верхний предел концентрации
Чтобы избежать пересыщения на аноде, можно было бы установить верхний предел концентрации  при котором проводимость составляет лишь
при котором проводимость составляет лишь  . В электроаналитической химии, в исследованиях кинетики электродных процессов и массопереноса обычно используется избыток фонового электролита. Причина этого состоит не только в том, что изменения потенциала в растворе оказываются небольшими; существенно и то, что коэффициенты активности, транспортные свойства и даже свойства межфазной границы мало изменяются при небольших изменениях концентрации реагента.
. В электроаналитической химии, в исследованиях кинетики электродных процессов и массопереноса обычно используется избыток фонового электролита. Причина этого состоит не только в том, что изменения потенциала в растворе оказываются небольшими; существенно и то, что коэффициенты активности, транспортные свойства и даже свойства межфазной границы мало изменяются при небольших изменениях концентрации реагента.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ
- Глава 1. ВВЕДЕНИЕ
- 1. Термодинамика, кинетика электродных процессов и процессы переноса
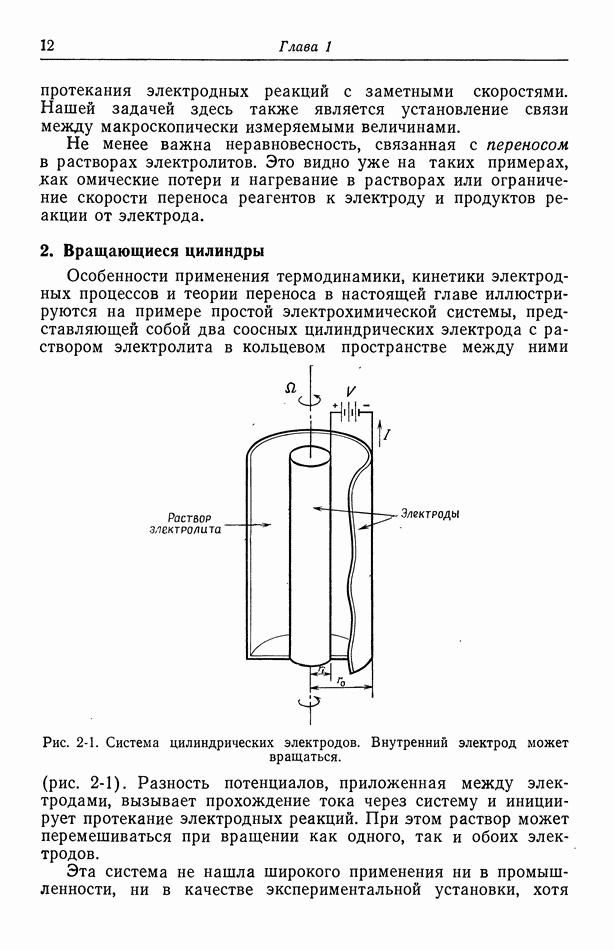
- 2. Вращающиеся цилиндры
- 3. Прохождение тока в электролитах
- 4. Течение жидкости
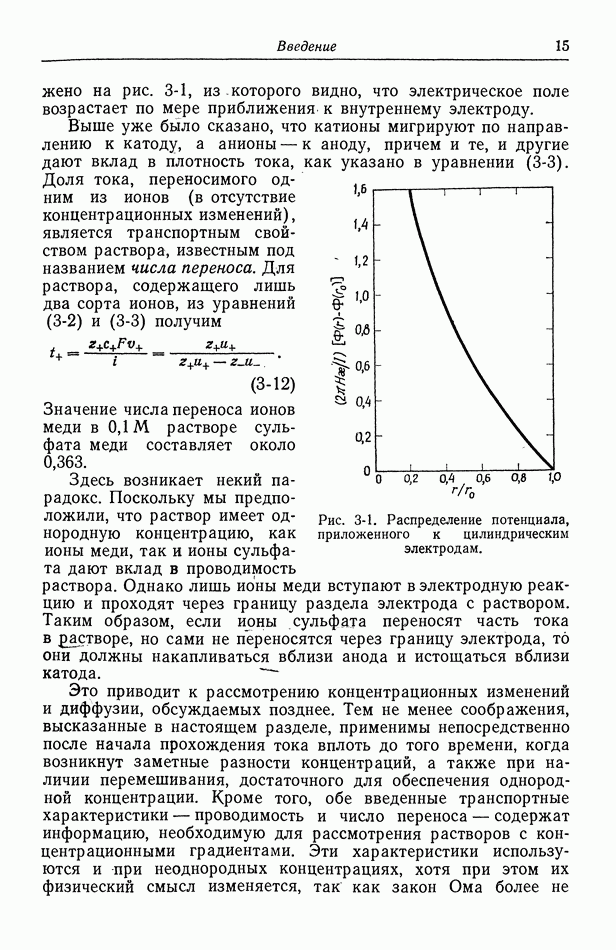
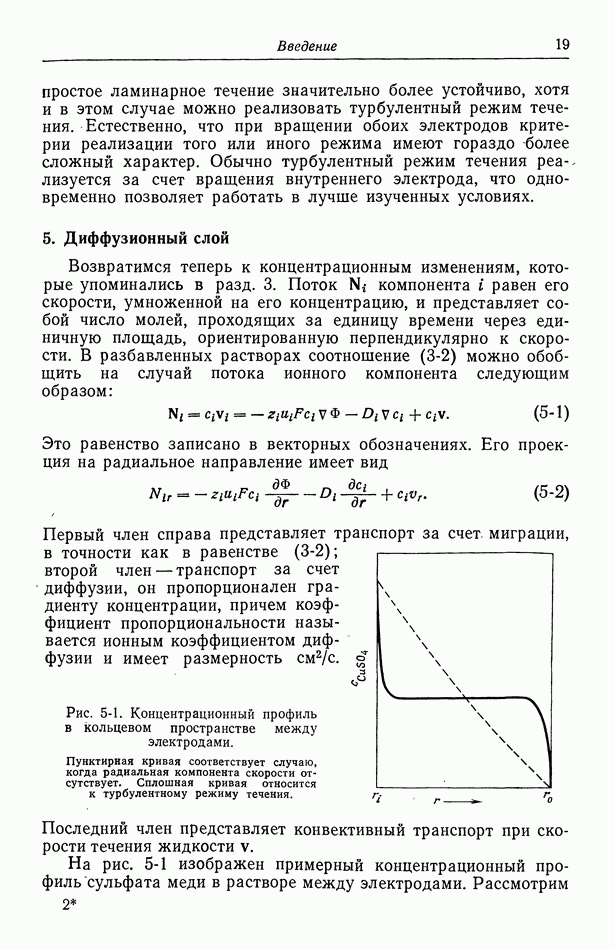
- 5. Диффузионный слой
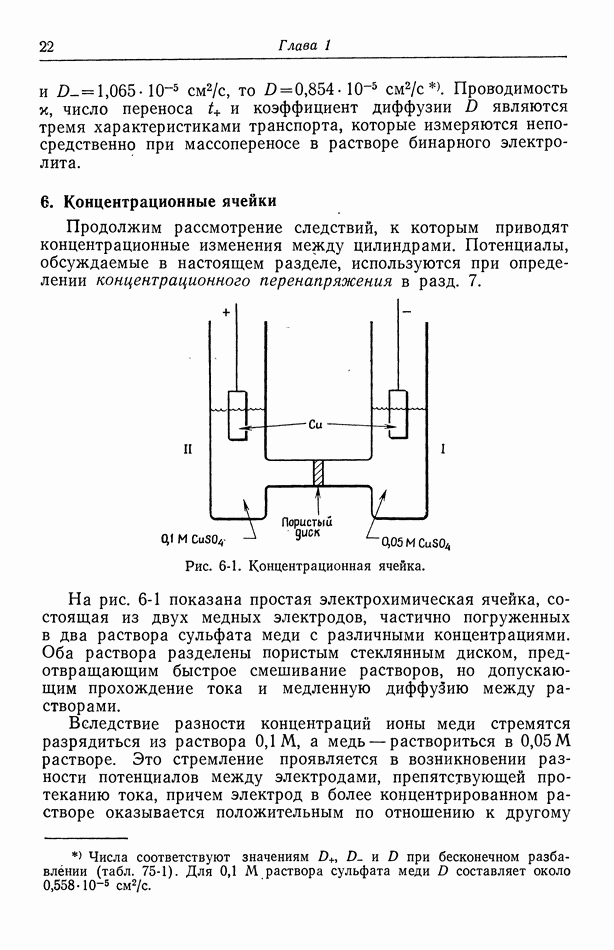
- 6. Концентрационные ячейки
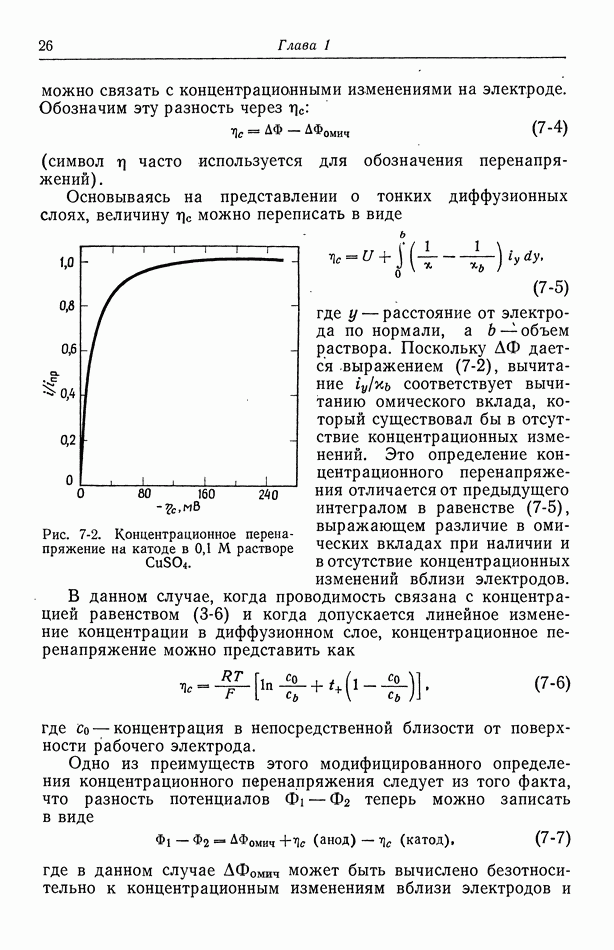
- 7. Концентрационное перенапряжение
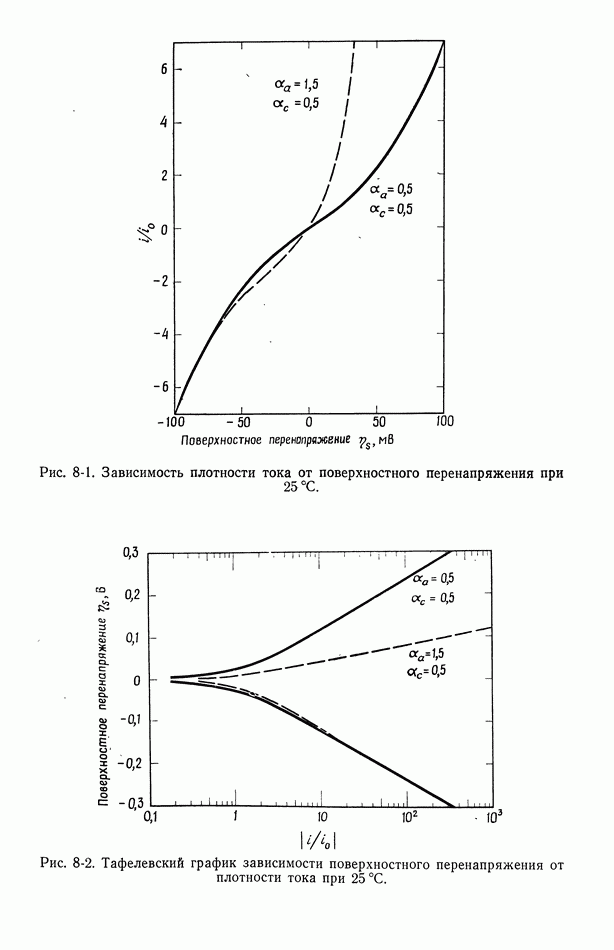
- 8. Поверхностное перенапряжение
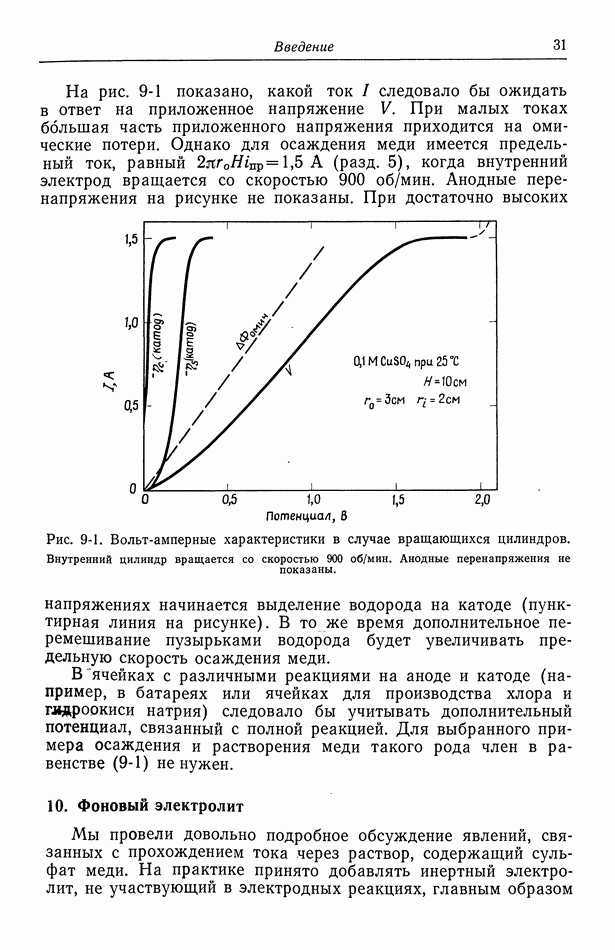
- 9. Потенциал ячейки
- 10. Фоновый электролит
- 11. Свободная конвекция
- Часть А. ТЕРМОДИНАМИКА ЭЛЕКТРОХИМИЧЕСКИХ ЯЧЕЕК
- Глава 2. ТЕРМОДИНАМИКА НА ЯЗЫКЕ ЭЛЕКТРОХИМИЧЕСКИХ ПОТЕНЦИАЛОВ
- 12. Равновесие фаз
- 13. Химический и электрохимический потенциалы
- 14. Определение некоторых термодинамических функций
- 15. Ячейка с раствором однородной концентрации
- 16. Процессы переноса в областях контакта
- 17. Ячейка с одним электролитом переменной концентрации
- 18. Ячейка с двумя электролитами, концентрация одного из которых почти однородна
- 19. Ячейка с двумя электролитами переменной концентрации
- 20. Стандартный потенциал ячейки и коэффициенты активности
- Глава 3. ЭЛЕКТРИЧЕСКИЙ ПОТЕНЦИАЛ
- 22. Электростатический потенциал
- 23. Межмолекулярные силы
- 24. Внешний и внутренний потенциалы
- 25. Потенциалы электродов сравнения
- 26. Электрический потенциал в термодинамике
- Глава 4. КОЭФФИЦИЕНТЫ АКТИВНОСТИ
- 27. Распределение ионов в разбавленных растворах
- 28. Электрический вклад в свободную энергию
- 29. Недостатки модели Дебая-Хюккеля
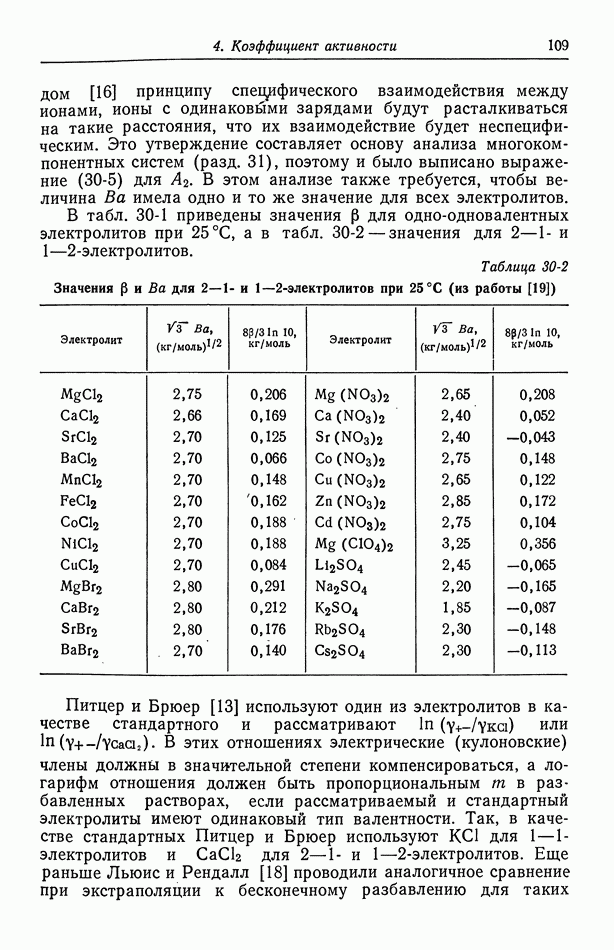
- 30. Растворы бинарных электролитов
- 31. Многокомпонентные растворы
- 32. Измерение коэффициентов активности
- 33. Слабые электролиты
- Глава 5. ЭЛЕКТРОДЫ СРАВНЕНИЯ
- 34. Критерии выбора электродов сравнения
- 35. Экспериментальные факторы, влияющие на выбор электродов сравнения
- 36. Водородный электрод
- 37. Каломельный электрод и другие электроды типа ртуть—соль ртути
- 38. Окиснортутный электрод
- 39. Электроды типа серебро—галогенид серебра
- 40. Потенциалы относительно данного электрода сравнения
- Глава 6. ПОТЕНЦИАЛЫ ЯЧЕЕК С ПЕРЕНОСОМ
- 41. Уравнение Нернста
- 42. Типы жидкостных соединений
- 43. Формулы для потенциалов жидкостных соединений
- 44. Определение концентрационных профилей
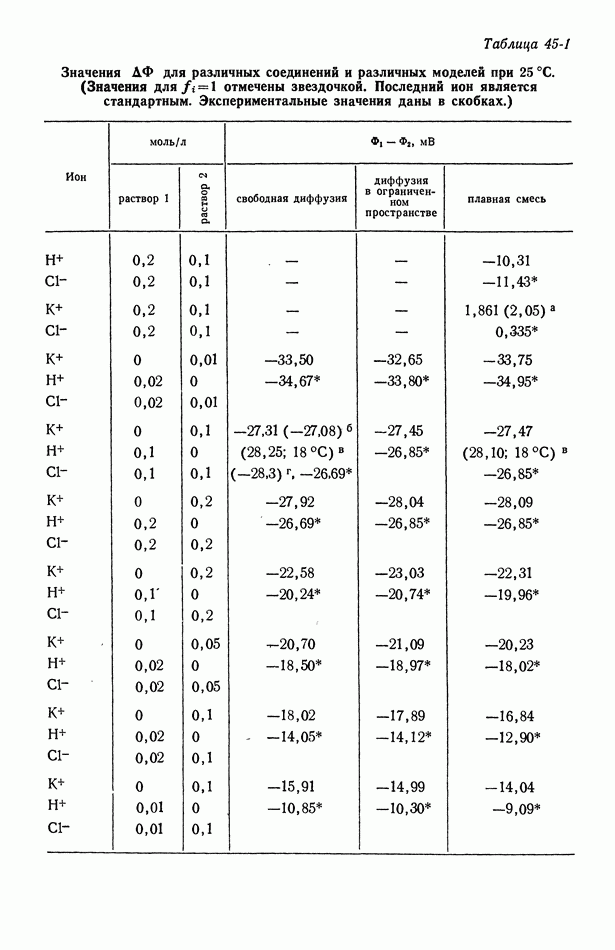
- 45. Численные результаты
- 46. Ячейки с жидкостным соединением
- 47. Поправки к уравнению Нернста
- 48. Мембранные потенциалы
- Часть Б. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ И ДРУГИЕ ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ
- Глава 7. СТРОЕНИЕ ЭЛЕКТРИЧЕСКОГО ДВОЙНОГО СЛОЯ
- 50. Изотерма адсорбции Гиббса
- 51. Уравнение Липпмана
- 52. Диффузная часть двойного слоя
- 53. Емкость двойного слоя в отсутствие специфической адсорбции
- 54. Специфическая адсорбция на границе раздела электрод—раствор
- Глава 8. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ
- 55. Гетерогенные электродные реакции
- 56. Зависимость плотности тока от поверхностного перенапряжения
- 57. Модели в кинетике электродных процессов
- 58. Влияние строения двойного слоя
- 59. Кислородный электрод
- 60. Методы измерения
- 61. Одновременно протекающие реакции
- Глава 9. ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ
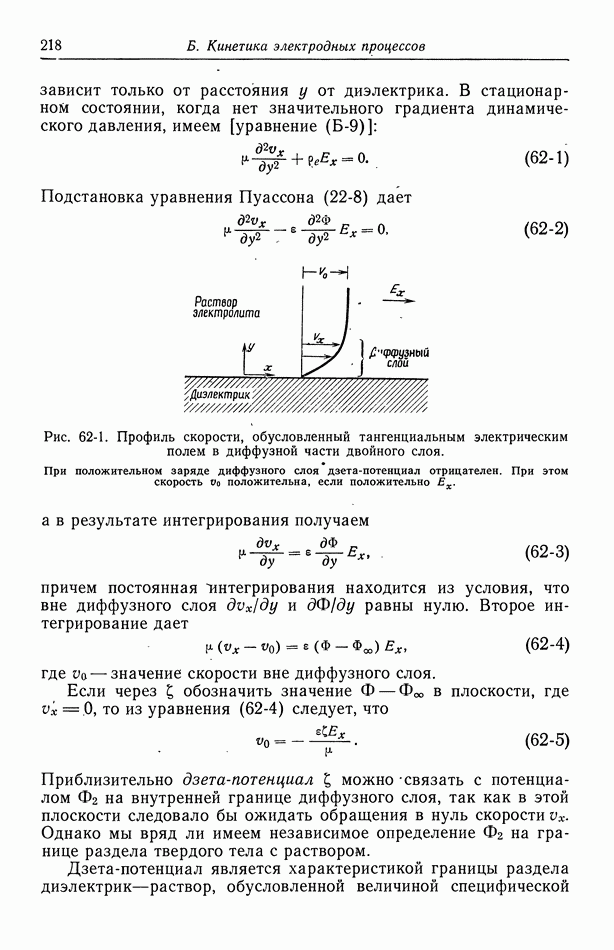
- 62. Разрывная скорость на границе раздела
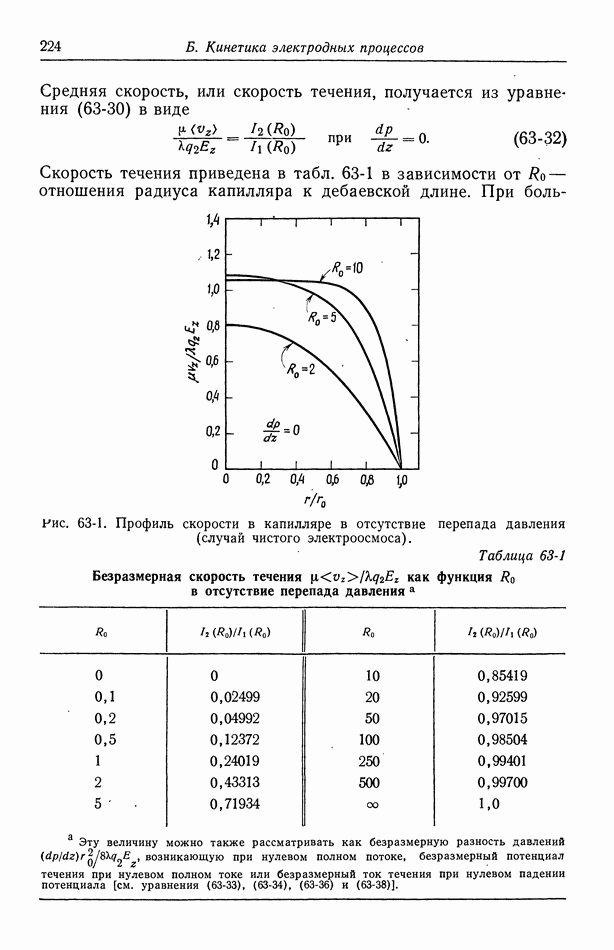
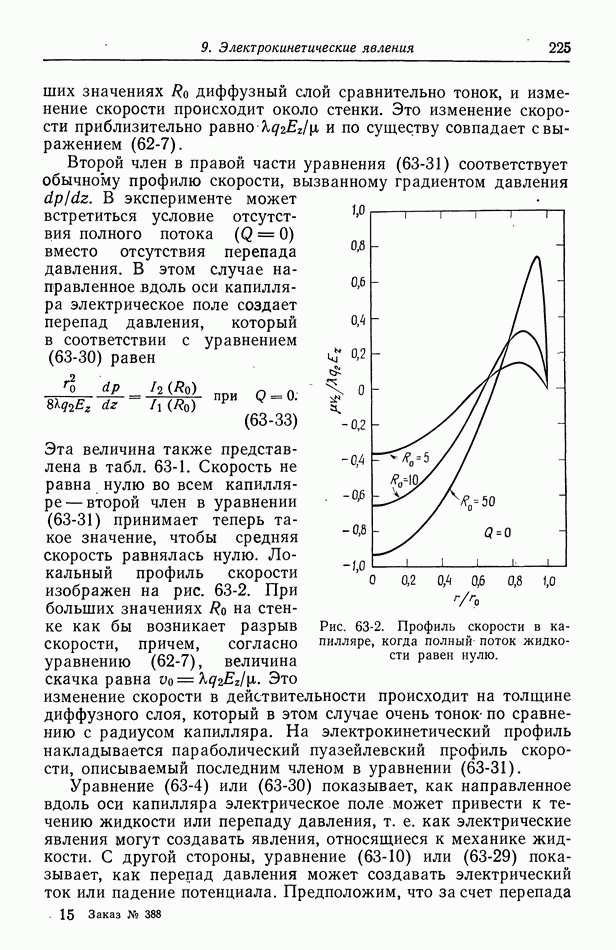
- 63. Электроосмос и потенциал течения
- 64. Электрофорез
- 65. Потенциал осаждения
- Глава 10. ЭЛЕКТРОКАПИЛЛЯРНЫЕ ЯВЛЕНИЯ
- 67. Электрокапиллярное движение ртутных капель
- 68. Потенциалы осаждения для падающих ртутных капель
- Часть В. ПРОЦЕССЫ ПЕРЕНОСА В РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- Глава 11. БЕСКОНЕЧНО РАЗБАВЛЕННЫЕ РАСТВОРЫ
- 70. Проводимость, диффузионные потенциалы и числа переноса
- 71. Сохранение заряда
- 72. Бинарный электролит
- 73. Фоновый электролит
- 74. Многокомпонентная диффузия, возникающая при исключении электрического поля
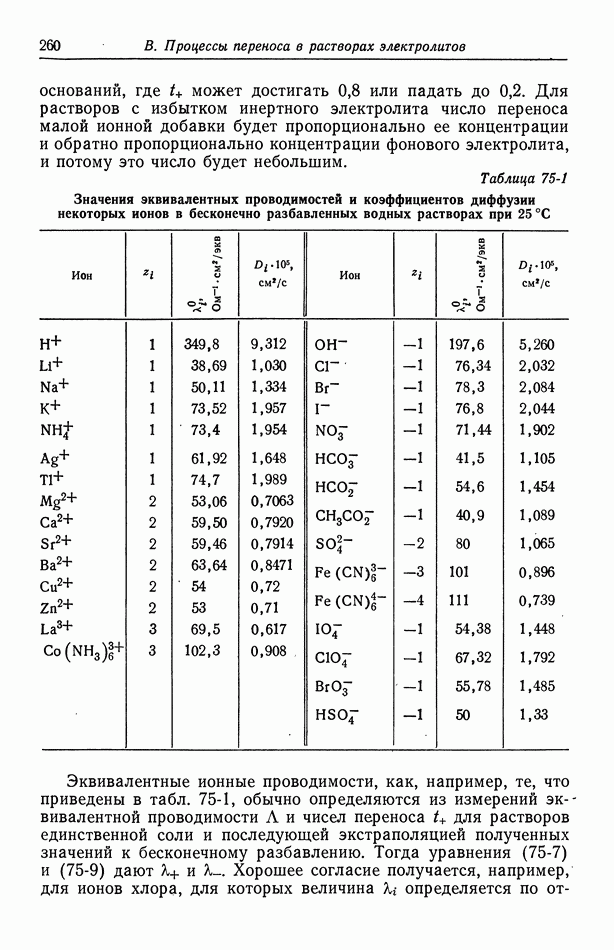
- 75. Подвижности и коэффициенты диффузии
- 76. Электронейтральность и уравнение Лапласа
- 77. Умеренно разбавленные растворы
- Глава 12. КОНЦЕНТРИРОВАННЫЕ РАСТВОРЫ
- 79. Бинарный электролит
- 80. Стандартные скорости
- 81. Потенциал
- 82. Связь с теорией разбавленных растворов
- 83. Многокомпонентный транспорт
- 84. Потенциалы жидкостного соединения
- Глава 13. ТЕПЛОВЫЕ ЭФФЕКТЫ
- 85. Термодиффузия
- 86. Выделение и перенос тепла
- 87. Тепловыделение на границе раздела фаз
- 88. Термогальванические ячейки
- Глава 14. ХАРАКТЕРИСТИКИ ПЕРЕНОСА
- 89. Бесконечно разбавленные растворы
- 90. Растворы, содержащие одну соль
- 91. Многокомпонентные растворы
- 92. Интегральные коэффициенты диффузии
- Глава 15. МЕХАНИКА ЖИДКИХ СРЕД
- 93. Баланс массы и импульса
- 94. Напряжение в ньютоновской жидкости
- 95. Граничные условия
- 96. Течение жидкости к вращающемуся диску
- 97. Величины электрических сил
- 98. Турбулентное течение
- 99. Массоперенос в турбулентном потоке
- Часть Г. РАСПРЕДЕЛЕНИЕ ТОКА И МАССОПЕРЕНОС В ЭЛЕКТРОХИМИЧЕСКИХ СИСТЕМАХ
- Глава 16. ОСНОВНЫЕ УРАВНЕНИЯ
- 100. Перенос в разбавленных растворах
- 101. Кинетика электродных процессов
- Глава 17. ЗАДАЧИ КОНВЕКТИВНОЙ ДИФФУЗИИ
- 102. Упрощенное описание конвективной диффузии
- 103. Вращающийся диск
- 104. Задача Граца
- 105. Кольцевой зазор
- 106. Двумерные диффузионные слои при вынужденной ламинарной конвекции
- 107. Осесимметричные диффузионные слои при вынужденной ламинарной конвекции
- 108. Плоская пластина в свободном потоке
- 109. Вращающиеся цилиндры
- 110. Растущие ртутные капли
- 112. Наложение свободной и вынужденной конвекции
- 113. Ограничения за счет поверхностных реакций
- 114. Бинарные и концентрированные растворы
- Глава 18. ПРИЛОЖЕНИЯ ТЕОРИИ ПОТЕНЦИАЛА
- 115. Упрощения в задачах теории потенциала
- 116. Первичное распределение тока
- 117. Вторичное распределение тока
- 118. Численное решение методом конечных разностей
- Глава 19. ВЛИЯНИЕ МИГРАЦИИ НА ПРЕДЕЛЬНЫЕ ТОКИ
- 120. Поправочный множитель в случае предельных токов
- 121. Изменение концентрации фонового электролита
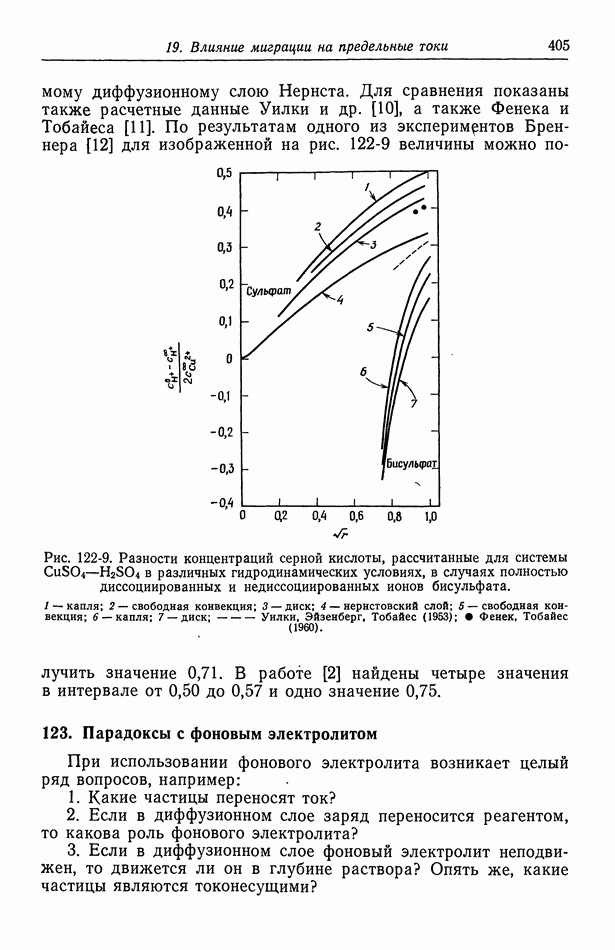
- 122. Роль ионов бисульфата
- 123. Парадоксы с фоновым электролитом
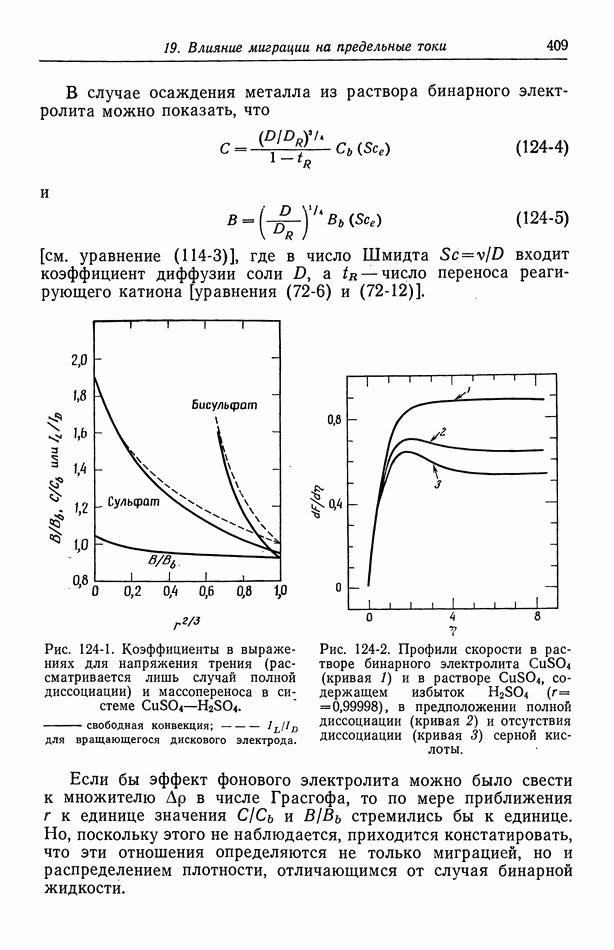
- 124. Предельные токи в случае свободной конвекции
- Глава 20. КОНЦЕНТРАЦИОННОЕ ПЕРЕНАПРЯЖЕНИЕ
- 126. Бинарный электролит
- 127. Фоновый электролит
- 128. Численные расчеты
- Глава 21. ДОПРЕДЕЛЬНЫЕ ТОКИ
- 129. Объем раствора
- 130. Диффузионные слои
- 131. Граничные условия и метод решения
- 132. Результаты для вращающегося диска
- Приложение А. ПАРЦИАЛЬНЫЕ МОЛЯРНЫЕ ОБЪЕМЫ
- Приложение Б. ВЕКТОРЫ И ТЕНЗОРЫ
- Приложение В. ЧИСЛЕННОЕ РЕШЕНИЕ СИСТЕМЫ ОБЫКНОВЕННЫХ ДИФФЕРЕНЦИАЛЬНЫХ УРАВНЕНИЙ