| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
39. Электроды типа серебро—галогенид серебра
Благодаря низкой растворимости галогенидов серебра электроды типа серебро—галогенид серебра являются электродами второго рода. Из них наиболее употребителен хлорсеребряный электрод  обратимый по иону хлора. Связь его стандартного потенциала со стандартным потенциалом серебряного электрода и с произведением растворимости хлорида серебра рассматривалась в задаче 2-13.
обратимый по иону хлора. Связь его стандартного потенциала со стандартным потенциалом серебряного электрода и с произведением растворимости хлорида серебра рассматривалась в задаче 2-13.
Можно указать на следующие преимущества электродов типа серебро—хлорид серебра: они компактны, могут использоваться при любой ориентации и обычно слабо загрязняют любую среду, в которую они погружены. Недостатком является зависимость их термодинамических характеристик от физических свойств твердых фаз, таких, как механическая деформация и кристаллическая, структура, а значит, и от способа приготовления электрода.
До сих пор нет метода изготовления идеального хлорсеребря-ного электрода. В экспериментальной работе, как правило, используются следующие три метода:
1. Электролитический. В качестве основы электрода обычно применяют металлическую платину, на которую наносят серебро методом электроосаждения из раствора  После тщательной промывки производится анодное галогенирование покрытой серебром платины: в 0,1 н. растворе
После тщательной промывки производится анодное галогенирование покрытой серебром платины: в 0,1 н. растворе  для хлорсереб-ряного электрода, а для бромсеребряного и иодсеребряного электродов — в 0,1 н. растворах
для хлорсереб-ряного электрода, а для бромсеребряного и иодсеребряного электродов — в 0,1 н. растворах  или
или  иногда слегка подкисленных соответствующей кислотой. Галогенируется около 10% серебра. Воспроизводимость изготовленных этим методом электродов типа серебро—галогенид серебра будет находиться в пределах
иногда слегка подкисленных соответствующей кислотой. Галогенируется около 10% серебра. Воспроизводимость изготовленных этим методом электродов типа серебро—галогенид серебра будет находиться в пределах 
2. Термический. Термические электроды изготовляются путем разложения смеси окиси серебра и хлората, бромата или иодата серебра, состоящей на  из окиси серебра. Для образования однородной массы к смеси добавляют воду. Полученной пастой покрывают спиральную платиновую проволоку и нагревают до температуры разложения
из окиси серебра. Для образования однородной массы к смеси добавляют воду. Полученной пастой покрывают спиральную платиновую проволоку и нагревают до температуры разложения  после чего медленно охлаждают до комнатной температуры.
после чего медленно охлаждают до комнатной температуры.
Для приготовления электродов типа серебро—иодид серебра иногда применяют иодид серебра, нагреваемый с  до
до  в течение 10—15 мин. При изготовлении хлорсеребряных электродов использовалась также смесь окиси серебра и перхлората серебра.
в течение 10—15 мин. При изготовлении хлорсеребряных электродов использовалась также смесь окиси серебра и перхлората серебра.
Термические электроды типа серебро — галогенид серебра менее надежны, чем электролитические или термоэлектролитические, что, по-видимому, объясняется более высокой воспроизводимостью поверхности последних.
3. Термоэлектрический. В этом методе серебро сначала получают разложением окиси серебра, а затем галогенируют электролитически. Воспроизводимость приготовленного этим методом хлорсеребряного электрода находится в пределах 
При изготовлении электродов типа серебро—галогенид серебра употреблялось также несколько менее общих методов, которые здесь не рассматриваются.
Полное исследование стандартного потенциала хлорсеребряного электрода проведено на ячейке

В области температур  результат можно представить в виде
результат можно представить в виде

где  температура
температура  Стандартные потенциалы бромсеребряного и иодсеребряного электродов также были исследованы в некоторой области температур, хотя для последнего стандартный потенциал труднее было получить непосредственными измерениями из-за экспериментальных трудностей, например из-за окисления раствора
Стандартные потенциалы бромсеребряного и иодсеребряного электродов также были исследованы в некоторой области температур, хотя для последнего стандартный потенциал труднее было получить непосредственными измерениями из-за экспериментальных трудностей, например из-за окисления раствора 
Некоторые примеси, такие, как иодид и сульфид, могут образовывать с серебром менее растворимые соли по сравнению с хлоридом и бромидом серебра. Эти соли могут осаждаться на поверхности электрода, изменяя его потенциал. Даже следы бромида в растворе сдвигают в положительную сторону потенциал хлорсеребряного электрода. Если в качестве электролитов используются  или
или  то имеющийся в растворе кислород может исказить свойства хлорсеребряного и бромсеребряного электродов за счет реакции медленного окисления
то имеющийся в растворе кислород может исказить свойства хлорсеребряного и бромсеребряного электродов за счет реакции медленного окисления

Для иодсеребряного электрода значительный кислородный эффект отмечен как в нейтральном, так и в кислом растворах.
Свойства электродов типа серебро—галогенид серебра зависят от их возраста. Потенциалы старых электродов несколько более положительны по сравнению с новыми. Этот эффект всегда имеет одно и то же направление и один и тот же порядок величины — около  Потенциал свежеприготовленного электрода серебро—галогенид серебра медленно увеличивается и достигает стабильного значения. Время изменения свойств электрода варьируется от нескольких минут до одного—двадцати дней. Этот эффект приписывается концентрационной поляризации, связанной с электролитическим галогенированием или начальным погружением электрода в исследуемый раствор.
Потенциал свежеприготовленного электрода серебро—галогенид серебра медленно увеличивается и достигает стабильного значения. Время изменения свойств электрода варьируется от нескольких минут до одного—двадцати дней. Этот эффект приписывается концентрационной поляризации, связанной с электролитическим галогенированием или начальным погружением электрода в исследуемый раствор.
Широкое использование электродов серебро—галогенид серебра в электрохимических измерениях объясняется их компактностью и легкостью изготовления. Наиболее важным применением хлорсеребряного электрода является исследование термодинамических свойств электролитов, таких, как стандартный электродный потенциал и коэффициенты активности. Электроды типа серебро—галогенид серебра могут также использоваться в неводных растворах. Однако это применение ограничено сильной тенденцией иона серебра к образованию комплексов, что значительно увеличивает растворимость галогенидов серебра. Хлорсеребряные электроды нашли важное применение в исследовании свойств биологических мембран.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Глава 1. ВВЕДЕНИЕ
- 1. Термодинамика, кинетика электродных процессов и процессы переноса
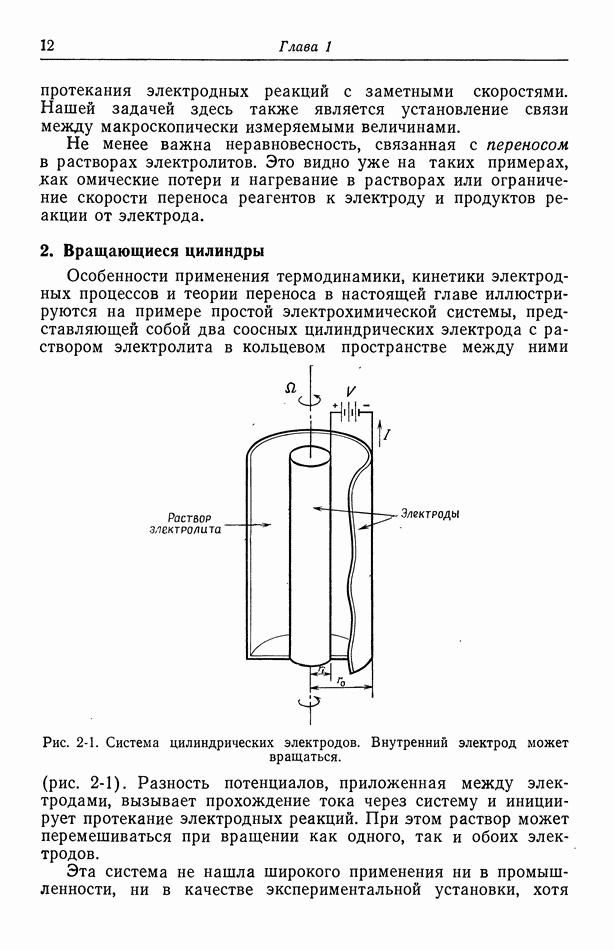
- 2. Вращающиеся цилиндры
- 3. Прохождение тока в электролитах
- 4. Течение жидкости
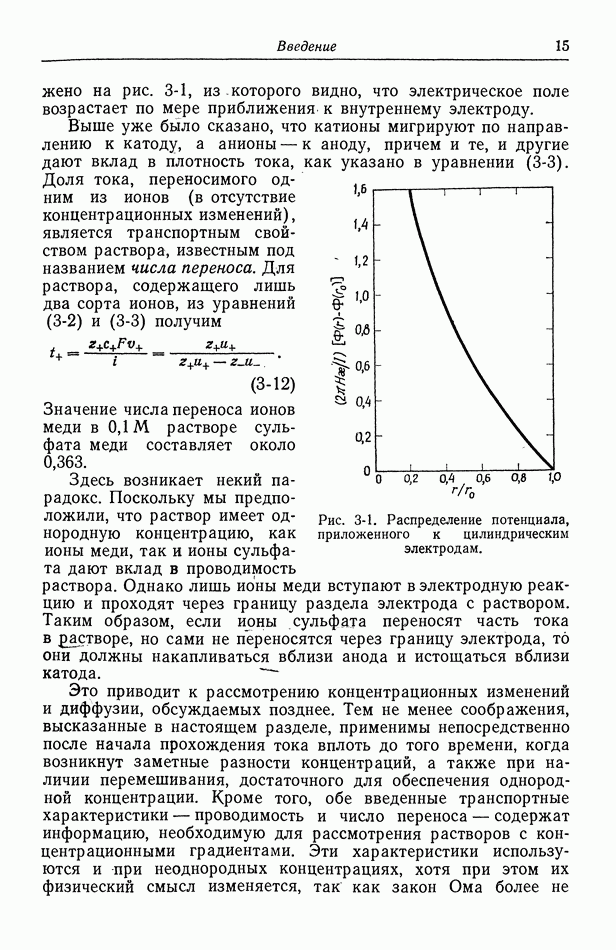
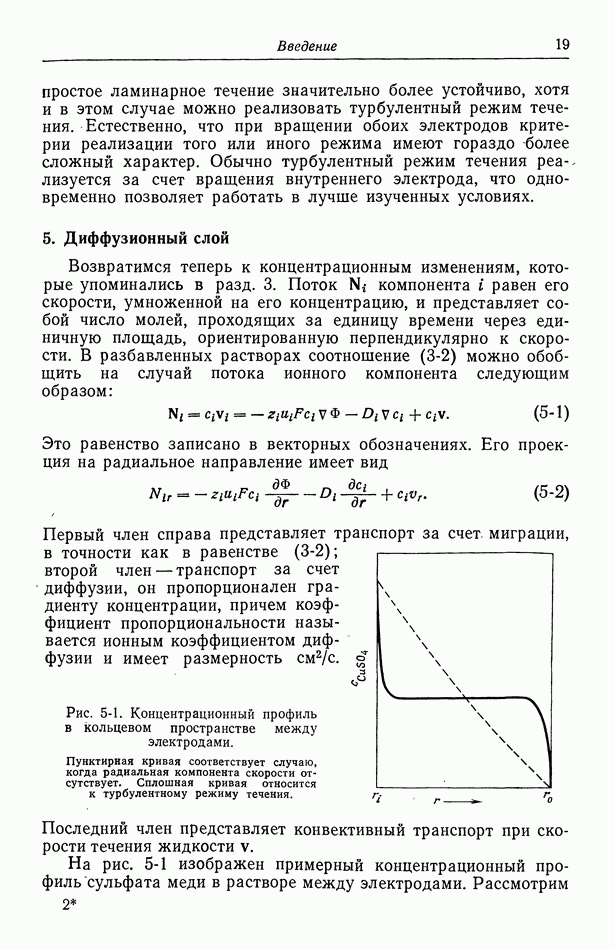
- 5. Диффузионный слой
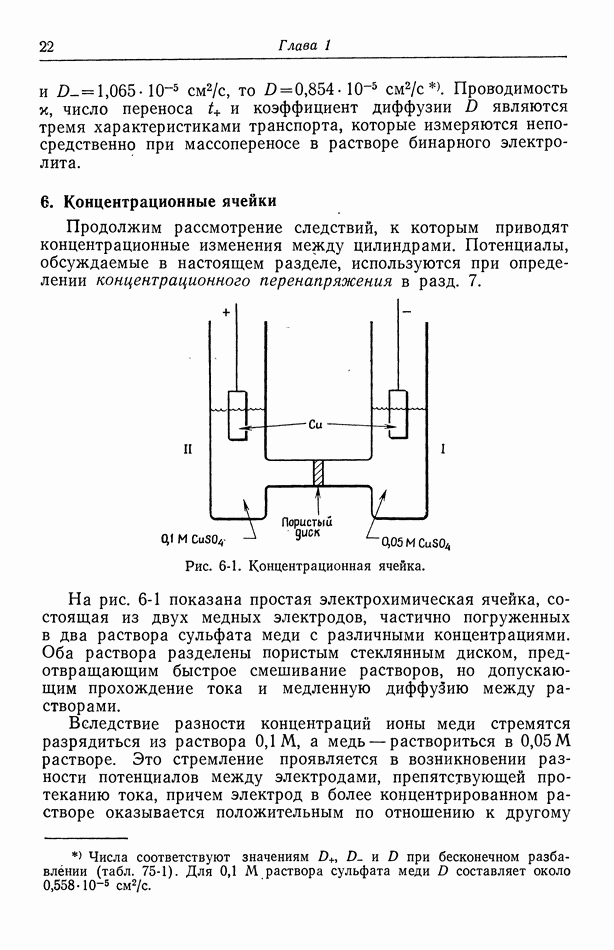
- 6. Концентрационные ячейки
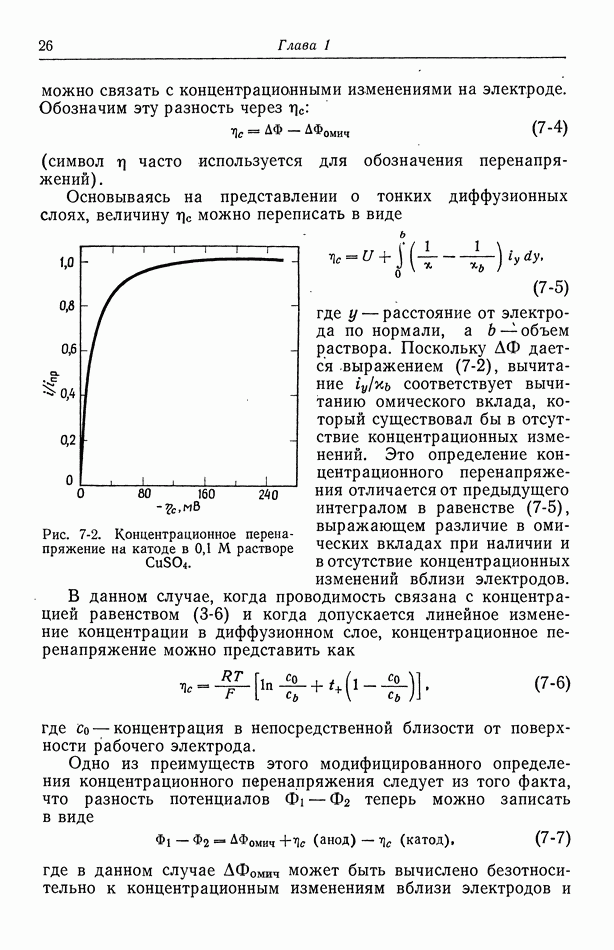
- 7. Концентрационное перенапряжение
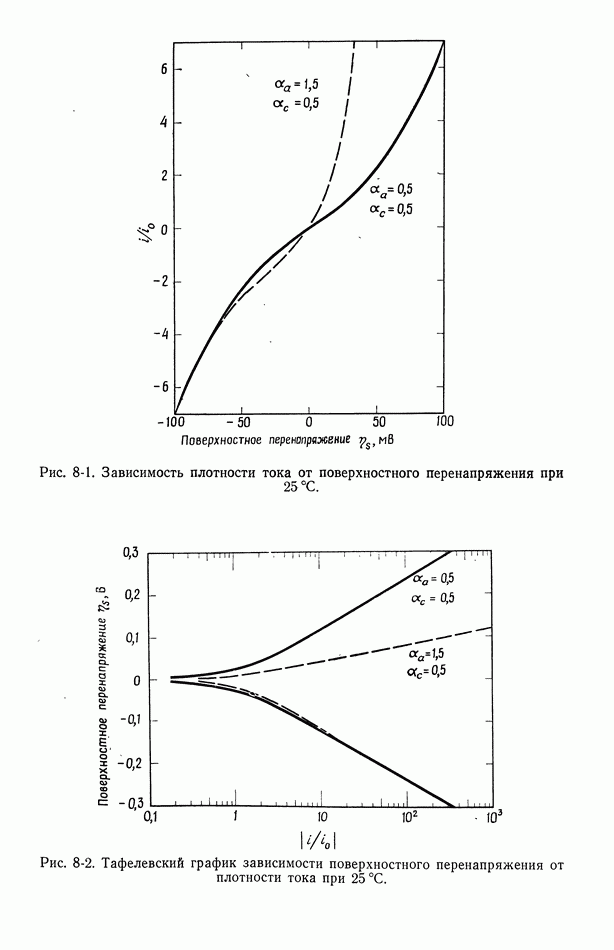
- 8. Поверхностное перенапряжение
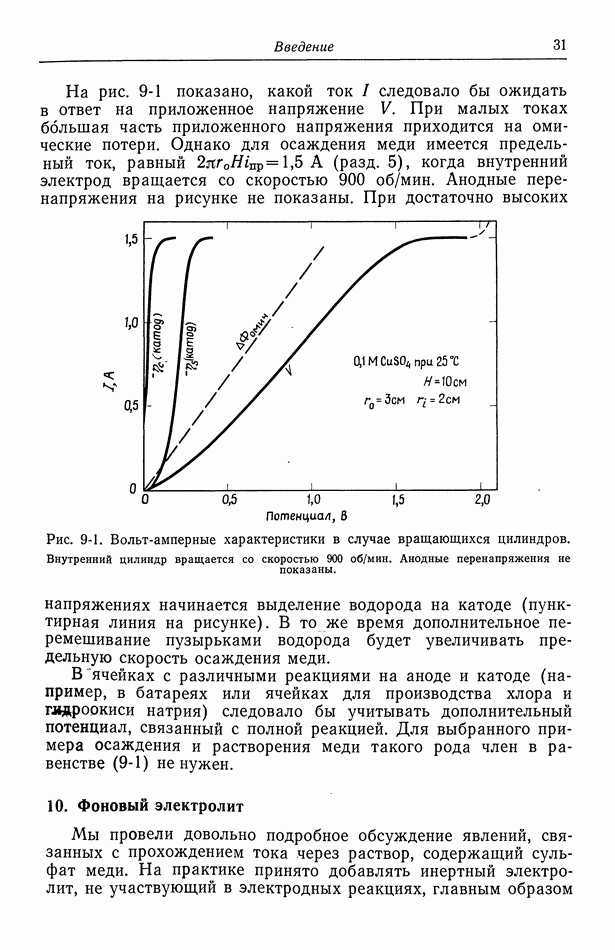
- 9. Потенциал ячейки
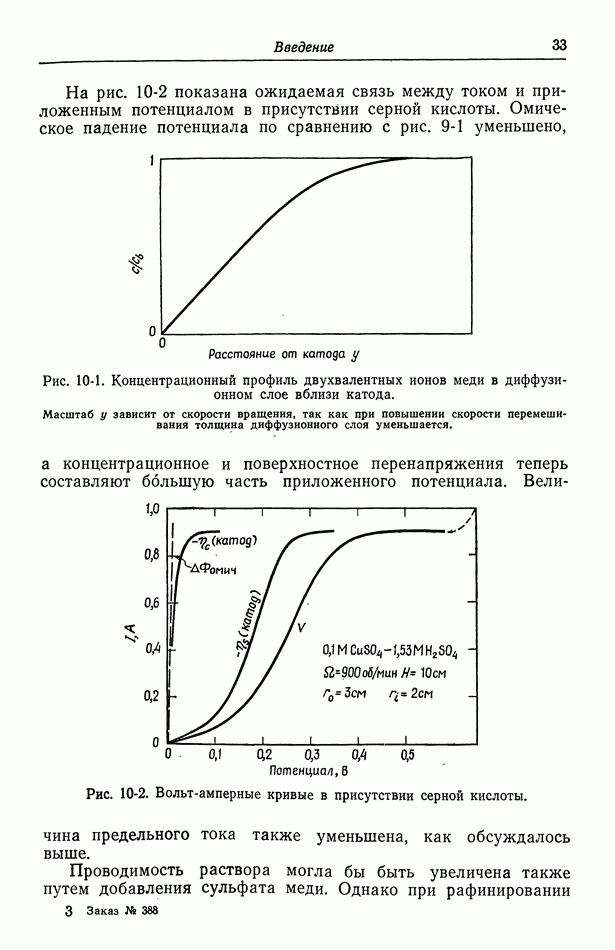
- 10. Фоновый электролит
- 11. Свободная конвекция
- Часть А. ТЕРМОДИНАМИКА ЭЛЕКТРОХИМИЧЕСКИХ ЯЧЕЕК
- Глава 2. ТЕРМОДИНАМИКА НА ЯЗЫКЕ ЭЛЕКТРОХИМИЧЕСКИХ ПОТЕНЦИАЛОВ
- 12. Равновесие фаз
- 13. Химический и электрохимический потенциалы
- 14. Определение некоторых термодинамических функций
- 15. Ячейка с раствором однородной концентрации
- 16. Процессы переноса в областях контакта
- 17. Ячейка с одним электролитом переменной концентрации
- 18. Ячейка с двумя электролитами, концентрация одного из которых почти однородна
- 19. Ячейка с двумя электролитами переменной концентрации
- 20. Стандартный потенциал ячейки и коэффициенты активности
- Глава 3. ЭЛЕКТРИЧЕСКИЙ ПОТЕНЦИАЛ
- 22. Электростатический потенциал
- 23. Межмолекулярные силы
- 24. Внешний и внутренний потенциалы
- 25. Потенциалы электродов сравнения
- 26. Электрический потенциал в термодинамике
- Глава 4. КОЭФФИЦИЕНТЫ АКТИВНОСТИ
- 27. Распределение ионов в разбавленных растворах
- 28. Электрический вклад в свободную энергию
- 29. Недостатки модели Дебая-Хюккеля
- 30. Растворы бинарных электролитов
- 31. Многокомпонентные растворы
- 32. Измерение коэффициентов активности
- 33. Слабые электролиты
- Глава 5. ЭЛЕКТРОДЫ СРАВНЕНИЯ
- 34. Критерии выбора электродов сравнения
- 35. Экспериментальные факторы, влияющие на выбор электродов сравнения
- 36. Водородный электрод
- 37. Каломельный электрод и другие электроды типа ртуть—соль ртути
- 38. Окиснортутный электрод
- 39. Электроды типа серебро—галогенид серебра
- 40. Потенциалы относительно данного электрода сравнения
- Глава 6. ПОТЕНЦИАЛЫ ЯЧЕЕК С ПЕРЕНОСОМ
- 41. Уравнение Нернста
- 42. Типы жидкостных соединений
- 43. Формулы для потенциалов жидкостных соединений
- 44. Определение концентрационных профилей
- 45. Численные результаты
- 46. Ячейки с жидкостным соединением
- 47. Поправки к уравнению Нернста
- 48. Мембранные потенциалы
- Часть Б. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ И ДРУГИЕ ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ
- Глава 7. СТРОЕНИЕ ЭЛЕКТРИЧЕСКОГО ДВОЙНОГО СЛОЯ
- 50. Изотерма адсорбции Гиббса
- 51. Уравнение Липпмана
- 52. Диффузная часть двойного слоя
- 53. Емкость двойного слоя в отсутствие специфической адсорбции
- 54. Специфическая адсорбция на границе раздела электрод—раствор
- Глава 8. КИНЕТИКА ЭЛЕКТРОДНЫХ ПРОЦЕССОВ
- 55. Гетерогенные электродные реакции
- 56. Зависимость плотности тока от поверхностного перенапряжения
- 57. Модели в кинетике электродных процессов
- 58. Влияние строения двойного слоя
- 59. Кислородный электрод
- 60. Методы измерения
- 61. Одновременно протекающие реакции
- Глава 9. ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ
- 62. Разрывная скорость на границе раздела
- 63. Электроосмос и потенциал течения
- 64. Электрофорез
- 65. Потенциал осаждения
- Глава 10. ЭЛЕКТРОКАПИЛЛЯРНЫЕ ЯВЛЕНИЯ
- 67. Электрокапиллярное движение ртутных капель
- 68. Потенциалы осаждения для падающих ртутных капель
- Часть В. ПРОЦЕССЫ ПЕРЕНОСА В РАСТВОРАХ ЭЛЕКТРОЛИТОВ
- Глава 11. БЕСКОНЕЧНО РАЗБАВЛЕННЫЕ РАСТВОРЫ
- 70. Проводимость, диффузионные потенциалы и числа переноса
- 71. Сохранение заряда
- 72. Бинарный электролит
- 73. Фоновый электролит
- 74. Многокомпонентная диффузия, возникающая при исключении электрического поля
- 75. Подвижности и коэффициенты диффузии
- 76. Электронейтральность и уравнение Лапласа
- 77. Умеренно разбавленные растворы
- Глава 12. КОНЦЕНТРИРОВАННЫЕ РАСТВОРЫ
- 79. Бинарный электролит
- 80. Стандартные скорости
- 81. Потенциал
- 82. Связь с теорией разбавленных растворов
- 83. Многокомпонентный транспорт
- 84. Потенциалы жидкостного соединения
- Глава 13. ТЕПЛОВЫЕ ЭФФЕКТЫ
- 85. Термодиффузия
- 86. Выделение и перенос тепла
- 87. Тепловыделение на границе раздела фаз
- 88. Термогальванические ячейки
- Глава 14. ХАРАКТЕРИСТИКИ ПЕРЕНОСА
- 89. Бесконечно разбавленные растворы
- 90. Растворы, содержащие одну соль
- 91. Многокомпонентные растворы
- 92. Интегральные коэффициенты диффузии
- Глава 15. МЕХАНИКА ЖИДКИХ СРЕД
- 93. Баланс массы и импульса
- 94. Напряжение в ньютоновской жидкости
- 95. Граничные условия
- 96. Течение жидкости к вращающемуся диску
- 97. Величины электрических сил
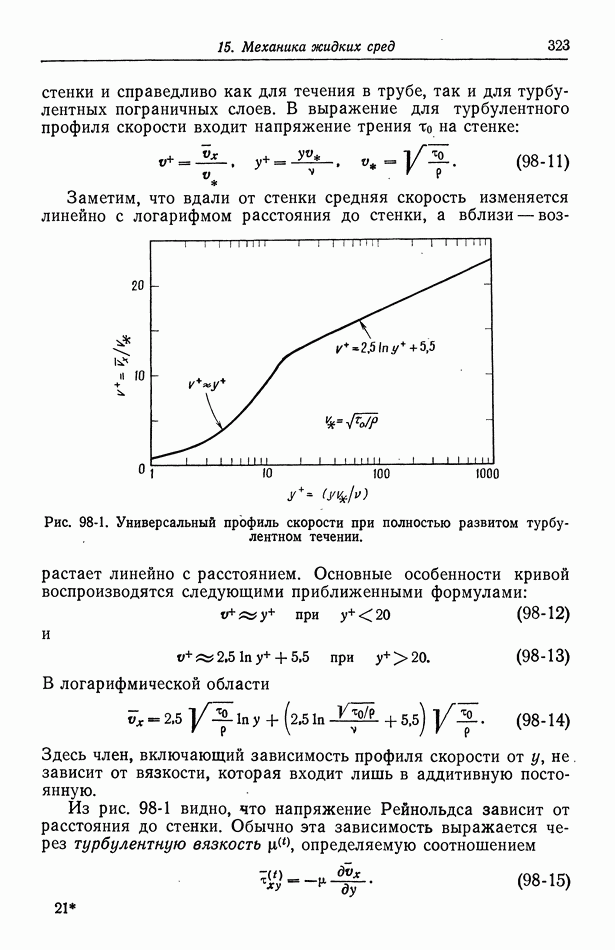
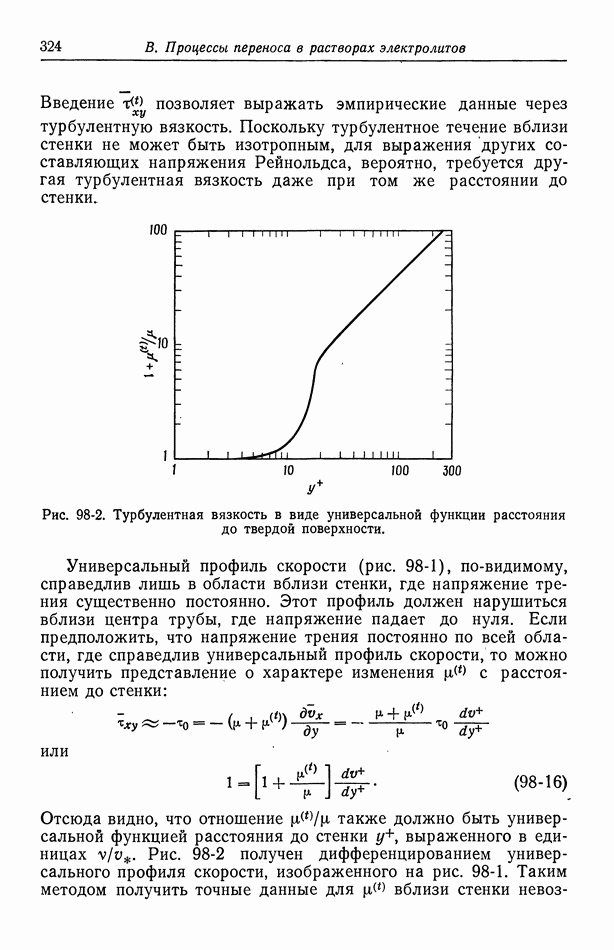
- 98. Турбулентное течение
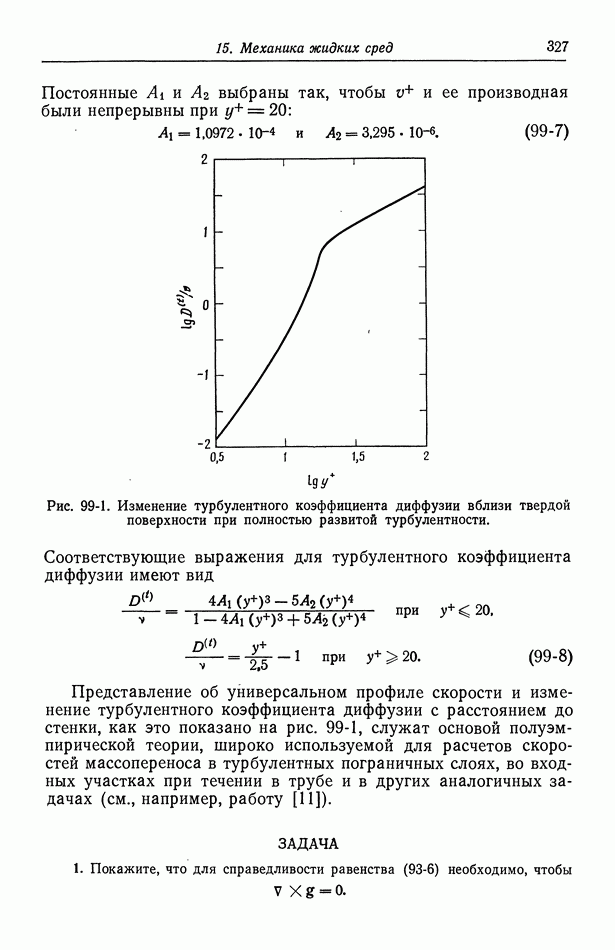
- 99. Массоперенос в турбулентном потоке
- Часть Г. РАСПРЕДЕЛЕНИЕ ТОКА И МАССОПЕРЕНОС В ЭЛЕКТРОХИМИЧЕСКИХ СИСТЕМАХ
- Глава 16. ОСНОВНЫЕ УРАВНЕНИЯ
- 100. Перенос в разбавленных растворах
- 101. Кинетика электродных процессов
- Глава 17. ЗАДАЧИ КОНВЕКТИВНОЙ ДИФФУЗИИ
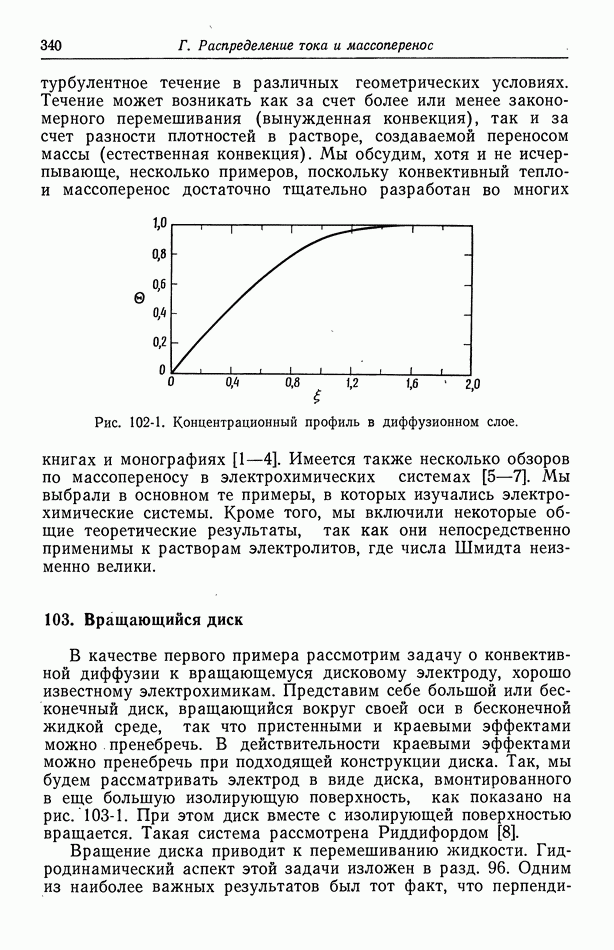
- 102. Упрощенное описание конвективной диффузии
- 103. Вращающийся диск
- 104. Задача Граца
- 105. Кольцевой зазор
- 106. Двумерные диффузионные слои при вынужденной ламинарной конвекции
- 107. Осесимметричные диффузионные слои при вынужденной ламинарной конвекции
- 108. Плоская пластина в свободном потоке
- 109. Вращающиеся цилиндры
- 110. Растущие ртутные капли
- 112. Наложение свободной и вынужденной конвекции
- 113. Ограничения за счет поверхностных реакций
- 114. Бинарные и концентрированные растворы
- Глава 18. ПРИЛОЖЕНИЯ ТЕОРИИ ПОТЕНЦИАЛА
- 115. Упрощения в задачах теории потенциала
- 116. Первичное распределение тока
- 117. Вторичное распределение тока
- 118. Численное решение методом конечных разностей
- Глава 19. ВЛИЯНИЕ МИГРАЦИИ НА ПРЕДЕЛЬНЫЕ ТОКИ
- 120. Поправочный множитель в случае предельных токов
- 121. Изменение концентрации фонового электролита
- 122. Роль ионов бисульфата
- 123. Парадоксы с фоновым электролитом
- 124. Предельные токи в случае свободной конвекции
- Глава 20. КОНЦЕНТРАЦИОННОЕ ПЕРЕНАПРЯЖЕНИЕ
- 126. Бинарный электролит
- 127. Фоновый электролит
- 128. Численные расчеты
- Глава 21. ДОПРЕДЕЛЬНЫЕ ТОКИ
- 129. Объем раствора
- 130. Диффузионные слои
- 131. Граничные условия и метод решения
- 132. Результаты для вращающегося диска
- Приложение А. ПАРЦИАЛЬНЫЕ МОЛЯРНЫЕ ОБЪЕМЫ
- Приложение Б. ВЕКТОРЫ И ТЕНЗОРЫ
- Приложение В. ЧИСЛЕННОЕ РЕШЕНИЕ СИСТЕМЫ ОБЫКНОВЕННЫХ ДИФФЕРЕНЦИАЛЬНЫХ УРАВНЕНИЙ