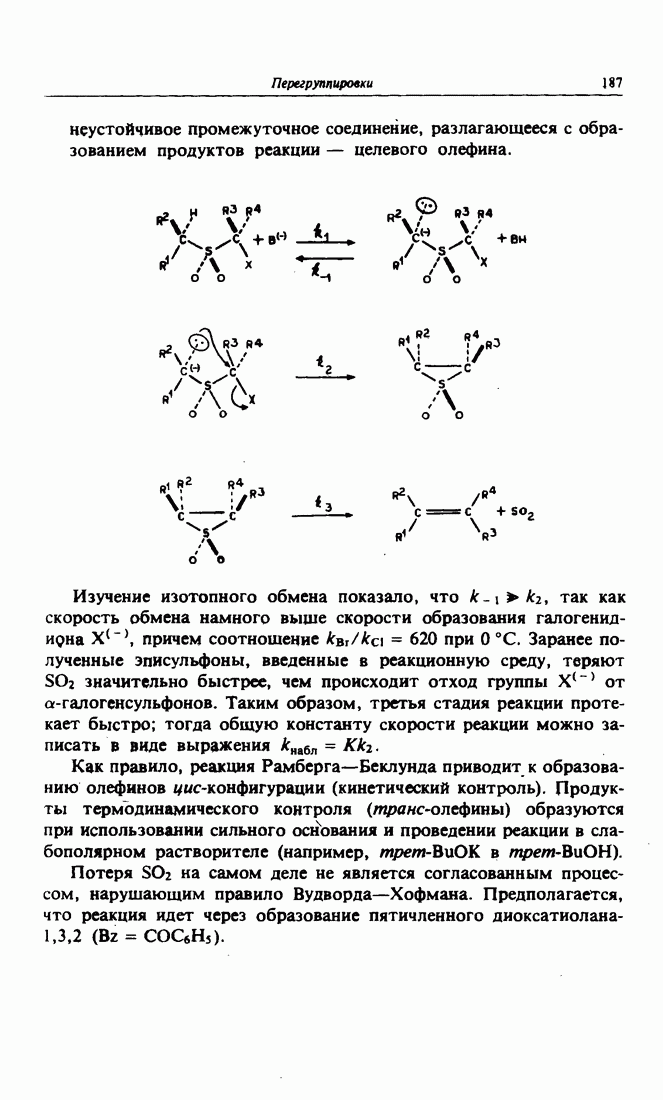
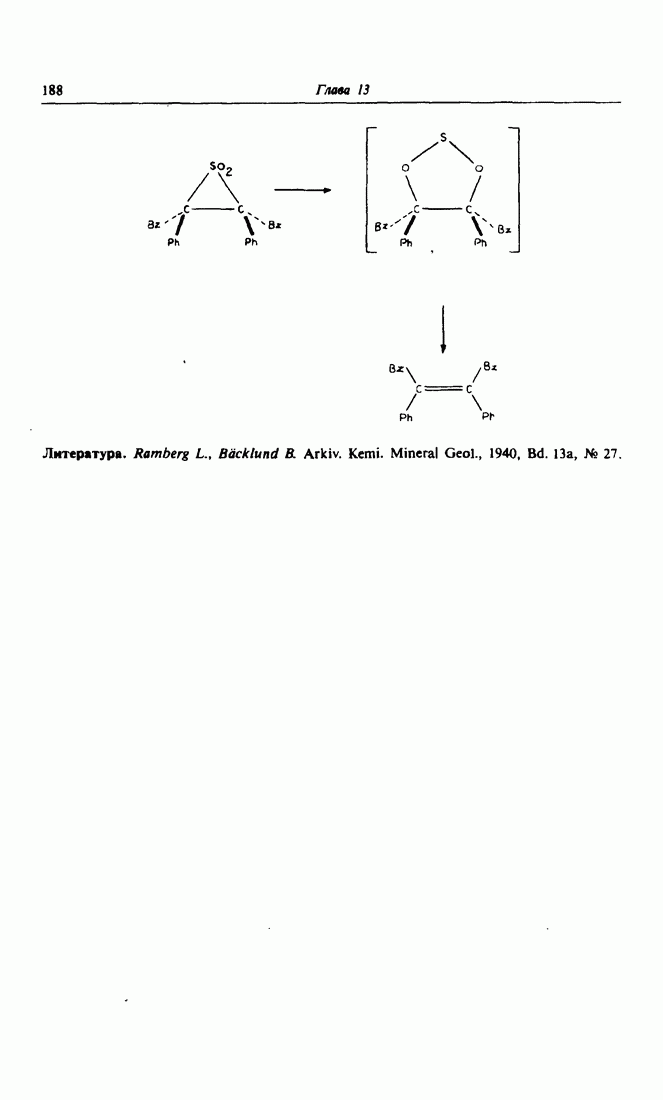
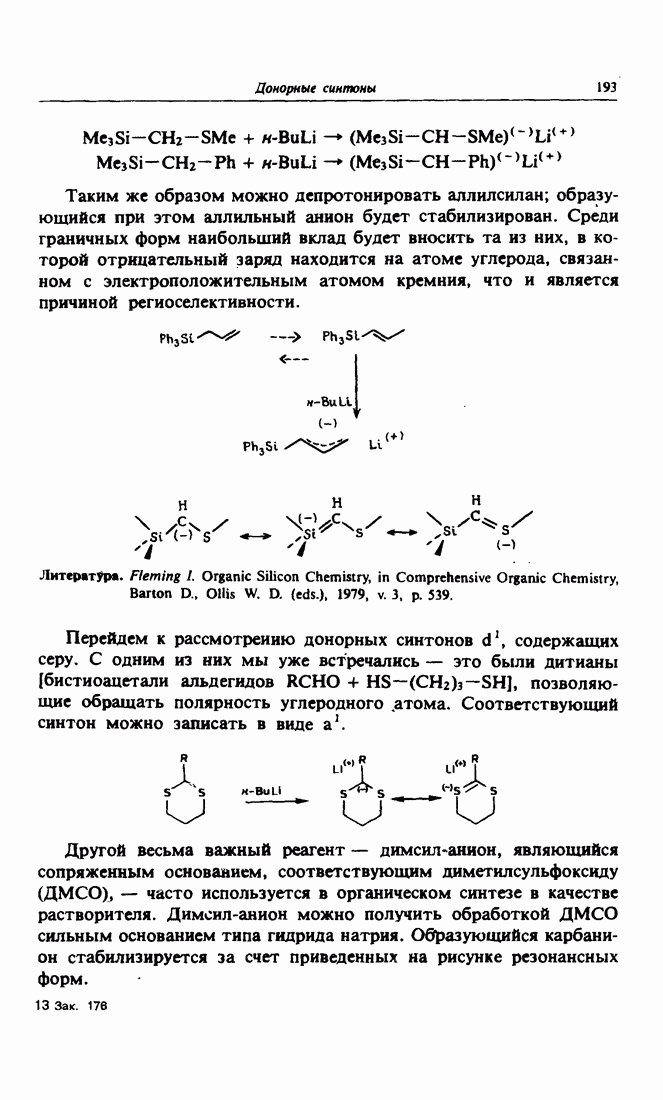
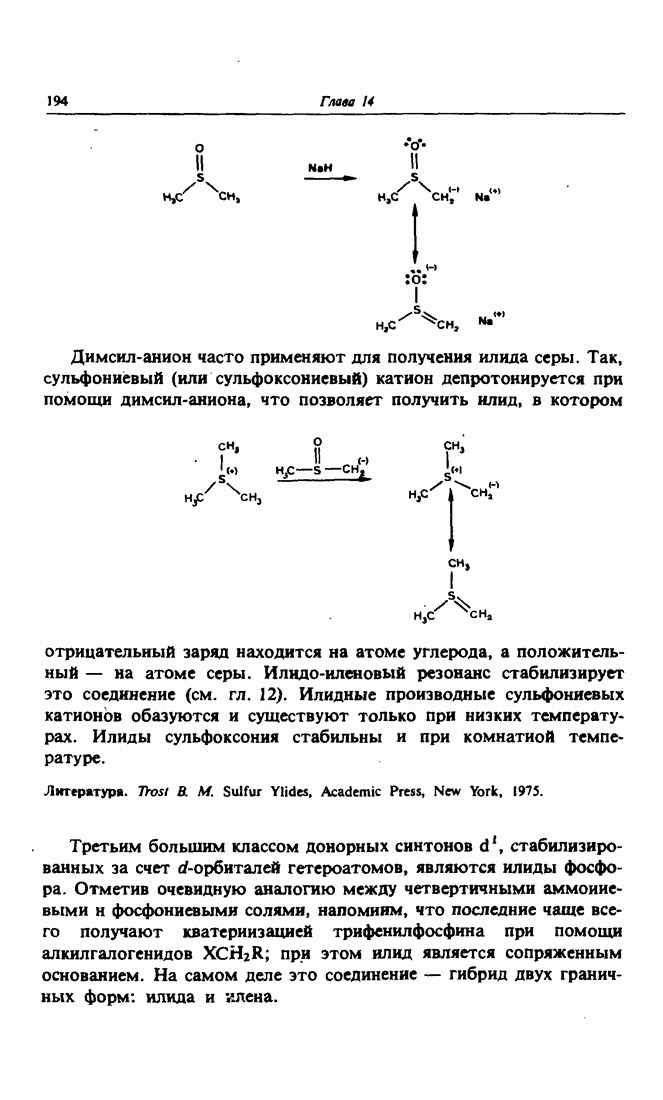
| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
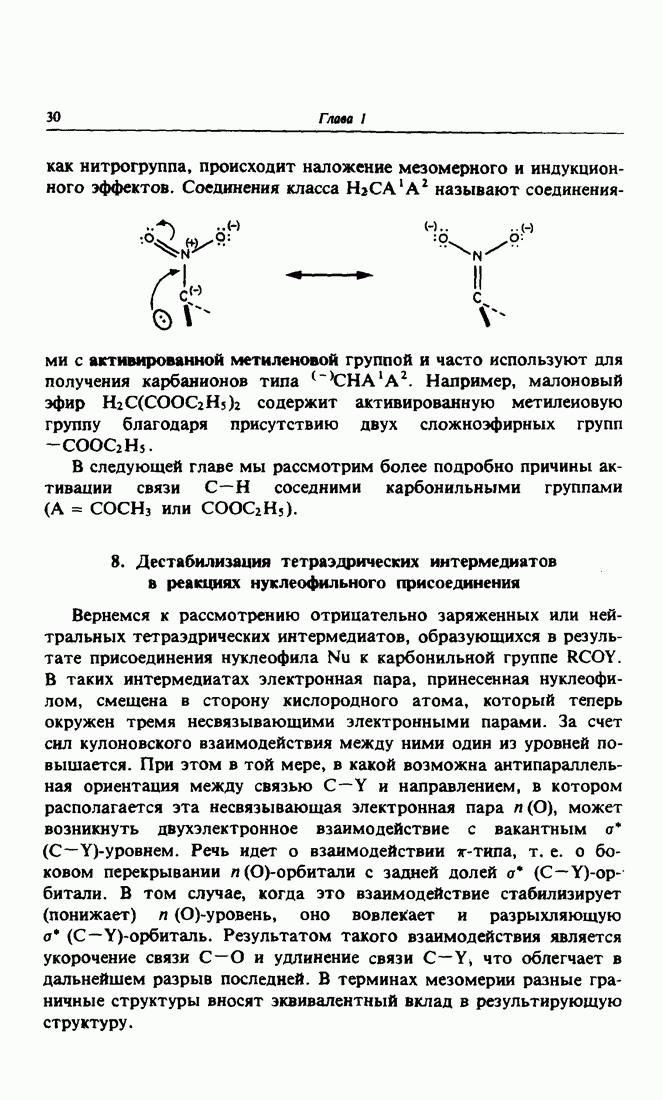
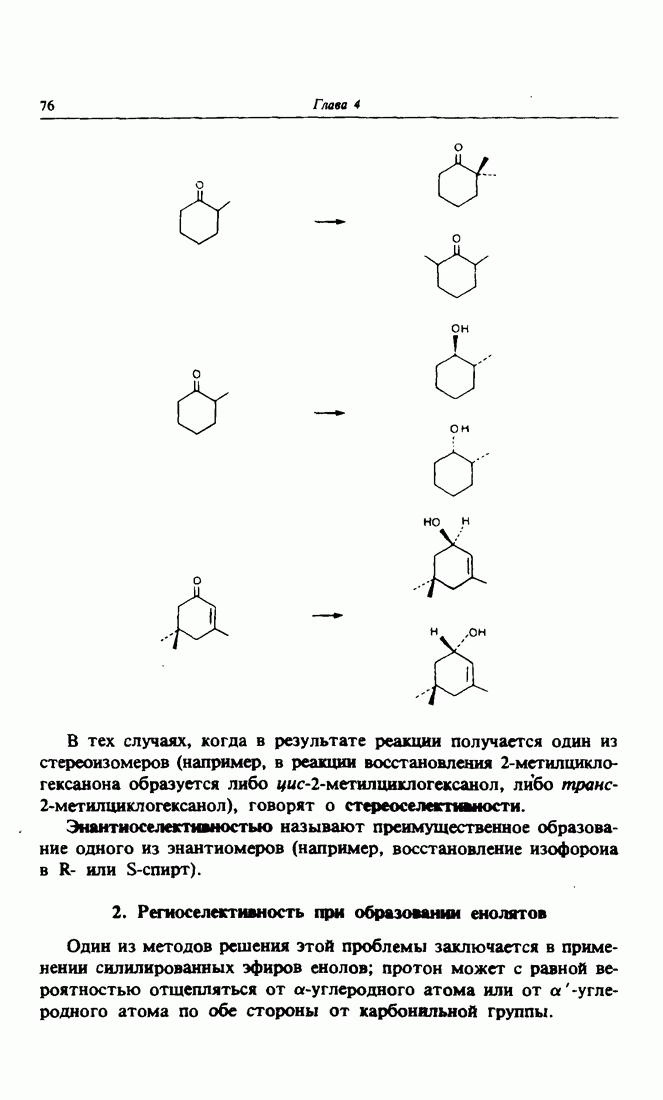
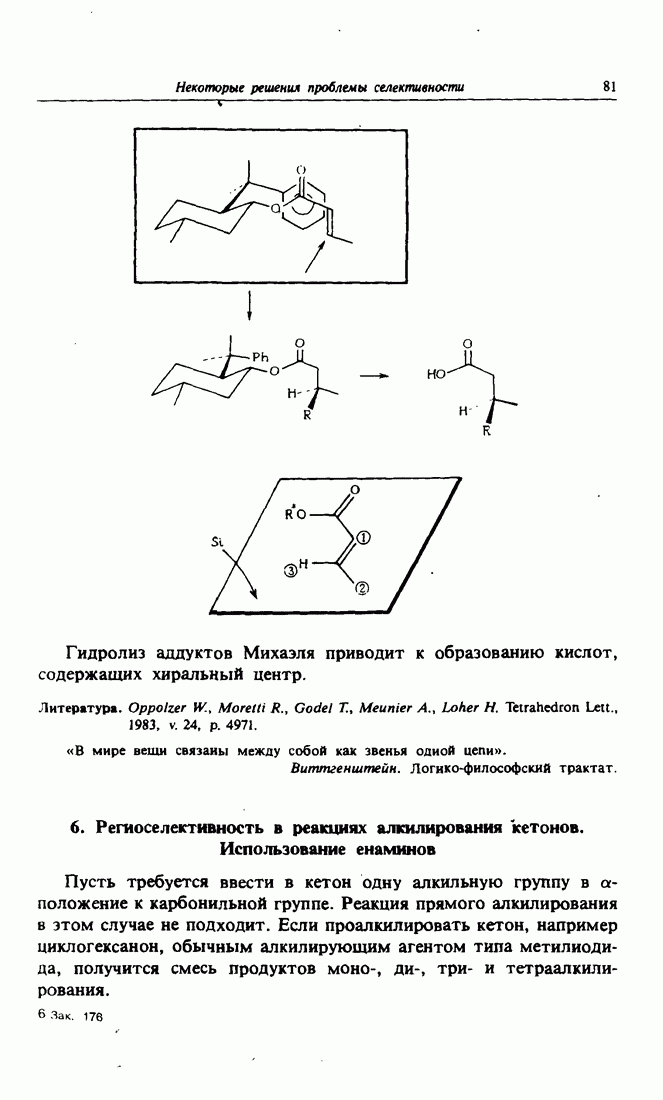
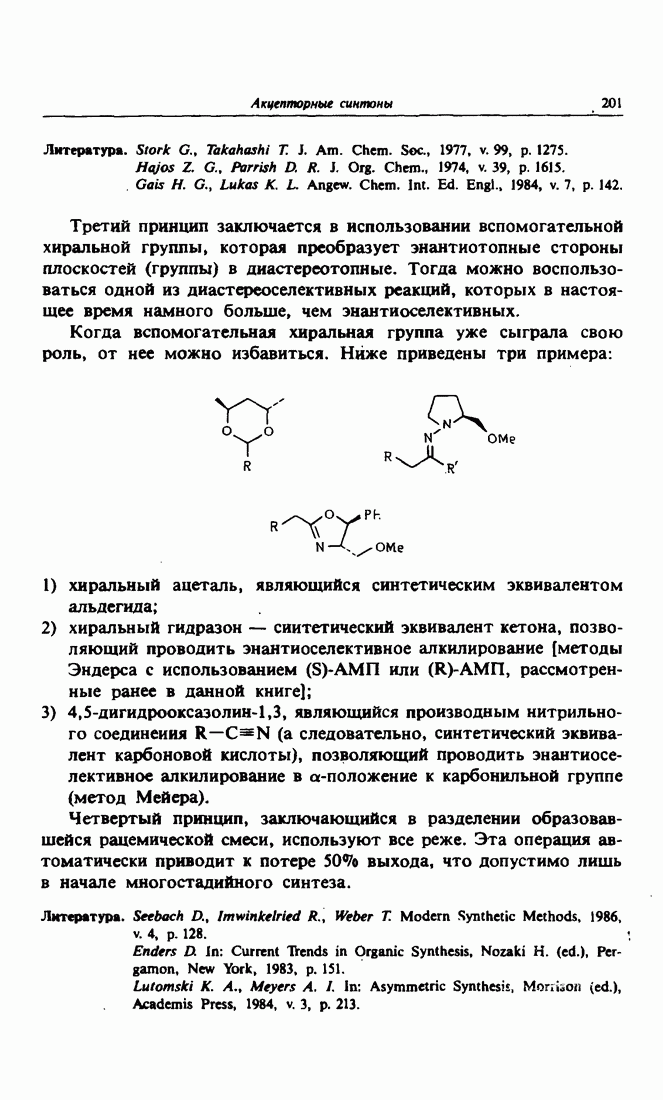
6. Получение различных металлоорганических производных
Рассмотрим более подробно использование карбанионов  в качестве нуклеофила. Они могут быть получены тремя основными методами:
в качестве нуклеофила. Они могут быть получены тремя основными методами:
1. Отщеплением протона от углеводорода  при помощи основания, причем отрыв протона от ацетиленового углеродного атома происходит быстро, в то время как отщепление протона от тригонального углеродного атома (алкены) или тетраэдрического (алканы) происходит медленно.
при помощи основания, причем отрыв протона от ацетиленового углеродного атома происходит быстро, в то время как отщепление протона от тригонального углеродного атома (алкены) или тетраэдрического (алканы) происходит медленно.
2. Реакцией обмена галогена X на одновалентный металл  в алкилгалогенидах
в алкилгалогенидах 
3. Введением двухвалентного металла, например магния, по связи  в алкилгалогенидах.
в алкилгалогенидах.

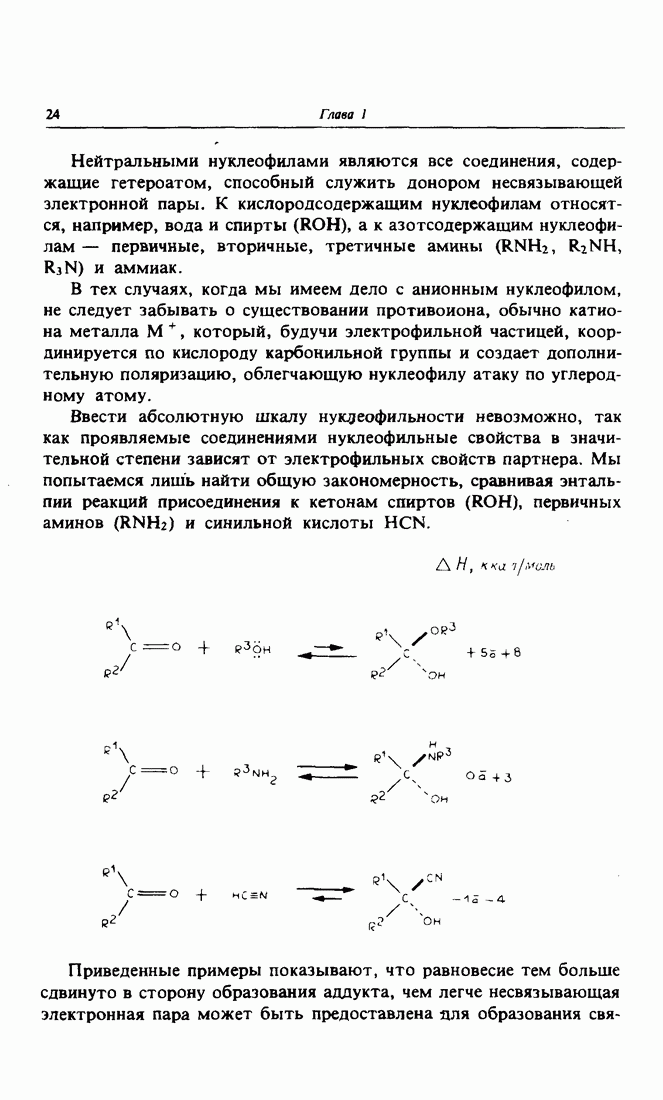
Нуклеофильное присоединение, как правило, представляет собой быструю реакцию по сравнению с «медленным переносом» протона и медленную по сравнению с «быстрым переносом» протона. Независимо от того, что происходит — нуклеофильное присоединение или перенос протона — скорость реакции определяется величиной  кислоты, сопряженной с основанием, которое образуется в результате обоих процессов; таким образом, наиболее выгодным является образование самого слабого основания. Предположим, например, что ацетилацетон реагирует с соединением
кислоты, сопряженной с основанием, которое образуется в результате обоих процессов; таким образом, наиболее выгодным является образование самого слабого основания. Предположим, например, что ацетилацетон реагирует с соединением  Если
Если  нуклеофил, то в результате реакции присоединения образуется алкоголят. В том случае, когда
нуклеофил, то в результате реакции присоединения образуется алкоголят. В том случае, когда  поведет себя как основание, перенос протона сопровождается образованием значительно более слабого сопряженного основания. Второй процесс будет преобладать, что и наблюдается на практике. Перенос протона связи
поведет себя как основание, перенос протона сопровождается образованием значительно более слабого сопряженного основания. Второй процесс будет преобладать, что и наблюдается на практике. Перенос протона связи  или
или  где X — галоген, также происходит очень
где X — галоген, также происходит очень

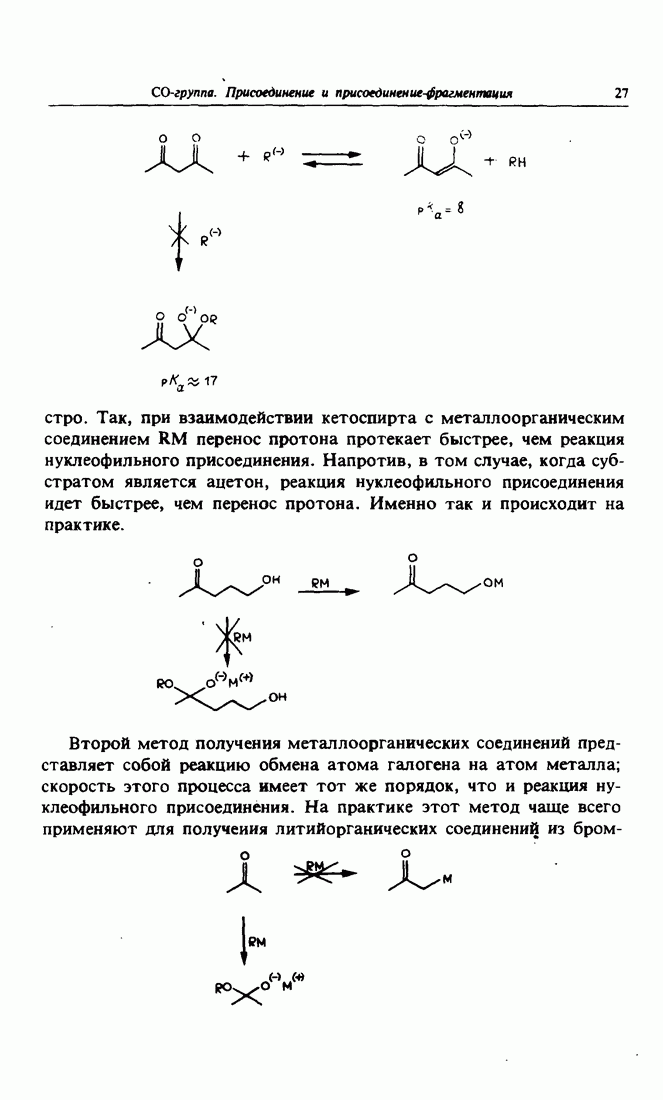
быстро. Так, при взаимодействии кетоспирта с металлоорганическим соединением  перенос протона протекает быстрее, чем реакция нуклеофильного присоединения. Напротив, в том случае, когда субстратом является ацетон, реакция нуклеофильного присоединения идет быстрее, чем перенос протона. Именно так и происходит на практике.
перенос протона протекает быстрее, чем реакция нуклеофильного присоединения. Напротив, в том случае, когда субстратом является ацетон, реакция нуклеофильного присоединения идет быстрее, чем перенос протона. Именно так и происходит на практике.

Второй метод получения металлоорганических соединений представляет собой реакцию обмена атома галогена на атом металла; скорость этого процесса имеет тот же порядок, что и реакция нуклеофильного присоединения. На практике этот метод чаще всего применяют для получения литийорганических соединений из

бром- или иодалкаиов, а иногда из хлоралканов (но ни в коем случае не из фторалканов). Литийорганические соединения существуют в виде олигомеров  обычно равно 4—6).
обычно равно 4—6).

Органокупраты, типа  также получают в виде олигомеров
также получают в виде олигомеров 
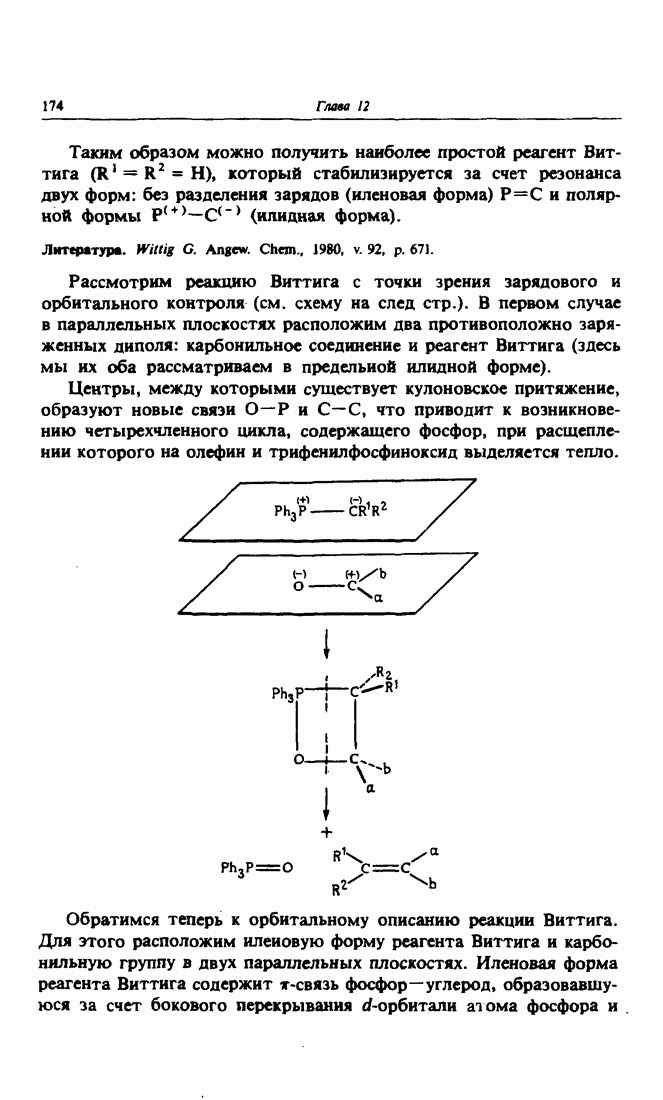
В реакциях присоединения металлоорганических реагентов  с карбонильными соединениями катион металла
с карбонильными соединениями катион металла  взаимодействует с кислородом, а карбанион
взаимодействует с кислородом, а карбанион  присоединяется по углероду карбонильной группы. Образуется тетраэдрический отрицательно заряженный интермедиат. При выделении продуктов реакции происходит замена катиона металла
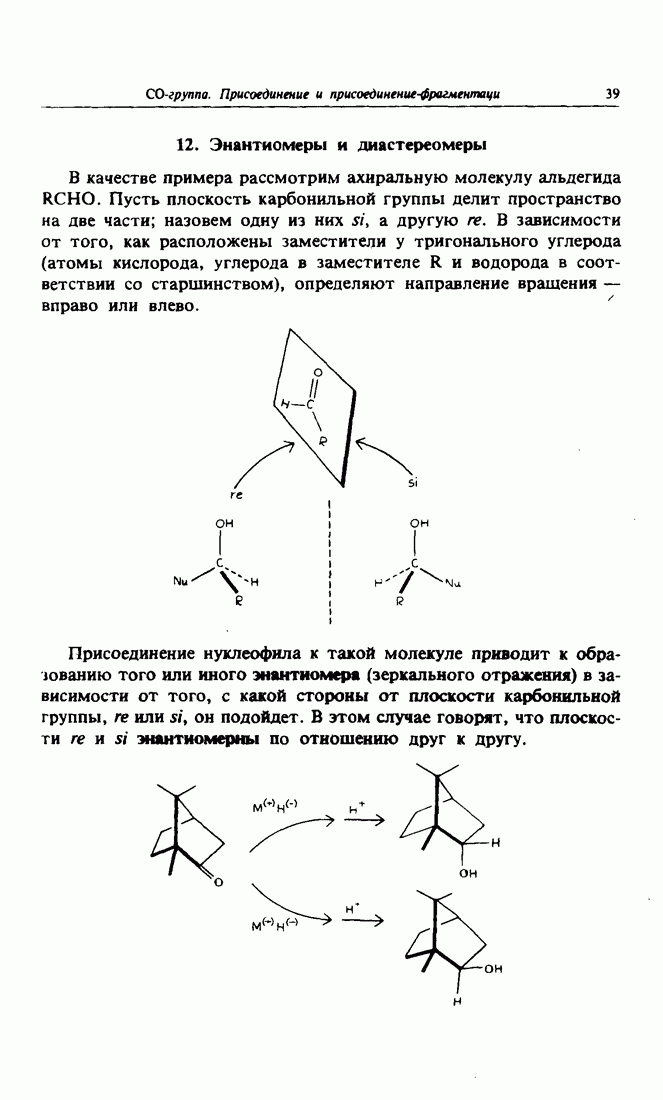
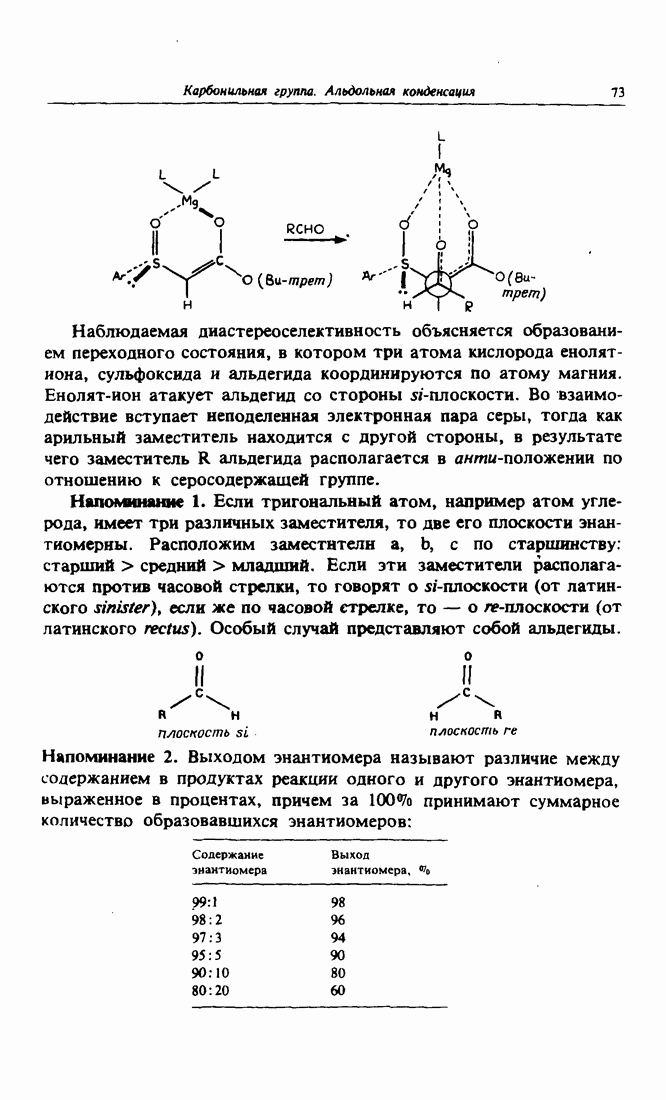
присоединяется по углероду карбонильной группы. Образуется тетраэдрический отрицательно заряженный интермедиат. При выделении продуктов реакции происходит замена катиона металла  на протон (реакция кислотного гидролиза), т. е. из алкоголята (алкоксида), являющегося промежуточным соединением, образуется спирт (для каждой из двух плоскостей приведено по одному энантиомеру). Таким образом, вторичные и третичные спирты можно получить реакцией присоединения металлоорганических соединений к альдегидам и кетонам.
на протон (реакция кислотного гидролиза), т. е. из алкоголята (алкоксида), являющегося промежуточным соединением, образуется спирт (для каждой из двух плоскостей приведено по одному энантиомеру). Таким образом, вторичные и третичные спирты можно получить реакцией присоединения металлоорганических соединений к альдегидам и кетонам.

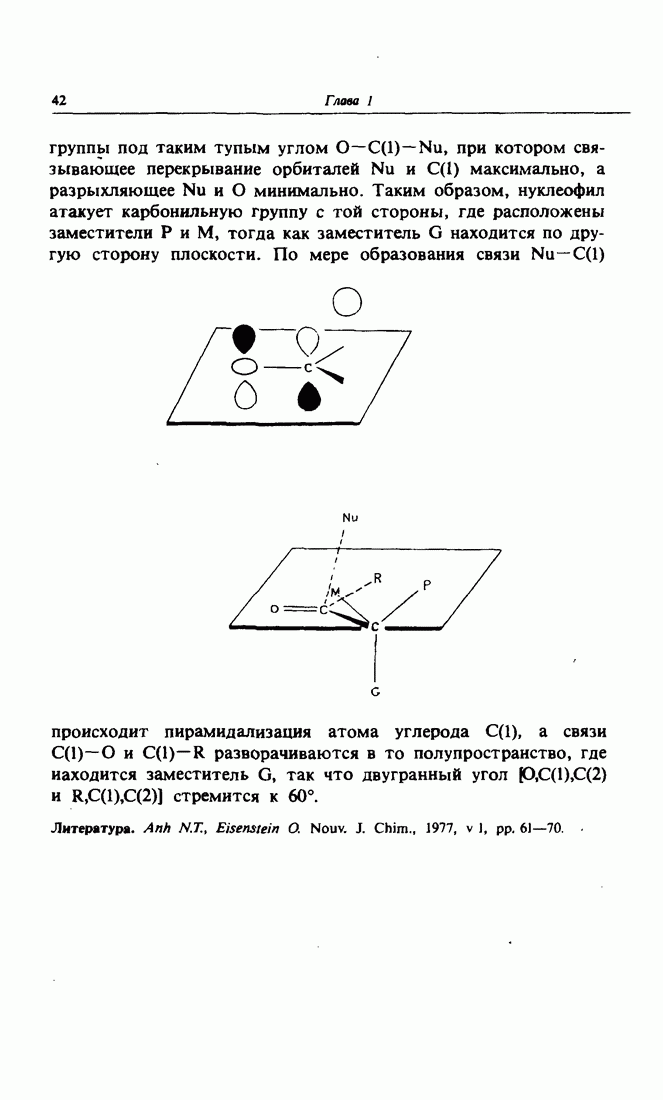
В качестве модельной была выбрана реакция формальдегида и метиллития, для которой было рассчитано, что в переходном состоянии катион лития взаимодействует с двумя центрами, несущими отрицательный заряд, — атомом кислорода карбонильной группы и атомом углерода метиленовой группы. В процессе реакции

происходит восстановление карбонильной группы, однако угол между связями  и
и  остается тупым (106° 94°). Углеродный атом карбонильной группы становится тетраэдрическим; при этом происходит смещение связей
остается тупым (106° 94°). Углеродный атом карбонильной группы становится тетраэдрическим; при этом происходит смещение связей  по обе стороны углерод-углеродной связи.
по обе стороны углерод-углеродной связи.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- ВВЕДЕНИЕ
- 1. Орбитальный и зарядовый контроль
- 2. Жесткие и мягкие кислоты и основания
- 3. Термохимические данные и их применение
- Глава 1. КАРБОНИЛЬНАЯ ГРУППА. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ПРИСОЕДИНЕНИЯ-ФРАГМЕНТАЦИИ
- 1. Карбонильная группа. Простое орбитальное описание
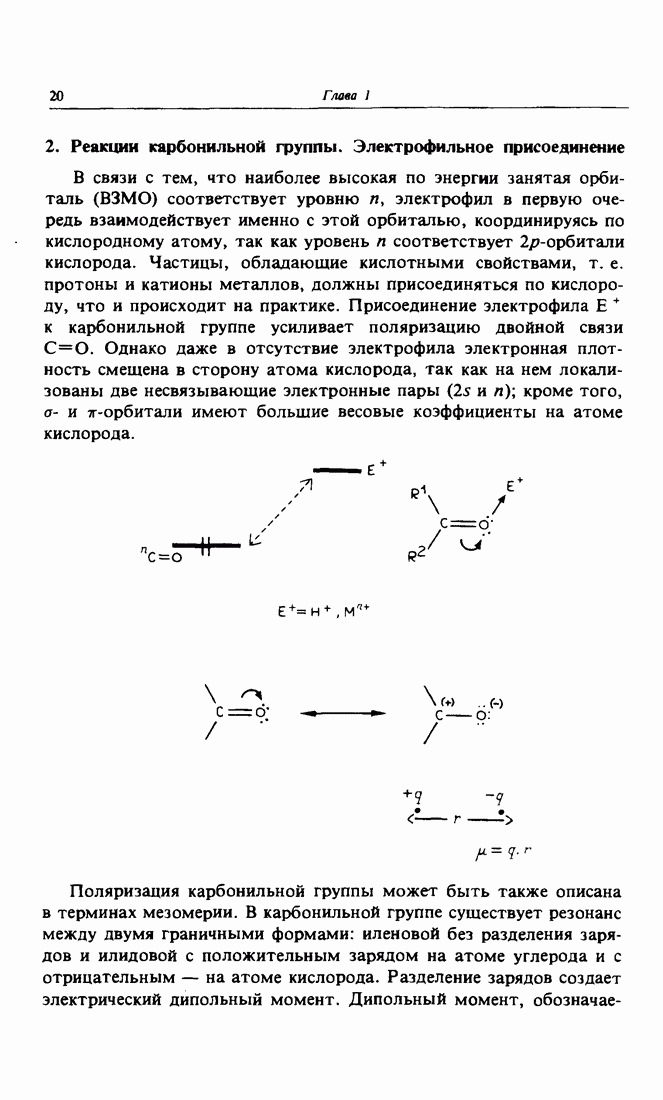
- 2. Реакции карбонильной группы. Электрофильное присоединение
- 3. Основность и нуклеофильность
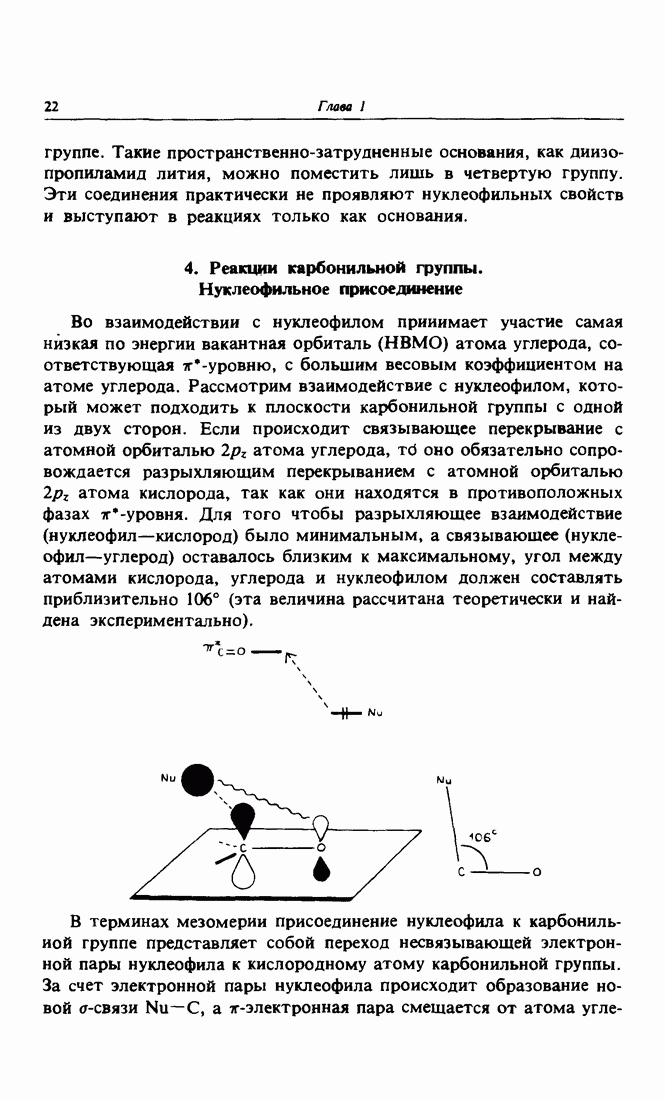
- 4 Реакции карбонильной группы. Нуклеофильное присоединение
- 5. Защита и регенерация
- 6. Получение различных металлоорганических производных
- 7. Активированная метиленовая группа
- 8. Дестабилизация тетраэдрических интермедиатов в реакциях нуклеофильного присоединения
- 9. Реакции присоединения-фрагментации
- 10. Восстановление гидридами металлов
- 11. Описание конфигурации асимметрического атома углерода
- 12. Энантиомеры и диастереомеры
- 13. Асимметрическая 1,2-индукция
- Глава 2. КАРБОНИЛЬНАЯ ГРУППА. ЕНОЛИЗАЦИЯ. КОНДЕНСАЦИЯ ПО МИХАЭЛЮ
- 1. Кето-енольное равновесие
- 2. Катализ кето-енольного равновесия
- 3. Стереохимия и реакция енолнэации
- 4. Причины ослабления связи Ca-H в кетонах
- 5. Еноляты и их получение
- 6. Эфиры енолов
- 7. Конфигурация енолов и эфиров енолов
- 8. Реакция Михаэля
- 9. Артур Михаэль
- 10. Региоселективность в реакции Михаэля
- 11. Применение органокулратов
- 12. Современный вариант реакции Михаэля
- 13. Сопряжение или отсутствие сопряжения?
- 14. Циклизация по Робинсону
- 15. Сэр Роберт Робинсон
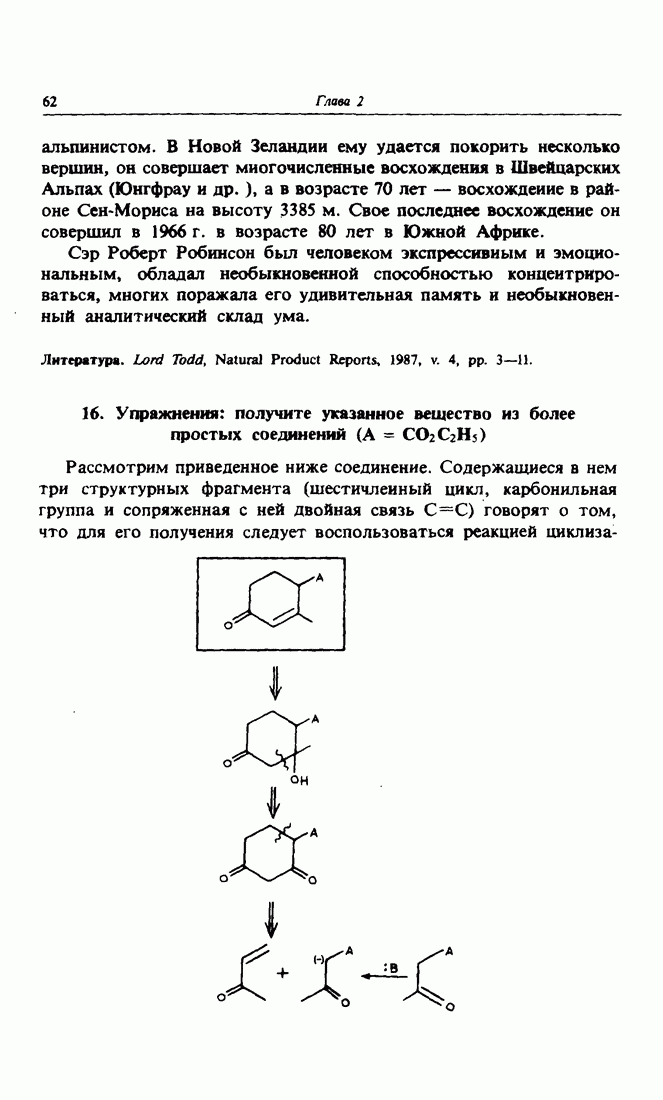
- 16. Упражнения: получите указанное вещество из более простых соединений (A=CO2C2H5)
- Глава 3. КАРБОНИЛЬНАЯ ГРУППА. АЛЬДОЛЬНАЯ КОНДЕНСАЦИЯ
- 2. Устойчивость продуктов альдольиой конденсации
- 3. Управление реакцией альдольной конденсации: доноры и акцепторы
- 4. Управление реакцией альдольной конденсации: син- и анти-диастереомеры
- 5. Стереоселективные реакции альдольной конденсации
- Глава 4. НЕКОТОРЫЕ РЕШЕНИЯ ПРОБЛЕМЫ СЕЛЕКТИВНОСТИ (ХИМИЧЕСКАЯ, РЕГИО- И СТЕРЕОСЕЛЕКТИВНОСТЬ)
- 2. Региоселективность при образовании енолятов
- 3. Селективное получение Е- и Z-енолятов
- 4. Двойной принцип стереоселективности
- 5. Энантиоселективная реакция Михаэля
- 6. Региоселективность в реакциях алкилирования кетонов. Использование енаминов
- 7. Получение хирального центра путем алкилирования енаминов
- 8. Энантиоселективное алкилирование енаминов
- 9. Перенос хиральности
- 10. Соотношение между реакционноспособностью и селективностью
- 11. Стереоэлектронный эффект
- 12. Конформации переходного состояния «кресло» и «ванна»
- Глава 5. ЗАЩИТА И РЕГЕНЕРАЦИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП. СПИРТОВАЯ И КАРБОНИЛЬНАЯ ГРУППЫ. ОБРАЩЕНИЕ ПОЛЯРНОСТИ
- 1. Защита карбонильной группы ацетальной
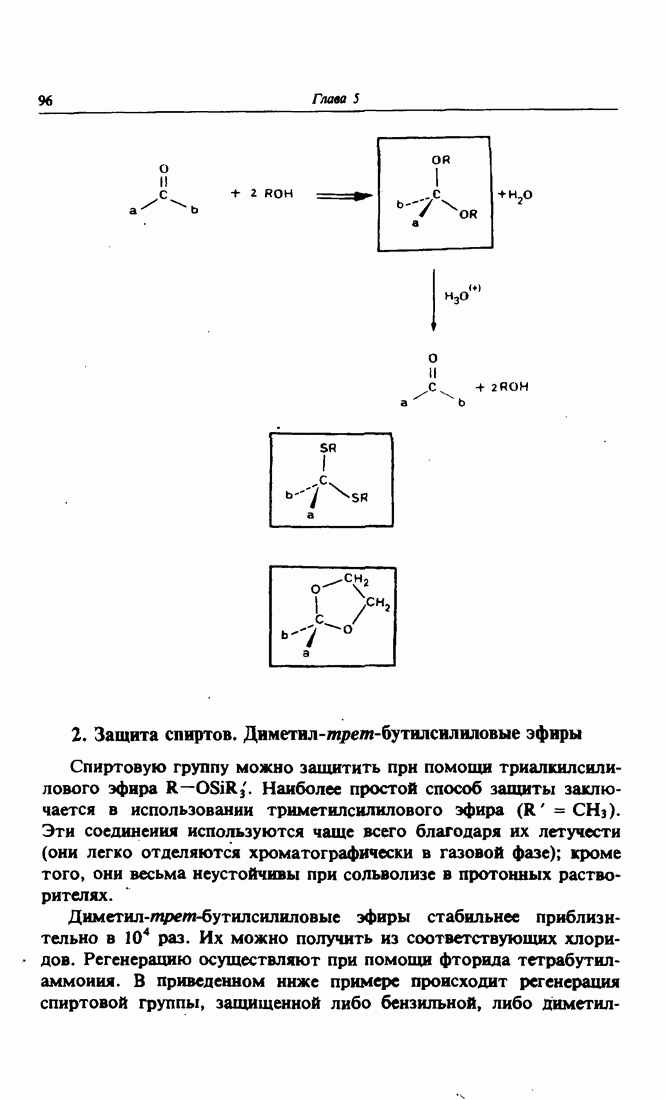
- 2. Защита спиртов. Диметил-трет-бутилсилиловые эфиры
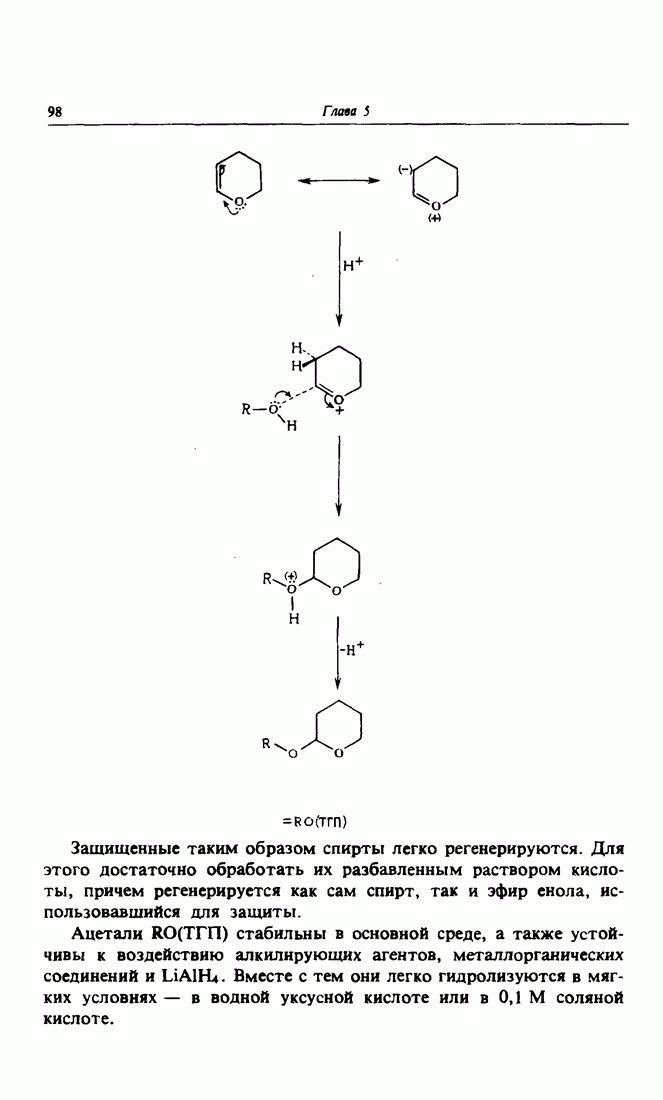
- 3. Защита спиртовых групп при помощи эфиров енолов
- 4. Обращение полярности
- 5. Э. Дж. Кори
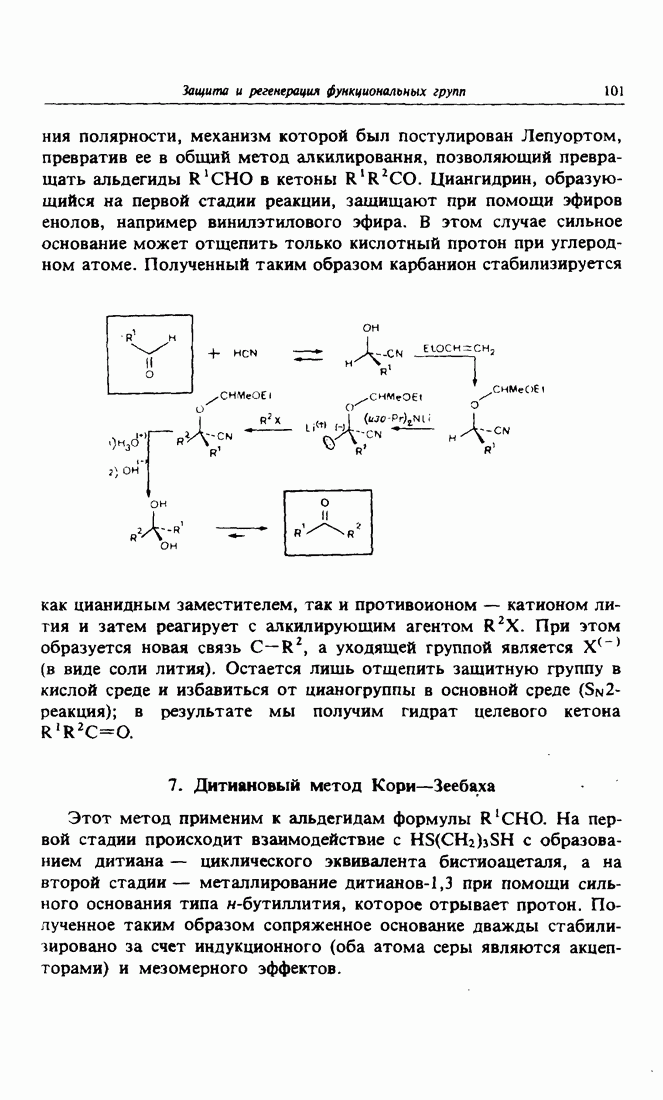
- 6. Инверсия полярности по методу Лепуорта — Шторка
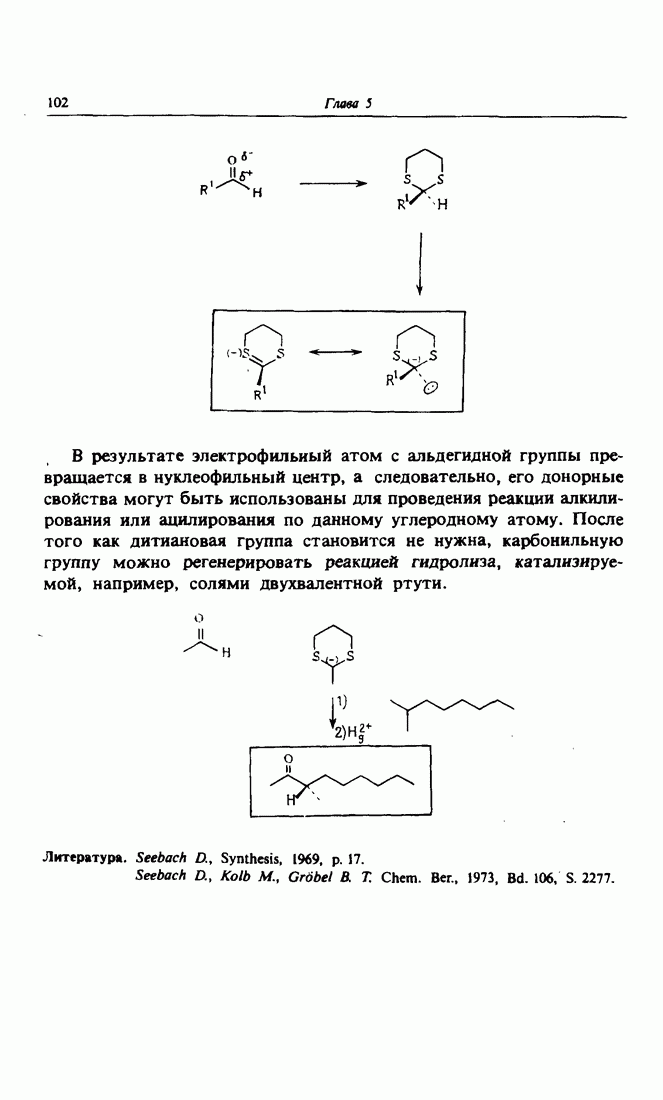
- 7. Дитиановый метод Кори-Зеебаха
- Главе 6. АКТИВАЦИЯ
- 2. Стабилизация конечного состояния
- 3. Дестабилизация начального состояния
- 4. Стабилизация переходного состояния
- Главв 7. ПОСТРОЕНИЕ ЦИКЛОВ
- 2. Региоселективность
- 3. Реакция Дильса — Альдера в условиях обращенного электронного соответствия
- 4. Стереоселективность в реакциях Дильса — Альдера
- 5. Напряжение в циклах
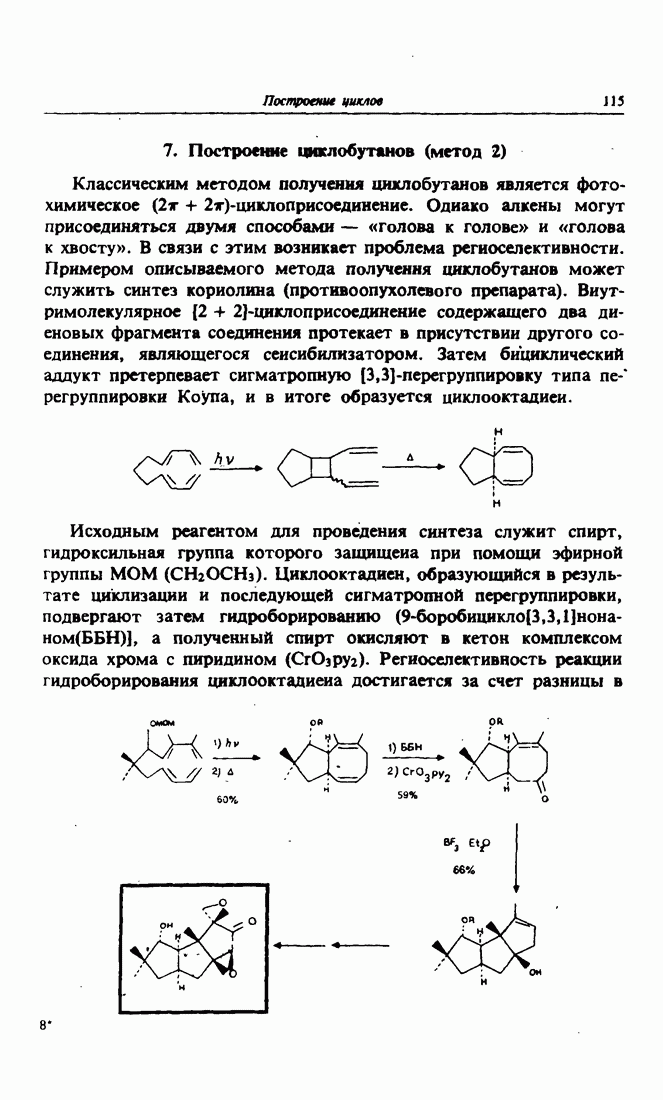
- 6. Построение циклобутанов (метод 1) Термическая димеризация
- 7. Построение циклобутанов (метод 2)
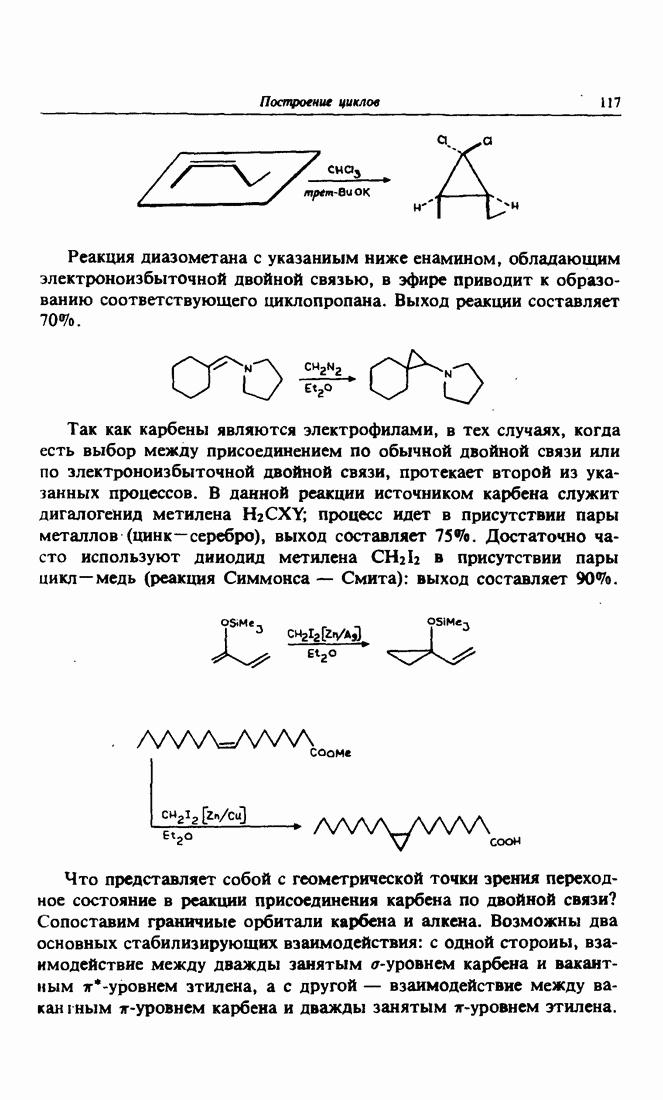
- 8. Синтез циклопропанов. Присоединение карбенов к алкенам
- Глааа 8. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ЗАМЕЩЕНИЯ
- 2. Соотношение структура — реакционноспособность
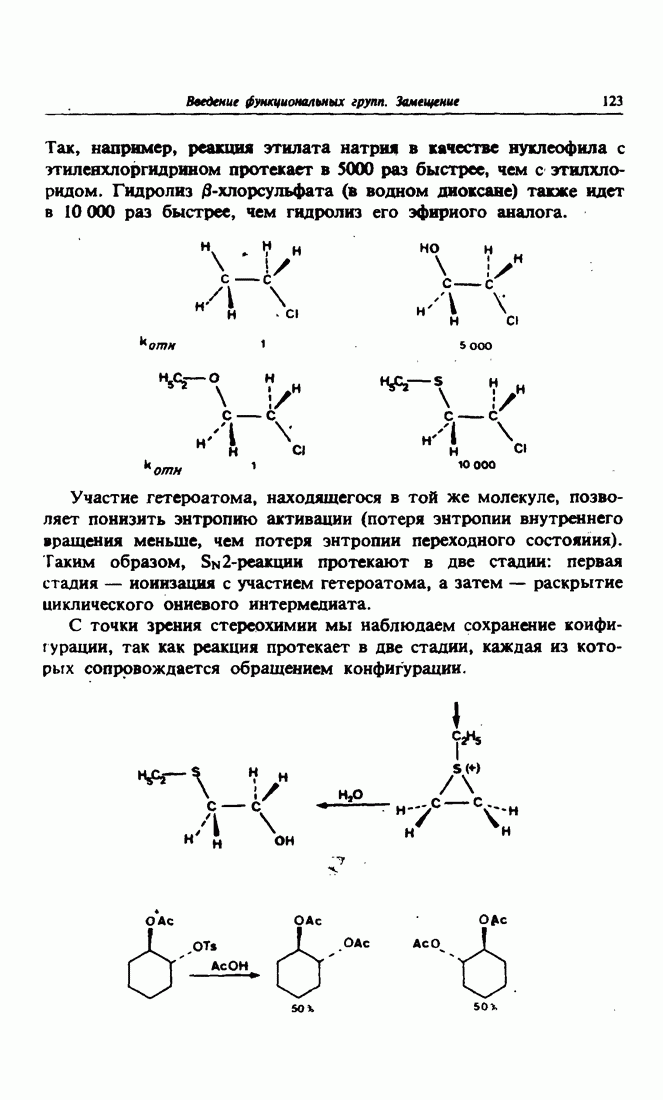
- 3. Участие соседней группы в Sn2-реакциях
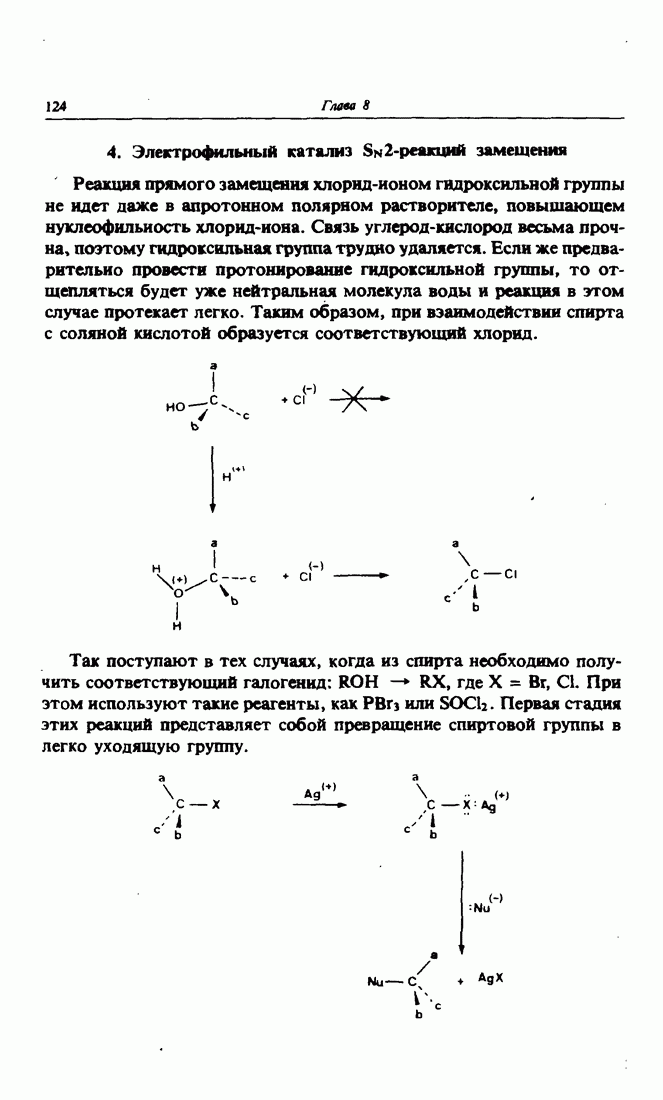
- 4. Электрофильный катализ Sn2-реакций замещения
- 5. Региоселеггивность в реакциях алкилирования
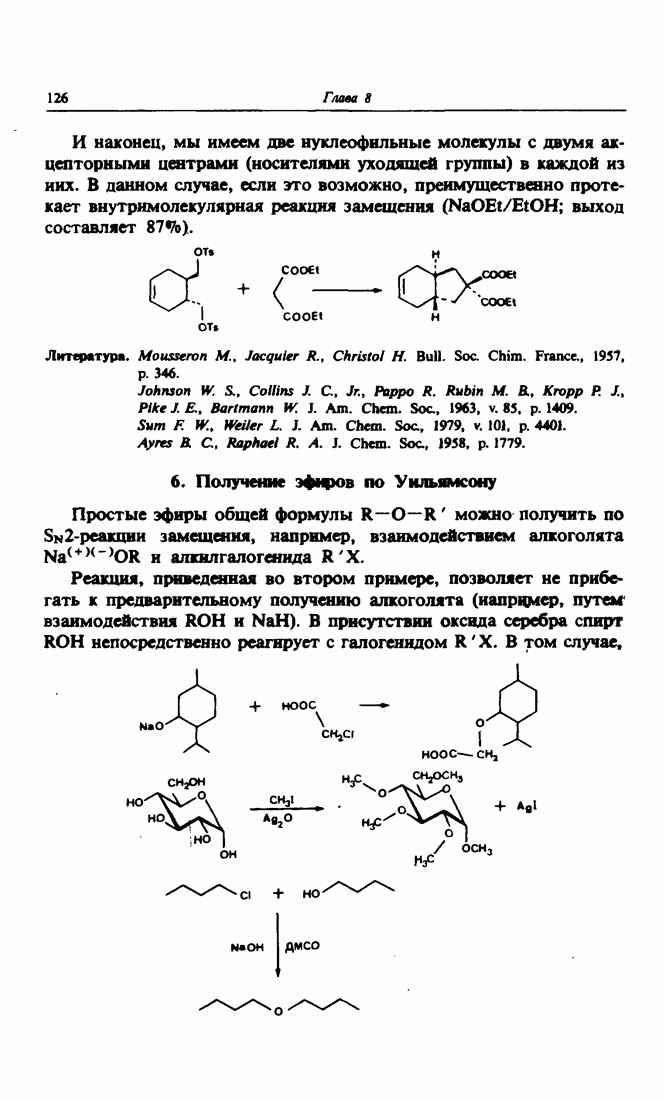
- 6. Получение эфиров по Уильямсону
- 7. К вопросу об обозначениях
- Глава 9. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ВОССТАНОВЛЕНИЯ
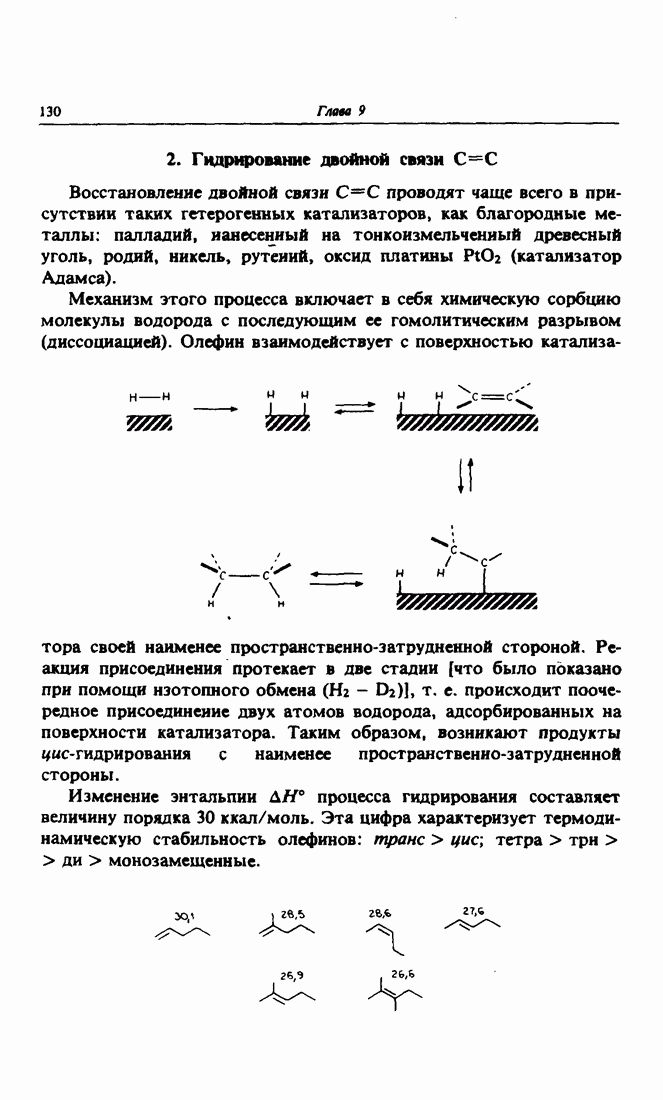
- 2. Гидрирование двойной связи С=С
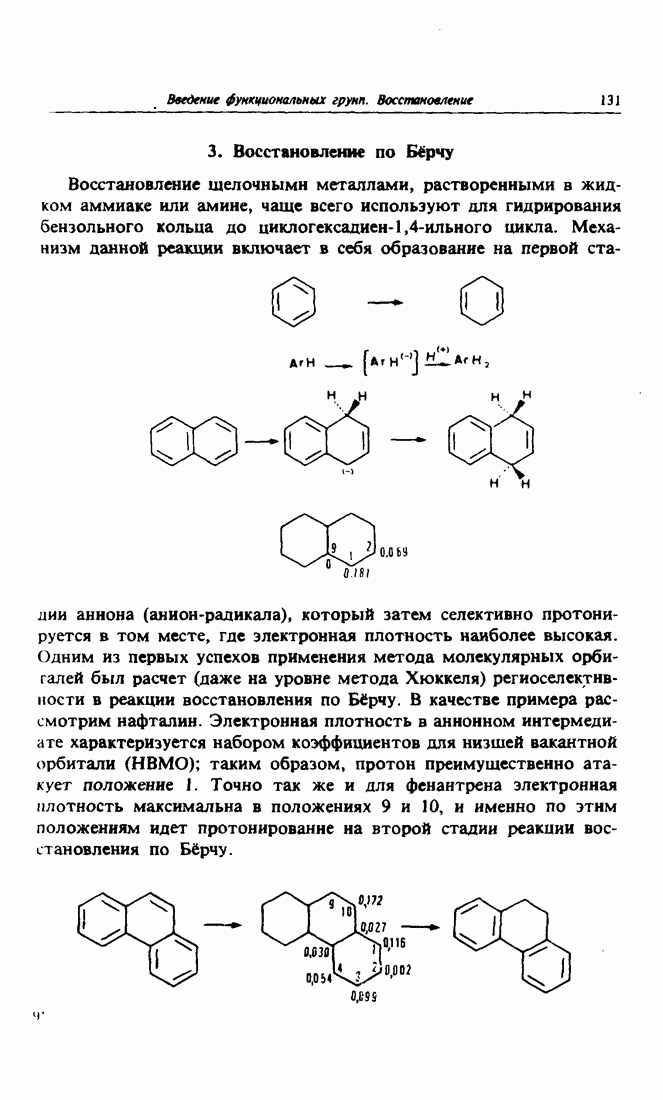
- 3. Восстановление по Бёрчу
- 4. Восстановление карбонильной группы
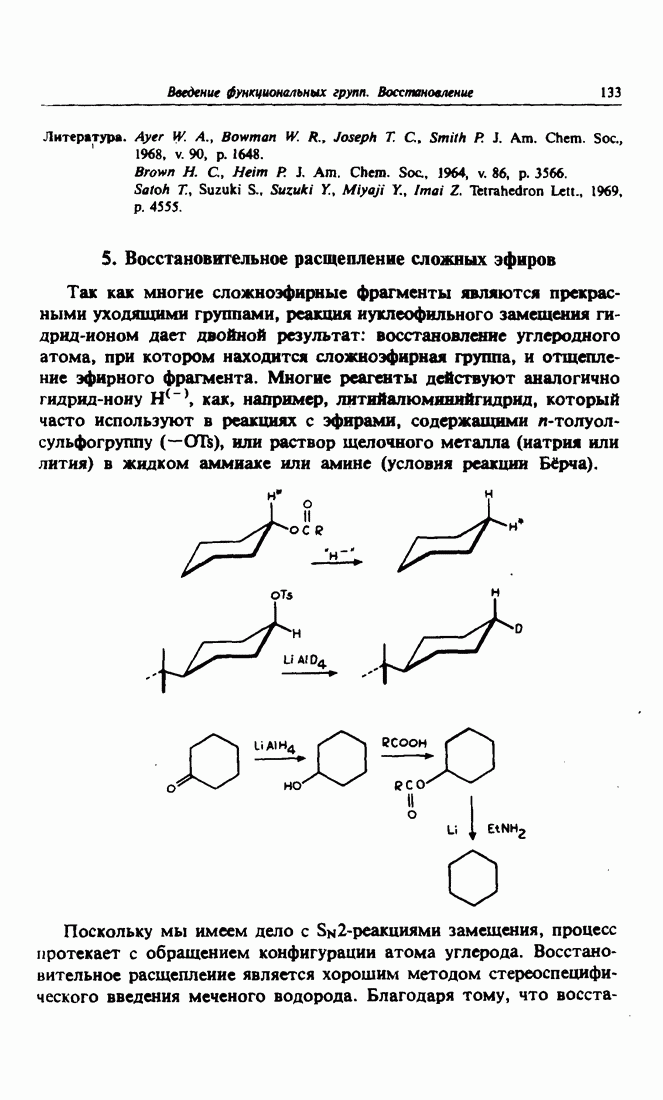
- 5. Восстановительное расщепление сложных эфиров
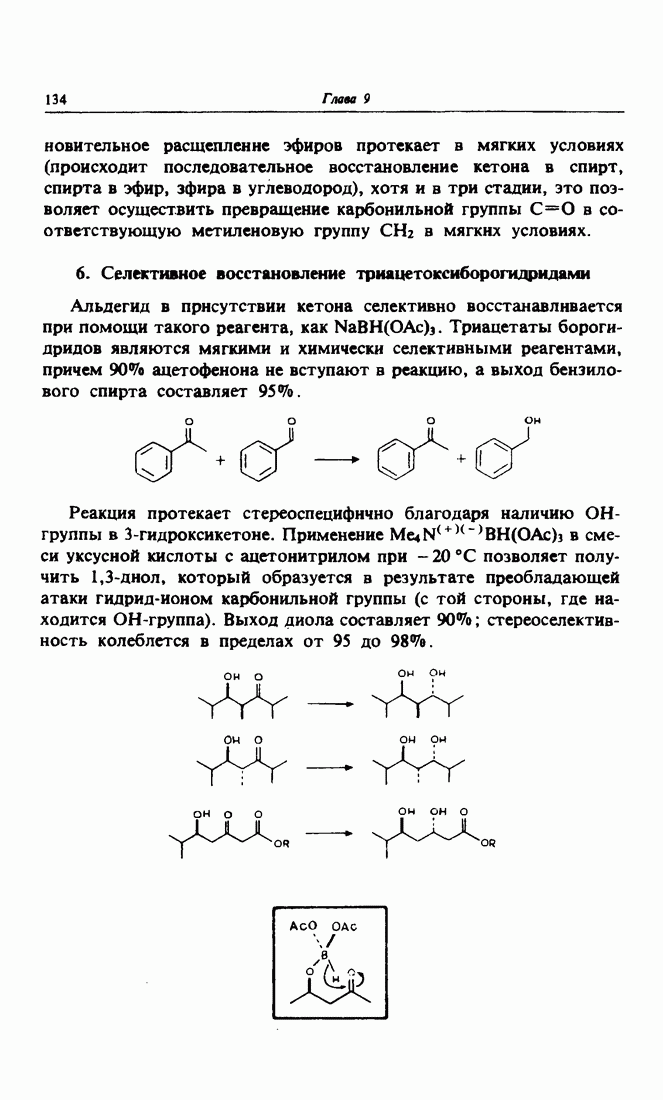
- 6. Селективное восстановление триацетоксиборогидридами
- Глава 10. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ОКИСЛЕНИЯ
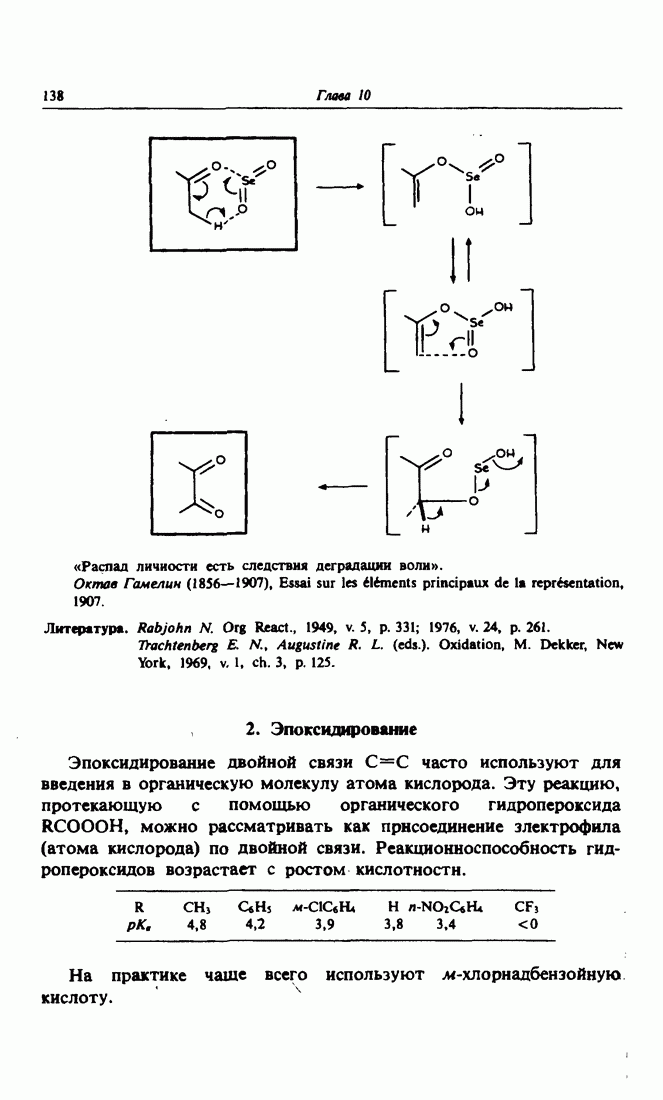
- 2. Эпоксидирование
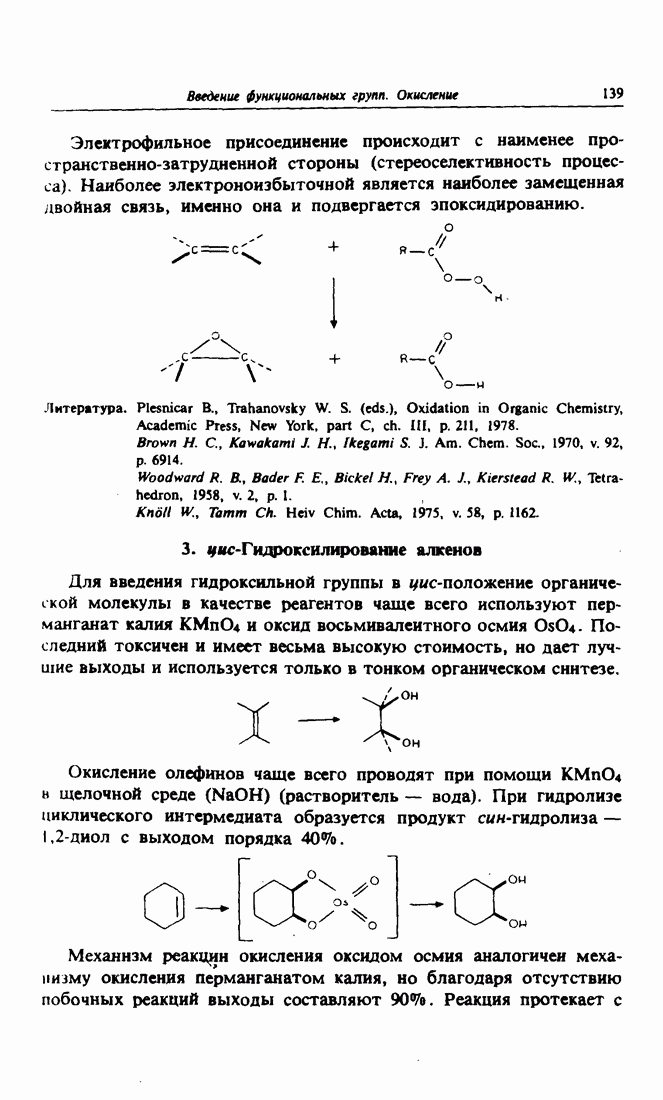
- 3. цис-Гидроксилирование алкенов
- 4. Расщепление 1,2-диолов
- 5. Озонолиз алкенов
- 6. Окисление спиртов
- Главе 11. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ЭЛИМИНИРОВАНИЯ
- 2. Классически механизм реакции электрофильного присоединения. Правило Марковникова
- 3. Основные электрофильные агенты
- 3.3. Присоединение гипохлоритов и гипобромитов
- 3.4. Оксимеркурирование
- 3.5. Гидроборирование
- 3.6. Окситаллирование
- 4. Стереохимия реакции присоединения по двойной связи С=С
- 5. Конкуренция нуклеофила и растворителя в реакции электрофильного присоединения
- 6. Присоединение к напряженным олефинам: цис-присоединение
- 7. Стереохимия реакций бимолекулярного элиминирования
- 8. Виды b-элиминирования
- Главв 12. ПЕРЕГРУППИРОВКИ ФУНКЦИОНАЛЬНЫХ ГРУПП. ПРЕВРАЩЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ В ОЛЕФИНЫ ПО РЕАКЦИИ ВИТТИГА
- 2. Реакция Дарзана
- 3. Дарзан — один из великих политехников
- 4. Обобщение и модернизация метода
- 5. Стереоселективность реакции Кори — Чайковского
- 6. Реакция Виттига
- 7. Георг Виттиг
- 8. Причины образования различных продуктов в реакциях Виттига и Кори — Чайковского
- 9. Разновидность реакции Виттига: олефинирование по Петерсону
- Главе 13. ПЕРЕГРУППИРОВКИ
- 2. 1,2-Переход в карбокатионах
- 3. Перегруппировка Бекмана
- 4. Перегруппировка Курциуса
- 5. Перегруппировка Байера — Виллигера
- 6. Реакция Рамберга-Беклунда
- Глава 14. ДОНОРНЫЕ СИНТОНЫ
- 2. Алкильные донорные синтоны
- 3. Донорные синтоны d1 с гетероатомами, обладающими d-орбиталью
- Глава 15. АКЦЕПТОРНЫЕ СИНТОНЫ
- 1. Синтоны-акцепторы
- 2. Синтетические эквиваленты
- 3. Контролируемое образование новых связей
- 4. Расчленение молекулы на фрагменты
- 5. Двойное расчленение молекулы
- 6. Изменение реакционноспособности в результате обращения полярности
- Глава 16. РЕТРОСИНТЕТИЧЕСКИЙ АНАЛИЗ
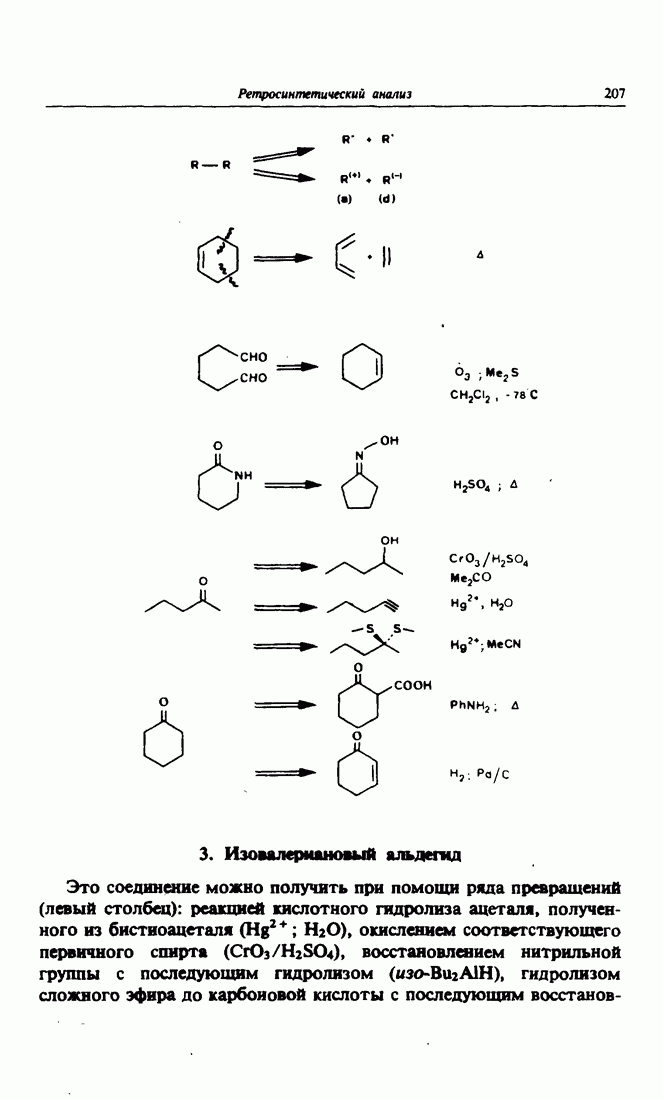
- 2. Цепь превращений
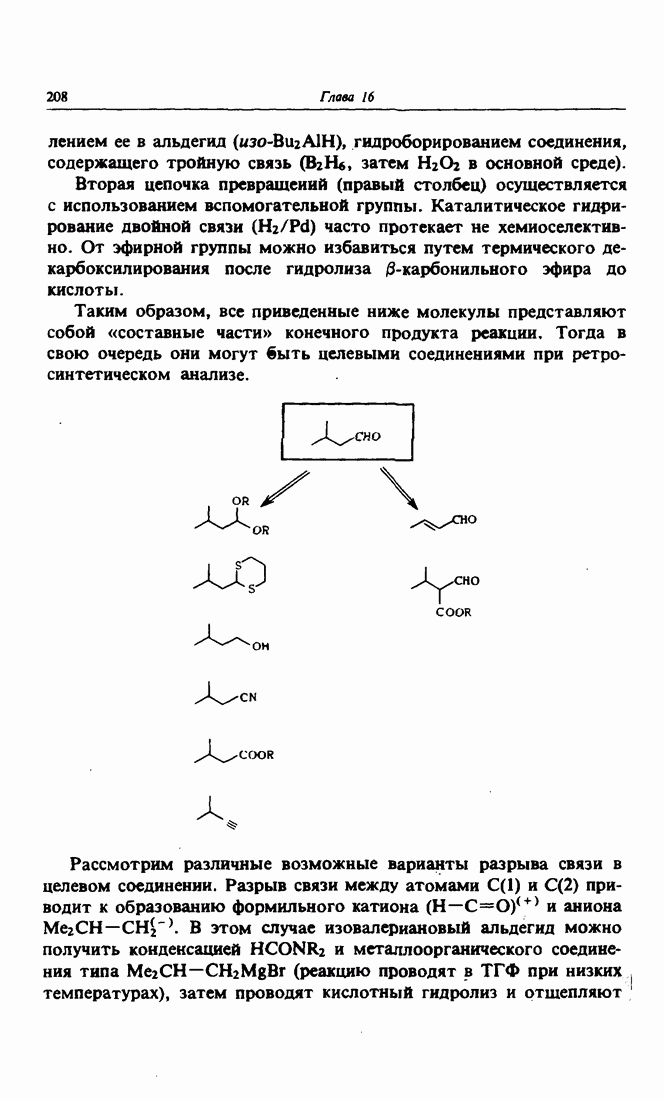
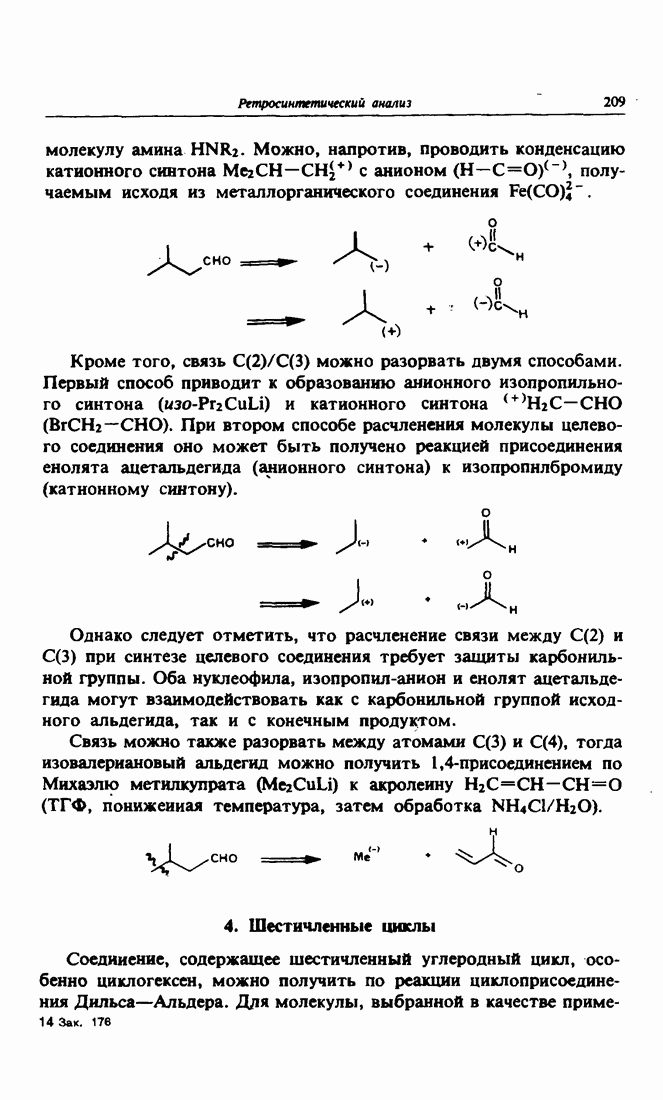
- 3. Изовалериановый альдегид
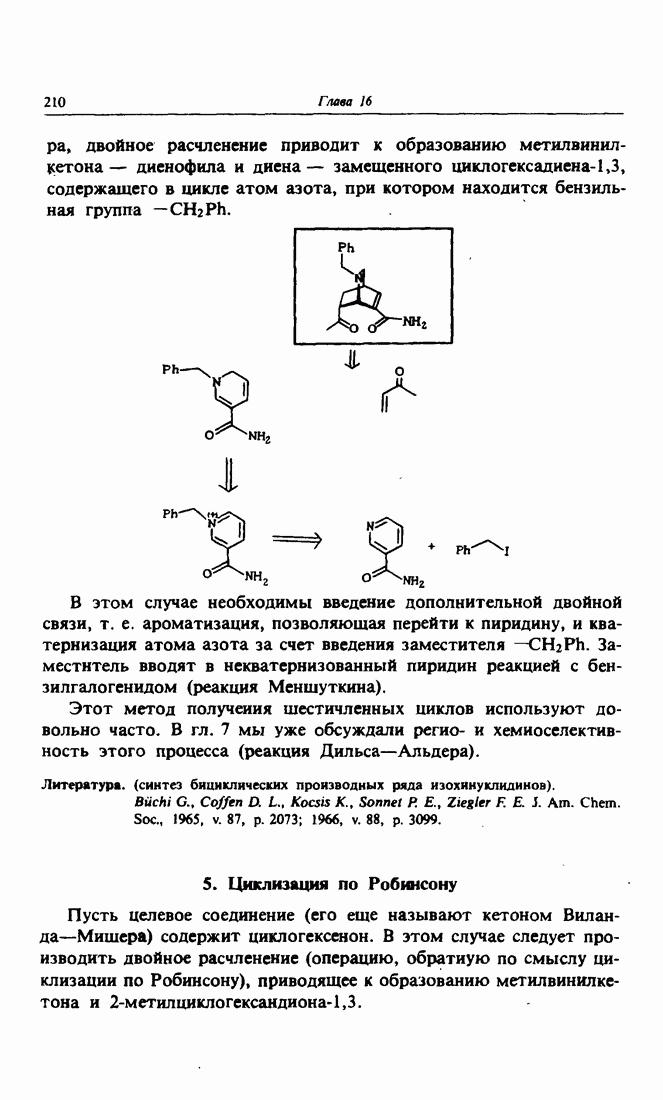
- 4. Шестичленные циклы
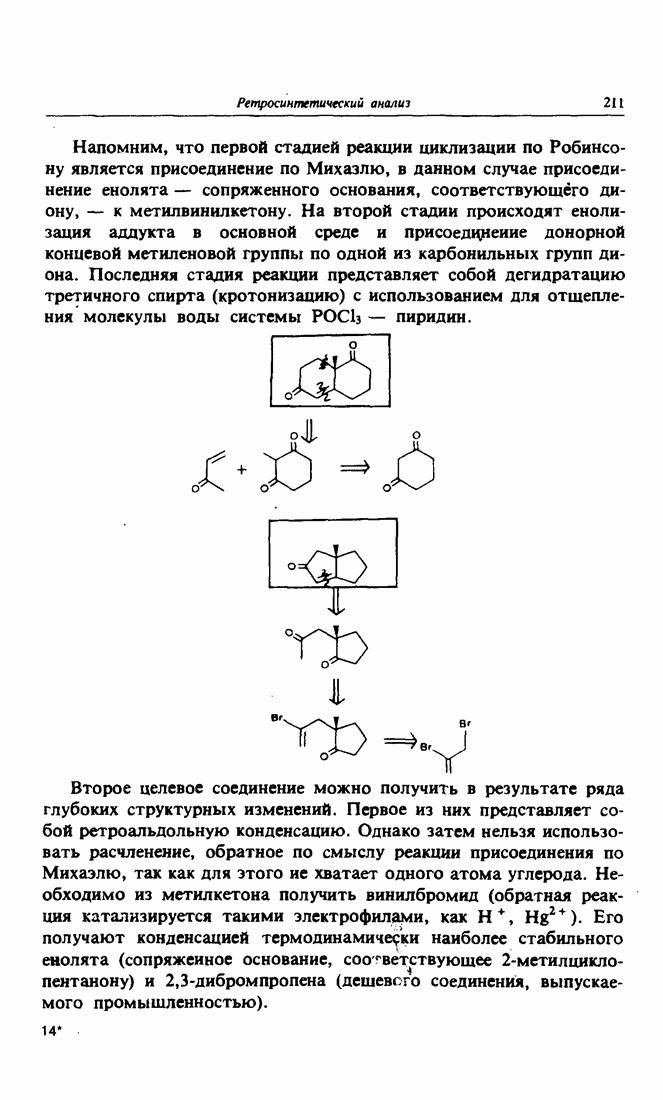
- 5. Циклизация по Робинсону
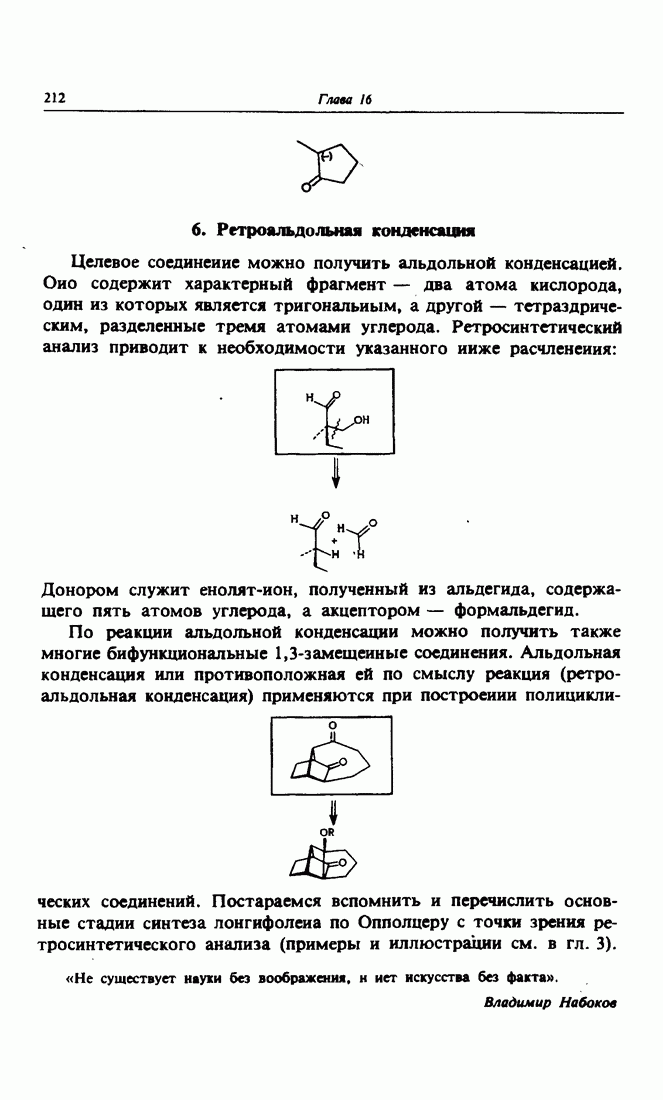
- 6. Ретроальдольная конденсация
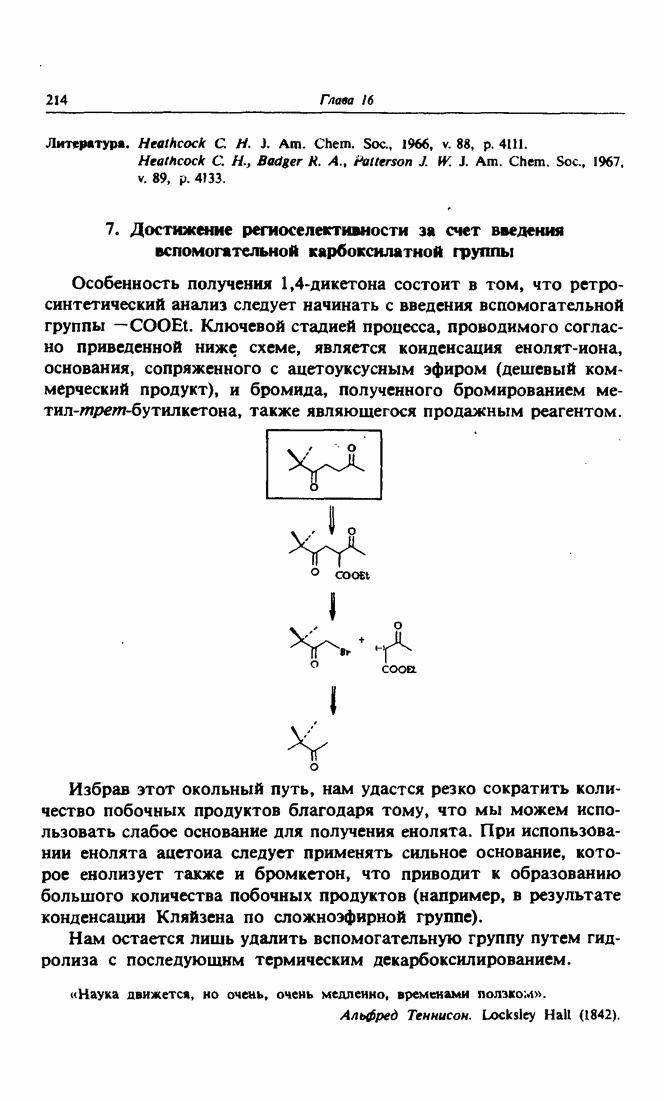
- 7. Достижение региоселективности за счет введения вспомогательной карбоксилатной группы
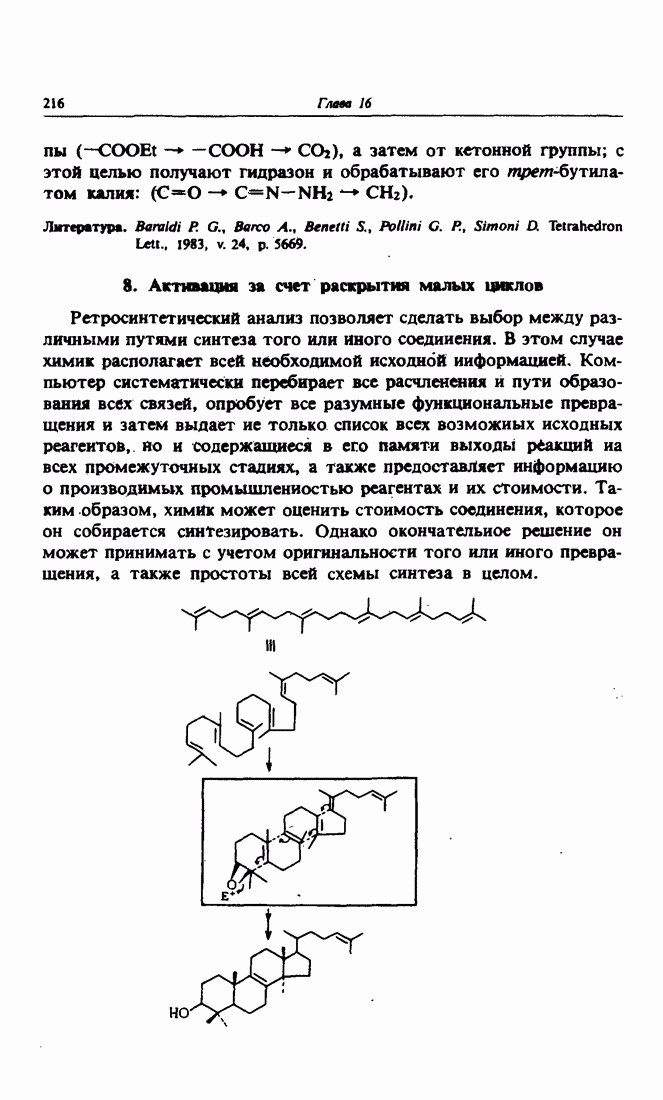
- 8. Активация за счет раскрытия малых циклов
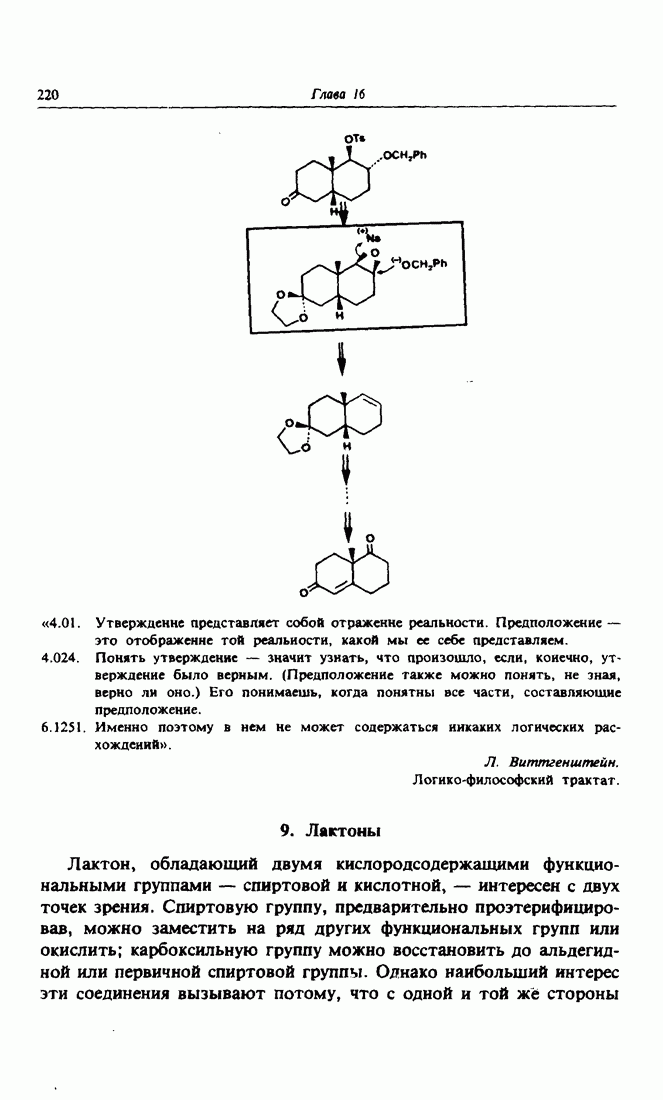
- 9. Лактоны
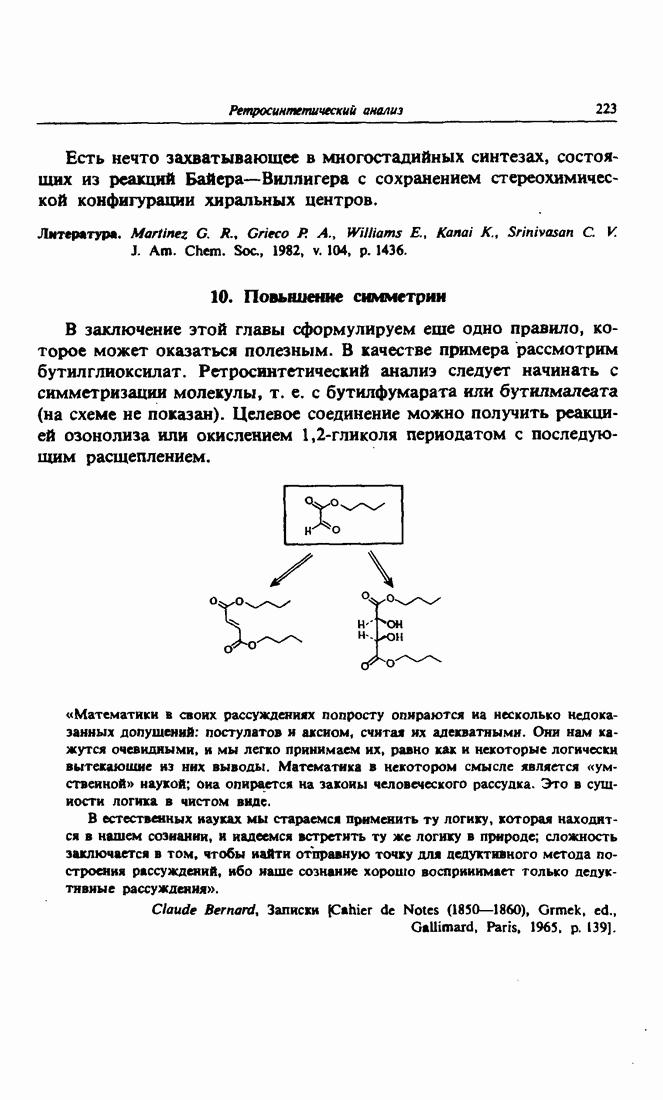
- 10. Повышение симметрии
- ПОСЛЕСЛОВИЕ